يمكن أن تنتقل بعض المواد الصلبة مباشرة إلى الحالة الغازية ، متجاوزة الحالة السائلة ، عبر عملية تعرف باسم التسامي. في درجة حرارة الغرفة والضغط القياسي ، قطعة من الثلج الجاف (CO2 الصلب) يتصاعد، ويبدو أنه يختفي تدريجيًا دون أن يتشكل أي سائل على الإطلاق. يتصاعد الثلج والجليد في درجات حرارة أقل من نقطة انصهار الماء، وهي عملية بطيئة قد تتسارع بفعل الرياح وانخفاض الضغط الجوي على ارتفاعات عالية. وعندما يتم تسخين اليود الصلب، يتصاعد الصلب ويتشكل بخار أرجواني زاهي. يسمى عكس التصاعد الترسيب، وهي عملية تتكثف فيها المواد الغازية مباشرة في الحالة الصلبة ، متجاوزة الحالة السائلة. وتشكيل الصقيع هو مثال على الترسيب.
مثل التبخر ، تتطلب عملية التصاعد مدخلات من الطاقة للتغلب على عوامل الجذب بين الجزيئات. وبالتالي ، فإن التصاعد هو انتقال طور ماص للحرارة. المحتوى الحراري للتسامي ،ΔHsub، هو الطاقة المطلوبة لتحويل مول واحد من مادة من الحالة الصلبة إلى الحالة الغازية. على سبيل المثال ، يتم تمثيل تصاعد ثاني أكسيد الكربون بواسطة:

وبالمثل، فإن التغير في المحتوى الحراري لعملية الترسيب العكسي يساوي الحجم ولكنه عكس ذلك في الإشارة إلى ذلك من أجل التسامي. نظراً لأن الترسيب ينطوي على تكوين قوى بين الجزيئات ، فهو مرحلة انتقالية طاردة للحرارة.

ضع في اعتبارك إلى أي مدى يجب التغلب على عوامل الجذب بين الجزيئات لتحقيق انتقال طور معين. يتطلب تحويل مادة صلبة إلى سائل التغلب على عوامل الجذب هذه جزئيًا فقط ؛ يتطلب الانتقال إلى الحالة الغازية التغلب عليها تمامًا. ونتيجة لذلك ، فإن المحتوى الحراري لانصهار مادة ما يكون أقل من المحتوى الحراري الخاص بالتبخير. يمكن استخدام هذا المنطق نفسه لاشتقاق علاقة تقريبية بين المحتوى الحراري لجميع تغييرات الطور لمادة معينة. على الرغم من أنه ليس وصفًا دقيقًا تمامًا ، يمكن تصميم نموذج التسامي بشكل ملائم باعتباره عملية ذوبان متتابعة من خطوتين متبوعة بالتبخير من أجل تطبيق قانون هيس. من هذا المنطلق ، يمكن تقدير المحتوى الحراري للتسامي لمادة ما كمجموع محتواه من الانصهار والتبخير.
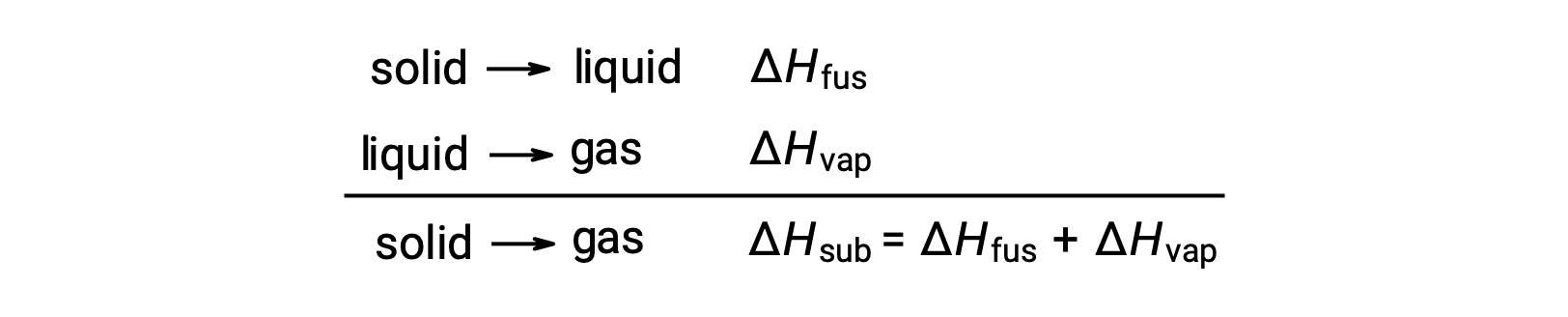
هذا النص مقتبس من Openstax, Chemistry 2e, Section 10.3: Phase Transitions.
From Chapter 11:

Now Playing
11.11 : انتقالات المرحلة: التصاعد والترسب
Liquids, Solids, and Intermolecular Forces
16.4K Views

11.1 : مقارنة جزيئية بين الغازات والسوائل والمواد الصلبة
Liquids, Solids, and Intermolecular Forces
39.6K Views

11.2 : القوى بين الجزيئية مقابل القوى الجزيئية
Liquids, Solids, and Intermolecular Forces
83.5K Views

11.3 : القوى بين الجزيئات
Liquids, Solids, and Intermolecular Forces
54.8K Views

11.4 : مقارنة القوى بين الجزيئيات
Liquids, Solids, and Intermolecular Forces
43.2K Views

11.5 : التوتر السطحي والعمل الشعري واللزوجة
Liquids, Solids, and Intermolecular Forces
27.1K Views

11.6 : انتقالات المرحلة
Liquids, Solids, and Intermolecular Forces
18.4K Views

11.7 : انتقالات المرحلة: التبخير والتكثيف
Liquids, Solids, and Intermolecular Forces
16.7K Views

11.8 : ضغط البخار
Liquids, Solids, and Intermolecular Forces
33.6K Views

11.9 : معادلة كلاوزيوس-كلايبرون
Liquids, Solids, and Intermolecular Forces
54.5K Views

11.10 : انتقالات المرحلة: الذوبان والتجميد
Liquids, Solids, and Intermolecular Forces
12.1K Views

11.12 : منحنيات التسخين والتبريد
Liquids, Solids, and Intermolecular Forces
21.7K Views

11.13 : مخطّطات المرحلة
Liquids, Solids, and Intermolecular Forces
38.0K Views

11.14 : تراكيب المواد الصلبة
Liquids, Solids, and Intermolecular Forces
13.3K Views

11.15 : المواد الصلبة الجزيئية والأيونية
Liquids, Solids, and Intermolecular Forces
16.3K Views
See More
Copyright © 2025 MyJoVE Corporation. All rights reserved