A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
تشريح وتلون ذبابة الفاكهة اليرقات المبايض
In This Article
Summary
كيف محاريب والخلايا الجذعية خلال نموذج التنمية هو السؤال المهم مع الآثار العملية. في ذبابة الفاكهة المبيض ، والخلايا الجذعية الجرثومية الخط والشكل الجسدي مطلبهم خلال نمو اليرقات. هذا الفيديو يوضح كيفية تشريح ، وصمة عار وجبل المناسل الإناث من طور مرحلي third المتأخرة (LL3) ذبابة الفاكهة اليرقات.
Abstract
العديد من الأجهزة تعتمد على الخلايا الجذعية من أجل تنميتها وخلال مرحلة التطور الجنيني للصيانة أو ترميم خلال فترة البلوغ. فهم كيفية تشكل الخلايا الجذعية ، وكيفية تفاعلها مع بيئتها ، من الأهمية بمكان لفهم التنمية ، التوازن والمرض. وقد عمل المبيض من melanogaster ذبابة الفاكهة ذبابة الفاكهة نموذجا للتفاعل مؤثر من الخلايا الجذعية الجرثومية خط (GSCs) مع دعم خلاياهم الجسدية (المتخصصة) 1 ، 2. وقد أتاح الموقع معروف من مكانة وGSCs ، ويقترن بالقدرة على معالجة وراثيا لهم والباحثين لتوضيح مجموعة متنوعة من التفاعلات بين الخلايا الجذعية ومطلبهم 12/03.
على الرغم من ثروة من المعلومات حول آليات مراقبة وصيانة GSC التمايز ، لا يعرف إلا القليل نسبيا حول كيفية GSCs مطلبهم والجسدية خلال نموذج التنمية. حوالي 18 محاريب الجسدية ، والتي تشمل المكونات الخلوية وخلايا شعيرات محطة كاب (الشكل 1) ، وشكل خلال طور مرحلي اليرقات third 13-17. GSCs تنشأ من خلايا جرثومية بدائية (PGCs). PGCs تتكاثر في مراحل اليرقات في وقت مبكر ، ولكن في أعقاب تشكيل مجموعة فرعية متخصصة ليصبح PGCs GSCs 7 ، 16 ، 18 ، 19. معا ، فإن الخلايا الجسدية وGSCs المتخصصة في جعل وحدة وظيفية التي تنتج البيض طوال فترة حياة الكائن الحي.
أسئلة كثيرة فيما يتعلق بتشكيل وحدة GSC تبقى دون جواب. وأفضل مثل عمليات التنسيق بين الخلايا السليفة للمحاريب والسلائف الخلايا الجذعية ، أو جيل من التباين داخل PGCs عندما تصبح GSCs ، يمكن دراستها في اليرقة. ومع ذلك ، دراسة منهجية للتنمية المبيض اليرقات يمثل تحديا جسديا. الأولى ، هي المبايض اليرقات الصغيرة. حتى في مراحل اليرقات أواخر هم فقط عبر 100μm. بالإضافة إلى ذلك ، المبيضين وشفافة هي جزء لا يتجزأ من الدهون في الجسم الأبيض. نحن هنا وصف بروتوكول خطوة بخطوة لعزل المبيضين من أواخر يرقات ذبابة الفاكهة طور مرحلي third (LL3) ، تليها تلطيخ مع الأضداد الفلورسنت. نحن نقدم بعض الحلول التقنية لمشاكل مثل تحديد المبيضين ، وتلطيخ وغسل الأنسجة التي لا تغرق ، والتأكد من أن الأجسام المضادة تخترق الأنسجة. ويمكن تطبيق هذا البروتوكول على مراحل في وقت سابق من اليرقات والخصيتين اليرقات كذلك.
Protocol
1. البيض
- قبل خمسة أيام من تشريح : السماح الإناث الملقحة لوضع البيض لمدة 2-4 ساعات على المواد الغذائية الطازجة تستكمل مع الخميرة. للحصول على اليرقات متزامنة ومتطورة ، فمن المهم ألا يكون المثقف مكتظة (حوالي 30 بيضة / فيال 25mm). عادة ، يتم استخدام 7-16 الإناث في قارورة ، اعتمادا على مدى نجاحها في إرساء.
2. اختيار اليرقات
- إعداد طبق زجاج 9 - جيدا تشريح مليئة المتوسطة رينغر (128mM كلوريد الصوديوم ، 2mm وبوكل ، 1.8mM CaCl 2 ، 4mM MgCl 2 ، 35.5mM السكروز ، 5mM Hepes الحموضة 6.9).
- إعداد مصافى الخلية في صفيحة تحتوي على ستة جيدا المتوسطة رينغر ووضعه على الجليد. بدلا من ذلك ، ونحن نستخدم قوالب معدة خصيصا مجهزة بشبكة من النايلون.
- اختيار توقيت اليرقات من الجدران باستخدام الملقط فيال البيولوجية الدقيقة (ملقط) ووضعها في صحن يحتوي على الجرس لتشريح.
- نقل اليرقة الإناث إلى بئر نظيفة. فنحن نميز الإناث من الذكور من قبل الغدد التناسلية الخاصة بهم. يتم التعرف عليها بسهولة كما ذكر الخصيتين الاهليليجات واضحة كبيرة مضمنة في الثلث الخلفي من الدهون في الجسم. يمكن التعرف على المبيضين الإناث ، التي تقع في نفس الجزء من الجسم الدهون ، وأصغر من ذلك بكثير ، المجالات ، واضحة وإيابا.
3. تشريح اليرقة
- عقد اليرقة أسفل الخلفي فقط إلى الدماغ مع ملقط وإزالة الرأس مع الزوج الثاني من الملقط.
- وضع الجزء المتبقي الخلفي على الجانب الظهري ، والقصبة الهوائية أسفل.
- عقد اليرقة التي spiracles الخلفي مع زوج واحد من الملقط ودفعها ببطء نحو الداخل في حين أن الزوج الآخر هو انزلاق إهاب خلفي حتى حوالي نصف الدهون في الجسم يخرج اليرقات.
- اعتقادا راسخا نهاية الخلفي واستخدام الملقط الزوج الأخرى لعقد فضفاضة للبشرة. برفق وببطء سحب بعيدا نهاية الخلفي بحيث إهاب والشريحة المرفقة الأمعاء من خلال هذه الثغرة. في نهاية هذه العملية ، ينبغي أن تكون منفصلة تماما الدهون في الجسم من الأمعاء وإهاب و. قطع الأمعاء من الجزء الأمامي من الدهون في الجسم. لجعل تلوين وتركيب أسهل ، فمن المهم أن الدهون في الجسم ستبقى على حالها.
- الرطب ماصة المراعي تماما مع رينغر المتوسطة ، ويفضل أن تحتوي على اليرقات من تشريح جيدا. ويساعد هذا معطف ماصة ويمنع الدهون في الجسم من الالتصاق به. استخدم ماصة المراعي لنقل الدهون في الجسم في المتوسط في رينغر الباردة الجليد في مصفاة الخلية.
4. التثبيت ويلطخ
يتم تنفيذ كافة الخطوات في درجة حرارة الغرفة ، باستثناء الحضانة مع الضد الأولى ، في 4 درجات مئوية.
- احتضان الجسم الدهون في الفورمالديهايد 5 ٪ في المتوسط رينغر. لمدة 20 دقيقة مع الإثارة لطيف.
- يغسل لمدة 5 دقائق مع PBT 1 ٪ (1 ٪ تريتون X - 100 في برنامج تلفزيوني). كرر هذه الخطوة لمدة 10 دقائق ، ومرة ثالثة لمدة 45 دقيقة. 1 ٪ تريتون X - 100 هو مطلوب لخرم المبيض اليرقات والسماح لاختراق الأجسام المضادة لها.
- كتلة مع PBTB 0.3 ٪ (0.3 ٪ تريتون س 100 و 1 ٪ في جيش صرب البوسنة PBS) لمدة 1 ساعة مع الانفعالات طيف
- احتضان مع الضد المطلوب ش 1 المخفف في PBTB 0.3 ٪ خلال الليل في 4 درجات مئوية مع الإثارة لطيف. وعادة ما يتم تنفيذ هذه الخطوة في 0.2 مل من الأنابيب على أسطوانات.
- نقل الدهون في الجسم مرة أخرى إلى مصافى الخلية.
- تغسل 3 مرات ، 30 دقيقة لكل منهما ، مع PBTB 0.3 ٪ مع الإثارة لطيف.
- كتلة مع PBTB 0.3 ٪ تستكمل مع 5 ٪ المصل الحمار العادي لمدة 1 ساعة مع الإثارة لطيف.
- احتضان مع الضد ثانوية المناسبة المخفف (وفقا لمواصفات الشركة المصنعة) في عرقلة الحل (0.3 ٪ PBTB تستكمل مع 5 ٪ المصل حمار عادي في PBT 0.3 ٪) لمدة 2 ساعة مع الإثارة لطيف. إذا كان الضد هو الفلورسنت ، واحتضان في الظلام من هذه النقطة فصاعدا. وعادة ما يتم تنفيذ هذه الخطوة في 0.2 مل من الأنابيب على أسطوانات.
- تغسل 3 مرات لمدة 30 دقيقة مع كل PBT 0.3 ٪ مع الإثارة لطيف.
5. متزايد
- نقل الدهون في الجسم لأنبوب إيبندورف نظيفة. جدا بعناية إزالة جميع السوائل بعيدا وتغطية مباشرة مع وسائل الاعلام Vectashield المتزايدة. نستخدم vectashield روتيني لأنه لا تتصلب في حين يجري فصل المبيضين من الدهون في الجسم.
ويمكن تخزين العينات المتزايدة في وسائل الإعلام في 4 درجة مئوية لمدة تصل الى اسبوع. - قطع نهاية طرف ماصة واستخدامه لنقل بدقة الدهون في الجسم مع حجم الحد الأدنى من وسائل الاعلام تركيب (حوالي 30 ميكرولتر عن زلة تغطية 30mm) على شريحة المجهر.
- استخدام اثنين من حاملي دبوس النيكل مطلي ، وعقد دبابيس قطرها 0.1 مم لتنتشر في الجسم الدهون. توجد في المبيضين الثالث الخلفي من الدهون في الجسم. تتشكل عادة من الدهون في الجسم التي تحيط بهم مثل "زهرة". هذا يساعد على تحديد مكان وجود المبيضين. تشريح خارج "زهور" عن بقية الجسم من الدهون والتخلص من هذا الأخير.
- surro إزالة الدهون في الجسمunding الغدد التناسلية عن طريق عبور دبابيس two حولها بعناية. مكان الغدة التناسلية معزولة على الشريحة بعيدا عن مخلفات الدهون في الجسم.
- مع تغطية زلة تغطية وختم بطلاء الأظافر.
- تصور مباشرة باستخدام المجهر مبائر. ويمكن تخزين العينات في 4 درجات مئوية لمدة تصل إلى ثلاثة أسابيع.
6. ممثل النتائج
لقد استخدمنا بروتوكول أعلاه لمتابعة إنشاء خلية الأنساب عدة داخل المبيض جسدية ، بما في ذلك GSCs ومطلبهم الجسدية. لهذا الغرض ، ونحن استخدام الاجسام المضادة المحددة وعلامات للتمييز بين أنواع مختلفة من الخلايا التناسلية في البلدان النامية. نعرض هنا مثالا على المبيضين LL3 two ملطخة تركيبات مختلفة من الأجسام المضادة. ويبرز الشكل 1A خيوط الخلايا الطرفية وقبعة (الأخضر) ، والتي تشكل معا الخلايا الجسمية من المحراب. 1B الشكل ، ويبين الخلايا المختلطة (ICS والأرجواني) ، والتي تتصل مباشرة الخلايا الجرثومية (الأزرق).
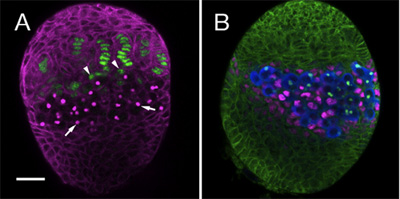
الشكل 1. LL3 المبيضين. (أ) وحيدة النسيلة 1B1 الأضداد (قرمزي) الخطوط العريضة الخلايا الجسدية والبقع وfusome ، وهي الخلايا داخل عضية PGCs (الأسهم). وأعرب في فخ محسن HH - lacZ (المضادة β - غالاكتوزيداز والأخضر) في الشعيرات الطرفية. ويمكن في قاعدة للخلايا الجسدية خيوط الغطاء (السهام) يمكن ملاحظتها. (ب) 1B1 الأضداد (الخضراء) وهي توضح كل الخلايا الجسدية في المبيض. مكافحة فاسا (الأزرق) تسميات جميع PGCs. PGCs الاتصال مباشرة على الخلايا المختلطة (ICS ، ومكافحة الاتجار المربى والأرجواني). بار (A و B) هي 20 ميكرومتر.
Discussion
هذا الفيديو يوضح عزلة والبروتوكول في الدقائق الاخيرة من تلطيخ المبيضين اليرقات طور مرحلي. لتنفيذ هذا البروتوكول بشكل روتيني وموثوق بها ، ينبغي إيلاء الانتباه إلى النقاط التالية :
- ليرقات متزامنة ومتطورا بشكل جيد ، ي?...
Disclosures
Acknowledgements
ويدعم الدردشة عن طريق منح ماري كوري إعادة الاندماج. وأيد هذا العمل من جانب إسرائيل لا علم منحة الصندوق. 1146-1108 ، من قبل هيلين ومارتن كيميل معهد أبحاث الخلايا الجذعية في معهد وايزمان للعلوم ، ومؤسسة Leir الخيرية.
Materials
| Name | Company | Catalog Number | Comments |
| NaCl | JT Baker | ||
| Kcl | Merck & Co., Inc. | ||
| CaCl2 | Sigma-Aldrich | ||
| MgCl2 | Merck & Co., Inc. | ||
| Sucrose | JT Baker | ||
| Hepes | Sigma-Aldrich | ||
| PBS | Sigma-Aldrich | ||
| Triton X-100 | Sigma-Aldrich | ||
| Albumin Bovine Fraction V | MP Biomedicals | 160069 | |
| Dumont biology tweezers 5 dumstar polished | Fine Science Tools | 11295-10 | |
| Nickel plated pin holder | Fine Science Tools | 26018-17 | |
| s.s minutien pins 0.1mm diam, 10mm long | Fine Science Tools | 26002-10 | |
| 9 well plates 85X100 mm, 22mm o.d.x7mm deep | Corning | 7220-85 | |
| Stereo Microscope MZ 16.5 with a standard transmitted light base TL ST | Leica Microsystems | ||
| 6 well plates | Costar | 3516 | |
| Slides | Menzel-Glaser | 798 | |
| Cover slips | Corning | 2940-223 | |
| Mounting media | Vectashield | H-1200 | |
| Cell strainer | Falcon BD | FAL352350 | |
| 1B1 antibody | Developmental Studies Hybridoma Bank | ||
| Anti-Traffic Jam | Laboratory of Dr. Dorothea Godt | ||
| Anti-Vasa | Laboratory of Dr. Ruth Lehmann | ||
| Anti β-Galactosidase | Cappel | ||
| Secondary Antibodies | Jackson ImmunoResearch |
References
- Fuller, M. T., Spradling, A. C. Male and female Drosophila germline stem cells: two versions of immortality. Science. 316, 402-404 (2007).
- Li, L., Xie, T. Stem cell niche: structure and function. Annual review of cell and developmental biology. 21, 605-631 (2005).
- Chen, D., McKearin, D. Gene circuitry controlling a stem cell niche. Curr Biol. 15, 179-184 (2005).
- Kai, T., Spradling, A. An empty Drosophila stem cell niche reactivates the proliferation of ectopic cells. Proceedings of the National Academy of Sciences of the United States of America. 100, 4633-4638 (2003).
- Kai, T., Spradling, A. Differentiating germ cells can revert into functional stem cells in Drosophila melanogaster ovaries. Nature. 428, 564-569 (2004).
- Lopez-Onieva, L., Fernandez-Minan, A., Gonzalez-Reyes, A. Jak/Stat signalling in niche support cells regulates dpp transcription to control germline stem cell maintenance in the Drosophila ovary. Development. 135, 533-540 (2008).
- Song, X., Zhu, C. H., Doan, C., Xie, T. Germline stem cells anchored by adherens junctions in the Drosophila ovary niches. Science. 296, 1855-1857 (2002).
- Tazuke, S. I. A germline-specific gap junction protein required for survival of differentiating early germ cells. Development. 129, 2529-2539 (2002).
- Xie, T., Spradling, A. C. decapentaplegic is essential for the maintenance and division of germline stem cells in the Drosophila ovary. Cell. 94, 251-260 (1998).
- Xie, T., Spradling, A. C. A niche maintaining germ line stem cells in the Drosophila ovary. Science. , 290-328 (2000).
- Guo, Z., Wang, Z. The glypican Dally is required in the niche for the maintenance of germline stem cells and short-range BMP signaling in the Drosophila ovary. Development. 136, 3627-3635 (2009).
- Wang, X., Harris, R. E., Bayston, L. J., Ashe, H. L. Type IV collagens regulate BMP signalling in Drosophila. Nature. 455, 72-77 (2008).
- Godt, D., Laski, F. A. Mechanisms of cell rearrangement and cell recruitment in Drosophila ovary morphogenesis and the requirement of bric a brac. Development. 121, 173-187 (1995).
- Sahut-Barnola, I., Godt, D., Laski, F. A., Couderc, J. L. Drosophila ovary morphogenesis: analysis of terminal filament formation and identification of a gene required for this process. Developmental biology. 170, 127-135 (1995).
- Song, X., Call, G. B., Kirilly, D., Xie, T. Notch signaling controls germline stem cell niche formation in the Drosophila ovary. 134, 1071-1080 (2007).
- Zhu, C. H., Xie, T. Clonal expansion of ovarian germline stem cells during niche formation in Drosophila. Development. 130, 2579-2588 (2003).
- Ward, E. J. Stem cells signal to the niche through the Notch pathway in the Drosophila ovary. Curr Biol. 16, 2352-2358 (2006).
- Gilboa, L., Lehmann, R. Repression of primordial germ cell differentiation parallels germ line stem cell maintenance. Curr Biol. 14, 981-986 (2004).
- Gilboa, L., Lehmann, R. Soma-germline interactions coordinate homeostasis and growth in the Drosophila gonad. Nature. 443, 97-100 (2006).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved