Method Article
مظاهرة من بروتين تفعيل قناة الصوديوم الظهارية (عناق) من خلال الجمع بين المقاييس الحالية مع الكشف عن الشق شظايا
In This Article
Summary
تنشيط بروتين للقناة الصوديوم الظهارية (عناق) أعرب heterologously في القيطم المورق يمكن البرهنة البويضات عن طريق الجمع بين القياسات الحالية مع نهج biotinylation للتحقيق في ظهور منتجات انشقاق القناة الايونية على سطح الخلية. ويمكن تحديد مواقع انشقاق مهم وظيفيا باستخدام الطفرات الموجهة الموقع.
Abstract
The described methods can be used to investigate the effect of proteases on ion channels, receptors, and other plasma membrane proteins heterologously expressed in Xenopus laevis oocytes. In combination with site-directed mutagenesis, this approach provides a powerful tool to identify functionally relevant cleavage sites. Proteolytic activation is a characteristic feature of the amiloride-sensitive epithelial sodium channel (ENaC). The final activating step involves cleavage of the channel’s γ-subunit in a critical region potentially targeted by several proteases including chymotrypsin and plasmin. To determine the stimulatory effect of these serine proteases on ENaC, the amiloride-sensitive whole-cell current (ΔIami) was measured twice in the same oocyte before and after exposure to the protease using the two-electrode voltage-clamp technique. In parallel to the electrophysiological experiments, a biotinylation approach was used to monitor the appearance of γENaC cleavage fragments at the cell surface. Using the methods described, it was demonstrated that the time course of proteolytic activation of ENaC-mediated whole-cell currents correlates with the appearance of a γENaC cleavage product at the cell surface. These results suggest a causal link between channel cleavage and channel activation. Moreover, they confirm the concept that a cleavage event in γENaC is required as a final step in proteolytic channel activation. The methods described here may well be applicable to address similar questions for other types of ion channels or membrane proteins.
Introduction
البروتياز هي الأنزيمات التي تشارك في مختلف التفاعلات الفسيولوجية بدءا من تدهور بروتين معروفة من البروتينات، في سياق عملية الهضم، إلى شلالات البروتيني متطورة للغاية المشاركة في مجمع مسارات الإشارات التنظيمية. تصنف البروتياز إلى سبع مجموعات وفقا لموقع نشط التحفيزي على: اسبارتاتي، الأسباراجين، السيستين وحمض الجلوتاميك، فلزية، سيرين، والبروتياز ثريونين. البروتياز مختلفة تستهدف مواقع متميزة الانقسام التي ليست دائما سهلة للتنبؤ من الهيكل الأساسي للبروتين. قاعدة بيانات MEROPS ( http://merops.sanger.ac.uk/ يوفر) معلومات مفصلة عن مجموعة واسعة من البروتياز والمواقع الانقسام التفضيلية الخاصة بهم. ويمكن تحديد المواقع ذات الصلة الانقسام وظيفيا باستخدام الطفرات الموجهة الموقع.
ومن الثابت أن معالجة بروتين عناق هو آلية هامة من تفعيل الهو خاص القناة الايونية 1،2. ومن المثير للاهتمام، وهناك أدلة على أن وظيفة الاستشعار حمض ذات الصلة قناة أيون 1A (ASIC1a) ويمكن أيضا تعديلها من قبل البروتياز 3-5. في الوقت الحاضر يبقى السؤال مطروحا عما إذا كان الانقسام قناة بروتين يلعب دورا الفسيولوجية ذات الصلة في تنظيم نشاط القنوات الأيونية أو غيرها من شركات النقل. ومع ذلك، فإنه من الثابت أيضا أن الانقسام بروتين ينشط مجموعة من G مستقبلات البروتين يقترن، المستقبلات تنشيط الأنزيم البروتيني (بارس) 6. العديد من البروتياز سيرين (مثل البروتياز-تفعيل قناة (CAP1-3)، كيموتربسين، التربسين، فورين، بلازمين، العدلة إيلاستاز، وكاليكريين) وقد ثبت لتفعيل proteolytically ENAC 2. بالإضافة إلى البروتياز سيرين، يمكن أن تشارك مجموعات أخرى من البروتياز في تفعيل ENAC بروتين. في الواقع، تظهر البيانات الأخيرة أن الفلزي meprin-β 7 والسيستين البروتيني كاتيبسين-S 8 ويمكن أيضا ACTIVAالشركة المصرية للاتصالات عناق. ومع ذلك، تظل (المرضية) البروتياز ذات الصلة من الناحية الفسيولوجية لتفعيل ENAC يتم تحديدها ويمكن أن تختلف من الأنسجة إلى الأنسجة.
ومن المعروف البروتياز ليلتصق بشكل تفضيلي في مواقع معينة في تسلسل الأحماض الأمينية. على سبيل المثال، يظهر كيموتربسين سيرين البروتياز نمط انشقاق الشق محددة بعد العطرية الأمينية حمض الفينيل ألانين والتيروزين مخلفات. في المقابل، فإن سيرين البروتيني التربسين تفضيلي يشق بعد مخلفات يسين الأساسية أو أرجينين. باستخدام متحولة يبني γENaC الإنسان الناتجة عن الطفرات الموجهة الموقع، ويمكن تحديد المواقع ذات الصلة الانقسام وظيفيا في عناق أعرب heterologously في نظام التعبير البويضة 8-13.
عن طريق حقن كرنا لمفارز عناق الثلاثة (αβγ) إلى البويضات معزولة، ENAC يمكن التعبير عنها وظيفيا في هذه الخلايا والنشاط من قنوات موجودة في غشاء البلازما يمكن أن تقاسباستخدام اثنين من القطب تقنية الجهد المشبك. باستخدام الأميلوريد مدر للبول، مثبط ENAC محددة، وعناق بوساطة خلية كاملة المكون الحساسة للأميلوريد الحالية (ΔI عامي) يمكن فصلها عن تسرب التيارات غير محددة أو من التيارات التي أجرتها القنوات الأيونية الأخرى. وبالتالي، والقيم ΔI عامي تعكس النشاط ENAC الشاملة ويمكن تحديده من خلال طرح تيارات خلية كاملة يقاس بحضور الأميلوريد من التيارات خلية كاملة المقابلة سجلت في غياب الأميلوريد. لاختبار ما إذا كان البروتيني له تأثير تنشيطية على ENAC، يتم قياس ΔI عامي مرتين في نفس البويضة، أي قبل وبعد حضانة البويضة في محلول يحتوي على الأنزيم البروتيني. بزيادة قدرها ΔI عامي من الأول إلى الثاني يشير قياس تنشيط بروتين عناق. ومن المعروف كيموتربسين التربسين أو الحد الأقصى لتحفيز ENAC في نظام التعبير البويضة 2،14 ويمكن استخدامها لconfiجمهورية مقدونيا أن تنشيط بروتين ENAC قابلا للاكتشاف في دفعة معينة من البويضات.
بالتوازي مع القياسات الحالية خلية كاملة، تم استخدام نهج biotinylation 9 إلى التحقيق في ما إذا كانت الزيادة في ΔI عامي الكشف عند التعرض للالبويضات لالبروتياز يرتبط ظهور ENAC الانقسام شظايا على سطح الخلية. وصفت البروتينات على سطح الخلية مع البيوتين ويمكن فصلها عن البروتينات داخل الخلايا بواسطة ربط البروتينات البيروكسيديز إلى حبات الاغاروز Neutravidin المسمى. ويمكن تحليل البروتينات البيروكسيديز بواسطة لطخة غربية. ويمكن الكشف عن γENaC شظايا الانقسام على سطح الخلية باستخدام الأجسام المضادة المحددة الموجهة ضد حاتمة في محطة سي من γENaC. لتحديد موقع انشقاق ذات الصلة وظيفيا (ق)، ويمكن توقع تحور مواقع انشقاق باستخدام الطفرات الموجهة الموقع. تتم مقارنة قنوات Wildtype ومتحولة في التجارب المتوازية باستخدام البويضات من لياليدفعة آمي.
مع هذا الأسلوب المنهجي وقد تجلى ذلك لأول مرة أن تنشيط بروتين من ENAC بوساطة تيارات خلية كاملة يرتبط مع تعتمد على الوقت ظهور ENAC الانقسام شظايا على سطح الخلية. هذه النتائج تشير إلى وجود علاقة سببية بين قناة الانقسام وتفعيل القناة. وعلاوة على ذلك، وذلك باستخدام الطفرات الموجهة موقع من المواقع الانقسام المفترضة في تركيبة مع اثنين من القطب تقنية الجهد المشبك، والمواقع ذات الصلة الانقسام وظيفيا لبلازمين، كيموتربسين كاتيبسين و13-S 8 تم تحديدها.
Protocol
1. عزل البويضات القيطم Microinjection من وكرنا
- الحصول على البويضات من الإناث البالغات القيطم المورق. تخدير الحيوانات في 0.2٪ MS222، ويقطع فصوص المبيض من خلال شق في البطن الصغيرة.
- عزل البويضات من المبيض عن طريق فصوص الهضم الأنزيمي في 19 درجة مئوية لمدة 3-4 ساعة مع 600-700 U / مل من النوع 2 كولاجيناز من نسج كلوستريديوم الكالسيوم المذاب في حل OR2 الحرة (وصفة في الجدول رقم 1).
- للاختيار، ووضع البويضات defolliculated في طبق بتري تحت المجهر مجهر في الصوديوم عالية تحتوي على محلول (ND96: صفة في الجدول رقم 1).
- حدد المرحلة البويضات V-VI ووضعها في طبق بتري أخرى مع ماصة باستور. ملاحظة: بلانت باستور ماصة بواسطة المشتعلة لمنع الإصابة البويضة.
- حقن البويضات مع كرنا (على سبيل المثال 0.2 نانوغرام لكل αβγENaC الوحيدات). تذوب في الماء cRNAs ريبونوكلياز خالية. ملاحظة: إجماليحجم تحقن كل بويضة هو 46 NL.
- متجر حقن البويضات في 19 درجة مئوية في حل الصوديوم منخفضة الصوديوم لمنع التحميل من البويضات (ND9: صفة في الجدول رقم 1). تكملة الحل مع البنسلين 100 U / مل الصوديوم و 100 ميكروغرام / مل الستربتوميسين كبريتات لمنع نمو البكتيريا. التعامل بعناية البويضات للحد من كمية من البويضات التالفة أو الميتة والمحافظة عليها في مجموعات صغيرة الفردية في الآبار 12 جيدا لوحة مليئة حل حمام خلال اليومين بعد الحقن كرنا.
2. أداء ثنائي القطب التجارب الجهد المشبك
- قياس البويضات بعد يومين من الحقن.
- ملء حقنة واحدة من خطورة تغذية نظام الارواء بمحلول ND96 وحقنة أخرى مع ND96 محلول يحتوي على الأميلوريد (2 ميكرومتر). جبل المحاقن 50 سم فوق غرفة حمام البويضة. وقد تم اختيار تركيز الأميلوريد ENAC المانع أن تكون أعلى 20 مرة من لIC 50: ملاحظة (100 نانومتر).
- بدوره على مصدر ضوء بارد 150 W الهالوجين وتعديله إلى 10 سم فوق غرفة حمام البويضة مما يسمح التصور جيدة مع المجهر مجهر. ثم اتجه على شفط وضبط أنبوب شفط في نهاية الغرفة حمام البويضة. تحديد موقع أنبوب الشفط مقابل superfusion أنابيب "محول دخول الحمام البويضة. ملاحظة: يجب أن تكون قوة الشفط كافية لدعم تدفق مستمر من الحل superfusing البويضة.
- ضبط سرعة superfusion كل حل ل3-5 مل / دقيقة باستخدام جهاز التحكم في التدفق الرابع الجاذبية. توصيل أنابيب superfusion مع محول إلى غرفة حمام البويضة.
- سحب الشعيرات الدموية الزجاج مع مجتذب micropipette للحصول على أقطار غيض من <1 ميكرون. ثم ملء الشعيرات الدموية إلى ~ 1/4 مع 3 M بوكل. ملاحظة: تأكد من أن الجزء المكلورة من الأسلاك الفضية لصاحب القطب مغمورة في محلول بوكل. التحقق من وجود فقاعات الهواء في غيض من الشعرية. فقاعات الهواء تنال من قنينةrement عن طريق زيادة مقاومة السعة طائشة.
- إدراج الشعيرات الدموية في أصحاب الكهربائي للتيار الكهربائي والجهد ووضعها في ND96 تحتوي على الأميلوريد (2 ميكرومتر) الحل باستخدام المتلاعبين الصغيرة.
3. قياس الأميلوريد تراعي التيارات خلية كاملة
- صفر إمكانات الكهربائي من القطب الجهد (V م) والقطب الحالي (V ه) عن طريق ضبط م V V ه وتعويض الأزرار ملاحظة: إن المقاومة يجب أن تكون 1-2 MΩ عن القطب لقياس V م و 0.5 -1 MΩ عن القطب الحقن الحالية.
- وضع البويضة في غرفة الحمام على مقربة من القطب الاستشعار الجهد. ملاحظة: لا يضر البويضة خلال أي من هذه الخطوات نقل. استخدام ماصة باستور لنقل البويضة. لتجنب إتلاف البويضة حواف ماصة ينبغي اضعافها عن طريق المشتعلة.
- أسعد OOcytes بلطف مع كل microelectrodes.
- تعيين المحتملة عقد في مكبر للصوت ل-60 بالسيارات وتشغيل مسجل التخطيط. بدوره على الأميلوريد (2 ميكرومتر) التي تحتوي على الحل. ملاحظة: يجب أن يكون الحالية حوالي 0 ± 0.5 أمبير. تسرب التيارات أكبر تشير إلى وجود التطويق تتسرب منها المياه. وبالتالي، ينبغي رفض هذه البويضات. وعلاوة على ذلك، ينبغي للتيارات تسرب يقاس بحضور الأميلوريد (2 ميكرون) تكون مشابهة في αβγ-WT معربا عن البويضات لتلك التي قيست في αβγ-ENAC متحولة معربا عن البويضات. هذا يشير إلى أن الطفرات لا تؤثر على الأميلوريد حساسية للقناة.
- بدء التسجيل. إذا لزم الأمر ضبط الربح.
- بعد أن تصل الحالي يقاس هضبة مستقرة، تغيير الحل خالية من الأميلوريد. ملاحظة: الانحرافات الحالية النزولية في آثار الحالية تتوافق مع التيارات الداخل، أي حركة شحنة موجبة (+ نا) من الجانب خارج الخلية إلى داخل الخلية.
- بالعربيةثالثا يتم التوصل إلى هضبة الحالي (بعد ~ 60 ثانية)، تبديل superfusion إلى حل الأميلوريد تحتوي على. بعد تيار البويضة تصل إلى خط الأساس الأولي الحالي، إيقاف المشبك الجهد وسحب بلطف الأقطاب.
- للسماح إعادة إغلاق غشاء البلازما في مواقع التطويق، ووضع البويضة في بئر واحدة من 96 لوحة جيدا تحتوي على 100-150 ميكرولتر من الحل البروتيني الحرة ND96.
- بعد 5 دقائق، ونقل البويضة إلى البروتيني تحتوي على الحل أو حل التحكم دون البروتيني لفترة الحضانة 30 دقيقة. ملاحظة: فترة حضانة يعتمد على الأنزيم البروتيني وقناة دراستها.
- بعد الخطوة الحضانة تكرار القياس الحالي (انظر 3.2 وما بعدها). ملاحظة: من الممكن لقياس> 90٪ من البويضات بعد الحضانة في حل البروتيني.
4. Biotinylation الفحص
- حدد وتجاهل البويضات معيبة تحت المجهر مجهر. ملاحظة: استخدام حقنإد البويضات من نفس دفعة للقياسات الحالية والتجارب biotinylation.
- الحفاظ على البيوتين في RT لمدة 20 دقيقة على الأقل قبل استخدامه في التجربة.
- إعداد الحلول: ND96 ND96 والتي تحتوي على الأنزيم البروتيني المناسب. إعداد ماصات باستور بواسطة اصفة إياهم والمشتعلة لفترة وجيزة نصائح لتجنب الإصابة من البويضات. ملاحظة: وهنا، يتم استخدام البروتيني كيموتربسين 2 ميكروغرام / مل في ND96. علاج كل مجموعة مع ماصة منفصلة لتجنب التلوث المتبادل من الحلول.
- ملء كل بئر من لوحة 6 جيدا مع 2.5 مل السيطرة ND96 ND96 أو تحتوي على الأنزيم البروتيني في RT. ثم إيداع 30 البويضات لكل بئر واحتضان لهم لمدة 30 دقيقة في RT. ملاحظة: بالنسبة للإجراءات اللاحقة فمن المهم للحفاظ على عينات على الجليد في جميع الأوقات. يتم في تنفيذ جميع الخطوات الطرد المركزي في 4 درجات مئوية.
- ملء كل بئر من جديد لوحة 6 جيدا مع 2.5 مل ND96 (يحتاج كل مجموعة 3 آبار للخطوات الغسيل) وتزن البيوتين. ملاحظة: 2.5 ملغ البيوتين عإيه جيدا (1 ملغ / مل) هو مطلوب. حل البيوتين في المخزن المؤقت biotinylation (أي 25 ملغ البيوتين (لمدة 10 مجموعات) في 25 مل biotinylation عازلة (وصفة في الجدول رقم 1).
- نقل كل مجموعة من البويضات لشغل جيدا مع 2.5 مل ND96. نقل البويضات بالتتابع في بئرين إضافية مع ND96 ليغسل أي البروتيني المتبقية. احتضان البويضات لمدة 5 دقائق في ND96.
- نقل البويضات إلى 2.5 مل من محلول يحتوي على البيوتين جيدا واحتضان لهم مع الإثارة لطيف ('شاكر') لمدة 15 دقيقة. ملاحظة: تصغير ND96 نقل مع ماصة لتجنب تخفيف من الحل البيوتين.
- نقل كل مجموعة من البويضات إلى 2.5 مل تحتوي كذلك إخماد عازلة (وصفة في الجدول 1) لوقف رد الفعل biotinylation. ثم، ونقل كل مجموعة من البويضات في بئر ثانية تحتوي أيضا إرواء 2.5 مل العازلة واحتضان لمدة 5 دقائق مع الإثارة لطيف.
- إزالة البويضات التالفة أو ميتا. ملاحظة:اختيار نفس العدد من البويضات في كل مجموعة لالإجراء التالي.
- نقل كل مجموعة من البويضات إلى 1.5 مل أنبوب microcentrifuge البلاستيك. ملاحظة: تصغير كمية من العازلة إخماد التي يتم نقلها.
- في وقت لاحق، ليز البويضات عن طريق تمريرها من خلال إبرة 27 G في 1 مل العازلة تحلل (وصفة انظر الجدول 1) تستكمل مع مثبطات الأنزيم البروتيني.
- الطرد المركزي لست] لمدة 10 دقيقة في 1،500 ز س.
- طاف نضح وتحويلها إلى أنبوب 1.5 مل microcentrifuge تحتوي 0.5٪ تريتون-X-100 و 0.5٪ NP40. تجاهل بيليه المتبقية. ملاحظة: طاف تحتوي على بروتينات غشاء البلازما والبروتينات داخل الخلايا البيروكسيديز غير البيروكسيديز.
- احتضان أنابيب microcentrifuge لمدة 20 دقيقة على الجليد. مرارا وتكرارا دوامة الأنابيب خلال هذه الفترة لتذوب تماما البروتينات في NP40 وتريتون-X-100.
- الطرد المركزي 100 ميكرولتر من الخرز الاغاروز لكل مجموعة البويضة لمدة 3 دقائق في ز × 1،500. بعدالطرد المركزي إزالة طاف من حل الخرز ويغسل ثلاث مرات مع العازلة تحلل لكي تتوازن مع حبات العازلة.
- ماصة 100 ميكرولتر من الخرز غسلها في كل أنبوب microcentrifuge التي تحتوي على البروتين المنظفات الحل أعد 4.13 للسماح ملزمة من البروتينات البيروكسيديز إلى الخرز.
- احتضان أنابيب microcentrifuge مع النفقات العامة التناوب O / N عند 4 درجة مئوية.
- الطرد المركزي أنابيب microcentrifuge لمدة 3 دقائق في ز × 1،500. ثم نقل طاف في أنبوب جديد. ملاحظة: لا يتم المسمى البروتينات داخل الخلايا مع البيوتين. ويمكن تخزين طاف في -20 درجة مئوية. لا نضح الخرز.
5. الكشف عن عناق الشق شظايا على سطح الخلية عن طريق ويسترن تحليل لطخة
- تغسل حبات ثلاث مرات مع العازلة تحلل وإضافة 100 ميكرولتر من 2X SDS-PAGE عينة العازلة. ملاحظة: يمكن تخزين العينات في -20 درجة مئوية أو مباشرة إعداده للتحليل لطخة غربية.
- يغلي لياليamples لمدة 5 دقائق عند 95 درجة مئوية ثم أنابيب مكان على الجليد.
- عينات الطرد المركزي لمدة 3 دقائق في 20،000 XG وماصة طاف في أنبوب microcentrifuge جديدة. ملاحظة: هذا طاف يحتوي على البروتينات البيروكسيديز غشاء البلازما من سطح الخلية من البويضة.
- تحليل 30 ميكرولتر من هذا طاف بواسطة لطخة غربية للتحقيق في شظايا الانقسام على سطح الخلية.
- فصل البروتينات البيروكسيديز بواسطة SDS-PAGE (الصوديوم كبريتات دوديسيل بولي أكريلاميد الكهربائي للهلام) باستخدام هلام المناسب (8٪، 10٪، 12٪ اعتمادا على الوزن الجزيئي للشظايا الانقسام التحقيق).
- نقل البروتينات إلى difluoride البولي فينيل (PVDF) الأغشية بواسطة النشاف شبه الجافة.
- بحث الغشاء مع الأجسام المضادة المحددة ضد γENaC الإنسان الموجهة ضد حاتمة في محطة سي (انظر الشكل 3 و 13).
- استخدام الفجل البيروكسيداز المسمى الماعز المضادة للأرنب الضد كما المضادة الثانويةالجسم.
- الكشف عن إشارات chemiluminescent.
النتائج
للتحقيق في ما إذا كان بلازمين البروتيني سيرين يمكن تنشيط التيارات ENAC بوساطة، تقرر ΔI عامي الفردية البويضات ENAC، معربا عن قبل وبعد 30 دقيقة حضانة البويضات في خالية من الأنزيم البروتيني (السيطرة) (الشكل 2A) أو التي تحتوي على حل بلازمين (الشكل 2B) باستخدام يومين القطب تقنية الجهد المشبك (انظر الشكل 1). التعرض لبلازمين زيادة ΔI عامي في كل بويضة قياسها. في المقابل، في تجارب السيطرة، وكان 30 دقيقة حضانة ENAC، معربا عن البويضات في محلول خالية من البروتيني له تأثير يذكر (الشكل 2 C، D). وبالتالي، باستخدام هذه الطريقة يمكن الكشف عن التحفيز الحالية ENAC بوساطة بلازمين.
لدراسة آثار تحور المواقع الانقسام المفترضة على تفعيل التيارات ENAC بوساطة، وكذلك على قناة الانقسام، وتمت مقارنة تأثير كيموتربسين على WT-ENAC مع ذلك علىوENAC متحولة مع prostasin تحور والمواقع الانقسام بلازمين (γ RKRK178AAAA؛ K189A). وكان التحقيق مجرى وقت التنشيط قناة كتبها كيموتربسين فضلا عن ظهور انشقاق ENAC المنتجات على سطح الخلية باستخدام مختلف الأوقات البروتيني الحضانة (الشكل 4A). وقد تبين أن التأخير قناة متحولة ويقلل من تفعيل الحالية ENAC بوساطة كيموتربسين. ويتوازى ذلك من خلال مظهر تأخر انخفاض الوزن الجزيئي γENaC انشقاق جزء من 67 كيلو دالتون الموافق الوحيدات المشقوق بالكامل. تم الكشف عن شظايا الانقسام باستخدام الأجسام المضادة γENaC الموجهة ضد حاتمة في محطة سي (الشكل 3). يوضح هذا النهج المنهجية التي مدار الساعة من تفعيل بروتين التيارات ENAC بوساطة يرتبط مع ظهور منتج انشقاق 67 كيلو دالتون γENaC على سطح الخلية (الشكل 4 B، C). هذا يدعم مفهومالعلاقة السببية بين قناة بروتين الانقسام وتفعيل القناة 13. علاوة على ذلك، من خلال الجمع بين القياسات الحالية والكشف عن شظايا γENaC على سطح الخلية وقد تبين أن المواقع الانقسام تحور ذات الصلة وظيفيا لتفعيل قناة بروتين.

الشكل 1. إجراءات تحديد تأثير تنشيطية لالبروتيني على ENAC أعرب heterologously في القيطم المورق البويضات. ويقدر النشاط ENAC عن طريق قياس حساسة للالأميلوريد خلية كاملة المكون الحالي ΔI عامي.
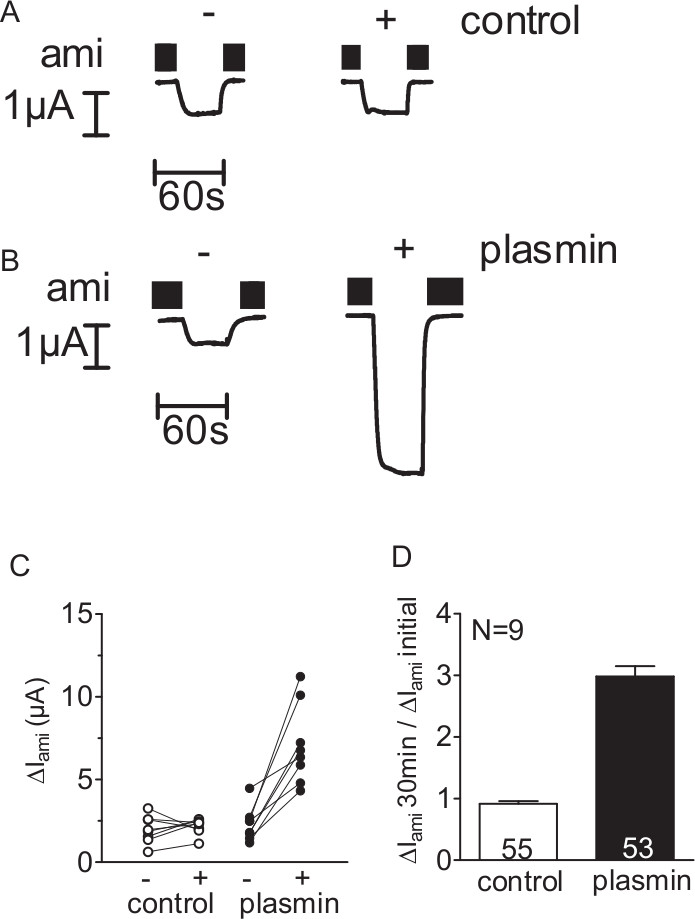
الشكل 2. بلازمين يحفز CURREN ENAC بوساطةTS في البويضات معربا عن عناق. وحضنت (AD) البويضات معربا عن عناق الإنسان لمدة 30 دقيقة في محلول خالية من الأنزيم البروتيني (السيطرة) أو في محلول يحتوي على بلازمين (10 ميكروغرام / مل). لتحديد ΔI عامي قبل (-) وبعد (+) الحضانة، وفرضت البويضات في إمكانية عقد -60 بالسيارات (A، B) أربعة خلية كاملة آثار الحالية ممثلة من دفعة واحدة من البويضات. كان الأميلوريد (عامي) موجودة في حل حمام لمنع تحديدا ENAC كما يتبين من أشرطة سوداء. (C) وترتبط نقطة البيانات التي تم الحصول عليها من بويضة الفردية عن طريق خط (D) ملخص تجارب مماثلة كما هو مبين في C. أعمدة تمثل تأثير تنشيطية النسبي على ΔI عامي تحسب كنسبة من ΔI عامي يقاس بعد 30 دقيقة الحضانة (ΔI عامي 30 دقيقة) إلى ΔI عامي الأولي (ΔI عامي الأولي) قياس قبل الحضانة. الأرقام داخل الأعمدة تشير إلىعدد من البويضات الفردية قياسها. يشير N عدد من دفعات مختلفة من البويضات. (تم تعديل هذا الرقم من [Haerteis وآخرون 2012 J الجنرال الفيزيولوجيا 140، 375-389، دوى: 10.1085/jgp.201110763])
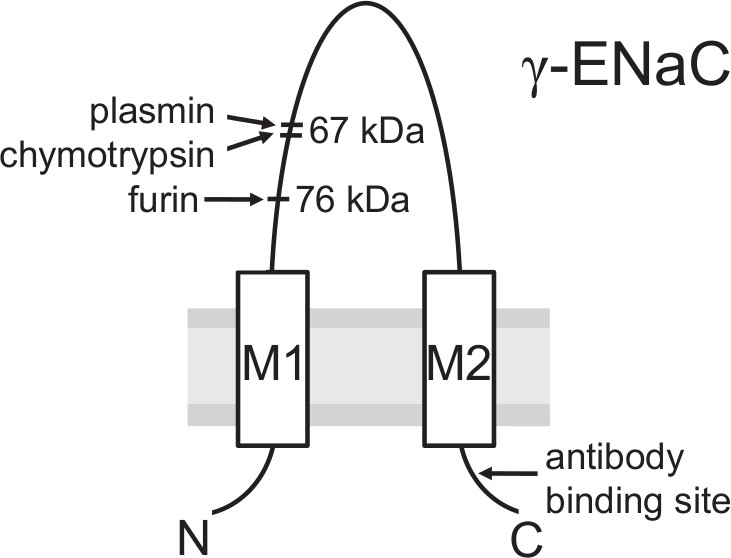
الشكل 3. نموذج من γENaC الوحيدات تبين مواقع الانقسام لتنشيط بروتين وموقع ملزم من الأجسام المضادة المستخدمة. انشقاق بروتين من قبل فورين كونفيرتاز جولجي المصاحب مهم لعناق النضج في مسار السكروز قبل أن تصل القناة غشاء البلازما. بعد الانقسام من قبل فورين 76 كيلو دالتون جزء يمكن الكشف على سطح الخلية باستخدام نهج biotinylation والأجسام المضادة ضد حاتمة في محطة سي من γ-الوحيدات. الخطوة النهائية محوريا في بروتين ENتفعيل تيار متناوب ربما يقام في غشاء البلازما حيث المشقوق γENaC بواسطة البروتياز خارج الخلية (مثل بلازمين أو كيموتربسين) في المنطقة البعيدة إلى موقع فورين مما أدى إلى انشقاق جزء 67 كيلو دالتون. (تم تعديل هذا الرقم من [Haerteis وآخرون 2012 J الجنرال الفيزيولوجيا 140، 375-389، دوى: 10.1085/jgp.201110763])
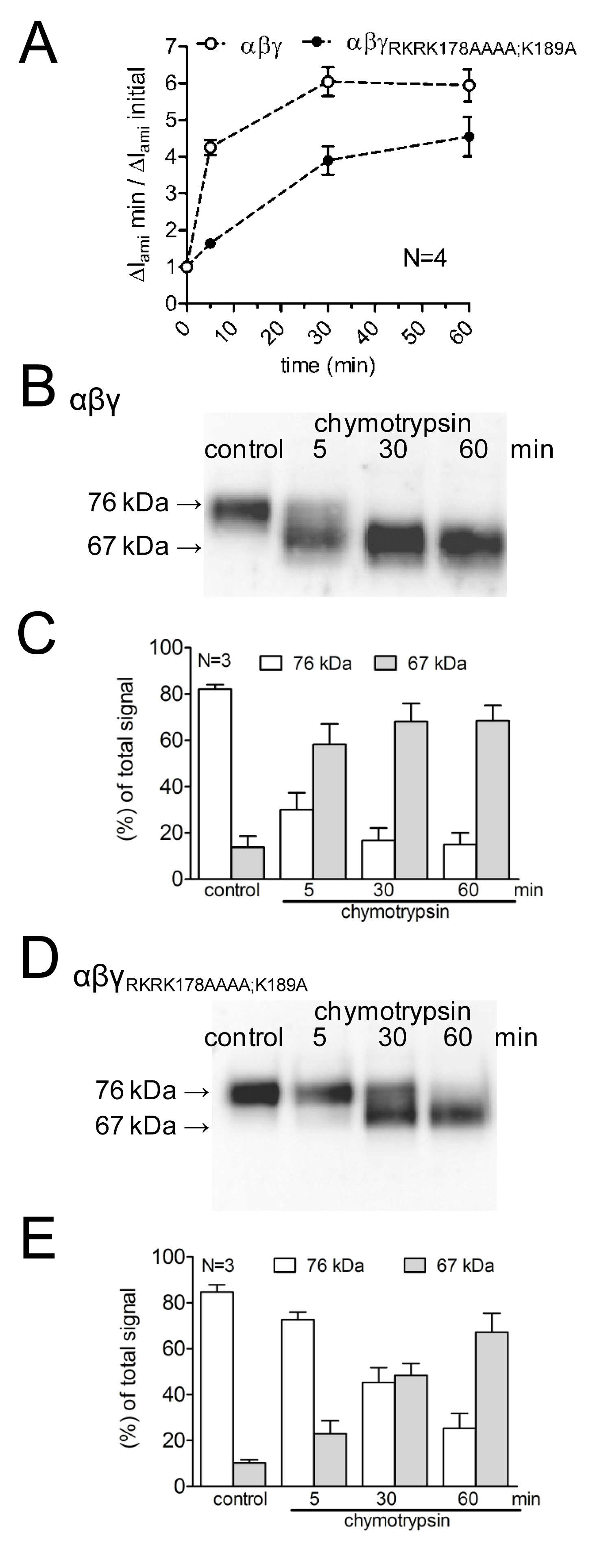
الشكل 4: تحور كل من بلازمين (K189) وموقع الانقسام prostasin (RKRK178) يؤخر تفعيل التيارات ENAC بوساطة وظهور منتج انشقاق 67 كيلو دالتون من القناة γ-الوحيدات البويضات معربا عن WT (حرف مفتوح) و γ RKRK178AAAA؛ حضنت K189A ENAC قناة متحولة (الرموز المغلقة) لمدة 30 دقيقة في محلول خالية من الأنزيم البروتيني (السيطرة) أو 5، 30، أو 60 دقيقة في محلول يحتوي على كيموتربسين (2 ميكروغرام / مل). (A) لتحديد ΔI عامي قبل وبعد الحضانة، وفرضت البويضات في إمكانية عقد -60 بالسيارات. الدوائر تمثل نسبة ΔI عامي قياس بعد 5 أو 30 أو 60 دقيقة الحضانة (ΔI عامي دقيقة) إلى ΔI عامي الأولي (ΔI عامي الأولي) قياس قبل الحضانة. كل نقطة بيانات يمثل متوسط ΔI عامي 22-24 في قياس البويضات الفردية أربع دفعات مختلفة. (BD) وبالتوازي مع الكشف عن ΔI عامي التعبير عن γENaC البيروكسيديز على سطح الخلية وتحليلها بواسطة SDS-PAGE. تم الكشف عن γENaC مع الأجسام المضادة ضد حاتمة في محطة سي من γENaC الإنسان. وتظهر البقع ممثل الغربي من دفعة واحدة من البويضات. (CE) تحليل الكثافة من ثلاثة البقع الغربية مشابهة لتلك التي تظهر في باء أو دال على كل حارة، لياليتم تحديد ignals الكشف في مناطق 76 دينار كويتي (أعمدة مفتوحة) و 67 دينار (الأعمدة الرمادي) وتطبيع للمجموع الكلي الكشف عن إشارة. يشير N عدد من دفعات مختلفة من البويضات. اضغط هنا لمشاهدة صورة أكبر.
Discussion
في هذه المخطوطة يوصف نهج المنهجية التي تم تطبيقها بنجاح لدراسة الآليات الكامنة وراء تفعيل ENAC بواسطة البروتياز 8،13. تم استخدام القيطم المورق البويضة نظام التعبير راسخة لصريحة وظيفيا عناق. تم تقييم وظيفة عناق مع التقليدية يومين القطب تقنية الجهد المشبك. كان يعمل موقع الموجه الطفرات لتحديد المواقع البروتيني انشقاق ذات الصلة وظيفيا. أدلى التجارب Biotinylation يقوم بالتوازي مع القياسات الكهربية من الممكن ربط ظهور ENAC الانقسام المنتجات على سطح الخلية مع تنشيط بروتين الحالي. هناك ارتباط بين بالطبع وقت التنشيط الحالية وظهور شظايا الانقسام بروتين على سطح الخلية تدعم مفهوم التنشيط قناة بروتين.
يومين القطب تسجيلات الجهد المشبك تتطلب التطويق من سocyte مع اثنين من microelectrodes. وعادة ما يتم تنفيذ هذا الإجراء مرة واحدة فقط في بويضة الفردية. ومع ذلك، كان من الممكن إزالة microelectrodes بعد خلية كاملة تسجيل الأولي الحالي دون ضرر واضح للبويضة. في الواقع، غشاء البلازما في مواقع التطويق يبدو أن ختم في غضون بضع دقائق. وهكذا، بعد الانتهاء من أول يومين القطب قياس الجهد المشبك، فمن الممكن لنقل البويضة من غرفة تدفق التجريبية من يومين القطب الإعداد الجهد المشبك إلى أنبوب microfuge أو بئر من لوحة 96 جيدا مليئة كمية صغيرة من الاختبار أو السيطرة الحل. بعد ذلك، ونفس البويضة يمكن نقلها إلى غرفة التدفق ويمكن مخوزق مرة أخرى لإجراء ثاني يومين القطب قياس الجهد المشبك. بشكل ملحوظ، لم التيارات ENAC بوساطة لا تختلف كثيرا بين القياس الأول والثاني عندما تمت المحافظة على البويضة في حل السيطرة. في المقابل، حضانة البويضة في البروتيني تحتوي على سولution بعد القياس الأول أسفر عن زيادة الحالي ENAC بوساطة في القياس الثاني (الشكل 2). هذه النتيجة تشير إلى تفعيل قناة بروتين.
أداء اثنين من القياسات الحالية منفصلة في بويضة واحدة يوفر ميزة أن البويضة يمكن أن يتعرض لالبروتياز أو وكلاء الدوائية الأخرى بين القياسين لفترة من الزمن المتغير في حجم صغير من محلول الاختبار. هذا هو المهم عند استخدام وكلاء والتي هي مكلفة و / أو غير متوفر بكميات كبيرة، مثل الاستعدادات البروتيني المنقى. محدودية توافر عوامل قد تجعل من المستحيل (أو لا يمكن تحمله) لاستخدامها في استمرار يومين القطب تسجيلات الجهد المشبك بسبب كميات كبيرة من محلول الاختبار المطلوبة لsuperfusing باستمرار البويضات مع معدلات تدفق من عدة ملليلتر في الدقيقة الواحدة. وعلاوة على ذلك، واثنين من القطب قياسات الجهد المشبك المستمر تقتصر من قبل ظاهرة معروفةينون عفوية قناة المتهدمة وصفها أيضا لENAC 15. في المقابل، كشف البويضات لاختبار الحلول بين اثنين من القياسات منفصلة لمدة تصل إلى ساعة أو أكثر لا يشكل مشكلة بصفة عامة (انظر الشكل 4A). أخيرا، واثنين من قياسات متتابعة يؤديها في نفس البويضة تسمح الملاحظات المقترنة من آثار المخدرات. هذا له ميزة على القياسات المفردة من مجموعتين منفصلتين من البويضات (المعاملة البروتيني والمعالجة السيارة)، لأنه يقلل من مشكلة التباين الشديد بين البويضات، لاحظ عادة في القناة الايونية التعبير. مع الملاحظات تقرن وإمكانية تطبيع البيانات إلى القياس الأول، وهناك حاجة إلى عدد أقل من البويضات في المجموعة التجريبية ليبرهن على وجود تأثير كبير لعامل الدوائية. تطبيع البيانات أيضا يجعل من السهل تلخيص البيانات من دفعات مختلفة من البويضات مع مختلف مستويات التعبير القناة الايونية والتيارات خط الأساس وبالتالي مختلفة (الشكل 2D). من الواضح، والتجارب السيطرة ضرورية لهذا النهج لإثبات أن النشاط قناة أيون ذات الاهتمام لا تزال مستقرة في البويضات ضبط تعامل مركبة من الأول إلى الثاني القياس (انظر الشكل 2).
لإثبات أن تفعيل بروتين يرتبط الحالي مع ظهور ENAC الانقسام المنتجات على سطح الخلية، وهو نهج biotinylation وصف في الأصل من قبل هاريس وآخرون. 9 يمكن استخدامها. وقد تم تكييف هذا الإجراء (كما هو مفصل في قسم البروتوكول ويظهر في الشكل 4) لإثبات أن التعرض للقنوات لالبروتياز وبموازاة تفعيل لاحقة من التيارات ENAC بوساطة من قبل تعتمد على الوقت مظهر من شظايا الانقسام. طريقة biotinylation يسمح أيضا تحليل زيادة أو نقصان الشاملة للبروتينات غشاء على سطح الخلية. وهكذا، وهذه الطريقة مناسبة للتحقيق في تأثير البروتياز وصيدلاني أخرىوكلاء macological على قناة الإدراج في غشاء البلازما أو عند استرجاع القناة. علاوة على ذلك، تحليل لطخة الغربي من البيروكسيديز بروتينات غشاء البلازما يسمح الكشف عن شظايا البروتين (مثل شظايا ENAC بروتين) أو تغييرات في نمط ارتباط بالغليكوزيل والتي قد تكون ذات صلة وظيفيا.
في الختام، فإن الجمع بين الأساليب المستخدمة لدراسة تأثير تنشيطية من البروتياز على ENAC بوساطة تيارات خلية كاملة لإثبات وجود علاقة مع وقوع انشقاق ENAC المنتجات على سطح الخلية قد تكون مفيدة لمجموعة واسعة من التطبيقات. على وجه الخصوص، قد تكون هذه الطرق المناسبة لمعالجة مسائل مماثلة بشأن تنظيم القنوات الأيونية الأخرى، نقل أو مستقبلات عبر الغشاء (على سبيل المثال تنشيط مستقبلات الأنزيم البروتيني بارس).
Disclosures
The authors have nothing to disclose.
Acknowledgements
The expert technical assistance of Céline Grüninger, Christina Lang, Sonja Mayer, and Ralf Rinke is gratefully acknowledged. We thank Dr. Morag K. Mansley for carefully reading the manuscript. This project was supported by a grant of the Deutsche Forschungsgemeinschaft (Grant SFB 423: Kidney Injury: Pathogenesis and Regenerative Mechanisms, to C. Korbmacher), grants of the Interdisziplinäres Zentrum für Klinische Forschung (to S. Haerteis and M. Krappitz), the ELAN program (to S. Haerteis) of the Friedrich-Alexander-Universität Erlangen-Nürnberg, and the University Library of Erlangen-Nürnberg.
Materials
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Bath clamp headstage for OC-725C-V | Warner Instrument Corporation | ||
| Cold light source - Schott KL 1500 LCD | Schott | #SCOC150200EU | brightness 4; mechanical aperture: D; color temperature: 3,000 K |
| E Series electrode holder (Str, Vent, Ag Wire, 1.2 mm) | ADinstruments | #ESW-F10v | |
| Left micromanipulator; MM-33L | Warner Instrument Corporation | #64-0055 | |
| LIH 1600 - computer interface | HEKA | ||
| Magnetic valve system (ALA BPS-8) in combination with a TIB14 interface (HEKA) | ALA Scientific Instruments, HEKA | ||
| OC-725C amplifier for two-electrode voltage-clamp recordings | Warner Instrument Corporation | ||
| P-97 FLAMING/BROWN Micropipette Puller | Sutter Instruments | heat = 550; velocity = 22; time = 200 | |
| Right micromanipulator; MM-33R | Warner Instrument Corporation | #64-0056 | |
| Series electrode holder (45°, Vent, Handle, Ag Wire, 1.2 mm) | ADinstruments | #E45w-f10vh | |
| STAT 2 IV gravity flow controller | Conmed | #P-S2V-60 | |
| Vacuum generator ejector SEG - for suction to remove bath solution | Schmalz | ||
| INFUJECT 60 ml pump syringes for solutions | Braun | #22050 | |
| Injekt-F for lysing the oocytes | Braun | #9166033V | |
| Standard wall borosilicate tubing with filament | Sutter Instruments | #BF150-86-10 | outside diameter: 1.5 mm; inside diameter: 0.86 mm; length: 10 cm |
| Complete, Mini, EDTA-free protease inhibitor cocktail tablets | Roche Applied Science | #11836170001 | |
| EZ-Link Sulfo-NHS-Biotin | Thermo Scientific | #21217 | |
| Horseradish peroxidase-labeled secondary goat anti-rabbit antibody | Santa Cruz Biotechnology | #sc-2004 | |
| NeutrAvidin Agarose | Thermo Scientific | #29200 | Neutravidin-labeled agarose beads |
| NP40 (Nonidet P-40) | Sigma-Aldrich | #I8896 | |
| Roti-Load 1 (2x SDS-PAGE sample buffer) | Carl Roth | #K929.2 | |
| SuperSignal West Femto Chemiluminescent Substrate for detection of chemiluminescent signals | Thermo Scientific | #34095 | |
| Triton-X-100 | Sigma-Aldrich | #T8787 |
References
- Kleyman, T. R., Carattino, M. D., Hughey, R. P. ENaC at the cutting edge: regulation of epithelial sodium channels by proteases. The Journal of Biological Chemistry. 284, 20447-20451 (2009).
- Rossier, B. C., Stutts, M. J. Activation of the epithelial sodium channel (ENaC) by serine proteases. Annu Rev Physiol. 71, 361-379 (2009).
- Poirot, O., Vukicevic, M., Boesch, A., Kellenberger, S. Selective regulation of acid-sensing ion channel 1 by serine proteases. The Journal of Biological Chemistry. 279, 38448-38457 (2004).
- Vukicevic, M., Weder, G., Boillat, A., Boesch, A., Kellenberger, S. Trypsin cleaves acid-sensing ion channel 1a in a domain that is critical for channel gating. The Journal of Biological Chemistry. 281, 714-722 (2006).
- Clark, E. B., Jovov, B., Rooj, A. K., Fuller, C. M., Benos, D. J. Proteolytic cleavage of human acid-sensing ion channel 1 by the serine protease matriptase. The Journal of Biological Chemistry. 285, 27130-27143 (2010).
- Ossovskaya, V. S., Bunnett, N. W. Protease-activated receptors: contribution to physiology and disease. Physiological reviews. 84, 579-621 (2004).
- Garcia-Caballero, A., et al. Activation of the epithelial sodium channel by the metalloprotease meprin β-subunit. Channels (Austin. 5, 14-22 (2011).
- Haerteis, S., et al. Proteolytic activation of the epithelial sodium channel (ENaC) by the cysteine protease cathepsin-S. Pflügers Archiv: European Journal of Physiology. 464, 353-365 (2012).
- Harris, M., Firsov, D., Vuagniaux, G., Stutts, M. J., Rossier, B. C. A novel neutrophil elastase inhibitor prevents elastase activation and surface cleavage of the epithelial sodium channel expressed in Xenopus laevis oocytes. The Journal of Biological Chemistry. 282, 58-64 (2007).
- Passero, C. J., Mueller, G. M., Rondon-Berrios, H., Tofovic, S. P., Hughey, R. P., Kleyman, T. R. Plasmin activates epithelial Na+ channels by cleaving the γ-subunit. The Journal of Biological Chemistry. 283, 36586-36591 (2008).
- Svenningsen, P., et al. Plasmin in nephrotic urine activates the epithelial sodium channel. Journal of the American Society of Nephrology : JASN. 20, 299-310 (2009).
- Patel, A. B., Chao, J., Palmer, L. G. Tissue kallikrein activation of the epithelial Na channel. American Journal of Physiology. Renal Physiology. 303, (2012).
- Haerteis, S., Krappitz, M., Diakov, A., Krappitz, A., Rauh, R., Korbmacher, C. Plasmin and chymotrypsin have distinct preferences for channel activating cleavage sites in the γ-subunit of the human epithelial sodium channel. The Journal of General Physiology. 140, 375-389 (2012).
- Chraibi, A., Vallet, V., Firsov, D., Hess, S. K., Horisberger, J. D. Protease modulation of the activity of the epithelial sodium channel expressed in Xenopus oocytes. The Journal of General Physiology. 111, 127-138 (1998).
- Volk, T., Konstas, A. A., Bassalay, P., Ehmke, H., Korbmacher, C. Extracellular Na+ removal attenuates rundown of the epithelial Na+-channel (ENaC) by reducing the rate of channel retrieval. Pflügers Archiv: European Journal of Physiology. 447, 884-894 (2004).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved