Method Article
أتمتة التجارب رقاقة وما يليها لتوليد الملامح جينية على خلايا هيلا 10،000
In This Article
Summary
Methods for mapping in vivo protein-DNA interactions are becoming crucial for every aspect of genomic research but they are laborious, costly, and time consuming. Here a commercially available robotic liquid handling system that automates chromatin immunoprecipitation for mapping in vivo protein-DNA interactions with limited amounts of cells is presented.
Abstract
Chromatin immunoprecipitation followed by next generation sequencing (ChIP-seq) is a technique of choice for studying protein-DNA interactions. ChIP-seq has been used for mapping protein-DNA interactions and allocating histones modifications. The procedure is tedious and time consuming, and one of the major limitations is the requirement for high amounts of starting material, usually millions of cells. Automation of chromatin immunoprecipitation assays is possible when the procedure is based on the use of magnetic beads. Successful automated protocols of chromatin immunoprecipitation and library preparation have been specifically designed on a commercially available robotic liquid handling system dedicated mainly to automate epigenetic assays. First, validation of automated ChIP-seq assays using antibodies directed against various histone modifications was shown, followed by optimization of the automated protocols to perform chromatin immunoprecipitation and library preparation starting with low cell numbers. The goal of these experiments is to provide a valuable tool for future epigenetic analysis of specific cell types, sub-populations, and biopsy samples.
Introduction
كما أصبحت الجيل التالي من التسلسل (NGS) التقنيات على نطاق واسع وأيسر منالا، والطريقة الأساسية لرسم خرائط الجينوم على نطاق التفاعلات-DNA البروتين لونين الآن مناعي تليها الكشف NGS (رقاقة وما يليها)، والتي تمكن من اكتشاف عامل النسخ مواقع أو أنماط من التعديلات هيستون ملزمة. رقاقة وما يليها هو مفيد في توفير بيانات عالية الإنتاجية من الجينوم بأكمله والتي يمكن استخدامها للتحليل الكمي والنوعي للتفاعلات-DNA البروتين عن طريق قياس شظايا الحمض النووي المخصب. ومع ذلك، هناك بعض العيوب في التجارب رقاقة وما يليها القياسية مثل صعوبة في الحصول على ما يكفي من المواد لإنشاء مكتبة التسلسل.
وتنقسم التجارب الشذرة إلى ستة الخطوات الأساسية بما في ذلك المناطق ملزمة 1) يشابك البروتين DNA 2) إعداد العينات التي تضم تحلل الخلايا والقص لونين من قبل صوتنة، 3) تشكيل immunocomplexes،4) هطول الأمطار من immunocomplexes، 5) غسل immunocomplexes، و6) شطف من اليورانيوم المخصب وتحليلها من قبل QPCR وNGS.
نجاح مقايسة الشذرة يعتمد على ثلاثة عوامل رئيسية هي: التحضير الجيد لونين، وكمية المستضد في العينة الأصلية، وخصوصية وتقارب من الأجسام المضادة للمستضد لها وما شابه ذلك. وجود قيود الرئيسي هو شرط لكميات عالية من بدء أعداد الخلايا من أجل الحصول على ما يكفي من الحمض النووي المخصب لإنشاء مكتبة التسلسل. للعلماء الذين يعملون مع كميات عينة محدودة، مثل عينات الخزعة أو خلية السكان الفرعية، والتجارب رقاقة وما يليها هي صعبة للغاية. وقد أظهرت الدراسات الحديثة أن المقايسات رقاقة وما يليها يمكن أن يؤديها عند العمل مع كمية قليلة من الخلايا 1 و 2. وقد وضعت Diagenode نظام الروبوتية معالجة السائل الذي يمكن أتمتة تماما التجارب رقاقة وما يليها عند البدء مع عدد محدود من الخلايا.
يوفر أتمتةمزايا عديدة أكثر من إعداد دليل للعينات رقاقة وما يليها كما أنه يقلل الأخطاء البشرية، ويقلل من التباين، ويقلل من تكلفة التجريبية. تم الإبلاغ عن بروتوكولات الآلي نصف لمناعي الكروماتين وإعداد مكتبة ولكن أيا من هذه الدراسات أظهرت البيانات عند استخدام أرقام الهواتف المحمولة منخفضة 3، 4، 5، 6.
في هذه الورقة يتم وصف سير العمل الآلي الكامل لكل من لونين مناعي وإعداد المقايسات مكتبة في نظام مناولة السائل الروبوتية التي تستخدم التكنولوجيا القائمة على حبة المغناطيسية والتي يمكن أن تعالج معلمات متعددة في تحسين البروتوكول. هنا، وأجريت التجارب رقاقة وما يليها الآلي بنجاح على عدد محدود من الخلايا مع هدف تبسيط وتوحيد، وتوفير حل موثوق بها لدراسة ملامح جينية في السكان الخلية الصغيرة. وقد تم تحسين بروتوكول الشذرة الآلي وصفها في هذه الورقة على خلايا هيلا باستخدام الأجسام المضادة هيستون محددة والكواشف بالتحرير سير العمل يمكن تكييفها لخطوط الخلايا الأخرى، والأجسام المضادة مع المقابلة الأمثل التجريبية.
Protocol
1. التجارب ستاندرد الشذرة
- جمع الخلايا والحمض النووي والبروتينات يشابك.
- تنمو خلايا هيلا-S3 لالتقاء مجموعة من 80٪ -90٪. إزالة مستنبت، وغسل الطبق مرتين مع 10 مل من الفوسفات 1X مخزنة المالحة (PBS)، وإضافة التربسين-EDTA (1X) لوحة مثقف. احتضان لمدة أقصاها 2 دقيقة لفصل الخلايا من الطبق. جمع الخلايا ويغسل مرتين مع 10 مل PBS.
سيؤدي أطول الأوقات الحضانة إلى تلف الخلايا: ملاحظة. - الطرد المركزي الخلايا لمدة 5 دقائق في 500 x ج و resuspend الخلايا في 20 مل من برنامج تلفزيوني. الشروع في عدد الخلايا.
- الطرد المركزي الخلايا لمدة 5 دقائق في 500 x ج، تجاهل طاف وإضافة 500 ميكرولتر من برنامج تلفزيوني. العدد الأمثل من الخلايا للخطوة التثبيت هو 10 مليون خلية لكل 500 ميكرولتر من برنامج تلفزيوني.
- إضافة 13.5 ميكرولتر من الطازجة الفورمالديهايد 37٪ في كل قسامة من 500 ميكرولتر من التعليق الخلية. يحملق الخلايا لمدة 8 دقائق في RT.
- إضافة 57 ميكرولتر من 1.25 M جليكاين solutأيون لوقف التثبيت. احتضان لمدة 5 دقائق على RT مع الخلط المستمر من قبل دوامة لطيف. العمل على الجليد من هذه النقطة فصاعدا.
- الطرد المركزي الخلايا في 500 x ج لمدة 5 دقائق في 4 درجات مئوية، وتجاهل طاف دون الإخلال بيليه الخلية.
- غسل الخلايا مرتين مع 1 مل PBS. تجاهل بلطف طاف والحفاظ على بيليه الخلية على الجليد.
- تنمو خلايا هيلا-S3 لالتقاء مجموعة من 80٪ -90٪. إزالة مستنبت، وغسل الطبق مرتين مع 10 مل من الفوسفات 1X مخزنة المالحة (PBS)، وإضافة التربسين-EDTA (1X) لوحة مثقف. احتضان لمدة أقصاها 2 دقيقة لفصل الخلايا من الطبق. جمع الخلايا ويغسل مرتين مع 10 مل PBS.
- تحلل الخلايا والكروماتين القص
- إضافة 10 مل من تحلل الباردة الجليد IL1 العازلة لبيليه الخلية (1 مل من العازلة تحلل لكل 1 مليون خلية هي النسبة المثلى). ماصة صعودا وهبوطا عدة مرات واحتضان لمدة 10 دقيقة في 4 درجات مئوية مع الخلط لطيف.
- الطرد المركزي المحللة لمدة 5 دقائق في 500 x ج و 4 ° C. تجاهل طاف.
- إضافة 10 مل من تحلل العازلة الجليد الباردة IL2 لللست] وتخلط بلطف بواسطة pipetting صعودا وهبوطا. احتضان لست] لمدة 10 دقيقة في 4 درجات مئوية.
- أجهزة الطرد المركزي لمدة 5 دقائق في 500 x ج و 4 درجات مئوية، وتجاهل طاف.
- Prepaإعادة المخزن المؤقت القص الكامل إضافة 200X كوكتيل مثبط البروتياز (PIC) إلى المخزن المؤقت القص IS1. إبقاء عازلة على الجليد لمدة 5 دقائق، والعمل على الجليد بعد ذلك. إضافة 1 مل من كامل IS1 عازلة القص لكل 10 ملايين الخلايا بيليه وتخلط بلطف بواسطة pipetting صعودا وهبوطا. قبل صوتنة احتضان العينات على الجليد لمدة 10 دقيقة للحد من اللزوجة من العينة.
- القص 300 مكل من لونين من قبل صوتنة باستخدام sonicator باث الماء لمدة 2 إلى 3 مجموعات من 10 دورات لكل منهما. تتكون دورة من 30 ثانية "ON" و30 ثانية "OFF" على وضع السلطة عالية. بدلا من ذلك، استخدام جهاز بيكو-صوتنة مع وقت أقصر صوتنة من 5 إلى 10 دورات من 30 ثانية "ON"، 30 ثانية "OFF". لفترة وجيزة دوامة وتدور الأنابيب بين أشواط. عند استخدام أنواع أخرى من sonicators، اتبع تعليمات الشركة الصانعة المقابلة لونين القص.
- أجهزة الطرد المركزي لونين المنفصمة في 16،000 x ج لمدة 10 دقيقة وجollect طاف لاستخدامها على الفور في خطوة IP. بدلا من ذلك، تخزين لونين في -80 درجة مئوية لمدة تصل إلى 2 أشهر لاستخدامها في المستقبل.
- تحليل كفاءة القص الكروماتين قبل خطوة مناعي باستخدام 1-1.5٪ المواد الهلامية TAE الاغاروز أو bionalyzer. وتتراوح أحجام جزء ونين المثلى بين 100-600 نقطة أساس.
2. منخفضة التجارب رقاقة الخلية
- جمع الخلايا والحمض النووي والبروتينات يشابك
- تنمو خلايا هيلا-S3 لالتقاء مجموعة من 80٪ -90٪. إزالة مستنبت، وغسل الطبق مرتين مع 10 مل من الفوسفات 1X مخزنة المالحة (PBS)، وإضافة 1X التربسين-EDTA لوحة مثقف. احتضان لمدة أقصاها 2 دقيقة لفصل الخلايا من الطبق.
سيؤدي أطول الأوقات الحضانة إلى تلف الخلايا: ملاحظة. - جمع الخلايا عن طريق إضافة 1 مل مستنبت المحتوية على مصل في أنبوب الطرد المركزي 1 مل. عدد الخلايا.
- الطرد المركزي الخلايا لمدة 5 دقائق في 500 × ز. جلب عدد الخلاياإلى 10،000 الخلايا لكل مل من مستنبت للتثبيت.
- إضافة 27 ميكرولتر من 36.5٪ الفورمالديهايد مستعد جديدة في كل أنبوب للتثبيت. عكس الأنبوب مرتين أو ثلاث مرات، واحتضان 10 دقيقة في RT.
- إضافة 115 ميكرولتر من 1.25 M حل الجلايسين لعينة، عكس الأنبوب مرتين أو ثلاث مرات، واحتضان 5 دقائق على RT. العمل على الجليد من هذه النقطة فصاعدا.
- الطرد المركزي الخلايا في 300 x ج لمدة 10 دقيقة على 4 درجات مئوية. تجاهل طاف ببطء.
- غسل الخلايا مع 1 مل الجليد الباردة HBSS مع الموافقة المسبقة عن علم (200X، وتركيز النهائي 1X). عكس الأنبوب مرتين أو ثلاث مرات إلى resuspend الخلايا وأجهزة الطرد المركزي في 300 x ج لمدة 10 دقيقة على 4 درجات مئوية. تجاهل بلطف طاف والحفاظ على بيليه الخلية على الجليد.
- تنمو خلايا هيلا-S3 لالتقاء مجموعة من 80٪ -90٪. إزالة مستنبت، وغسل الطبق مرتين مع 10 مل من الفوسفات 1X مخزنة المالحة (PBS)، وإضافة 1X التربسين-EDTA لوحة مثقف. احتضان لمدة أقصاها 2 دقيقة لفصل الخلايا من الطبق.
- تحلل الخلايا والكروماتين القص
- إضافة 25 ميكرولتر من كامل الاحتياطي تحلل TL1 (الاحتياطي تحلل TL1 + PIC) لكل 10،000 الخلايا وتستنهض الهمم يدويا السفلي من الأنبوب إلى resuspend الخلايا. احتضان على الجليد لمدة 5 دقائق.
- إضافة 75 ميكرولتر من HBSS كاملة (HBSS + PIC) العازلة في كل قسامة تحتوي على 10،000 الخلايا.
- القص 100 مكل من 10،000 الخلايا عن طريق صوتنة لمدة 5 مجموعات من 5 دورة لكل منهما. تتكون دورة من 30 ثانية "ON" و30 ثانية "OFF" على وضع السلطة عالية. بدلا من ذلك، استخدام جهاز بيكو-صوتنة استخدامها مع الوقت صوتنة أقصر من 5 دورات من 30 ثانية "ON"، 30 ثانية "OFF". وتتراوح أحجام جزء ونين المثلى بين 100-600 نقطة أساس. لاحظ أن الاستعدادات لونين، أنواع الخلايا وsonicators مختلفة تتطلب تجارب القص الأمثل منفصلة.
- أجهزة الطرد المركزي لونين المنفصمة في 14،000 x ج لمدة 10 دقيقة للتخلص من المواد غير القابلة للذوبان وجمع طاف لاستخدامها على الفور في خطوة IP. بدلا من ذلك، تخزين لونين في -80 درجة مئوية لمدة تصل إلى 2 أشهر لاستخدامها في المستقبل.
- تحليل كفاءة القص الكروماتين قبل خطوة مناعي باستخدام 1-1.5٪ TAE المواد الهلامية الاغاروز أووbionalyzer. عينات علاج مع ريبونوكلياز قبل الاغاروز تحليل هلام من أجل تحسين تقييم البصري من القص. وتتراوح أحجام جزء ونين المثلى بين 100-600 نقطة أساس.
3. مناعي لونين ومكتبة الإعدادية
- لمعيار الآلي التجارب الشذرة
- إضافة 120 ميكرولتر من رقاقة العازلة H (رقاقة العازلة H + PIC) إلى 100 ميكرولتر المنفصمة لونين. استخدام 200 ميكرولتر لIP والحفاظ على 2 ميكرولتر إلى 20 ميكرولتر كما عينة الإدخال.
- حدد الآلي الشذرة 200 بروتوكول ميكرولتر في الصك الأتمتة. الإنتاجية للبروتوكول من 1 إلى 16 عينة في التشغيل.
- تشغيل تجربة الشذرة الآلي باستخدام، لونين المقابلة إلى 1-2 مليون خلية، 1-2 ميكروغرام المضادة للH3K79me3، الصف -H3K27me3، -H3K4me3، -H3K4me2، -H3K9ac، -H3K9 / 14ac، -H3K36me3 وH3K9me3 رقاقة وما يليها أرنب الأجسام المضادة. كميات الأجسام المضادة المثلى تختلف تبعا لتعديل هيستون وتقارب والمواصفاتificity من الأجسام المضادة المقابلة.
- استخدام كميات متساوية من غير المحصنين مفتش أرنب بمثابة الضد isotype السيطرة. بدلا من ذلك، استخدام الخرز المصقول أو الأجسام المضادة المحددة منعت عناصر تحكم رقاقة. إضافة 20 ميكرولتر من البروتين-A حبات مغناطيسية المغلفة لكل رد فعل.
- استخدام هيستون الآلي رقاقة وما يليها الكواشف عدة لإجراء تجارب الشذرة الآلي مع anti-H3K79me3 و-H3K4me2 الأجسام المضادة. استخدام مثالية الكواشف عدة رقاقة وما يليها لإجراء تجارب رقاقة مع مكافحة H3K27me3، -H3K4me3، -H3K9ac، -H3K9 / 14ac، -H3K36me3 و-H3K9me3.
- حدد البروتوكول الشذرة الآلي اتباع التعليمات البرامج التي تنفذ في الجهاز الآلي. تعيين المعلمات التجريبية الشذرة إلى 4 ساعات للخطوة الأجسام المضادة الطلاء و 15 ساعة للخطوة مناعي. الخطوة يشابك العكس يحدث في الصك الآلي عند 65 درجة مئوية لمدة 4 ساعات.
- تنقية الحمض النووي عبر ربط العكسي على النظام الآلي. حدد AUTبروتوكولات omated لتنقية الحمض النووي مع بروتوكول أو عدة تستخدم المغناطيسية تنقية الحمض النووي استنادا حبة. أزل الحمض النووي في 25 ميكرولتر من الماء.
- قياس DNA immunoprecipitated عن طريق استخراج 10٪ من الحمض النووي immunoprecipitated. العائد DNA immunoprecipitated يعتمد على نوعية من لونين والأجسام المضادة، نوع من الخلايا وتعديل هيستون الهدف. قياس الحمض النووي باستخدام طقم الفحص وفقا لتعليمات الشركة الصانعة.
- تحليل نوعية الحمض النووي immunoprecipitated بواسطة PCR الكمي باستخدام بادئات لا يقل عن 1 إيجابي و1 السيطرة السلبية المناطق الجينومية. لا تستخدم أكثر من 10٪ من إجمالي DNA immunoprecipitated لتقييم التخصيب الشذرة.
- إعداد ردود الفعل QPCR. إضافة 10 ميكرولتر من مزيج الرئيسي 2X SyberGreen QPCR، 1 ميكرولتر من مزيج التمهيدي، 1-5 ميكرولتر من الحمض النووي immunoprecipitated أو المدخلات والماء المعقم تصل إلى 20 ميكرولتر حجم رد الفعل النهائي. ويتضمن البرنامج QPCR خطوة تمسخ الأولي في 95 ° Cلمدة 5-10 دقيقة اعتمادا على مقدم البلمرة طق ويجب تعيين درجات الحرارة الصلب وفقا لالاشعال المحدد.
- استخدام بروتوكولات الآلي مكتبة الإعدادية متوافقة مع المتاحة تجاريا الكواشف إعداد مكتبة البورشيد رقاقة وما يليها لبناء المكتبات باستخدام كل رقاقة الحمض النووي وكذلك DNA المدخلات المحفوظة من نفس التحضير لونين. استخدام 10-20 نانوغرام من الحمض النووي immunoprecipitated من كل الأجسام المضادة لإعداد مكتبة. إعداد ما يصل إلى 16 المكتبات الآلي في التشغيل.
- تسلسل المكتبات وتوليد مجموعات وفقا لتعليمات البورشيد الشركة الصانعة. لتحليل الأساسي المعلوماتية الحيوية (تصفية العنقودية، الدعوة القاعدة، وما إلى ذلك) في أعقاب القياسية البورشيد خط أنابيب، تصفية ومحاذاة يقرأ لأحدث التجمع الجينوم البشري (الإصدار الحالي هو GRCh38) مع اليجنر إلاند. استخدام SICER 7 أو 8 MACS لذروة الدعوة وإجراء التحليلات المصب من قمم ثإيث هوميروس 9، 10 BEDTools أو البرامج المفضلة.
- للحصول على رقم الآلي خلية منخفضة التجارب الشذرة
- إضافة 120 ميكرولتر من كامل عازلة الشذرة TC1 (رقاقة العازلة TC1 + PIC) إلى 100 ميكرولتر المنفصمة لونين. استخدام 200 ميكرولتر لIP والحفاظ على 20 ميكرولتر كإدخال.
- حدد الآلي الشذرة 200 بروتوكول ميكرولتر في نظام التشغيل الآلي. الإنتاجية للبروتوكول من 1 إلى 16 عينة في التشغيل.
- تشغيل تجربة رقاقة وما يليها الآلي باستخدام الكواشف الشذرة الآلي والأجسام المضادة الصف رقاقة الأمثل للعمل على كميات الكروماتين منخفضة. استخدام لونين الموافق 10،000 100،000 الخلايا والخلايا، 0.5 ميكروغرام من مكافحة H3K27me3، 0.25 ميكروغرام -H3K4me3، 0.1 ميكروغرام -H3K27ac، 0.25 ميكروغرام -H3K9me3 أرنب قسط رقاقة وما يليها الصف الأجسام المضادة بولكلونل الأرنب. كميات الأجسام المضادة المثلى تختلف تبعا لتعديل هيستون وتقارب وخصوصية من الأجسام المضادة المقابلة.
- استخدام كمية مساوية من رب غير المحصنينمفتش بت الضد isotype السيطرة. بدلا من ذلك، استخدام الخرز المصقول أو الأجسام المضادة المحددة منعت عناصر تحكم رقاقة. إضافة 10 ميكرولتر من البروتين-A حبات مغناطيسية المغلفة لكل رد فعل.
- حدد البروتوكول الشذرة الآلي اتباع التعليمات البرامج التي تنفذ في الجهاز الآلي. تعيين المعلمات التجريبية الشذرة إلى 4 ساعات للخطوة الأجسام المضادة الطلاء و 15 ساعة للخطوة مناعي. الخطوة يشابك العكس يحدث في الصك الآلي عند 65 درجة مئوية لمدة 4 ساعات.
- تنقية العكسي DNA عبر ربط باستخدام الأعمدة تدور التالية تعليمات الشركة الصانعة وأزل في أحجام الفترة من 6 إلى 25 ميكرولتر ميكرولتر من الماء.
- قياس الحمض النووي باستخدام طقم الفحص التجارية. تحليل النتائج وفقا لQPCR باستخدام بادئات للمناطق الإيجابية والسلبية التحكم لتقييم جودة الشذرة.
- استخدام إعداد ملف المكتبة مع الكواشف إعداد مكتبة الأمثل لإعداد المكتبات مع انخفاض تشيوان DNAعلى كميات. استخدام 30 خريج و 300 خريج من رقاقة الحمض النووي (الموافق 10،000 و 100،000 خلايا التجارب على التوالي) لإعداد مكتبة. إعداد مكتبات باستخدام بروتوكول الآلي متوافق مع الكواشف إعداد المكتبات. المكتبة الآلي الإعدادية الإنتاجية هي 1-48 المكتبات في التشغيل.
- بعد إصلاح نهاية قوالب DNA المزدوج تقطعت بهم السبل، ligate شطورة محولات الجذعية حلقة تحتوي على المواقع التمهيدي التسلسل. في أعقاب خطوة التمديد DNA، تضخيم عينة مع أسلوب التضخيم عالية الدقة وصفها في مكتبة بروتوكول إعداد عدة.
- بعد التضخيم مكتبة وقياس وتنقية المكتبات التالية المبادئ التوجيهية إعداد عدة المكتبة. لاحظ أن اختيار الحجم بعد تنقيتها ليست ضرورية.
- تسلسل المكتبات وتوليد مجموعات وفقا لتعليمات الشركة الصانعة. لتحليل الأساسي المعلوماتية الحيوية (تصفية العنقودية، الدعوة القاعدة، وما إلى ذلك) في أعقاب موقفخط أنابيب مصنع ARD والتصفية، ومحاذاة يقرأ لأحدث التجمع الجينوم البشري (الإصدار الحالي هو GRCh38) مع اليجنر إلاند 7. استخدام SICER 8 أو 9 MACS لذروة الدعوة وإجراء التحليلات المصب من قمم مع هوميروس، BEDTools 10، أو أي برنامج المفضل.

الشكل 1. لقطات من البرنامج تبين كيفية إعداد التجارب رقاقة الآلي في العهد IP-ستار. البرنامج يوفر المرونة اللازمة لتحديد كمية عينة في المدى فضلا عن تغيير معالم التجريبية الرئيسية (الضد طلاء، IP ويغسل ) وفقا لاحتياجات الباحث. يسمح الإجراء الآلي اختبار ظروف مختلفة بالتوازي (أي أنواع مختلفة وكميات من الأجسام المضادة، وأنواع مختلفة وكميات من الخلايا ور حتى مختلفypes وكميات من حبات مغناطيسية في نفس المدى. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.

الشكل 2. لقطات من البرنامج تبين كيفية إعداد إعداد مكتبة الآلي للجيل القادم التسلسل استخدام عدة مكتبة في نظام التشغيل الآلي. يرجى النقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
النتائج
تحسين تجارب رقاقة وما يليها الآلي لمدة ثماني علامات هيستون مختلفة
من أجل تطوير بنجاح والتحقق من صحة البروتوكولات الشذرة الآلي، والأجسام المضادة الصف رقاقة وما يليها التي تم التحقق من صحتها من قبل في تجارب اليدوية رقاقة تسلسل (لا تظهر البيانات) وقد تم اختيار. وقد تم اختيار الأجسام المضادة الصف رقاقة وما يليها التالية لهذه الدراسة: مكافحة H3K79me3، -H3K27me3، -H3K4me3، -H3K4me2، -H3K9ac، -H3K9 / 14ac، -H3K36me3 و-H3K9me3. وأكد على خصوصية كل الأجسام المضادة الصف رقاقة وما يليها من قبل لطخة نقطة، صفائف الببتيد والتجارب البقعة الغربية (لا تظهر البيانات). وأجريت التجارب الرائدة الشذرة-QPCR مع زيادة كميات الأجسام المضادة لتحديد حساسية الأجسام المضادة (الشكل 3). QPCR مع اثنين على الأقل إيجابية وهدفين سيطرة سلبية وقد تم تحليل وملامح مع التخصيب الإيجابية على الهدف السلبي أعلى من خمسة أضعاف مؤهلون لتسلسل والخبير iments. من المهم لأداء رقاقة ورقاقة وما يليها التجارب مع جودة عالية من لونين المنفصمة. أجريت جميع التجارب الشذرة هو مبين في هذا المنشور باستخدام لونين الطازجة. ومن الممكن أيضا لتجميد الخلايا الثابتة في -80 ° C والمضي قدما في التحضير لونين والقص في يوم مختلف. ومع ذلك، لونين أعد من خلايا ثابتة المجمدة قد تتصرف بشكل مختلف من لونين الطازجة، وبالتالي قد يحتاج إلى أن يكون الأمثل لكل إعداد لونين الظروف صوتنة. عند العمل مع أنواع مختلفة من الخلايا، ومخازن القص مع تركيبة المنظفات المختلفة (SDS) يمكن استخدامها. أنواع الخلايا مثل خطوط الخلايا الأولية أو خلية تزرع في تعليق هي خلايا صعبة للقص وسوف تتطلب تركيزات عالية SDS (1٪) في حين خطوط الخلايا التي يسهل القص مثل هيلا سيتطلب تركيزات منخفضة SDS (0.1٪) في مخازن القص.
res.jpg "/>
الشكل 3. التحقق من الأجسام المضادة الشذرة الصف باستخدام نظام الأتمتة. تم تنفيذ الشذرة مع anti-H3K79me3، -H3K27me3، -H3K4me3، -H3K4me2، -H3K9ac، H3K9 / 14ac، -H3K36me3 و-H3K9me3 الأجسام المضادة الأرنب بولكلونل على لونين المنفصمة من 1 مليون دولار خلايا هيلا-S3 اعتمادا على التعديلات هيستون. واستخدمت بروتوكولات الشذرة الآلي مع وحدات التخزين العمل 200 ميكرولتر في الصك الآلي للتجارب الأجسام المضادة المعايرة. تم اختبار الأجسام المضادة كميات من 1، 2، 5 و 10 ميكروغرام في التجربة الشذرة واستخدمت 2 ميكروغرام مفتش كما سيطرة سلبية في كل تجربة. تم تقييم التخصيب التي كتبها QPCR. وتظهر نتائج كنسبة مئوية من المدخلات (المبلغ النسبي من الحمض النووي DNA immunoprecipitated مقارنة المدخلات بعد تحليل QPCR). الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
بعد التأكد من صحتها وتحديد أوبتيما كميات لتر من الأجسام المضادة الشذرة الصف لاستخدامها في نظام التشغيل الآلي، وأجريت التجارب رقاقة وما يليها الآلي من أجل إنشاء ملفات تعريف التسلسل لكل التعديل هيستون (الشكل 4).

الشكل 4. هيستون رقاقة وما يليها محات المتولدة عن تجارب رقاقة وما يليها الآلي. ويوضح الشكل لمحات رقاقة وما يليها في المناطق الجينومية مختلفة لH3K4me3، H3K9ac وH3K9 / 14acH3K4me2 H3K79me3، وH3K36me3. يظهر 4A توزيع الذروة على طول X الكامل -chromosome و4B التوزيع في منطقة 75 كيلو بايت المحيطة الجينات GAPDH. يظهر 4C لمحات من H3K27me3، H3K36me3 وH3K4me3 في منطقة 500 كيلو بايت المحيطة الجين MYT1 و4D يظهر توزيع H3K9me3 في ZNF12 المحيطة 200 كيلوبايت المنطقة.large.jpg "الهدف =" _ فارغة "> الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
تم إنشاء هيستون ملامح جينية لمدة ستة التعديلات هيستون مختلفة تترافق مع التعبير الجيني (H3K4me3، H3K9ac، H3K9 / 14ac، H3K4me2، H3K79me3 وH3K36me3). ويبين الشكل 4A ملامح رقاقة وما يليها على طول الكروموسوم X لعلامات هيستون مختلفة. العلاقة ذروة عالية لوحظ بين 6 محات هيستون المختلفة يدل على قدرات نظام آلي لتوليد بيانات دقيقة وموثوق بها. الشكل 4B، 4C و 4D تظهر توزيع قمم للتعديلات هيستون مختلفة في المناطق الجينومية محددة.
الآلي التجارب الكروماتين مناعي وصولا الى 200 خلية
الحد الأدنى من الخلايا التي يمكن استخدامها في التجارب الشذرة يعتمد على نوعية من لونين، وspecificitذ وحساسية الأجسام المضادة وفرة من التعديل هيستون أو البروتين دراستها. اختيار الأجسام المضادة جيدة رقاقة وما يليها الصف المهم عند العمل مع كميات محدودة من العينة واختيار الكواشف الأمثل وشركات مختلفة يحسن كفاءة الانتعاش DNA والمساهمة في نجاح التجربة الشذرة. لتحديد الحد الأدنى من الخلايا التي بروتوكول الشذرة الآلي يمكن معالجة كميات مختلفة من لونين، الأجسام المضادة، وحبات مغناطيسية تم اختبارها في النظام الآلي IP-ستار باستخدام الكواشف الشذرة على وجه التحديد الأمثل للعمل مع كميات منخفضة من لونين.
أولا، كان sonicated لونين من 10،000 الخلايا كما هو موضح في البروتوكول. تم تأكيد النتائج الشذرة التي كتبها QPCR (الشكل 5A) مما يدل على التخصيب كبيرة مع H3K4me3 الأجسام المضادة في مناطق السيطرة الإيجابية وإشارة تذكر في مناطق سيطرة سلبية. وعلى سبيل المقارنة وإثبات الاتساق، additionaوتقدم البيانات التي تم الحصول عليها لتر مع H3K27ac، H3K9me3، والأجسام المضادة H3K27me3، وذلك باستخدام 10،000 الخلايا.
وأجريت التجارب الشذرة الآلي ثم لإثبات قدرات النظام الآلي للعمل مع كميات منخفضة من الخلايا باستخدام نفس H3K4me3 الأجسام المضادة. رقاقة الآلي أداء جيدا، ويتجلى ذلك سلسلة من عشرة ردود الفعل IP التي كانت استنساخه وقابلة للمقارنة إلى حد كبير مع اليدوية النتائج الشذرة (الشكل 5B). وأجريت التجارب اليدوية والآلية وشوهدت فوائد البروتوكولات الآلي في الحد من تجربة إلى تجربة تقلب (الشكل 5C).
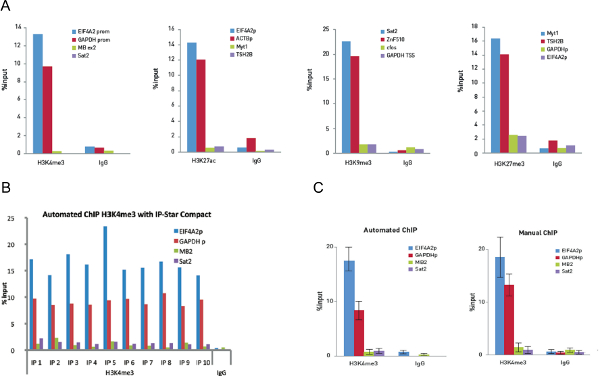
الشكل 5. الأمثل من رقاقة والسيارات رقاقة تجارب على خلايا 10،000 أجريت التجارب الشذرة دليل على 10،000 الخلايا وباستخدام 0.25 ميكروغرام من H3K4me3، 0.1 ميكروغرام من H3K27ac، و 0.5 ميكروغرام من H3K9me3 و 0.25 ميكروغرام من الأجسام المضادة H3K27me3. واستخدمت كميات مماثلة من أرنب مفتش كمجموعة تحكم. تم إجراء QPCR مع الاشعال لمدة مواضع إيجابي واثنين من مواضع السلبي لكل مقايسة الشذرة. ويبين الشكل 5A الانتعاش، كنسبة مئوية من المدخلات (المبلغ النسبي من الحمض النووي DNA immunoprecipitated مقارنة المدخلات بعد تحليل QPCR). الشكل 5B العروض 10 ردود الفعل رقاقة تعمل على النجوم IP المدمجة باستخدام 0.25 ميكروغرام H3K4me3 الأجسام المضادة بولكلونل و 0.25 ميكروغرام من أرنب مفتش سيطرة سلبية لأنه الأجسام المضادة. ثم تم إجراء تحليل QPCR مع الاشعال للالإيجابي المروج مواضع EIF4A2 وGAPDH TSS والسلبية مواضع الميوجلوبين exon2 وSAT2. ويوضح الشكل الانتعاش، معبرا عنه كنسبة مئوية من المدخلات (مبلغ النسبي من الحمض النووي DNA immunoprecipitated مقارنة المدخلات بعد تحليل QPCR). ويبين الشكل 5C البيانات H3K4me3 الشذرة من 10 تجارب الشذرة اليدوية بالمقارنة مع 10 رقاقة التجارب الآلي. أشرطة الخطأ تمثل الصورة الانحرافات tandard كل من مكررات عشرة. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
من أجل فهم حساسية البروتوكولات الشذرة الآلي، وأجريت التجارب باستخدام مبلغ من الخلايا التي تراوحت بين 100،000 الى 200 خلية لكل IP. تم استخدام الأجسام المضادة لمكافحة H3K27me3 كما هو تعديل هيستون شائع جدا. استخدام أخرى هيستون أو عدم هيستون الأجسام المضادة قد تتطلب خلايا أكثر أو أقل، اعتمادا على وفرة حاتمة ونوعية الأجسام المضادة. تم التحقق من صحة التجارب التي كتبها الكمي PCR ولوحظ أن من خلال تقليل كميات من الخرز والخلفية الأجسام المضادة في التجارب يتم تخفيض السماح نتائج ناجحة الشذرة-QPCR مع اقل من 200 خلية الأجسام المضادة (الشكل 6).
ديزيل / ftp_upload / 52150 / 52150fig6highres.jpg "/>
الشكل 6. الآلي المقايسات رقاقة على 200 خلية. خلايا هيلا-S3 والأجسام المضادة الموجهة ضد H3K27me3. تم المنفصمة لونين من 1 مليون خلية والتخفيفات المسلسل من هذه الكروماتين (من 100،000 إلى 200 أي ما يعادل الخلية) استخدمت في رد الفعل الشذرة. واستخدمت 1 ميكروغرام من H3K27me3 و 10 ميكرولتر من البروتين المغلفة وحبات مغناطيسية على التجربة 100،000 الخلايا، 0.5 ميكروغرام من H3K27me3 و 10 ميكرولتر من الخرز على 10،000 و 1،000 خلايا، و 0.25 ميكروغرام من H3K27me3 و 5 ميكرولتر من الخرز مع 500 و 200 الخلايا. استخدمت 1 ميكروغرام و 0.5 ميكروغرام من أرنب مفتش كما سلبي تحكم الأجسام المضادة عند إجراء التجارب مع 100،000 الخلايا وخلايا 1،000 على التوالي. ويظهر 6A إشغال TSH2B وGAPDH الجينات في المائة خلال الإدخال. يظهر 6B الإشغال النسبي للTSH2B مقابل السيطرة GAPDH السلبية المنطقة الجينومية.
تحليل المصب من النتائج الشذرة وما يليها على10،000 خلايا
من أجل تقييم الجودة العالمية من التجارب الآلي رقاقة وما يليها مع أرقام انطلاق منخفضة من الخلايا، وأجريت فحوصات الآلي رقاقة وما يليها مع 0.25 ميكروغرام من الأجسام المضادة H3K4me3 على 10،000 خلايا هيلا والتجارب رقاقة على واستخدمت 100،000 خلايا هيلا-S3 كما السيطرة الإيجابية للتجربة. تم إعداد المكتبات الآلي باستخدام مكتبة MicroPlex الكواشف إعداد عدة تتكيف مع المكتبات مستعدة مع كميات DNA منخفضة. لاحظ أنه على الرغم من أنه من الممكن أن تؤدي ناجحة الآلي الشذرة-التجارب مع أقل من 10،000 الخلايا، فإن كميات من الحمض النووي انزلوا لا تكون كافية لإعداد المكتبات باستخدام الكواشف عدة. وأجريت الجيل العنقودية والتسلسل وفقا لتعليمات الشركة الصانعة. يحلل المعلوماتية الحيوية بعد العرض التسلسل نتائج باهرة من العينات منخفضة الشذرة عدد الخلايا. مجموعة البيانات 30 خريج (الموافق 10،000 الخلايا من المواد ابتداء من ) يحتوي على انخفاض الضوضاء في الخلفية وقمم تخصيب موثوق بها للغاية والتي أكدت من قبل كل من مجموعة البيانات 300 خريج (الموافق 100،000 الخلايا من المواد ابتداء) ومجموعة البيانات H3K4me3 الناتجة عن المعهد واسعة للمشروع ترميز والذي تم استخدامه بمثابة مرجع خارجي. ومن المهم أن نلاحظ أعلى 40 التداخل نسبة البيانات، والتي تشير إلى الطريقة القياسية المستخدمة في المشروع ENCODE 11 التي تعتبر رقاقة وما يليها استنساخه إذا بمقارنة مجموعتين من البيانات هناك ما لا يقل عن التداخل 80٪ من أفضل 40٪ من القمم التي كتبها درجة الأهمية في المرتبة. مجموعة البيانات 30 خريج يحقق هذه المعايير بالمقارنة مع كل من مجموعة البيانات 300 خريج (النظر في جميع مستويات الذروة التي بلغتها، وليس فقط أفضل 40٪) وبيانات معهد برود (الجدول 1). ويوضح بيانات 300 خريج قمم مماثلة تقريبا لبيانات معهد برود مع 98٪ أعلى 40 نسبة التداخل (الشكل 7).
ighres.jpg "/>
تم إنشاء الشكل 7. المقايسات رقاقة وتوليد المكتبة على 10،000 خلايا التجارب رقاقة وما يليها على 10،000 و 100،000 خلايا هيلا-S3 باستخدام H3K4me3 الأجسام المضادة (0.25 ميكروغرام / ميكرولتر). تم تعيين علامات غليان 35 إلى الجينوم البشري مع اليجنر إلاند. خلال ذروة اللاحقة يدعو SICER يمكن تحديد موثوق التخصيب من أعداد الخلايا منخفضة وكذلك من ملايين الخلايا. تم تحليل مجموعات البيانات ومقارنتها مع بعضها البعض، وإلى البيانات المرجعية التي تولدها معهد برود. عينات الخلايا منخفضة تتفق ولها تشابه عالية جدا. تلبي العينة 30 خريج معايير ترميز 11 (دقيقة. 80٪ من أعلى 40٪ من القمم يجب أن تتداخل). الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم.
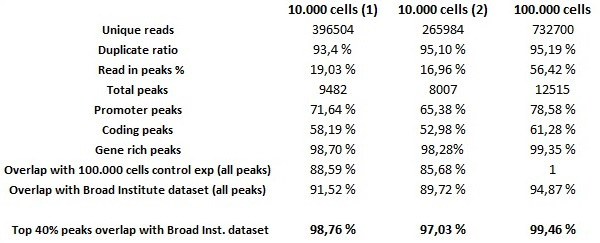
الجدول 1.
Discussion
مناعي لونين تليها التسلسل هو الآن إجراء القياسية. هنا يرد على رقاقة وما يليها بروتوكول الآلية التي يمكن أن تولد ملامح جينية لونين مع عدد قليل من 10،000 خلايا بدءا المادية.
أتمتة الشذرة وإعداد المقايسات مكتبة يتيح توحيد الإجراء الشذرة الأمثل والحد من التقلبات التجريبية. نظام معالجة السائل المقدمة هنا يلغي العديد من الإجراءات اليدوية المرتبطة الشذرة الحد يد في الوقت المناسب لدقيقة فقط 30، ويقلل من فقدان العينة، وتمكن دقيق رقاقة وما يليها مع عدد قليل من بيكوغرام من المدخلات المكتبة. من أجل تحقيق نجاح التجارب رقاقة وما يليها الآلي، بل هو أيضا حاسما لاستخدام ذات جودة عالية التحضيرات لونين المنفصمة والأجسام المضادة الصف رقاقة وما يليها في كل تجربة نظام يستخدم التكنولوجيا القائمة على حبة المغناطيسي، ويوفر المرونة اللازمة لتغيير المعلمات التجريبية الرئيسية مثل حضانة الوقت للمعطف الأجسام المضادةخطوات مناعي أو تعديل الشروط غسل السماح للباحث لإجراء جميع التجارب اللازمة لرقاقة وما يليها الأمثل جي و. النظام الآلي هو منصة "فتح" التي تسمح أيضا مقارنة الكواشف متعددة في نفس الوقت لتعظيم الاستفادة من الظروف التجريبية لكل خط الخلية الفردية والأجسام المضادة وتمكن المقارنة المباشرة من مختلف الأنواع وتركيزات الكروماتين، والأجسام المضادة المختلفة وأنواع مختلفة من حتى المغناطيسي الخرز.
واحد من أوجه القصور في النظام الآلي هو الحاجة للأتمتة كافة البروتوكولات في وحدات التخزين التي تتراوح بين 5 ميكرولتر إلى 200 ميكرولتر. ومع ذلك، فإن التصغير من التجارب في هذا المنبر الآلي يمكن أيضا توفير التكاليف في الكواشف.
وبالإضافة إلى البروتوكولات المذكورة في هذه الدراسة، فإن هذا النظام قابل للتكيف وبأتمتة مجموعة متنوعة من التطبيقات الأخرى المستندة حبة المغناطيسية مثل مناعي وأيضاالثانية القبض على الحمض النووي ميثليته (تقنيات MeDIP وMethylCap)، مناعي من الحمض النووي hydroxylmethylated (hMEDIP)، متتابعة مناعي لونين (ReChIP)، مناعي RNA (RNA-IP)، وتحويل بيسلفيت، والمقايسات تنقية DNA.
Disclosures
The authors of this article, at the time of its writing, are employed by Diagenode S.A. and Diagenode, Inc., the manufacturer of the automated system described.
Acknowledgements
This work was supported by the BLUERPINT EU grant (BLUEPRINT – A BLUEPRINT of Haematopoietic Epigenomes). We also thank the Walloon Region (DG06) for its financial support.
Materials
| Name | Company | Catalog Number | Comments |
| PBS | Life technologies | 14190-094 | |
| Trypsin-EDTA | Sigma | T3924-100ML | |
| Formaldehyde 37% | Sigma | F8775-25 | |
| 1.25 M Glycine Solution | Diagenode | C01020010 | Component of the ideal ChIP-seq kit |
| Lysis Buffer iL1 | Diagenode | C01020010 | Component of the ideal ChIP-seq kit |
| Lysis Buffer iL2 | Diagenode | C01020010 | Component of the ideal ChIP-seq kit |
| Shearing Buffer iS1 | Diagenode | C01020010 | Component of the ideal ChIP-seq kit |
| Protease Inhibitors Mix (200x) | Diagenode | C01010130 | Component of the Auto True Micro ChIP kit |
| HBSS (no calcium, no magnesium, no phenol red) | Life technologies | 14175-053 | |
| Lysis Buffer tL1 | Diagenode | C01010130 | Component of the Auto True Micro ChIP kit |
| ChIP Buffer tC1 | Diagenode | C01010130 | Component of the Auto True Micro ChIP kit |
| ideal ChIP-seq kit | Diagneode | C01010051 | |
| ChIP-Buffer H | Diagenode | C01010020 | Component of the Auto Histone ChIP-seq kit |
| Auto Histone ChIP-seq kit | Diagenode | C01010020 | |
| Auto True Micro ChIP kit | Diagenode | C01010130 | |
| H3K79me3 polyclonal antibody-Classic | Diagenode | C15310068 | |
| H3K27me3 polyclonal antibody-Classic | Diagenode | C15410069 | |
| H3K4me3 polyclonal antibody-Classic | Diagenode | C15410030 | |
| H3K4me2 polyclonal antibody-Classic | Diagenode | C15410035 | |
| H3K9ac polyclonal antibody-Premium | Diagenode | C15410004 | |
| H3K9/14ac polyclonal antibody-Premium | Diagenode | C15410200 | |
| H3K36me3 polyclonal antibody-Premium | Diagenode | C15410058 | |
| H3K9me3 polyclonal antibody-Premium | Diagenode | C15410193 | |
| Rabbit IgG | Diagenode | C15410206 | |
| Protein-A coated paramagnetic beads | Diagenode | C01010020 | |
| Auto IPure | Diagenode | C03010010 | |
| MicroChIP DiaPure columns | Diagenode | C03040001 | |
| Universal SyberGreenMaster Mix 1.25 ml | Diagenode | DMMLD2D100 | |
| Quant-IT dsDNA | Invitrogen | Q32854 | |
| Illumina Sample Preparation kit fro Genomic DNA | Illumina | FC-121-3001 | |
| Illumina True-seq kit ChIP library Prep kit | Illumina | IP-202-1012 | |
| MicroPlex Library Preparation Kit | Diagenode | C05010010 | |
| Agencourt AMPure XP beads | Beckman Coulter | A63881 | |
| Illumina Library prep Quantification kit | Kapa Biosystems | KK4844 | |
| IP-Star Compact Automated System | Diagenode | B03000002 | |
| Bioruptor Plus | Diagenode | B01020001 | |
| Bioruptor Pico | Diagenode | B01060001 | |
| Qubit system | Invitrogen | Q32857 | |
| Illumina Hiseq systems | Illumina |
References
- Dahl, J. A., Collas, P. A rapid micro chromatin immunoprecipitation assay (microChIP). Nature Protocols. 3, 1032-1045 (2008).
- Adli, M., Bernstein, B. E. Whole-genome chromatin profiling from limited numbers of cells using nano-ChIP-seq. Nature Protocols. 6, 1656-1668 (2011).
- Blecher-Gonen, R., et al. High-throughput chromatin immunoprecipitation for genome-wide mapping of in vivo protein-DNA interactions and epigenomic states. Nature Protocols. 8, 539-554 (2013).
- Aldridge, S., et al. AHT-ChIP-seq: a completely automated robotic protocol for high-throughput chromatin immunoprecipitation. Genome Biology. 14, 124 (2013).
- Farias-Hesson, E., et al. Semi-automated library preparation for high-throughput DNA sequencing platforms. Journal of Biomedicin., & Biotechnology. 2010, (2010).
- Callejas, S., Alvarez, R., Benguria, A., Dopazo, A. AG-NGS: a powerful and user-friendly computing application for the semi-automated preparation of next-generation sequencing libraries using open liquid handling platforms. BioTechniques. 56, 28-35 (2014).
- Zang, C., et al. A clustering approach for identification of enriched domains from histone modification ChIP-Seq data. Bioinformatics. 25, 1952-1958 (2009).
- Zhang, Y., et al. Model-based analysis of ChIP-Seq (MACS). Genome Biology. 9, 137 (2008).
- Heinz, S., et al. Simple combinations of lineage-determining transcription factors prime cis-regulatory elements required for macrophage and B cell identities. Molecular Cell. 38, 576-589 (2010).
- Quinlan, A. R., Hall, I. M. BEDTools: a flexible suite of utilities for comparing genomic features. Bioinformatics (Oxford, England). 26, 841-842 (2010).
- Landt, S. G., et al. ChIP-seq guidelines and practices of the ENCODE and modENCODE consortia. Genome Research. 22, 1813-1831 (2012).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved