Method Article
التحضير والتصوير، والكمي لالسطحية الجرثومي على الحركة فحوصات
In This Article
Summary
Swarming motility is influenced by physical and environmental factors. We describe a two-phase protocol and guidelines to circumvent the challenges commonly associated with swarm assay preparation and data collection. A macroscopic imaging technique is employed to obtain detailed information on swarm behavior that is not provided by current analysis techniques.
Abstract
الحركة سطح البكتيرية، مثل يحتشدون، يتم فحص عادة في المختبر باستخدام المقايسات لوحة التي تستلزم تركيزات محددة من أجار وأحيانا إدراج العناصر المغذية المحددة في وسط النمو. إعداد هذه الوسائط صريحة وظروف النمو سطح يعمل على توفير الظروف المواتية التي تسمح نمو البكتيريا وليس فقط ولكن الحركة منسقة من البكتيريا على هذه الأسطح ضمن الأفلام السائل رقيقة. استنساخ لوحة سرب وغيرها من المقايسات لوحة حركية سطح يمكن أن يكون تحديا كبيرا. خاصة بالنسبة للأكثر "swarmers المعتدلة" التي تظهر حركية فقط ضمن نطاقات أجار 0.4٪ -0.8٪ (وزن / المجلد)، تغييرات طفيفة في بروتوكول أو بيئة معملية يمكن أن تؤثر بشكل كبير نتائج الفحص سرب. "بلل"، أو محتوى الماء في واجهة السائل الصلبة في الهواء من هذه المقايسات لوحة، وغالبا ما يكون متغير رئيسي أن يكون للرقابة. تحديا إضافيا في تقييم يحتشدون هو كيفية قياس سالخلافات bserved بين أي اثنين (أو أكثر) التجارب. نحن هنا التفاصيل بروتوكول مرحلتين تنوعا لإعداد المقايسات وصورة سرب. نحن وتشمل المبادئ التوجيهية للتحايل على التحديات المرتبطة عادة مع إعداد وسائل الاعلام سرب الفحص النوعي والكمي لبيانات من هذه المقايسات. ونحن على وجه التحديد إظهار أسلوبنا باستخدام البكتيريا التي تعبر عن صحفيين الجيني الفلورسنت أو إضاءة الحيوية مثل الأخضر بروتين فلوري (GFP)، و luciferase (لوكس الاوبرون)، أو البقع الخلوية لتمكين التصوير الضوئي الوقت الفاصل بين. علينا أن نظهر كذلك قدرة لدينا وسيلة لتتبع المتنافسة يحتشدون الأنواع في نفس التجربة.
Introduction
العديد من أنواع البكتيريا تتحرك على الأسطح باستخدام مختلف وسائل الدفع الذاتي. بعض الظواهر الحركة يمكن البحث في المختبر باستخدام المقايسات لوحة التي تتأثر البيئة السائلة المرتبطة شبه صلبة تكوين لوحة الفحص. مجموعة فرعية من سطح مفيدا المقايسات لوحة حركية أخرى تنطوي على هواء الغرفة الغاز مراحل عادة. وفقا لذلك، ونتائج معين أي فحص الحركة السطح، يتطلب مراقبة دقيقة واجهة من ثلاث مراحل: سطح صلب البيئي المحلي والبيئة السائلة، وخصائص البيئة الغاز.
ومن المعروف أن وضع الحركة الأكثر دراسة عادة في مثل هذا الفحص من ثلاث مراحل كما يحتشدون. يحتشدون الحركة هي الحركة مجموعة منسقة من الخلايا البكتيرية التي تدفعها سياط من خلال الأفلام السائل رقيقة على السطوح 1. وعادة ما درسه في المختبرات باستخدام المقايسات لوحة شبه صلبة تحتوي على 0.4٪ -0.8٪ (وزن / المجلد) أجار 1. مجموعة منمسببات الأمراض البشرية تستغل هذا السلوك الحركة لاستكشاف واستعمار المضيف البشري. على سبيل المثال، يستخدم المتقلبة الرائعة يحتشدون حركية لنقل ما يصل مجرى البول، ووصلت واستعمار المثانة والكلى 2. ويعتبر يحتشدون حركية عموما خطوة تمهيدية لتشكيل بيوفيلم، والسبب الرئيسي لالمرضية في كثير من مسببات الأمراض البشرية 3.
النمط الظاهري يحتشدون متنوع للغاية بين الأنواع البكتيرية. نجاح التجريبية والتكاثر تعتمد بقوة على عوامل مثل تكوين المغذيات، نوع أجار وتكوينها، بروتوكول التعقيم (على سبيل المثال، التعقيم)، علاج وسائل الإعلام شبه صلبة، والرطوبة المحيطة (على سبيل المثال، والتغيرات الموسمية)، من بين أمور أخرى 3-5. تباين ردود حركية سطح يؤكد على التحديات التي واجهتها في هذه الدراسات ووسائل الإعلام تأثير كبير والبيئة يمكن أن تمارس. بالنسبة لبعض الأنواع يحتشدون، مثل الزائفة، يحتشدون يذكرهيمكن أن يحدث ility على مجموعة متنوعة من التراكيب وسائل الإعلام، على الرغم من أن النمط الظاهري المرصود والمصاحبة معدل التوسع سرب سوف تختلف اختلافا كبيرا 3. ويمكن الجمع بين هذه العوامل تجعل دراسات الحركة سطح صعبة للغاية. تغيرات موسمية داخل المختبر يمكن أن تؤثر هذه المقايسات ثلاث مراحل: المقايسات قد تعمل على نحو أفضل في الهواء الرطبة من الصيف وأسوأ في الهواء الجاف من الشتاء. هنا نقدم المبادئ التوجيهية العامة للتحايل بعض من أبرز التحديات عند تنفيذ الدراسات سطح لوحة حركية.
وبالنسبة لبعض الدراسات حركية السطح، وتطوير الظواهر المحددة هي ذات أهمية كبيرة. معظم، ولكن ليس كل شيء، الدراسات المنشورة لدراسة يحتشدون من P. الزنجارية تظهر تشكيل المحلاق أو فركتلات يشع من مركز التلقيح 3-9. الاختلافات بين P. وقد تم توثيق سلالات الزنجارية 5،8، ولكن الكثير من وجود أو عدم وجود المحلاق يمكن أن يعزى إلى specifiج المتوسطة وبروتوكول يستخدم لهذه المقايسات لوحة سرب الحركة. نحن هنا تتضمن تفاصيل حول كيفية تعزيز أسراب تشكيل حالق لP. الزنجارية. لأن P. الزنجارية هي مجرد واحدة من العديد من أنواع البكتيريا يحتشدون، ندرج أيضا تفاصيل عن طريقة لدينا لدراسة يحتشدون من العصوية الرقيقة ومزلق من المكورة المخاطية زانثس. مثل P. الزنجارية، والبحث الحالي على B. الرقيقة وM. زانثس يمتد مجموعة من الموضوعات مثل الباحثين يعملون على تمييز جوانب تبوغ، حركية، استجابة الإجهاد، والسلوك الانتقالي 1،10. هناك حاجة لتحديد الأنماط وديناميات سلوك معين (ق) لهذه الخلايا في مجموعات يحتشدون.
الحصول على البيانات الحركة السطح، ويمكن تحليل، وتفسير تكون مرهقة والنوعي. لقد قمنا بتطوير بروتوكول لتحليل العيانية مفصل لأسراب البكتيرية التي توفر بالإضافة إلى سرب التشكل منطقة والصورةإيزي (على سبيل المثال، قطر)، المعلومات الحيوية الكمية المتعلقة معدل التوسع سرب وتوزيع المنتجات الحيوية البكتيرية أو الكثافة 7. وعلاوة على ذلك، يمكن لهذا الأسلوب الاستفادة من البروتينات المتاحة الفلورسنت، والتلألؤ، والأصباغ للحصول على رؤية شاملة من التفاعلات البكتيرية 8، وكذلك لتتبع تركيب المنتجات الحيوية (على سبيل المثال، rhamnolipid P. الزنجارية 7،8) ضمن سرب.
Protocol
1. سرب الفحص تحضير الوسائط والتلقيح 4،5،7،8،11
- إعداد وسائل الاعلام
ملاحظة: تكوين المتوسط هو موضح أدناه ينطبق على P. الزنجارية الدراسات تشكيل حالق. يرجى الاطلاع على المواصفات وسائل الإعلام على الجدول رقم 1 لP. الزنجارية، B. الرقيقة، وM. زانثس المقايسات الحركة السطح.- مزيج 200 مل من FAB-ناقص (NH 4) 2 SO 4 سرب المتوسطة (مواد الجدول)، 0.9 غرام من نوبل أجار، و 0.2 غرام من الأحماض Casamino (الجدول 1) عن طريق اثارة مع شريط مغناطيسي. استخدام كميات صغيرة (100-300 مل) لتحسين الاتساق بين التجارب.
- الأوتوكلاف الخليط 200 مل أجار / وسائل الإعلام باستخدام وقت التعرض لل 22 دقيقة، ودرجة الحرارة التعرض لل121.1 ° C، وخيار تنفيس سريع. سوف الإعدادات الأوتوكلاف تسمح التعقيم السليم وذوبان أجار، ولكن منع انتاج الكراميل أجار.
ملاحظة: أجار نوبل هي عرضة للالكراميلسعودة. يتم تبديل الحركة البكتيرية على أجار بالكراميل. - على الفور بعد الانتهاء من دورة التعقيم، وأغلق الغطاء للزجاجة وسائل الإعلام لمنع فقدان الماء عن طريق التبخر. ومع ذلك، لاحظ أن السد ضيق يمكن أن يؤدي إلى "فراغ الختم" تأثير اندفاع يشبه على الزجاجة.
- تبريد وسائل الإعلام إلى 50 درجة مئوية مع التحريك في درجة حرارة الغرفة (RT) وإضافة 2 مل من معقم 1.2 M الجلوكوز. بدلا من ذلك، وضع وسائل الإعلام في 60 ° C حاضنة أو ماء الحمام حتى جاهزة للاستخدام (في وقت لاحق إلى 15 ساعة)، والمضي قدما على النحو المشار إليه. لمنع تشكيل فقاعات في وسائل الإعلام، تخلط جيدا باستخدام شريط مغناطيسي. فقاعات على سطح آغار سيمنع حتى يحتشدون.
ملاحظة: لفحوصات أخرى، إضافة في هذه الخطوة المكونات الحساسة للحرارة التي لا يمكن تعقيمها مثل المواد الغذائية أو الأصباغ إضافية، حسب الحاجة (على سبيل المثال، إضافة 8 ميكرولتر إينفيتروجن Syto 63 صبغ لكل 100 مل ذابت أجار إلى صورة M. زانثس كما هو مبين في Representatiلقد النتائج، أدناه). إضافة بعض الأصباغ قد يؤثر على سلوك يحتشدون خط الأساس، والتي يجب أن يتم التحقق ضد السيطرة غير صبغ. - في غطاء المختبرات، وقسامة 7.5 مل من وسائل الإعلام معقمة لكل 60 مم البوليسترين طبق بتري والحفاظ على لوحات في طبقة واحدة (وليس مكدسة). لعرض أكبر سطح يحتشدون، قسامة 25 مل من وسائل الإعلام في 100 مم طبق بتري. من المهم لملء الأطباق على سطح حتى الأفقي. استخدام مستوى العين الثور للتحقق مما إذا أن يتم تسوية السطح.
ملاحظة: للحصول على P. سوف المقايسات الزنجارية، وذلك باستخدام وسائل الإعلام حجم محددة لكل لوحة تحسين الاتساق والتكاثر. لB. الرقيقة وM. المقايسات زانثس، ومن ناحية سكب النتائج عوائد مماثلة لحجم مأخوذة محددة.
- لوحة علاج
- لوحات صغيرة (60 ملم)، والسماح للالمتوسطة أجار ذاب لعلاج (سواء المقرر أن شبه صلبة وجافة السائل الزائد) في غطاء محرك السيارة كشفت (أي بدون أغطية) لمدة 30 دقيقة. أكبرلوحات (100 ملم) تتطلب وقتا أطول علاج (انظر مناقشة).
ملاحظة: بدلا من ذلك، قد تتطلب بعض المقايسات لوحات لعلاج في أعلى مقاعد البدلاء بين عشية وضحاها (20-24 ساعة) مغطاة (أي، والأغطية على) في طبقة واحدة (الجدول 1). يحتشدون حساس لكلا الرطوبة الزائدة وغير كافية. الرطوبة، تدفق الهواء، ودرجة الحرارة في أي مختبر معين قد يستلزم الاختلاف لوحة علاج لتعزيز يحتشدون الأمثل لللك بكتيريا. - تطعيم لوحات مباشرة بعد فترة التجفيف قد انتهت. لا تخزن لوحات لاستخدامها مرة أخرى.
- نفذ "الحبر انتشار الاختبار" قبل اكتشاف لوحة اختبار مع مزيج 10 ميكرولتر من 0.50٪ (المجلد / المجلد) هيغنز مقاوم للماء الأسود الهند الحبر واللقاح البكتيري 11. إذا كان خليط الحبر / اللقاح ينتشر بسهولة (أي لا تحتفظ شكل قطرة) على سطح وسائل الإعلام، فإن وسائل الإعلام تحتاج إلى وقت إضافي لتجف.
ملاحظة: بالنسبة للأنواع التي تعتبر حساسة بشكل خاص للرطوبة (<م> على سبيل المثال، P. الزنجارية)، إجراء سريع "انتشار الحبر اختبار" 11 لتحديد ما إذا كانت لوحات جافة بما فيه الكفاية.
- نفذ "الحبر انتشار الاختبار" قبل اكتشاف لوحة اختبار مع مزيج 10 ميكرولتر من 0.50٪ (المجلد / المجلد) هيغنز مقاوم للماء الأسود الهند الحبر واللقاح البكتيري 11. إذا كان خليط الحبر / اللقاح ينتشر بسهولة (أي لا تحتفظ شكل قطرة) على سطح وسائل الإعلام، فإن وسائل الإعلام تحتاج إلى وقت إضافي لتجف.
- لوحات صغيرة (60 ملم)، والسماح للالمتوسطة أجار ذاب لعلاج (سواء المقرر أن شبه صلبة وجافة السائل الزائد) في غطاء محرك السيارة كشفت (أي بدون أغطية) لمدة 30 دقيقة. أكبرلوحات (100 ملم) تتطلب وقتا أطول علاج (انظر مناقشة).
- سرب الفحص التلقيح
- تطعيم 6 مل من وسائل الإعلام ثقافة مرق (انظر الجدول 1 للتفاصيل) مع مستعمرة معزولة من (<5 أيام القديمة إذا ترك في درجة حرارة الغرفة) استذابة مرق (LB) ثقافة لوحة جديدة. احتضان الثقافات مرق بين عشية وضحاها (≤18 ساعة) عند 30 درجة مئوية أو 37 درجة مئوية مع اهتزاز الأفقي (240 دورة في الدقيقة).
- تطعيم لوحات سرب من اكتشاف مع 1-5 ميكرولتر من ثقافة مرق بين عشية وضحاها، أو عن طريق "بدس" آغار مع الأسنان معقم اختيار أو أسلاك التلقيح الإبرة.
ملاحظة: نحن نفضل الأسلوب الأخير لأنه يقلل من احتمال يتناثر قيحة ويمنع مضيفا رطوبة إضافية إلى منطقة سطح سرب.
- سرب الفحص الحضانة
- للفحص العام، واحتضان لوحات فحص سرب في 30 درجةC أو 37 درجة مئوية (أو حتى 42 درجة مئوية لمدة B. الرقيقة، الجدول 1)، وهذا هو بكتيريا محددة. عكس لوحات أثناء الحضانة حتى يتكثف أن الرطوبة الزائدة على الغطاء، لا آغار.
ملاحظة: درجة الحرارة يمكن أن يؤثر على النمط الظاهري وكذلك حركية. لP. أسراب الزنجارية، الحضانة عند 37 درجة مئوية يؤدي إلى زيادة النمو والتوسع سرب من الحضانة عند 30 درجة مئوية. ومع ذلك، فإن مورفولوجية هذه الأسراب غالبا ما يختلف مع هذا التغير في درجة الحرارة. - للتصوير مرور الزمن، واحتضان لوحات سرب في درجة الحرارة المناسبة قبل نقل إلى محطة التصوير (انظر الجدول 1 للتفاصيل).
ملاحظة: هذه الحضانة ما قبل التصوير تسمح أسراب لبدء تنميتها وأصبح راسخا قبل نقله إلى بيئة جديدة، والتي قد تكون أو لا تكون الأمثل ليحتشدون حركية.
- للفحص العام، واحتضان لوحات فحص سرب في 30 درجةC أو 37 درجة مئوية (أو حتى 42 درجة مئوية لمدة B. الرقيقة، الجدول 1)، وهذا هو بكتيريا محددة. عكس لوحات أثناء الحضانة حتى يتكثف أن الرطوبة الزائدة على الغطاء، لا آغار.
2. التصوير ترى بالعين المجردة والسطحية على الحركة فحوصات 7،8
<رأ>3. معالجة البيانات وتفسير 7،8
- معالجة الصور
- استخدام MI البرمجيات لتصدير الصور دفعة كملفات TIFF 16 بت: ملف> تصدير أو تصدير متعددة> اختر ملف (ق) لتصدير والمكان التصدير.
- استخدام يماغيج لفتح صورة واحدة أو استيراد سلسلة الوقت الفاصل:
- فتح صورة واحدة: ملف> فتح
- استيراد الوقت الفاصل بين تسلسل الصور: ملف> استيراد تسلسل، واختر "أسماء ترتيب عدديا".
- لملفات الوقت الفاصل بين أكبر، حدد "استخدام كومة الظاهري" في "استيراد تسلسل" نافذة إلى كومة من الصور تصديرها إلى فئات المناسبة (أي GFP، RFP، الخ).
- إذا لزم الأمر، تغيير الصور من ملفات 16 بت إلى الملفات 8 بت: صورة> نوع> 8 بت
ملاحظة: بعض أدوات يماغيج تتطلب الصور 8 بت. - تحديد ما إذا كان إشارة كثافة لتسلسل الصور أو مرور الزمن يحتاج إلى مقلوب. ضع المؤشر على نقطة مضيئة في الصورة (على سبيل المثال، والنمو fluorescently المسمى) ونلاحظ كثافة إشارة "قيمة" من شريط الأدوات يماغيج. ثم، ضع المؤشر في بقعة مظلمة خارج منطقة لوحة ونلاحظ كثافة الإشارة. إذا كانت كثافة إشارة لبقعة مظلمة أكبر من كثافة لنقطة مضيئة، تحتاج كثافة إشارة الصورة لتكون معكوسة (اتبع substeps 1-2 أدناه).
- عكس إشارات كثافة: تحرير> المقلوب
- عكس جدول البحث: صورة> طاولات بحث> عكس طرفية
- طرح الخلفية: عملية> طرح الخلفية، واستخدام "المتداول نصف قطر الكرة" مع دائرة نصف قطرها بكسل التي هي واحدة من نصف واحد البعد الصورة (على سبيل المثال، 1،000 بكسل لس 2،000 2،000 صixel الصورة).
- مصطنع اللون صورة أو الوقت الفاصل بين تسلسل: صورة> طاولات البحث، واختيار اللون المناسب من الخيارات القائمة.
- للأفلام مع اثنين أو أكثر من القنوات، ودمج وتحقيق التوازن بين الألوان قبل حفظ كفيلم (معالجة الصور، الخطوة 8). لدمج الصور معا، وفتح كل رزمة الصورة في يماغيج، ثم اختر صورة> اللون> دمج القنوات، وتعيين كل كومة إلى قناة اللون.
- حفظ تسلسل الوقت الفاصل بين ما افي أو كويك تايم الفيلم: ملف> حفظ باسم، واختيار الشكل والمواصفات المطلوبة.
- تحليل البيانات
- الحصول البكتيرية منطقة نمو السطحية لقياس نسبة الانتشار
- صورة مفتوحة (ق) في يماغيج
- لحساب قطر من لوحة بالبكسل، رسم خط عبر مركز لوحة الفحص مع أداة "مستقيم" من وقياس طوله: تحليل> قياس
- وحدة القياس الافتراضية في يماغيج هي بيXEL. الحصول على عامل التحويل عن طريق تقسيم القطر من لوحة فحص (على سبيل المثال، 60 لوحة 60 ملم) من خلال طول بكسل تم الحصول عليها في الخطوة السابقة.
- تغيير وحدة القياس من بكسل إلى مم: صورة> خصائص
- تغيير "وحدة من طول" إلى "مم"، و "بكسل العرض"، "بكسل الطول"، و "فوكسل العمق" لعامل التحويل المحسوبة في الخطوة السابقة. حدد خانة "جلوبل" للحفاظ على هذا العامل التحويل عبر صور متعددة.
ملاحظة: إذا تم إغلاق يماغيج وأعيد فتح، أو يتم تغيير مجال الرؤية للصورة (أي، وأسرع صورة واحدة في أكثر من الآخر)، يجب إعادة حساب عامل التحويل. بدلا من ذلك، نفذ جميع التحليلات بالبكسل ثم تحويلها إلى مم.
- تغيير "وحدة من طول" إلى "مم"، و "بكسل العرض"، "بكسل الطول"، و "فوكسل العمق" لعامل التحويل المحسوبة في الخطوة السابقة. حدد خانة "جلوبل" للحفاظ على هذا العامل التحويل عبر صور متعددة.
- لكل إطار، وتتبع وقياس المنطقة سرب باستخدام "حر مختارات" أداة في شريط الأدوات لتتبع أووtline من سرب وقياس المنطقة باستخدام: تحليل> قياس. هذا وسوف تولد القياسات سجل التي يمكن حفظها لمزيد من التحليل في Microsoft Excel أو برامج مماثلة: ملف> حفظ باسم
- الحصول البكتيرية كثافة النمو السطحي لتحديد السطح معدل النمو
- مرة واحدة وطرح الخلفية (معالجة الصور، الخطوة 5)، استخدم الإطار الأخير من تسلسل لتحديد المساحة القصوى من سرب (تحليل البيانات، الخطوة 1).
- استخدام "البيضاوي" أداة التحديد من شريط الأدوات لرسم مربع حول النمو سطح البكتيريا.
- تعيين يعني قياس كثافة بكسل في مربع باستخدام: تحليل> تعيين القياسات، وحدد "يعني قيمة الرمادية".
- للحصول على قياسات كثافة إشارة لكل إطار في تسلسل الوقت الفاصل، بينما على الإطار الأول من تسلسل انتقل إلى: تحليل> قياس. هذا وسوف تولد القياسات سجل التي يمكن حفظها لمزيد من التحليل في ميcrosoft إكسل أو برامج مماثلة: ملف> حفظ باسم
- بديل إلى القسم السابق (تحليل البيانات، الخطوة 2). استخدام البرنامج المساعد يماغيج وحدات الماكرو لإعداد وتشغيل نمو سطح النصي قياس كثافة وحدات الماكرو.
- إعداد برنامج نصي القياس الآلي لتحليل إطارات متعددة في وقت واحد: البرنامج المساعد> جديد> ماكرو، ولصق النصي المقدمة (أدناه) داخل منطقة الجزاء وحفظ كملف نص يماغيج وحدات الماكرو: ملف> حفظ، وحفظ إلى مجلد التطبيق يماغيج تحت عنوان " وحدات الماكرو ".
numberOfFrames = N
ل(ط = 0؛ ط تشغيل ('قياس')؛
تشغيل ('شريحة التالي [>]')؛
}
ملاحظة: هنا المتغير "N" هو لعدد غير معروف من الإطارات. - تحرير "numberOfFrames" في البرنامج المساعد وحدات الماكرو لكل تجربة لعكس عدد من الإطارات في تسلسل الصور قبل تشغيل البرنامج النصي. الاستخدام: البرنامج المساعد> وحدات الماكرو>تحرير، واكتب في العدد الصحيح من الإطارات في تسلسل وحفظ (ملف> حفظ).
- اتبع substeps 1-3 في تحليل البيانات-الخطوة 2، وبينما كان في الإطار الأول من تسلسل تشغيل وحدات الماكرو المساعد: المساعد> وحدات الماكرو> تشغيل. هذا وسوف تولد القياسات سجل التي يمكن حفظها لمزيد من التحليل في Microsoft Excel أو برامج مماثلة: ملف> حفظ باسم
- إعداد برنامج نصي القياس الآلي لتحليل إطارات متعددة في وقت واحد: البرنامج المساعد> جديد> ماكرو، ولصق النصي المقدمة (أدناه) داخل منطقة الجزاء وحفظ كملف نص يماغيج وحدات الماكرو: ملف> حفظ، وحفظ إلى مجلد التطبيق يماغيج تحت عنوان " وحدات الماكرو ".
- الحصول البكتيرية منطقة نمو السطحية لقياس نسبة الانتشار
النتائج
الاختلاف في إعداد لوحة يمكن أن تؤثر بشكل كبير يحتشدون حركية. لعلاج أو التجفيف مرة بعد صب ذاب المتوسطة أجار يؤثر رقيقة الحاضر الفيلم السائل على سطح المقايسات الحركة والحركة البكتيرية مع مرور الوقت. تغييرات في تكوين المواد الغذائية تؤثر أيضا يحتشدون لعدة البكتيريا. الشكل 1A يظهر تأثير على المدى القصير من وقت التجفيف على انتشار الهند الحبر ونشر من اللقاح الأولي من العصوية الرقيقة (11). ويبين الشكل 1B تأثير وقت التجفيف ويظهر الشكل 1C آثار كبريتات الأمونيوم [(NH 4) 2 SO 4] على التنمية حالق اللاحقة التي كتبها يحتشدون P. الزنجارية 5.
ويمكن الحصول على البيانات الكمية من الصور نقطة النهاية من الحركة السطحية باستخدام استراتيجيات التصوير متعددة الشكل 2 يوضح النتائج نمو سطح تمثيلية لل P. الزنجارية يحتشدون وصورتها مضان GFP المرتبطة بها؛ B. الرقيقة يحتشدون وصورة تلألؤ بيولوجي المرتبط به. والنمو سطح المكورة المخاطية زانثس وما يرتبط بها من الصورة مضان الحمراء من خلايا SYTO 64 الملون.
التوسع في الحصول على البيانات وراء التفتيش عادل والتصوير النتائج نقطة النهاية يسمح لدراسة السلوك الديناميكي (ق) لسطح البكتيريا النمو. الشكل 3 7 يوضح مثال P. الزنجارية يحتشدون (تصوير لخلايا GFP التعبير) وإنتاج rhamnolipid المرتبط به (تصوير باستخدام النيل الأحمر الدهون وصمة عار) يتم عرض -THE الكمي من البيانات من هذه الصور أيضا لإظهار معدل التوسع في P. الزنجارية يحتشدون. فيديو 1 يظهر الفاصل بين وقت B. تصوير الرقيقة يحتشدون باستخدام التلألؤ من سلالة -expressing لوكس. فيديو 2 8 يظهر الفاصل بين وقت P. الزنجارية (GFP، معربا عن الأخضر) والسالمونيلا الملهبة للضرب مصلي التيفية الفأرية (التعبير الحمراء لوكس) في سرب فحص تنافسية.
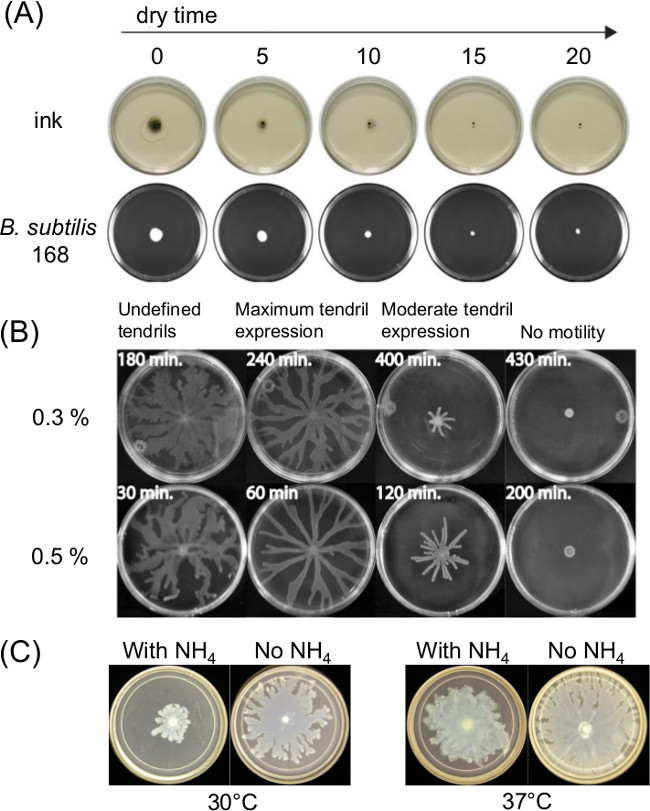
الشكل 1: أمثلة من العوامل في إعداد السطح الحركة الفحص التي تؤثر على نتيجة الفحص تأثير (A) وقت أجار على تجفيف رطوبة سطح أجار وانتشار اللقاح لB.. الرقيقة (المرجع 8)، (ب) وقت أجار على تجفيف P. الزنجارية يحتشدون (أعيد طبعها من المرجع 5 بإذن)، و (C) وجود أو عدم وجود كبريتات الأمونيوم على P. الزنجارية يحتشدون وتشكيل حالق.
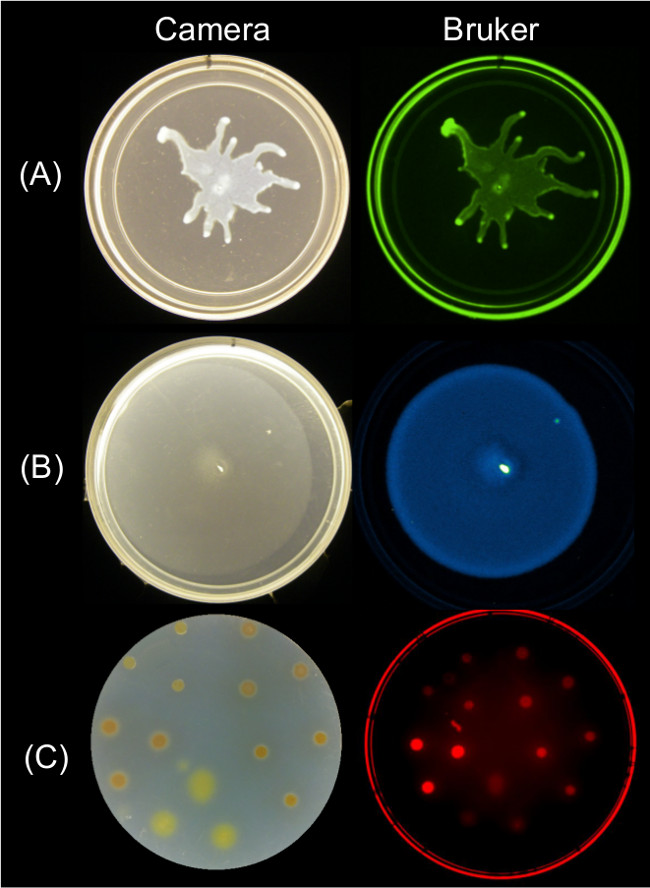
الشكل 2: Alternatiلقد النهج للنمو سطح التصوير والحركة من البكتيريا باستخدام محطة التصوير بروكر. جنبا إلى جنب صورة من كاميرا (يسار) وصورة بروكر (يمين) تظهر (A) P. الزنجارية التعبير باستخدام إعدادات الخضراء الإسفار،-تصوير GFP (ب) B. الرقيقة معربا عن وكس تلألؤ بيولوجي باستخدام إعدادات التلألؤ، وتصوير مراسل (C) M. زانثس ملطخة SYTO 64-تصوير باستخدام إعدادات الأحمر الإسفار II. انظر الجدول رقم 2 لوضع التفاصيل.
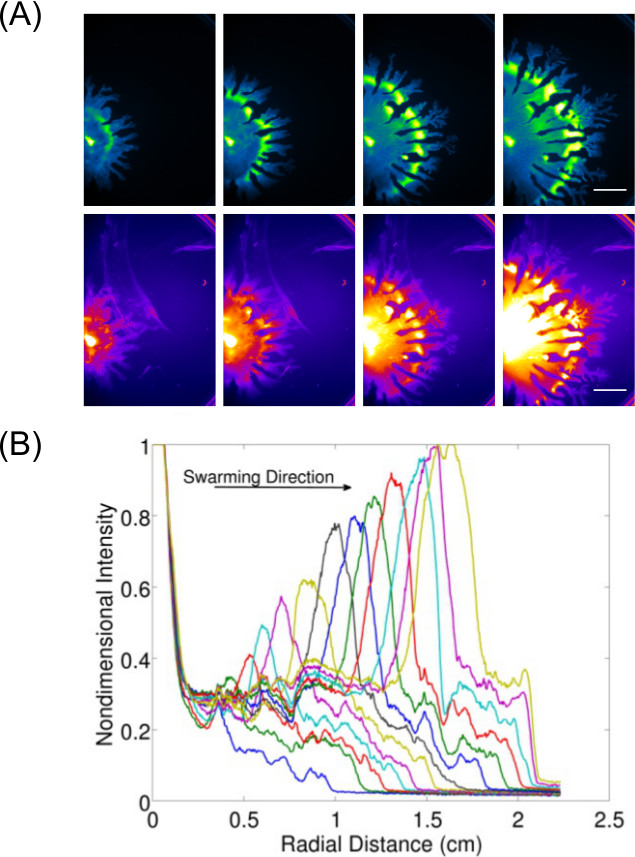
الرقم 3: التحليل النوعي والكمي للمقايسة حركية السطح (A) تحليل الوقت الفاصل بين التوزيع كثافة الخلايا، التقط إنتاج rhamnolipid (النيل الأحمر الدهون وصمة عار باستخدام الإسفار الأحمرI الإعدادات. شريط النطاق = 15 ملم)، و (ب) القياس الكمي لللتوسع معدل من الصور توزيع كثافة الخلية من P. الزنجارية سرب. (نقلا عن المرجع 6 بإذن).
فيديو 1. الوقت الفاصل بين التصوير من B. الرقيقة سرب. B. الرقيقة معربا عن وكس وتسجيلها باستخدام الإعدادات التلألؤ. انظر الجدول رقم 2 لوضع التفاصيل.
فيديو 2. المنافسة بين الأنواع تصور بواسطة التصوير مرور الزمن. أسراب من P. الزنجارية (الأخضر، معربا عن GFP وتسجيلها باستخدام الإعدادات الأخضر الإسفار) وS. التيفية الفأرية الملهبة للضرب مصلي (أحمر، مورينداتاهيتيانونيالغناء لوكس وتسجيلها باستخدام الإعدادات التلألؤ). انظر الجدول رقم 2 لوضع التفاصيل. (طبع بإذن من المرجع 7).
| P. الزنجارية | P. الزنجارية الدراسات تشكيل حالق | B. الرقيقة | M. زانثس | |
| مرق بين عشية وضحاها سائل الإعلام والثقافة | FAB بالإضافة إلى 30 ملي الجلوكوز | FAB بالإضافة إلى 30 ملي الجلوكوز | رطل | CTT |
| مرق بين عشية وضحاها في درجة الحرارة الثقافة حضانة | 37 ° C | 37 ° C | 37 ° C | 30 ساعة على 30 ° C |
| وسائل الإعلام سرب | FAB | FAB ناقص (NH 4) 2 SO 4 | 2٪ (وزن / المجلد) LB | CTT |
| وسائل الإعلام سرب: مكونات إضافية | 12 ملي الجلوكوز ل | 10٪ (وزن / المجلد) الجهاز المركزي للمحاسبات، 12 ملي الجلوكوز ل | ن / أ | SYTO® 64 ل |
| نوع أجار | أجار، نوبل | أجار، نوبل | حبيبات أجار | أجار، نوبل Affymetrix |
| تركيز أجار (وزن / المجلد) | 0.45٪ | 0.45٪ | 0.60٪ | 1.50٪ |
| سرب حجم لوحة | 60 ملم | 60 ملم | 100 مم | 150 مم |
| حجم وسائل الإعلام في لوحة | 7.5 مل | 7.5 مل | ومن ناحية سكب | ومن ناحية سكب |
| إعداد وسائل الاعلام سرب / طريقة التجفيف | غطاء محرك السيارة. لوحات كشفت | غطاء محرك السيارة. لوحات كشفت | الفوق. لوحات غطت | الفوق. لوحات غطت |
| إعداد وسائل الاعلام سرب / وقت التجفيف | 30 دقيقة | 30 دقيقة | بين عشية وضحاها (20 -24 ساعة) | بين عشية وضحاها (20 -24 ساعة) |
| سرب درجة حرارة فحص حضانة | 30 أو 37 درجة مئوية | 30 ° C | 37 ° C | 30 ° C |
| الحضانة لوقت التصوير مرور | 30 درجة مئوية لمدة لا تقل عن 4 ساعة | 30 درجة مئوية لمدة لا تقل عن 4 ساعة | 37 درجة مئوية لمدة 2 ساعة | RT لمدة 12 ساعة |
| الوقت الفاصل بين القبض على طول | 24 ساعة | 24 ساعة | 10 ساعة | 66 ساعة |
| إعداد الوقت الفاصل بين | 1 الإطار / 10 دقيقة | 1 الإطار / 10 دقيقة | 1 الإطار / 6 دقيقة | 1 الإطار / 10 دقيقة |
| واضاف بعد التعقيم. | ||||
الجدول 1: مواصفات السطحية على الحركة الفحص يشمل إعداد السطحمواصفات إعداد مقايسة حركية لP. الزنجارية، B. الرقيقة، وM. زانثس.
| إشارة | الإسفار الأخضر | الأحمر الإسفار I | الأحمر الإسفار II | التلألؤ |
| البروتين أو صبغ | الإسفار البروتين الأخضر (GFP) | بروتين mCherry أو النيل الأحمر rhamnolipid وصمة عار | SYTO® 64 | luciferase المراسل من لوكس الاوبرون |
| الطول الموجي الإثارة (نانومتر) | 480 ± 10 | 540 ± 10 | 590 ± 10 | بعيدا |
| الطول الموجي الانبعاثات (نانومتر) | 535 ± 17.5 | 600 ± 17.5 | 670 ± 17.5 | لا مرشح |
| زمن التعرض (ثانية) | 30 | 60 | 60 | 240 |
| توقف و- | 4.0 | 4.0 | 2.5 | 1.1 |
| فوف (مم) | 190 | 190 | 140 | 120 |
| المستوى البؤري (مم) | 27.5 | 27.5 | 12.2 | 4 |
| Binning (بكسل) | لا شيء | 2 × 2 | لا شيء | 8 × 8 |
الجدول 2: التصوير مواصفات مواصفات محطة بروكر التصوير للأحمر وأخضر مضان، والتصوير التلألؤ للنمو البكتيري السطح.
Discussion
يمكن تحقيق يحتشدون استنساخه في المختبر أن يكون تحديا، والمقايسات سرب شديدة الحساسية للعوامل البيئية مثل الرطوبة والمواد المغذية المتاحة. الجانب الأكثر أهمية من سطح لوحة حركية الاختبار هو الرطوبة على سطح أجار. قبل التلقيح، يجب أن تكون وسائل الإعلام سرب الجاف بما يكفي لمنع الخلايا البكتيرية من السباحة عبر السائل السطح، ولكن لم يجف وذلك لمنع يحتشدون حركية 5. حضانة ينبغي أن يتم في بيئة رطبة بما فيه الكفاية: الرطوبة قليلة جدا يمكن أن يؤدي إلى جفاف الفحص من خلال الحضانة، بينما الكثير من الرطوبة يمكن أن يؤدي إلى سطح الاصطناعي أو مصطنعة الانتشار. ما لم حاضنة التي تسيطر عليها الرطوبة في متناول اليد، ويمكن الحاضنة ومختبر الرطوبة تختلف بشكل كبير. ونتيجة لذلك، خزان إضافي للمياه، المرطب، أو مزيل الرطوبة داخل الحاضنة قد تكون هناك حاجة لمنع أكثر من تجفيف أو تراكم الرطوبة الزائدة مع الحفاظ على تعصبإيف الرطوبة بالقرب من 80٪. الحفاظ على هذه الرطوبة المثالية قد تكون صعبة إذا كانت التغييرات الموسمية والرطوبة كبيرة. إذا كان هذا هو الحال، فإن بروتوكول سرب الفحص تتطلب بعض التعديلات لحساب التغيرات الموسمية في الرطوبة. لقد وجدنا أن تعديل وقت التجفيف وسائل الإعلام سرب هو أبسط وسيلة لضبط التغييرات الرطوبة الموسمية. مراقبة الرطوبة ثابتة، على حد سواء داخل وخارج الحاضنة، يوصى. وعلاوة على ذلك، فمن المستحسن أن الباحثين معايرة والتحقق من صحة من الصكوك، وحاضنات، والمقاييس، الخ الأخطاء الطفيفة كما هو الحال في درجة الحرارة، وحجم أو مبالغ مكونات وسائل الإعلام يمكن أن تؤثر استنساخ هذه المقايسات.
كما ينبغي الإشارة إلى أن نوع وحجم لوحة المستخدمة في الفحص يمكن أن تؤثر على لوحة الرطوبة، وبالتالي يحتشدون. لوحات محكم لا تنفيس قبالة الرطوبة الزائدة، وبالتالي تشجيع الحركة السباحة. في المقابل، لوحات مفتوحة الوجه تسمح الكثير من رطوبة من الفرار. طبق بيترييوفر بيئة مثالية لأنه منافس خارج ما يكفي من الرطوبة الزائدة لمنع السائل تتراكم، ولكن يحتفظ رطوبة كافية لمنع وسائل الإعلام من الجفاف. تفاصيل هذه الطريقة بروتوكول فحص الحركة السطحية التي تسمح للتصوير عالية الجودة. للحفاظ على أجار واضحة للأطباق بقطر 60 ملم التصوير تمتلئ 7.5 مل من وسائل الإعلام أجار. إذا لم يكن مطلوبا التصوير بالتفصيل، يمكن أحجام تصل إلى 20 مل أيضا تقديم نتائج قابلة للتكرار.
بينما يحتشدون حركية يمكن أن يتحقق على مجموعة واسعة من تركيزات آغار، ومجموعة الأمثل للأجار اللازمة ليحتشدون يعتمد على الأنواع. وعموما، تركيزات أعلى أجار تمنع يحتشدون حركية، وبالتالي الوقت اللازم لإنتاج AN-صورة جاهزة زيادات سرب. P. الزنجارية تكتظ عادة على تركيزات أجار بين 0.4-0.7٪ 1، ومع ذلك نجد أن يحتشدون الأمثل يحدث في نطاق أضيق بكثير (0،4-0،5٪). آخرون، مثل B. الرقيقة وS. المعويسرب عند 0.6٪ أجار، والضمة نظيرة الحالة للدم بنسبة 1.5٪ أجار 10. يتم تحديد تركيز أجار مطلوب أيضا حسب نوع ونوع من أجار. agars نقاء أعلى، مثل نوبل أجار، وتعزيز بقوة يحتشدون في P. ويفضل الزنجارية وأكثر من حبيبات أجار 13،14. ومع ذلك، هذه الإصدارات تنقيته من أجار هي أيضا أكثر عرضة للانتاج الكراميل خلال دورة التعقيم الأوتوكلاف. اعتمادا على الصك، و/ تعديل تسلسل التعقيم تقصير (لربما يغير من دورة العادم لمنع التعرض للحرارة لفترة طويلة) قد تكون هناك حاجة لإعداد وسائل الاعلام سرب باستخدام نوبل أجار.
تكوين وسائل الإعلام أيضا يلعب دورا في سرب النمط الظاهري لوحظ 3. P. عادة ما يتم تنفيذ الزنجارية الدراسات يحتشدون حركية باستخدام الحد الأدنى من وسائل الإعلام المغذيات. نحن نفضل فاب المتوسط 4،8 (مواد الجدول)، ولكن وسائل الإعلام الأخرى، مثل M9، LB، أو اختلافات طفيفة في وسائل الإعلام هذه الشائعة،وقد استخدمت بنجاح 9،15،16. وأفضل طريقة لتحقيق تشكيل حالق على FAB المتوسطة الحد الأدنى تستكمل مع الجلوكوز كمصدر للكربون والأحماض casamino (CAA)، ولكن من دون مصدر النيتروجين إضافية (أي، (NH 4) 2 SO 4) 6،13. إذا تشكيل حالق أو التشكل ليس هو المحور الرئيسي لهذه الدراسة، ثم FAB الحد الأدنى من المتوسط (مواد الجدول، الجدول 1) تخلو من الجهاز المركزي للمحاسبات يوصى بحيث آثار مصادر الكربون محددة و / أو مغذيات إضافية يمكن دراستها بالتفصيل. الأنواع الأخرى، مثل B. الرقيقة (المقدمة هنا)، هي swarmers تنوعا، وقادرة على يحتشدون على LB وأجار المحبب. هذه الأنواع سرب بسهولة، لا تتطلب سوى ~ 10 ساعة لتطوير سرب كامل. هذا المعدل يحتشدون بسرعة يجعل التالية من تطور سرب المحتمل أن تكون صعبة ولكن لدينا بروتوكول يجعل هذا ممكنا تتبع للغاية. القدرة على أداء سرب الوقت الفاصل بين التصوير توفر substanللمحاكمة سهولة في الحصول على البيانات سرب، ولا سيما من مثل هذا swarmers متعطشا.
ونحن نقدم قوية، شامل، والبروتوكول على مرحلتين والمبادئ التوجيهية التي تهدف إلى تعزيز التنفيذ واستنساخ البكتيريا البحوث الحركة السطحية وأكدت في المقام الأول الجوانب الهامة لدراسة بوساطة سوطي يحتشدون. تفاصيل هذا البروتوكول سرب فحص جوانب هامة من تكوين وسائل الإعلام والتعامل مع لوحات حركية سطح لتوفير قدر أكبر من الاتساق والتكاثر داخل وبين المجموعات البحثية. سيؤدي ذلك إلى تحسين أساس المقارنة بين الدراسات البحثية المختلفة. وبالإضافة إلى ذلك، فإن النهج المقدمة وبروتوكول يوفر وسيلة لجعل البحث على سطح يحتشدون وحركية أقل عرضة للتغيرات البيئية من خلال جعل الباحثون على علم بأن هذه العوامل تؤثر على عملهم وتوفير الحلول الممكنة (على سبيل المثال، كيف يمكن للتغييرات صغيرة في أجار تؤثر يحتشدون 4،5 ). وعلاوة على ذلك، قدم بروتوكول لتحديد جوانب العيانية من يحتشدون، ويوفر فرصة لقياس العديد من سمات النمو سطح البكتيريا التي كانت في السابق غير قابل للقياس.
نحن لم فحص كل البكتيريا متحركة السطح في تطوير هذا البروتوكول. على هذا النحو، فمن المتوقع أن سيطلب تعديلات بروتوكول للأنواع لم يقدم هنا. ويقتصر كفاءة هذا البروتوكول في إطار حدود المتأصلة في المعدات والمواد المستخدمة. على سبيل المثال، والدراسات المتعلقة درجة الحرارة ليست ممكنة حتى الآن مع محطة التصوير بروكر، منذ التحكم في درجة الحرارة ليست سمة من سمات المعدات. وبالإضافة إلى ذلك، يمكن استخدام الأصباغ (مثل النيل الأحمر إلى وصمة عار rhamnolipids) على قيود الحركية وتركيز 8. هذه التقنية تعتمد بقوة على معالجة وتحليل الصور الرقمية. تحسين التشغيل الآلي لتحليل البيانات (على سبيل المثال، وذلك باستخدام وحدات الماكرو إضافية وظيفة البرنامج النصي في يماغيج) من شأنه أن يقلل من الوقت اللازم لتحليلوتوسيع فائدة البيانات. وأخيرا، نظرا لمتانة بروتوكول التصوير، وينبغي أن تهدف التطبيقات المستقبلية في توسيع هذه التقنية لدراسة السطوح نمو أقل موحدة التي هي أكثر أهمية على الأسطح مستعمرة من قبل البكتيريا المسببة للأمراض البيئية و.
Disclosures
رسوم النشر لهذه المادة رعيت جزئيا من قبل شركة بروكر.
Acknowledgements
وقدم الدعم الجزئي لهذا العمل من قبل المعهد الوطني للصحة (1R01GM095959-01A1 وR01GM100470، لMA وJDS) ومنحة مرفق الأساسية من معهد العلوم السريرية وبالحركة إنديانا (بتمويل جزئي من المعاهد الوطنية للصحة منحة # UL1 TR000006، ل JDS).
Materials
| Name | Company | Catalog Number | Comments |
| Reagentsa | |||
| FAB Minimal Media: | Prepare every ~4 weeks. Top to 1 L with nanopure H2O. | ||
| (NH4)2SO4 | Sigma | A4418 | 2 g. Not used in P. aeruginosa tendril formation studies. |
| Na2HPO4 x 7H2O | Sigma-Aldrich | S9390 | 9 g |
| KH2PO4 | Sigma | P5655 | 3 g |
| NaCl | BDH | BDH8014 | 3 g |
| MgCl2 x 6H2O solution (198 g/L) | Fisher Scientific | M33 | 1 ml |
| CaCl2 x 2H2O solution (14 g/L) | Fisher Scientific | C79 | 1 ml |
| Trace metal solution (see below) | n/a | n/a | 1 ml |
| Trace Metal Solution: | Top to 1 L with nanopure H2O. Maintain in a glass bottle, stirring and covered with foil. | ||
| CaSO4 x 2H2O | Sigma-Aldrich | 255548 | 200 mg |
| MnSO4 x H2O | Sigma-Aldrich | M7634 | 20 mg |
| CuSO4 x 5H2O | Fisher Scientific | C493 | 20 mg |
| ZnSO4 x 7H2O | Sigma-Aldrich | Z4750 | 20 mg |
| CoSO4 x 7H2O | Sigma-Aldrich | C6768 | 10 mg |
| NaMoO4 x 2H2O | Sigma | S6646 | 10 mg |
| H3BO3 | Fisher Scientific | A74 | 5 mg |
| FeSO4 x 7H2O | Sigma-Aldrich | F7002 | 200 mg |
| CTT Media: | Prepare as needed. Top to 100 ml with nanopure H2O. | ||
| Tris-HCl, 1 M solution (adjust to pH 8.0) | Amresco | 0234 | 1 ml. Prepare a 1 M stock solution in nano pure H2O. Adjust pH to 8.0 and filter sterilize (0.2 μm pore). |
| K2HPO4, 1 M solution (adjust to pH 7.6) | Sigma-Aldrich | P3786 | 0.1 ml. Prepare a 1 M stock solution in nano pure H2O. Adjust pH to 7.6 and filter sterilize (0.2 μm pore). |
| MgSO4 solution | Fisher Scientific | M65 | 0.8 ml. Prepare a 1 M stock solution in nano pure H2O. Filter sterilize (0.2 μm pore). |
| Casitone | BD Diagnostics | 225930 | 1 g |
| Additional Reagents: | |||
| LB Broth, Lennox | BD Diagnostics | 240230 | 2% (wt/vol) |
| D-(+)-Glucose | Sigma-Aldrich | G5767 | 30 mM for overnight broth cultures; 12 mM for swarm media. Prepare a 1.2 M filter sterilized stock solution in nano pure H2O. Add to media after autoclaving. |
| Casamino acids (CAA) | Amresco | J851 | 0.10% (wt/vol). Recommended for P. aeruginosa tendril formation studies. Add to media prior to autoclaving. |
| Agar, Noble | Sigma-Aldrich | A5431 | 0.45% (wt/vol). Preferred Noble agar for P. aeruginosa surface motility studies. Add to media prior to autoclaving. |
| Agar, Noble | Affymetrix | 10907 | 1.50% (wt/vol). Used in M. xanthus surface motility studies. Not recommended for P. aeruginosa motility studies. Add to media prior to autoclaving. |
| Agar, Granulated | Fisher Scientific | BP1423 | 0.60% (wt/vol) |
| Higgins Waterproof Black India Ink | Higgins | HIG44201 | 0.50% (vol/vol). Mix ink with inoculum to test swarm media surface moisture. |
| SYTO® 64 Red Fluorescent Nucleic Acid Stain | Invitrogen | S-11346 | Use 4 μl (for P. aeruginosa) or 8 μl (for M. xanthus) of SYTO® 64 per 100 ml of molten agar (added after autoclaving). |
| Relevant Materials and Equipment | |||
| Petri dish, sterile, 150 mm x 15 mm (Dia. x H) | VWR | 25384-326 | |
| Petri dish, sterile, 100 mm x 15 mm (Dia. x H) | VWR | 25384-342 | |
| Petri dish, sterile, 60 mm x 15 mm (Dia. x H) | VWR | 25384-092 | |
| In-Vivo Xtream | Bruker | Use for the macroscopic imaging of surface motility studies. http://www.bruker.com/products/preclinical-imaging/opticalx-ray-imaging/in-vivo-xtreme/overview.html | |
| Bruker MI software | Bruker | http://www.bruker.com/fileadmin/user_upload/8-PDF-Docs/PreclinicalImaging/Brochures/MI-software-brochure.pdf | |
| ImageJ software | NIH | http://imagej.nih.gov/ij/ | |
| aSee MSDS of reagents for handeling and disposal information. | |||
References
- Kearns, D. B. A field guide to bacterial swarming motility. Nature Reviews: Microbiology. 8 (9), 634-644 (2010).
- Burall, L. S., et al. et al.Proteus mirabilis. genes that contribute to pathogenesis of urinary tract infection: Identification of 25 signature-tagged mutants attenuated at least 100-fold. Infection and Immunity. 72 (5), 2922-2938 (2004).
- Shrout, J. D., et al. The impact of quorum sensing and swarming motility on Pseudomonas aeruginosa. biofilm formation is nutritionally conditional. Mol Microbiol. 62 (5), 1264-1277 (2006).
- Kamatkar, N. G., Shrout, J. D. Surface hardness impairment of quorum sensing and swarming for Pseudomonas aeruginosa. PLoS One. 6 (6), e20888 (2011).
- Tremblay, J., Déziel, E. Improving the reproducibility of Pseudomonas aeruginosa. swarming motility assays. Journal of Basic Microbiology. 48 (6), 509-515 (2008).
- Caiazza, N. C., Shanks, R. M., O'Toole, G. A. Rhamnolipids modulate swarming motility patterns of Pseudomonas aeruginosa. Journal of Bacteriology. 187 (21), 7351-7361 (2005).
- Du, H., et al. High density waves of the bacterium Pseudomonas aeruginosa. in propagating swarms result in efficient colonization of surfaces. Biophysical Journal. 103 (3), 601-609 (2012).
- Morris, J. D., et al. Imaging and analysis of Pseudomonas aeruginosa. swarming and rhamnolipid production. Appl Environ Microbiol. 77 (23), 8310-8317 (2011).
- Tremblay, J., Richardson, A. P., Lépine, F., Déziel, E. Self-produced extracellular stimuli modulate the Pseudomonas aeruginosa. swarming motility behaviour. Environmental Microbiology. 9 (10), 2622-2630 (2007).
- Partridge, J. D., Harshey, R. M. Swarming: flexible roaming plans. J Bacteriol. 195 (5), 909-918 (2013).
- Patrick, J. E., Kearns, D. B. Laboratory strains of Bacillus subtilis .do not exhibit swarming motility. Journal of Bacteriology. 191 (22), 7129-7133 (2009).
- . . Molecular Imaging. , (2014).
- Harshey, R. M., Matsuyama, T. Dimorphic transition in Escherichia coli. and Salmonella typhimurium.: surface-induced differentiation into hyperflagellate swarmer cells. Proceedings of the National Academy of Sciences, USA. 91 (18), 8631-8635 (1994).
- Rashid, M. H., Kornberg, A. Inorganic polyphosphate is needed for swimming, swarming, and twitching motilities of Pseudomonas aeruginosa. Proc Nat Acad Sci U.S.A.. 97 (9), 4885-4890 (2000).
- Caiazza, N. C., Merritt, J. H., Brothers, K. M., O'Toole, G. A. Inverse regulation of biofilm formation and swarming motility by Pseudomonas aeruginosa. PA14. Journal of Bacteriology. 189 (9), 3603-3612 (2007).
- Kuchma, S. L., et al. Cyclic-di-GMP-mediated repression of swarming motility by Pseudomonas aeruginosa.: the pilY1. gene and its impact on surface-associated behaviors. J Bacteriol. 192 (12), 2950-2964 (2010).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved