A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
رقاقة المستندة إلى خلية ثقافة ثلاثي الأبعاد في المفاعلات الصغيرة Perfused
In This Article
Summary
تصف لنا منبرا يعتمد على الشرائح الالكترونية لزراعة ثلاثية الأبعاد من الخلايا في الدقيقة المفاعلات الحيوية. يمكن للمرء منزل رقاقة تصل إلى 10 ميو. الخلايا التي يمكن زراعتها في ظل ظروف محددة بدقة فيما يتعلق بتدفق السائل والأكسجين الخ التوتر في العقيمة ، حلقة الدوران مغلقة.
Abstract
قمنا بتطوير ثقافة الخلية يعتمد على الشرائح الالكترونية لنظام زراعة ثلاثية الأبعاد من الخلايا. عادة ما يتم تصنيعها من شرائح غير القابلة للتحلل البوليمرات ، على سبيل المثال ، أو البولي ميتاكريلات بواسطة حقن الصغرى ، والنقش الساخنة الصغرى أو الصغيرة بالحرارة. ولكن ، يمكن أيضا أن تكون مصنوعة من البوليمرات الحيوية القابلة للتحلل. أبعادها الشاملة هي 0.7 1 × 20 × 20 × 0.7 ملم 1 (hxwxl). الميزات الرئيسية للرقائق المستخدمة هي إما الشبكة تصل إلى 1156 مكعب الحاويات الصغيرة (CF - رقاقة) كل منها في حجم 120-300 × 300 × 300 μ (hxwxl) أو تجاويف مستديرة بأقطار من 300 μ وبعمق 300 μ (ص رقاقة). يمكن للسقالة 10 منزل ميو. خلايا في تكوين ثلاثي الأبعاد. للحصول على المواد الغذائية الأمثل والغاز ، ويتم إدراج الشريحة في السكن مفاعل حيوي. في مفاعل حيوي هو جزء من حلقة مغلقة steril تداول أنه في أبسط التكوين ، وتتألف من additionaly مضخة وخزان أسطواني مع المتوسط لتوريد الغاز. يمكن تشغيل مفاعل حيوي في التروية ، superfusion ، أو حتى وضع عملية مختلطة. لقد نجحنا في زراعة خطوط الخليوي ، وكذلك الخلايا الأولية لفترات تتراوح من عدة أسابيع. لخلايا الكبد الأولية الفئران يمكن أن تظهر لنا الحفاظ على وظائف عضوي النمط لأكثر من 2 اسابيع. لخطوط سرطان الخلايا الكبدية يمكننا إظهار تحريض جينات معينة لا الكبد أو قليلا عنها في الثقافة المونولاير القياسية. قد يكون النظام المفيد أيضا زراعة الخلايا الجذعية النظام منذ التجارب الأولى مع تمايز الخلايا الجذعية واعدة.
Protocol
توضح هذه الورقة استخدام منصة يعتمد على الشرائح الالكترونية (الشكل 1) لزراعة ثلاثي الأبعاد من خطوط الخلايا وكذلك الخلايا الأولية. منذ قيام العديد من الخلايا وظائف عضوي النمط التعبير فقط في بيئة 3D ، قمنا بتطوير شرائح البوليمر الذي يوفر السقالة التي يمكن أن تلتزم الخلايا في كل الاتجاهات المكانية ، والتي يمكن تركيبها في السكن مفاعل حيوي من أجل السيطرة على تدفق السوائل والأكسجين وما إلى ذلك التوتر واعتمادا على التصميم التجريبي ، يمكن تعديل سطح البوليمر من خلال تقنيات مختلفة ، مثل الأشعة فوق البنفسجية تشعيع ، PECVD ، γ تطعيم أو الكيمياء الرطبة التقليدية.
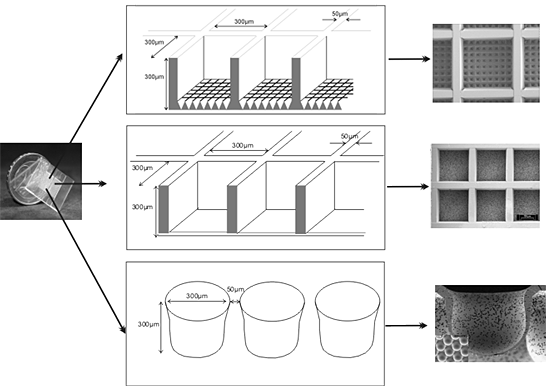
الرقم 01
1. دي تهوية وhydrophilisation من الشريحة
قبل الاستخدام ، ورقاقة يجب أن يكون وdeaerated hydrophilized. لهذا ، يتم إجراء سلسلة من الكحول. وتعد حلول الأيزوبروبانول تتألف من 100 ٪ ، 70 ٪ ، 50 ٪ ، 30 ٪ في الأيزوبروبانول DMPC المياه المعالجة ، وانخفض في كل رقاقة الاعتقال ، بدءا من حل 100 ٪ ، لتصل إلى 30S. الخطوة الأخيرة من سلسلة تتكون من ثنائي ميثيل pyrocarbonate النقي (DMPC) معاملة المياه. من هذه النقطة ، فمن المهم للحفاظ على رقاقة الرطب.
2. أنا الكولاجين طلاء
بعد سلسلة الكحول ، وهي مغلفة عادة مع رقاقة حلا أنا الكولاجين من ذيل الفأر. من الكولاجين محلول المخزون من 2 ملغ / مل في حمض الخليك المخفف هو 0.2 ٪ an قسامة الموافق 30 ميكروغرام بروتين الكولاجين مع DMPC معاملة المياه الى الحجم النهائي من 150 ميكرولتر. هذه النتائج في طلاء الكولاجين من سطح الرقاقة ذات الكثافة من 10 ميكروغرام الكولاجين أنا سم في منطقة السطح 2.
3. تلقيح خلايا سرطان الكبد
وtrypsinized خلايا سرطان الكبد والتهاب الكبد من خط G2 وفرزها. على المدى القصير التجارب (1 إلى 6 أيام) يتم تلقيح 5 * 10 6 خلايا في كل رقاقة والمناظرة التحكم الأنسجة 6 سم ثقافة أطباق بتري. لinoculte ، ومعلق في الشريحة 5 * 10 6 خلايا في 150 مستنبت ميكرولتر ووضعها على رأس منطقة microstructured من الشريحة (الشكل 2). بعد ذلك ، يتم وضعها في حاضنة لمدة 2-3 ساعات. خلال هذه الفترة حضانة الخلايا الرواسب في الحاويات الصغيرة والتمسك الكولاجين أنا المغلفة السقالة.

الشكل 2
4. إدراج شريحة في السكن مفاعل حيوي
بعد فترة الحضانة ، يتم إزالة الشريحة من الحاضنة والتي تقام في السكن مفاعل حيوي. لهذا ، وتحت مقاعد البدلاء النظيفة ، ويتم إزالة مفاعل حيوي مجمعة سلفا من التعبئة المعقمة وتفكيكها إلى درجة أنه يسمح للالإدراج للرقاقة. يتم التعامل بعناية مع ملقط معقم شرائح ويوضع في الأخدود الذي يحتوي على الأختام طوقا التي الرقاقة والذي ينتج جيل من المقصورة العليا والسفلى في مفاعل حيوي. بعد ذلك ، يتم تجميعها في مفاعل حيوي مرة أخرى ونقلها إلى الحاضنة حيث يتم توصيله إلى المضخة ، وإمدادات الغاز ومحلل الأوكسجين.
5. شغل النظام
حالما يتم توصيل مفاعل حيوي لخزان المتوسطة ، ضخ امدادات الغاز ويتم تعبئة حلقة مغلقة مع تداول المتوسط. يتم ذلك عن طريق وضع طريقة - 3 - الموصلات في مثل هذه الطريقة التي يتحقق superfusion ، الذي يعرف بأنه تدفق متوسط فوق الجزء العلوي من الشريحة. هذا يؤدي إلى تفريغ الهواء من التداول المغلقة مفاعل حيوي دون إزالة الخلايا من السقالة. بعد يتم تعبئة تماما مع نظام المتوسط ، ويتم تبديل طريقة - 3 - الموصلات في مثل هذه الطريقة التي يتحقق التروية ، الذي يعرف بأنه التدفق من دون رقاقة من خلال الأنسجة. في التكوين نضح يتم ضبط تدفق لاحتياجات الخلية التي لخلايا الكبد يتراوح عادة 6-50 ميكروليتر / دقيقة.
6. أخذ العينات
ويمكن خلال هذه التجربة يمكن استخلاص عينات المتوسط. لهذا ، ترتبط المحاقن المعقمة للمنافذ على الجزء العلوي من الخزان المتوسط. بعد أخذ العينات ، ويتم تعقيم المنافذ مع الأيزوبروبانول 70 ٪.
7. عزل خلايا سليمة من رقائق للتطبيقات المصب
في نهاية التجربة ، وقطع من المفاعلات الحيوية لامدادات الغاز والمضخة الدوارة ، ونقله إلى مقاعد البدلاء النظيفة وتفكيكها كما هو موضح سابقا. مع ملقط معقم يتم إزالة الشريحة من مفاعل حيوي السكن ، وضعتفي طبق بتري الطول 3.5 وتشطف مع برنامج تلفزيوني. بعد ذلك ، يتم تحضين الشريحة مع التربسين / EDTA (0.25 ٪ / 0.53mM) ل15/05 دقيقة في حاضنة لفصل الخلايا من منطقة microstructured. يتم طرد تعليق الخلية التي تم جمعها لمدة 5 دقائق في 600 غرام. ثم يمكن للخلايا أن تستخدم للتطبيقات المصب التقليدية ، مثل الحمض النووي الريبي مجموع العزلة أو البروتين. بشكل روتيني ، ونحن عزل الحمض النووي الريبي مجموع (باريس عدة ، Ambion شركة أوستن ، تكساس ، الولايات المتحدة الأمريكية) للتحليل [ميكروأري في الوقت الحقيقي وRT PCR. ويتم تحليل تعبير البروتين بعد تلطيخ المناعى للخلايا داخل الرقاقة مع مجهر المسح الضوئي ليزر ، ولكن يمكن أيضا أن تحلل خلاف ذلك ، على سبيل المثال ، من خلال التدفق الخلوي.
Discussion
وقد وضعنا برنامجا يعتمد على الشرائح الالكترونية لزراعة ثلاثية الأبعاد من الخلايا في المفاعلات الصغيرة perfused بنشاط. ويمكن تصنيع رقائق من غير القابلة للتحلل ، وكذلك البوليمرات القابلة للتحلل بواسطة حقن الصغرى ، والنقش الساخنة وكذلك التقنيات الدقيقة بالحرارة 3. اعتمادا على ...
Disclosures
The authors have nothing to disclose.
Acknowledgements
نود أن نشكر Mechthild Herschbach وDech انكه للحصول على مساعدة فنية ممتازة.
Materials
| Name | Company | Catalog Number | Comments | |
| Cells | Other | ATCC | HB-8065 | |
| Collagen I from rat tail | Reagent | Roche Group | 11 179 179 001 | |
| PARIS kit | Reagent | Ambion | AM1921 | |
| Syto16 | Reagent | Invitrogen | S7578 | |
| anti cytokeratin 18 | Antibody | Abcam | ab668 | Primary Ab, Mouse monoclonal, used 1/100 in PBS |
| Anti E-cadherin | Antibody | Abcam | ab1416 | Primary Ab, Mouse monoclonal, used 1/50 in PBS. |
| Goat anti-albumin | Reagent | Bethyl Laboratories | E80-129 | Primary Ab, goat anti-human Albumin, used 1/200 in PBS |
| Rabbit anti-mouse IgG1 | Antibody | Invitrogen | A11059 | Secondary Ab, Alexa Flour 488 conjugated, used 1/100 in PBS + 0.5 % BSA |
| Cy3 anti-goat IgG | Reagent | Jackson ImmunoResearch | 705-165-003 | Cy3 AffiniPure donkey a-goat IgG Ab, used 1/700 in PBS + 0.5% BSA |
References
- Berry, M. N., Friend, D. S. High-yield preparation of isolated rat liver parenchymal cells: A biochemical and fine structural study. J. Cell Biol. 53, 506-520 (1969).
- Seglen, P. O. Preparation of rat liver cells. 3. Enzymatic requirements for tissue dispersion. Exp. Cell Res. 82, 391-398 (1973).
- Giselbrecht, S., Gietzelt, T., Gottwald, E., Trautmann, C., Truckenmueller, R., Weibezahn, K. F., Welle, A. 3D tissue culture substrates produced by microthermoforming of pre-processed polymer films. Biomed. Microdev. 8, 191-199 (2006).
- Welle, A., Gottwald, E. UV-based patterning of polymeric substrates for cell culture applications. Biomed. Microdev. 4, 33-41 (2002).
- Gottwald, E., Giselbrecht, S., Augspurger, C., Lahni, B., Dambrowsky, N., Truckenmueller, R., Piotter, V., Gietzelt, T., Wendt, O., Pfleging, W., Welle, A., Rolletschek, A., Wobus, A. M., Weibezahn, K. -. F. A chip-based platform for the in vitro generation of tissues in three-dimensional organization. Lab Chip. 7, 777-785 (2007).
- Eschbach, E., Chatterjee, S. S., Noldner, M., Gottwald, E., Dertinger, H., Weibezahn, K. -. F., Knedlitschek, G., G, Microstructured scaffolds for liver tissue with high density: Morphological and biochemical characterization of tissue aggregates. J. Cell. Biochem. 95, 243-255 (2005).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved