A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
ضبط حموضة محفزات Pt/CNTs للإثير ثنائي الفينيل
In This Article
Summary
يتم تقديم بروتوكول لتركيب HNbWO6، HNbMoO6، HTaWO6 ورقة نانوية حمض صلب تعديل Pt / CNTs.
Abstract
نقدم هنا طريقة لتركيب HNbWO6، HNbMoO6، HTaWO6 ورقة نانوية حمض صلب تعديل Pt / CNTs. من خلال تغيير وزن مختلف صفائح نانوية حمض الصلبة، سلسلة من Pt/xHMNO6/CNTs مع تركيبات حمض صلب مختلفة (س = 5، 20 wt٪؛ M = Nb, Ta; N = مو، W) وقد أعدت من قبل المعالجة المسبقة nanotube الكربون، وتبادل protonic، تقشير حمض الصلبة، وتجميع وأخيرا التشريب جزيئات Pt. تتميز Pt/xHMNO 6/CNTs بإنعراج الأشعة السينية، والفحص المجهري الإلكتروني المسح الضوئي، والفحص المجهري الإلكتروني للإرسال، وNH3-temperatureالمبرمجة desorption. وكشفت الدراسة أن HNbWO6 nanosheets كانت تعلق على CNTs، مع بعض حواف النانوشيتات عازمة في الشكل. القوة الحمضية للمحفزات Pt المدعومة يزيد بالترتيب التالي: Pt/CNTs <Pt/5HNbWO 6/CNTs < Pt/20HNbMoO 6/CNTs < Pt/20HNbWO6/CNTs< Pt/20HTaWO6/CNTs. وبالإضافة إلى ذلك، تم التحقيق في التحويل المائي الحفاز لمجمع النموذج المشتق من الليغينين: الإيثر الثنائي الفينيل باستخدام محفز Pt/20HNbWO6 المركب.
Introduction
العديد من العمليات الصناعية لتصنيع المواد الكيميائية تنطوي على استخدام حمض مائي غير عضوي. ومن الأمثلة النموذجية على ذلك العملية التقليدية H2SO4 لترطيب السيكلوهيكسان لإنتاج السيكلوهيكسانول. وتنطوي هذه العملية على نظام بيهاسي، حيث يجري السيكلوهيكسان في المرحلة العضوية ويكون منتج السيكلوهيكسانول في المرحلة المائية الحمضية، مما يجعل عملية الفصل عن طريق التقطير البسيط صعبة. وبصرف النظر عن صعوبة في الانفصال والانتعاش، وحمض غير عضوي هو أيضا شديدة السمية وتآكل للمعدات. في بعض الأحيان، يؤدي استخدام حمض غير عضوي إلى توليد منتجات ثانوية من شأنها أن تخفض إنتاج المنتج ويجب تجنبها. على سبيل المثال، فإن الجفاف من 2-سيكلوهيكسين-1-رلإنتاج 1,3-سيكلوهيكسادين باستخدام H2SO4 سيؤدي إلى منتجات ثانوية البلمرة1. وهكذا، فإن العديد من العمليات الصناعية تتحول نحو استخدام محفزات الأحماض الصلبة. وتستخدم مختلف الأحماض الصلبة المتسامحة مع المياه لحل المشكلة المذكورة أعلاه وتعظيم غلة المنتج، مثل استخدام HZSM-5 وAmberlyst-15. وقد ثبت استخدام عالية السيليكا HZSM-5 الزيوليت لتحل محل H2SO4 في إنتاج سيكلوهيكسانول من البنزين2. وبما أن الزيوليت موجود في المرحلة المائية المحايدة، فإن المنتج سوف يذهب إلى المرحلة العضوية حصرا، وبالتالي تبسيط عملية الفصل. ومع ذلك، بسبب لويس حمض قاعدة adduct تشكيل جزيئات الماء إلى مواقع حمض لويس، والمواد الزيوليتيك لا تزال أظهرت انتقائية أقل بسبب وجود مواقع غير نشطة3. من بين كل هذه الأحماض الصلبة، Nb2O5 هي واحدة من أفضل المرشحين التي تحتوي على كل من لويس وBrØnsted مواقع حمض. الحموضة من Nb2O5∙nH2O يعادل 70٪ H2SO4 الحل، وذلك بسبب وجود البروتونات الصفراء. حموضة BrØnsted، والتي هي مماثلة لمواد الزيوليت البروتونيك، مرتفعة جدا. هذه الحموضة سوف تتحول إلى الحموضة لويس بعد القضاء على المياه. في وجود الماء، Nb2O5 يشكل NbO رباعي الهدريال4-H2O adducts، والتي قد تنخفض في حموضة لويس. ومع ذلك، فإن مواقع حمض لويس لا تزال فعالة منذ NbO4 رباعي الهدريال لا تزال لديها رسوم إيجابية فعالة4. وقد ثبت بنجاح هذه الظاهرة في تحويل الجلوكوز إلى 5-(هيدروكسي ميثيل) فورفورال (HMF) وحليف البنزالدهايد مع القصدير رباعي النمل في الماء5. وبالتالي، فإن المواد الحفازة التي تتحمل المياه لها أهمية حاسمة في تحويل الكتلة الأحيائية في تطبيقات الطاقة المتجددة، ولا سيما عندما تتم التحويلات في المذيبات البيئية الحميدة مثل المياه.
من بين العديد من محفزات الأحماض الصلبة الحميدة البيئية، والمواد النانوية الكربونية وظيفية باستخدام الجرافين، والأنابيب النانوية الكربونية، وألياف الكربون النانوية، ومواد الكربون المسامية تلعب دورا هاما في تثمين الكتلة الحيوية بسبب المسامية القابلة للضبط، ومساحة سطح عالية للغاية محددة، وهيدروفوبيسيتي ممتازة6،7. المشتقات الكبريتية هي مواد محفزة محفزة مستقرة ونشطة للغاية. ويمكن إما أن يتم إعدادها عن طريق الكربنة غير المكتملة من المركبات العطرية الكبريتية8 أو عن طريق كبريتونيشن السكريات الكربونية غير الكاملة9. وقد ثبت أن تكون محفزات فعالة جدا (على سبيل المثال، لإسترة الأحماض الدهنية أعلى) مع نشاط مماثل لاستخدام السائل H2SO4. الجرافينات وCNTs هي مواد الكربون مع مساحة كبيرة، خصائص ميكانيكية ممتازة، ومقاومة حمض جيدة، وتوزيعات حجم المسام موحدة، فضلا عن مقاومة لترسب فحم الكوك. وقد تم العثور على الجرافين Sulfonated لتحفيز بكفاءة التحلل المائي من خلات الإيثيل10 وقد تم العثور على محفزات الجرافين ثنائية الوظائف لتسهيل تحويل وعاء واحد من حمض الليفولينك إلى γ-valerolactone11. المعادن ثنائية الوظائف المدعومة على CNTs هي أيضا محفزات فعالة جدا للتطبيق في تحويل الكتلة الحيوية12،13 مثل الأكسدة الهوائية انتقائية للغاية من HMF إلى 2،5-diformylfuran على VO2-PANI / CNT محفز14.
الاستفادة من الخصائص الفريدة من Nb2O5 حمض الصلبة، CNTs وظيفية والمعادن ثنائية الوظائف المدعومة على CNTs، ونحن تقرير بروتوكول لتركيب سلسلة من Nb(Ta) القائمة على حمض الصلب ة nanosheet المعدلة Pt / CNTs مع ارتفاع المساحة السطحية بواسطة طريقة تجميع ورقة نانوية. وعلاوة على ذلك، أظهرنا أنPt/20HNbWO 6/CNTs، نتيجة للتأثير التآزري لجسيمات Pt المشتتة بشكل جيد والمواقع الحمضية القوية المستمدة من صفائح النانو HNbWO6، تظهر أفضل نشاط وانتقائية في تحويل المركبات النموذجية المشتقة من الليغينين في الوقود عن طريق الأوكسجين المائي.
Protocol
تحذير: للاطلاع على أساليب المناولة السليمة وخصائص وسمية المواد الكيميائية الموصوفة في هذه الورقة، يرجى الرجوع إلى صحائف بيانات سلامة المواد ذات الصلة. بعض المواد الكيميائية المستخدمة سامة ومسرطنة ويجب توخي عناية خاصة. قد تشكل المواد النانوية مخاطر على السلامة وآثار صحية. وينبغي تجنب الاستنشاق والاتصال بالبشرة. ويجب توخي احتياطات السلامة، مثل إجراء التوليف الحفاز في غطاء الدخان وتقييم أداء المحفز باستخدام مفاعلات الأوتوكلاف. يجب ارتداء معدات الحماية الشخصية.
1- المعالجة المسبقة للأجهزة الوطنية
- تزج 1.0 غرام من CNTs في 50 مل من حمض النيتريك في كوب 100 مل.
- Sonicate الحل في 25 درجة مئوية لمدة 1.5 ساعة لإزالة الشوائب السطحية وتعزيز تأثير رسو محفز.
- نقل الحل إلى قارورة أسفل جولة 100 مل.
- الجزر الحل في خليط من حمض النيتريك (65٪) وحامض الكبريتيك (98٪) عند 60 درجة مئوية خلال الليل. تعيين نسبة الصوت في 3:1. سيؤدي ذلك إلى ظهور عيوب سطحية على النفثالينات.
- تصفية الحل للحصول على متعددة الجدار الكربون nanotube الصلبة. اغسل السّد بماء منزوع الأيونات.
- تجفيف الصلبة في 80 درجة مئوية لمدة 14 ساعة.
2. إعداد HNbWO6 صفائح نانوية حمض الصلبة15 عن طريق تبادل بروتونيك تليها تقشير
- مزيج كميات stoichiometric من لي2CO3 (0.9236 غرام) وأكاسيد المعادن Nb2O5 (3.3223 غرام) وWO3 (5.7963 غرام) بنسبة الأضراس 1:1:2.
- [كلسن] الخليط صلبة في 800 [ك] ل 24 [ه] مع واحدة طحن متوسّطة.
- ضع 10.0 غرام من مسحوق LiNbWO6 في 200 مل من 2 M HNO3 محلول مائي عند 50 درجة مئوية وتحريك خليط الحل لمدة 5 أيام (120 ساعة) مع استبدال واحد للحمض في 60 ساعة.
- تبادل السائل الحمضي كل يوم وكرر الخطوة 2.3.
- تصفية الصلبة وغسل الصلبة مع الماء منزوع الأيونات 3X.
- تجفيف الصلبة في 80 درجة مئوية بين عشية وضحاها.
- إضافة كمية من 25 wt.% TBAOH (رباعي (ن-butylammonium) هيدروكسيد) إلى 150 مل من محلول المياه منزوع الأيونات مع 2.0 غرام من المركب بروتونات تم الحصول عليها في الخطوة 2.6 حتى يصل درجة الحموضة 9.5 - 10.0.
- حرّك الحل أعلاه لمدة 7 أيام.
- طرد مركزي الحل أعلاه وجمع الحل الفائق الذي يحتوي على النانوشيتات المشتتة.
3. إعداد HNbMO6 صفائح نانوية حمض الصلبة
ملاحظة: الإجراء مشابهة للخطوة 2 باستثناء الخطوتين الأولى والثالثة.
- مزيج كميات stoichiometric من لي2CO3 وأكاسيد المعادن Nb2O5 و MoO3 في نسبة الأضراس من 1:1:2.
- [كلسن] الخلائط صلبة أعلاه في 800 [ك] في هواء ل 24 [ه] مع واحدة طحن متوسّطة.
- ضع 10.0 غرام من مسحوق LiNbMoO6 في 200 مل من 2 M HNO3 محلول مائي عند 50 درجة مئوية وتحريك خليط الحل لمدة 5 أيام (120 ساعة) مع استبدال واحد للحمض في 60 ساعة.
4. إعداد HTaWO6 صفائح نانوية حمض الصلبة
ملاحظة: الإجراء مشابهة للخطوة 2 باستثناء الخطوتين الأولى والثالثة.
- مزيج كميات stoichiometric من لي2CO3 وأكاسيد المعادن تا2O5 و WO3 في نسبة الأضراس من 1:1:2.
- [كلسن] الخلائط صلبة أعلاه في 900 [ك] في هواء ل 24 [ه] مع واحدة طحن متوسّطة.
- ضع 10.0 غرام من مسحوق LiTaWO6 في 200 مل من 2 M HNO3 محلول مائي عند 50 درجة مئوية وتحريك خليط الحل لمدة 5 أيام (120 ساعة) مع استبدال واحد للحمض في 60 ساعة.
5. إعداد HNbWO6/ MWCNTs بواسطة طريقة تجميع النانوشيت
- إضافة 2.0 غرام من CNTs متعددة الجدران التي تم الحصول عليها في الخطوة 1 إلى حل 100 مل من HNbWO6 nanosheets في قارورة أسفل جولة 250 مل.
- إضافة 100 مل من 1.0 M HNO3 حل مائي في قارورة أسفل جولة قطرة. سيؤدي ذلك إلى تجميع عينات النانوشيتات.
- استمر في تحريك الحل عند 50 درجة مئوية لمدة 6 ساعة.
- تصفية الصلبة وغسل الصلبة مع الماء منزوع الأيونات 3X.
- تجفيف الصلبة في 80 درجة مئوية بين عشية وضحاها.
- وزن الصلبة المجففة وتسجيل ٪ من تحميل حمض الصلبة على MWCNT.
6. إعداد Pt/20HNbWO6/CNTs بواسطة طريقة التشريب
- إذابة H2PtCl6∙H2O في الماء (1.0 غرام/100 مل).
- التشريب النانوشيتات المعدة كما عدّلت مواد CNTs بـ 1.34 مل من الحل المائي Pt أعلاه.
- تجفيف المواد النانوشيتات CNTs في 80 درجة مئوية، وتكلس المواد في 400 درجة مئوية لمدة 3 ساعة.
- الحصول على Nb(Ta) القائم على صفائح نانوية حمض الصلبة تعديل Pt / CNTs محفزات.
7- إثير عطري مشتق من الليغينين
ملاحظة: الإيثر الأثير العطري المشتق من الليغينين هو الإيثر الثنائي الفينيل في هذه التجربة. والإيثر الأثير العطري المستمد من الليغينين هو الإيثر الثنائي الفينيل في هذه التجربة. نشاط Pt/20HTaWO6/CNTs (تحويل 88.8٪، غير مبين في هذه الورقة) هو أقل من Pt/20HNbWO6/CNTs (99.6٪)، وبالتالي فإن العائد من السيكلوهيكسان ينخفض. وبالتالي، على الرغم من أنه تم الحصول على انتقائية أعلىمن السيكلوهيكسان على Pt/20HTaWO 6/CNTs، فإن انخفاض تحويل الإيثر الثنائي الفينيل ثنائي الفينيل يحد من استخدامه. استخدام معدات الحماية المناسبة وغطاء الدخان لأداء رد الفعل باستخدام الكواشف المسببة للسرطان.
- تخفيف 0.05 غرام من محفز في 5 ملليلتر من الكوارتز وللانزم. تحميل الحل في منتصف مفاعل سرير ثابت بين اثنين من الوسائد من الصوف الكوارتز.
- تقليل المحفز في H2 (40 مل / دقيقة) في 300 درجة مئوية لمدة 2 ساعة.
- ضخ المواد الوسيطة للإيثر الثنائي الفينيل ثنائي الفينيل (بما في ذلك 5.0 م.في المائة متفاعلة في n-decane و2.0 wt.% n-dodecaneكمعيار داخلي لتحليل كروماتوغرافيا الغاز) في مفاعل السرير الثابت بمعدلات تدفق مختلفة (0.05-0.06 مل/دقيقة)
- جمع المنتجات في أوقات الفضاء المختلفة المحددة على أنها نسبة بين كتلة محفز W (ز) ومعدل تدفق الركيزة F (ز / دقيقة).
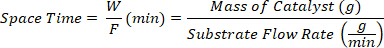
- تحديد المنتجات السائلة بواسطة GC (HP-5، 30 م × 0.32 مم × 0.25 م) مع 5977A MSD وتحليل خارج الخط عن طريق الكروماتوغرافيا الغاز (GC 450، FID، FFAP العمود الشعري 30 م × 0.32 مم × 0.25 م).
- تحديد تحويل المتفاعلين(محدبة٪)،الانتقائية تجاه المنتج الأول (S i٪)، وغلة المنتج i (Yi%) باستخدام المعادلات التالية:
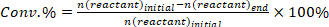 (1)
(1)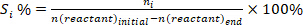 (2)
(2)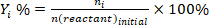 (3)
(3)
النتائج
وقد تمت دراسة أنماط انعراج الأشعة السينية (XRD) للسلائف LiNbWO6 وعينة محفزة مقابلة تبادل البروتون HNbWO6 لتحديد المرحلة (الشكل1 والشكل 2). تم استخدام NH3-درجة الحرارة المبرمجة desorption (NH3-TPD) للتحقيق في الحموضة السطحية للعينات محفز (الش?...
Discussion
المعالجة المسبقة للنفثالينات مع حمض النيتريكلا تزيد من مساحة سطح محددة (S BET) بشكل ملحوظ. النفثالينات الخام لها مساحة سطح ية محددة من 103 م2/ز بينما بعد العلاج، تم زيادة المساحة السطحية إلى 134 م2/ز. ولذلك، فإن هذه المعالجة المسبقة لخلق عيوب على سطح CNT سيكون لها تأثير إيجابي على ...
Disclosures
ليس لدينا ما نكشف عنه
Acknowledgements
وحظي العمل الوارد وصفه في هذه الورقة بدعم كامل بمنحة من مجلس المنح البحثية لمنطقة هونغ كونغ الإدارية الخاصة، الصين (UGC/FDS25/E09/17). كما نعرب عن امتناننا للمؤسسة الوطنية للعلوم الطبيعية في الصين (21373038 و21403026) لتوفيرها أدوات تحليلية لتوصيف المحفز ومفاعل السرير الثابت لتقييم أداء المحفز. ويود الدكتور هونغشو تشي أن يشكر على المساعدة البحثية التي منحها مجلس المنح البحثية في هونغ كونغ (UGC/FDS25/E09/17).
Materials
| Name | Company | Catalog Number | Comments |
| Carbon nanotubes (multi-walled) | Sigma Aldrich | 724769 | |
| Nitric acid (65%) | Sigma Aldrich | V000191 | |
| sulphuric acid (98%) | MERCK | 100748 | |
| Lithium carbonate (>99%) | Aladdin | L196236 | |
| Niobium pentaoxide (99.95%) | Aladdin | N108413 | |
| Tungsten trioxide (99.8%) | Aladdin | T103857 | |
| Molybdenum trioxide (99.5%) | Aladdin | M104355 | |
| Tantalum oxide (99.5%) | Aladdin | T104746 | |
| Chloroplatinic acid hexahydrate, ≥37.50% Pt basis | Sigma Aldrich | 206083 | |
| tetra (n-butylammonium) hydroxide 30-hydrate | Aladdin | D117227 | |
| Diphenyl ether, 98% | Aladdin | D110644 | |
| 2-Bromoacetophenone,98% | Aladdin | B103328 | |
| Diethyl ether,99.5% | Sinopharm | 10009318 | |
| n-Decane,98% | Aladdin | D105231 | |
| n-Dodecane,99% | Aladdin | D119697 | |
| Autoclave Reactor | CJF-0.05—0.1L (Dalian Tongda Equipment Technology Development Co., Ltd) | ||
| Tube furnace | SK2-1-10/12 (Luoyang Huaxulier Electric Stove Co., Ltd) |
References
- Jensen, J. L., Uaprasert, V., Fujii, C. R. Acid-Catalyzed Hydration of Dienes. 2. Changes in Activity Coefficient Ratios, Enthalpy, and Entropy as a Function of Sulfuric Acid Concentration. Journal of Organic Chemistry. 41 (10), 1675-1680 (1976).
- Ishida, H., Ono, M., Kaji, S., Watanabe, A. Synthesis of 1,3-Cyclohexadiene through Liquid Phase Dehydration of 2-Cyclohexen-1-ol in Aqueous Solution using Zeolite Catalyst. Nippon Kagaku Kaishi. 4, 267-275 (1997).
- Ishida, H. Liquid-phase hydration process of cyclohexene with zeolites. Catalysis Surveys from Japan. , 241-246 (1997).
- Ushikubo, T., Iizuka, T., Hattori, H., Tanabe, K. Preparation of highly acidic hydrated niobium oxide. Catalysis Today. 16, 291-295 (1993).
- Nakajima, K., et al. Nb2O5.nH2O as a heterogeneous catalyst with water-tolerant Lewis acid sites. Journal of the American Chemical Society. 133 (12), 4224-4227 (2011).
- Lam, E., Luong, J. H. T. Carbon Materials as Catalyst Supports and Catalysts in the Transformation of Biomass to Fuels and Chemicals. ACS Catalysis. 4 (10), 3393-3410 (2014).
- Sudarsanam, P., et al. Functionalised heterogeneous catalysts for sustainable biomass valorisation. Chemical Soceity Review. 47 (22), 8349-8402 (2018).
- Hara, M., et al. A carbon material as a strong protonic acid. Angewandte Chemie International Edition English. 43 (22), 2955-2958 (2004).
- Toda, M., et al. Biodiesel made with sugar catalyst. Nature. 438 (7065), (2005).
- Ji, J., et al. Sulfonated graphene as water-tolerant solid acid catalyst. Chemical Science. 2 (3), 484-487 (2011).
- Wang, Y., et al. Graphene-Based Metal/Acid Bifunctional Catalyst for the Conversion of Levulinic Acid to γ-Valerolactone. ACS Sustainable Chemistry & Engineering. 5 (2), 1538-1548 (2016).
- Ma, Q., et al. Catalytic depolymerization of lignin for liquefied fuel at mild condition by rare earth metals loading on CNT. Fuel Processing Technology. , 220-225 (2017).
- Rahzani, B., Saidi, M., Rahimpour, H. R., Gates, B. C., Rahimpour, M. R. Experimental investigation of upgrading of lignin-derived bio-oil component anisole catalyzed by carbon nanotube-supported molybdenum. RSC Advances. 7 (17), 10545-10556 (2017).
- Guo, Y., Chen, J. Bicomponent Assembly of VO2and Polyaniline-Functionalized Carbon Nanotubes for the Selective Oxidation of Biomass-Based 5-Hydroxymethylfurfural to 2,5-Diformylfuran. ChemPlusChem. 80 (12), 1760-1768 (2015).
- He, J., et al. Characterization of HNbMoO6, HNbWO6 and HTiNbO5 as solid acids and their catalytic properties for esterification reaction. Applied Catalysis A: General. , 145-152 (2012).
- Tagusagawa, C., Takagaki, A., Hayashi, S., Domen, K. Characterization of HNbWO6 and HTaWO6 Metal Oxide Nanosheet Aggregates As Solid Acid Catalysts. Journal of Physical Chemistry C. 113, 7831-7837 (2009).
- Niwa, M., Katada, N., Sawa, M., Murakami, Y. Temperature-Programmed Desorption of Ammonia with Readsorption Based on the Derived Theoretical Equation. Journal of Physical Chemistry. 99, 8812-8816 (1995).
- Leiva, K., et al. Conversion of guaiacol over supported ReOx catalysts: Support and metal loading effect. Catalysis Today. , 228-238 (2017).
- Deng, W., Liu, M., Tan, X., Zhang, Q., Wang, Y. Conversion of cellobiose into sorbitol in neutral water medium over carbon nanotube-supported ruthenium catalysts. Journal of Catalysis. 271 (1), 22-32 (2010).
- Huang, B., Huang, R., Jin, D., Ye, D. Low temperature SCR of NO with NH3 over carbon nanotubes supported vanadium oxides. Catalysis Today. 126 (3-4), 279-283 (2007).
- Takagaki, A., Tagusagawa, C., Hayashi, S., Hara, M., Domen, K. Nanosheets as highly active solid acid catalysts for green chemical syntheses. Energy & Environmental Science. 3 (1), 82-93 (2010).
- Hu, L. -. F., et al. Structure and photocatalytic performance of layered HNbWO6nanosheet aggregation. Journal of Nanophotonics. 9 (1), (2015).
- Geim, A. K. Graphene: Status and Prospects. Science. 324, 1530-1534 (2009).
- Golberg, D., et al. Boron Nitride Nanotubes and Nanosheets. ACS Nano. 4 (6), 2979-2993 (2010).
- Wilson, J. A., Yoffe, A. D. The transition metal dichalcogenides discussion and interpretation of the observed optical, electrical and structural properties. Advances in Physics. 18 (73), 193-335 (1969).
- Ma, R., Sasaki, T. Nanosheets of oxides and hydroxides: Ultimate 2D charge-bearing functional crystallites. Advanced Materials. 22 (45), 5082-5104 (2010).
- Pope, T. R., Lassig, M. N., Neher, G., Weimar Iii, R. D., Salguero, T. T. Chromism of Bi2WO6 in single crystal and nanosheet forms. Journal of Materials Chemistry C. 2 (17), 3223-3230 (2014).
- Yu, Y., et al. Controlled scalable synthesis of uniform, high-quality monolayer and few-layer MoS2 films. Scientific Reports. 3, 1866 (2013).
- Prasomsri, T., Shetty, M., Murugappan, K., Román-Leshkov, Y. Insights into the catalytic activity and surface modification of MoO3 during the hydrodeoxygenation of lignin-derived model compounds into aromatic hydrocarbons under low hydrogen pressures. Energy & Environmental Science. 7 (8), 2660-2669 (2014).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved