需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
制备和评价
摘要
Here, we describe a protocol for radiolabeling and in vivo testing of tridentate 99mTc(I) chelate-tetrazine derivatives for pre-targeting and bioorthogonal chemistry.
摘要
Pre-targeting combined with bioorthogonal chemistry is emerging as an effective way to create new radiopharmaceuticals. Of the methods available, the inverse electron demand Diels-Alder (IEDDA) cycloaddition between a radiolabeled tetrazines and trans-cyclooctene (TCO) linked to a biomolecule has proven to be a highly effective bioorthogonal approach to imaging specific biological targets. Despite the fact that technetium-99m remains the most widely used isotope in diagnostic nuclear medicine, there is a scarcity of methods for preparing 99mTc-labeled tetrazines. Herein we report the preparation of a family of tridentate-chelate-tetrazine derivatives and their Tc(I) complexes. These hitherto unknown compounds were radiolabeled with 99mTc using a microwave-assisted method in 31% to 83% radiochemical yield. The products are stable in saline and PBS and react rapidly with TCO derivatives in vitro. Their in vivo pre-targeting abilities were demonstrated using a TCO-bisphosphonate (TCO-BP) derivative that localizes to regions of active bone metabolism or injury. In murine studies, the 99mTc-tetrazines showed high activity concentrations in knees and shoulder joints, which was not observed when experiments were performed in the absence of TCO-BP. The overall uptake in non-target organs and pharmacokinetics varied greatly depending on the nature of the linker and polarity of the chelate.
引言
99m锝保留在核医学诊断中使用的主导放射性同位素,每年全球1,2,3进行超过5000万的成像程序。大多数临床使用99m锝剂是灌流型的放射性药物。有在其中99m锝涉及通过结扎特定生物标志物结合至靶向构建积极靶向化合物的数量有限。靶向99m锝放射性药物的创建通常是由99m锝-配体复合的对靶向分子的能力的影响阻碍了对感兴趣的生物标记物结合,或同位素半衰期不够长为具有更高分子量的生物分子用如抗体。后者通常需要数天的图像,以获得前的生物分子从非目标清除做卷烟的UE。预靶向提供了一种替代的方法来克服这些挑战。
预靶向结合生物正交化学已被证明是开发用于两个荧光和放射成像4,5,6,7,8个新的分子成像探针的有效方法。 -1,2,4,5-四(TZ)和反式 -cyclooctene(TCO)的衍生物之间的逆电子需求狄尔斯-阿尔德(IEDDA)反应, 如图1,已被证明是特别有效的6。这些组件的IEDDA反应可在PBS呈现快速动力学(K 2≈6000 M -1秒-1)和高选择性,因此非常适合在体内预先指定的应用9,10。
e_content">使用的最常见的方法包括施用的TCO源性靶向载体和以下足够长的延迟时间,放射性标记的四嗪是基于11℃,(18)F,64的Cu,89 Zr和111在已经施用。放射性标记的四嗪报告11,12,13,14,15,相反,仅存在一个一个99m锝标记Tz的,其使用一个HYNIC型配位体需要使用共配体的,以防止在体内蛋白结合和降解制备的报告16。作为替代方案,我们在这里报告99m锝(Ⅰ)的合成中使用的是家族,其形成具有稳定的三齿络合物的配体的标记的四嗪[99m锝(CO)3] +核心。 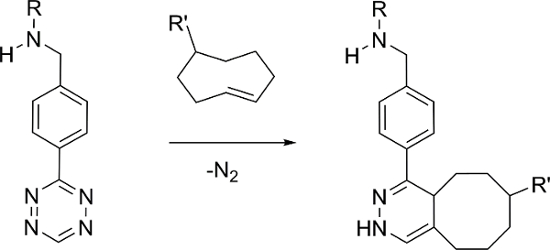
图1:四嗪和反 -cyclooctene之间的生物正交反应IEDDA。 请点击此处查看该图的放大版本。
制备配体的家族包含三齿螯合物,在极性和连接基团的金属结合区和Tz的( 图2)之间的性质不同而不同。该目标是确定一个99m锝-四嗪构造,可以有效地定位和在体内的TCO标记位点和当未结合迅速明确反应,以产生高靶-非靶比率。为了测试配位体,二膦酸盐的TCO-衍生物(TCO-BP),使用17。之前我们已经表明,TCO-BP定位于活跃的骨代谢领域,可以与反应放射性四嗪在体内 18。它是一种方便的试剂测试新四嗪,因为它可以在一个单一的步骤进行制备和实验可以在本地化主要发生在关节(膝和肩)正常小鼠进行。
研究方案
动物实验是由动物研究伦理委员会麦克马斯特大学按照加拿大议会关于动物饲养(廉政公署)的指导方针批准。
1. 99m锝TZ-齿配体的放射性标记
注意:以下步骤需要使用放射性化合物。工作只应在有执照的实验室进行与遵守安全和处置法规。微波反应应该专门为化学合成设计的微波炉进行。
- 合成[99m锝(CO)3(H 2 O)3] + 19,20
- 在微波小瓶中,合并8毫克K 2 [BH 3 CO 2],15毫克的 Na 2 CO 3,20毫克的 Na 2 B 4 O 7·10H 2 O和25毫克KOCO [CH(OH)]2 COONa·4H 2 O吹扫小瓶10分钟用氩气。
- 在0.9%的盐水(〜1100活度,〜30毫居里)到小瓶-添加4mL的标99m TCO 4。
- 热在微波反应在110℃下10秒后搅拌3.5分钟,以确保试剂的彻底混合。
- 使用〜400微升的1M HCl调节溶液的pH至3.5-4。验证使用pH试纸。
- 四嗪的放射性标记配体1-5
- 在250μL甲醇溶解21毫克2每配体(化合物1-5)。
- 添加250微升[99m锝(CO)3(H 2 O)3] +(〜74活度,〜2毫居里)向每个溶液中。
- 加热在60℃下用20分钟微波反应混合物中。
注:此步骤是所有5个四嗪相同。 - 对化合物2-5,使溶剂蒸发并重新dissol已经将所得产物在1毫升1:1的体积/体积的DCM:TFA。
- 在60℃下加热溶解反应产物(2-5)在6分钟(2-4)或10分钟(5)一台微波炉。
- 在冷却至室温后,蒸发用蒸发器(36℃,8毫巴,3分钟,6000转)的溶剂,并溶解在1干燥化合物:1的ACN:H 2 O或1:1的MeOH:H 2 O,之前HPLC纯化。
- 净化99m锝标记的化合物(1-5),包括使用HPLC(C18反相)分离未标记的四嗪配体的标记产物。通常情况下,使用30:70的ACN梯度洗脱:H 2 O(均含有0.1%TFA),以40:60的ACN:H 2 O在20分钟内(18分钟)和C 18的分析4.6×100毫米柱。同时使用UV(254纳米)和伽马探测。
- 每次取标记产品的一个小样本及其HPLC保留时间比较,一个共同的注射ected,无放射性,重新标记的标准(0.125毫克20%甲醇- H 2 O)。 [重新标记的标准是在UV HPLC迹识别,并且将在同一时间,在γ-HPLC跟踪该99m锝标记的化合物洗脱。此共注射示出了在可比较的保留时间的峰,确认了99m锝标记的化合物的身份。
- 蒸发从用蒸发器(36℃,8毫巴,3分钟,6000转)的HPLC级分的溶剂。
- 配制纯化的化合物在7.4 KBQ /微升在PBS中的浓度,含有0.5%BSA和0.01%吐温-80。
- 为了确保标记的化合物是稳定的,执行的体外稳定性研究。孵育在37℃配制的化合物为1,4和6小时,在每个时间点注射该混合物在HPLC上少量(3.7活度)评估稳定性。
2.预靶向生物分布研究
- 动物的制备
- 使用7-9周龄,雌性BALB / c小鼠(N = 3),管理TCO-BP生理盐水(20毫克/公斤)(5微克/μL)制定的,经尾静脉注射。
- 放置鼠标在物理约束装置,和识别位于尾部的横向表面上的静脉和用酒精棉签擦拭。在从尾部的端部大约2厘米,以小角度,平行于静脉插入一个30号针头。慢慢地压低柱塞注入,去掉针头和注射部位有轻微的压力施加干净的纱布海绵,直到出血停止。
- 在1小时后注射的TCO-BP,辖〜99m锝四嗪0.74活度(20微居里)的100微升0.5%的BSA的配制,0.01%吐温80在PBS中,通过尾静脉注射。
- 生物分布研究
- 在期望的时间点(T = 6小时),麻醉用3%异氟烷和2%的氧的气体混合物的小鼠。表现出以在麻醉鼠标ê捏撤离,以确保它们麻醉手术平面之下。
- 通过使用注射器肝素预处理心脏穿刺收集血液(1mL)中。它与鼻子的鼻锥为继续回麻醉将鼠标和定位对动物剑突。
- 插入地下25针,略向剑突下动物的中线的左边,在一个20°的角度。完全插入针,慢慢向后拉柱塞看到血针毂如果心脏被刺破。略微调整针的同时保持柱塞如果必要,刺穿心脏。慢慢地抽取血液到注射器中。
- 通过颈脱位安乐死的动物,而在麻醉下。
- 将每个动物在一个塑料袋,并使用剂量校准(99m锝设置)来测量全身活性水平。
- 收集在下面的组织和体液的预称重ED计数管:血液,骨(膝盖和肩部),胆,肾,肝,胃(有内容),小肠(有内容),大肠和盲肠(有内容),甲状腺和气管,有尿膀胱和尾部。
- 在冲洗PBS适当组织(不包括血液,胆囊和膀胱)将组织以适当的计数管之前去除血液和吸干。
- 放置动物胴体在一个塑料袋中并使用剂量校准测量剩余全身活性。
- 称量每个管含有组织样品。该管的减去初始重量以获得组织的质量。
- 使用剂量校准(99m锝设置)在注射为每只小鼠的时间来测量酶活性的测试样品(100μL)中的量。
注意:此测试样本等于注射体积,从而在注射时给予活动计数。 - 在组织的测量,一个时liquot5μL的以前使用的测试样品。使用多检测器γ计数器(99m锝设置)并计数,以获得每分钟(CPM)的计数为5微升试样。
- 使用所获得的两个值中2.2.9和2.2.10计算使用等式1获得的换算因子(CPM微居里-1)的活性和CPM关系。
(1)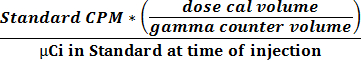
- 使用γ计数器测定在每个组织或流体样品的放射性的量。
- 使用方程1在相对于总注射剂量的测量的时间来计算每个组织或流体的活动量。此值然后通过器官重量归一化并且报告为组织的每克百分比注射剂量( 即,%ID /克)。
- 按照步骤2.1.2 2.2.13在艾比森用99m锝标记的四嗪配体进行阴性对照实验TCO-BP的行政长官。牺牲小鼠(n = 3)为0.5,1,4和6小时后注射,将获得的组织或流体,如上所述。
结果
该配体通过一个简单的还原胺化的策略( 图2),随后将产物的耦合到市售四嗪22,23使用不同的连接体和螯合剂合成。放射性标记物使用的所有化合物中相同的方法进行,并且是高度可重复的。 83%(1),45%(2),31%:该过程通过改变pH值,配体,反应时间和温度的量,随后在99m?...
讨论
不同极性的四嗪联三齿螯合物的集合被制备,并且与在体内的TCO衍生物IEDDA反应其99m锝复合物的效用进行评价。一种有效的和可再现的99m锝标记方法是五四嗪螯合物,其中该配位体的浓度为10 -3 M的标记步骤之后是叔丁基基(化合物2-5)的脱保护的发展。配体的高浓度使用以提高放射化学产率,并减少反应时间,这减少了四嗪21的...
披露声明
The authors declare they have no competing financial interests.
致谢
This work supported by research grant funding from the Natural Sciences and Engineering Research Council (NSERC) of Canada, the Ontario Institute for Cancer Research (OICR, #P.SI.015.8), and the Canadian Cancer Society (CCS, #703857). The authors acknowledge the contributions of Dr. Denis Snider who provided assistance in preparing the manuscript.
材料
| Name | Company | Catalog Number | Comments |
| Argon gas | Alphagaz | --- | --- |
| Na2CO3 | EMD Millipore | 106395 | --- |
| Na2B4O7·10H2O | Anachemia | S9640 | --- |
| KNaC4H4O6·4H2O | Anachemia | 217255 | --- |
| Technelite 99mTc generator | Lantheus medical imaging | --- | Source of 99mTcO4- |
| 0.9% Saline | Lantheus medical imaging | --- | To elute generator |
| 1 M HCl | Lab Chem | --- | --- |
| MeOH | Caledon | --- | --- |
| ACN | Caledon | --- | HPLC grade |
| Millipore H2O | Thermo Fisher Scientific | Barnstead Nanopure | --- |
| DCM | Caledon | --- | --- |
| TFA | Caledon | --- | --- |
| PBS | Thermo Fisher Scientific | 10010023 | pH 7.4 1x |
| BSA | Sigma Aldrich | A7906 | --- |
| Tween80 | Sigma Aldrich | P8047 | --- |
| Isoflurane | CDMV | 108737 | Supplier: Fresenius Kabi Animal Health |
| HPLC | Waters | 1525 Binary Pump, 2998 Photodiodde Array Detector, E-SAT/IN, Bioscan Flowcount PMT detector (item # 15590) | --- |
| HPLC column for analysis and purification of compounds 2-4 | Phenomenex | 00G-4435-E0 | Gemini® 5 µm C18 110 Å, LC Column 250 x 4.6 mm |
| HPLC column for analysis and purification of compounds 1 and 5 | Waters | 186003115 | XBridge BEH C18 Column, 130 Å, 5 µm, 4.6 mm x 100 mm |
| Microwave Reactor | Biotage | Initiator 8 | --- |
| Biotage V10 Evaporator | Biotage | Serial # V1041 | --- |
| Dose calibrator | Capintec, Inc. | CRC-25R | --- |
| Gamma counter | Perkin Elmer | Wizard 1470 Automatic Gamma Counter | --- |
| Animal room scale | Mettler Toledo | XP105 Delta Range | --- |
| Microwave vials | Biotage | 355629 | 0.5-2 mL |
参考文献
- Jurisson, S. S., Lydon, J. D. Potential Technetium Small Molecule Radiopharmaceuticals. Chem. Rev. 99 (9), 2205-2218 (1999).
- Kluba, C. A., Mindt, T. L. Click-to-chelate: Development of Technetium and Rhenium-Tricarbonyl Labeled Radiopharmaceuticals. Molecules. 18, 3206-3226 (2013).
- Amato, I. Nuclear Medicines Conundrum. Chem. Eng. News. 87 (36), 58-70 (2009).
- Hnatowich, D. J., Virzi, F., Rusckowski, M. Investigations of Avidin and Biotin for Imaging Applications. J. Nucl. Med. 28 (8), 1294-1302 (1987).
- Blackman, M. L., Royzen, M., Fox, J. M. Tetrazine Ligation: Fast Bioconjugation Based on Inverse-Electron-Demand Diels-Alder Reactivity. J. Am. Chem. Soc. 130 (41), 13518-13519 (2008).
- Devaraj, N. K., Weissleder, R., Hilderbrand, S. A. Tetrazine-Based Cycloadditions: Application to Pretargeted Live Cell Imaging. Bioconjugate Chem. 19 (12), 2297-2299 (2008).
- Rossin, R., et al. In Vivo Chemistry for Pretargeted Tumor Imaging in Live Mice. Angew. Chem., Int. Ed. 49 (19), 3375-3378 (2010).
- Zeglis, B. M., et al. Optimization of a Pretargeted Strategy for the PET Imaging of Colorectal Carcinoma via the Modulation of Radioligand Pharmacokinetics. Mol. Pharmaceutics. 12 (10), 3575-3587 (2015).
- Rossin, R., et al. Highly Reactive trans-Cyclooctene Tags with Improved Stability for Diels-Alder Chemistry in Living Systems. Bioconjugate Chem. 24 (7), 1210-1217 (2013).
- Rossin, R., Robillard, M. S. Pretargeted Imaging Using Bioorthogonal Chemistry in Mice. Curr. Opin. Chem. Biol. 21, 161-169 (2014).
- Denk, C., et al. Development of a 18F-Labeled Tetrazine with Favorable Pharmacokinetics for Bioorthogonal PET Imaging. Angew. Chem., Int. Ed. 53 (36), 9655-9659 (2014).
- Herth, M. M., Andersen, V. L., Lehel, S., Madsen, J., Knudsen, G. M., Kristensen, J. L. Development of a 11C-labeled Tetrazine for Rapid Tetrazine-Trans-Cyclooctene Ligation. Chem. Commun. 49 (36), 3805-3807 (2013).
- Li, Z., et al. Tetrazine-Trans-Cyclooctene Ligation for the Rapid Construction of 18F Labeled Probes. Chem. Commun. 46 (42), 8043 (2010).
- Nichols, B., Qin, Z., Yang, J., Vera, D. R., Devaraj, N. K. 68Ga Chelating Bioorthogonal Tetrazine Polymers for the Multistep Labeling of Cancer Biomarkers. Chem. Commun. 50 (40), 5215-5217 (2014).
- Zeglis, B. M., et al. A Pretargeted PET Imaging Strategy Based on Bioorthogonal Diels-Alder Click Chemistry. J. Nucl. Med. 54 (8), 1389-1396 (2013).
- García, M. F., et al. 99mTc-Bioorthogonal Click Chemistry Reagent for In Vivo Pretargeted Imaging. Bioorg. Med. Chem. 24 (6), 1209-1215 (2016).
- Russell, R. G. G. Bisphosphonates: The First 40 Years. Bone. 49 (1), 2-19 (2011).
- Yazdani, A., et al. A Bone-Seeking Trans-Cyclooctene for Pretargeting and Bioorthogonal Chemistry: A Proof of Concept Study Using 99mTc and 177Lu-Labeled Tetrazines. J. Med. Chem. , (2016).
- Alberto, R., et al. A Novel Organometallic Aqua Complex of Technetium for the Labeling of Biomolecules: Synthesis of [99mTc(OH2)3(CO)3]+ from [99mTcO4]- in Aqueous Solution and its Reaction with a Bifunctional Ligand. J. Am. Chem. Soc. 120 (31), 7987-7988 (1998).
- Alberto, R., Ortner, K., Wheatley, N., Schibli, R., Schubiger, A. P. Synthesis and properties of boranocarbonate: A convenient in situ CO source for the aqueous preparation of [99mTc(OH2)3(CO)3. J. Am. Chem. Soc. 123 (13), 3135-3136 (2001).
- Lu, G., et al. Synthesis and SAR of 99mTc/Re-labeled Small Molecule Prostate Specific Membrane Antigen Inhibitors with Novel Polar Chelates. Bioorg. Med. Chem. Lett. 23 (5), 1557-1563 (2013).
- Maresca, K. P., et al. Small Molecule Inhibitors of PSMA Incorporating Technetium-99m for Imaging Prostate Cancer: Effects of Chelate Design on Pharmacokinetics. Inorg. Chim. Acta. 389, 168-175 (2012).
- Bartholomä, M. D., et al. Insight into the Mode of Action of Re(CO)3 Thymidine Complexes. ChemMedChem. 5 (9), 1513-1529 (2010).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。