需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
用细胞色素 P450s 检测亚硝胺的体外Nitrosamide 形成的一般方法
摘要
细胞色素 P450s 致癌亚硝胺的α-羟基化是公认的代谢途径, 产生 DNA 损伤的中间体, 导致突变。然而, 新的数据表明进一步的氧化 nitrosamides 可能发生。我们描述了一个一般的方法, 检测 nitrosamides 产生的体外细胞色素 P450-catalyzed 代谢的亚硝胺。
摘要
N-亚硝胺是一种公认的环境致癌物质, 需要细胞色素 P450 氧化来表现活性。代谢活化机制包括自发分解为 DNA 烷剂的α-hydroxynitrosamines 的形成。DNA 损伤的积累和由此产生的突变最终会导致癌症。新的证据表明, α-hydroxynitrosamines 可以进一步氧化到 nitrosamides processively 细胞色素 P450s。因为 nitrosamides 一般比α-hydroxynitrosamines 更稳定, 也可以烷基化 DNA, nitrosamides 可能在癌变中起到作用。在本报告中, 我们描述了一个一般的协议, 评估 nitrosamide 生产从体外细胞色素 P450-catalyzed 代谢亚硝胺。该协议采用了一般的方法合成相关的 nitrosamides 和一个体外细胞色素 P450 代谢测定的液相色谱-nanospray 电离-高分辨率串联质谱检测。此方法在示例研究中检测到′-nitrosonorcotinine 作为′nitrosonornicotine 的次要代谢物。该方法具有较高的灵敏度和选择性, 是由于质量检测准确。该方法在多种硝细胞色素 P450 系统中的应用将有助于确定这种转化的普遍性。由于细胞色素 P450s 的多态性和活动性的变化, 更好地了解 nitrosamide 的形成有助于个别癌症风险评估。
引言
N-亚硝胺是一种在饮食、烟草制品和一般环境中发现的大量致癌物质;它们也可以在人体内形成内1。超过 300 N-硝基化合物已经被测试和 #62; 90% 被评估了作为致癌物在动物模型2,3。为了展示它们的致癌性, 这些化合物必须首先激活细胞色素 P450s1,2,3。研究表明, 细胞色素 P450s 容易氧化亚硝胺为α-hydroxynitrosamines (图 1), 这是高度活性化合物与半衰期的〜 5 s 之前自发分解到 alkyldiazohydroxides。后者可以在丢失 H2O 和 N2之后烷基化 DNA。由此产生的 DNA 加, 如果未, 可以导致突变, 如果在关键的 onco 或抑癌基因, 导致癌症的发展1。因此, 为了充分了解细胞色素 P450 氧化致癌亚硝胺的代谢途径、DNA 加和下游代谢产物, 已经花费了大量的精力。这些知识在个人癌症风险评估中具有潜在的应用价值4。
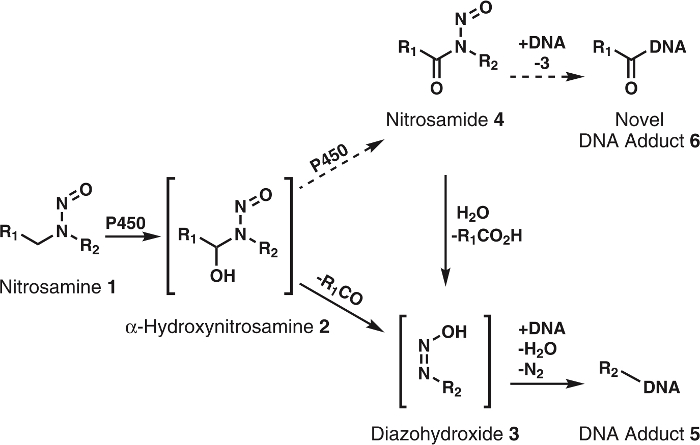
图 1: 一般和建议的亚硝胺代谢。
亚硝胺 (1) 被 P450s 氧化为α-hydroxynitrosamines (2), 自发分解为 alkyldiazohydroxides (3)。这些化合物可以与 dna 结合形成 dna 加。假设2被 P450s 进一步氧化为 nitrosamides 4。这些可以直接绑定到 dna, 形成新的 dna 加或水解到3 , 形成已知的 dna 加。r1和 r2表示任何烷基组。请单击此处查看此图的较大版本.
虽然α-hydroxynitrosamine 假说得到了大量数据的坚实支持, 但也存在一些不一致之处。主要的一个是α-hydroxynitrosamines 的短半衰期5,6。众所周知, 这些化合物是在内质网膜和后来的烷基化核 DNA 中产生的。鉴于他们的生命的几秒钟, 这是令人费解的这些中间体如何生存所需的旅行, 虽然胞。一个假说是, α-hydroxynitrosamines 的一部分被 processively 氧化为 nitrosamides7,8, 在比较9中相当稳定。这可能会发生通过保留α-hydroxynitrosamines 在细胞色素 P450 活性部位。这种类型的氧化的先例已经看到与尼古丁10, 酒精的11, 和简单的 alkylnitrosamines12,13。另外, nitrosamides 是直接作用的致癌物质2,3。根据它们的反应性9, 这些化合物被认为产生的 dna 加与α-hydroxynitrosamines 和新的, 未经探索的 dna 加 (图 1) 的结果相同。因此, 这一假说不仅解释了通过胞的运输, 也说明了 DNA 损伤产物的形成。
本文介绍了一种用于评价亚硝胺的细胞色素 P450-mediated 转化为 nitrosamides 的体外的通用协议。先前报告的′-nitrosonornicotine (NNN) 转换为′-nitrosonorcotinine (NNC) 的细胞色素 P450 2A6 被展示为示例14。该协议在广泛的基质酶系统的应用将有助于确定 nitrosamides 在整体硝代谢中的重要性。
Access restricted. Please log in or start a trial to view this content.
研究方案
1. 材料和常规过程
- 将 NNN 合成为以前描述的 15 。获得 norcotinine, P450 2A6 Baculosomes, 再生系统, 0.5x 和 #160; 反应缓冲器, 以及试剂级商业来源的所有其他化学品或溶剂.
- 在 500 MHz 光谱仪上记录核磁共振谱。报告化学变化为每百万分之 (ppm)。使用残余溶剂峰值作为内部参考为 1 H-nmr (7.26 ppm CDCl 3 ) 和 13 C-nmr (77.2 ppm CDCl 3 ).
注意: 峰值分裂使用了以下简称: s = 单线态, d = 双峰, dd = 双峰的双峰, dt = 三胞胎的双峰, dq = 双峰的四重奏, ddd = 双峰的双峰, 和 m = multiplet. - 对 LTQ Orbitrap Velos 上所选化合物执行高分辨率质谱 (人力资源), 并将数据报告为 m/z .
- 使用金预硅胶薄层色谱片 (40 毫米 x 80 毫米, 0.2 毫米厚) 与 254 nm 荧光指示剂 (tlc)。通过 UV 灯照射来可视化薄层色板.
- 在60和 #197 上执行闪光色谱; 70-150 目硅胶使用 1.5 cm x 15 cm 玻璃柱.
2。nitrosamide 阳性控制 ( N & #8242; -nitrosonorcotinine, NNC)
- 干燥, 在烤箱过夜 (16 小时, 〜140和 #176; C), 一个25毫升, 圆底烧瓶含有磁性搅拌棒。早上, 在 n 2 流下冷却烧瓶, 同时使用油起泡使 n 2 流速保持在每秒一个气泡下.
注: 冷却后, 不需要在 N 2 下保持烧瓶的预防措施. - 在通风罩中添加 norcotinine (31.8 毫克、0.196 摩尔)、醋酸酐 (5 毫升) 和乙酸 (1 毫升) 到冷却烧瓶中。在冷却到0和 #176 时, 将此混合物连续搅拌; C 冰浴.
警告: 醋酸酐和乙酸具有腐蚀性. - 添加纳米 2 (33.3 毫克, 0.483 摩尔) 在一个部分和连续搅拌的混合物为2.5 小时. 监测反应进展的 TLC (100% EtOAc, R f = 0.19, 参见步骤 1.4).
注: 在这段时间, 混合物将变得越来越黄与偶尔起泡. - 通过将混合物倒入 ice-cold H 2 O (18 毫升) 来淬火反应。在 100 ml 分漏斗中, 立即用18毫升 CH 2 Cl 2 提取水溶液。用 CH 2 Cl 2 (9 毫升) 将水层至少再抽出2次.
- 干燥100毫克 MgSO 的混合有机物 4 用于2分钟的过滤, 并通过旋转蒸发浓缩溶液以产生原油、黄油。在蒸发过程中, 将水浴加热到30和 #176; C.
注意: 如果化合物在 CH 2 Cl 2 中被溶解, 并且该解决方案在黑暗中存储在 2-8 和 #176 中, 则可以暂停该协议; C. - 用硅胶作为固定相和 100% EtOAc 为淋洗 16 , 通过柱层析 (见步骤 1.5) 净化粗化合物.
警告: NNC 和相关的 nitrosamides 应小心处理, 因为它们被认为是人类致癌物. - 溶解 CDCl 中的纯化合物 3 并使用 NMR (参见步骤 1.2) 确认结构并确定此解决方案的浓度 17 。将此解决方案存储在 2-8 和 #176 的黑暗中, 直到需要为止.
注意: 此解决方案将用作 体外 检测 (步骤 3.5) 中的正向控制。在支持信息中提供了核磁共振波谱和化学位移. - 使用纯 NNC 解决方案, 通过在步骤1.3 和4.3 中描述的参数直接注入高分辨率质谱仪 (人力资源), 确定准确的母体质量并测定产品离子质量.
注: 产品质量将用于检测该化合物在 体外 代谢试验 (步骤 4.3).
3。一个例子 nitrosamine-P450 体外 孵化
- 删除 P450 2A6 Baculosomes, 生动-再生系统, 和 10 mM NADP + 库存解决方案从-80 和 #176; C 冷冻, 让他们解冻冰。一旦解冻, 稀释 Baculosomes 和再生系统1:10 和1:50 分别, 成一个单一的1毫升管与0.5X 反应缓冲器。同样, 添加3和 #956; NADP + 库存解决方案为97和 #956; l 0.5X 反应缓冲器.
注意: NADP + 是光敏的。通过将容器包装在铝箔中来保护此解决方案。酶解对冻融循环敏感;将此限制为不超过2个周期。为将来的实验做必要的准备等分. - 对于每个孵化, 添加50和 #956; 酶溶液 l (含 5 pmol P450) 至1毫升管, 包含40和 #956; l 4 和 #956; M NNN 的解决方案, 由反应缓冲器。预孵化这种新的混合物为2分钟, 在37和 #176; C 使用水浴, 然后添加10和 #956; 稀释的 NADP + 解决方案。孵育整个系统 1-30 分钟, 在37和 #176; C.
注: 使用5分钟的潜伏期 (如 5, 10, 15 分钟等) 将提供足够的 nitrosamide 形成时间的过程. - 在所需的孵育时间后, 先将10和 #956 进行淬火; 3.0 n ZnSO 4 , 然后是10和 #956; 3.0 n Ba (哦) 2 的 l. 漩涡这个解决方案和白色沉淀将形成。离心样品在 8000 x g 为4分钟颗粒的沉淀.
注: 此步骤不能暂停, 因为形成的 nitrosamides 在水溶液中的稳定性有限。长时间的停顿可能导致错误的底片. - 立即将上清液移出, 并分析2和 #956; 用液体色谱法正 nanoelectrospray 电离高分辨串联质谱法 (LC-NSI + -人力资源/毫秒, 步骤 4.1-4.3).
- 对于正控制孵化, 将含有 100 fmol 的合成 NNC 溶液的分蒸发到1毫升的管下, 在 N 的流下为 2 。对这个小瓶, 添加完整的酶系统从步骤3.2 和继续按照描述的步骤 3.3-3.4.
- 对于负控制孵化, 执行所描述的实验 (步骤 3.2-3.4), 除替换50和 #956; L 酶溶液与0.5X 反应缓冲器.
4。用于 lc 组件的 lc-NSI + -人力资源/MS
- 的 nitrosamide 检测参数的示例, 请将步骤4.2 中的以下多级渐变应用于使用商用、手动包装的 18 C18 (5 和 #956; m) 的 UPLC 系统,100毫米 x 75 和 #956; m, 15 和 #956; m 孔毛细管柱.
- 使用 5 mM NH 4 华侨作为溶剂 a 和 MeCN 作为溶剂 b, 通过在1和 #956 的 5% b 处运行, 将样品加载到列上; L/分钟从 0-5 分钟, 然后减慢流速到0.3 和 #956; 之后的升/分钟。接下来, 运行从5到 20% b 以上4分钟的渐变, 后跟一个斜坡到 55% b 以上10分钟, 然后 re-equilibration 到 5% b.
- 在 LTQ Orbitrap 上执行 LC-NSI + -人力资源/MS。通过全扫描和 MS 2 碎片监视 NNC。以6万的分辨率进行全扫描, 并以 5 ppm 的质量公差提取准确的母质量 (192.07670)。使用 ms 2 碎片分离父离子 (2.0) 和由碰撞引发的离解 (CID) 与 25 eV 的碰撞能量, 分辨率 1.5万, 和扫描时间30毫秒提取的产品离子的准确质量 NNC ( m/z 192 m/z 134.04739 和 162.07874) 的质量公差为 5 ppm.
Access restricted. Please log in or start a trial to view this content.
结果
基于白色et al的工作。19, norcotinine 是硝化 NNC 清洁和高产 (80-92%), 以产生一个标准的体外实验。一个成功的反应的结构证据获得了从光谱分析包括1H 核磁共振, 13C 核磁共振, 舒适, 和 HSQC (支持信息) 与人力资源证实了父质量 [M + h]+在 5 ppm 的理论值 (图 2)。MS2的碎片 NNC 被用来确定最丰富的?...
Access restricted. Please log in or start a trial to view this content.
讨论
阐明亚硝胺的代谢是了解其致癌性的重要组成部分。由于涉及的细胞色素 P450s 和其他代谢酶是多态的, 进一步应用这一知识可能会发现高危个体1,4。新的数据表明, 进一步氧化α-hydroxynitrosamines, 推定主要代谢物的亚硝胺参与 DNA 结合, 以 nitrosamides 是可能的;然而, 这并没有在广泛的基板上进行强有力的测试。我们已经描述了一个协议来确定性氧化亚硝胺的...
Access restricted. Please log in or start a trial to view this content.
披露声明
作者没有什么可透露的。
致谢
这项研究得到了格兰特号的支持。CA-81301 来自国家癌症研究所我们感谢鲍勃的编辑协助, Dr. 彼得 Villalta 和鲁迅的质谱协助分析生物化学共享资源共济会癌症中心, 和 Dr. 亚当 t. Zarth 和 Dr. 安娜 k. 米歇尔的宝贵讨论和输入。分析生物化学共享资源由国家癌症研究院癌症中心资助 CA-77598 部分支持
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
参考文献
- Rom, W. N., Markowitz, S. Environmental and Occupational Medicine. , 4th ed, Wolters Kluwer/Lippincott Williams & Wilkins. 1226-1239 (2007).
- Preussmann, R., Stewart, B. W. Chemical Carcinogens, ACS Monograph 182. Searle, C. E. 2, 2nd ed, American Chemical Society. 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R. Chemical Carcinogens. ACS monograph 173. Searle, C. E. , American Chemical Society. 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. ACS Symposium Series. 101, American Chemical Society. 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5'(1')iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochemistry. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N'-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N'-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。