需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
闪烁表面增强拉曼散射的观测与分析
摘要
该协议描述了由于在银色表面上使用幂定律的单个分子的随机游走而引起的表面增强拉曼散射的分析。
摘要
从一个单一的分子在银 nanoaggregate 结, 闪烁的表面增强拉曼散射 (SERS) 观察。本文介绍了如何制备 SERS 活性银 nanoaggregate, 在显微图像中记录某些闪烁点的视频, 并分析闪烁的统计数据。在这个分析中, 幂律再现了明亮事件相对于其持续时间的概率分布。黑暗事件的概率分布由幂律和指数函数拟合。幂定律的参数代表了光明和黑暗状态的分子行为。随机游走模型和分子在整个银色表面的速度可以估计。即使使用平均值、自相关函数和超分辨率 SERS 成像, 也难以估计。在未来, 幂律分析应与频谱成像相结合, 因为这种分析方法不能单独证实闪烁的起源。
引言
表面增强拉曼散射 (SERS) 是高灵敏度的拉曼光谱从一个高贵的金属表面。由于拉曼光谱提供了基于尖峰位置的分子结构的详细信息, 通过分子中官能团的振动模式, 可以研究金属表面上的单个分子的信息使用 SERS1,2,3。从银 nanoaggregate 与吸附在分子水平, 一个闪烁的信号被 观察1,2,3,45,7,8,9,10,11,12,13,14,15, 16, 频谱波动1,2,3,4,5,67,8, 9,10,11,12,13,14。眨眼可以由一个单一的分子, 随机进出一个增强电磁 (EM) 领域在一个纳米银 nanoaggregate 交界处。因此, 闪烁被认为是分子检测的简单证据, 与使用 SERS 强度的泊松分布和双分析物2、3、17的技术相比。然而, 闪烁和波动频谱的详细机制, 可能强烈依赖于分子行为在 Ag 表面, 仍然是有争议的。
在先前的研究中, 用自相关函数分析了闪烁的 SERS, 它可以计算在增强的 EM 场中进出的分子的扩散系数和浓度12,13,14.此外, 一个标准化的标准偏差评分, 代表了不稳定性的总强度, 是从信号的时间剖面的15。然而, 这些分析方法可能是基于一些分子的行为。相比之下, 在一个超分辨率成像的闪烁 SERS, 分子行为在增强 EM 领域可以识别16。但是, 这些技术只能在增强的 EM 域中获得这些参数。单个分子在广泛范围内的随机行为 (例如, 在闪烁的 SERS 中) 可以表示为幂定律, 而不是平均4,5,6,7,8 ,9,10,11, 类似于单个半导体量子点 (数字)18,19中闪烁的荧光。通过使用幂律分析4、5、6、7、8、91011, 分子行为可以估计在明亮状态 (在增强的 EM 领域) 和黑暗状态10;那是, 分子的行为在整个银色表面可以估计。
对于此技术, 银胶体粒子使用4,5,6,,8,9,10,11。这些粒子显示各种局部的表面等离子共振 (LSPR) 波段, 强烈影响增强的电磁场时, 他们是在一定的波长兴奋。因此, SERS 活性银纳米粒子存在于胶体悬浮液中, 并能立即获得一些数据。在简单的纳米结构的情况下, 有特定的大小, 形状和安排, LSPR 依赖的 SERS 闪烁可以隐藏其他依赖性7;也就是说, 如果使用了 LSPR 的好的或坏的纳米结构, 则参数将是恒定的, 因此其他的依赖将被隐藏。幂律分析已被用于发现从银胶体粒子的各种依赖的闪光 SERS, 4,5,6,7,89,10,11。
Access restricted. Please log in or start a trial to view this content.
研究方案
1. 样品制备
-
制备银胶体纳米粒子20
- 制备银胶体纳米粒子, 溶解0.030 克硝酸银和0.030 克柠檬酸三钠, 在150毫升水中的200毫升圆形底烧瓶。
- 将烧瓶与回流 (Dimroth) 冷凝器结合。
- 用磁力搅拌器和搅拌棒在烧瓶中搅拌溶液。然后, 在150° c 的油浴中, 在烧瓶中加热搅拌溶液60分钟。
注: 溶液将变成黄色, 然后是乳白色的灰色。 - 在室温下冷却悬浮液, 并保持在冰箱内用铝箔覆盖的烧瓶中的悬浮。
注意: 在此点可以暂停协议。在一个月内, 用胶体纳米微粒储存在冰箱里。
-
多色闪烁发射样品的制备11
- 要准备一个显微镜幻灯片, 用手用肥皂冲洗玻璃盘子, 并用清水冲洗。
- 在玻璃板上加入0.1% 多聚 l-赖氨酸水溶液, 用鼓风机将溶液取出。
- 将银胶体悬浮液添加到玻璃板上, 然后用鼓风机将悬浮液除去。
- 用液体阻挡笔将玻璃板上的拖放区域括起来。
- 将蒸馏水滴在玻璃板上, 用另一玻璃板盖上, 以制造显微镜滑动, 防止水蒸发。
-
为单调的彩色闪烁 SERS 进行样品制备7,8,9,10
- 要准备一个显微镜幻灯片, 用手用肥皂冲洗玻璃盘子, 并用清水冲洗。
- 将银胶体悬浮液与 thiacyanine 或 thiacarbocyanine 染料 (分别为25或4µM) 和氯化钠 (10 毫米) 水溶液混合, 体积比为 2:1: 1。
- 将样品悬浮液放在玻璃板上, 然后用鼓风机将悬挂装置卸下。
- 用液体阻挡笔将玻璃板上的拖放区域括起来。
- 将氯化钠 (1 米) 的水溶液滴在玻璃板上, 使银纳米颗粒固定, 并用另一玻璃板盖住, 以制造显微镜滑动板, 防止溶液蒸发。
2. 闪光银纳米粒子的观察
-
样品照明
- 将使用协议1.2 或1.3 的样品玻璃板放在倒置显微镜的舞台上。
- 通过暗场冷凝器照亮样品玻璃板, 用物镜 (60X) 在玻璃板上聚焦各种彩色斑点 (蓝色、绿色、黄色和红色)。
- 用衰减光束照射样品玻璃板, 其相对于样品表面的角度为30°, 从二极管泵浦固态 (DPSS) continuous-wave (cw) 激光器通过干涉滤光片。
- 利用激光照射在同色的环境中观察银粒子为单调的彩色斑点, 将激光照射区移至视图中心, 并通过调整 z 方向上的舞台来聚焦在玻璃板上的斑点上。
-
闪烁的观察
- 在物镜后插入一个 long-pass 过滤器, 并通过干涉滤光片, 在30°相对于样品表面的情况下, 用 DPSS 的连续激光光束照射样品玻璃板。
- 通过在 x 和 y 方向移动舞台, 查找图 1中显示的闪烁点 (也请参见辅助材料中的图 S1 )。
- 用倒置显微镜记录闪烁斑点的视频, 耦合到一个冷却的数字电荷耦合器件 (CCD) 相机, 它的时间分辨率为 61-120 毫秒, 为20分钟。
3. 闪光 SERS 的分析
-
从视频中推导时间剖面
- 在控制 CCD 摄像机的软件中, 打开视频文件。
- 若要选择闪烁的斑点和暗区, 请拖动单独覆盖视频图像中有斑点的区域的区域。
- 若要从视频中的闪烁点和暗区域派生信号强度时间配置文件, 请在分析中选择时间分析, 然后在时间分析窗口中单击计算。
- 将数据另存为文本文件。
-
时间剖面分析
- 通过从暗区和/或与多项式函数的拟合中减去时间轮廓来拼合时间模板的基线, 如图 2A和2B所示。
- 计算由大约2000点、 I基和基线强度标准偏差 (σ) 组成的平均基线强度, 如图 2C和2D中所示。
- 使用比I基+ 3 的阈值更大的强度来区分明亮事件和暗事件, 并记录每个事件的持续时间。例如, 在图 3中, 将事件从0记录为黑色事件 (其持续时间为t = 3.5476 秒), 并将事件从3.5476 个到4.0981 秒记录为明亮事件 (持续时间为t = 0.5505 秒)。重复过程, 如表 1所示。
- 按照表 2的第一和第二行中的表示, 计算每个持续时间内的亮和暗事件数。
- 对每个工期的事件数求和, 但事件少于持续时间t。例如, 在表 2的第二和第三行中表示, 对每个持续时间的事件数进行求和 ( t = 0.0612 秒的事件除外) 为 41 + 18 + 9 +..。结果等于t = 0.1223 s 的求和,即103。
- 按每个工期划分总结, 并对其进行规范化。例如, 如表 2所示, 将持续时间的总和t = 0.0612 s 除以持续时间0.0612 秒。结果是3351.5791。然后, 将结果除以表 2中第四行中的结果总数。概率分布被导出为0.64494。
- 将明亮事件的概率分布绘制为Pon(t), 并将其持续时间t在对数对数图中, 并适合日志10P(t) 的日志10()
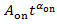 在上为特定的闪烁点推断幂定律指数α。
在上为特定的闪烁点推断幂定律指数α。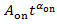 如果Pon(t) 是由安装的, 则拟合的行将在P(t)上的小数值上偏离图形, 如图 4A中的虚线所示。
如果Pon(t) 是由安装的, 则拟合的行将在P(t)上的小数值上偏离图形, 如图 4A中的虚线所示。 - 按日志10将暗事件的概率分布绘制为P关(t), 并将其持续时间t在对数对数图中, 并适合日志10P关闭(t)。从相同的闪烁点推断出幂律指数α
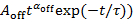 off和截断时间τ 。如果Poff(t) 是由安装的, 则拟合的曲线将从位于
off和截断时间τ 。如果Poff(t) 是由安装的, 则拟合的曲线将从位于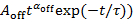 P关闭(t) 的小值中偏离图形。
P关闭(t) 的小值中偏离图形。 - 对视频中的其他闪烁点重复3.2.1 到3.2.8。
Access restricted. Please log in or start a trial to view this content.
结果
从1.2 号协议制备的多聚 l-赖氨酸银粒子, 观察到了 SERS 和表面增强荧光的多色闪烁斑点, 如图 111所示。相比之下, 由 1.37、8、9、10所制备的染料分子, 在银粒子上观察到来自 SERS 的单调彩色闪烁点。有两种类型的 "阴性" 结果: 连续的结果...
Access restricted. Please log in or start a trial to view this content.
讨论
从银 nanoaggregate 结, SERS 被发射。因此, 我们需要准备粒子而不是胶体纳米粒子, 这是被柠檬酸阴离子覆盖。银聚合体是由添加多聚 l-赖氨酸所产生的盐析效应形成的, 它具有-NH3+ , 是来自氯化钠的 SERS、Na+阳离子的来源, 如补充材料的图 S2所示。此外, 为了照亮宽区的许多斑点, 不聚焦的激光光束是通过一个不附着在显微镜上的透镜, 相对于样品表面, 以30°的角度?...
Access restricted. Please log in or start a trial to view this content.
披露声明
作者没有什么要透露的。
致谢
作者感谢 Prof. y Ozaki (Kwansei 学院大学) 和 Dr. (国家高等工业科技研究院) 对这项工作进行了卓有成效的讨论。这项工作得到了教育、文化、体育、科学和技术部 (No. 16K05671) 的 KAKENHI (补助金) 的支持。
Access restricted. Please log in or start a trial to view this content.
材料
| Name | Company | Catalog Number | Comments |
| Silver nitrate, 99.8% | Wako | 194-00832 | |
| Trisodium citrate dihydrate, 99. % | Wako | 191-01785 | |
| Poly-L-lysine aqueous solution, 0.1% | Sigma-Aldrich | P8920 | |
| 3,3'-disulfopropylthiacyanine triethylamine | Hayashibara Biochemical Laboratories | NK-2703 | a kind of thiacyanine dyes |
| 3,3'-diethyl-5,5'-dichloro-9-methylthiacarbocyanine iodine salt | Hayashibara Biochemical Laboratories | SMP-9 | a kind of thiacarobocyanine dyes |
| Sodium chloride, 99.5% | Wako | 191-01665 | |
| Dimroth condenser | Iwaki | 61-9722-22 | perchased from AS ONE |
| Magnetic stirrer | Corning | DC-420D | |
| Oil bath | Advantech | OS-220 | |
| Glass plate | Matsunami | S-1112 | Microscope slide |
| Blower | Hozan | Z-288 | Air duster |
| Liquid blocker pen | Daido Sangyo | LIQUID BLOCKER (Super Pap Pen). Ready-to-use hydrophobic barrier pen designed for immunohistochemistry applications | |
| Inverted microscope | Olympus | IX-70 | |
| Objective lens | Olympus | LCPlanFl 60× | NA 0.7 |
| Dark field condenser | Olympus | U-DCD | NA 0.8–0.92 |
| Cooled digital CCD camera | Hamamatsu | ORCA-AG | controlled by software Aqua Cosmos |
| Software for the cooled digital CCD camera | Hamamatsu | AquaCosmos | used for also derivation of the time-profiles from the blinking spots in the video |
| Color CCD camera | ELMO | TNC-C920 | not used for analysis |
| DPSS laser | RGB laser system | NovaPro532-75 | λ = 532 nm; 60 mW (corresponds to a power density of 600 W/cm2) |
| Interference filter | Semrock | LL01-532-12.5 | |
| Long pass filter | Semrock | BLP01-532R-25 | |
| Software for the distinguishment and counting of the bright/dark events | home-maid | programmed by C++ | |
| Software for the fitting by a power law | LightStone | Origin6.1 |
参考文献
- Qian, X. M., Nie, S. M. Single-molecule and single-nanoparticle SERS: from fundamental mechanisms to biomedical applications. Chem. Soc. Rev. 37, 912-920 (2008).
- Pieczonka, N. P. W., Aroca, R. F. Single molecule analysis by surfaced-enhanced Raman scattering. Chem. Soc. Rev. 37, 946-954 (2008).
- Kneipp, J., Kneipp, H., Kneipp, K. SERS -a single-molecule and nanoscale tool for bioanalytics. Chem. Soc. Rev. 37, 1052-1060 (2008).
- Kitahama, Y., Ozaki, Y. Analysis of blinking SERS by a power law with an exponential function. Frontiers of Surface-Enhanced Raman Scattering: Single-Nanoparticles and Single Cells. , Wiley. Chichester. Chapter 6 (2014).
- Kitahama, Y. Truncated Power Law Analysis of Blinking SERS. Frontiers of Plasmon Enhanced Spectroscopy Volume 1 (ACS Symposium series Vol. 1245). , American Chemical Society. Washington DC. Chapter 4 (2016).
- Bizzarri, A. R., Cannistraro, S. Lévy Statistics of Vibrational Mode Fluctuations of Single Molecules from Surface-Enhanced Raman Scattering. Phys. Rev. Lett. 94, 068303(2005).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Power-law analysis of surface-plasmon-enhanced electromagnetic field dependence of blinking SERS of thiacyanine or thiacarbocyanine adsorbed on single silver nanoaggregates. Phys. Chem. Chem. Phys. 13, 7439-7448 (2011).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of excitation laser intensity dependence of blinking SERRS of thiacarbocyanine adsorbed on single silver nanoaggregates by using a power law with an exponential function. Chem. Commun. 47, 3888-3890 (2011).
- Kitahama, Y., Enogaki, A., Tanaka, Y., Itoh, T., Ozaki, Y. Truncated power law analysis of blinking SERS of thiacyanine molecules adsorbed on single silver nanoaggregates by excitation at various wavelengths. J. Phys. Chem. C. 117, 9397-9403 (2013).
- Kitahama, Y., Araki, D., Yamamoto, Y. S., Itoh, T., Ozaki, Y. Different behaviour of molecules in dark SERS state on colloidal Ag nanoparticles estimated by truncated power law analysis of blinking SERS. Phys. Chem. Chem. Phys. 17, 21204-21210 (2015).
- Kitahama, Y., Nagahiro, T., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of blinking from multicoloured SERS-active Ag colloidal nanoaggregates with poly-L-lysine via truncated power law. J. Raman. Spectrosc. 48, 570-577 (2017).
- Habuchi, S., et al. Single-Molecule Surface Enhanced Resonance Raman Spectroscopy of the Enhanced Green Fluorescent Protein. J. Am. Chem. Soc. 125, 8446-8447 (2003).
- Weiss, A., Haran, G. Time-Dependent Single-Molecule Raman Scattering as a Probe of Surface Dynamics. J. Phys. Chem. B. 105, 12348-12354 (2001).
- Emory, S. R., Jensen, R. A., Wenda, T., Han, M., Nie, S. Re-examining the origins of spectral blinking in single-molecule and single-nanoparticle SERS. Faraday Discuss. 132, 249-259 (2006).
- Itoh, T., Iga, M., Tamaru, H., Yoshida, K., Biju, V., Ishikawa, M. Quantitative evaluation of blinking in surface enhanced resonance Raman scattering and fluorescence by electromagnetic mechanism. J. Chem. Phys. 136, 024703(2012).
- Willets, K. A. Super-resolution imaging of SERS hot spots. Chem. Soc. Rev. 43, 3854-3864 (2014).
- Dieringer, J. A., Lettan, R. B., Scheidt, K. A., Van Duyne, R. P. A Frequency Domain Existence Proof of Single-Molecule Surface-Enhanced Raman Spectroscopy. J. Am. Chem. Soc. 129, 16249-16256 (2007).
- Cichos, F., von Borczyskowski, C., Orrit, M. Power-law intermittency of single emitters. Curr. Opin. Colloid Interface Sci. 12, 272-284 (2007).
- Tang, J., Marcus, R. A. Mechanisms of fluorescence blinking in semiconductor nanocrystal quantum dots. J. Chem. Phys. 123, 054704(2005).
- Lee, P. C., Meisel, D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J. Phys. Chem. 86, 3391-3395 (1982).
- Krichevsky, O., Bonnet, G. Fluorescence correlation spectroscopy: the technique and its applications. Rep. Prog. Phys. 65, 251-297 (2002).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and Chemical Applications of Fluorescence Correlation Spectroscopy: A Review. Biochemistry. 41, 697-705 (2002).
Access restricted. Please log in or start a trial to view this content.
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。