Method Article
正交胰腺肿瘤的产生与肿瘤渗透T细胞细胞毒性的外体特征
摘要
该协议描述了正交胰腺肿瘤的外科生成和新鲜分离的鼠胰腺肿瘤的快速消化。消化后,可行的免疫细胞群可用于进一步下游分析,包括通过流式细胞测定检测细胞内细胞因子的T细胞外体刺激。
摘要
胰腺癌的体内模型为研究疾病动态、免疫渗透和新的治疗策略提供了宝贵的工具。正交鼠模型可以同时对大量免疫能力小鼠进行,价格相对便宜,并保存了共生组织的微环境。正交肿瘤中T细胞渗透和细胞毒性活性的定量提供了抗肿瘤反应的有用指标。
该协议描述了通过将少量合成肿瘤细胞重新悬浮在5μL基底膜中直接注入胰腺,从而手术生成正交胰腺肿瘤的方法。携带正交肿瘤的小鼠大约需要 30 天才能到达终点,此时可以采集和处理肿瘤,以表征肿瘤渗透 T 细胞活性。使用胶原酶和DNase的快速酶消化允许从肿瘤中提取单细胞悬浮液。保存从肿瘤中提取的免疫细胞的生存能力和细胞表面标记物;因此,它适用于多种下游应用,包括用于培养或RNA提取的免疫细胞的流量辅助细胞分类、免疫细胞群的流式细胞测定分析。在这里,我们将T细胞群对细胞内细胞因子定量(IFN®和TNF®)和脱粒活性(CD107a)的体外刺激描述为整体细胞毒性的量度。在抗CD107a抗体存在的情况下,用醋酸和电霉素刺激全肿瘤消化5小时,以调节细胞因子的产生和脱粒。在最后4小时中加入布雷芬丁A和莫嫩辛,以阻止细胞外传输,并最大化细胞因子检测。然后对细胞进行细胞外和细胞内染色,进行流式细胞测定分析,其中对IFN+ 、TNF+和CD107a+CD4+和CD8+T细胞的比例进行了量化。
该方法为肿瘤微环境的综合分析提供了基础。
引言
该方法详细介绍了使用少量细胞材料生成正交胰腺肿瘤的外科手术,以及随后对已建立肿瘤的快速解离,以便对免疫细胞群进行全面的流式细胞测定分析,包括T细胞功能的体外分析。
胰腺导管腺癌(PDAC)是一种侵略性癌,只有8%的患者存活5年1。由于只有不到20 % 的病人有资格接受第2次手术切除手术,因此,新的病人样本不易获得研究,因此体内模型为研究这种疾病提供了必要的工具。PDAC有多个小鼠模型:正射、皮下、转基因、静脉注射和患者衍生异种移植(PDX),这里广泛描述了3。此处描述的正交模型允许将合成PDAC细胞注入免疫能力小鼠的胰腺中。这可以在大量野生型或突变小鼠中执行,从而为治疗剂的比较提供了一个经济高效且一致的模型。重要的是,正交模型为肿瘤细胞生长和转移提供共生微环境,我们手中和其他4个转移到临床相关部位(如肝脏),使其比皮下或化学诱导模型更具临床相关性。正交肿瘤显示PDAC的主要特征,如具有很强的脱塑性反应,具有丰富的成纤维细胞和细胞外基质沉积5。PDAC的转基因模型是鼠种模型的黄金标准,最常用的是KPC模型,它表示突变KrasG12D/+和Trp53R172H/+在胰腺特异性Pdx-1-Cre启动子6下。这里将审查KPC和其他体内PDAC模型。KPC小鼠自发地发展胰腺肿瘤与疾病进展,忠实地复制人类PDAC6的特点。然而,对于所有转基因模型,育种方案成本高昂,肿瘤进展是可变的,因此往往需要大量的小鼠。PDX模型使用患者衍生的肿瘤细胞或片段,然后由正射或更常见地在免疫功能低下小鼠中分皮生长。异种移植模型为筛选治疗化合物和考虑患者异质性提供了有用的工具。然而,它们不能提供完全的免疫微环境,从而限制了其应用8,9。
一旦建立,正交肿瘤通常需要约1个月或更长时间生长(取决于使用的细胞系),并形成大肿瘤,可以很容易地成像通过超声波或MRI跟踪进展,并确定治疗效果4,5,10。然而,一旦呈指数增长,肿瘤生长的最后阶段可以迅速,所以大多数治疗方案是相对早开始(例如,14天)11,12。免疫系统在肿瘤发育中起着关键作用,包括PDAC,其特征是免疫抑制肿瘤渗透与相对缺乏T细胞和频繁存在的骨髓细胞13。在PDAC中T细胞的高存在可以产生更好的预后14,15。然而,作为单一剂,免疫检查点抑制剂,缓解T细胞免疫抑制,如抗CTLA-416和抗PD-L117,在PDAC患者中没有表现出临床效益,很可能是因为整体T细胞反应性非常低。然而,抗CD40等主要T细胞反应的试剂可以克服抗PD-L1/CTLA-4的抗抗18、19,以及用GM-CSF分泌异体PDAC疫苗(GVAX)接种疫苗,可增加PDAC肿瘤20的免疫原性,表明增强T细胞反应形成重要的治疗途径。
抗肿瘤T细胞反应的关键是通过T细胞受体(TCR)识别肿瘤衍生抗原,以及随后产生的细胞毒性细胞因子和颗粒。虽然T细胞抗原识别可以通过TCR测序来确定,但这种方法既昂贵又耗时。然而,肿瘤渗透T细胞子集的定量提供了抗肿瘤反应的良好指示。进一步检查T细胞活动外体内的脱粒,细胞因子生产和其他细胞毒性因子提供了更深入的功能分析。这些测定可以在新鲜肿瘤样品上进行,通过流式细胞测定可以快速测量T细胞功能的许多参数。
CD8+和CD4+T细胞产生细胞因子,如IFN®和TNF®,以增强免疫反应21。IFN- 诱导MHCI对靶细胞的调节,诱导免疫细胞的分化和招募,帮助细胞死亡。由CD8+T细胞生产的IFN®具有很好的特征,是抗肿瘤反应的一部分,与肿瘤回归22、23相关。TNF® 是 CD8+和 CD4+ T 细胞产生的另一种抗炎细胞因子。它增强了TCR依赖性的激活和T细胞的增殖,有助于抗肿瘤反应。在TCR参与时,细胞毒性CD8+T细胞可以进行脱粒,其中含有细胞毒性分子的预形成分泌的岩体被释放到免疫突触中,导致靶细胞降解21。这些分子包括Perforin,一种与靶细胞膜结合的蛋白质,形成孔隙,然后破坏膜完整性,并允许扩散21或内分泌24其他细胞毒性分子,如Granzyme B,直接进入目标细胞的细胞质。Granzyme B是一种蛋白酶,它导致靶细胞内多种蛋白质的降解,导致细胞死亡21。这种分子的释放需要内分泌体外向细胞表面,其中内体标记CD107a(也称为LAMP-1)被暂时地并入细胞膜25。
T细胞对细胞体分泌的测量需要通过流量辅助细胞分选或基于珠的分离测定进行分离,这在大量样品上无法同时进行。然而,细胞内细胞因子的测量不需要任何预隔离步骤,并且一次可以在多个样品上轻松执行,从而允许采用更高的通量方法。由于细胞因子被T细胞迅速分泌,细胞内水平可能检测不到,因此T细胞需要刺激以增加基底细胞因子的产生。为了评估抗原驱动的细胞因子的产生,TCR确认的抗原必须由在体外注的APC呈现给T细胞。在不知道抗原特异性的情况下,需要广泛的刺激方法。TCR刺激可以使用抗CD3/28珠进行模拟,提供TCR激活和共刺激,诱导细胞因子的产生和增殖。然而,一个更具成本效益的替代物是使用PMA和电霉素,它们共同广泛激活信号通路,导致细胞内细胞因子的合成和释放。具体来说,PMA激活蛋白激酶C(PKC)和碘霉素提高细胞内Ca2+离子,导致细胞信号增加。为了保持细胞因子的细胞内含量,这种刺激可以有效地与蛋白运输抑制剂布雷芬A和莫嫩辛结合,后者阻断了Golgi中的蛋白质,从而防止细胞外释放。使用PMA/电霉素是刺激T细胞的成熟方法,细胞外释放和细胞内细胞因子26之间有很强的相关性。用PMA和电霉素刺激T细胞也会增加对细胞膜的细胞体贩运,因此CD107a在被回收到细胞之前在细胞表面暂时地整合。通过在刺激过程中加入抗CD107a抗体,可以将其用作脱粒活性25的标记物。
该方法快速消化肿瘤,提供单细胞悬浮液。此时,单个群体可以直接染色进行流式细胞测定,或通过下游方法进行纯化:流量辅助细胞分选或磁珠分离。制备用于流式细胞测定分析的单细胞悬浮液,可对多个免疫细胞群及其表型标记进行高通量分析,从而准确量化免疫细胞数量和表型。
最后,此处描述的消化方案可防止细胞表面标记物损失,并保持免疫细胞活力,使免疫细胞能够根据需要进行进一步的细胞纯化步骤和培养。然而,这种方法尚未测试从这种消化中衍生上皮细胞。
研究方案
根据1986年英国内政部动物和科学程序法以及2010/63/EU欧洲指令,正交性胰腺肿瘤如前所述产生。所有小鼠都接受术前监测疼痛或痛苦的迹象,包括但不限于体重减轻(> 15%,在72小时或20%在任何特定时期),皮毛,眼睛变窄,步态升高,驼背外观,以及伤口感染的迹象,包括出血,发红和溃疡。肿瘤生长通过触觉监测,其他临床症状,如人工呼吸,黄斑和冷四肢也被监测,以评估是否达到终点的迹象。所有程序都应在无菌条件下进行。流式细胞染色前使用的所有试剂都应在无菌条件下制备。
1. 注射用肿瘤细胞的制备
- 从-20°C取基底膜的等分,在4°C的冰上过夜。
注:基底膜浓度可能因批次而异;因此,必须在体内测试很多特定的基底膜批次,以确保可重复性。一批新的基底膜在4°C的冰上解冻,然后在用户定义的等分中,在冰上,然后进一步储存在-20°C,直到需要。这样,在使用基底膜时,可最大限度地减少移液和冻融。- 将无菌 PBS 置于 4°C 过夜以冷却。
- 将无菌 200 μL 和 1000 μL 移液器吸头置于 -20°C 过夜以冷却。
- 使用无支原体的肿瘤细胞,在解冻后和收获前生长的日志阶段至少生长2-10个通道。该协议使用雌性鼠C57BL/6 KPC衍生的细胞系:TB32048作为慷慨的礼物由大卫·塔夫森实验室提供。
- 当收获需要肿瘤细胞时,在PBS中从烧瓶中取出培养基并洗涤细胞两次(预热至37°C)。
- 在37°C(到T175烧瓶中,加5 mL)在烧瓶中加入2x胰蛋白酶(预热至37°C)10分钟。
- 10分钟后,通过轻轻敲击烧瓶并在介质中重新悬浮,向烧瓶和分离细胞中加入同等体积的完整介质(10%FBS、1x 青霉素、DMEM 中的1倍链霉素)。
- 在300 x g和室温(RT)下将细胞转移到管和离心机5分钟。
- 取出上清液,并在完整的培养基中重新悬浮细胞,以便细胞计数。
- 在300 x g和RT下再次离心细胞5分钟,并去除上清液。
- 在预冷冻PBS中重新悬浮细胞,达到1x106细胞/mL的浓度。
注:此库存浓度准备在 5 μl 中最终注射浓度为 1000 个细胞。我们发现,在低注射量下注射数量较低的细胞最大限度地减少了细胞泄漏,因此增加了可重复性,但是,肿瘤的生长可能是细胞系依赖性的,因此用户应优化每个细胞系。
- 除此之外,将预先引用的地下室膜等分放在冰上,放入发动机罩。
- 注射准备的PBS中基底膜、PBS和肿瘤细胞的最终溶液比例为5:3:2。因此,在基底膜的500μL等分液中,使用预冷却的1000μL移液器尖端添加300μL的预冷却PBS。
- 将 PBS 直接添加到地下室膜等分,以尽量减少移液。
- 将 p1000 设置为 300 μL,并重新悬浮 PBS 和地下室膜,确保将管保持在冰上,以保持地下室膜处于液态状态。
- 完成从 p1000 尖端弹出所有地下室膜后,将尖端留在管中,让任何地下室膜/PBS从移液器尖端下。
- 5-10分钟后,将更多的基底膜从p1000尖中弹回管子中,让管子放在冰上。
- 在PBS中取取200μL的再悬浮肿瘤细胞,并使用预冷却的200μL移液器尖端直接添加到基底膜中。
- 取一个新鲜的预冷却 p1000 移液器尖端,将移液器设置为 300 μL,然后重新悬浮 30-40 次。较大的移液器尖端(设置在低体积上)更可取,因为地下室膜可以在重新悬浮期间向上移动,并触摸移液器尖端过滤器。
- 肿瘤细胞准备注射。手术期间将肿瘤细胞/基底膜放在冰上。
2. 肿瘤细胞的正交注射
- 在动物设施中使小鼠适应7天。
- 手术前约2小时,刮伤腹部和背部的左侧,然后在颈部刮毛下进行术前镇痛(50-100微克/千克的布丙诺啡)。
- 准备手术现场,用热垫将鼠标放在一起,并覆盖周围设备和鼠标的窗帘。消毒所有手术工具;为每个鼠标准备足够的工具集。
- 将鼠标放入带有 O2腔室的 5% 无氟胶,直到失去知觉。
- 将鼠标(躺在其背上)转移到热垫上,并使用面罩维持麻醉,通常以较低的2-3%的离形剂。
- 确认深层麻醉;当后爪被捏住并监测呼吸速率保持不变时,通过踏板退步反射的丢失来识别。
- 用窗帘盖住身体,只露出被遮盖的部分。确保鼠标牢固地在麻醉面罩中。
- 使用无菌棉芽,在被覆盖区域以圆形运动添加碘溶液:从中心开始,向边缘盘旋。再次重复处理新鲜棉芽和碘。
- 使用手术刀在胰腺/脾脏位置(左上象限)上方进行 1 厘米切口。无菌剪刀也可用于切口(如果愿意)。
- 用钳子把皮肤拉开。使用新的钳子,找到围肠壁,并使用剪刀通过围肠壁再切1厘米。
- 使用第二对钳子从体内提取胰腺,这可能与脾脏一起。
- 轻轻反转肿瘤细胞/基底膜的瓶数次混合。
- 在地下室膜中用含有1,000个肿瘤细胞的5μL制备玻璃注射器,并在热垫上放置几秒钟,使其温暖。
注:注射器的短暂加热将使地下室膜开始凝固,使其更容易注射而不会泄漏。然而,这必须保持简短,如果离开太久,地下室膜将完全凝固,不会注射。使用玻璃注射器可以精确注射低体积。 - 将胰腺放在尾部以将其伸出,然后将针头直接插入胰腺中心,与胰腺本身平行,努力避免可见血管。
注:胰腺中心有大面积,最容易注射。然而,胰腺的头部或尾部也可以特别注射,如果首选。 - 将5μL的基底膜缓慢注入胰腺,并在注射后将针头稳定在胰腺中至少30s,使基底膜凝固并防止渗漏。基底膜应可见,因为小透明气泡将形成;但是,它可能不可见。
注:可注射大体积肿瘤细胞/基底膜;但是,必须测试确切的体积,以确保不会发生泄漏。 - 从胰腺中取出针头,等待确认没有出血。轻轻地将胰腺插入腹腔,注意不要接触地下室膜气泡。
- 将围肠壁拉在一起,执行单缝合线,如果需要,执行两个中断缝合。
- 将皮肤切口的两侧拉在一起,根据需要执行多个中断缝合或插入两个手术夹。
- 再次将丁丙诺啡皮下注射到刮毛中。
- 将小鼠转移到加热的 37°C 保持架内至少 30 分钟,在手术后保持体温,然后再移回新的笼子。
- 在笼子里准备一种混合饮食,以确保补液和体重。
- 建议重新管理术后痛感,并密切注意伤口开口、疼痛或感染和体重减轻的迹象。如果使用手术夹,可以使用夹子去除器在 7-10 天后将其取出。
- 大约14天后,疤痕组织将愈合到足以开始对腹部进行小口。通过触觉密切监测肿瘤大小,直到小鼠到达终点。
- 在终点,小鼠通过宫颈脱位进行剔除,然后斩首。皮肤和围肠腔用剪刀打开,胰腺肿瘤用钳子切除,用钳子抓住肿瘤,用剪刀切除周围组织。
3. 胰腺肿瘤的消化
- 将解剖的胰腺肿瘤、转移位点肿瘤或健康的胰腺组织置于冰冷的PBS中,并储存在冰上。
- 使用钳子将肿瘤转移到培养皿上。
- 将5.0 mL的消化介质(2毫克/mL胶原酶,0.025毫克/mLDNase RPMI)加入50 mL管中;储存在冰上,以防止酶活性开始。
注:此协议使用胶原酶V型,其活性为+1单位/毫克FALGPA和>125胶原蛋白消化单位(CDU)/毫克固体。胶原酶和DNase等分可以储存在-20°C,并在使用前在冰上解冻。当两者都在无菌 RPMI 中完全溶解时,它们可以通过 0.2 μm 过滤器去除污染物。胶原酶在过滤前必须完全溶解,以避免材料损失。 - 采取这个溶液的小等分,以覆盖培养皿上的肿瘤。
- 使用无菌手术刀和钳子将肿瘤切成小块,长度大约小于3毫米。
- 将肿瘤片片刮入管中,轻轻倒置管,直到所有片件都浸入消化介质中。如果其他肿瘤样本需要分批制备,则储存在冰上。
- 在37°C下转移到摇动装置上20分钟。确保所有肿瘤被浸没,不要粘在管的边缘。如果无法晃动,则每 5 分钟涡旋一次样品以帮助消化。
4. 从消化肿瘤中制备单细胞悬浮液
- 在消化步骤之后,立即将管子放在冰上以减缓酶活性。
- 加入EDTA,最终浓度达到20 mM,并短暂涡旋样品混合。这将进一步减缓酶活性。
- 打开管,用新鲜的RPMI培养基冲洗管盖上的任何肿瘤消化。
- 在冰上 50 mL 的开管上准备 70 μm 滤网(滤网的 μm 大小可根据需要改变)。
- 用介质预湿过滤器。
- 重新悬浮消化的细胞,并使用25 mL或更大的条纹清洗管的侧面。条纹的更宽开口对于使厚层易于通过非常重要。
- 使用 25 mL 条纹将所有摘要转移到滤网上。
- 使用 1 mL 注射器柱塞将肿瘤捣碎在过滤器顶部。只直接上下混合,以尽量减少对细胞的剪切应力。
- 使用 RPMI 通过滤网持续清洗细胞。确保用足够的力洗涤,以推动细胞通过。
- 如果仍有要混料,但 RPMI 停止冲洗,则滤网将饱和。因此,将样品转移到新的筛选器中并继续。
注:最终只有细胞外基质分量将留在过滤器中,所有单个细胞都应该通过。
- 在 300 x g和 4 °C 下将管离心 5 分钟。
- 小心地将细胞颗粒重新悬浮在完整的 RPMI 中,然后直接通过另一个过滤器,以去除任何无法充分重新悬浮的细胞外基质或大细胞团块。
- 此时,如果不需要刺激,请立即通过跳到步骤 6.1 来染色分离的细胞,以便进行流式细胞分析。或者,将它们重新悬浮在冷冻介质中(FBS中为10%DMSO),然后储存在-80°C,然后长期储存在液氮中。
注:冷冻步骤可以允许在以后纯化免疫细胞;然而,免疫细胞子集的定量可能需要优化,以确认细胞数和表型不受冻结/解冻过程的影响。前体T细胞刺激最好在新鲜肿瘤样本上进行。此时,样品可以通过基于珠的死细胞去除或免疫细胞富集测定(如果需要)进一步纯化。
5. 为细胞进行外体刺激准备
- 计算细胞在完整介质(RPMI 10 % FBS、1X 青霉素和 1X 链霉素) 中的浓度为 2 x 106/ 100 μL。
注: 镀层细胞总数高,可确保本示例中有足够的 T 细胞进行分析。但是,根据样品可用性和感兴趣的 T 细胞子集的罕见性质,可以向上或缩小该数量。- U 底 96 孔板中 100 μL 的电池板。
- 加入含有2倍PMA/碘霉素制备的完整介质100μL(根据制造商的建议,分别达到最终浓度0.081μM和1.34μM)。
注:如果测量脱粒/外泄,请在此处在介质中加入荧光结合抗小鼠CD107a。还必须执行不包含 CD107a 的控制样本。 - 放入 37 °C 培养箱中,5% CO2可放置 1 小时。
- 在完整介质中分别加入20 μL的10倍制备的布雷芬A和莫嫩辛(分别达到最终浓度1.06μM和2.0μM(根据制造商的建议)。
注:布雷费尔丁A和莫嫩辛是蛋白质运输抑制剂,因此阻止细胞因子细胞外释放等,允许通过流式细胞测定检测。如果通过 ELISA 或类似方法测量细胞因子释放到上清液中, 则可以跳过此步骤。 - 将板放入 37°C 的培养箱中,其中 5% CO2可再放置 4 小时。
6. 流式细胞学的细胞外和细胞内染色
- 拆下板并重新悬挂每个孔,将所有材料转移到放在冰上的 V 底板上。
注:表皮细胞、巨噬细胞和其他附着细胞可能无法通过重新悬浮完全恢复。然而,由于下游分析仅在 T 单元上,因此这不是问题。- 6.1.1 在 300 x g和 4 °C 下将板离心 5 分钟(除非另有说明,否则使用这些条件执行后续步骤)。
- 在一次剧烈运动中将板倒置,取出上清液。
- 在50μL的可修复活力染料中重新悬浮,在冰冷的PBS中制备。重新悬挂时,将移液器设置为较低的音量,以避免出现气泡。
- 在黑暗中,在4°C下孵育20分钟。
- 洗涤步骤:加入100 μL的FACS缓冲液,离心机并去除上清液。
- 在FACS缓冲液(0.5 % BSA,2.0 mM EDTA中,在PBS中)用50μL的抗CD16/CD32(2.5 μg/mL)重新悬浮每口井,以阻止检测抗体与Fc受体的非特异性结合。
- 在黑暗中,在4°C下孵育15分钟。
- 在FACS缓冲液中直接为每个孔添加2x荧光铬结合抗小鼠CD45、CD3、CD4和CD8(可根据需要添加进一步的细胞外标记)
- 在黑暗中,在4°C下孵育30分钟。
- 洗涤步骤:加入100 μL的FACS缓冲液,离心机并去除上清液。
- 加入100 μL的1x细胞内(IC)固定缓冲液,在黑暗中在RT孵育30分钟。
- 在 RT 处准备离心机。
- 加入100 μL的FACS缓冲液,在300 x g和RT下离心5分钟,并去除上清液。在300 x g下用1x渗透缓冲液和离心机重复5分钟;然后删除上清液。
- 加入50μL的1x主混合物的氟铬结合抗小鼠IFN®,TNF®,和其他细胞内标记制备在1x渗透缓冲液。
- 在RT下,在黑暗中孵育1小时。
- 加入100 μL的渗透缓冲液进行洗涤。然后在300 x g和RT下离心5分钟,并去除上清液。
- 加入100 μL的FACS缓冲液清洗,在300 x g和RT下离心5分钟,并去除上清液。
- 在此最终离心后,在与流细胞计兼容的体积中重新悬浮细胞。它可能因 FACS 管的大小而异。
- 将此卷转移到适当的 FACS 管中进行采集。
- 从光盖和存储在冰箱和获取样品在24小时内。
结果
将1000TB32048细胞注射到胰腺后,正交肿瘤大约需要30天才能发展(图1A,B)。手术期间的基底膜渗漏可能导致大肿瘤直接在围膜壁上形成,这些肿瘤在皮肤上可见(图1C)。我们将把这些老鼠从研究中去除。然而,良好的手术技能,泄漏的发生率最小化。在终点收获的正交肿瘤在C57BL/6野生型小鼠中可以长到相当大的大小(图1D)。收获的正交肿瘤需要在胶原酶/DNase中消化20分钟,以实现单细胞悬浮(图2)。此时,肿瘤衍生细胞可在 U 底板中镀在 2 x 106细胞/孔。根据样本中T细胞的患病率,可改变镀层细胞的数量;如果T细胞处于高密度,细胞数量可以降低。控制脾脏或淋巴结样品也可以在此点镀刺激。每口井均用PMA和电霉素刺激5小时,孵育1小时后,加入布雷芬A和莫嫩辛,以阻止细胞因子细胞外释放(图2)。孵育后,样品被染色用于细胞外表位和细胞内细胞因子,以便通过流式细胞学进行分析(图2)。
用流式细胞法对携带正位肿瘤小鼠的脾脏和肿瘤样本进行了分析。脾脏和正交肿瘤流动细胞学分析中使用的浇注策略排除了使用FSC-A、SSC-A、FSC-A/FSC-H和SSC-A/SSC-W的双片碎片,然后死细胞或凋亡细胞为可修复活力染料阳性(图3A)。免疫细胞然后作为CD45+进行封闭,T细胞进一步封闭为CD3+CD4+和CD8+子集定义(图3A)。执行荧光减1(FMO)以确定浇注的背景荧光,仅执行布雷芬A/monensin控制以确定细胞因子的基础生产(图3B-D)。
对于IFN®,用布雷芬A/莫尼辛孵育,在脾脏和肿瘤样本中,在FMO对照下,IFN+没有增加。然而,PMA和电霉素的加入增加了细胞内IFN+在脾和肿瘤衍生CD4和CD8+T细胞中可检测到的百分比。
脾CD4+和CD8+T细胞,用作阳性对照,其IFN® 产量比肿瘤渗透T细胞子集相对较高,平均为6.60± 1.5%和12.97 ± 3.4%,而4.81 ± 1.0 % 和 4.13 ± 1.3%,表明免疫抑制发生在肿瘤内(图3B和4A)。使用TNF®的相同策略,我们设想,与肿瘤渗透CD4+T细胞(22.45 ±5.4%)相比,高比例的脾CD4+T细胞对细胞内TNF®呈阳性(65.93 ± 2.3%)。脾脏和肿瘤渗透CD8+ T细胞产生类似的TNF®水平(分别为25.15 ± 3.7 % 和 19.91 ± 5.1%)(图3C,图4B)。
最后,CD107a是一种内皮标记物,在细胞毒性颗粒和细胞因子的外泄过程中在细胞表面瞬时地表达,因此,它被用作细胞毒性的代理标记。在刺激过程中染色CD107a的好处是,荧光抗体捕获所有瞬态细胞表面表达的CD107a。CD107a的基础水平显示在仅处理的白蛋白A/monensin细胞中。对于脾CD8+ T细胞,用PMA/电霉素刺激增加检测到的CD107a水平,在CD8中最强的上升调节为23.95 ± 3.5% CD107a+, 相比肿瘤渗透 CD8+细胞的 5.8 ± 1.9%, 表明 scellcd8=具有更高的去角率。另一方面,脾脏和肿瘤渗透CD4=表示CD107a 9.37 ± 1.5% 和11.50 ± 1.8% 的可比水平 (图 3D和4C)。
总体而言,这些结果突出表明,将非常低的(1,000)肿瘤细胞注射到胰腺中,可以产生正交肿瘤。这些肿瘤可以迅速消化,以分离T细胞的外体刺激。与继发淋巴器官中的T细胞相比,细胞内细胞因子的检测是可能的,并突出了渗透T细胞的免疫抑制的基础水平。
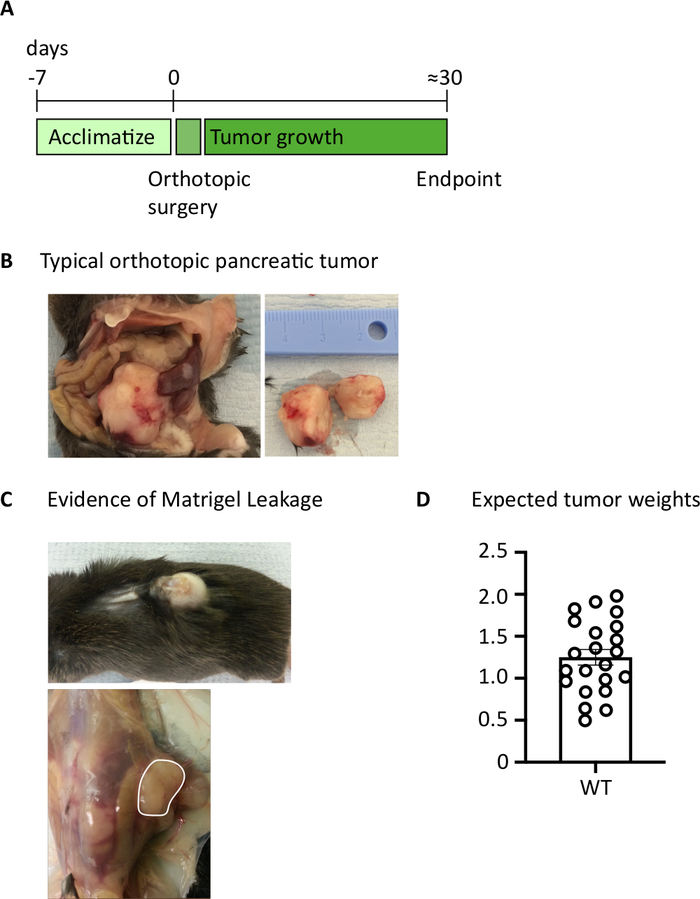
图1:正交胰腺肿瘤的生成。(A)体内实验时间表.(B) 腹腔内(左)和切除后(右)的正交肿瘤的宏观外观,其中显示的肿瘤已切成两半。(C) 手术期间基底膜渗漏的证据可能导致肿瘤发展,这些肿瘤通过皮肤(上部照片)可见,并在围膜壁上形成(下图)。(D) 从达到终点(n=22)的小鼠身上采集的正交胰腺肿瘤重量。每个数据点表示单个鼠标,条形图显示均值 = SEM。此图中的数据已由以前发布的工作10进行了修改。请点击此处查看此图的较大版本。
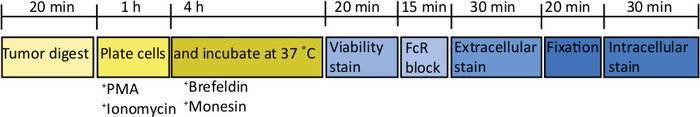
图2:处理外体T细胞刺激的正交肿瘤的原理图。收获后,胰腺肿瘤在胶原酶(2mg/mL)和DNase(0.025mg/mL)中快速消化20分钟,在37°C下。之后,在完全 RPMI 介质中,在 2 x 106/mL 处重新悬浮细胞,并在 U 底板中镀层。将PMA和电霉素的刺激作用加入5小时,此时抗小鼠CD107a抗体也可添加到培养物中。孵育1小时后,加入细胞内运输阻滞剂,布雷费尔丁A和莫嫩辛。在体外刺激后,细胞被转移到V底板中,用可修复的可活性染料染色(在PBS中),20分钟4°C。细胞在FACS缓冲液中洗涤,在抗CD16/32(FcR块)中孵育15分钟(在FACS缓冲液中),然后用额外的细胞荧光结合抗体孵育30分钟(在FACS缓冲液中)。细胞在FACS缓冲液中再次洗涤,并在细胞内固定缓冲液中重新悬浮20分钟。在此之后,在 FACS 缓冲区中洗涤一次,在 1x 渗透缓冲液中洗涤一次。细胞在RT下在细胞内荧光结合抗体中重新悬浮1小时1小时(在1倍渗透缓冲液中)。细胞在1x渗透缓冲液中洗涤一次,在FACS缓冲液中重新悬浮一次,在24小时内在流细胞仪上采集。
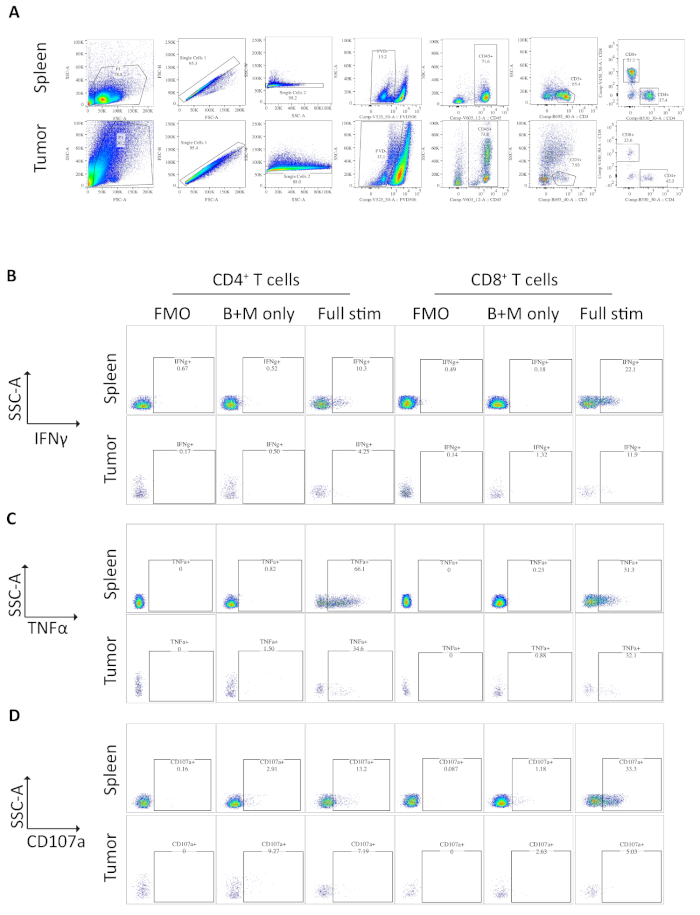
图3:外体刺激脾脏和肿瘤衍生T细胞的流式细胞测定分析。(A) 用于脾脏(阳性对照)和正位肿瘤样本的流式细胞测量门控策略。使用 FSC-A/SSC-A 对碎屑进行区分,使用 FSC-A/FSC-H 和 SSC-A/SSC-W 进一步隔离单个单元。死细胞或凋亡细胞被排除使用可修复的可生存染料-FVD506和免疫细胞被关在CD45+ 。在此 CD3+ T 细胞和 CD4+ CD8+子集定义。数据是在 BD Fortesa 上获取的。(B) 用于量化 IFN++ CD4+和 CD8+ T 细胞的浇注策略。在完全刺激的样品(PMA/电霉素/血亚霉素A/单宁)上使用荧光减1(FMO)控制来确定背景荧光。仅控制白蛋白A/单一蛋白(仅限B+M)用于确定基基细胞因子的产生。然后,使用完全刺激的样本计算 IFN++ T 细胞百分比。(C) 用于量化 TNF++ CD4 + CD8+ T细胞的浇注策略。FMO 控制在完全刺激的样品 (PMA/碘霉素/布雷芬 A/单宁)上,以确定背景荧光。仅控制白蛋白A/单一蛋白(仅限B+M)用于确定基基细胞因子的产生。然后,使用完全刺激的样品计算 TNF++ T 细胞的百分比。(D) 用于定义 CD107a + CD4+ CD8+ T 单元的浇注策略。FMO 控制在完全刺激的样品 (PMA/碘霉素/布雷芬 A/单宁)上,以确定背景荧光。仅控制(仅限 B+M)的布雷芬 A/单一蛋白用于确定基底脱粒。然后,使用完全刺激的样本计算 CD107a+ T 细胞 %。在 FlowJo 版本 10.6.1 上分析了所有流式细胞测定数据。此图中的数据已由以前发布的工作10进行了修改。请点击此处查看此图的较大版本。
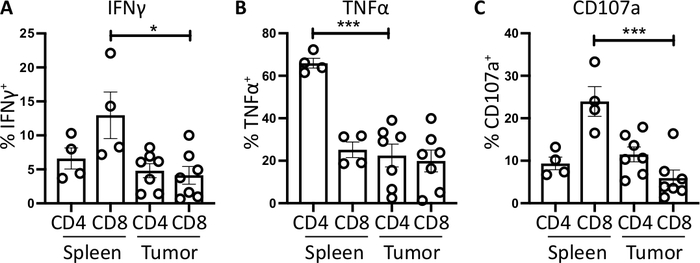
图4:体外脾脏和肿瘤衍生T细胞活性的定量。CD4+和 CD8+ T 细胞对 (A) IFN +( B) TNF +和(C) CD107a+的比例在脾脏 (n_4) 和肿瘤 (n_7) 中用于正交肿瘤携带小鼠。每个数据点表示单个鼠标和误差条显示平均值 = SEM。 统计显著性使用未配对的 t 检验测试进行测试,其中 = p<0.05 和 = p<0.001。所有数据都使用棱镜 8 进行分析。此图中的数据已由以前发布的工作10进行了修改。请点击此处查看此图的较大版本。
讨论
胰腺癌的体内模型提供了宝贵的工具,以了解疾病进展和评估新的治疗目标3。特别是正交模型是一种经济高效和可重复的模型,可同时应用于大群小鼠4,27。正交模型还为肿瘤生长提供了共生微环境和完整的免疫系统,使其比皮下和PDX模型更合适。然而,我们发现,免疫渗透的某些元素可以不同,在正交模型和KPC小鼠,金标准鼠模型10。原因之一可能是在正交模型中看到的肿瘤生长加速。在正射体和皮下模型3,28之间描述了免疫细胞子集密度的进一步差异。因此,虽然转基因KPC模型成本更高,而且可变6,但关键发现应尽可能在一小群KPC小鼠中验证。
肿瘤细胞的制备是手术的关键步骤。细胞应始终处于生长和支原体和无感染的日志阶段。如果对肿瘤细胞生长有任何顾虑,应推迟进行正交手术。使用基底膜可提高注射细胞的肿瘤发病率,而不将其29,减少细胞泄漏,从而围层扩散27。然而,一旦悬浮在基底膜中,肿瘤细胞应迅速注射(2小时内),以避免任何细胞损失。产生肿瘤所需的肿瘤细胞数量可能是细胞系依赖的,应测试一系列细胞数量(例如,从100到100,000之间),这也可能决定到达终点的时间。在准备每只小鼠注射1,000个细胞时,可能会有误差幅度;因此,如果需要多天的手术,组的治疗应均匀地分布在几天内,以控制批次效应。大多数手术步骤可以根据喜好修改;但是,在更换腹腔中的胰腺或关闭腹膜壁时,必须小心不要干扰地下室膜。基底膜渗漏可导致围膜壁上的肿瘤细胞生长,这种生长迅速形成,并可能导致动物更早地牺牲。
理想情况下,胰腺肿瘤应在收获后迅速消化,并立即做好体外刺激的准备。然而,这可能是不可能,如果有一大批肿瘤收获,在这种情况下,肿瘤应保存在冰上,并分批消化。暴露于消化酶的类型、浓度和长度都证明会影响免疫细胞30、31、32的大量表面分子。消化时间也故意短,以限制细胞死亡33。消化细胞可冷冻在冷冻介质中,用于长期储存;然而,解冻时会发生一些细胞损失。如果肿瘤片在胶原酶孵育前没有充分切碎,消化过程可能不太理想,这是显而易见的,因为硬肿瘤片在消化后会留在过滤器中。如果使用健康的胰腺或早期肿瘤,胶原酶浓度可以降低;关于提取健康的胰腺导管细胞的报告使用显著低浓度34。在消化过程中,预计有高度的上皮细胞死亡;然而,免疫细胞应该很好地容忍这个过程。替代方法存在分离有机体生长的活上皮细胞35或保留组织结构36。
根据分析所需的读出和免疫细胞(例如巨噬细胞或B细胞),可以轻松修改刺激方案。使用泛刺激试剂PMA/电霉素不区分TCR抗原特异性,使其在抗原不为人所知时有用。然而,IFN+的生产与TCR参与37密切相关,IFN+和TNF®生产在PDAC抗肿瘤反应38中至关重要。PMA/电霉素刺激反映了T细胞产生细胞因子的最大能力,细胞因子可能或可能不会由肿瘤微环境中的T细胞产生。内源性生产无需刺激即可测量;然而,水平可能低得多或检测不到。有其它方法刺激T细胞:抗CD3/28涂层珠,也不需要抗原或其他免疫细胞群。这种方法的好处是允许通过特定的T细胞子集对细胞因子的产生进行定量,而无需分离方法。细胞毒性的其他标志物(颗粒B和PerforinA),活性(IL-2)或免疫抑制(IL-10)也可以添加21。然而,高质量的流式细胞学抗体无法检测所有细胞因子和感兴趣的因素。因此,如果有其他应用,如ELISA要求刺激可以进行刺激,而不包括布雷芬A/莫宁,允许细胞因子释放到上清液。然而,值得注意的是,这将允许细胞因子总释放,将无法确定哪些细胞群贡献。
IFN® 生产是抗肿瘤 T 细胞反应的主要特征,常用作 TCR 抗原识别的替代品37,38。其他能更精确地定义抗原特异性反应的体内方法利用表达已知抗原的肿瘤细胞,如Ovalbumin或SV40。然后,通用抗原可用于在体内测试T细胞识别,或与TCR限制的宿主小鼠结合使用。或者,如果抗原未知,可以通过批量TCR测序或最近单细胞TCR测序39、40进行T细胞克隆扩张的定量。为了充分理解肿瘤T细胞反应的状态,还应测量指示疲惫或抑制受体的标记物,包括:CTLA-4、PD-1、LAG-3、TIM3、2B4。以及效应器T细胞(CD44 hi,CD62lo)和增殖活性的标记物,Ki67+或CSFE稀释41,42,43,44。总体而言,正交模型提供了一个有用的平台,以快速测试治疗策略,特别是可能调节抗肿瘤T细胞反应,然后可以在较小的转基因组,KPC,小鼠验证。
披露声明
作者没有什么可透露的。
致谢
我们要感谢动物技术员服务和阿尔兹贝塔·塔拉罗维乔娃博士(英国伦敦玛丽女王大学巴特斯癌症研究所)在矫形外科手术期间给予的帮助。我们还要感谢詹妮弗·莫顿博士(英国格拉斯哥比森癌症研究所)在外科技术方面的指导,克里斯蒂娜·吉雷利博士(英国伦敦玛丽女王大学巴特斯癌症研究所)就肿瘤消化问题提出建议,以及法比安·麦克拉纳汉博士(英国伦敦玛丽女王大学巴特斯癌症研究所)就超活性T细胞治疗方案提供的建议。我们还要感谢医学研究委员会(MRC)、胰腺癌研究基金(PCFR)和卵巢癌行动组织为这项研究提供资金。
材料
| Name | Company | Catalog Number | Comments |
| 6/0 gauge coated vicryl absorbable sutures | Ethicon | W9500T | |
| 70 μm pore-size cell strainer | Fisher Scientific | 11597522 | |
| 9 mm Clay Adams clips | VetTech Solutions | IN015A | |
| anti-CD107a PE (clone 1D4B) | Biolegend | 121612 | 1:100 to culture media |
| anti-CD16/CD32 | BD Biosciences | 553142 | Use at final dilution 1:200 |
| anti-CD3 PerCP eFluor710 (clone 17A2) | Biolegend | 46-0032 | Use at final dilution 1:50 |
| anti-CD4 FITC (clone GK1.5) | eBioscience | 11-0041 | Use at final dilution 1:100 |
| anti-CD45 Brilliant Violet 605 (clone 30-F11) | Biolegend | 103140 | Use at final dilution 1:200 |
| anti-CD8 Brilliant Violet 421 (clone 53-6.7) | Biolegend | 100738 | Use at final dilution 1:100 |
| anti-IFN-gamma PE/Cy7 (clone XMG1.2) | Biolegend | 505826 | Use at final dilution 1:50 |
| anti-TNF-alpha Alexa Fluor 647 (clone MP6-X) | Biolegend | 506314 | Use at final dilution 1:50 |
| BD Matrigel Basement Membrane Matrix High Concentration | BD Biosciences | 354248 | Aliquot on ice and store in -20 °C |
| Bovine Serum Albumin (BSA) | Sigma-Aldrich | A4503 | |
| Cell Stimulation Cocktail (500x) (phorbol 12-myristate 13-acetate (PMA) and ionomycin) | eBioscience | 00-4970-03 | 1x Final concentration PMA 0.081 μM, ionomycin 1.34 μM |
| Clay Adams Autoclip Applier | VetTech Solutions | IN015B | |
| Clay Adams Autoclip remover | VetTech Solutions | IN015B | |
| Collagenase Type V from Clostridium histolyticum | Sigma-Aldrich | C9263 | 2 mg/mL in media |
| Dimethyl sulphoxide (DMSO) | Sigma-Aldrich | D2650-100mL | |
| DMEM High glucose (4.5 g/L) with L-Glutamine | PAA | E15-810 | |
| DNase (Deoxyribonuclease I from bovine pancreas Type II-S) stock 10 mg/mL in 0.15 M NaCl | Sigma-Aldrich | D4513 | Final concentration in digestion media 0.025 mg/mL |
| Fixable Viability Dye 506 (FVD506) | eBioscience | 65-0866 | Use at 1:200 in PBS |
| Foetal calf-serum (FCS) | GE Healthcare | A15-104 | 10% in RPMI |
| Hamilton syringe 700 series, 25 μL volume, 22s gauge needle bevel tip | Fisher Scientific | 10100332 | |
| Intracellular Fixation buffer and Intracellular Permeabilisation Buffer | eBioscience | 88-8824-00 | Dilute permeabilisation buffer to 1x in H2O |
| Penicillin/streptomycin | PAA | 15140122 | 100 units/mL Penicillin, 100 μg/mL Streptomycin |
| Protein transport inhibitor cocktail (500x) (brefeldin A and monesin) | eBioscience | 00-4980-03 | 1x Final concentration Brefeldin A 10.6 μM, monensin 2 μM |
| RPMI-1640 (containing 0.3 g/L Glutamine) | Sigma-Aldrich | R8758 | |
| Surgical Scalpel Blade No.10 | Swann-Morton | 0501 | |
| Trypsin-EDTA Solution 10x | Sigma-Aldrich | 594-18C | Trypsin (0.1%) EDTA (0.4%) final concentration |
| U-bottomed 96 microwell plate | VWR | 734-2080 | |
| Universal Cotton Tipped Applicators - 6 inch x 100 | Medisave | UN982 | |
| V-bottomed 96 microwell plate | VWR | 735-0184 |
参考文献
- Siegel, R. L., Miller, K. D., Jemal, A. Cancer statistics. CA: A Cancer Journal for Clinicians. 68 (1), 7-30 (2018).
- Conroy, T., et al. Current standards and new innovative approaches for treatment of pancreatic cancer. European Journal of Cancer. 57, 10-22 (2016).
- Lee, J. W., Komar, C. A., Bengsch, F., Graham, K., Beatty, G. L. Genetically engineered mouse models of pancreatic cancer: The KPC model (LSL-KrasG12D/+;LSL-Trp53R172H/+;Pdx-1-Cre), its variants, and their application in immuno-oncology drug discovery. Current Protocols in Pharmacology. 2016, (2016).
- Tseng, W. W., et al. Development of an Orthotopic Model of Invasive Pancreatic Cancer in an Immunocompetent Murine Host. Clinical Cancer Research. 16 (14), 3684-3695 (2010).
- Majumder, K., et al. A Novel Immunocompetent Mouse Model of Pancreatic Cancer with Robust Stroma: a Valuable Tool for Preclinical Evaluation of New Therapies. Journal of Gastrointestinal Surgery. 20 (1), 53-65 (2016).
- Hingorani, S. R., et al. Trp53R172H and KrasG12D cooperate to promote chromosomal instability and widely metastatic pancreatic ductal adenocarcinoma in mice. Cancer Cell. 7 (5), 469-483 (2005).
- Herreros-Villanueva, M., Hijona, E., Cosme, A., Bujanda, L. Mouse models of pancreatic cancer. World Journal of Gastroenterology. 18 (12), 1286-1294 (2012).
- Witkiewicz, A. K., et al. Integrated Patient-Derived Models Delineate Individualized Therapeutic Vulnerabilities of Pancreatic Cancer. Cell Reports. , (2016).
- Nicolle, R., et al. Pancreatic Adenocarcinoma Therapeutic Targets Revealed by Tumor-Stroma Cross-Talk Analyses in Patient-Derived Xenografts. Cell Reports. , (2017).
- Spear, S., et al. Discrepancies in the Tumor Microenvironment of Spontaneous and Orthotopic Murine Models of Pancreatic Cancer Uncover a New Immunostimulatory Phenotype for B Cells. Frontiers in Immunology. 10, 542 (2019).
- Zhu, Y., et al. CSF1/CSF1R blockade reprograms tumor-infiltrating macrophages and improves response to T-cell checkpoint immunotherapy in pancreatic cancer models. Cancer Research. , (2014).
- Lee, J. J., Huang, J., England, C. G., McNally, L. R., Frieboes, H. B. Predictive Modeling of In vivo Response to Gemcitabine in Pancreatic Cancer. PLoS Computational Biology. , (2013).
- Clark, C. E., et al. Dynamics of the Immune Reaction to Pancreatic Cancer from Inception to Invasion. Cancer Research. 67 (19), 9518-9527 (2007).
- Fukunaga, A., et al. CD8+ tumor-infiltrating lymphocytes together with CD4+ tumor-infiltrating lymphocytes and dendritic cells improve the prognosis of patients with pancreatic adenocarcinoma. Pancreas. 28 (1), 26-31 (2004).
- Tewari, N., et al. The presence of tumor-associated lymphocytes confers a good prognosis in pancreatic ductal adenocarcinoma: an immunohistochemical study of tissue microarrays. BMC Cancer. 13 (1), 436 (2013).
- Royal, R. E., et al. Phase 2 Trial of Single Agent Ipilimumab (Anti-CTLA-4) for Locally Advanced or Metastatic Pancreatic Adenocarcinoma. Journal of Immunotherapy. 33 (8), 828-833 (2010).
- Brahmer, J. R., et al. Safety and Activity of Anti–PD-L1 Antibody in Patients with Advanced Cancer. New England Journal of Medicine. 366 (26), 2455-2465 (2012).
- Winograd, R., et al. Induction of T-cell Immunity Overcomes Complete Resistance to PD-1 and CTLA-4 Blockade and Improves Survival in Pancreatic Carcinoma. Cancer Immunology Research. 3 (4), 399-411 (2015).
- Beatty, G. L., et al. CD40 Agonists Alter Tumor Stroma and Show Efficacy Against Pancreatic Carcinoma in Mice and Humans. Science. 331 (6024), 1612-1616 (2011).
- Lutz, E. R., et al. Immunotherapy converts nonimmunogenic pancreatic tumors into immunogenic foci of immune regulation. Cancer Immunology Research. 2 (7), 616-631 (2014).
- Barry, M., Bleackley, R. C. Cytotoxic T lymphocytes: all roads lead to death. Nature Reviews. Immunology. 2 (6), 401-409 (2002).
- Mojic, M., Takeda, K., Hayakawa, Y. The dark side of IFN-γ: Its role in promoting cancer immunoevasion. International Journal of Molecular Sciences. , (2018).
- Castro, F., Cardoso, A. P., Gonçalves, R. M., Serre, K., Oliveira, M. J. Interferon-gamma at the crossroads of tumor immune surveillance or evasion. Frontiers in Immunology. , (2018).
- Thiery, J., et al. Perforin pores in the endosomal membrane trigger the release of endocytosed granzyme B into the cytosol of target cells. Nature Immunology. , (2011).
- Betts, M. R., et al. Sensitive and viable identification of antigen-specific CD8+ T cells by a flow cytometric assay for degranulation. Journal of Immunological Methods. 281 (1-2), 65-78 (2003).
- Schuerwegh, A. J., De Clerck, L. S., Bridts, C. H., Stevens, W. J. Comparison of intracellular cytokine production with extracellular cytokine levels using two flow cytometric techniques. Cytometry. 55 (1), 52-58 (2003).
- Partecke, L. I., et al. A syngeneic orthotopic murine model of pancreatic adenocarcinoma in the C57/BL6 mouse using the panc02 and 6606PDA cell lines. European Surgical Research. , (2011).
- An, X., et al. Immunophenotyping of Orthotopic Homograft (Syngeneic) of Murine Primary KPC Pancreatic Ductal Adenocarcinoma by Flow Cytometry. Journal of Visualized Experiments. (140), (2018).
- Jiang, Y. J., et al. Establishment of an orthotopic pancreatic cancer mouse model: Cells suspended and injected in Matrigel. World Journal of Gastroenterology. , (2014).
- Autengruber, A., Gereke, M., Hansen, G., Hennig, C., Bruder, D. Impact of enzymatic tissue disintegration on the level of surface molecule expression and immune cell function. European Journal of Microbiology & Immunology. 2 (2), 112-120 (2012).
- Trapecar, M., et al. An Optimized and Validated Method for Isolation and Characterization of Lymphocytes from HIV+ Human Gut Biopsies. AIDS Research and Human Retroviruses. , (2017).
- Liu, Q., et al. Effects of enzymatic digestion, cell culture and preservation conditions on surface CD62L expression of primary murine CD3+CD4+T cells. Biomedical Research (India). 29 (10), 2153-2159 (2018).
- Seaman, S. A., Tannan, S. C., Cao, Y., Peirce, S. M., Lin, K. Y. Differential effects of processing time and duration of collagenase digestion on human and murine fat grafts. Plastic and Reconstructive Surgery. , (2015).
- Huch, M., et al. Unlimited in vitro expansion of adult bi-potent pancreas progenitors through the Lgr5/R-spondin axis. EMBO Journal. , (2013).
- Boj, S. F., et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. , (2015).
- Misra, S., et al. Ex vivo organotypic culture system of precision-cut slices of human pancreatic ductal adenocarcinoma. Scientific Reports. , (2019).
- Moran, A. E., Polesso, F., Weinberg, A. D. Immunotherapy Expands and Maintains the Function of High-Affinity Tumor-Infiltrating CD8 T Cells In Situ. The Journal of Immunology. , (2016).
- Stromnes, I. M., et al. T Cells Engineered against a Native Antigen Can Surmount Immunologic and Physical Barriers to Treat Pancreatic Ductal Adenocarcinoma. Cancer Cell. , (2015).
- Singh, M., et al. High-throughput targeted long-read single cell sequencing reveals the clonal and transcriptional landscape of lymphocytes. Nature Communications. 10 (1), 3120 (2019).
- Jiang, N., Schonnesen, A. A., Ma, K. Y. Opinion Ushering in Integrated T Cell Repertoire Profiling in Cancer. Trends in Cancer. 5, 85-94 (2019).
- Schietinger, A., et al. Tumor-Specific T Cell Dysfunction Is a Dynamic Antigen-Driven Differentiation Program Initiated Early during Tumorigenesis. Immunity. 45 (2), 389-401 (2016).
- Raghav, S. K., et al. Exhaustion of tumor-specific CD8+ T cells in metastases from melanoma patients. Journal of Clinical Investigation. , (2011).
- Gros, A., et al. PD-1 identifies the patient-specific in filtrating human tumors. The Journal of Clinical Investigation. , (2014).
- Miller, B. C., et al. Subsets of exhausted CD8 + T cells differentially mediate tumor control and respond to checkpoint blockade. Nature Immunology. , (2019).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。