使用活细胞STED成像可视化神经元细胞模型中的线粒体内膜超微结构
摘要
该协议提供了培养的SH-SY5Y细胞和原代大鼠海马神经元的繁殖,分化和染色的工作流程,用于使用受激发射耗竭(STED)显微镜进行线粒体超微结构可视化和分析。
摘要
线粒体在细胞中起着许多重要作用,包括能量产生、Ca2+ 稳态的调节、脂质生物合成和活性氧 (ROS) 的产生。这些线粒体介导的过程在神经元中发挥特殊作用,协调有氧代谢以满足这些细胞的高能量需求,调节 Ca2+ 信号传导,为轴突生长和再生提供脂质,并为神经元发育和功能调整 ROS 的产生。因此,线粒体功能障碍是神经退行性疾病的核心驱动因素。线粒体结构和功能是密不可分的。形态复杂的内膜具有称为嵴的结构内褶皱,拥有许多执行线粒体特征过程的分子系统。内膜的结构特征是超微结构,因此太小,无法通过传统的衍射极限分辨显微镜进行可视化。因此,关于线粒体超微结构的大多数见解都来自固定样品的电子显微镜。然而,超分辨率荧光显微镜的新兴技术现在提供低至数十纳米的分辨率,从而可以可视化活细胞中的超微结构特征。因此,超分辨率成像提供了前所未有的能力,可以直接对线粒体结构、纳米级蛋白质分布和嵴动力学的精细细节进行成像,从而提供将线粒体与人类健康和疾病联系起来的基本新见解。该协议介绍了使用受激发射耗竭(STED)超分辨率显微镜来可视化活的人神经母细胞瘤细胞和原代大鼠神经元的线粒体超微结构。该程序分为五个部分:(1) SH-SY5Y 细胞系的生长和分化,(2) 原代大鼠海马神经元的分离、铺板和生长,(3) 用于活 STED 成像的细胞染色程序,(4) 使用 STED 显微镜进行活细胞 STED 实验的程序作为参考,以及 (5) 使用示例进行分割和图像处理的指导,以测量和量化内膜的形态特征。
引言
线粒体是内共生起源的真核细胞器,负责调节几个关键的细胞过程,包括中间代谢和 ATP 产生、离子稳态、脂质生物合成和程序性细胞死亡(细胞凋亡)。这些细胞器拓扑复杂,包含建立多个亚区室的双膜系统1(图1A)。线粒体外膜 (OMM) 与胞质溶胶相互作用并建立直接的细胞器间接触 2,3。线粒体内膜 (IMM) 是一种能量守恒膜,可维持主要以电膜电位 (ΔΨm) 形式存储的离子梯度,以驱动 ATP 合成和其他需要能量的过程 4,5。IMM 进一步细分为紧密贴合 OMM 的内边界膜 (IBM) 和由嵴膜 (CM) 结合的称为嵴的突出结构。该膜从嵴内空间 (ICS) 和膜间空间 (IMS) 描绘了最内层的基质隔室。
线粒体具有基于连续和平衡的裂变和融合过程的动态形态,该过程由动力蛋白超家族6 的机械酶控制。融合允许增加连接和网状网络的形成,而裂变导致线粒体碎片化,并能够通过线粒体自噬去除受损的线粒体7。线粒体形态因组织类型8 和发育阶段9 而异,并受到调节以允许细胞适应包括能量需求10,11 和压力源12 在内的因素。线粒体的标准形态特征,例如网络形成的程度(互连与碎片化)、周长、面积、体积、长度(纵横比)、圆度和分支程度,可以通过标准光学显微镜测量和量化,因为这些特征的大小大于光的衍射极限 (~200 nm)13。
Cristae 结构定义了线粒体的内部结构(图 1B)。嵴形态的多样性可大致分为扁平(层状或盘状)或管状囊泡状14。所有嵴都通过称为嵴结 (CJ) 的管状或槽状结构附着在 IBM 上,这些结构可用于将 IMS 与 ICS 和 IBM 与 CM15 分开。嵴形态受 IMM 的关键蛋白质复合物调控,包括 (1) 位于 CJ 并稳定 IMM-OMM 触点 16 的线粒体接触位点和嵴组织系统 (MICOS),(2) 调节嵴重塑的视萎缩 1 (OPA1) GTP 酶17,18,19,以及 (3) 在嵴尖端 (CT) 形成稳定寡聚体组装体的 F1FO ATP 合酶 20,21.此外,IMM 富含非双层磷脂磷脂酰乙醇胺和心磷脂,可稳定高度弯曲的 IMM22。Cristae 也是动态的,在各种条件下表现出形态变化,例如不同的代谢状态 23,24、不同的呼吸基质 25、饥饿和氧化应激 26,27、细胞凋亡 28,29 和衰老30.最近,研究表明,嵴可以在几秒钟的时间尺度上经历重大的重塑事件,这突显了它们的动态性质31.嵴的几个特征可以量化,包括单个嵴内结构的尺寸(例如,CJ宽度,嵴长度和宽度)以及将单个嵴与其他结构相关的参数(例如,嵴内间距和嵴相对于OMM的入射角)32。这些可量化的嵴参数显示出与功能的直接相关性。例如,线粒体 ATP 产生的程度与嵴的丰度呈正相关,量化为嵴密度或归一化为另一个特征的嵴数(例如,每个 OMM 面积的嵴)33,34,35。由于IMM形态由纳米级特征定义,因此它包括线粒体超微结构,这需要成像技术提供大于光衍射极限的分辨率。如下所述,此类技术包括电子显微镜和超分辨率显微镜(nanoscopy)。
中枢神经系统(CNS)的神经和神经胶质细胞特别依赖线粒体功能。平均而言,大脑仅占总重量的 2%,但利用了 25% 的葡萄糖,占身体耗氧量的 20%,使其容易受到能量代谢的损害36.进行性神经退行性疾病 (ND),包括阿尔茨海默病 (AD)、肌萎缩侧索硬化症 (ALS)、亨廷顿舞蹈症 (HD)、多发性硬化症 (MS) 和帕金森病 (PD),是迄今为止研究最广泛的病理学,研究工作范围从了解这些疾病的分子基础到寻求潜在的治疗预防和干预措施。ND 与氧化应激增加有关,部分源于线粒体电子传递链 (ETC) 37 产生的活性氧 (ROS),以及线粒体钙处理 38 和线粒体脂质代谢39 的改变。这些生理改变伴随着与 AD 40、41、42、43、44、ALS 45,46、HD 47、48,49、MS 50 和 PD51,52,53 相关的线粒体形态缺陷.这些结构和功能缺陷可以通过复杂的因果关系耦合。例如,鉴于嵴形态稳定了 OXPHOS 酶54,线粒体 ROS 不仅由 ETC 产生,而且还会破坏 ETC 所在的基础设施,促进前馈 ROS 循环,从而增强对氧化损伤的敏感性。此外,嵴紊乱已被证明会触发线粒体 DNA (mtDNA) 释放和与自身免疫、代谢和年龄相关疾病相关的炎症通路等过程55。因此,线粒体结构的分析是全面了解ND及其分子基础的关键。
观察嵴的流行方法,包括透射电子显微镜、电子断层扫描和冷冻电子断层扫描 (cryo-ET) 以及 X 射线断层扫描,特别是冷冻软 X 射线断层扫描,已经揭示了重要的发现,并适用于各种样品类型 56、57、58、59、60.尽管最近在更好地观察细胞器超微结构方面取得了进展,但这些方法仍然需要样品固定,因此无法直接捕获嵴的实时动态。超分辨荧光显微镜,特别是结构照明显微镜(SIM)、随机光学重建显微镜(STORM)、光活化定位显微镜(PALM)、膨胀显微镜(ExM)和受激发射耗尽(STED)显微镜等形式,已成为观察结构的流行方法,这些结构需要低于衍射极限的分辨率,这限制了经典的光学显微镜方法。当ExM与另一种超分辨率技术结合使用时,结果令人印象深刻,但样品必须固定并在凝胶61中染色。相比之下,SIM、PALM/STORM 和 STED 都已成功用于活体样品,通常对 IMM 进行染色的新型和有前途的染料为线粒体嵴动力学的实时成像提供了一种新颖而简单的方法 62,63,64,65,66。用于STED成像的活体染料的最新进展改善了染料的亮度和光稳定性,并且这些染料以比其前身更高的特异性靶向IMM。这些发展允许通过超分辨率成像收集长期延时和 z 堆栈实验,为更好地分析线粒体超微结构和动力学的活细胞打开了大门。
本文提供了使用 STED63 用 PKmito Orange (PKMO) 染料染色的未分化和分化的 SH-SY5Y 细胞的活细胞成像方案。SH-SY5Y 细胞系是从亲本细胞系 SK-N-SH 的三个亚克隆衍生物,由转移性神经母细胞瘤67、68、69、70 的骨髓活检产生。该细胞系是ND研究中常用的体外模型,特别是AD、HD和PD等疾病,其中线粒体功能障碍与10,43,71,72,73密切相关。通过操纵培养基将 SH-SY5Y 细胞分化为具有神经元样表型的细胞的能力已被证明是神经科学研究的合适模型,而无需依赖原代神经元细胞10,74。在该方案中,将视黄酸(RA)加入细胞培养基中以诱导SH-SY5Y细胞的分化。RA 是一种维生素 A 衍生物,已被证明可以调节细胞周期并促进调节神经元分化的转录因子的表达75。还提供了从大鼠海马中分离的神经元的培养和活细胞成像的方案。海马体已被证明受到线粒体变性的影响,并与皮层一起在衰老和ND 76,77,78,79,80中起重要作用。
研究方案
1. SH-SY5Y细胞的增殖和分化
- 制备用于细胞生长和维持的培养基
- 制备完整的高葡萄糖 Dulbecco 改良 Eagle 培养基(DMEM,4.5 g/L D-葡萄糖、4 mM L-谷氨酰胺、110 mg/L 丙酮酸钠),补充有最终的 1% (v/v) 抗生素-抗真菌药(10,000 单位/mL 青霉素、10,000 μg/mL 链霉素和 25 μg/mL 两性霉素 B)和不同量的胎牛血清 (FBS)(参见 材料表)。分化培养基中的FBS含量在最终的10%、5%或2%(v/v)FBS之间变化。
- 细胞维护
- 将细胞维持在补充有10%(v / v)FBS的DMEM中,并将它们置于37°C和5%CO2中,然后接种在含有5%(v / v)FBS的DMEM中进行分化。将冷冻细胞储备液储存在含有 10% (v/v) 二甲基亚砜 (DMSO) 的 FBS 中,浓度为 1-2 x 107 个细胞 /mL。
- 视黄酸(RA)的制备
- 将 7.51 mg 全反式 RA(参见材料表)溶解在 5 mL 新鲜制备的 95% 乙醇中,以获得 5 mM 储备溶液。使用从制造商协议81的产品信息表中获得的350nm处的吸光度(ɛ = 44,300M-1cm-1)处的浓度验证浓度,使用在乙醇中以5μM稀释储备溶液。将5 mM原液储存在4°C避光保存长达6周。
- 用于盖玻片包衣的聚-D-赖氨酸的制备
注:聚-D-赖氨酸 (PDL) 产品方案位于供应商网站82 的“文档和下载”部分下,提供了有关包被各种培养容器的信息。- 该协议包括基于2孔腔室容器的体积,每孔面积为4cm2 ,无菌#1.5硼硅酸盐盖玻片底部(参见 材料表)。用Dulbecco's PBS(DPBS;不含钙,不含镁)将PDL储备溶液稀释两倍至50μg/ mL。
注意: #1.5 或 #1.5H 盖玻片都是可接受的厚度,这对图像质量至关重要。其他厚度会引起球差,应避免。
- 该协议包括基于2孔腔室容器的体积,每孔面积为4cm2 ,无菌#1.5硼硅酸盐盖玻片底部(参见 材料表)。用Dulbecco's PBS(DPBS;不含钙,不含镁)将PDL储备溶液稀释两倍至50μg/ mL。
- PDL盖玻片涂层
注意:盖玻片可以在生物安全柜中暴露在紫外线 (UV) 下 10-15 分钟以进行进一步灭菌。- 将 1.2 mL 的 50 μg/mL PDL 溶液应用于细胞培养柜中无菌腔室盖玻片的每个孔中,并在室温下孵育 1 小时。取出PDL溶液,用3.6 mL蒸馏水冲洗三次。完成最终洗涤后,让涂层室在空气中干燥2小时,然后冲洗并立即使用或与4°C的密封容器一起储存长达2周。
注意:彻底冲洗盖玻片,因为过量的PDL可能对细胞有毒。
- 将 1.2 mL 的 50 μg/mL PDL 溶液应用于细胞培养柜中无菌腔室盖玻片的每个孔中,并在室温下孵育 1 小时。取出PDL溶液,用3.6 mL蒸馏水冲洗三次。完成最终洗涤后,让涂层室在空气中干燥2小时,然后冲洗并立即使用或与4°C的密封容器一起储存长达2周。
- SH-SY5Y细胞与RA的分化
注意:不要使用第 15 次以上的单元格。细胞以80%-90%的汇合度传代。鉴别程序不同,但遵循相似的步骤。通过用脑源性神经营养因子(BDNF)68,83,84,85进一步治疗,获得从神经母细胞瘤到成熟神经元的额外分化,但未在该方案中进行。
可选:在盖玻片上接种之前建立细胞至少 24 小时。为了从冷冻储备液中制备细胞,快速解冻 1 mL 冷冻细胞小瓶,并加入补充有 10% FBS 的 9 mL 预热培养基中,然后以 350 x g 旋转 10 分钟(在室温下)并弃去上清液以除去 DMSO。将细胞沉淀重悬于 5 mL 预热培养基中,并将细胞接种在 T-25 烧瓶中。一旦细胞达到 80%-90% 汇合度,通过计数和接种进行传代,以便在适用时进行分化。- 第 0 天:接种细胞。
- 将细胞从冷冻原液或工作烧瓶接种到有腔的盖玻片上。使用接种密度为 1.5 x 104 个细胞/cm2。
注:培养面积为 4 cm 2 的标准2 孔盖玻片中的单孔需要 6.0 x 104 个细胞。未分化的细胞应接种补充有 10% (v/v) FBS 的 DMEM,将要分化的细胞应接种补充有 5% (v/v) FBS 的 DMEM。
- 将细胞从冷冻原液或工作烧瓶接种到有腔的盖玻片上。使用接种密度为 1.5 x 104 个细胞/cm2。
- 第 1 天:开始 RA 分化治疗。
- 制备补充有 5% (v/v) FBS、1% (v/v) 抗生素 - 抗真菌剂和终浓度为 10 μM RA 或相同添加剂体积的乙醇的 DMEM,作为该分化过程的载体对照。取出用于播种的腔室盖玻片中的培养基,用1x PBS冲洗,并将新的DMEM添加到孔中。
- 第 3 天:用新鲜的 RA 或含乙醇的培养基替换培养基。
- 从第 1 天取出培养基,并用补充有 2% (v/v) FBS、1% (v/v) 抗生素 - 抗真菌剂和相同添加剂体积的 10 μM RA 或 95% 乙醇的新鲜培养基代替,作为该分化过程的载体对照。取出用于播种的腔室盖玻片中的培养基,用1x PBS冲洗,然后向孔中加入新培养基。
- 第 6 天:对细胞进行成像。
注:细胞分化时间因方案而异,但暴露于 RA 六天足以诱导 SH-SY5Y 细胞中的神经元样表型86。- 执行实时成像,详情见第 3 节和第 4 节(图 2)。
- 第 0 天:接种细胞。
2.原代大鼠海马神经元培养
- 大鼠海马神经元分离的材料制备。
- 准备新鲜补充的DMEM。
- 对补充有 10% (v/v) 热灭活 FBS、1% (v/v) 丙酮酸钠溶液和 1% (v/v) 青霉素-链霉素 (10,000 U/mL) 的 DMEM(高葡萄糖,无丙酮酸钠)的混合物进行过滤灭菌。在4°C下储存长达2周。
- 准备新鲜补充的神经元生长培养基。
- 过滤灭菌补充有 2% (v/v) B27 补充剂、0.25% (v/v) 谷氨酰胺补充剂和 1% (v/v) 青霉素 - 链霉素的神经元生长培养基混合物(参见 材料表)。在4°C下储存长达2周。
- 准备新鲜补充的DMEM。
- 准备原代海马神经元培养物。
- 按照先前发表的工作87 和制造商网站上的产品方案制备原代海马神经元培养物,从中获得解剖的E18大鼠海马体88 (参见 材料表)。该协议导致大多数神经元群体具有 <2% 的星形胶质细胞。
注意:运输此组织的冬眠培养基将用于本协议的后续步骤。不要丢弃它。 - 准备用于组织解离的材料和培养基。
- 点燃巴斯德移液器以减小孔径,并将其存放在箔纸中以防止使用前污染。将制备的DMEM,1X Hank缓冲盐溶液(HBSS)和神经元生长培养基预热至37°C。 用无菌镊子将 2 片 DNA 酶加入 15 mL 锥形管中。
- 进行组织解离。
- 在将组织放入含有DNAase的15mL锥形管中并在37°C下短暂孵育之前,尽可能多地去除解剖的E18大鼠海马体储存的冬眠培养基。 加入 900 μL 1X HBSS,然后加入 100 μL 0.5% 胰蛋白酶。将组织在37°C孵育15分钟。
注意:PDL涂层板可以从储存中取出并放置在培养箱中,直到在此培养时间内使用。
- 在将组织放入含有DNAase的15mL锥形管中并在37°C下短暂孵育之前,尽可能多地去除解剖的E18大鼠海马体储存的冬眠培养基。 加入 900 μL 1X HBSS,然后加入 100 μL 0.5% 胰蛋白酶。将组织在37°C孵育15分钟。
- 进行组织匀浆和细胞计数。
- 与胰蛋白酶孵育后,除去培养基,将上一步预热的冬眠培养基-DNAase加入组织中,并用巴斯德移液管匀浆。介质看起来不透明,然后随着均质化的继续而逐渐清晰。
- 将解离的神经元加入到装有 4 mL 预热 DMEM 的新管中,然后使用细胞计数器对细胞进行计数。
- 进行原代细胞的细胞铺板和生长。
- 在DMEM中以约1.65×104 个细胞/cm2 的密度铺板细胞。对于 2 孔腔盖玻片 (4 cm 2),每孔接种 65,000 – 70,000 个细胞,加入2 mL DMEM。在检查粘附性之前,将细胞在37°C和5%CO 2下孵育2 小时。一旦细胞开始粘附,取出 1 mL 培养基并用相同体积的冬眠培养基代替,然后轻轻搅拌混合。混合培养基后,重复此过程并去除一半的培养基,并用相同体积的神经元生长培养基替换,然后轻轻混合。
注:接种日被认为是 体外 日(DIV)0,细胞准备在DIV 7处成像(图2)。
- 在DMEM中以约1.65×104 个细胞/cm2 的密度铺板细胞。对于 2 孔腔盖玻片 (4 cm 2),每孔接种 65,000 – 70,000 个细胞,加入2 mL DMEM。在检查粘附性之前,将细胞在37°C和5%CO 2下孵育2 小时。一旦细胞开始粘附,取出 1 mL 培养基并用相同体积的冬眠培养基代替,然后轻轻搅拌混合。混合培养基后,重复此过程并去除一半的培养基,并用相同体积的神经元生长培养基替换,然后轻轻混合。
- 按照先前发表的工作87 和制造商网站上的产品方案制备原代海马神经元培养物,从中获得解剖的E18大鼠海马体88 (参见 材料表)。该协议导致大多数神经元群体具有 <2% 的星形胶质细胞。
3. 活细胞成像的细胞制备
注:细胞类型和来源(即培养细胞和原代细胞)的染色要求可能不同;详见已发布的报告62,63.
- PKmito橙的制备
注:据报道,通常对 IMM 进行染色的其他染料为64,65,66,并且是市售的。PKMO是该协议中唯一使用的。- 按照制造商的说明将粉末 PKMO(见材料表)重悬于DMSO中89。从细胞中吸出培养基,并在预热的无酚红培养基中洗涤。在预热的、无酚红的DMEM中制备PKMO储备液,补充有2%(v / v)FBS或10%(v / v),具体取决于分化状态,HEPES至终浓度为20mM和1%(v / v)抗生素 - 抗真菌剂,然后按照制造商的说明对细胞进行染色。该配方不含PKMO,是活细胞成像介质。
- 用PKMO进行细胞染色
- 将细胞与染料在37°C和5%CO2 下孵育30分钟。用活细胞成像培养基洗涤细胞三次,并在37°C,5%CO2下孵育30分钟。
- 加入新鲜的预热活细胞成像培养基。细胞现在可以进行成像了。
注意:急性治疗(例如,药物和/或应激源)在使用时,在实时成像之前添加;请参阅“讨论”部分和 补充图 1。
4. 通过STED显微镜对活细胞进行成像
注意:该协议使用围绕倒置显微镜构建的STED系统,该系统在 材料表中指定。该系统配备了脉冲激发激光器(561 nm激光器,标称功率~300 μW)和脉冲775 nm STED耗尽激光器(标称功率1.2 W),连续可调的振镜扫描仪和基于615/20 nm滤光片的雪崩光电二极管探测器(APD)。这里使用用于 STED 的 100x/1.40 油浸镜头。Lightbox 软件用于图像采集。提供的所有详细信息都与此软件和系统设置直接相关。
- 影像学检查的一般指南和步骤
- 使用载物台顶部培养箱或环境室来保持细胞活力,但短期室温实验也是可以接受的。这些步骤特定于上述 STED 设置。
- 选择用于成像的激光器和滤光片组。
- 通过从染料列表中选择染色中使用的染料或光谱特性与所用染料最接近的染料,使用橙色 染料的参数。通过双击或将它们拖动到样品列表中来激活它们,其中显示“在此处拖动染料”。
- 选择要成像的区域。
- 在概述中,通过选择矩形 ROI 按钮 并单击并拖动来塑造感兴趣区域 (ROI),在感兴趣的线粒体周围创建感兴趣区域 (ROI)。可以使用将鼠标悬停在角落上时出现的 ROI 角 或 弯曲边缘 来调整 ROI 的大小和旋转。
注:建议的成像参数摘要见 表1。使用先前报道的该STED设置和染料组合63的参数对这些参数进行经验调整。
- 在概述中,通过选择矩形 ROI 按钮 并单击并拖动来塑造感兴趣区域 (ROI),在感兴趣的线粒体周围创建感兴趣区域 (ROI)。可以使用将鼠标悬停在角落上时出现的 ROI 角 或 弯曲边缘 来调整 ROI 的大小和旋转。
- 设置门控。
- 在 “常规 ”菜单旁边,选择“ 门控 ”菜单,或单击并按住以将菜单添加到视图中。建议将STED检测器门控调整为1-1.05至7.8-7.85 ns,如下所示。门控时间可以变化,短至 1-1.05 至 7-7.05 ns。
- 根据样品适当调整强度。
注:通常,用于STED的激发功率是共聚焦使用的功率的2-3倍,因此需要5%激发激光功率进行共聚焦的样品在STED采集过程中可以使用10%-15%的激发激光功率。- 将STED的激发激光设置为15%-20%,将STED耗尽激光设置为20%-25%,并有10条线累积。使用4 μs的像素停留时间,像素尺寸为20-25 nm。培养细胞的针孔保持在 1.0 AU,原代大鼠海马细胞的针孔保持在 0.7 AU,以改善更密集的线粒体中的光学切片。
注意:共聚焦和STED图像都可以采集以进行并排比较(图3A,B,图4A),或者只能采集STED。
- 将STED的激发激光设置为15%-20%,将STED耗尽激光设置为20%-25%,并有10条线累积。使用4 μs的像素停留时间,像素尺寸为20-25 nm。培养细胞的针孔保持在 1.0 AU,原代大鼠海马细胞的针孔保持在 0.7 AU,以改善更密集的线粒体中的光学切片。
- 有关时间序列/z 系列的其他信息
- 选择时间序列。
- 选择时间下拉菜单。定义延时摄影所需的迭代次数(此处使用的 5 次)和时间间隔(此处使用的 25 或 30 秒)(图 3C、D、图 4B)。
注意:如果间隔短于采集时间,则迭代将继续进行,没有任何延迟。在进行延时摄影时,强烈建议使用完美的对焦单元或类似的对焦跟踪,以避免潜在的漂移。
- 选择时间下拉菜单。定义延时摄影所需的迭代次数(此处使用的 5 次)和时间间隔(此处使用的 25 或 30 秒)(图 3C、D、图 4B)。
- 设置音量范围。
- 通过启用 Volume 选项并调整范围的两端,根据需要设置 z 体积范围。该协议用于2D成像的步长为150-200nm。关于原始STED反卷积所需的奈奎斯特采样的推荐步长可以使用在线工具90计算。
注意:STED耗尽激光功率和成像的平面数量会将染料光漂白和细胞的光暴露增加到有害水平。采集后检查是否有光毒性和光损伤的迹象。
- 通过启用 Volume 选项并调整范围的两端,根据需要设置 z 体积范围。该协议用于2D成像的步长为150-200nm。关于原始STED反卷积所需的奈奎斯特采样的推荐步长可以使用在线工具90计算。
- 选择时间序列。
5. 线粒体超微结构的加工和分析工具
注意:图像处理(即反卷积)是可选的,但通常用于制作和分析 STED 图像以供发布。强烈建议进行反卷积以提高对比度和减少噪声,以优化单个嵴的分割,如下所述(图 2)。
- STED 图像反卷积
注:本协议中用于反卷积的软件在 材料表中提供。- 设置图像的微观参数。
注意:确保在图像 显微参数中正确输入显微镜元数据。这包括安装介质的折射率;浸泡介质;像素大小;激发波长、发射波长和耗尽波长;以及任何其他相关信息。可以保存具有这些参数的模板以供重复使用。 - 使用软件算法对原始 STED 图像进行去卷积。
- 通过访问反卷积软件中的自动反卷积算法,可以进行不干涉的反卷积图像处理。选择“快速”按钮,并将反卷积类型设置为“快速”、“标准”、“主动”或“保守”,以获得不同程度的反卷积能力。显示了使用具有激进设置的快速反卷积的代表性图像(图 3、图 4 和图 5)。
- 将反卷积软件中的图像保存为 ICS2 格式。
- 对于手动反卷积,请执行以下步骤。
- 简而言之,在执行手动反卷积时,请保存反卷积向导模板以保持一致性,并可以选择在启动向导时加载模板。使用测量点扩散函数 (PSF) 信息(如果通过采集设置和参数生成)。
- 如果需要,在让反卷积软件自动稳定图像之前,先裁剪原始 STED 图像。反卷积软件包的附加组件允许对可能的成像伪影进行特定补偿,例如热漂移和色差。
- 接下来,生成一个对数直方图以手动或自动执行背景减法。选择经典的最大似然估计 (CMLE) 反卷积算法。
注意:对于反卷积,要调整的关键值是信噪比阈值、迭代次数和质量阈值。可以调整这些值,并且可以预览反卷积以确定最佳设置。
- 设置图像的微观参数。
- 分割和颗粒分析
注意:该协议使用 FIJI(Is Just ImageJ),一种开源软件(请参阅 材料清单),进行分割和分析。其他类似的软件,包括 CellProfiler、Icy、Ilastik 和 QuPath,也可用于这些目的。- 准备用于分割的图像。
- 通过转到 “文件”→“打开 ”或单击并将文件拖动到 ImageJ 工具栏,从反卷积软件中打开 .obf 原始 STED 图像或 .ics2 文件。从这里开始,可以在分割之前执行任何使图像更容易分割的处理。
- 要保持一致更改,请使用 插件 → 宏 →录制 功能,并将关键命令复制并粘贴到新宏中,从 插件 →新建 →宏。确保在运行宏之前选择要处理的映像。
注意:通常可接受的大小和形状定量更改包括裁剪、投影 z 堆栈和禁用平滑的背景减法。更改应在数据集内的图像之间一致地执行并报告。
- 调整可训练的 Weka 分段设置
注:使用半自动分割工具和线粒体下游分析的分步说明的更多详细信息已发布91。- 在可训练的 Weka Segmentation (TWS)92 插件中打开去卷积的 STED 图像,该插件位于 Plugins → Segmentation → Trainable Weka Segmentation 下。在分割 设置中,选择 高斯模糊、 膜投影和 Sobel 滤波器 要素。膜厚度默认值为 1,膜贴片大小默认值为 19。
- 将 1 类或 2 类标记为“Cristae”,将另一个标记为“背景”(图 2)。也可以使用 “保存分类器 ”按钮保存模型。选择 “加载分类器 ”以将这些设置重用于其他图像。
- 执行TWS类跟踪。
- 使用线条工具或其他形状突出显示一些嵴或背景。至少一些背景选择应该在嵴之间包括空格。在结构上画一条线以分配给任一类,然后选择右侧的“ 添加到 ”按钮作为嵴或背景。双击跟踪以从该标签中删除结构。
- 进行TWS分类训练。
- 选择左侧的“训练分类器”按钮,根据提供给插件的信息生成映射。可以使用“切换叠加”按钮打开和关闭分段类的叠加,并且可以在“设置”中调整叠加的不透明度。可以使用其他标签重新训练分类器。满意后,选择“获取概率”按钮。
- 测量颗粒。
- 使用嵴概率图,对图像设置阈值以生成蒙版,然后转到“分析”→“分析 粒子”。通常,可以使用默认阈值类型并调整范围以确保考虑整个嵴。通过分析颗粒提供的测量值可以通过分析→设置测量值进行调整。
注:尺寸和形状参数的示例,例如嵴的面积、周长、圆度和纵横比,是根据选定的测量值测量和显示的(图2, 图5A, 补充表1)。 - 可选:选择与反卷积图像具有相同尺寸的原始 STED 图像,并从管理器中应用 ROI,然后在 ROI 管理器中选择 测量 以获取强度值。
- 使用嵴概率图,对图像设置阈值以生成蒙版,然后转到“分析”→“分析 粒子”。通常,可以使用默认阈值类型并调整范围以确保考虑整个嵴。通过分析颗粒提供的测量值可以通过分析→设置测量值进行调整。
- 获取折线图。
- 从去卷积的STED图像生成线图。绘制一条多点线,将线条粗细调整到几个像素宽以平均噪声,然后将线样条以适合线粒体(图2, 图5B)。生成的线图用于测量峰峰值距离,以报告一定范围内嵴的周期性和分布。
注:与此相关的是,嵴密度可以报告为通过测量线粒体外部确定的给定区域内独立嵴的数量。线粒体面积可以通过对去卷积或原始 STED 图像应用过滤器来生成掩模来确定。在测量该区域之前,确保面罩准确贴合线粒体的轮廓。
- 从去卷积的STED图像生成线图。绘制一条多点线,将线条粗细调整到几个像素宽以平均噪声,然后将线样条以适合线粒体(图2, 图5B)。生成的线图用于测量峰峰值距离,以报告一定范围内嵴的周期性和分布。
- 准备用于分割的图像。
代表性结果
该协议描述了培养细胞和原代细胞的细胞生长条件,重点是活细胞STED成像和线粒体嵴的后续分析。使用ImageJ对未分化的SH-SY5Y(图3A)和RA分化的SH-SY5Y(图3B)细胞的线粒体进行的投影可以收集为具有传统共聚焦和STED的z-stacks,然后可以对原始STED图像进行反卷积。也可以进行延时成像,然后进行去卷积(图3C,D)。使用原代大鼠海马神经元的成像参数略有不同(表1),共聚焦和原始STED图像可以作为z堆栈获得,并且可以对原始STED图像进行反卷积(图4A)。也可以对原代神经元的线粒体进行延时成像(图4B)。一般来说,延时图像应该能够显示线粒体动态事件。
当用于分割的样本的原始 STED 和解卷积 STED z 堆栈投影看起来一致时,将执行定量测量。TWS插件使用去卷积的STED图像进行分割以制作概率掩码,然后用于创建嵴的二进制掩码以获得尺寸和形状参数(图5A)。此模板中的区域保存在 ROI 管理器中,如果需要,可以应用于原始 STED 图像以测量相对强度的差异。去卷积的STED投影也可用于确定给定区域的嵴周期性和密度(图5B)。
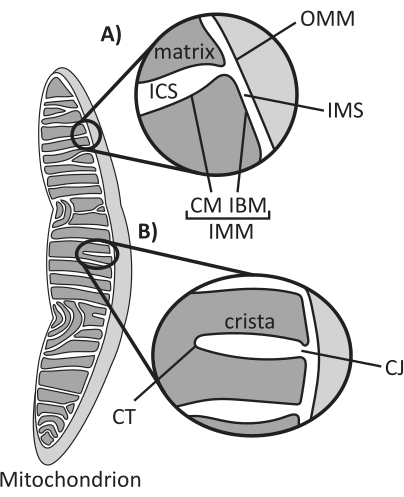
图1:线粒体形态。 线粒体有一个定义不同亚区室 (A) 的双膜系统。Cristae 是具有明确特征的内膜的内褶 (B)。缩写:OMM,线粒体外膜;ICS,嵴内间隙;IMS,膜间空间;CM, 嵴膜;IBM,内边界膜;IMM,线粒体内膜;CT,嵴尖;CJ, 嵴交界处。 请点击这里查看此图的较大版本.
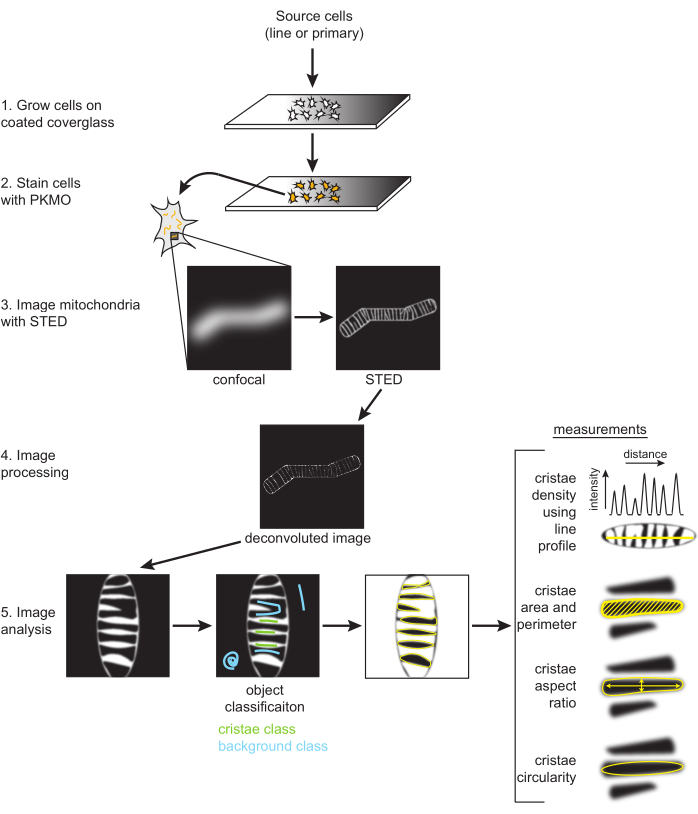
图 2:工作流程示意图。 SH-SY5Y细胞或原代大鼠海马神经元在PDL涂层的盖玻片上生长。SH-SY5Y细胞平行生长,在六天内保持未分化或RA分化。从海马切片中分离出 7 天后,在 PDL 涂层的盖玻片上生长原代大鼠海马神经元。一旦准备好成像,用PKMO染色细胞并用STED成像。然后对原始STED图像进行反卷积处理,并在FIJI中处理解卷积图像,以获得尺寸和形状测量值,例如嵴密度、面积、周长、圆度和纵横比。 请点击这里查看此图的较大版本.
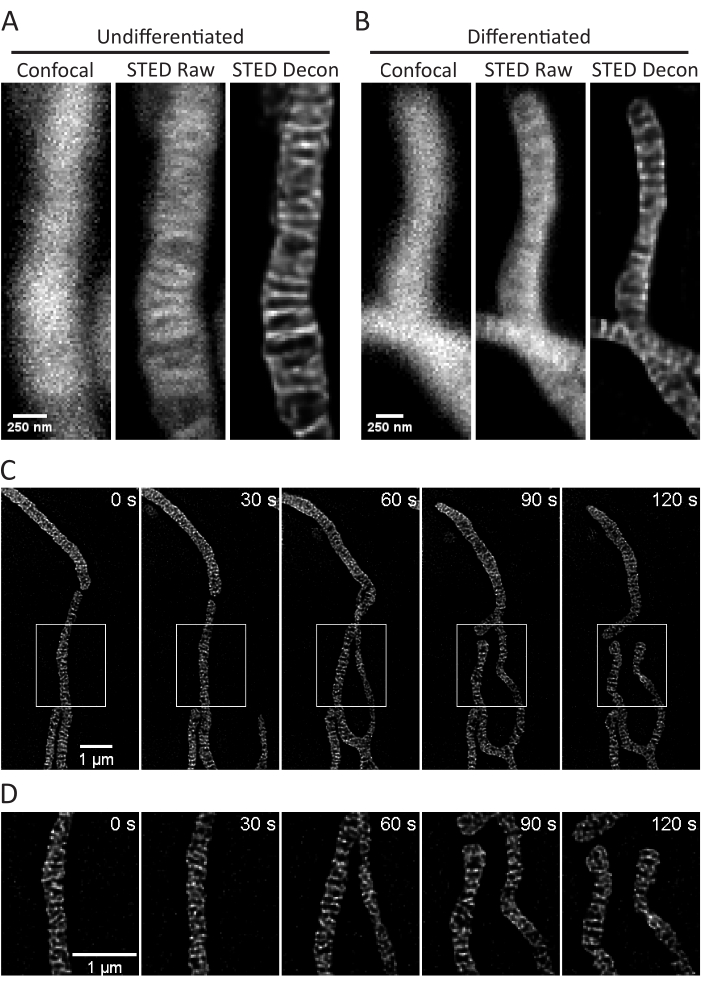
图 3:SH-SY5Y 细胞中线粒体的成像。 显示了具有PKMO染色的非分化(A)和RA分化(B)SH-SY5Y细胞的线粒体的代表性共聚焦(左)、原始STED(中)和惠更斯去卷积STED图像z堆栈投影(右)。显示了 RA 分化的 SH-SY5Y 细胞的 30 秒间隔和 5 次迭代的延时摄影 (C),其中选定的区域(白框)在 (D) 上使用这些区域的缩放图像进行扩展,而无需插值。比例尺: A,B,250 nm; C,D, 1 μm. 请点击这里查看此图的较大版本.
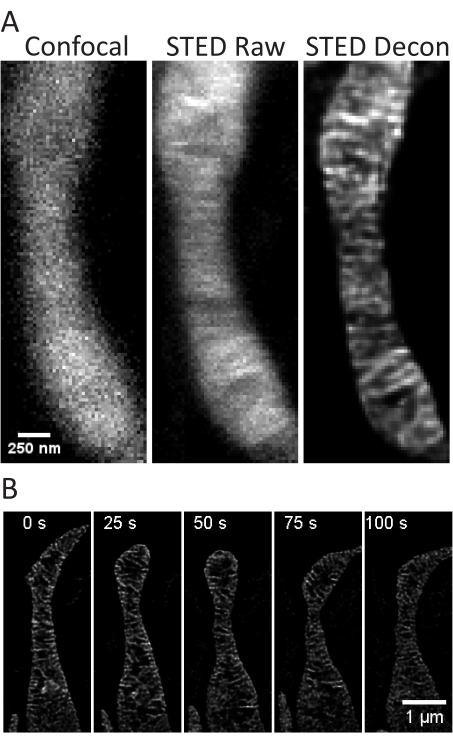
图 4:原代大鼠海马神经元中线粒体的成像。 显示了来自原代大鼠海马神经元的线粒体的代表性共聚焦(左)、原始 STED(中)和惠更斯去卷积 STED(右)图像 z 堆栈投影 (A)。显示了这些神经元中线粒体间隔 25 秒和 5 次迭代的延时 (B)。比例尺: A,250 nm; B, 1 μm. 请点击这里查看此图的较大版本.
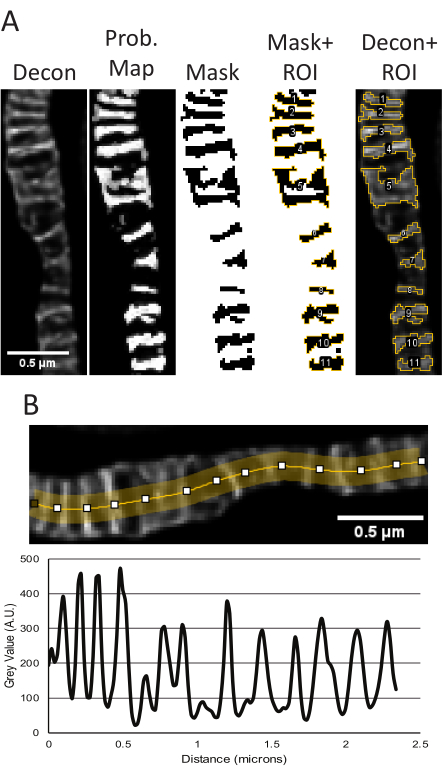
图 5:在 ImageJ 中处理去卷积的 STED 图像。 显示了 Trainable Weka Segmentation 插件测量嵴大小和形状的代表性用法 (A)。从左到右,显示了以下图像:去卷积的STED图像,基于TWS插件分割的概率图,使用概率图作为输入的FIJI阈值掩码,带有ROI轮廓的掩码,以及覆盖在原始去卷积STED图像上的ROI。与这些物体相对应的面积、周长、圆度和纵横比测量值可在 补充表1中找到。图中显示了使用去卷积STED图像测量峰峰值距离的线图,作为嵴密度的读数(B)。比例尺:0.5 μm。 请点击这里查看此图的较大版本.
| 像素尺寸 (nm) | 停留时间 (μs) | 线路符合 | STED 采集期间的 561 nm 激发 (%) | 775 nm STED 耗尽功率 (%) | 步长 (nm) | 针孔 (AU) | 延时摄影间隔(秒) | 延时迭代 | |
| 无差分 SH-SY5Y | 20 | 4 | 10 | 15 | 20 | 200 | 1.0 | 30 | 5 |
| RA-Differe-ntiated SH-SY5Y | 20-25 | 4 | 10-12 | 15 | 20-22 | 150-200 | 1.0 | 30 | 5 |
| 原代神经元 | 20-25 | 4 | 10 | 10 | 25 | 200 | 0.7 | 30 | 5 |
| 注意:像素大小可能因成像要求和对图像进行反卷积的意图而异。反卷积需要适当的采样。没有反卷积的原始 STED 图像的像素大小可以达到 30 nm。 | |||||||||
表 1:STED 采集参数摘要。 显示用于每种细胞类型、未分化 SH-SY5Y、RA 分化的 SH-SY5Y 和原代大鼠海马神经元的 2D STED 成像的设置。对于所有延时摄影,根据 ROI 大小以不同的间隔进行了 5 次迭代。
补充图1:添加淀粉样蛋白-β(Aβ)的SH-SY5Y细胞成像。 显示了具有PKMO染色(顶部)和Aβ-HiLyte647(底部)的RA分化的SH-SY5Y细胞的代表性共聚焦(左)、原始STED(中)和去卷积STED(右)图像(A)。显示了原始 PKMO STED(绿色)与原始 Aβ STED(品红色)(B)或去卷积 PKMO STED(绿色)与去卷积 Aβ STED(品红色)(C) 的合并 z 堆栈投影。比例尺:0.5μm。 请点击这里下载此文件。
补充表1:分段嵴的大小和形状测量。 显示了面积 (μm2)、周长 (μm)、圆度和纵横比的大小和形状测量值,对应于 图 5A 中从分段线粒体中概述的物体。 请点击这里下载此文件。
补充表2:淀粉样蛋白β样品的采集参数摘要。 显示用于未分化和RA分化的SH-SY5Y细胞中PKMO和Aβ-HiLyte647的2D STED成像的设置。Aβ-HiLyte647 的共聚焦可以单独使用,因为没有特定的结构可以解析;此处显示了较小粒径的 Aβ-HiLyte647 的 STED 图像。 请点击这里下载此文件。
补充文件 1:淀粉样蛋白β治疗方案。请点击这里下载此文件。
讨论
该协议介绍了使用人神经母细胞瘤细胞系SH-SY5Y和原代大鼠海马神经元与新型IMM靶向PKMO染料进行活细胞STED成像。由于PKMO的新颖性,目前很少有使用这种染料进行STED活体成像的出版物。使用这些细胞类型进行STED成像带来了挑战,特别是因为神经元细胞的线粒体较窄。该协议的一个局限性是使用的PKMO染料,因为它可能对细胞有毒。不同的细胞和细胞系对染料的反应不同,因此可能需要调整染料浓度和孵育时间,以在不伤害细胞的情况下优化强信号的结果。建议的解决方案是降低浓度并增加染色时间63;然而,这可能会导致染色较差,而不会增加细胞活力。
与PKMO类似,商业染料Live Orange mito(材料表)也表现出一些细胞毒性。该染料用于多种培养细胞,但无法在 RA 分化的 SH-SY5Y 细胞中成功表现出与未分化对应物相同的参数(我们未发表的观察结果)。然而,可以针对该探针和所选细胞类型优化合适的染色方案。使用这种染料时,检测器设门时间为1-1.05至7-7.05 ns, 表1 中的所有其他参数保持不变。通常,用 200-250 nM 活橙线粒体染色细胞 45 分钟可产生与 PKMO 结果相当的结果。较短时间的较高浓度染色或相同时间或稍长的较低浓度染色会产生不同的结果,并且可能有利于其他细胞类型或生长条件。
由于轴突和树突投射的性质以及成像时的线粒体分布,原代大鼠海马神经元成像与永生化细胞不同。协议这一部分的一个困难是,接种密度决定了原代培养物是否能够粘附和健康生长,并且在更高的密度下,投影往往会过度生长 DIV 10。因此,从这些原代神经元成像的线粒体可能来自细胞体,而不是投射;然而,从较低的起始细胞密度成功生长会在后期生长时产生更好的成像结果。关键是要确保低背景和失焦光,以便为STED提供最佳对比度。为了解决对细胞群的担忧,在补充 B27 的神经元生长培养基中培养原代海马细胞可防止神经胶质细胞的生长,并且来源报告说 <5% 的细胞是星形胶质细胞,并且生长培养基中缺乏 NbActiv1 补充剂可将培养物中的星形胶质细胞数量减少到 <2%87。对于培养的SH-SY5Y细胞和原代大鼠海马神经元,用于生长的PDL涂层会导致图像中的背景雾度。使用(表1)中报告的设置可以实现足够的信噪比,并且反卷积消除了观察到的大部分背景。
除了这里介绍的成像外,还可以在成像之前或期间对细胞进行治疗或施加压力。例如,添加叔丁基过氧化氢 (tBHP) 会诱导氧化应激,并且可以监测添加后线粒体随时间的变化。添加带有荧光标签的淀粉样蛋白-β (Aβ) 可以监测该肽与线粒体的关系以及线粒体结构随时间变化的分布。线粒体健康与AD密切相关,并被广泛支持在Aβ毒性中发挥作用43,71,72。值得注意的是,SH-SY5Y 细胞的分化状态会影响 Aβ 蛋白前体 (AβPP) 定位85,应仔细构建使用 AβPP 的实验。
作为如何调整该方案的一个例子,显示荧光变体Aβ(1-42)-HiLyte 647可以在成像前15分钟添加到PKMO染色的细胞中(补充图1)。成像参数相似(补充表2),主要区别在于对较窄的线粒体进行成像时需要更小的针孔。使用 STED 对 Aβ-HiLyte647 进行成像需要较少的总激发 (6%-8%) 和 STED 耗尽 (10%-12%) 激光功率和较少的累积 (6)。检测器门控也从 0.1 ns 扩展到 10 ns。虽然不需要Aβ的STED分辨率,但原始STED的整体信噪比和Aβ粒径优于共聚焦图像,也可以进行后续的反卷积。当与PKMO染色的原始STED或去卷积STED图像合并时,收集STED图像和Aβ的原始STED z堆栈投影似乎特别有用(补充图1B,C)。两个通道都是在单帧步长中收集的。在应力处理或其他添加后,可以获得与 图 2 中列出的类似和 图 5 中所示的瞬态定位的测量值(如适用)和嵴架构差异。
此处未报道但已被其他人报道的线粒体活细胞 STED 中双标记的其他可能方法包括使用 SNAP 标记蛋白93、Halo 标记蛋白,以及使用具有通用靶标的其他细胞渗透性染料,例如 mtDNA63。值得注意的是,SNAP 和 Halo 标记的标记策略会影响成像时产生的荧光信号强度和寿命94。此外,虽然该协议提供了可应用于分割线粒体的几个分析示例,但软件包可以对这些图像执行许多其他分析。
披露声明
作者没有什么可透露的。
致谢
原代大鼠海马神经元由康涅狄格大学(美国康涅狄格州斯托尔斯)生物医学工程系的George Lykotrafitis博士和Shiju Gu提供。Abberior STED仪器位于开放研究资源和设备中心的先进光学显微镜设施中,由NIH资助S10OD023618授予Christopher O'Connell。这项研究由美国国立卫生研究院资助R01AG065879授予Nathan N. Alder。
材料
| Name | Company | Catalog Number | Comments |
| 0.05% Trypsin-EDTA | Gibco | 25300054 | |
| 0.4% Trypan blue | Invitrogen | T10282 | |
| 0.5% Trypsin-EDTA, no phenol red | Gibco | 15400054 | |
| 100 X antibiotic-antimycotic | Gibco | 15240062 | |
| 100 X/1.40 UPlanSApo oil immersion lens | Olympus | Equipped in Olympus IX83 microscope for STED setup described in Section 4 | |
| All-trans-retinoic acid | Sigma | R2625 | |
| Amyloid-β (1-42, HiLyte Fluor647, 0.1 mg) | AnaSpec | AS-64161 | Other fluorescent conjugates available |
| B27 supplement (50 X), serum free | Gibco | 17504044 | |
| Cell Counter (Countess II FL) | Life Technologies | AMQAF1000 | |
| Centrifuge | Eppendorf | 5804-R | |
| Counter slides | Invitrogen | C10283 | |
| Conical tubes (15 mL) | Thermo Fisher Scientific | 339650 | |
| Cuvettes (Quartz Cells) | Starna Cells, Inc. | 9-Q-10 | Used with Spectrometer as described in Section 1.3 |
| DMEM (high glucose with sodium pyruvate) | Gibco | 11995073 | Used for SH-SY5Y cell materials as described in Section 1 |
| DMEM (high glucose no sodium pyruvate) | Gibco | 11965092 | Used for primary cell materials as described in Section 2 |
| DMEM (phenol red-free) | Gibco | 31053028 | Used for imaging as described in Section 3 |
| DMSO | Sigma | D8418 | |
| DNAase I from bovine pancreas | Sigma | DN25 | Used for primary cell materials as described in Section 2.2.1 and 2.2.2 |
| DPBS (no calcium, no magnesium) | Gibco | 14190144 | |
| E18 Rat Hippocampus | Transnetyx Tissue | SDEHP | |
| Ethanol (200 proof) | Fisher Bioreagents | BP28184 | |
| Fetal bovine serum (FBS), not heat-inactivated | Gibco | 26140079 | For cultured cells, in Section 1 |
| Fetal bovine serum (heat inactivated) | Gibco | 10082147 | For primary cell culture, Section 2 |
| Filter sterilization unit (0.1 µm, 500 mL) | Thermo Fisher Scientific | 5660010 | |
| FIJI (Is Just ImageJ) and Trainable Weka Segmentation (TWS) plug-in | -- | -- | Free, open-source image analysis software that includes plug-ins including Trainable Weka Segmentation described in Section 5; TWS plug-in from ref. 90 of the main text |
| GlutaMAX supplement (100 X) | Gibco | 35050061 | Glutamine supplement used for primary cell materials described in Section 2.1.2 |
| Hausser Scientific bright-Line and Hy-Lite Counting Chambers | Hausser Scientific | 267110 | |
| HBSS (no calcium, no magnesium) | Gibco | 14170120 | Used for primary cell materials described in Section 2.2.1 and 2.2.2 |
| HEPES | Gibco | 15630080 | |
| Huygens Professional deconvolution software (V. 20.10) | Scientific Volume Imaging (SVI) | -- | The deconvolution software used in this protocol and described in Section 5 |
| IX83 inverted microscope with Continuous Autofocus | Olympus | -- | This paper uses a STED Infinity Line system built around an Olympus IX83 inverted microscope, described in Section 4 |
| Lightbox software (V. 16.3.16118) | Abberior | -- | Vendor software used for STED image acquisition, described in Section 4 |
| Live Orange Mito dye | Abberior | LVORANGE-0146-30NMOL | Live cell imaging IMM-targeting dye described in Discussion |
| Neurobasal media | Gibco | 21103049 | Used for primary cell materials referred to in Section 2.1.2 |
| Nunc Lab-Tek II 2-well chambered coverglass | Nunc | 155379 | Can purchase a variety of chambers but make sure the coverglass is #1.5 |
| Pasteur Pipets (Fisherbrand) | Thermo Fisher Scientific | 22183632 | |
| Penicillin-Streptomycin (10,000 U/mL) | Gibco | 15140122 | |
| PKmito Orange dye | Spirochrome | SC053 | |
| Poly-D-lysine | Gibco | A3890401 | |
| SH-SY5Y Cell line | ATCC | CRL2266 | |
| Sodium pyruvate (100 mM) | Gibco | 11360070 | Used for primary cell materials described in Section 2 |
| Spectrometer (GENESYS 180 UV-Vis) | Thermo Fisher Scientific | 840309000 | |
| STED Expert Line microscope | Abberior | -- | STED setup can be customized, but at time of purchase instrument was considered Abberior’s Expert Line; brief description of setup is available in Section 4 of protocol |
| T25 flask (TC-treated, filter cap) | Thermo Fisher Scientific | 156367 | Other culture vessels and sizes available |
参考文献
- Iovine, J. C., Claypool, S. M., Alder, N. N. Mitochondrial compartmentalization: emerging themes in structure and function. Trends in Biochemical Sciences. 46 (11), 902-917 (2021).
- Gupta, A., Becker, T. Mechanisms and pathways of mitochondrial outer membrane protein biogenesis. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1862 (1), 148323 (2021).
- Gordaliza-Alaguero, I., Cantó, C., Zorzano, A. Metabolic implications of organelle-mitochondria communication. EMBO Reports. 20 (9), e47928 (2019).
- Klecker, T., Westermann, B. Pathways shaping the mitochondrial inner membrane. Open Biology. 11 (12), 210238 (2021).
- Navarro, A., Boveris, A. The mitochondrial energy transduction system and the aging process. American Journal of Physiology-Cell Physiology. 292 (2), C670-C686 (2007).
- Yu, R., Lendahl, U., Nistér, M., Zhao, J. Regulation of mammalian mitochondrial dynamics: opportunities and challenges. Frontiers in Endocrinology. 11, 374 (2020).
- Horn, A., Raavicharla, S., Shah, S., Cox, D., Jaiswal, J. K. Mitochondrial fragmentation enables localized signaling required for cell repair. The Journal of Cell Biology. 219 (5), e201909154 (2020).
- Glancy, B., Kim, Y., Katti, P., Willingham, T. B. The functional impact of mitochondrial structure across subcellular scales. Frontiers in Physiology. 11, 541040 (2020).
- Bahat, A., et al. MTCH2-mediated mitochondrial fusion drives exit from naïve pluripotency in embryonic stem cells. Nature Communications. 9 (1), 5132 (2018).
- Detmer, S. A., Chan, D. C. Functions and dysfunctions of mitochondrial dynamics. Nature Reviews Molecular Cell Biology. 8, 870-879 (2007).
- Bertholet, A. M., et al. Mitochondrial fusion/fission dynamics in neurodegeneration and neuronal plasticity. Neurobiology of Disease. 90, 3-19 (2016).
- Zemirli, N., Morel, E., Molino, D. Mitochondrial dynamics in basal and stressful conditions. International Journal of Molecular Sciences. 19 (2), 564 (2018).
- Harwig, M. C., et al. Methods for imaging mammalian mitochondrial morphology: a prospective on mitograph. Analytical Biochemistry. 552, 81-99 (2018).
- Pánek, T., Eliáš, M., Vancová, M., Lukeš, J., Hashimi, H. Returning to the fold for lessons in mitochondrial crista diversity and evolution. Current Biology. 30 (10), R575-R588 (2020).
- Gottschalk, B., Madreiter-Sokolowski, C. T., Graier, W. F. Cristae junction as a fundamental switchboard for mitochondrial ion signaling and bioenergetics. Cell Calcium. 101, 102517 (2022).
- Khosravi, S., Harner, M. E. The MICOS complex, a structural element of mitochondria with versatile functions. Biological Chemistry. 401 (6-7), 765-778 (2020).
- Frezza, C., et al. OPA1 controls apoptotic cristae remodeling independently from mitochondrial fusion. Cell. 126 (1), 177-189 (2006).
- Meeusen, S., et al. Mitochondrial inner-membrane fusion and crista maintenance requires the dynamin-related GTPase Mgm1. Cell. 127 (2), 383-395 (2006).
- Patten, D. A., et al. OPA1-dependent cristae modulation is essential for cellular adaptation to metabolic demand. The EMBO Journal. 33 (22), 2676-2691 (2014).
- Paumard, P., et al. The ATP synthase is involved in generating mitochondrial cristae morphology. The EMBO Journal. 21 (3), 221-230 (2002).
- Strauss, M., Hofhaus, G., Schröder, R. R., Kühlbrandt, W. Dimer ribbons of ATP synthase shape the inner mitochondrial membrane. The EMBO Journal. 27 (7), 1154-1160 (2008).
- Basu Ball, W., Neff, J. K., Gohil, V. M. The role of nonbilayer phospholipids in mitochondrial structure and function. FEBS Letters. 592 (8), 1273-1290 (2018).
- Hackenbrock, C. R. Ultrastructural bases for metabolically linked mechanical activity in mitochondria. I. Reversible ultrastructural changes with change in metabolic steady state in isolated liver mitochondria. The Journal of Cell Biology. 30 (2), 269-297 (1966).
- Dlasková, A., et al. Mitochondrial cristae narrowing upon higher 2-oxoglutarate load. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1860 (8), 659-678 (2019).
- Pérez-Hernández, C. A., et al. Mitochondrial ultrastructure and activity are differentially regulated by glycolysis-, krebs cycle-, and microbiota-derived metabolites in monocytes. Biology. 11 (8), 1132 (2022).
- Mannella, C. A. Structural diversity of mitochondria: functional implications. Annals of the New York Academy of Sciences. 1147, 171-179 (2008).
- Plecitá-Hlavatá, L., Ježek, P. Integration of superoxide formation and cristae morphology for mitochondrial redox signaling. The International Journal of Biochemistry & Cell Biology. 80, 31-50 (2016).
- Scorrano, L., et al. A distinct pathway remodels mitochondrial cristae and mobilizes cytochrome c during apoptosis. Developmental Cell. 2 (1), 55-67 (2002).
- Heath-Engel, H. M., Shore, G. C. Mitochondrial membrane dynamics, cristae remodelling and apoptosis. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1763 (5-6), 549-560 (2006).
- Brandt, T., et al. Changes of mitochondrial ultrastructure and function during ageing in mice and Drosophilia. eLife. 6, e24662 (2017).
- Kondadi, A. K., et al. Cristae undergo continuous cycles of membrane remodelling in a MICOS-dependent manner. EMBO Reports. 21, e49776 (2020).
- Quintana-Cabrera, R., Mehrotra, A., Rigoni, G., Soriano, M. E. Who and how in the regulation of mitochondrial cristae shape and function. Biochemical and Biophysical Research Communications. 500 (1), 94-101 (2018).
- Nielsen, J., et al. Plasticity in mitochondrial cristae density allows metabolic capacity modulation in human skeletal muscle: Enlarged mitochondrial cristae density in athletes. The Journal of Physiology. 595 (9), 2839-2847 (2017).
- Afzal, N., Lederer, W. J., Jafri, M. S., Mannella, C. A. Effect of crista morphology on mitochondrial ATP output: A computational study. Current Research in Physiology. 4, 163-176 (2021).
- Heine, K. B., Parry, H. A., Hood, W. R. How does density of the inner mitochondrial membrane influence mitochondrial performance. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 324 (2), R242-R248 (2023).
- Wang, W., Zhao, F., Ma, X., Perry, G., Zhu, X. Mitochondria dysfunction in the pathogenesis of Alzheimer's disease: recent advances. Molecular Neurodegeneration. 15, 30 (2020).
- Singh, A., Kukreti, R., Saso, L., Kukreti, S. Oxidative stress: a key modulator in neurodegenerative diseases. Molecules. 24, 1583 (2019).
- Pchitskaya, E., Popugaeva, E., Bezprozvanny, I. Calcium signaling and molecular mechanisms underlying neurodegenerative diseases. Cell Calcium. 70, 87-94 (2018).
- Estes, R. E., Lin, B., Khera, A., Davis, M. Y. Lipid metabolism influence on neurodegenerative disease progression: is the vehicle as important as the cargo. Frontiers in Molecular Neuroscience. 14, 788695 (2021).
- Calkins, M. J., Manczak, M., Mao, P., Shirendeb, U., Reddy, P. H. Impaired mitochondrial biogenesis, defective axonal transport of mitochondria, abnormal mitochondrial dynamics and synaptic degeneration in a mouse model of Alzheimer's disease. Human Molecular Genetics. 20 (23), 4515-4529 (2011).
- Petersen, C. A. H., et al. The amyloid beta-peptide is imported into mitochondria via the TOM import machinery and localized to mitochondrial cristae. Proceedings of the National Academy of Sciences of the United States of America. 105 (35), 13145-13150 (2008).
- Gan, X., et al. Inhibition of ERK-DLP1 signaling and mitochondrial division alleviates mitochondrial dysfunction in Alzheimer's disease cybrid cell. Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1842 (2), 220-231 (2014).
- Baloyannis, S. J., Costa, V., Michmizos, D. Mitochondrial alterations Alzheimer's disease. American Journal of Alzheimer's Disease & Other Dementias. 19 (2), 89-93 (2004).
- Tillement, L., Lecanu, L., Papadopoulos, V. Alzheimer's disease: Effects of β-amyloid on mitochondria. Mitochondrion. 11 (1), 13-21 (2011).
- Choi, S. Y., et al. C9ORF72-ALS/FTD-associated poly(GR) binds Atp5a1 and compromises mitochondrial function in vivo. Nature Neuroscience. 22 (6), 851-862 (2019).
- Smith, E. F., Shaw, P. J., De Vos, K. J. The role of mitochondria in amyotrophic lateral sclerosis. Neuroscience Letters. 710, 132933 (2019).
- Costa, V., et al. Mitochondrial fission and cristae disruption increase the response of cell models of Huntington's disease to apoptotic stimuli. EMBO Molecular Medicine. 2 (12), 490-503 (2010).
- Costa, V., Scorrano, L. Shaping the role of mitochondria in the pathogenesis of Huntington's disease: Mitochondrial and Huntington's disease. The EMBO Journal. 31 (8), 1853-1864 (2012).
- Vanisova, M., et al. Mitochondrial organization and structure are compromised in fibroblasts from patients with Huntington's disease. Ultrastructural Pathology. 46 (5), 462-475 (2022).
- de Barcelos, I. P., Troxell, R. M., Graves, J. S. Mitochondrial dysfunction and multiple sclerosis. Biology. 8 (2), 37 (2019).
- Park, J., et al. Mitochondrial dysfunction in Drosophila PINK1 mutants is complemented by parkin. Nature. 441, 1157-1161 (2006).
- Meng, H., et al. Loss of Parkinson's disease-associated protein CHCHD2 affects mitochondrial crista structure and destabilizes cytochrome c. Nature Communications. 8, 15500 (2017).
- Lu, L., et al. CHCHD2 maintains mitochondrial contact site and cristae organizing system stability and protects against mitochondrial dysfunction in an experimental model of Parkinson's disease. Chinese Medical Journal. 135 (13), 1588-1596 (2022).
- Cogliati, S., et al. Mitochondrial Cristae shape determines respiratory chain supercomplexes assembly and respiratory efficiency. Cell. 155 (1), 160-171 (2013).
- He, B., et al. Mitochondrial cristae architecture protects against mtDNA release and inflammation. Cell Reports. 41 (10), 111774 (2022).
- Polo, C. C., et al. Three-dimensional imaging of mitochondrial cristae complexity using cryo-soft X-ray tomography. Scientific Reports. 10, 21045 (2020).
- Rybka, V., et al. Transmission electron microscopy study of mitochondria in aging brain synapses. Antioxidants. 8 (6), 171 (2019).
- Mannella, C. A. Structure and dynamics of the mitochondrial inner membrane cristae. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1763 (5-6), 542-548 (2006).
- Fry, M. Y., et al. In situ architecture of Opa1-dependent mitochondrial cristae remodeling. biorxiv. , (2023).
- Barad, B. A., Medina, M., Fuentes, D., Wiseman, R. L., Grotjahn, D. A. Quantifying organellar ultrastructure in cryo-electron tomography using a surface morphometrics pipeline. The Journal of Cell Biology. 222 (4), 202204093 (2023).
- Kunz, T. C., Götz, R., Gao, S., Sauer, M., Kozjak-Pavlovic, V. Using expansion microscopy to visualize and characterize the morphology of mitochondrial cristae. Frontiers in Cell and Developmental Biology. 8, 617 (2020).
- Yang, Z., et al. Cyclooctatetraene-conjugated cyanine mitochondrial probes minimize phototoxicity in fluorescence and nanoscopic imaging. Chemical Science. 11 (32), 8506-8516 (2020).
- Liu, T., et al. Multi-color live-cell STED nanoscopy of mitochondria with a gentle inner membrane stain. Proceedings of the National Academy of Sciences. 119 (52), e2215799119 (2022).
- Yang, X., et al. Mitochondrial dynamics quantitatively revealed by STED nanoscopy with an enhanced squaraine variant probe. Nature Communications. 11, 3699 (2020).
- Zheng, S., et al. Long-term, super-resolution HIDE imaging of the inner mitochondrial membrane in live cells with a cell-permeant lipid probe. biorxiv. , (2022).
- Wang, C., et al. A photostable fluorescent marker for the superresolution live imaging of the dynamic structure of the mitochondrial cristae. Proceedings of the National Academy of Sciences of the United States of America. 116 (32), 15817-15822 (2019).
- Feles, S., et al. Streamlining culture conditions for the neuroblastoma cell line sh-sy5y: a prerequisite for functional studies. Methods and Protocols. 5 (4), 58 (2022).
- Shipley, M. M., Mangold, C. A., Szpara, M. L. Differentiation of the SH-SY5Y human neuroblastoma cell line. Journal of Visualized Experiments. (108), e53193 (2016).
- Kovalevich, J., Langford, D., Amini, S., White, M. K. Considerations for the use of SH-SY5Y neuroblastoma cells in neurobiology. Neuronal Cell Culture. 1078, 9-21 (2013).
- Biedler, J. L., Helson, L., Spengler, B. A. Morphology and growth, tumorigenicity, and cytogenetics of human neuroblastoma cells in continuous culture. Cancer Research. 33 (11), 2643-2652 (1973).
- Swerdlow, R. H. Mitochondria and mitochondrial cascades in alzheimer's disease. Journal of Alzheimer's Disease. 62 (3), 1403-1416 (2018).
- Wang, W., Zhao, F., Ma, X., Perry, G., Zhu, X. Mitochondria dysfunction in the pathogenesis of Alzheimer's disease: recent advances. Molecular Neurodegeneration. 15, 30 (2020).
- Reddy, P. H. Mitochondrial dysfunction in aging and alzheimer's disease: strategies to protect neurons. Antioxidants & Redox Signaling. 9 (10), 1647-1658 (2007).
- Horn, A., Raavicharla, S., Shah, S., Cox, D., Jaiswal, J. K. Mitochondrial fragmentation enables localized signaling required for cell repair. Journal of Cell Biology. 219 (5), e201909154 (2020).
- Korecka, J. A., et al. Phenotypic characterization of retinoic acid differentiated SH-SY5Y cells by transcriptional profiling. PLoS ONE. 8 (5), e63862 (2013).
- Baghel, M. S., Thakur, M. K. Vdac1 downregulation causes mitochondrial disintegration leading to hippocampal neurodegeneration in scopolamine-induced amnesic mice. Molecular Neurobiology. 56 (3), 1707-1718 (2019).
- Jiang, S., et al. Mfn2 ablation causes an oxidative stress response and eventual neuronal death in the hippocampus and cortex. Molecular Neurodegeneration. 13 (1), 5 (2018).
- Mu, Y., Gage, F. H. Adult hippocampal neurogenesis and its role in Alzheimer's disease. Molecular Neurodegeneration. 6, 85 (2011).
- Rao, Y. L., et al. Hippocampus and its involvement in Alzheimer's disease: a review. 3 Biotech. 12 (2), 55 (2022).
- Weerasinghe-Mudiyanselage, P. D. E., Ang, M. J., Kang, S., Kim, J. -. S., Moon, C. Structural Plasticity of the hippocampus in neurodegenerative diseases. International Journal of Molecular Sciences. 23 (6), 3349 (2022).
- . Poly-D-Lysine Available from: https://www.thermofisher.com/order/catalog/product/A3890401 (2023)
- Dravid, A., Raos, B., Svirskis, D., O'Carroll, S. J. Optimised techniques for high-throughput screening of differentiated SH-SY5Y cells and application for neurite outgrowth assays. Scientific Reports. 11, 23935 (2021).
- Hromadkova, L., et al. Brain-derived neurotrophic factor (BDNF) promotes molecular polarization and differentiation of immature neuroblastoma cells into definitive neurons. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1867 (9), 118737 (2020).
- Riegerová, P., et al. Expression and Localization of AβPP in SH-SY5Y cells depends on differentiation state. Journal of Alzheimer's Disease. 82 (2), 485-491 (2021).
- Hoffmann, L. F., et al. Neural regeneration research model to be explored: SH-SY5Y human neuroblastoma cells. Neural Regeneration Research. 18 (6), 1265-1266 (2022).
- Abiraman, K., Tzingounis, A. V., Lykotrafitis, G. K. Ca 2 channel localization and regulation in the axon initial segment. The FASEB Journal. 32 (4), 1794-1805 (2018).
- E18 Rat Hippocampus. Transnetyx Tissue Available from: https://tissue.transnetyx.com/E18-Rat-Hippocampus_4 (2023)
- Kmito ORANGE - Probe for live cell imaging of mitochondria. Spirochrome Available from: https://spirochrome.com/product/pkmito_orange/ (2023)
- Nyquist Calculator. Scientific Volume Imaging Available from: https://svi.nl/Nyquist-Calculator (2023)
- Segawa, M., et al. Quantification of cristae architecture reveals time-dependent characteristics of individual mitochondria. Life Science Alliance. 3 (7), e2019000620 (2020).
- Arganda-Carreras, I., et al. Trainable Weka Segmentation: a machine learning tool for microscopy pixel classification. Bioinformatics. 33 (15), 2424-2426 (2017).
- Stephan, T., Roesch, A., Riedel, D., Jakobs, S. Live-cell STED nanoscopy of mitochondrial cristae. Scientific Reports. 9, 12419 (2019).
- Erdmann, R. S., et al. Labeling strategies matter for super-resolution microscopy: A comparison between HaloTags and SNAP-tags. Cell Chemical Biology. 26 (4), 584-592 (2019).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。