在体外使用 邻 苯二甲醛在培养的哺乳动物细胞中快速定量氧化和还原形式的谷胱甘肽
摘要
通过使用 邻苯二甲醛 (OPA) 实现了氧化型和还原型谷胱甘肽(分别为 GSSG 和 GSH)的定量。OPA一旦与GSH偶联,就会变得高度荧光,但在还原之前无法与GSSG偶联。在这里,我们描述了一种多参数测定法,以使用蛋白质定量进行归一化来量化两者。
摘要
谷胱甘肽长期以来一直被认为是确定细胞抗氧化反应的关键生物标志物。因此,它是活性氧研究的主要标志物。该方法利用 邻苯二甲醛 (OPA) 来量化谷胱甘肽的细胞浓度。OPA通过巯基结合与还原型谷胱甘肽(GSH)偶联,随后形成异吲哚,产生高荧光偶联物。为了获得氧化谷胱甘肽(GSSG)和GSH的准确结果,需要在本协议中实施的掩蔽剂和还原剂的组合。治疗也可能影响细胞活力。因此,在这种多参数测定中提出了通过蛋白质测定的归一化。该测定表明,对 GSH 具有特异性的伪线性检测范围为 0.234 - 30μM (R2=0.9932±0.007 (N=12))。所提出的测定方法还允许通过添加掩蔽剂N-乙基马来酰亚胺结合还原型谷胱甘肽来测定氧化型谷胱甘肽,并引入还原剂三(2-羧乙基)膦来切割GSSG中的二硫键以产生两个分子的GSH。该测定与经过验证的二辛可宁酸测定法结合使用,用于蛋白质定量,与腺苷酸激酶测定法结合使用,用于细胞毒性评估。
引言
活性氧(ROS)是氧化应激的主要诱导剂;氧化应激在 DNA 突变、细胞衰老/死亡、各种癌症、糖尿病、神经系统疾病(如帕金森氏症和阿尔茨海默氏症)以及其他几种使人衰弱的疾病中已经得到充分证实 1,2,3,4,5。对抗 ROS 的关键防御是硫醇、非酶促抗氧化剂,它们能够通过充当质子供体来减少氧化剂或自由基 6,7。谷胱甘肽 (GSH) 和半胱氨酸是在哺乳动物中发现的两种最普遍的硫醇8,而存在各种其他低分子量硫醇(如麦角硫因)、GSH 和半胱氨酸是文献9、10、11 中发现的最常测量的非酶促抗氧化剂,与对抗 ROS 最相关 8,12,13,14。
当 GSH 用作抗氧化剂时,两个 GSH 分子通过二硫键共价连接在一起,形成谷胱甘肽二硫化物 (GSSG)。谷胱甘肽的消耗通常被用作氧化应激的指标15,16。该评估也可以与 GSSG 的检测相结合,尽管细胞中 GSSG 的增加通常受到活性输出过程的限制,因为 GSSG 在细胞中可能相对具有反应性,导致与其他蛋白硫醇形成二硫键16。
测量 GSH 和 GSSG 的传统方法不是简单的过程,需要许多步骤,包括使用裂解试剂进行细胞提取17,18。这里概述的方案简化了这些方法,并允许准确测量非酶促硫醇和使用细胞蛋白含量或腺苷酸激酶释放进行归一化。此外,还可以在 GSH/GSSG 提取之前测量细胞活力。以前有几种方法试图有效地靶向和定量还原和氧化的非酶促硫醇;方法包括使用HPLC 19,20,21,平板测定(生化)22,23,24,25,以及使用常用试剂进行硫醇偶联,如5,5-二硫代双-(2-硝基苯甲酸)(DTNB/Ellman试剂)19,一氯二鳃(mBCI)26,27,28 .几家公司还准备了用于检测谷胱甘肽的专有试剂盒;然而,他们没有公布试剂不相容性,这会带来取决于所用处理方法的问题29.
该协议概述了一种多参数测定法,该测定法通过 邻苯二甲醛(OPA)偶联检测还原硫醇(如GSH),以产生分别在340/450 Ex / Em下可检测的荧光信号。该测定通过使用掩蔽剂(N-乙基马来酰亚胺)和GSSG还原剂(三(2-羧乙基)膦)同时(在板中)检测GSH和GSSG。这种多生物标志物方案还为细胞裂解阶段提供了一个机会,通过二辛可宁酸测定法定量蛋白质,以便在完成最终测量时对样品进行归一化,或通过细胞培养基中的腺苷酸激酶测定法进行量化。该测定可以使用大多数实验室中现成的几种试剂进行,并且只需要一些额外的不常见化学品即可进行。该过程简单易行,并且可以在不到 2 小时的时间内完成而无需费力的阶段。
在该方案中,选择了各种纳米材料,这些纳米材料先前被证明可以诱导ROS或怀疑可以诱导氧化应激30,31。探索了一个浓度范围,以观察这些纳米材料暴露对各种细胞系的影响,以及该测定在量化抗氧化剂硫醇方面的有效性。
研究方案
注:以下方案的设计具有与二辛可宁酸(BCA)蛋白测定和腺苷酸激酶(AK)测定结合使用的能力,以使样品标准化为治疗。在整个材料的准备和使用过程中,确保操作员穿着适当的服装和必要的安全设备,例如 Howie 实验室外套、丁腈手套和 I 类安全眼镜。该协议分为几个阶段。
1. 储备液和工作溶液的制备
- 在1mM HCl中制备100mM GSH标准品的储备溶液(由37%HCl在双蒸水(ddH2O)中制备)。
注意: 如果从高浓度酸(例如 37% HCl)稀释,请确保在 I 类通风橱中向水中添加酸的正确过程。 - 在无水乙醇中制备22.35mM OPA的储备液。在一类通风橱中执行此步骤。在ddH2O中制备25mM N-乙基马来酰亚胺(NEM)。
注意:这三种溶液可以在 -20 °C 下储存长达 3 个月。 - 制备 0.01 M 三(2-羧乙基)膦 (TCEP) 至总体积为 500 μL,用于 100 孔。制备 100 μL 1 mM GSH 标准品,使用 ddH2O 从 100 mM 原液中稀释。
- 使用免疫沉淀 (IP) 裂解缓冲液或以下制剂:394 mg Tris-HCl(终浓度 25 mM)、877 mg NaCl(终浓度 150 mM)、29 mg EDTA(终浓度 1 mM)、1 mL 100% NP-40 或 IGEPAL CA-630(终浓度为 1% V/V)、5 mL 甘油(终浓度 5% V/V)、 84 mL ddH2O. 通过轻轻搅拌混合组分并将 pH 调节至 7.4。倒入 100 mL 容量瓶中,加入剩余体积的 ddH2O 以达到最终体积 100 mL。通过0.22μm过滤器的无菌过滤器,并在2-8°C下储存长达6个月。
注意:裂解溶液在该测定中确实起到污染物/干扰剂的作用;因此,指定了上述公式。 - 制备 1 L 0.1 M 磷酸盐缓冲盐水,补充有乙二胺四乙酸 (PBS-EDTA),浓度为 3 种不同的 pH 值,特别是 7.2、8.5 和 9.0。使用补充有 1 mM EDTA (292.24 mg/L) 或以下 10x (1 L) 配方的商业 0.1 M PBS 缓冲液:80 g NaCl、2.0 g KCl、14.4 g Na2HPO4、2.4 g KH2PO4、800 mL ddH2O。 添加并混合;加满 1 L。 高压灭菌溶液以达到无菌状态,并在室温下储存 12 个月。从10x储备溶液中,制备PBS的工作溶液,并用EDTA(如前所述的浓度)补充。
注意:pH 值至关重要;在开始实验方案之前,确保 pH 值准确。 - 使用 ddH2O(1 mM、500 μM、250 μM、125 μM、62.5 μM、31.25 μM、15.625 μM 和 7.8125 μM)进行 1:2 连续稀释 1 mM GSH。向标准孔中加入每种浓度 10 μL(一式两份)。样品将在裂解缓冲液中进一步稀释;因此,浓度将是其原始浓度的 1/5(200、100、50、25、12.5、6.25、3.125、1.5625 μM)。
注意:校准的最终浓度为 30 μm、15 μm、7.5 μm、3.75 μm、1.875 μm、937.5 nm、468.8 nm 和 234.4 nm。
2. 测定制备
注:该协议使用人类细胞系HepG2,A549和J774,这些细胞系是从ATCC商业购买的。这些细胞系是根据大学的动物和组织培养法案和条例制定的批准指南使用的。
- 在测定开始前24小时,以 表1所示的浓度接种细胞;但是,根据所使用的细胞系/类型和处理方式,根据需要调整密度。在具有 10% 热灭活胎牛血清 (HIFS)、1% Penstrep(10,000U/mL 青霉素/10mg/mL 链霉素)和 1% 非必需氨基酸的完全生长培养基(Eagles 改良必需品培养基 (EMEM))中培养细胞。
- 使用常规细胞接种方法接种细胞32.如果不使用测定后显微镜,则在全黑板中接种细胞。在使用之前,通过显微镜评估 T75 烧瓶中的细胞汇合度和总体健康状况。
- 在干净、无菌的 II 类生物安全柜中,并遵循严格的无菌技术,丢弃细胞培养基,用 ~15 mL 无菌室温 (RT) PBS 轻轻洗涤细胞,然后丢弃。
- 向细胞烧瓶中加入5mL无菌1x胰蛋白酶,轻轻摇晃以确保覆盖细胞单层,然后放入37°C的培养箱中5分钟以促进细胞分离。
- 通过加入含有热灭活胎牛血清 (10%) 的生长培养基(约 10 mL)停止胰蛋白酶消化。
- 将细胞转移到 50 mL 离心管中,并以 200 x g 沉淀 5 分钟。丢弃培养基并用 5 mL 相同培养基替换。将细胞重悬于试管中,直至均匀且无法观察到结块。
- 取出 20 μL 细胞悬液并放入血细胞计数器中进行计数。计算出所需的细胞数量后,进行稀释以制备具有正确细胞密度的溶液。
- 在 96 孔板(容量为 350 μL)中含有细胞的移液器培养基,每孔最大体积为 200 μL。将细胞置于含有5%CO2 的37°C培养箱中24小时以粘附在板表面。
- 为了评估总谷胱甘肽和GSSG,请处理两种情况的样品。播种和处理 6 个孔,提供 2 套 GSH 和 GSSG,并进行 3 个技术重复(图 1 演示布局)。
- 确保在检测开始之前适当制备所有试剂;在开始构建缓冲液或在测定中使用之前,确保所有缓冲液组分和试剂均处于室温状态,但 pH 值为 7.4 的 PBS(不含 EDTA)除外,其应保存在冰上/冷藏直至使用。
注意:至关重要的是,将气泡的形成限制在最低限度,以允许在测定中发生所需的反应,并允许通过酶标仪进行准确定量。
| 细胞系 | 接种密度(96孔板) |
| HepG2 | 10,000 个细胞/孔 |
| 空客A549 | 5,000 个细胞/孔 |
| J774型 | 10,000 个细胞/孔 |
表 1:所选细胞系的建议接种密度。 演示了表示数据中使用的三种不同细胞系的不同接种密度,特别是 A549、J774 和 HepG2。
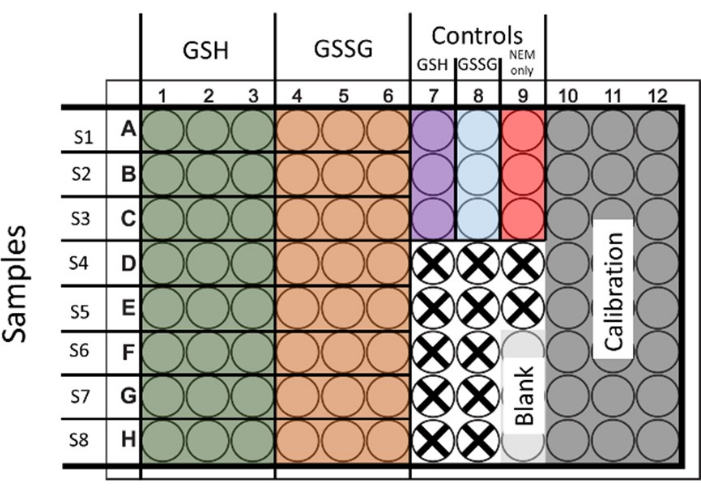
图 1:用于同时测定总谷胱甘肽和谷胱甘肽二硫化物的 96 孔板接种的拟议布局。 此外,还演示了用于校准和控制的孔。未使用的井用十字表示。 请点击这里查看此图的较大版本.
3.纳米材料处理
- 在具有μg能力的重量秤中称量纳米材料(特别是ZnO,TiO 2,CuO和Ag)。进行计算以达到每种纳米材料 1 mg/mL 的初始浓度。
- 将纳米材料溶液转移到超声仪中,并使用超声处理浴(38W)超声处理16分钟,以产生均匀的溶液。以 125、62.5、31.25、15.625 μg/mL 对每种纳米材料进行一系列稀释。
- 从培养箱中取出细胞,并用 RT PBS 轻轻洗涤。在确保所有 PBS 均已去除后,使用对照品(不含 HIFS 的培养基)将 100 μL 处理物加入平板中。对细胞进行处理后,在37°C培养箱(5%CO2)中与纳米材料孵育4小时;然后,使用以下方案量化 GSH:GSSG、蛋白质浓度和 AK 释放。
4. 检测方案
- 暴露于治疗后(图2A),通过腺苷酸激酶(AK)活性(可选)评估活力。按照制造商的说明使用商业试剂盒进行此测定。
- 在离心机中以200× g 离心板5分钟,轻轻沉淀处理和细胞碎片(图2B)。
- 从每个样品和对照孔(如上所述)中轻轻取出 20 μL 培养基上清液,然后以相同的布局格式移液到相邻的 96 孔白板中(图 2C)。
- 向每个孔中加入 100 μL AK 试剂盒的工作溶液,将板避光,并在室温下发酵 10 分钟。使用酶标仪以 1000 计数/秒的速度记录发光。
- 对于GSH标准品,向每个孔中加入40μL总谷胱甘肽缓冲液(图2D;可选,定量需要)。
- 从板中吸出剩余的培养基,并用冰冷的0.1M PBS(pH7.2)洗涤3次,丢弃每次洗涤(图2E),标准品除外。将最后的洗涤液留在板中,直到 GSH 校准液已装入板中。
- 将 10 μL 每种谷胱甘肽浓度和空白 (ddH2O) 一式三份加入孔中。
- 取出最终的PBS洗涤液,并按照表2将混合物添加到每个孔中,以获得所需的目标定量(图2E)。在开始此步骤之前计算所需的体积,因为在使用完整缓冲区时,活动会对时间敏感。确保在开始分析过程之前制备这些试剂混合物,但在使用前不要让它们静置超过 30 分钟。
- 放置在轨道板振荡器上,让板以300RPM振荡2分钟(图2F)。
- 从振荡器中取出,向每个孔中加入 5 μL 0.01M TCEP 溶液,不包括 NEM 对照孔。将板放回振荡器中并孵育10分钟(图2F)。
- 将板移至离心机并以200× g 旋转5分钟。将 25 μL 从每个样品孔转移到另一个 96 孔板(透明);这将用于蛋白质浓缩(参见步骤 4.15 ; 图2G)。请勿转移标准品或测定对照品。
- 确保每个孔的最终体积为 30 μL;从对照和标准品中去除体积以满足此要求(图2H)。
- 向每个孔中加入 170 μL 工作 OPA 溶液,将板避光并置于振荡器上 15 分钟(图 2I)。
- 使用酶标仪在Ex340 / Em450上读取荧光(图2J)。确保在测量阶段不存在气泡;它们将对反应和通过酶标仪进行定量分析产生不利影响。
- 要定量裂解细胞的蛋白质含量,请使用商业 BCA 检测试剂盒。将从步骤 4.12 中取出的样品以每孔 25 μL 的速度转移到新的 96 孔板(透明)中。
- 使用在 IP 裂解缓冲液中稀释的牛血清白蛋白 (BSA) 标准品,一式三份加入板中,每孔 25 μL。确切的浓度在 BCA 试剂盒方案中定义。
- 从 BCA 试剂盒中制备由 50:1 比例的试剂 A 和 B 组成的工作溶液,并向含有样品、标准品和对照品的每个孔中加入 200 μL。屏蔽板避光并在 37°C 下孵育 30 分钟 (图 2K)。
- 从培养箱中取出样品,在室温下平衡5分钟,然后通过酶标仪在562nm处读取吸光度(图2L)。
| 总谷胱甘肽浓度裂解试剂混合物 | |
| 元件 | 卷 |
| 裂解缓冲液 | 50微升 |
| 总体积/孔 | 50微升 |
| 氧化谷胱甘肽浓度裂解试剂混合物 | |
| 元件 | 卷 |
| 裂解缓冲液 | 49.5微升 |
| NEM(25毫米) | 0.5微升 |
| 总体积/孔 | 50微升 |
| 在混合物组成后 30 分钟内使用两种溶液 | |
| OPA检测解决方案组件 | 卷 |
| OPA 3毫克/毫升 | 5微升 |
| PBS (pH 9.0) | 165微升 |
| 总体积/孔 | 170微升 |
表 2:执行方案所需的试剂体积。 测定总谷胱甘肽、谷胱甘肽二硫化物和所需工作试剂所需的每孔体积。确保计算所需的体积,并包含超额,以说明传输过程中的体积损失。
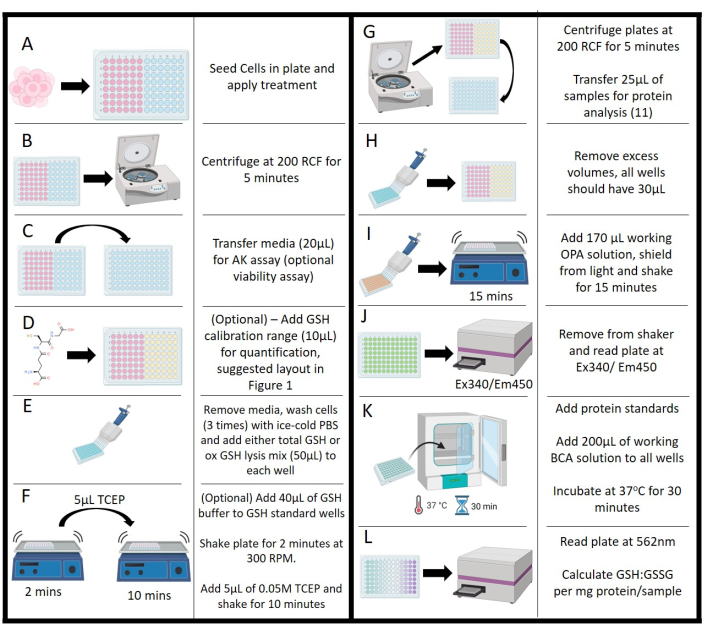
图 2:协议的示意图。 (A) 细胞的初始接种、孵育和处理。(B) 离心以将培养基与悬浮固体分离。(C) 腺苷酸激酶测定的培养基转移。(D) 添加谷胱甘肽浓度用于校准范围。(E) 洗涤阶段和裂解试剂添加。(F)缓冲液加入和三(2-羧乙基)膦加入与振荡步骤。(G) 离心裂解细胞以去除培养基以进行蛋白质分析。(H) 去除介质以平衡整个板的体积。(I) 邻苯二甲醛工作溶液的加入,振荡孵育。(J) 通过酶标仪测量 邻苯二甲醛荧光。(K) 用于蛋白质测定的二辛可宁酸测定的孵育阶段。(L) 测量蛋白质浓度,使谷胱甘肽标准化:谷胱甘肽二硫化物值。 请点击这里查看此图的较大版本.
代表性结果
按照该方案,分别以5,000个细胞/孔和10,000个细胞/孔的密度接种A549和J774细胞系,并在37°C的5%CO2 中培养48小时。纳米材料处理后的AK分析见 附表1,蛋白质浓度见 补充表2。
校准图表
图3所示的是使用规定浓度范围(0.234 - 30μM终浓度)从三种不同细胞类型的三个独立板进行的三次校准(尽管不应影响校准),在三个不同的非连续天。虽然显示了 3 个样本,但观察到 N 为 12,并表现出相似的线性回归,平均 R2 值为 0.9932 ± 0.007。
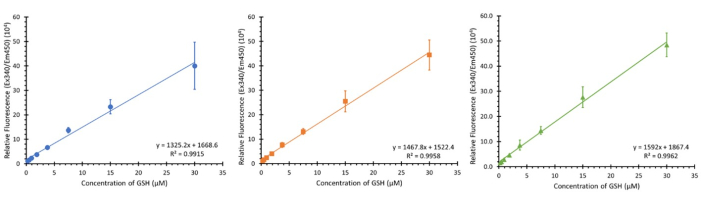
图 3:用于测定的谷胱甘肽校准图。 来自不同板内谷胱甘肽校准范围的三个校准图,每个校准图相隔一周进行;误差线 ± SD (n=3, N=12) n=技术重复,N=生物重复。 请点击这里查看此图的较大版本.
示例结果
HepG2、A549 和 J774 细胞用于评估各种纳米材料,这些纳米材料涉嫌通过氧化应激诱导细胞机制的变化。使用了所描述的检测和定量方案。
从 3 次测量(AK、BCA 和 GSH/GSSG)接收的数据处理如下。实施 AK 和 BCA 测定以实现标准化;使用推荐试剂盒的 AK 测定将提供释放到细胞培养基中的 AK 量的最快、最简单的数据。预计 AK 值的增加会增加细胞死亡。因此,需要 -ve(Alive)和 +ve(Dead)控件。这将允许基于百分比进行规范化。
BCA测定是一个较长的过程,但允许通过蛋白质定量(mg/mL)获得可量化的结果。这不需要像 AK 中那样的 -ve 或 +ve 控件,但仍需要通用的 -ve 控件(未处理的单元格)以实现值的归一化。
在这个具有代表性的结果部分中,发现处理(纳米材料)有可能对AK测定造成干扰。因此,所有归一化都是使用 BCA 数据执行的。因此,信息以每 mg/mL 蛋白质(通过 BCA 测定)的检测物种(GSH 或 GSH+GSSG(然而,从总 GSH+GSSG 浓度中减去 GSH 浓度以获得 GSSG 浓度)的浓度表示。如果需要,可以将其转换为比率,以评估所需处理后 GSH:GSSG 的变化。
图 4 中显示的是使用 OPA 方案获取的三种不同细胞系(A549、J774 和 HepG2)的 GSH:GSSG 比率数据,并通过 BCA 归一化为蛋白质表达 (μg/mL),指定额外 GSH 和 GSSG 值的进一步数据可在补充图 1 中找到。
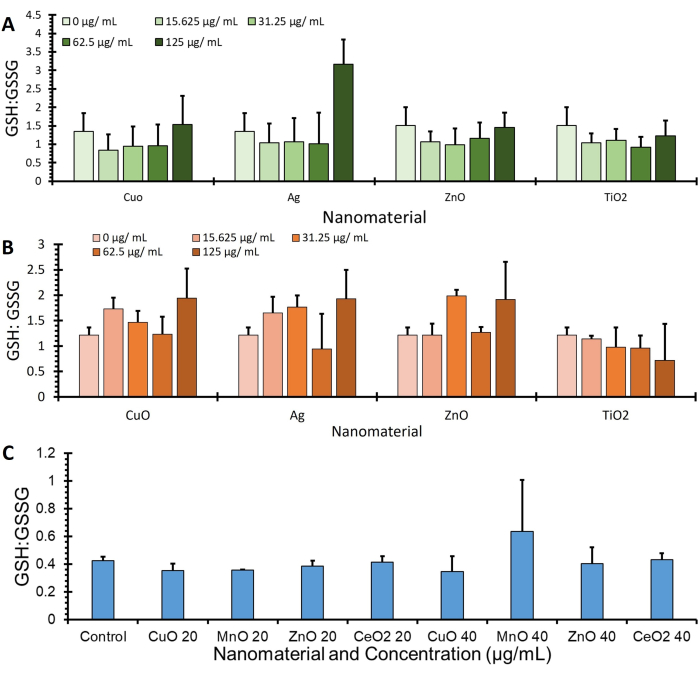
图 4:谷胱甘肽:谷胱甘肽二硫化物比率。 图中所示为3种细胞系的谷胱甘肽:谷胱甘肽二硫化物比率,即(A)A549、(B)J774和(C)HepG2。将细胞与处理物(无血清培养基中的各种纳米材料)一起孵育 4 小时。使用此方案处理细胞以量化谷胱甘肽和谷胱甘肽二硫化物的变化,并通过蛋白质定量、误差线± SE (n = 3, N=3) 进行归一化 请单击此处查看此图的较大版本.
该板还包含一系列对照品,以确保检测正确运行。NEM 作为单独的组件添加,以证明缺乏与 OPA 检测介质的交互。校准标准品表明,GSH浓度呈线性增加,这表明OPA检测试剂有效结合浓度增加的GSH浓度。
必须注意的是,该测定专门针对硫醇中常见的游离巯基(例如GSH,通常被认为是抗氧化剂)。一种可能的相互作用是OPA与蛋白质硫醇的结合,这将导致不准确的数据收集。因此,BCA测定是将数据归一化为蛋白质并允许准确反映游离GSH的关键阶段。
补充图1: 显示 3 种细胞系(即 (A) A549、(B) J774 和 (C) HepG2 的谷胱甘肽、谷胱甘肽二硫化物和谷胱甘肽:谷胱甘肽二硫化物比率的图表。将细胞与处理物(无血清培养基中的各种纳米材料)一起孵育 4 小时。使用此方案处理细胞以量化谷胱甘肽和谷胱甘肽二硫化物的变化,并通过蛋白质定量、误差线± SE (n = 3, N=3) 进行归一化 请单击此处下载此文件。
附表1: A549 和 J774 细胞腺苷酸激酶值的元数据。 请点击这里下载此文件。
附表2: 校准 A549、J774 和 HepG2 细胞的二辛可宁酸值的元数据。 请点击这里下载此文件。
讨论
如前所述,了解细胞氧化还原、监测氧化应激状态和抗氧化反应对于理解和预防癌症和神经退行性疾病(如癌症和神经退行性疾病)一直至关重要33,34。本文展示了一种通过提高准确 GSH 的可及性来改善转化环境的方法:GSSG 检测具有快速、最少的准备工作。
该方案展示了用于测定细胞内谷胱甘肽/硫醇种类(还原和氧化)的多参数测定序列,具有通过BCA蛋白测定和/或AK测定的2种归一化方法。该测定法也可以通过初始介质提取步骤进行修改以检测各种其他标记物,并且可以以一种方式进行简化,即简单地给出氧化/还原硫醇比率,而不排除校准范围。
在考虑分析物的评估时,对 mBCI 和 OPA 进行了探索和比较。虽然 mBCl 最初表现出良好的信号潜力,但发现使用上存在重大局限性。首先,使用活细胞证明了 mBCl 的最佳利用;然而,在细胞裂解后,发现信号被淬灭,与 OPA35 相比,信号通常以多孔形式减弱。另一个问题是通过mBCl测量GSSG,关于这一点的文献很少,通过协议优化/探索,没有实现通过mBCl准确检测GSSG。
我们已经证明,OPA 测定具有非常可靠的校准范围,在 0.234 - 30 μM GSH 浓度范围内,R2 平均值为 0.9932 ± 0.007 (N=12)。之所以选择这个范围,是因为在文献35中发现了以前的参考范围。从理论上讲,可以在这些范围之外检测到谷胱甘肽,但需要修改试剂浓度、孵育时间以及可能用于检测的设备。必须注意的是,每个板都需要有自己的定量标准范围;在不同日期进行的板之间最微小的时间差异会对测量过程中获得的值产生重大影响。
从该协议中获得准确可靠的数据取决于严格遵守的几个关键步骤。在构建方案中所需的各种缓冲液时,pH值的准确性至关重要。因此,要求 pH 值为 9 的缓冲液的偏差不应超过 ± 0.1。这是由于缓冲液组分可能在错误的pH值下从溶液中沉淀出来;完全遵循此协议将防止此问题。
在裂解前完全去除处理和准确洗涤对于防止在孔板读数阶段出现伪影和不准确的数据采集也至关重要。一旦细胞被裂解(步骤4.8),就不可能去除处理物,并且板将无法挽救。由于在整个方案中添加的缓冲液/试剂的体积在样品和标准品之间有所不同,因此在步骤4.12和4.13中,用户了解不同的体积至关重要。此外,检测操作人员还需要了解这些不同的体积,并指示他们确保所有体积都相同,以便实现准确的测量。由于样品和标准品之间的体积并不明显,因此在样品孔中含有过量溶液时,很容易犯错误。
该协议存在一些局限性,这些限制依赖于关键步骤,而这些步骤对于获取准确可靠的数据至关重要。执行此测定的用户需要具备合理水平的实验室技能,以防止出现不必要的问题,例如气泡形成。气泡的形成对微孔板内发生反应的能力和荧光的测量都有巨大的影响。该协议中使用的裂解剂含有去污剂,这给可能难以防止气泡形成的新手研究人员带来了困难。立即离心可以挽救这种误差。该协议在细胞类型方面也可能受到限制;细胞系 A549、J774 和 HepG2 用于优化和生成该协议的数据。其他细胞系可能需要不同的接种密度和方案的优化才能获得准确的数据。
与几种现有的测定相比,该协议具有许多优势。虽然使用邻苯二甲醛检测硫醇并不是一个新概念,但在像这样的组合测定形式中,在微孔板中使用所需的材料和设备,为所有实验室使用该协议提供了巨大的潜力。大多数来自商业供应商的硫醇/谷胱甘肽试剂盒不披露其试剂的成分。因此,可能很难预见到不兼容/干扰的可能性。在这里,我们介绍了所有使用的试剂的每个组成部分,以限制这种潜力。
在初始治疗期完成后,该方案也相当迅速地执行。考虑到孵育阶段之间的用户处理,该协议的硫醇定量方面可以在1小时内进行。样品同时裂解和结合,以防止样品的自氧化,这对于这些反应物种来说是最佳的。虽然方案中没有指定,但从技术上讲,样品可以在板中裂解并密封,从而可以冷冻以备将来分析。然而,对协议的这种改变尚未得到探索。
披露声明
作者声明没有利益冲突。
致谢
这项研究由欧洲项目GRACIOUS (GA760840)和SUNSHINE (GA952924)资助。作者还要感谢所有以某种方式协助制定该议定书的人的努力。
材料
| Name | Company | Catalog Number | Comments |
| 0.22µm filter (optional-For lysis buffer) | Fisher scientific | 12561259 | |
| 100mL volumetric flask | Fisher scientific | 15290866 | |
| 1L Volumetric flask | Fisher scientific | 15230876 | |
| 250mL beaker (optional-For lysis buffer) | Fisher scientific | 15409083 | |
| 8-Channel micropipette (20-200µL) | SLS | FA10011D2 | |
| 8-Channel micropipette (2-20µL) | SLS | B2B06492 | |
| 96 well plates - black with clear bottom, TC treated | Fisher scientific | 10000631 | Preferred plate for seeding and fluoresence, use TC treated clear if unavailable |
| 96 well plates - clear (TC treated and untreated) | Fisher scientific | 10141161 | If black plates with clear bottom is not available/ suitable use TC treated clear |
| 96 well plates - white, Not TC treated | Fisher scientific | 11457009 | |
| A549 (lung carcinoma) cell line | ATCC | CCL-185 | |
| Absolute ethanol | Merck (Sigma-Aldrich) | 1.08543 | |
| Aluminium foil | Fisher scientific | 11779408 | For protecting plates from light |
| BCA Assay Kit | Thermo | 23225 | |
| Benchtop Centrifuge (with 96 plate rotor) | Eppendorf | 5804 | |
| Ethylenediaminetetraacetic acid (EDTA) | Merck (Sigma-Aldrich) | E9884 | |
| Glutathione (GSH) | Merck (Sigma-Aldrich) | G6013 | |
| Glutathione disulfide (GSSG) | Merck (Sigma-Aldrich) | G4501 | |
| Glycerol | Merck (Sigma-Aldrich) | G5516 | |
| HCl, 37% | Merck (Sigma-Aldrich) | 258148 | Dilute to 1mM for GSH stock, pH adjustment also |
| HepG2 (Hepatocarcinoma) cell line | ATCC | HB-8065 | |
| IGEPAL CA-630 | Merck (Sigma-Aldrich) | 18896 | Use either IGEPAL CA-630 or NP-40 for solution, not both |
| IP lysis buffer | Fisher scientific | 11825135 | |
| J774 (monocyte, macrophage) cell line | ATCC | TIB-67 | |
| KCl | Merck (Sigma-Aldrich) | P3911 | |
| KH2PO4 | Merck (Sigma-Aldrich) | P0662 | |
| Micropipette (20-200µL) | SLS | B2B06482 | |
| Micropipette (2-20µL) | SLS | B2B06478 | |
| Microplate shaker | VWR | 444-0041 | |
| Na2HPO4 | Merck (Sigma-Aldrich) | S9763 | |
| NaCl | Merck (Sigma-Aldrich) | S9888 | |
| NaOH, 10M | Merck (Sigma-Aldrich) | 72068 | For pH adjustment only |
| N-Ethylmaleimide (NEM) | Merck (Sigma-Aldrich) | E3876 | |
| NP-40 | Merck (Sigma-Aldrich) | 492016 | Use either IGEPAL CA-630 or NP-40 for solution, not both. NP-40 alternative suggested |
| Ortho -Phthaldialdehyde (OPA) | Merck (Sigma-Aldrich) | P1378 | |
| PBS 0.1M | Merck (Sigma-Aldrich) | P2272 | PBS can either be acquired pre-made or made in house, see notes |
| Plate reader (with fluoresence capacity) | Tecan | SPARK | |
| Stir bar (optional-For lysis buffer) | Fisher scientific | 16265731 | |
| Toxilight bioassay kit (AK assay) | Lonza | LT17-217 | |
| Tris(2-carboxyethyl)phosphine hydrochloride (TCEP) 0.5M in H2O | Alfa Aesar | H51864 | Can also be purchased crystalised and suspended |
| TRIS-HCl | Merck (Sigma-Aldrich) | 93363 | |
| X100 phosphatase and protease cocktail | Fisher scientific | 10025743 |
参考文献
- Barnham, K. J., Masters, C. L., Bush, A. I. Neurodegenerative diseases and oxidative stress. Nat Rev Drug Discov. 3 (3), 205-214 (2004).
- Arfin, S., et al. Oxidative stress in cancer cell metabolism. Antioxidants. 10 (5), 642 (2021).
- Cooke, M. S., Evans, M. D., Dizdaroglu, M., Lunec, J. Oxidative DNA damage: mechanisms, mutation, and disease. The FASEB Journal. 17 (10), 1195-1214 (2003).
- Ghezzi, P., Jaquet, V., Marcucci, F., Schmidt, H. H. H. W. The oxidative stress theory of disease: levels of evidence and epistemological aspects. Br J Pharmacol. 174 (12), 1784-1796 (2017).
- Bhattacharyya, A., Chattopadhyay, R., Mitra, S., Crowe, S. E. Oxidative stress: An essential factor in the pathogenesis of gastrointestinal mucosal diseases. Physiol Rev. 94 (2), 329-354 (2014).
- Yin, F., Sancheti, H., Cadenas, E. Mitochondrial thiols in the regulation of cell death pathways. Antioxi Redox Sig. 17 (12), 1714-1727 (2012).
- Balcerczyk, A., Bartosz, G. Thiols are main determinants of total antioxidant capacity of cellular homogenates. Free Rad Res. 37 (5), 537-541 (2003).
- McBean, G. J. Cysteine, glutathione, and thiol redox balance in astrocytes. Antioxidants. 6 (3), 62 (2017).
- Nimse, S. B., Pal, D. Free radicals, natural antioxidants, and their reaction mechanisms. RSC Adv. 5 (35), 27986-28006 (2015).
- Nordberg, J., Arnér, E. S. J. Reactive oxygen species, antioxidants, and the mammalian thioredoxin system1. Free Rad Biol Med. 31 (11), 1287-1312 (2001).
- Pham-Huy, L. A., He, H., Pham-Huy, C. Free radicals, antioxidants in disease and health. Int J Biomed Sci. 4 (2), 89 (2008).
- Harris, I. S., DeNicola, G. M. The complex interplay between antioxidants and ROS in cancer. Trend Cell Biol. 30 (6), 440-451 (2020).
- Traverso, N., et al. Role of glutathione in cancer progression and chemoresistance. Oxid Med Cell Longev. 2013, 972913 (2013).
- Day, R. M., Suzuki, Y. J. Cell proliferation, reactive oxygen and cellular glutathione. Dose-Resp. 3 (3), 425-442 (2005).
- Aquilano, K., Baldelli, S., Ciriolo, M. R. Glutathione: new roles in redox signaling for an old antioxidant. Front Pharmacol. 5, 196 (2014).
- Zitka, O., et al. Redox status expressed as GSH: GSSG ratio as a marker for oxidative stress in paediatric tumour patients. Onco Lett. 4 (6), 1247-1253 (2012).
- Childs, S., Haroune, N., Williams, L., Gronow, M. Determination of cellular glutathione: glutathione disulfide ratio in prostate cancer cells by high performance liquid chromatography with electrochemical detection. J Chrom A. 1437, 67-73 (2016).
- Giustarini, D., et al. glutathione disulfide, and S-glutathionylated proteins in cell cultures. Free Rad Biol Med. 89, 972-981 (2015).
- Özyürek, M., et al. Determination of biothiols by a novel on-line HPLC-DTNB assay with post-column detection. Analytica Chimica Acta. 750, 173-181 (2012).
- Zhang, L., Lu, B., Lu, C., Lin, J. Determination of cysteine, homocysteine, cystine, and homocystine in biological fluids by HPLC using fluorosurfactant-capped gold nanoparticles as postcolumn colorimetric reagents. J Sep Sci. 37 (1-2), 30-36 (2014).
- Tsiasioti, A., Georgiadou, E., Zacharis, C. K., Tzanavaras, P. D. Development and validation of a direct HPLC method for the determination of salivary glutathione disulphide using a core shell column and post column derivatization with o-phthalaldehyde. J Chromat B. 1197, 123216 (2022).
- Huang, D., Ou, B., Prior, R. L. The chemistry behind antioxidant capacity assays. J Agri Food Chem. 53 (6), 1841-1856 (2005).
- Berker, K. I., Güçlü, K., Tor, &. #. 3. 0. 4. ;., Demirata, B., Apak, R. Total antioxidant capacity assay using optimized ferricyanide/prussian blue method. Food Anal Meth. 3 (3), 154-168 (2010).
- Rahman, I., Kode, A., Biswas, S. K. Assay for quantitative determination of glutathione and glutathione disulfide levels using enzymatic recycling method. Nat Prot. 1 (6), 3159-3165 (2007).
- Kampa, M., et al. A new automated method for the determination of the Total Antioxidant Capacity (TAC) of human plasma, based on the crocin bleaching assay. BMC Clin Pathol. 2 (1), 3 (2002).
- Fernández-Checa, J. C., Kaplowitz, N. The use of monochlorobimane to determine hepatic GSH levels and synthesis. Anal Biochem. 190 (2), 212-219 (1990).
- Nauen, R., Stumpf, N. Fluorometric microplate assay to measure glutathione S-transferase activity in insects and mites using monochlorobimane. Anal Biochem. 303 (2), 194-198 (2002).
- Stevenson, D., Wokosin, D., Girkin, J., Grant, M. H. Measurement of the intracellular distribution of reduced glutathione in cultured rat hepatocytes using monochlorobimane and confocal laser scanning microscopy. Toxicol in vitro. 16 (5), 609-619 (2002).
- McBeth, C., Stott-Marshall, R. J. Interference of reversible redox compounds in enzyme catalysed assays–Electrochemical limitations. Anal Biochem. 662, 114972 (2023).
- Yu, Z., et al. Reactive oxygen species-related nanoparticle toxicity in the biomedical field. Nanoscale Res Lett. 15 (1), 115 (2020).
- Boyles, M., et al. Development of a standard operating procedure for the DCFH2-DA acellular assessment of reactive oxygen species produced by nanomaterials. Toxicol Mech Meth. 32 (6), 439-452 (2022).
- Segeritz, C. P., Vallier, L. Cell culture: Growing cells as model systems in vitro. Basic Sci Meth Clin Res. , 151-172 (2017).
- Ma, Q. Role of nrf2 in oxidative stress and toxicity. Ann Rev Pharmacol Toxicol. 53, 401-426 (2013).
- Calabrese, V., Cornelius, C., Dinkova-Kostova, A. T., Calabrese, E. J., Mattson, M. P. Cellular stress responses, the hormesis paradigm, and vitagenes: novel targets for therapeutic intervention in neurodegenerative disorders. Antioxid redox Signal. 13 (11), 1763-1811 (2010).
- Ishkaeva, R. A., Zoughaib, M., Laikov, A. V., Angelova, P. R., Abdullin, T. I. Probing cell redox state and glutathione-modulating factors using a monochlorobimane-based microplate assay. Antioxidants. 11 (2), 391 (2022).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。