需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
使用光谱气体分析仪测量水生生态系统中的溶解甲烷
摘要
本研究展示了一种使用便携式光学分析仪测量水性样品中甲烷气体浓度的方法,该分析仪在闭环中耦合到注射室。结果与传统气相色谱法相似,提供了一种实用且低成本的替代方案,特别适用于远程现场研究。
摘要
由于与气候变化相关,测量生态系统中的温室气体 (GHG) 通量和储存库在生态研究中变得越来越普遍。因此,对能够适应测量研究小组内不同池和通量的分析平台的需求也在增长。本研究旨在开发一种程序,使用最初设计和销售用于气体通量测量的便携式基于光谱的气体分析仪来测量水性样品中的 GHG 浓度。该方案涉及传统的顶空平衡技术,然后将顶空气体子样品注入通过闭环连接到气体分析仪入口和出口的腔室中。该腔室由通用梅森罐和简单的实验室用品制成,是可能需要进样前稀释的样品的理想解决方案。使用腔室测得的甲烷浓度与通过气相色谱-火焰电离检测 (GC-FID) 对来自同一样品瓶的子样品分别测定的浓度密切相关 (r2 > 0.98)。该程序特别适用于色谱设备和用品不易获得的偏远地区的现场研究,为测量水生系统中甲烷和其他溶解温室气体浓度提供了一种实用、更便宜、更有效的解决方案。
引言
陆地-水生界面的生态系统,如湿地、湖泊、水库、河流和小溪,是二氧化碳 (CO2)、甲烷 (CH4) 和一氧化二氮 (N2O) 等温室气体 (GHG) 的重要汇和来源1,2。具体来说,CH4 是在沉积物孔隙的饱和孔隙中厌氧呼吸过程中产生的。一旦产生,一部分就会被氧化并转化为 CO2,而其余部分最终会通过水柱和植被扩散或爆裂成气泡3。在给定时间,使沉积物孔隙(即孔隙水)饱和的水中的 CH4 浓度可以让我们得以一窥 CH4 产生、消耗和运输4 之间的平衡。当在垂直剖面或时间上测量时,孔隙水浓度还可以识别 CH4 生产和消费中更活跃的区域及其季节性变化。
传统上,确定生态系统中孔隙水中温室气体浓度的方法涉及处理在现场收集的水样,以平衡形成的顶部空间中的气体。然后,通过气相色谱分析顶空以确定浓度5.虽然这种方法在生态学研究中得到广泛应用,但它需要台式气相色谱-火焰电离检测 (GC-FID) 系统,该系统需要分配传统的实验室空间和高度的专业知识来校准和作(例如6)。它还需要使用专门的耗材,例如大型载气罐(即氮气 (N2) 和氦气 (He)),这些气体在偏远地区不容易获得。这些要求以及将样品运输到实验室的相关物流可能会限制采样设计,在某些情况下,当色谱设备不可用时,会限制研究的范围。
本研究旨在开发一种替代方法,使用基于便携式光谱的气体分析仪测量水溶液顶部空间样品中的溶解温室气体浓度。这种类型的光学气体分析仪是标准 GC-FID 系统的一种经济高效的替代方案,其便携性使其成为野外工作应用的理想选择。基于光谱法的便携式气体分析仪可产生高频气体浓度测量(即 ~ 1 s-1),响应时间为 2 - 5 s,具体取决于品牌和型号。这些仪器的设计和销售主要用于测定土壤、水和植被等温室气体排放表面的气体通量 7,8,9。光学分析仪允许在感兴趣的发射表面上部署的非稳态顶空室中通过连续浓度测量来计算通量。在表面腔室的常规预期用途中,对腔室中观察到的浓度变化率以及已知的腔室尺寸、压力和温度的高频测量允许将这些数据解释为单位表面积(即表面通量)的发射(或吸收)速率(即表面通量)10。然而,便携式气体分析仪既没有配备也没有针对水性介质中的溶解浓度进行优化,因此需要对此类分析进行额外的调整和解释。
利用之前使用光学分析仪测定顶空8 离散样品中浓度的演示,我们设计了一个小型封闭腔室(即无发射表面),以闭环方式连接到分析仪。注射顶空气体子样品后浓度的变化,然后进行稀释计算,可以确定原始顶空浓度。通过将其结果与通过 GC-FID 在相同样品中获得的结果进行比较来评估该方法的精密度。该方法通过一个用例进一步证明了该方法,该用例分析了从路易斯安那州淡水沼泽实验地点收集的孔隙水样品中 CH4 的垂直剖面。
研究方案
1. 孔隙水采样和分析
- 使用孔隙水透析采样器 (peepers)11 收集样品。将窥视器部署在研究地点的相关位置。在示范研究中,在淡水沼泽的两个主要植被斑块上部署了 6 个窥视器:三个在以 Sagitaria lancifolia 为主的斑块上,另外 3 个在 S. lancifolia 和 Typha latifolia 植被共同主导的斑块上。
- 在 6 月、9 月、10 月和 12 月采集 4 次样品。从土壤表面到土壤表面以下 ~50 厘米的 10 个不同深度收集样品。采样遵循12,13 中描述的方法。
- 采样前 ~20 天用 61 mL 去离子水填充采样池。在实验室中用 N2 将去离子水泡 5 分钟以去除氧气,然后再在现场使用。
- 在采样过程中,使用连接到细胞提取管线的注射器从细胞中取出 25 mL 水。然后,通过二级电池充电管线,用预先注入 N2 的新鲜去离子水重新填充电池。如果在采集后需要立即测量浓度,请继续执行步骤 2.1。
- 将提取的水加入 10 mL 玻璃瓶中,玻璃瓶中保存有 0.2 mL 0.1 M HCl,用隔垫封盖,然后冷藏直至实验室分析。
注意:欢迎此方法的用户根据特定的研究需求修改采集深度、采样计划和频率。
2. 温室气体浓度测量
- 对注射器中的孔隙水样品进行顶空平衡
- 使用平衡技术创建顶空气体样品14.使用 30 mL 注射器从现场收集的样品中抽取 5 mL 水 (Vpw),然后加入 15 mL N2 (超高纯度 99.999%)以产生顶空 (Vhs)。
- 用力持续地搅拌注射器 5 分钟,手动或使用摇床(如果有)。按照以下步骤,将 12 mL 顶空气体亚样品注入 10 mL 预真空小瓶中,用于使用光学分析仪进行气体浓度测量(图 1)。使用蠕动泵15 排空样品瓶,或手动将 60 mL 注射器的柱塞拉到封闭的样品瓶上,然后将空气抽出 3 次。
注意:可以使用 He 代替 N2 来创建顶空。向注射器中添加 N2 或 He 的程序取决于用户可用的实际水箱的具体调整或调节器。这种添加通常涉及使用匹配的管道将注射器连接到水箱,或从适合水箱的采样端口与注射器进行萃取。根据现场条件和相关物流,用户可以使用环境空气来创造顶部空间。
- 创建注射室
- 制造一个进样室,该进样室可以接受少量空气 (~1 - 5 mL) 进入密封体积的空气,该空气连接到气体分析仪的入口和流出处,形成一个闭环(材料表)。进样室和分析仪是该系统的两个主要元件(图 2)。
- 修改 365 mL 梅森罐的金属盖,钻一个直径为 11 mm 的孔,以适合一个隔膜作为进样口,并钻两个直径为 7 mm 的孔以插入与分析仪连接的旋塞阀。使用环氧树脂胶拧紧注射口和接头,确保腔室密封。
- 将进样室连接到光学分析仪
- 使用 5/32 英寸内径 (I.D.) 和 1/4 英寸外径 (O.D.) 将广振罐与分析仪的入口和出口连接PFA 塑料管,并考虑其增加的体积。确保管路符合仪器制造商的建议,并且清洁干燥且无冷凝。
- 将连接进样室和仪器的阀门设置为打开,以创建一个闭环空气回路。等待气体浓度稳定。
- 在腔室中注入样品
- 当腔室中的浓度和分析仪中的信号稳定(即标准偏差 <0.03 ppm)时,从包含步骤 2.1.2 中创建的顶空样品的小瓶中注入 2 mL 子样品。等待分析仪中的浓度再次稳定,然后再注入下一个子样品(图 3)。
- 如果浓度接近 100 ppm,则最多连续进样 20 个子样品,或者更少(参见8了解高于此阈值的准确度对准确性的影响)。分析每 5 个样品的 CH4 检查标准品,并使用相对标准偏差 (RSD) 评估与实际测量值的差异。
- 完成一组重迭进样后,拔下连接到仪器的一条管路,将腔室重置为环境压力,避免压力和甲烷浓度显著升高。
注:根据多次测试运行,确定信号在进样后 ~15 秒稳定,但可能需要不同的时间以响应其他仪器记录规格(图 3)。所用仪器的流速为 ~1 L/min,响应时间为 5 s,不同日期不同分析期间的腔体压力范围为 720 至 745 Torr。
- 计算顶空中的 CH4 浓度
- 对于每个子样品,使用公式 1 计算顶部空间 (Chs - μmol/mol) 中目标 GHG(例如,CH4、CO2、N2O)的浓度:
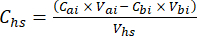 方程 [1]
方程 [1]
其中 Vhs 是顶空子样本的体积。 - 计算注射前 (Cbi - μmol -1) 和之后 (Cai - μmol -1) 的浓度,作为注射前 15 次测量 (~15 s) 和注射后信号稳定后 15 次测量的平均值。使用公式 2 和 3 计算进样前 (Vbi) 和进样后 (Vai) 的体积(以 mL 为单位):
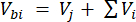 [2]
[2]
和
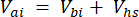 [3]
[3]
其中 Vj (mL) 是染色缸 (365 mL) 和软管 (125.4 mL) 的添加体积, Vi (mL) 是注射的子样品的累积体积。
- 对于每个子样品,使用公式 1 计算顶部空间 (Chs - μmol/mol) 中目标 GHG(例如,CH4、CO2、N2O)的浓度:
- 计算孔隙水浓度
- 使用顶部空间中气体的摩尔分数和样品处理过程中的大气压 (P) 计算顶部空间 CO2、CH4 或 N2O 在顶部空间的分压 (Pi - MPa),使用公式 4:
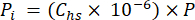 [4]
[4] - 使用稀释方程(方程 5)计算孔隙水中 GHG 的水当量浓度,其中顶部空间和水当量浓度和体积:
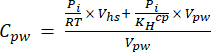 [5]
[5]
其中 R 是通用气体常数 (0.008314 L MPa mol−1 K−1),是空气温度 (K),Vhs 是顶空体积 (mL),K Hcp 是 CO2、CH4 或 N2O 的亨利挥发性常数(分别为 2.96、67.13 和 3.82 L MPa/mol)16,V pw 是用于创建顶空的液体子样品的体积 (mL)。 - 在测量过程中使用记录的 T 和 P。示范工程样品分析过程中的平均 T 和 P 分别为 295.15 K 和 0.101325 MPa。
- 使用顶部空间中气体的摩尔分数和样品处理过程中的大气压 (P) 计算顶部空间 CO2、CH4 或 N2O 在顶部空间的分压 (Pi - MPa),使用公式 4:
3. 根据标准色谱测量进行验证
- 在常规气相色谱仪中分析 10 mL 样品瓶中不同的已知 CH4 浓度。使用三组相同的 20 个标准品。最低浓度范围为 5 至 100 ppm,并以 5 ppm 的增量增加。
- 通过在气相色谱仪上进行火焰离子化检测来确定 CH4 浓度。色谱仪使用多孔聚合物吸收剂填充柱,以 He (25 mL/min) 作为载气。要测量标准品的浓度,请将色谱仪校准至曲线拟合 (r2) > 0.99。
- 色谱后,使用制造商校准的光学分析仪(即精密度(300 s,1σ):0.3 ppb CH4),使用上述方法继续测定相同标准样品瓶中的 CH4 浓度。
- 通过对三个标准组的色谱和光学分析仪结果进行线性回归来评估方法的准确性。通过比较每组标准品中执行的回归的斜率和截距来评估方法的可重复性。使用标准最小二乘模型评估比较,重点是 Effect Leverage。以 0.05 的显著性水平评估所有回归和比较。
结果
光学分析仪与气相色谱法
通过气相色谱和光学分析仪获得的三组标准品的结果显示良好的线性拟合(即 r2 > 0.98),斜率接近 1(图 4)。三个实验中回归的斜率在统计学上相似 (F(2) = 0.478,p = 0.623),表明结果的可重复性。需要注意的是,所有三种情况下的斜率都大于 1,这表明平均而言,与通过色谱法获得的浓度?...
讨论
本研究证明了基于便携式光谱的气体分析仪与定制进样室耦合分析水样形成的顶部空间的适用性。演示的重点是 CH4,但该协议可应用于分析其他相关 GHG,如 CO2 和 N2O8。目标是扩展以前对这些闭环系统的系统评估,这些系统代表了 GHG 浓度测量研究中传统气相色谱法的替代分析平台。
与气相色谱法类似,在?...
披露声明
作者声明没有利益冲突。
致谢
这项工作由 DOE 奖励 DE-SC0021067、DE-SC0023084 和 DE-SC0022972 资助。沼泽采样点的孔隙水浓度数据可在 ESS-DIVE 数据档案(https://data.ess-dive.lbl.gov/view/doi:10.15485/1997524,于 2024 年 6 月 21 日访问)中公开获得。
材料
| Name | Company | Catalog Number | Comments |
| 1/4 in. I.D. x 3/8 in. O.D. Clear Vinyl Tubing | Home Depot | SKU # 702098 | Use to couple stopcocks and tubing connected to the instrument. Two short pieces (~4 cm). |
| 5/16 - 5/8 in. Stainless Steel Hose Clamp | Everbilt | 6260294 | Use to secure tubing connecting the stopcock valves and tubing connected to the instrument. |
| Crack-Resistant Teflon PFA Semi-Clear Tube for chemicals, 5/32" ID, 1/4" OD | McMaster-Carr | 51805K86 | Use to connect the injection chamber to the inlet and outlet ports of the instrument. We used two 0.68 m-long tubing in our experiment. |
| Drill with titanium step drillbit | Multiple companies | Use to drill the holes for septum and stopcocks in the jar's metallic lid. | |
| Gay butyl septum (stopper) | Weathon Microliter | 20-0025-B | Use as injection port and as vial septum (if compatible). |
| Headspace vials 20ml (23x75mm), Clear, Crimp Rounded Bottom | Restek | 21162 | Use to store the headspace sample. |
| Heavy Duty Steel Bond Epoxy GorillaWeld | Gorilla | 4330101 | Use to glue stopcock valves and septum to the jar's metallic lid. |
| Hypodermic Needles | Air-Tite Products Co. | N221 | Use to extract water from field vials, inject heaspace sample in vial and inject subsample to the injection chamber. |
| Mason jar (12 oz) | Ball, Kerr, Jarden | Larger or smaller chamber volumes can be chosen depending on sample concentrations. | |
| Optical spectroscopy-based gas analyzer | Multiple companies | Picarro G4301, Licor 7810, Licor 7820, ABB GLA131-GGA | These are some specific examples of analyzers that could be coupled to the injection chamber. We recognize that it is not an extensive list and other optical spectroscopy analyzers may also be suitable for the method. |
| Stopcock valve | DWK Life Sciences | 420163-0001 | Keep the valves open during normal operation. |
| Syringe (2.5 mL) | Air-Tite Products Co. | R2 | Use to extract subsamples from the headspace vials and inject them in the injecion chamber for analysis. |
| Syringe (30 mL) | Air-Tite Products Co. | R30HJ | Use to create headspace for gas analysis. |
参考文献
- Bastviken, D., Tranvik, L. J., Downing, J. A., Crill, P. M., Enrich-Prast, A. Freshwater methane emissions offset the continental carbon sink. Science. 331 (6013), 50 (2011).
- Quick, A. M., et al. Nitrous oxide from streams and rivers: A review of primary biogeochemical pathways and environmental variables. Earth-Sci Rev. 191, 224-262 (2019).
- Bridgham, S. D., Cadillo-Quiroz, H., Keller, J. K., Zhuang, Q. Methane emissions from wetlands: biogeochemical, microbial, and modeling perspectives from local to global scales. Glob Chang Biol. 19 (5), 1325-1346 (2013).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- McAuliffe, C. Gas chromatographic determination of solutes by multiple phase equilibrium. Chem Technol. 1, 46-51 (1971).
- Hoyos Ossa, D. E., Gallego Rios, S. E., Rodríguez Loaiza, D. C., Peñuela, G. A. Implementation of an analytical method for the simultaneous determination of greenhouse gases in a reservoir using FID/µECD gas chromatography. Int J Environ Anal Chem. 103 (12), 2915-2929 (2023).
- Kittler, F., et al. Long-term drainage reduces CO2 uptake and CH4 emissions in a Siberian permafrost ecosystem. Glob Biogeochem Cycles. 31 (12), 1704-1717 (2017).
- Wilkinson, J., Bors, C., Burgis, F., Lorke, A., Bodmer, P. Measuring CO2 and CH4 with a portable gas analyzer: Closed-loop operation, optimization and assessment. PLoS One. 13 (4), e0193973 (2018).
- Villa, J. A., et al. Ebullition dominates methane fluxes from the water surface across different ecohydrological patches in a temperate freshwater marsh at the end of the growing season. Sci Tot Environ. 767, 144498 (2021).
- Holland, E. A., et al. Soil CO2, N2O and CH4 exchange. Std Soil Meth Long-Term Ecol Res. , 185-201 (1999).
- MacDonald, L. H., Paull, J. S., Jaffé, P. R. Enhanced semipermanent dialysis samplers for long-term environmental monitoring in saturated sediments. Environ Monitor Assess. 185 (5), 3613-3624 (2013).
- Villa, J. A., et al. Plant-mediated methane transport in emergent and floating-leaved species of a temperate freshwater mineral-soil wetland. Limnol Oceanography. 65, 1635-1650 (2020).
- Villa, J. A., et al. Methane and nitrous oxide porewater concentrations and surface fluxes of a regulated river. Sci Tot Environ. 715, 136920 (2020).
- Kampbell, D. H., Wilson, J. T., Vandegrift, S. A. Dissolved oxygen and methane in water by a GC headspace equilibration technique. Int J Environ Anal Chem. 36 (4), 249-257 (1989).
- Rochette, P., Bertrand, N. Soil air sample storage and handling using polypropylene syringes and glass vials. Canadian J Soil Sci. 83 (5), 631-637 (2003).
- Sander, R. Compilation of Henry's law constants (version 4.0) for water as solvent. Atmos Chem Phys. 15 (8), 4399-4981 (2015).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- Comer-Warner, S. A., et al. Seasonal variability of sediment controls of carbon cycling in an agricultural stream. Sci Total Environ. 688, 732-741 (2019).
- U.S. Government Publishing Office. Title 42 - The Public Health and Wefare. U.S. Government Publishing Office. , (2009).
- Magen, C., et al. A simple headspace equilibration method for measuring dissolved methane. Limnol Oceanography Meth. 12 (9), 637-650 (2014).
- Regmi, B. P., Agah, M. Micro gas chromatography: An overview of critical components and their integration. Anal Chem. 90 (22), 13133-13150 (2018).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。