Case Report
单切口加单端口腹腔镜近端胃切除术联合双通道吻合术治疗胃癌
摘要
单切口加单端口腹腔镜近端胃切除术联合双通道吻合术最初用于近端胃癌的根治性切除术。这项研究证明了该程序的可行性,并为进一步的研究奠定了基础。
摘要
单切口加单端口腹腔镜近端胃切除术双通道吻合术 (SILT-DT) 是一种治疗近端胃癌的微创手术方法。该技术包括腹腔镜近端胃的全面切除术、淋巴结清扫术和双道吻合术。通过将单孔腹腔镜手术与辅助手术孔相结合,SILT-DT 降低了手术难度,同时促进了腹部引流管的放置。与传统的五孔腹腔镜胃切除术相比,SILT-DT 需要的端口更少,切口长度更短,有助于减轻术后疼痛并加快恢复速度。进行了全面的术前评估以确保手术成功,仔细考虑了肿瘤大小、分期、位置和患者 BMI 等因素。这种全面的评估有助于优化患者选择和手术计划。术后随访显示无明显并发症,强调了 SILT-DT 的安全性和有效性。这种创新技术为治疗近端胃癌提供了一种有前途的微创替代方案,同时保持了出色的临床结果。
引言
腹腔镜技术最近已成为胃癌手术治疗的主要方向之一 1,2。胃癌的常规腹腔镜手术主要使用 5 孔法进行。随着手术技术的进步和医疗设备的不断改进,缩小端口腹腔镜胃癌手术逐渐发展起来,以进一步减少手术创伤,最大限度地减少对腹腔的干扰,并加速术后恢复 3,4,5,6。
Omori7 于 2011 年首次报道了单孔腹腔镜远端胃癌手术。胃癌的纯单孔腹腔镜根治性胃切除术比传统的五孔腹腔镜胃切除术更困难。为了解决这个问题,在单孔腹腔镜手术中增加了一个辅助手术孔,这降低了手术的难度并促进了腹腔引流管的放置 8,9。单切口腹腔镜手术加单端口(SILS+1)是一种针对胃癌患者的微创技术,近年来因其端口数量减少和切口长度较短而广受欢迎。
目前,单孔腹腔镜或 SILS+1 胃癌手术在远端胃切除术中相对常见,而在全胃切除术中的应用较少。此外,尚未报道使用全腹腔镜双道胃癌吻合术。
基于此,我们首先尝试了单孔加单孔全腹腔镜近端胃切除术双道吻合术 (SILT-DT)。经脐口作为主手术口,左上腹引流口作为辅助手术口。该技术用于进行近端胃切除术、D2 淋巴结清扫术和双道吻合术以进行消化道重建。
案例介绍:
该患者是一名 63 岁的男性,在胃镜检查中发现食管胃交界处有肿瘤后被送入医院(图 1)。胃镜活检结果提示中分化腺癌(图2)。术前胸部和腹部增强 CT 扫描显示没有远处转移的证据(图3)。患者既往健康,无腹部手术史。
患者选择
如果患者经组织学证实为 Siewert II 型或 III 型胃食管交界处腺癌,且术前腹部 CT 显示胃周围没有淋巴结肿大或远处转移,则患者有资格参加。要求肿瘤的最大直径小于 3 cm,肿瘤下极与胃角的距离必须超过 5 cm。排除标准包括既往接受过腹部手术的患者、术前肿瘤直径超过 3 cm 和/或需要多脏器切除术的患者、接受过多学科团队 (MDT) 讨论的新辅助放化疗的患者,或接受过新辅助放化疗的患者,以及对腹腔镜手术不耐受的患者。
研究方案
该作遵循标准程序并获得了道德批准。本研究得到湖北文理大学附属襄阳市中心医院伦理委员会的批准。已获得患者的知情书面同意。研究内容和方法符合医学伦理规范和要求。研究中使用的试剂和设备列在 材料表中。
1. 术前步骤
- 指导患者在手术前 1 天口服磷酸钠盐进行肠道准备。患者禁食 8 h,手术前 2 h 内允许饮水。在进入手术室之前插入了一根上胃管。
- 患者处于仰卧分腿位,头部抬高并略微向右倾斜。
- 进行气管插管,并根据机构批准的方案进行全身麻醉。
2. 外科手术
- 在肚脐周围创建一个 3.0-3.5 厘米的横向切口,以插入配备四个内置穿刺器的 SILS 端口(图 4A)。在左上腹插入一个额外的 12 mm 套管针,作为手术器械的手术端口,包括超声剪切器、内窥镜线性吻合器和术后引流管。
- 用超声刀解剖第 1、2、3、4、7、8a、9 和 11p 组的脂肪淋巴组织(图 5A、B)。确保了大约 5-7 cm 的较低食管段长度(图 5C),并且保持了胃的大曲率和小曲率的自由度。
注意:SILT-DT 程序如图 5 所示。胃和淋巴结清扫术根据胃癌腹腔镜手术指南(2023 年版)10 进行。完成 D2 淋巴结清扫术和近端胃切除术。 - 建立食管空肠 (EJ) 吻合术。EJ 吻合部位在空肠上确定,距 Treitz 韧带远端 20 cm,靠近食管下部。EJ 吻合是通过左上象限的 12 毫米端口使用 60 毫米内窥镜线性吻合器完成的(图 5D)。
注意:说明消化道重建的示意图如图 4B 所示。 - 使用 60 毫米内窥镜线性吻合器切除食管标本并关闭空肠和食管之间的吻合口开口(图5E)。
- 创建胃空肠 (GJ) 吻合术,该部位标记在 EJ 吻合口远端 8-15 cm 的空肠上和剩余胃大曲率的后壁上(图 5F)。
- 空肠空肠吻合术成立。空肠空肠吻合术是使用 60 毫米内窥镜线性吻合器通过肚脐处 3.5 厘米的切口进行的,标记 GJ 吻合部位远端 5 厘米(图5G)。
- 单个吻合口被闭合并加强。GJ 吻合口和空肠空肠吻合口的公共开口均使用 3-0 micro Joe 线闭合。系膜裂孔用连续缝合闭合。
- 将引流管放置在 EJ 吻合口后面并从左上腹部流出(图 5H)。
3. 术后管理
- 术后实施水禁食,用留置袋排空胃管。
- 观察 48 小时后取出胃管,确保没有明显的血性引流液存在。
- 输液以维持水、电解质和酸碱平衡,同时抑制酸。预防性抗生素的持续时间限制为最长 48 小时。
- 术后 6-24 h 内积极促进早期活动。在恢复期间开始流质饮食 2-3 天。
- 评估吻合口瘘,并在第 7 天通过上消化道 X 线片评估残余胃的发展。
- 出院后 5 至 7 天内拔除腹腔引流管。
结果
手术在 150 min 内完成,术中出血量最小,为 5 mL。无短期并发症,患者术后恢复成功。共回收 24 个淋巴结,未发现淋巴结转移。手术时间为 150 min,估计失血量为 5 mL。患者卧床 2 天。首次排气时间为 70 h,患者在 3 天后开始食用流质食物和饮料。第 4 天拔除胃管,7 天内拔除引流管。造影剂在残胃中持续存在 30-50 分钟,没有反流到食道(图6)。术后腹部切口的美容效果令人满意 (图 4C)。疼痛通过 11 点数字评定量表 (NRS) 进行评估,其中 0 表示没有疼痛,10 表示可以想象到的最严重的疼痛11。患者的详细数据见 Table 1。
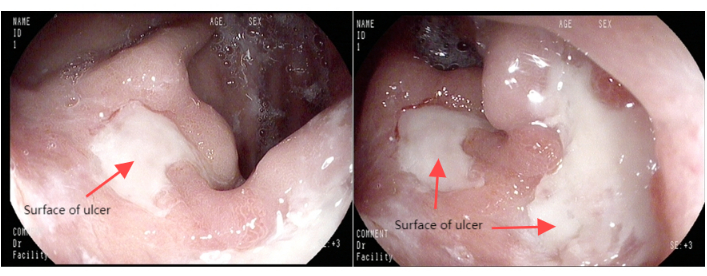
图 1:胃镜图像。 请单击此处查看此图的较大版本。
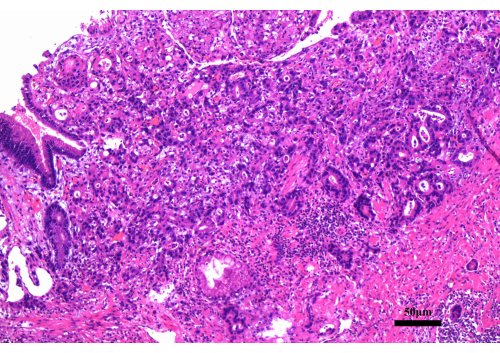
图 2:胃镜活检的结果。 胃镜活检显示中分化腺癌。比例尺:50 μm;放大倍率:200 倍。 请单击此处查看此图的较大版本。
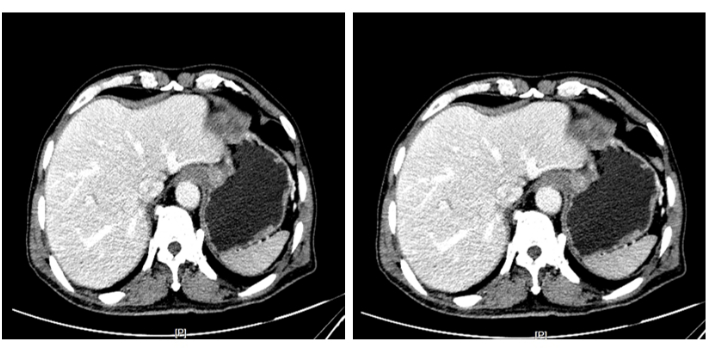
图 3:腹部增强 CT 扫描。 在贲门中观察到异质性增强,这被认为是肿瘤病变,肿瘤没有侵入肌肉层。 请单击此处查看此图的较大版本。
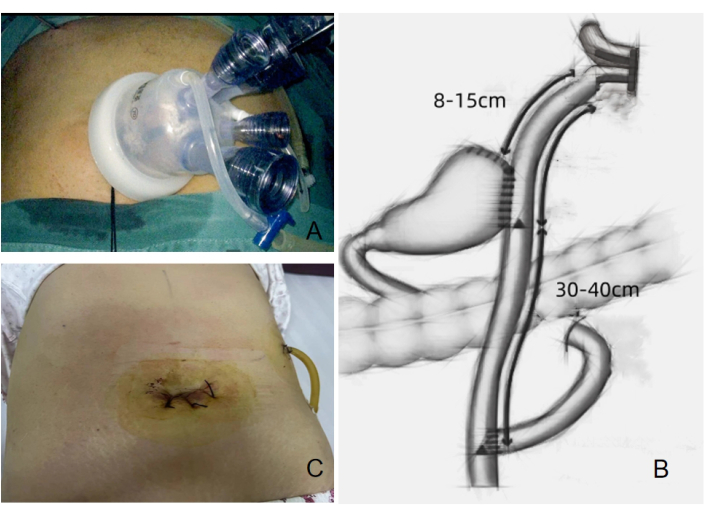
图 4:手术设置和术后伤口状况。 (A) 手术中使用的四个内置穿刺器。(B) 手术期间进行的双道吻合术。(C) 手术后显示的术后伤口状况。 请单击此处查看此图的较大版本。
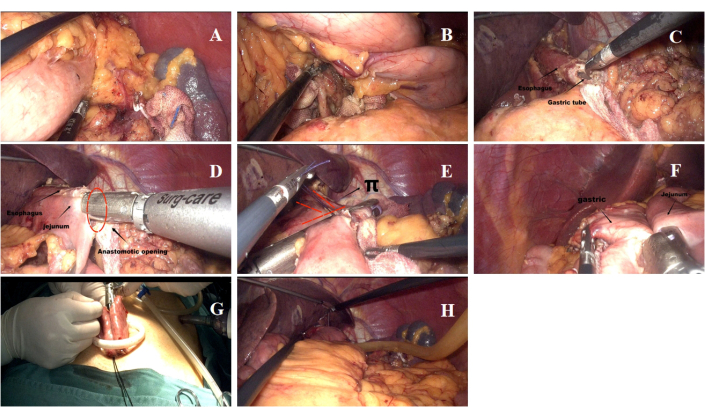
图 5:手术程序细节。 (A,B) 手术过程中清洁淋巴结的过程。(C) 食管横切和食管下端开口。(D) 作为吻合术的一部分进行左右食管空肠吻合术。(E) 关闭食管空肠吻合部位的公共开口。(F) 残余胃空肠吻合术完成。(G) 通过脐带切口进行的侧对侧肠吻合术。(H) 引流管的位置。 请单击此处查看此图的较大版本。
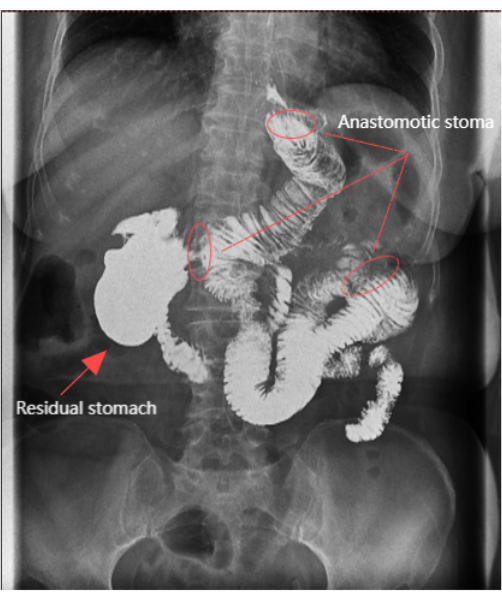
图 6:上消化道 X 光片。 上消化道 X 线检查显示吻合口是开放的,剩余的胃清晰可见。 请单击此处查看此图的较大版本。
| 项目 | 结果 |
| 性 | 雄 |
| 年 | 63 |
| 体重指数 (kg/m2) | 23.5 |
| 麻醉级 | 第三 |
| 术前 TNM 分期 | cT1N0M0 |
| 作时间 (min) | 150 |
| 切口长度 (cm) | 2.8 |
| 术中出血量 (mL) | 5 |
| 病理学 | 中分化腺癌 |
| 近端边缘的距离 (cm) | 3.4 |
| 远端边缘的距离 (cm) | 5.5 |
| 肿瘤大小 (cm) | 1.5*2*1.2 |
| 检索到的淋巴结数量 | 24 |
| TNM 分期 | pT2N0M0 |
| 手术后胃管拔除的持续时间 (d) | 4 |
| 到第一餐的持续时间 | 3 |
| 床上活动的持续时间 | 2 |
| 肠胃胀气的持续时间 (h) | 70 |
| 排便时间 (d) | 6 |
| 引流管的持续时间 (d) | 7 |
| 手术后第一天的疼痛评分 | 2 |
| 术后住院时间(天) | 8 |
| 并发症 | 没有 |
表 1:患者的围手术期数据。 有关患者围手术期数据的详细信息,包括关键测量值和结果。
讨论
单端口和减径腹腔镜根治性胃切除术已成为治疗胃癌的创新方法,并正在稳步获得认可。这些技术因其优点而受到越来越多的关注,包括改善美容效果、减少术后疼痛、降低手术部位感染的风险和更快的恢复时间。
涉及 343 例的 12 项研究结果表明,单端口和减径腹腔镜手术可有效治疗远端胃癌,占病例总数的大多数 3,4,12,13,14,15,16,17,18,19,20,21 .然而,只有 4 项研究侧重于全胃切除术 22,23,24,25。这些发现表明,由于手术难度高、需要广泛的解剖和淋巴结切除以及内窥镜消化道重建技术复杂,单孔胃癌手术,尤其是全胃切除术的临床研究和应用受到限制。
我们成功实施了第一例腹腔镜双道吻合术近端胃切除术,使用单切口加一个端口治疗近端胃癌。与传统手术方法相比,单切口加单孔手术更具微创性。相对于单端口技术,增加左上腹部端口提高了手术过程中的便利性,并允许通过左上腹部的切口合理放置引流管。
Lee 等人26 报道了 2016 年第一例针对早期胃癌的单孔腹腔镜近端胃切除术联合双道重建病例。与 SILS 相比,单切口加单端口手术包括一个额外的左上腹部端口,形成一个由脐带区域、左上腹部和手术区域组成的三角形结构。这种创新方法有效地解决了纯单切口手术的局限性,例如抗牵引和线性可视化不足。此外,它还增强了外科医生右手器械的灵活性,从而显着提高手术效率并降低全腹腔镜下每次吻合术的复杂性。
此外,多种策略可以提高运营效率并缩短手术时间。外科医生可以考虑在淋巴结清扫术和消化道重建过程中改变自己的位置,例如将自己定位在患者的左侧或患者的双腿之间,以优化手术区域的暴露。对于食管空肠吻合术和胃空肠吻合术等手术,建议一名助理或主任外科医生保持稳定姿势,而另一名助理或主任外科医生进行对接,从而提高吻合效率并最大限度地降低组织撕脱的风险。此外,建议使用集成的腹腔镜器械,以尽量减少光纤与其他器械之间的干扰。
综上所述,单切口加单孔腹腔镜近端胃切除术联合双通道吻合术治疗近端胃癌是可行的。在这种情况下,患者成功康复。手术微创,恢复更快。然而,该方案的局限性包括需要早期胃癌或良性胃肿瘤,患者的 BMI 不会过高。不建议将该方案应用于局部晚期疾病或高 BMI 患者,因为存在肿瘤切缘阳性的潜在风险和手术复杂性增加。该方案仍处于技术探索阶段,没有既定的指南,临床数据不足,无法充分验证其长期疗效。该协议的制定需要医疗机构的道德批准并严格遵守手术适应症。需要进一步的临床研究和探索来确定 SILT-DT 技术的临床适用性。
披露声明
作者没有需要披露的利益冲突或财务关系。
致谢
这项工作得到了湖北省卫生健康委员会科研项目和襄阳市医疗卫生领域科技重点项目 (2021YL15) 的资助。
材料
| Name | Company | Catalog Number | Comments |
| 3D laparoscope | KARL STORZ SE & Co. KG | 26605BA | |
| Absorbability surgical sutures | Johnson & Johnson | TLBJXZ | |
| Absorbable ligature clip | Hangzhou KANGJI Medical Instrument co., LTD | KJ-JZJ02ML | |
| Disposable puncture device | Hangzhou KANGJI Medical Instrument co., LTD | Type IV sets F | |
| Disposable step type endoscopic cutting stapler and nail bin | Nanjing Maidixin Medical Device Co.,Ltd | MLCR-Mb,MLCNC-60b-purple, MLCNC-45b-white | |
| laparoscopic instruments | Hangzhou KANGJI Medical Instrument co., LTD | ||
| Ultrasound knife | INNOLCON, Medical Science and Technology (suzhou) co., LTD |
参考文献
- Bray, F., et al. Global cancer statistics 2018: Globocan estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 68 (6), 394-424 (2018).
- Chevallay, M., et al. Cancer of the gastroesophageal junction: A diagnosis, classification, and management review. Ann N Y Acad Sci. 1434 (1), 132-138 (2018).
- Omori, T., et al. A randomized controlled trial of single-port versus multi-port laparoscopic distal gastrectomy for gastric cancer. Surg Endosc. 35 (8), 4485-4493 (2021).
- Kang, S. H., et al. Postoperative pain and quality of life after single-incision distal gastrectomy versus multiport laparoscopic distal gastrectomy for early gastric cancer - a randomized controlled trial. Surg Endosc. 37 (3), 2095-2103 (2023).
- Teng, W., et al. Short-term outcomes of reduced-port laparoscopic surgery versus conventional laparoscopic surgery for total gastrectomy: A single-institute experience. BMC Surg. 23 (1), 75 (2023).
- Podda, M., Saba, A., Porru, F., Pisanu, A. Systematic review with meta-analysis of studies comparing single-incision laparoscopic colectomy and multiport laparoscopic colectomy. Surg Endosc. 30 (11), 4697-4720 (2016).
- Omori, T., et al. Transumbilical single-incision laparoscopic distal gastrectomy for early gastric cancer. Surg Endosc. 25 (7), 2400-2404 (2011).
- Teng, W., et al. Comparison of short-term outcomes between single-incision plus one-port laparoscopic surgery and conventional laparoscopic surgery for distal gastric cancer: A randomized controlled trial. Transl Cancer Res. 11 (2), 358-366 (2022).
- Du, G. S., et al. Single-incision plus one-port laparoscopic gastrectomy versus conventional multi-port laparoscopy-assisted gastrectomy for gastric cancer: A retrospective study. Surg Endosc. 36 (5), 3298-3307 (2022).
- Chinese Society of Laparoscopic and Endoscopic Surgery, C. S. S., Chinese Medical Association, Association, R. a. L. S. C. O. C. R. H., Endoscopic and Robotic Surgical Society, C. a.-C. A., Endoscopy and Minimally Invasive Technology Society, C. a. O. M. E. Guideline for laparoscopic gastrectomy for gastric cancer (2023 edition). Chinese J Digest Surg. 22 (4), 425-436 (2023).
- Hjermstad, M. J., et al. Studies comparing numerical rating scales, verbal rating scales, and visual analogue scales for assessment of pain intensity in adults: A systematic literature review. J Pain Symptom Manage. 41 (6), 1073-1093 (2011).
- Park, D. J., Lee, J. H., Ahn, S. H., Eng, A. K., Kim, H. H. Single-port laparoscopic distal gastrectomy with d1+β lymph node dissection for gastric cancers: Report of 2 cases. Surg Laparosc Endosc Percutan Tech. 22 (4), e214-e216 (2012).
- Ahn, S. H., Jung, D. H., Son, S. Y., Park, D. J., Kim, H. H. Pure single-incision laparoscopic d2 lymphadenectomy for gastric cancer: A novel approach to 11p lymph node dissection (midpancreas mobilization). Ann Surg Treat Res. 87 (5), 279-283 (2014).
- Ahn, S. H., Son, S. Y., Jung, D. H., Park, D. J., Kim, H. H. Pure single-port laparoscopic distal gastrectomy for early gastric cancer: Comparative study with multi-port laparoscopic distal gastrectomy. J Am Coll Surg. 219 (5), 933-943 (2014).
- Kim, S. M., et al. Techniques of the single-port totally laparoscopic distal gastrectomy. Ann Surg Oncol. 22 (Suppl 3), S341 (2015).
- Jeong, O., Park, Y. K., Ryu, S. Y. Early experience of duet laparoscopic distal gastrectomy (duet-ldg) using three abdominal ports for gastric carcinoma: Surgical technique and comparison with conventional laparoscopic distal gastrectomy. Surg Endosc. 30 (8), 3559-3566 (2016).
- Kim, S. M., et al. Comparison of single-port and reduced-port totally laparoscopic distal gastrectomy for patients with early gastric cancer. Surg Endosc. 30 (9), 3950-3957 (2016).
- Lee, B., et al. Learning curve of pure single-port laparoscopic distal gastrectomy for gastric cancer. J Gastric Cancer. 18 (2), 182-188 (2018).
- Omori, T., et al. The safety and feasibility of single-port laparoscopic gastrectomy for advanced gastric cancer. J Gastrointest Surg. 23 (7), 1329-1339 (2019).
- Kang, S. H., et al. Long-term outcomes of single-incision distal gastrectomy compared with conventional laparoscopic distal gastrectomy: A propensity score-matched analysis. J Am Coll Surg. 234 (3), 340-351 (2022).
- Lee, S., et al. Intracorporeal modified delta-shaped gastroduodenostomy during 2-port distal gastrectomy: Technical aspects and short-term outcomes. Ann Surg Treat Res. 105 (3), 172-177 (2023).
- Ahn, S. H., Park, D. J., Son, S. Y., Lee, C. M., Kim, H. H. Single-incision laparoscopic total gastrectomy with d1+beta lymph node dissection for proximal early gastric cancer. Gastric Cancer. 17 (2), 392-396 (2014).
- Ertem, M., Ozveri, E., Gok, H., Ozben, V. Single incision laparoscopic total gastrectomy and d2 lymph node dissection for gastric cancer using a four-access single port: The first experience. Case Rep Surg. 2013, 504549 (2013).
- Lee, I. Y., Lee, D., Lee, C. M. Case report: Single-port laparoscopic total gastrectomy for gastric cancer in patient with situs inversus totalis. Front Oncol. 13, 1094053 (2023).
- Luo, Y., et al. A novel single-port robot for total gastrectomy to treat gastric cancer: A case report (with video). Asian J Endosc Surg. 17 (2), e13292 (2024).
- Lee, C. M., et al. Single-port laparoscopic proximal gastrectomy with double tract reconstruction for early gastric cancer: Report of a case. J Gastric Cancer. 16 (3), 200-206 (2016).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。