Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Topographische Schätzung von Visual Bevölkerung rezeptiven Felder von fMRI
In diesem Artikel
Zusammenfassung
It is important to obtain unbiased estimates of visual population receptive fields (pRFs) by functional magnetic resonance imaging. We use mild regularization constraints to estimate pRF topography without a-priori assumptions about pRF shape, allowing us to choose specific pRF models post-hoc. This is particularly advantageous in subjects with visual-pathway lesions.
Zusammenfassung
Sehrinde wird retinotop organisiert, so dass benachbarte Populationen von Zellen abzubilden, um benachbarte Teile des Gesichtsfeldes. Funktionelle Magnetresonanz-Bildgebung ermöglicht uns voxelbasierten Population rezeptiven Felder (PRF), dh zu schätzen, der Teil des Sichtfeldes, die die Zellen innerhalb jedes Voxel aktiviert. Vor, direkt, pRF Schätzmethoden 1 leiden unter gewissen Einschränkungen: 1) die pRF Modell ist a priori gewählt und können die tatsächlichen pRF Form nicht vollständig zu erfassen, und 2) pRF Zentren sind anfällig für Fehllokalisation der Nähe der Grenze des Stimulus Raum. Hier eine neue topographische pRF Schätzmethode 2 wird vorgeschlagen, die weitgehend umgeht diese Einschränkungen. Ein lineares Modell verwendet, um den Blutsauerstoffpegel-abhängiger (BOLD) Signal durch Faltung des linearen Antwort des pRF zur visuellen Stimulus mit der kanonischen hämodynamischen Antwortfunktion vorherzusagen. PRF Topographie wird als Gewichtsvektor, dessen Komponenten die str vertretenength der Gesamtreaktion der Voxel-Neuronen zu unterschiedlichen Gesichtsfeld Standorten präsentiert Reize. Die daraus resultierenden linearen Gleichungen können für die pRF Gewichtsvektor mit Firstregressions 3, was das pRF Topographie gelöst werden. Ein pRF Modell, das dem geschätzten Topographie angepassten können dann Post-hoc gewählt werden, so die Schätzungen der pRF Parameter wie pRF Stadtlage, pRF Ausrichtung, Größe, etc. zu verbessern. Mit der pRF Topographie vorhanden ermöglicht auch die visuelle Überprüfung der pRF Parameterschätzungen ermöglicht die Extraktion von verschiedenen pRF Eigenschaften, ohne a priori Annahmen über die pRF Struktur zu machen. Dieser Ansatz verspricht besonders nützlich für die Untersuchung der pRF Organisation von Patienten mit Störungen des visuellen Systems zu sein.
Einleitung
Die funktionelle Magnetresonanztomographie (fMRT) misst nicht-invasiv die funktionelle Organisation des visuellen Kortex auf makroskopischer Ebene (in der Regel in der Größenordnung von Millimetern). Frühe fMRI Retinotopie Studien eine Kohärenzmaßes zwischen Reiz Lage und löste BOLD Antworten 4-7. Diese Studien in der Regel nicht zu schätzen Bevölkerung rezeptiven Feld Größe. Später, Dumoulin und Wandell 1 ein Verfahren vorgeschlagen, eine solche Beschränkung durch die explizite Modellierung der pRF Lage und Größe, mit einer linearen Funktion des Modells, das BOLD Antwort vorhersagen zu überwinden. Allerdings ist eine Beschränkung dieser bahnbrechenden Verfahren, dass die parametrische pRF Modell muss a priori gewählt werden und kann zu fehlerhaften pRF schätzt, wenn sich herausstellt, nicht angemessen.
Um Einschränkungen des parametrischen pRF-Modell-Methode zu überwinden, wurden neue Methoden vor kurzem entwickelt worden. Diese Methoden direkt sagen die BOLD Antwort auf die stimulus durch die Rekonstruktion der PRF-Topographie. Ein von Greene und Kollegen vorgeschlagene Methode 8 rekonstruiert die pRF Topographie durch Rückprojektion der BOLD-Antworten auf die einzelnen 1D Reiz Flächen und den Bau der pRF Topographie in der 2D-Stimulus Raum wie ein typischer Computer-Tomographie-Technik. Andererseits ist die von uns vorgeschlagene Verfahren 2 direkt schätzt den 2D pRF Topographie unter Verwendung linearer Regression und Anlegen einer Regularisierung Technik. In diesem Verfahren wird die PRF Topographie als ein Satz von Gewichten, die durch den Stimulus, multipliziert wird, um den neuronalen Population Antwort eines gegebenen Voxels Abschätzung dargestellt. Dann wird der endgültige Sauerstoffgehalt des Blutes-Dependent (fett) Reaktion des Stimulus hervorgerufen durch Faltung des neuronalen Population Antwort und die kanonische hämodynamischen Antwortfunktion geschätzt. Um die unter beschränkte Linearsystem zu lösen, zusätzlich Firstregressions Regularisierung wird zur Kargheit durchzusetzen (siehe Abbildung 1unten). Die Regularisierung Technik unterdrückt Rauschen und Artefakte und ermöglicht unsere Methode, um die Topographie pRF robuster zu schätzen.
Die topographischen Methoden nicht pRF Form zu zwingen, eine bestimmte parametrische Form haben, und kann daher die tatsächliche pRF Struktur aufzudecken. Eine geeignete parametrische Modell kann dann auf der Basis der Topographie pRF gewählt werden. Beispielsweise kann die pRF Topographie verwendet, um die pRF Center- und Surround trennen, und dann können die anschließende pRF Zentrum Modellierung genauer zu sein, mit minimalem Einfluss von Surround-Unterdrückung sowie den Einfluss von anderen potenziellen Artefakte, die sich in Bereichen entfernt, um die werden pRF Zentrum. Wir haben vor kurzem durchgeführt, einen quantitativen Vergleich zwischen unseren Verfahren und verschiedene andere Verfahren, die direkt (dh vor der Schätzung der Topographie) fit isotropen Gaußschen 1, anisotrope Gaußsche und Differenz von isotropen Gauß an die pRF 9. Es wurde, dass der topogr gefundenO S-basierte Methode besser als diese Methoden im Hinblick auf pRF Zentrum Modellierung durch das Erreichen höherer erklärte Varianz des BOLD-Signal Zeitreihen.
Genaue Schätzung pRF Eigenschaften in verschiedenen Bereichen zeigt, wie sie das Sichtfeld abdecken, und ist wichtig für die Untersuchung der funktionellen Organisation des visuellen Kortex insbesondere in Bezug auf die visuelle Wahrnehmung. Eigenschaften wie, wie pRF Größenänderungen mit Exzentrizität 1,10 und pRF Surround-Center-Organisation 9 sind in der menschlichen Literatur studierte. Das vorgeschlagene Verfahren zum Schätzen der pRF Topographie führt zu genaueren pRF Parameter Modellierung und eher unbekannten Gesetzmäßigkeiten offenbaren, nicht leicht in den Direkt parametrischer Modelle modelliert a-priori. Dieser Ansatz wird besonders für das Studium pRF Organisation bei Patienten mit Sehbahnläsionen, für die pRF Struktur ist nicht unbedingt vorhersehbar a priori sein. Im Folgenden wird beschrieben, wie man schätzen, the pRF Topographie und wie man die Topographie verwenden, um die pRF Zentrum zu modellieren.
Protokoll
1. Datenerfassung
- Bereiten Sie einen Stimulus-Protokoll, das wirksam bei der Auslösung einer zuverlässigen retinotope visuelle Antwort wie zuvor in Dumoulin und Wandell 1 und Lee et al ist. 2. Jedoch sind auch andere etablierte Paradigmen auch anwendbar in Abhängigkeit von der spezifischen experimentellen Fragen angesprochen werden.
- Präsentieren bar Reize driften über den Bildschirm nacheinander entlang 8 Richtungen des Raumes, in Schritten von 45 Grad. Stellen Sie sicher, dass die Bewegung synchron mit Scanner Rahmen Erwerb (TR ~ 2 sec), so dass der Balken bewegt sich einen Schritt einmal eine fMRI Rahmen beginnt und bleibt an der neuen Position, bis der Rahmen endet.
- Um eine korrekte Ausgangssignal zu messen, fügen Epochen ohne Stimulation 1 bar.
- Definiert ein Sichtfeld (10 bis 15 ° Radius) in Sichtwinkel, über den der dargeboten wird. Präsentieren bewegenden oder flackerndes Schachbrettmuster (checker size = 0,94 x 0,94 Grad 2, pattern Aktualisierungsrate = 250 ms / Muster) in der Bar zu starken visuellen Reaktionen hervorrufen.
- Geben Sie die folgenden spezifischen Parameter: 8 gleichmäßig verteilte Bewegungsrichtungen, Breite bar gleich 1,875 ° und Bars zu bewegen um die halbe Strichbreite pro Bild (2 sec). Weitere Details finden sich in Lee et al. 2.
- Generieren Sie einen Ort (~ 0,25 °) in die Mitte des Bildschirms, auf dem die Augen der Person während des Experiments zu fixieren. Farbe des Spots ändern zufällig in der Zeit.
- Scannen Sie das Gehirn eines Subjekts in einem MRI-Scanner mit einem typischen Echo-Planar-Bildgebung (EPI) Scan, 192 Frames Dauer (24 Bilder in jede Bewegungsrichtung) hat. Wiederholen Sie die Scans 4-8 mal, um das Signal-Rausch-Verhältnis zu erhöhen.
- Stellen Sie die Parameter für den EPI-Sequenz wie folgt: TR = 2 sec, TE = 40 ms, Matrixgröße = 64 x 64, 28 Scheiben, Voxelgröße = 3 x 3 x 3 mm 3, Flip-Winkel = 90 °, alternativ gelten Sequenzen mit einer feineren Auflösung (z.g., 2 x 2 x 2 mm 3) oder ein Kurz TR (beispielsweise 1-1,5 sec), die ausschließlich die Sehrinde 2.
- Spur Augenbewegungen mit einem Augenverfolgungssystem während funktionellen Scans Fixierung sicherzustellen innerhalb 1-1,5 ° vom Fixationspunkt gehalten.
Anmerkung: Hier wird ein Kopf-Koordinate basierend Augenverfolger in einer Schutzbrille System verwendet wird, aber andere geeignete Augenverfolgungssysteme können stattdessen verwendet werden. - Weisen Sie die Themen, um die Stelle auf die Mitte des Bildschirms in Schritt 1.3.2 erzeugt fixieren. Um sicherzustellen, dass die Probanden fixiert, sie anweisen, die Farbveränderungen der Befestigungspunkt zu melden.
- Erhalten anatomischen Scans auf 1 x 1 x 1 mm 3 Auflösung (zB T1-MPRAGE; TR = 1900 ms, TE = 2,26 ms, TI = 900 ms, Flipwinkel = 9 °, 176 Partitionen).
ANMERKUNG: Diese anatomischen Scans zur Segmentierung sowie zum Ausrichten der funktionellen Bilder der Anatomie sowohl innerhalb der Abtastungen verwendet werden. Für eine bessere Ausrichtung zwischen Funktional (EPI) von Bildern und die Anatomie, erhalten auch eine inplane Anatomie Scans mit einer Auflösung identisch mit der EPI, mit T1-gewichteten schnell verdorben Gradientenecho (SPGR) Folge 1.
2. Datenvorverarbeitung
HINWEIS: Vor der Schätzung pRF Eigenschaften, einige typische fMRT-Daten vor, eine Bearbeitungsschritte benötigt werden, wie zum Beispiel Kopfbewegungskorrektur und die Ausrichtung der Funktionsvolumen der anatomischen Scan. In diesem Artikel werden alle Vorverarbeitung, Schätzung, Analyse und Präsentation der Ergebnisse erhalten werden unter Verwendung des Open-Source-MATLAB-basierte Software-Toolbox VISTA LAB auf der VISTA-Software zur Verfügung. http://white.stanford.edu/newlm/index.php/Main_Page.
- Laden Sie die anatomischen Scan in MATLAB und bereiten ein Volumen Anatomie mit einer Funktion namens createVolAnat.
- Segment graue Substanz, weiße Substanz und CSF mit der Funktion "ItkGray".
- Bereiten Funktionsdaten durch Umwandlung DICOM (dh , roh MRI-Dateiformat für Siemens) Dateien in NIfTI (dh Standard-funktionellen MRT-Format) -Dateien, und Laden von Daten in VISTA mit einer Funktion namens mrInit.
- Correct Kopf-Bewegung, und richten Funktionsaufnahmen der Anatomie in Schritt 2.1 mit rxAlign basierend auf einer affinen Matrix-Transformation geladen.
- Durchschnittliche funktionelle Bewegungskorrigierten Scans für die Verbesserung der Signal-zu-Rausch-Verhältnis, indem Sie auf mrVISTA Analyse Timeseries Durchschnittliche tseries. Ausschließen von durchschnittlich Scans, während der Augenbewegungen weicht von Fixierung mehr als 1 bis 1,5 °. Wenn Signale von verschiedenen Läufen unterschiedliche DC-Drifts, durchschnittliche Funktions Scans nach dem Entfernen der DC-Drifts.
- Berechnen Sie die Mapping-Koordinaten zwischen funktionalen Scans und graue Substanz und Bestimmung der entsprechenden Grau Sache Voxel in den funktionalen Scans, indem Sie die folgenden Menüs: mrVISTA Fenster öffnen Grau Fenster 3-View. Vergeben BOLD-Signale in der grauen Substanz Voxel durch Interpolation, die Wahl einer der Optionen einvailable in mrVISTA.
3. Die Einschätzung der pRF Topographie und Parametric Modeling
- Laden Sie sich die Code-Dateien über den folgenden Link: https://sites.google.com/site/leesangkyun/prf/codes.zip, extrahieren Sie die komprimierte Datei und legen Sie sie in einem bevorzugten Ort für den lokalen Computer. Fügen Sie den Pfad des Ordners, in MATLAB.
- Stellen Sie die Stimulationsparameter in das Experiment, indem Sie die folgenden Menüs: mrVISTA Analyse retinotope Modell Parameter einstellen. Geben Sie die folgenden Parameter wie Stimulus Bilder, Stimulus Größe, die kanonische hämodynamischen Funktion, die Bildrate der fMRI-Scanner.
- Vor der pRF Schätzung, bereiten die Anfangsparametersätze (Abbildung 1B).
- Stellen Sie die Kreuzvalidierung Sets in "tprf_set_params.m" aus den Codedateien. Teilen Sie Zeitreihen in mindestens zwei Teilmengen (ein Satz für die Prüfung und die verbleibenden Sätze für die Ausbildung), die lang genug für die Bar zu Swee sindp die ganze Reiz Raum. Alternativ ohne Mittelung Scans in Schritt 2.4, Validierung Scans durch das Weglassen von einem Scan zum Testen und mit den restlichen Scans für die Ausbildung.
- Stellen Sie eine grobe Parametersatz (λ in 1; λ = [10 -2 10 -1 1 10 1 10 2]) in "tprf_set_params.m". Stellen Sie dann eine feine Skalenbereich ([0,1 0,3 0,5 0,7 0,9 1 3 5 7 9]) in "tprf_set_params.m".
HINWEIS: Das Programm verwendet die Grob gesetzt, um den λ was zu den höchsten erklärte Varianz zu wählen. Dann sucht das Programm den Raum um den ausgewählten λ mit dem Feinmessbereich, weitere Verfeinerung der Auswahl von λ, die den höchsten erklärte Varianz ergibt. - Einen Schwellenwert (0,2) der erklärten Varianz für visuell ansprechende Voxel in "tprf_set_params.m".
HINWEIS: Diese Schwelle wird als Referenz für die Auswahl von visuell ansprechenden Voxel verwendet. Alternativ können Sie einROI für eine nicht-optisch ansprechenden Bereich (beispielsweise durch Ziehen einer Kugel mit einem Radius von 1 cm in einer nicht optisch ansprechenden Bereich des Gehirns), wobei der Schwellenwert automatisch berechnet werden. - Festlegen eines Satzes von Schwellenwerten ([0,3, 0,5, 0,7]) zum Definieren der pRF Mittelbereich in dem normalisierten Topographie "tprf_set_params.m" (dh, [0-1] oder [-1 bis 1] mit Epochen ohne bar Stimulations in Schritt 1.3.1).
HINWEIS: Aus dem Satz von Schwellenwerten das Programm vorgesehen wählt den "besten" Schwelle, dh die Schwelle, die eine pRF zentralen Region, für die das Zentrum pRF Modell erklärt die größte Signalvarianz definiert. Alternativ wählen Sie eine andere Menge von Schwellenwerten in Abhängigkeit von den Eigenschaften der Topographie.
- Ausführen "tprf_runpRFest.m" berechnen die pRF Topographie (1) entfernen und 2D anisotrope Gaußsche. Nach Angabe aller in diesem Protokoll beschriebenen Parameter, undAusführen des Codes, erhalten die endgültigen Schätzergebnisse.
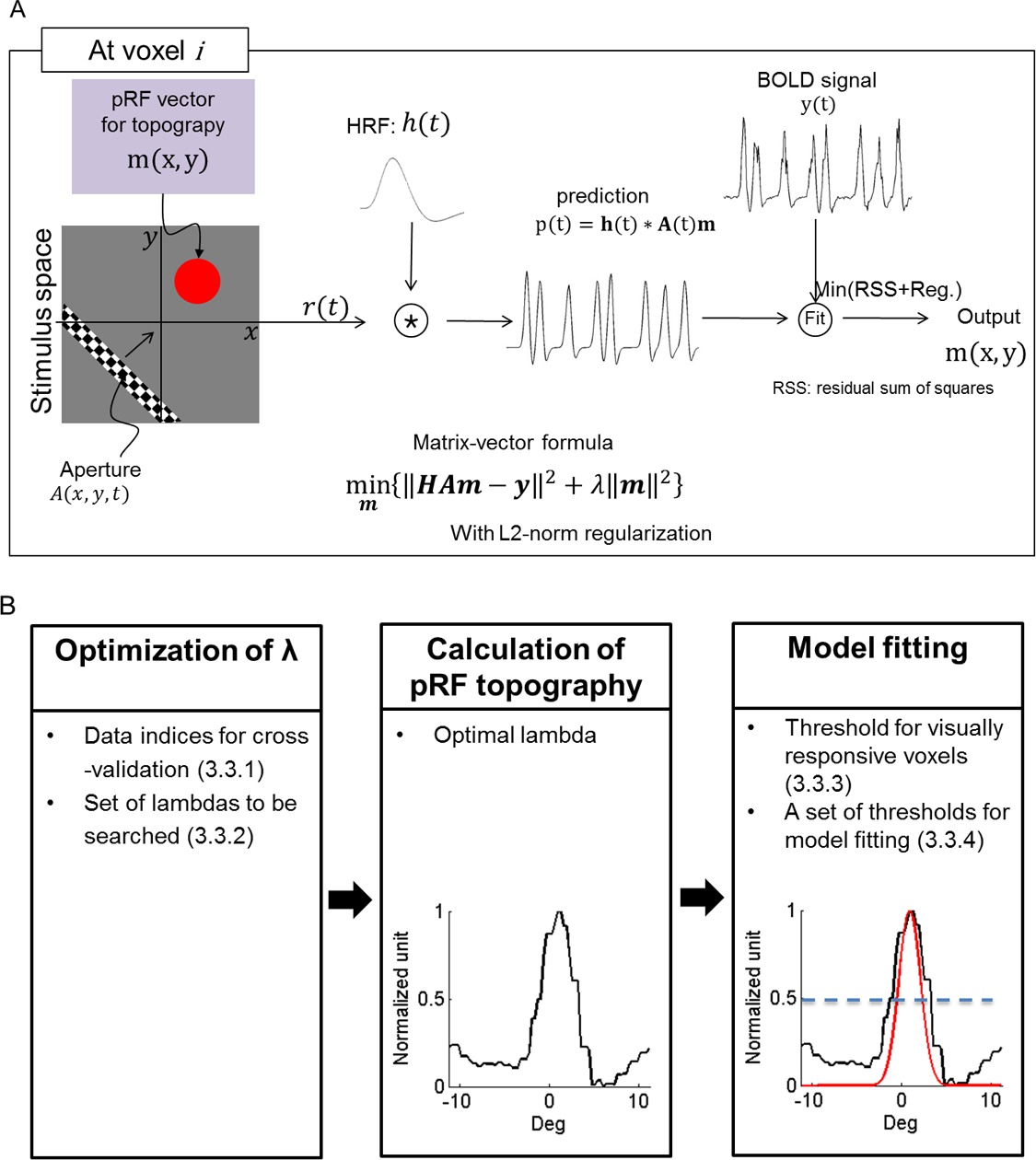
Abbildung 1: PRF Schätzverfahren. (A) Schematische Darstellung des Prozesses folgte für pRF Topographie Schätzung h (t):. Hämodynamischen Antwortfunktion A (t): Reiz, m: pRF, Reg. L2-Norm Regularisierung (B) Spezifische Schritte für pRF Topographie Schätzung und pRF Zentrum Modellierung. Die Menge der für die Bestimmung erforderlichen Parameter in jedem Schritt aufgelistet. Eine eindimensionale Abschnitt Topographie und sein Modell veranschaulicht. Unter "Modell Fitting", schwarze und rote Kurven stellen die Topographie und seiner pRF Zentrum-Modell mit einem Zentrum Schwelle von 0,5. Die blau gestrichelte Linie gibt einen Schwellenwert für die pRFZentralregion.
Ergebnisse
Genaue pRF Modellierung erfordert korrekt erfassen pRF Formen. Ohne Kenntnis der pRF Topographie, die Auswahl der kreissymmetrische Modelle in früheren Studien verwendet 1,9-11 ist eine vernünftige Wahl. Dies ist, weil, wenn die lokale retinotopic Organisation ist in allen Richtungen des Gesichtsfeldes homogen, könnte eine lokale Bevölkerung Antwort als eine kreissymmetrische kumulativen Summe von neuronalen Antworten dargestellt werden. Jedoch haben unsere Beobachtungen zeigen, dass dies nicht unbedingt ...
Diskussion
Dieser Artikel beschreibt, wie die Topographie der visuellen Bevölkerung rezeptiven Felder im menschlichen visuellen Kortex und wie man es benutzt, um eine geeignete parametrisches Modell für die rezeptiven Feld auswählen zu schätzen. Für eine erfolgreiche Retinotopie sollte eine geeignete Stimulationsprotokoll und eine effiziente Analyseverfahren ausgewählt werden, und Versuchsparameter des Subjekts (Bewegung und Fixierung) optimiert werden. Bar Reize Ablauf eines ganzen Gesichtsfeld sind eine effiziente Anregung...
Offenlegungen
The authors declare that they have no competing financial interests.
Danksagungen
We thank the VISTA software group (Brian Wandell and associates, at Stanford).
S. S. was supported by McNair 2280403105,NEI R01-EY109272, and NEI R01-EY024019 and as HHMI Early Carrer Award. A. P. and G. K. was supported by the Max-Planck Society, G. K. was supported by the PLASTICISE project of the 7th Framework Programme of the European Commission, Contract no. HEATH-F2-2009-223524.
Materialien
| Name | Company | Catalog Number | Comments |
| MRI scanner | Siemens/Philips/GE | ||
| MATLAB | The Mathworks, Inc. | http://www.mathworks.com | |
| VISTA software | VISTA software group | http://white.stanford.edu/newlm/index.php/Software | |
| PsychoToolbox | PsychoToolbox | http://psychtoolbox.org | |
| Eye Tracker (VisuaStimDigital) | Resonance Technology Inc | http://mrivideo.com/ |
Referenzen
- Dumoulin, S. O., Wandell, B. A. Population receptive field estimates in human visual cortex. Neuroimage. 39, 647-660 (2008).
- Lee, S., Papanikolaou, A., Logothetis, N. K., Smirnakis, S. M., Keliris, G. A. A new method for estimating population receptive field topography in visual cortex. Neuroimage. 81, 144-157 (2013).
- Hastie, T., Tibshirani, R., Friedman, J. H. . The elements of statistical learning : data mining, inference, and prediction. , (2009).
- Sereno, M. I., et al. Borders of multiple visual areas in humans revealed by functional magnetic resonance imaging. Science. 268, 889-893 (1995).
- Engel, S. A., Glover, G. H., Wandell, B. A. Retinotopic organization in human visual cortex and the spatial precision of functional MRI. Cereb Cortex. 7, 181-192 (1997).
- Engel, S. A., et al. fMRI of human visual cortex. Nature. 369, 525 (1994).
- DeYoe, E. A., et al. Mapping striate and extrastriate visual areas in human cerebral cortex. Proc Natl Acad Sci U S A. 93, 2382-2386 (1996).
- Greene, C. A., Dumoulin, S. O., Harvey, B. M., Ress, D. Measurement of population receptive fields in human early visual cortex using back-projection tomography. J Vis. , (2014).
- Zuiderbaan, W., Harvey, B. M., Dumoulin, S. O. Modeling center-surround configurations in population receptive fields using fMRI. J Vis. , (2012).
- Harvey, B. M., Dumoulin, S. O. The relationship between cortical magnification factor and population receptive field size in human visual cortex: constancies in cortical architecture. J Neurosci. 31, 13604-13612 (2011).
- Haak, K. V., Cornelissen, F. W., Morland, A. B. Population receptive field dynamics in human visual cortex. PLoS One. 7, e37686 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten