Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Z-Scores zur Beurteilung der ovariellen Reserve bei jungen Patientinnen, die sich einer Fertilitätserhaltung unterziehen
In diesem Artikel
Zusammenfassung
Das vorliegende Protokoll beschreibt ein Verfahren zur Beurteilung der ovariellen Reserve bei Patientinnen unter 25 Jahren, die eine Fertilitätserhaltung durch Kryokonservierung des Ovarialgewebes benötigen. Diese Methode umfasst: (1) die histologische Beurteilung der ovariellen Reserve in kortikalen Proben, (2) den Vergleich mit einem Referenzdatensatz und (3) die Berechnung von Z-Scores.
Zusammenfassung
Frauen werden mit einem nicht erneuerbaren Pool von Eierstockfollikeln geboren, der als Eierstockreserve bezeichnet wird. Diese Reserve besteht aus primordialen Follikeln in den Eierstöcken und kann von vielen Faktoren beeinflusst werden, wie z. B. genetischen und endokrinen Störungen, medizinischen Eingriffen und endokrinen Disruptoren. Die Erhaltung der Fruchtbarkeit wird empfohlen, wenn gonadotoxische Behandlungen erforderlich sind. Die bevorzugten Optionen für Frauen sind die Kryokonservierung von Eizellen und Embryonen. Bei sehr jungen, sexuell unreifen Patientinnen ist die Kryokonservierung des Eierstockgewebes jedoch die einzige Option. Die Kenntnis der Follikeldichte von kryokonservierten Gewebeproben ist für die Kinderwunschberatung für junge Patientinnen unerlässlich. Dieses Protokoll zeigt die Verwendung von Z-Scores für die kortikale Follikeldichte als Instrument zur Bewertung der Qualität des Eierstockgewebes bei Mädchen und jungen Frauen im Alter von 25 Jahren und darunter, die sich einer Fertilitätserhaltung unterziehen. Die Follikeldichte in Patientenproben wird mit altersnormalisierten Referenzstandards verglichen, die von Hassan et al. entwickelt wurden, um mögliche Abweichungen vom Standard abzuschätzen. Die Follikeldichte wird durch histologische Quantifizierung gemessen. Zu diesem Zweck wird ein kleines Stück kortikales Gewebe der Eierstöcke (~2 mm x 2 mm x 2 mm) entweder in Bouin- oder Formaldehydlösung fixiert, in Paraffin eingebettet, bei einer Dicke von 4 μm geschnitten, mit Hämatoxylin und Eosin gefärbt und mit einem Objektträgerscanner digitalisiert. Die in der Hirnrinde vorhandenen Follikelstadien reichen von den primordialen bis zu den primären Follikeln. Der kortikale Bereich war in histologischen Schnitten 1 mm vom Oberflächenepithel entfernt. Die Follikeldichte wird unter Verwendung einer modifizierten Formel von Schmidt et al. berechnet, und der Z-Score wird anhand des Referenzmittelwerts und der Standardabweichung bestimmt. Der Z-Wert gibt an, wie stark der gemessene Wert vom Referenzmittel abweicht, und bestimmt die reduzierte (<-1,7 Z-Wert) ovarielle Reserve. Mit dieser Methode können Follikeldichten als wertvolles Maß für die ovarielle Reserve für junge Patientinnen verwendet werden, die eine Fertilitätserhaltung benötigen.
Einleitung
Der Eierstock ist ein dynamisches, endokrinologisch aktives Organ, das aus einer äußeren Rinde und einer inneren Medulla besteht. Heterogen in den Eierstöcken verteilt sind Follikel, die die gonadale Eizelle enthalten, die von stromalen Granulosazellen umgeben ist1. Alle Follikel werden bereits während der Entwicklung des Fötus gebildet und erreichen ihren Höhepunkt in der 20. Schwangerschaftswoche, gefolgt von einem exponentiellen Rückgang. Bei der Geburt verbleiben 1-2 Millionen Primordialfollikel in der Hirnrinde, und nur wenige hunderttausend Follikel überleben bis zur Pubertät2. Der nicht wachsende Follikelpool, der auch als ovarielle Reserve bezeichnet wird, beeinflusst unter anderem die Fruchtbarkeit einer Frau. Die Eierstockreserve befindet sich in der Rinde und wandert in die Medulla, wenn die Follikel wachsen und reifen. Einige Forscher gehen davon aus, dass die ovarielle Reserve nur aus primordialen Follikeln besteht, während andere alle unilaminaren Follikel (d. h. primordiale, intermediäre und primäre) umfassen3,4,5,6. Im Laufe des Lebens einer Frau reifen nur 300-400 Follikel heran und überleben, um schließlich den Eisprung zu durchlaufen. Die Menopause beginnt, wenn die Follikelzahl auf etwa tausend sinkt, was typischerweise im Alter von etwa 50 Jahren der Fall ist 2,7. Derzeit gibt es eine anhaltende Debatte über das Vorhandensein von Eizellstammzellen (OSCs) in adulten menschlichen Eierstöcken, die nach einer Xenotransplantation Eizellen bilden können. Einige Studien deuten darauf hin, Zellen zu isolieren, die ein Genprofil primitiver Keimzellen exprimieren und sich zu Eizellen differenzieren 8,9, während andere darauf hinweisen, dass es sich bei den angeblichen OSCs um perivaskuläre Zellen der Blutgefäße handelt 10,11,12.
Die vorzeitige Ovarialinsuffizienz (POI) ist definiert als das Abbrechen des Menstruationszyklus mit erhöhten FSH-Werten vor dem 40. Lebensjahr13. Die Ursachen für POI sind multifaktoriell und können idiopathisch auftreten; Sie entsteht jedoch häufig als Folge von Erkrankungen14. Zum Beispiel sind bestimmte angeborene genetische Erkrankungen aufgrund einer reduzierten Eierstockreserve bereits bei der Geburt mit POI verbunden, wie z. B. das Turner-Syndrom15. POI kann auch als Nebenwirkung gonadotoxischer Behandlungen auftreten, was besonders bei sehr jungen Patientinnen problematisch ist, da es zu einer Unfähigkeit führen kann, eine normale Pubertät zu durchlaufen und die Eierstockreserve drastisch zu beeinträchtigen. Abhängig vom Risiko eines POI und dem Alter der Patientin stehen verschiedene Optionen zur Erhaltung der Fruchtbarkeit zur Verfügung, wie z. B. die Kryokonservierung reifer Eizellen, die Kryokonservierung von Embryonen nach der In-vitro-Fertilisation und die Kryokonservierung von Eierstockgewebe (OTC). Für präpubertäre Patienten ist OTC aufgrund ihrer sexuellen Unreife die einzige praktikable Option16,17. In den Vereinigten Staaten wurde die Erhaltung der Fruchtbarkeit durch OTC in letzter Zeit als akzeptable klinische Routine angesehen18. In vielen europäischen Ländern gilt OTC jedoch immer noch als experimentell, und insbesondere für die Autotransplantation ist eine ethische Zulassung erforderlich19,20. Daher müssen die Einschlusskriterien für OTC-Protokolle sorgfältig abgewogen werden, und für jeden Patienten sollte eine Nutzen-Risiko-Analyse durchgeführt werden. Nicht alle Kinder, die gonadotoxische Therapien erhalten, kommen für eine Fertilitätserhaltung in Frage. In Schweden wird nur Patienten mit hohem oder sehr hohem Risiko empfohlen, sich einer Fertilitätserhaltung gemäß den Leitlinien zur Fertilitätserhaltung der Nordischen Gesellschaft für pädiatrische Hämatologie und Onkologie21 zu unterziehen. Zu dieser Gruppe gehören (1) prä- und postpubertäre Kinder, die eine Stammzelltransplantation benötigen oder eine Strahlentherapie mit dem Eierstock im Bereich der Reichweite erhalten, und (2) postpubertäre Kinder mit hohen kumulativen Dosen einer alkylierenden Chemotherapie. Bei Mädchen vor der Menarche gehören zu den Einschlusskriterien für ein sehr hohes Unfruchtbarkeitsrisiko solche, die mit einem der folgenden Mittel behandelt wurden: Strahlendosis >10 Gy für den Eierstock oder allogene oder autologe hämatopoetische Stammzelltherapie (HSCT). Ausschlusskriterien sind Personen, die vor der Operation zusätzliche Blutprodukte für andere gerinnungshemmende Präparate benötigen oder eine Neutrophilenzahl <1 aufweisen. Bei Mädchen/Frauen nach der Menarche umfassen die Einschlusskriterien für ein hohes oder sehr hohes Risiko für Unfruchtbarkeit diejenigen, die mit einem der folgenden Mittel behandelt wurden: Strahlendosis >10 Gy für den Eierstock oder allogene HSCT, Cyclophosphamid >9 g/m², Ifosfamid >60 g/m², Procarbazin oder Nitrosoharnstoffe (BCNU/CCNU) >360 mg/m². Zu den Ausschlusskriterien gehören Personen mit einem erhöhten Blutungsrisiko, einem erhöhten Infektionsrisiko, einem erhöhten Risiko für chirurgische Komplikationen oder einem erhöhten Risiko für Schmerzprobleme, die vom behandelnden Arzt beurteilt werden.
Bei OTC wird Eierstockgewebe bei Bauchoperationen durch Laparotomie oder Laparoskopie durch einseitige Oophorektomie oder Biopsie entnommen. Das Mark wird aus dem gesammelten Eierstockgewebe entfernt, und die verbleibende Rinde wird dann in kleinere Fragmente geschnitten, um sie durch kontrolliertes Einfrieren oder Vitrifikation für die spätere Verwendung bei der Wiederherstellung der Fruchtbarkeit zu kryokonservieren22. Die Proben werden dann in flüssigem Stickstoff gelagert, bis sich die Patientin von ihrer Behandlung erholt hat und eine Familie gründen möchte. Abhängig von der Art der Krebserkrankung und in Ermangelung von Kontraindikationen für eine Transplantation von Eierstockgewebe wird das Gewebe dann aufgetaut und autotransplantiert, um die Hormon- und Eierstockfunktion wiederherzustellen. OTC hat sich als erfolgreich erwiesen, mit einer Schwangerschaftsrate von 50 % und mehr als 200 Lebendgeburten nach Transplantation von kryokonserviertem Eierstockgewebe, das im Erwachsenenalter entnommen wurde 23,24,25. Es wurden nur wenige Lebendgeburten nach Autotransplantation von Eierstockgewebe berichtet, das in der Kindheit entnommen wurde, und nach einer Autotransplantation von zweifellos präpubertärem Eierstockgewebe wurde keine berichtet 26,27,28,29,30. Die Qualität des Gewebes ist eine Voraussetzung für eine erfolgreiche Wiederherstellung der Fruchtbarkeit31. Daher ist es wichtig, die Qualität der entnommenen Gewebeproben zu untersuchen.
Derzeit kann die Qualität des Eierstockgewebes durch histologische Schnitte und manuelle Zählung der Follikel abgeschätzt werden. Die Beurteilung der Normalität der Follikeldichte ist jedoch aufgrund des natürlichen Rückgangs der Reserve mit zunehmendem Alter und der heterogenen Verteilung der Follikel schwierig. Darüber hinaus ist der Vergleich mit Referenzwerten eine Herausforderung, da diese nicht für Biopsiegröße und -alter standardisiert sind. Andere Bestimmungsoptionen, wie z. B. AMH-Serumspiegel oder die Färbung von verdauter Gewebe mit Calcein oder Neutralrot, sind entweder nicht gut etabliert oder haben ihre eigenen Einschränkungen. Wallace und Kelsey veröffentlichten zuvor ein Modell der normalen Eierstockreserve über das Alter, indem sie Daten über die Follikelzahl ganzer Eierstöcke von Patientinnen ohne bekannte Eierstockpathologien sammelten2. Da Biopsien nicht repräsentativ für den gesamten Eierstock sind, entwickelten Schmidt et al. eine Methode zur Abschätzung der Gesamtzahl der Follikel auf der Grundlage von kortikalen Biopsien32. Unter Verwendung einer modifizierten Version dieser Methode und des Modells der normalen ovariellen Reserve wurde ein Referenzdatensatz für die Follikeldichte von Frauen im Alter von 0-25 Jahren erstellt33.
In diesem Artikel wird die Strategie zur Beurteilung der Normalität der Follikeldichte anhand kleiner ovarieller Proben durch (1) direkte Quantifizierung der Follikel mittels Histologie und (2) Vergleich der Ergebnisse mit altersnormalisierten Standardreferenzen über Z-Scores beschrieben. Die Verwendung von Z-Scores beschreibt das Verhältnis der Follikeldichte einer Ovarialbiopie zu einem alters- und größenstandardisierten Referenzgruppenmittelwert. Dies wird für Ärzte von großem Wert sein, wenn sie ihre Patienten für eine Autotransplantation und die weitere Behandlung nach Erhalt der Fruchtbarkeit beraten.
Protokoll
Alle durchgeführten Verfahren wurden von der schwedischen Ethikprüfungsbehörde (Sveafertil-Patienten, Dnr: 2019-03802) und von der Ethikkommission des Universitätskrankenhauses Helsinki (HCH-Patienten, Dnr 340/13/03/03/2015) genehmigt. Schriftliche und mündliche Informationen über die Studie wurden von den Forschungsschwestern zur Verfügung gestellt, und es wurde eine Einverständniserklärung gemäß der Erklärung von Helsinki eingeholt. Für Patienten unter 18 Jahren wurde die Einverständniserklärung der Erziehungsberechtigten eingeholt. Alle Proben wurden pseudonymisiert und gemäß der europäischen Datenschutz-Grundverordnung (DSGVO) verarbeitet. Die Einzelheiten zu den in dieser Studie verwendeten Reagenzien und Geräten sind in der Materialtabelle aufgeführt.
1. Entnahme und Verarbeitung von Eierstockgewebe
HINWEIS: Identifizieren Sie alle Patienten, die für eine Fertilitätserhaltung in Frage kommen, wenn eine Indikation für ein hohes oder sehr hohes Risiko für Unfruchtbarkeit gemäß den lokalen Richtlinien (z. B. nordische, europäische oder internationale spezifische Leitlinien) besteht. In Europa sollten minderjährige Patienten nur im Rahmen von Forschungsprogrammen zur Erhaltung der Fruchtbarkeit rekrutiert werden. Bestimmen Sie das Risiko einer Unfruchtbarkeit anhand der Richtlinien Ihres Landes zur Erhaltung der Fruchtbarkeit.
- Führen Sie den chirurgischen Eingriff unter Vollnarkose durch. Verabreichen Sie intravenös Propofol (2 mg/kg), Sufentanil (0,5 Mikrogramm/kg) und Rocuroniumbromid (0,6 mg/kg) zur Einleitung der Anästhesie.
- Intubieren und beatulieren Sie den Patienten mit einem Tidalvolumen von 6-8 ml/kg und einem positiven exspiratorischen Druck von 6-8 cm H2O. Geben Sie Sevofluran 1 % bis 2 % über den Endotrachealtubus ab, um die Inhalationsanästhesie aufrechtzuerhalten.
- Aufrechterhaltung einer neuromuskulären Blockade mit Rocuroniumbromid (0,15 mg/kg) während des chirurgischen Eingriffs, um eine angemessene Muskelentspannung zu gewährleisten und eine Laparoskopie bei niedrigerem intraabdominalem Insufflationsdruck zu ermöglichen.
- Verwenden Sie den bispektralen Index, um die Narkosetiefe zu steuern und ein schnelles Erwachen mit einer reduzierten Anästhesiedosis zu ermöglichen. Antagonisieren Sie den verbleibenden neuromuskulären Block mit Sugammadex (2-4 mg/kg).
- Mit einer Drei-Port-Technik wird ein 10-mm-Trokar in die Peritonealhöhle am Nabel eingeführt, um eine optische Linse mit aufgesetzter Kamera einzuführen, und zwei 5-mm-Trokare in der linken und rechten Beckenregion (2 cm oberhalb und 2 cm medial der jeweiligen vorderen oberen Beckenwirbelsäule) unter direkter Sicht für die chirurgische Instrumentierung und die Gewebeentnahme. Untersuchen Sie die Beckenorgane, einschließlich beider Eierstöcke, um die Normalität zu bestätigen.
- Identifizieren Sie den Eierstock, der am einfachsten zu erreichen ist, und fassen Sie ihn dann. Schneiden Sie ein Volumen ab, das etwa ein Drittel des Eierstocks ausmacht (oder wie in Ihrer ethischen Erlaubnis angegeben), und verwenden Sie dann, falls erforderlich, Diathermie, um die Blutstillung zu sichern.
HINWEIS: Führen Sie die Biopsie nur durch, wenn keine Kontraindikationen vorliegen, wie z. B. Risikofaktoren für übermäßige intra- oder postoperative Blutungen oder ein erhöhtes Infektionsrisiko. Geben Sie klar an und befolgen Sie die Ein- und Ausschlusskriterien des Landes. Der gesamte Eierstock kann entnommen werden, wenn das Risiko einer Unfruchtbarkeit sehr hoch ist und/oder das Risiko, nur einen Teil abzuschneiden, als zu hoch angesehen wird (z.B. aufgrund von Blutungen). Vermeiden Sie die Verwendung von Diathermie vor der Entnahme der Probe, da dies das Gewebe schädigen kann.
- Identifizieren Sie den Eierstock, der am einfachsten zu erreichen ist, und fassen Sie ihn dann. Schneiden Sie ein Volumen ab, das etwa ein Drittel des Eierstocks ausmacht (oder wie in Ihrer ethischen Erlaubnis angegeben), und verwenden Sie dann, falls erforderlich, Diathermie, um die Blutstillung zu sichern.
- Im Operationssaal wird das Gewebe in ein Röhrchen gegeben, das 5 mL Dulbecco's Phosphate Buffer Saline (PBS) mit CaCl2, MgCl2, 1 g/L D-Glucose, 36 mg/L Pyruvat enthält, entweder auf 37 °C erwärmt, wenn die Probe sofort im Labor verarbeitet wird (innerhalb von 30 min) oder während längerer Transporte (bis zu 24 h) bei 4 °C gehalten wird.
HINWEIS: Zu den Transportlösungen gehören eine Reihe von kommerziell erhältlichen Organtransport-/Perfusionslösungen sowie einfache Puffer wie PBS und MEM34. - Schneide ein kleines Stück des Eierstockgewebes (2 mm x 2 mm x 2 mm) von der Oberfläche des Eierstocks ab. Dieses Stück enthält die Hirnrinde, d. h. den äußeren Teil des Eierstocks, in dem sich die Eierstockfollikel befinden35.
VORSICHT: Behandeln Sie menschliches Gewebe wie den Eierstock unter Verwendung von Praktiken und Verfahren der Biosicherheitsstufe 2.
HINWEIS: Eine spezialisierte Abteilung für Reproduktionsmedizin konserviert klinisch den Rest des Eierstockgewebes für eine mögliche zukünftige Verwendung bei der Wiederherstellung der Fruchtbarkeit der Patientinnen. - Legen Sie das Gewebe 2 h lang in 350 μl Bouin-Lösung bei Raumtemperatur oder über Nacht in 350 μl 4%iges Formaldehyd bei 4 °C, wobei Sie darauf achten, dass das Gewebe vollständig eingetaucht ist. Waschen Sie das Gewebe nach der Inkubation dreimal mit 70% Ethanol.
- Für die Bouin-Lösung waschen, bis die gelbe Farbe verschwindet. Das Gewebe wird in Paraffinwachs36 einbettet. Schneiden Sie mindestens 30 serielle Gewebeschnitte mit einer Dicke von 4 μm und legen Sie sie auf Objektträger.
ACHTUNG: Behandeln Sie die Bouin-Lösung und Formaldehyd in einer Chemikalienhaube und mit geeigneter Schutzausrüstung.
HINWEIS: Formaldehyd kann zu schrumpfungsbedingten Artefakten im Gewebe führen. Die Lösung von Bouin ist daher die bevorzugte Wahl für die Konservierung der Histologie. Die Lösung von Bouin birgt jedoch zusätzliche Risiken, was dazu führt, dass mehrere Institutionen die Verwendung von Formaldehydbevorzugen 37.
- Für die Bouin-Lösung waschen, bis die gelbe Farbe verschwindet. Das Gewebe wird in Paraffinwachs36 einbettet. Schneiden Sie mindestens 30 serielle Gewebeschnitte mit einer Dicke von 4 μm und legen Sie sie auf Objektträger.
2. Hämatoxylin- und Eosin-Färbung (H&E)
- Wiegen Sie 5 g Eosin-Y-Pulver in eine 100-ml-Flasche aus autoklaviertem Glas. Fügen Sie 800 ml 95%iges Ethanol und 200 ml entionisiertes Wasser hinzu, um eine 0,5%ige Eosin-Stammlösung herzustellen. Bereiten Sie eine 0,25%ige Eosin-Arbeitslösung vor, indem Sie 200 ml der 0,5%igen Eosin-Stammlösung mit 160 ml 100%igem Ethanol, 1 ml Essigsäure und 40 ml deionisiertem Wasser verdünnen.
HINWEIS: Das Pulver löst sich möglicherweise nicht vollständig auf. Filtern Sie die Lösung vor Gebrauch, um den Niederschlag zu reduzieren. - Legen Sie die Objektträger in die Regale. Tauchen Sie das Gestell mit den Objektträgern in der folgenden Reihenfolge in die entsprechenden Behälter: 15 min in Xylol, 5 min in 100 % Ethanol, 10 Mal in 70 % Ethanol, 10 Mal in 50 % Ethanol tauchen und dann 10 Mal in entionisiertes Wasser tauchen.
- Tauchen Sie das Gestell mit den Objektträgern 3 Minuten lang in Hämatoxylinlösung und geben Sie dann das Gestell mit den Objektträgern für 30 s in einen Behälter mit destilliertem Leitungswasser, um überschüssige Hämatoxylinflecken zu entfernen.
- Stellen Sie das Gestell mit den Objektträgern für 1 Minute in einen Behälter mit Differenzierungslösung (1 ml 37 % HCl zugesetzt zu 100 ml 70 % Ethanol), dann übertragen Sie das Gestell mit den Objektträgern für 30 s in einen Behälter mit destilliertem Leitungswasser.
HINWEIS: Stellen Sie sicher, dass die Gewebeabschnitte in die Flüssigkeit eingetaucht sind. Geben Sie bei Bedarf mehr Reagenz in den Behälter. Wechseln Sie das Xylol nach jeweils 5 Anwendungen, wenn Sie große Mengen färben. Bereiten Sie 50 % Ethanol vor, indem Sie 70 % Ethanol verdünnen (z. B. fügen Sie 35 ml 70 % Ethanol zu 15 ml DPBS hinzu, um 50 ml 50 % Ethanol herzustellen).
ACHTUNG: Greifen Sie mit Xylol in einer Haube und mit geeigneter Schutzausrüstung um.
- Stellen Sie das Gestell mit den Objektträgern für 30-60 s in Scott's Leitungswasser (auch bekannt als Bläuelösung) und stellen Sie dann das Gestell mit den Objektträgern für 30 s in einen Behälter mit destilliertem Leitungswasser. Tauchen Sie das Gestell mit den Objektträgern 1 Minute lang in die Arbeitslösung eosin.
- Dehydrieren Sie die Objektträger, indem Sie sie in die folgenden Reagenzien legen: 100 % Ethanol für 30 s, einen zweiten Behälter mit 100 % Ethanol für 30 s und tauchen Sie sie dann zweimal in Xylol. Nachdem Sie das Gestell aus der Xylollösung genommen haben, lassen Sie es in einem Glasbehälter trocknen, um zu verhindern, dass Xylol in die Haube tropft.
- Montieren Sie die Rutsche mit 2 Tropfen Montagelösung. Platzieren Sie die Abdeckfolien vorsichtig, um Blasen zu vermeiden, und lassen Sie die Montagelösung trocknen.
ACHTUNG: Greifen Sie mit Xylol in einer Haube und mit geeigneter Schutzausrüstung um.
- Digitalisieren Sie Objektträger, indem Sie sie nach Möglichkeit mit Objektträgerscannern scannen. Wenn diese Option nicht verfügbar ist, verwenden Sie ein normales inverses Mikroskop mit 20-40-facher Vergrößerung, um die Follikel direkt zu zählen. Stellen Sie sicher, dass Sie ein Bild der gesamten Biopsie aufnehmen, um die Bereichsmessung in der Bildanalysesoftware zu erleichtern.
3. Follikelzählung
- Wenn Objektträger digitalisiert wurden, öffnen Sie die Dateien mit einer geeigneten Software (z. B. der Open-Source-Software QuPath38). Wenn nicht digitalisiert, führen Sie die Analyse direkt mit einem inversen Mikroskop und der entsprechenden Software durch.
- Ziehen Sie die Datei in das Hauptfenster von QuPath. Legen Sie den Bildtyp auf Hellfeld H&E fest (siehe Abbildung 1A). Definieren Sie mit der Maßstabsleiste einen Abstand von 1 mm zum Oberflächenepithel (eine einzelne Schicht quaderförmiger Zellen, die die Oberfläche auskleiden). Klicken Sie auf das Ellipsenwerkzeug und kommentieren Sie die Follikel (siehe Abbildung 1B).
- Zählen Sie die Anzahl der Follikel in diesem 1-mm-Bereich, vom Urstadium bis zum Primärstadium. Identifizieren Sie das Stadium jedes Follikels (primordial - eine Schicht abgeflachter Granulosazellen, die die Eizelle umgibt; Zwischenstadium - eine Mischung aus abgeflachten und quaderförmigen Granulosazellen; primär - eine volle Schicht quaderförmiger Granulosazellen, die die Eizelle umgibt).
- Geben Sie die Proben-ID, das Alter, die Anzahl der Follikel für jeden Objektträger, die Schnittdicke und denn-ten gezählten Abschnitt in das Blatt Follikel in mm3 in die Excel-Datei des Follikel-Z-Score-Rechners ein (siehe Ergänzende Datei 1 und Abbildung 2A).
HINWEIS: Aufgrund des Durchmessers der Follikel (kleinste Follikel >35 μm) kann derselbe Follikel in aufeinanderfolgenden Abschnitten auftreten. Seien Sie besonders vorsichtig, wenn Sie Abschnitte zählen, bei denen der Abstand zwischen den Abschnitten kleiner als der Follikeldurchmesser ist. Zählen Sie vorzugsweise Follikel aus jedem 10. Abschnitt (z. B. Abschnitt #10, #20, #30). Das Oberflächenepithel kann sich während der Gewebeaufbereitung ablösen und ist möglicherweise nur teilweise in den Objektträgern vorhanden. Zählen Sie nur Follikel mit sichtbarem Zytoplasma. Lassen Sie zur Qualitätskontrolle zwei Personen unabhängig voneinander die Follikel zählen und bestimmen Sie, wie gut ihre Zählungen übereinstimmen. Berechnen Sie die Konkordanz zwischen den Beobachtern mit einer einfachen Korrelationsfunktion zwischen den Follikelzahlen der einzelnen Beobachter für dieselbe Probe.
- Identifizieren Sie die größten 10% der Follikel in jedem gezählten Abschnitt durch Augäpfel. Messen Sie den mittleren Durchmesser dieser Eizellen, indem Sie auf das Linienwerkzeug klicken, zwei senkrechte Linien durch die Eizellmembran ziehen und Messen und dann Anmerkungsmessungen anzeigen auswählen (siehe Abbildung 1C).
- Notieren Sie die Messungen unter der Spalte Länge μm (siehe Abbildung 1D). Geben Sie den mittleren Durchmesser aller Eizellen in das Feld Mittlerer Eizelldurchmesser (μm) für jeden Objektträger in der Excel-Datei des Follikel-Z-Score-Rechners ein (Follikel in mm3, siehe Zusatzdatei 1 und Abbildung 2A).
- Platzieren Sie das Bild in der Mitte des Bildschirms in QuPath und klicken Sie dann auf das ImageJ-Symbol . Wählen Sie Snapshot an ImageJ senden (siehe Abbildung 3A). Begrenzen Sie in ImageJ mit dem Pinselwerkzeug 1 mm vom Rand ab. Klicken Sie auf das Bild, dann auf Typ, und wählen Sie 8-Bit aus (siehe Abbildung 3B).
- Klicken Sie auf das Linienwerkzeug und zeichnen Sie eine Linie auf der Maßstabsleiste unten links auf dem Bildschirm (siehe Abbildung 3C). Klicken Sie auf Analysieren, dann auf Maßstab festlegen, geben Sie die in der Maßstabsleiste angegebene Länge in das Feld Bekannte Entfernung ein und klicken Sie auf OK (siehe Abbildung 3C). Klicken Sie auf Bild, dann auf Anpassen, Helligkeit/Kontrast und wählen Sie Auto (siehe Abbildung 3D).
- Klicken Sie auf Bild, dann auf Anpassen, Schwellenwert und wählen Sie Auto (siehe Abbildung 3E). Klicken Sie auf das Zauberstab-Werkzeug, wählen Sie den Bereich aus und drücken Sie dann Strg + M (siehe Abbildung 3F). Geben Sie den Flächenwert in die Excel-Datei des Follikel-Z-Score-Rechners ein (Follikel in mm3, siehe Zusatzdatei 1 und Abbildung 2A).
4. Berechnung der Follikeldichte, des kortikalen Volumens und des Z-Scores
- Verwenden Sie die bereitgestellte Excel-Datei für den Follikel-Z-Score-Rechner, um die unten beschriebenen Berechnungen automatisch durchzuführen. Die Ergebnisse erscheinen im Excel-Rechner in der Tabelle "Z-Wert (Follikel pro mm³)" (siehe Zusatzdatei 1), sofern die in Abschnitt 3 angegebenen Angaben in das Blatt "Follikel in mm³" eingetragen sind.
- Um die Follikeldichten in diesen Abschnitten zu berechnen, verwenden Sie die modifizierte Formel von Schmidt et al.32. Wenden Sie zunächst den Korrekturfaktor α an, um die Doppelzählung desselben Follikels zu berücksichtigen. Die geänderte Formel lautet wie folgt:
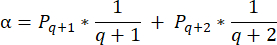
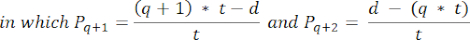
HINWEIS: In dieser Formel ist t die Schnittdicke, d der Durchmesser der Eizelle und q der Quotient aus dem Follikeldurchmesser geteilt durch die Schnittdicke. - Extrapolieren Sie die Gesamtzahl der Follikel (n Follikel) in der Hirnrinde aus der Follikelzahl in diesem Abschnitt mit der folgenden Formel33:
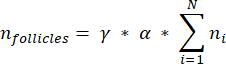
HINWEIS: Diese Formel berücksichtigt auch alle nicht berechneten Querschnitte. Hier stellt γ die Anzahl der Abschnitte dar, die nicht berechnet werden (z. B. γ = 10, wenn jeder 10. Abschnitt gezählt wird), α ist der in 4.1 berechnete Korrekturfaktor, N ist die Anzahl der gezählten Abschnitte und n i ist die Gesamtzahl der Follikel in den gezählten Abschnitten.- Extrapolieren Sie das gesamte kortikale Volumen (V) aus den gezählten Bereichen mit der folgenden Formel33:
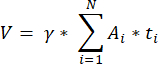
HINWEIS: Hier ist Ai die Fläche des Schnitts und ti die Gewebedicke. Bitte überprüfen Sie Schritt 4.2 für γ und N. - Verwenden Sie die folgende Formel33 , um die Follikeldichte zu berechnen:
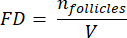
- Extrapolieren Sie das gesamte kortikale Volumen (V) aus den gezählten Bereichen mit der folgenden Formel33:
- Stellen Sie fest, ob eine verringerte ovarielle Reserve (<-1,7 Z-Wert) vorhanden ist, indem Sie den Z-Wert mit der Formel33 berechnen:
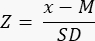
HINWEIS: Der Z-Score wird automatisch im Blatt "Z-Score (Follikel pro mm³)" im Excel-Rechner (siehe Zusatzdatei 1) auf der Grundlage der Informationen in Abschnitt 3 (Follikelzählung) berechnet (Abbildung 2B). In dieser Formel steht Z für den Z-Score, x für die berechnete Follikeldichte (Follikel/cm 3) der Studienstichprobe (Schritt 4.4), M für die mittlere Follikeldichte der jeweiligen Altersgruppe und SD für die Standardabweichung der jeweiligen Altersgruppe. Referenzwerte für Frauen im Alter von 0-25 Jahren wurden in Hassan et al.33 festgelegt. Mittelwerte und Standardabweichungen der Follikeldichten der jeweiligen Altersgruppen können in der Excel-Datei des Follikel-Z-Score-Rechners (Ergänzungsdatei 1) gefunden und für die Z-Score-Berechnungen verwendet werden.
Ergebnisse
Ovarialfollikel werden nach erfolgreichem Schneiden, Färben und Scannen von Objektträgern quantifiziert. Die verschiedenen Stadien und die Gesundheit der Follikel werden unterschieden und weiter analysiert. In Abbildung 4A ist ein HE-gefärbter Querschnitt eines Bouin-fixierten Eierstocks eines Erwachsenen mit Beispielen von kortikalem und medullärem Gewebe dargestellt. Abbildung 4B zeigt ein repräsentatives Bild des Eiersto...
Diskussion
Frauen werden mit einem endlichen Pool an Eizellen geboren, der nicht aufgefüllt werden kann. Die ovarielle Reserve ist ein wichtiger Faktor für das Fortpflanzungspotenzial einer Frau. In diesem Artikel wird eine Methode zur histologischen Quantifizierung der Follikeldichte und deren Vergleich mit Referenzstandards anhand von Z-Scores der ovariellen kortikalen Follikeldichten bei jungen Patientinnen und Frauen bis zum Alter von 25 Jahren vorgestellt.
In dies...
Offenlegungen
Die Autoren haben keine Interessenkonflikte.
Danksagungen
Wir danken den medizinischen Fachkräften, die uns bei der Rekrutierung der Teilnehmerinnen und der Gewebeentnahme geholfen haben, sowie allen Patientinnen, die ihr Eierstockgewebe gespendet haben. Wir danken auch dem Kinderkrebsfonds (PR2020-0096) und dem Karolinska Institutet PhD Funding KID, deren Finanzierung diese Arbeit ermöglicht hat. Wir danken auch der Abteilung für morphologische Phänotypanalyse für die Erstellung der histologischen Objektträger. Wir danken Nicola Byers für die sprachliche Bearbeitung dieses Manuskripts.
Materialien
| Name | Company | Catalog Number | Comments |
| 1x Dulbecco's Phosphate Buffered Saline | Thermo Fisher | 14190144 | |
| 1x Phosphate Buffered Saline w/ CaCl2, MgCl2, 1 g/L D-glucose, 36 mg/L pyruvate | Thermo Fisher | 14287-080 | |
| 37% Hydrochloric acid | Sigma-Aldrich | 1.09057.1000 | |
| 70% ethanol | Histolabs | 01370.01L | |
| 95% ethanol | Fisher scientific | 10572143 | |
| Absolute ethanol | Histolabs | 01399.01L | |
| Bouin's solution | Sigma-Aldrich | HT10132-1L | |
| Eosin Y Free acid | Sigma-Aldrich | E4009-5G | |
| Formaldehyde | Thermo Fisher | 28908 | |
| Haematoxylin solution according to Delafield | Sigma-Aldrich | 03971-250ML | |
| ImageJ | |||
| Microsoft Excel | |||
| Microtome | |||
| Pertex mounting solution | Histolabs | 00840-05 | |
| Propofol | Baxter Holding B.V. | N01AX10 | ATC-code provided instead of catalog number |
| QuPath | https://qupath.github.io/ | ||
| Rocuronium bromide | B. Braun Melsungen AG | M03AC09 | ATC-code provided instead of catalog number |
| Scott's tap water substitute concentrate | Sigma-Aldrich | S5134-6x100ml | |
| Sevoflurane | Baxter Medical AB | N01AB08 | ATC-code provided instead of catalog number |
| Slide scanner | |||
| Sufentanil | Hameln Pharma gmbh | N01AH03 | ATC-code provided instead of catalog number |
| Sugammadex | Baxter Holding B.V. | V03AB35 | ATC-code provided instead of catalog number |
| SuperFrost plus white | Histolabs | 06400 | |
| SuperFrost Plus White microscope slides | Histolabs | 06400 | |
| Xylene | Saveen Werner | 131769.1611 |
Referenzen
- Richards, J. A. S. The ovarian cycle. Vitam Horm. 107, 1-25 (2018).
- Wallace, W. H. B., Kelsey, T. W. Human ovarian reserve from conception to the menopause. PLoS One. 5 (1), 1-9 (2010).
- Monniaux, D., et al. The ovarian reserve of primordial follicles and the dynamic reserve of antral growing follicles: What is the link. Biol Reprod. 90 (4), 1-11 (2014).
- Gougeon, A., Trounson, A., Gosden, R., Eichenlaub-Ritter, U. . The early stages of follicular growth in biology and pathology of the oocyte. , 50-61 (2013).
- Gougeon, A. Human ovarian follicular development: From activation of resting follicles to preovulatory maturation. Ann Endocrinol. 71 (3), 132-143 (2010).
- Hansen, K. R., Craig, L. B., Zavy, M. T., Klein, N. A., Soules, M. R. Ovarian primordial and non-growing follicle counts according to the stages of reproductive aging workshop (STRAW) staging system. Menopause. 19 (2), 164-171 (2012).
- Gold, E. B. The timing of the age at which natural menopause occurs. Obstet Gynecol Clin North Am. 38 (3), 425-440 (2011).
- Alberico, H., et al. Workflow optimization for identification of female germline or oogonial stem cells in human ovarian cortex using single-cell RNA sequence analysis. Stem Cells. 40, 523-536 (2022).
- White, Y. A. R., et al. Oocyte formation by mitotically active germ cells purified from ovaries of reproductive-age women. Nat Med. 18 (3), 413-422 (2012).
- Wagner, M., et al. Single-cell analysis of human ovarian cortex identifies distinct cell populations but no oogonial stem cells. Nat Commun. 11, 1147 (2020).
- Yoshihara, M., et al. In reply: Revisiting claims of the continued absence of functional germline stem cells in adult ovaries. Stem Cells. 41 (2), 205-206 (2023).
- Yoshihara, M., et al. The continued absence of functional germline stem cells in adult ovaries. Stem Cells. 41, 105-110 (2023).
- Van Kasteren, Y. M., Schoemaker, J. Premature ovarian failure: A systematic review on therapeutic interventions to restore ovarian function and achieve pregnancy. Hum Reprod Update. 5 (5), 483-492 (1999).
- McGlacken-Byrne, S. M., Conway, G. S. Premature ovarian insufficiency. Best Pract Res Clin Obstet Gynaecol. 81, 98-110 (2022).
- Viuff, M., Gravholt, C. H. Turner syndrome and fertility. Ann Endocrinol. 83 (4), 244-249 (2022).
- Poirot, C., et al. Ovarian tissue cryopreservation for fertility preservation in 418 girls and adolescents up to 15 years of age facing highly gonadotoxic treatment: Twenty years of experience at a single center. Acta Obstet Gynecol Scand. 98 (5), 630-637 (2019).
- Jensen, A. K., et al. Cryopreservation of ovarian tissue for fertility preservation in a large cohort of young girls: Focus on pubertal development. Hum Reprod. 32 (1), 154-164 (2017).
- The Practice Committee of the American Society for Reproductive Medicine. Fertility preservation in patients undergoing gonadotoxic therapy or gonadectomy: A committee opinion. Fertil Steril. 112 (6), 1022-1033 (2019).
- . ART Fact Sheet Available from: https://www.eshre.eu/Press-Room/Resources (2020)
- Antonouli, S., et al. A comprehensive review and update on human fertility cryopreservation methods and tools. Front Vet Sci. 10, 1151254 (2023).
- Bahroudi, Z., et al. Review of ovarian tissue cryopreservation techniques for fertility preservation. J Gynecol Obstet Hum Reprod. 51 (2), 102290 (2022).
- Jensen, A. K., et al. 86 successful births and 9 ongoing pregnancies worldwide in women transplanted with frozen-thawed ovarian tissue: Focus on birth and perinatal outcome in 40 of these children. J Assist Reprod Genet. 34 (3), 325-336 (2017).
- Donnez, J., Dolmans, M. -. M. Fertility preservation in women. N Engl J Med. 377 (17), 1657-1665 (2017).
- Dolmans, M. M., Falcone, T., Patrizio, P. Importance of patient selection to analyze in vitro fertilization outcome with transplanted cryopreserved ovarian tissue. Fertil Steril. 114 (2), 279-280 (2020).
- Demeestere, I., et al. Live birth after autograft of ovarian tissue cryopreserved during childhood. Hum Reprod. 30 (9), 2107-2109 (2015).
- Ernst, E., Kjærsgaard, M., Birkebæk, N. H., Clausen, N., Andersen, C. Y. Case report: Stimulation of puberty in a girl with chemo- and radiation therapy-induced ovarian failure by transplantation of a small part of her frozen/thawed ovarian tissue. Eur J Cancer. 49 (4), 911-914 (2013).
- Rodriguez-Wallberg, K. A., et al. Successful pregnancies after transplantation of ovarian tissue retrieved and cryopreserved at time of childhood acute lymphoblastic leukemia - a case report. Haematologica. 106 (10), 2783-2787 (2021).
- Matthews, S. J., Picton, H., Ernst, E., Andersen, C. Y. Successful pregnancy in a woman previously suffering from β-thalassemia following transplantation of ovarian tissue cryopreserved before puberty. Minerva Ginecol. 70 (4), 432-435 (2018).
- Kristensen, S. G., et al. Use of cryopreserved ovarian tissue in the Danish fertility preservation cohort. Fertil Steril. 116 (4), 1098-1106 (2021).
- Donfack, N. J., et al. Expectations and limitations of ovarian tissue transplantation. Zygote. 25 (4), 391-403 (2017).
- Schmidt, K. L. T., Byskov, A. G., Andersen, A. N., Müller, J., Andersen, C. Y. Density and distribution of primordial follicles in single pieces of cortex from 21 patients and in individual pieces of cortex from three entire human ovaries. Hum Reprod. 18 (6), 1158-1164 (2003).
- Hassan, J., et al. Reference standards for follicular density in ovarian cortex from birth to sexual maturity. Reprod Biomed Online. 47, 103287 (2023).
- Vilela, J. d. e. M. V., Dolmans, M. M., Amorim, C. A. Ovarian tissue transportation: A systematic review. Reprod Biomed Online. 42 (2), 351-365 (2021).
- Gibson, E., Mahdy, H. . Anatomy, abdomen and pelvis, ovary. , (2023).
- Nagaraj, A. S., et al. Establishment and analysis of tumor slice explants as a prerequisite for diagnostic testing. J Vis Exp. (141), e58569 (2018).
- Adeniran, B. V., Bjarkadottir, B. D., Appeltant, R., Lane, S., Williams, S. A. Improved preservation of ovarian tissue morphology that is compatible with antigen detection using a fixative mixture of formalin and acetic acid. Hum Reprod. 36 (7), 1871-1890 (2021).
- Bankhead, P., et al. QuPath: Open-source software for digital pathology image analysis. Sci Rep. 7 (1), 1-7 (2017).
- Björvang, R. D., et al. Persistent organic pollutants and the size of ovarian reserve in reproductive-aged women. Environ Int. 155, 106589 (2021).
- Kwok, R., Johnson, N. P. Ovarian biopsy has no role as a routine diagnostic test of ovarian reserve: A systematic review. Reprod Biomed Online. 24, 492-495 (2012).
- Ahmad, A., et al. High-throughput spatial sensitive, quantitative phase microscopy using low spatial and high temporal coherent illumination. Sci Rep. 11 (1), 1-13 (2021).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten