Method Article
HLA-Ig celdas en función de antígeno artificiales presentación para mejorar la eficiencia Ex vivo Ampliación de los Derechos Humanos CTL
En este artículo
Resumen
Un nuevo método de CC independiente para la inducción y la expansión de células T específicas de antígeno se describe. HLA A2-Ig células antígeno artificial basada en la presentación (AAPC) se cargan con el HLA-A2 péptidos restringidos a expandirse de manera eficiente CTL del antígeno específico diverso. Esta tecnología tiene un gran potencial para el CTL basado inmunoterapia adoptiva.
Resumen
CTL con función efectora óptima desempeñar un papel fundamental en la mediación de la protección contra diversas infecciones intracelulares y el cáncer. Sin embargo, los individuos pueden presentar microambiente inmunosupresores y, en contraste con la activación de CTL, sus células antígeno autólogo presenta tienden a tolerize o anergize CTL antígeno específico. Como resultado de ello, aunque todavía en fase experimental, CTL basado en inmunoterapia adoptiva ha evolucionado hasta convertirse en un prometedor tratamiento para diversas enfermedades como el cáncer y las infecciones de virus. En los experimentos iniciales ex vivo ampliado CMV (citomegalovirus) CTL específicas se han utilizado para el tratamiento de la infección por CMV en pacientes inmunocomprometidos trasplante alógeno de médula ósea. Si bien es común que amenaza la vida viremia por CMV en estos pacientes, ninguno de los pacientes que reciben ampliado CTL desarrollar enfermedades relacionadas con el CMV, lo que implica la inmunidad anti-CMV es establecido por la adoptively transferido CTL 1. Prometedores resultados también se han observado para el melanoma y puede extenderse a otros tipos de cáncer 2.
Si bien hay muchas maneras de ex vivo de estimular y ampliar CTL humanos, los enfoques actuales están restringidas por las limitaciones técnicas y de costos. Por ejemplo, el estándar de oro actual se basa en el uso de la DC autólogas. Esto requiere que cada paciente para donar un número importante de los leucocitos y también es muy caro y laborioso. Por otra parte, se detalla en la caracterización in vitro de la DC amplió CTL ha revelado que estos tienen una función efectora sólo subóptima 3.
Aquí presentamos un muy eficiente sistema de AAPC base para la expansión ex vivo de los derechos humanos CMV CTL específicas para inmunoterapia adoptiva (Figura 1). La AAPC se hicieron mediante el acoplamiento magnético de células cuentas de tamaño humano con HLA-A2-Ig anti-dímero y CD28mAb 4. Una vez que se hacen AAPC, que puede ser cargado con varios péptidos de interés, y seguir funcionando durante meses. En este informe, AAPC se cargaron con un péptido dominante de CMV, pp65 (NLVPMVATV). Después del cultivo humano purificado CD8 + CTL de un donante sano con AAPC por una semana, el CMV específica CTL se puede aumentar de manera espectacular en la especificidad de hasta el 98% (Figura 2) y se amplifica más de 10.000 veces. Si hay más CMV-CTL específicos se requiere, una mayor expansión se puede conseguir fácilmente por la estimulación repetitiva con AAPC. Caracterización fenotípica y funcional muestra que estas células se han ampliado el fenotipo de un efectoras de memoria y hacer que cantidades significativas de TNF-alfa y IFN (Figura 3).
Protocolo
1. Decisiones, HLA-A2-Ig base AAPC
- Prepare el buffer de borato estéril
- Disolver el ácido bórico en agua para 0,1 M. Ajustar el pH a 7.0.
- Filtrar a través de un filtro de 0.22μm estéril y se almacenan a 4 ° C.
- Prepare el buffer de lavado estéril bolas
- Tomar 956ml PBS w / o magnesio o calcio.
- Añadir 30 ml de suero humano AB.
- Añadir EDTA 2 mM de concentración final.
- Añadir 0.1gsodium azida.
- Filtrar a través de un filtro de 0,22 micras estéril y se almacenan a 4 ° C.
- Tomar 1 ml de perlas de Invitrogen Epoxy M-450 en stock, aproximadamente 400 millones de cuentas (cuentas se pueden contar por hemocitómetro), y poner en un frasco estéril, tornillo de la tapa de cristal.
- Ponga el frasco en contra de un imán Dynal MPC-1, mientras que las cuentas se adhieren a la pared del vial, separar el sobrenadante por aspiración. Lávese las cuentas de una vez con 1 ml de solución tampón de borato.
- Volver a suspender las bolas en una mezcla de 1 ml de solución tampón de borato y 20 mg de HLA-A2-Ig dímero y 20 mg de CD28 mAb anti-humano (clon 9.3).
- Proteína de la conjugación de bolas: poner el frasco de vidrio en los rotadores y girar a 4 ° C durante 24 horas.
- Colocar el tubo en MPC-1 imán y eliminar todos los tampón borato.
- Lave las cuentas dos veces con buffer de lavado de 1 ml de bolas.
- Incubar las cuentas en un tampón de lavado 1 ml de bolas, gire a 4 ° C durante 24 horas. Debido a tampón de lavado bolas contiene suero humano AB, que bloqueará todos los sitios de unión a proteínas residuales en las cuentas.
- Eliminar el sobrenadante del frasco de vidrio, sustituya con 1 ml de solución tampón fresca Lavar bolas.
2. Control de calidad de AAPC y el péptido de carga, almacenamiento
- Añadir ~ 5 × 10 5 gotas de tampón de lavado FACS 100μl en tubos de FACS, y se tiñen con 1μl de anti-ratón IgG1-PE (reconocer la porción Fc de HLA-A2-Ig) y 1μl de anti-ratón IgG2a-FITC (reconocer la parte Fc de mAb anti-CD28). Después de la tinción durante 20 minutos en FACS buffer de lavado, lavado de nuevo y leer el resultado de la tinción de inmediato por citómetro de flujo (Figura 4).
- Carga de péptidos en las cuentas: lavar las cuentas dos veces en frasco de vidrio con 1 ml de PBS estéril. Resuspender con 1 ml de PBS estéril a continuación, agregar 10μl de CMV péptido (1mg/ml)
- Contar las gotas de hemocitómetro, y la etiqueta del vial con la fecha y la concentración.
- AAPC están listos para su uso después de por lo menos 3 días de incubación del péptido a 4 ° C, para permitir suficiente tiempo de unión del péptido en el dímero HLA-A2-Ig. Las cuentas se pueden almacenar a 4 ° C y seguir funcionando por lo menos durante 6 meses.
3. Aislamiento humano CTL
- Recoger ~ 100 ml de sangre periférica fresca de salud de los donantes HLA-A2 positivo en 10 tubos de sodio BD Vacutainer de heparina. Use una aguja de calibre 21 o mayor para evitar la hemólisis.
- Centrifugar a 300xg durante 10 minutos a temperatura ambiente
- Retire con cuidado la capa de plasma superior por aspiración. El plasma puede ser utilizado como suplemento para el medio de cultivo.
- Vuelva a colocar el plasma recogido con PBS estéril y la transferencia de la sangre en un frasco de cultivo estéril T75 o 50 ml tubos cónicos. Mezclar la sangre con PBS y pipeteando arriba y hacia abajo.
- Una vez que toda la sangre se recoge, prepara otros cuatro tubos cónicos de 50 ml y agregar 15 ml de Ficoll-Paque Plus.
- Poco a poco superposición 30-35 ml de células de la sangre en la parte superior de la Ficoll de cada tubo. Mantener la interfaz entre los distintos Ficoll y las células sanguíneas.
- Centrifugar a 500xg durante 20 minutos a temperatura ambiente. A su vez el freno de "off" y la aceleración lo más bajo posible para mantener una relación clara entre las capas.
- Con una pipeta seriological, cuidadosamente aspirar la capa de PBMC y recoger las PBMC en un nuevo tubo cónico de 50 ml. Cuando todos los PBMC se cosechan agregar 30 ml de PBS y se giran a 400xg durante 10 minutos. Descartar el sobrenadante y lavar una vez más con 30 ml de PBS para eliminar todos los Ficoll residual.
- Proceder a CD8 + aislamiento de células T mediante el uso de Miltenyi humana de células T CD8 + kit de aislamiento de acuerdo con el protocolo del fabricante. Este kit muy enriquece de las células CD8 + (normalmente> 95%) por el agotamiento de CD8 - las células.
- Cuente los linfocitos T CD8 +. La pureza de la esperada debe ser mayor al 95%. Para confirmar este uso de 2x10 5 células y realizar un análisis CD4/3/8 FACS. El CTL restante puede ser utilizado de inmediato para el antígeno específico de la estimulación AAPC o pueden ser congelados para su uso futuro.
4. En el sistema de cultivo in vitro basado en AAPC
- Preparar medio de cultivo
- De TF (de células T del factor de crecimiento, realizado en el laboratorio 4) 2X medio de cultivo: medio RPMI completo, más el 5% de los donantes autólogos de plasma y un 8% el factor de células T de crecimiento. donantes autólogos pueden ser sustituidos por inactivado por calor suero humano AB.
- Resuspender 1.000.000 CTL en 8 ml de medio TF cultura 2X más de 8 ml de medio RPMI completo, agregue 1 × 10 6 AAPC, mezclar bien.
- Utilice una pipeta de canales múltiples de células de la placa en 96 y U fondo placas de cultivo de tejidos. (160 l por pocillo)
- Las células de cultivo a 37 ° C, 5% de CO 2 incubater durante 7 días. Alimentar a las células en el día 4 con 80 l / pocillo mediano TF 2X.
- Las células están listas para ser cosechadas en el día 7. Después de la cosecha, el lugar a las células contra el imán y eliminar la AAPC de edad.
- Antígeno específico puede ser determinado por tinción tetrámero de acuerdo con el protocolo del fabricante. Tinción fenotipo y tinción intracelular de citoquinas se realizó de acuerdo a nuestros tres estudios anteriores.
- Las células pueden ser cosechadas replated con AAPC de nuevo en las mismas condiciones. El número de células y la especificidad del antígeno se espera que aumente después de la estimulación repetida.
5. Los resultados representativos:
Un ejemplo de AAPC después de la conjugación HLA A2-Ig y anti-CD28 se muestra en la Figura 4. Conjugación de proteínas con éxito es evidente un claro desplazamiento de la tinción de anticuerpos correspondientes. Mientras que la frecuencia de linfocitos T citotóxicos específicos de CMV en la sangre periférica es generalmente 0,5-1%, después de una semana de la AAPC mediada por la estimulación, la especificidad puede alcanzar el 55 - 93% (Figura 2 y 3). La expansión de CTL antígeno específico puede ser muy variable entre los diferentes donantes, pero los resultados son reproducibles dentro de un mismo donante. Por extrapolación, la expansión de las células específicas de CMV puede ser miles de veces en comparación con los niveles de precursor directamente ex vivo (datos no mostrados). Tinción intracelular de citoquinas (Figura 3) muestra que estos CTL ampliado son polifuncionales, más que agotado, después de cultivo celular y la proliferación prolongada significativa.

Figura 1. Diagrama de flujo del Representante AAPC expansión ex vivo de la base CTL humanos para la inmunoterapia adoptiva en pacientes TCPH alogénicos
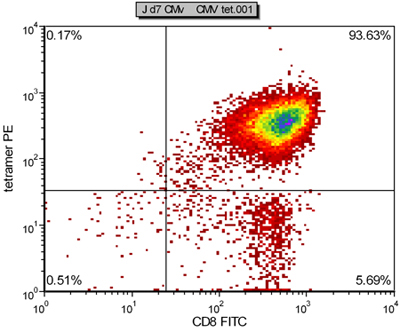
Figura 2. Representante tetrámero de la tinción de linfocitos T citotóxicos específicos generados por CMV AAPC después de una semana de la cultura
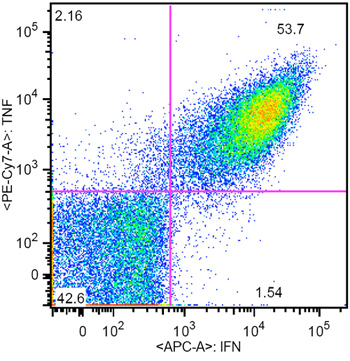
Figura 3. Representante resultado tinción intracelular de citoquinas de linfocitos T citotóxicos específicos generados por CMV AAPC (CMV especificidad fue del 61%)
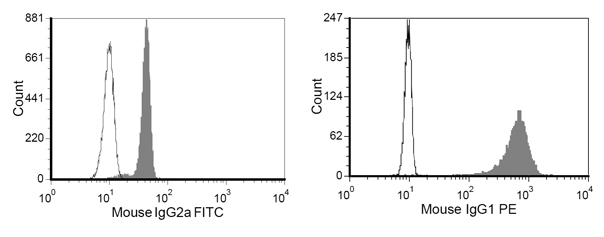
Figura 4. Representante de la tinción de la M-450 Epoxy cuentas después de la conjugación de proteínas teñidas con anti-ratón IgG1-PE y anti-ratón IgG2-FITC
Discusión
El sistema de AAPC que describimos aquí es un sistema eficiente para la expansión ex vivo de linfocitos T citotóxicos humanos contra una variedad de antígenos. Especial cuidado se debe tomar con respecto a la calidad de la conjugación de la proteína y la distribución uniforme de la AAPC y CTL en el cultivo en placa de 96 pocillos. El uso de este enfoque que hemos sido capaces de ampliar CTL por más de 8 semanas, durante el cual hemos ampliado antígeno-específica CTL hasta un millón de veces 4. Ha habido varios sistemas de APC artificial utilizando líneas de células u otras plataformas acelular 5, sin embargo, de acuerdo con los datos publicados cada sistema tiene su perfil único en lo que respecta a la expansión y la especificidad de soporte de aplicaciones diferentes. Importante, ya que la calidad de CTL es tan importante como la cantidad, la polifuncionalidad de los CTL CMV específicos generados por nuestro sistema se espera que confieren superior anti-viral eficiencia.
Divulgaciones
Agradecimientos
Nos gustaría dar las gracias a Aaron Selya útil para el debate. Este trabajo fue apoyado por el NIH subvención AI29575, CA108835, AI077097 a JS, una subvención piloto de la Johns Hopkins malaria Instituto de Investigación y el Departamento de Defensa de conceder PC 040972 para MO
Materiales
| Name | Company | Catalog Number | Comments |
| Reactivo | Empresa | Número de catálogo | |
|---|---|---|---|
| Vacutainer tubo (contiene heparina) | Becton Dickinson | 367874 | |
| Humana de células T CD8 + Kit de aislamiento | Miltenyi | 130-094-156 | |
| Dynabeads M-450 Epoxy | Invitrogen | 140,11 | |
| Dynal MPC-1 Imán | Invitrogen | 120-01D | |
| Ficoll-Paque Plus | GE Healthcare | 17-1440-03 | |
| Medio RPMI 1640 | Gibco | 11875 | |
| HLA-A2-Ig dímero X | Becton Dickinson | 551263 | |
| iTAgMHC tetrámero (HLA-A2-CMV)-PE | Beckman Coulter | T20099 | |
| Falcon claro de 96 pocillos placa de Microtest | Becton Dickinson | 353077 | |
| Rata anti-ratón IgG2a-FITC | Becton Dickinson | 553390 | |
| Cabra anti-ratón IgG1-PE | Invitrogen | P21129 | |
| Suero humano AB | Atlanta biológicos | S40110 | |
| Ratón anti-humano CD8a-FITC | Sigma-Aldrich | F0772 | |
| Ratón anti-humano CD8a-APC | Becton Dickinson | 340684 | |
| Ratón anti-humano IFN-FITC | Becton Dickinson | 340449 | |
| Mouse anti-TNFa humano-PE | Becton Dickinson | 340512 |
Referencias
- Walter, E. A. Reconstitution of cellular immunity against cytomegalovirus in recipients of allogeneic bone marrow by transfer of T-cell clones from the donor. N Engl J Med. 333, 1038-1038 (1995).
- Rosenberg, S. A. Adoptive cell transfer: a clinical path to effective cancer immunotherapy. Nat Rev Cancer. 8, 3669-3669 (2008).
- Oelke, M. Ex vivo induction and expansion of antigen-specific cytotoxic T cells by HLA-Ig-coated artificial antigen-presenting cells. Nat Med. 9, 619-619 (2003).
- Oelke, M. Artificial antigen-presenting cells: artificial solution for real diseases. Trends Mol Med. 11, 412-412 (2005).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados