Method Article
Teratoma generación en la cápsula del testículo
En este artículo
Resumen
Las células madre pluripotentes (hPSCs) tienen el potencial para tratar una gran variedad de enfermedades diferentes. La utilidad de estas células reside en el hecho de que pueden diferenciarse en cualquier tipo de célula en el cuerpo. Aquí se describe el ensayo de teratoma, que se utiliza para demostrar la pluripotence de hPSCs.
Resumen
Las células madre pluripotentes (PSC) tiene la característica única que pueden diferenciarse en células de las tres capas germinales. Esto los convierte en una herramienta potencialmente valiosa para el tratamiento de muchas enfermedades diferentes. Con la llegada de células madre pluripotentes inducidas (iPSCs) y la investigación continúa con células madre embrionarias humanas (hESCs) es necesario para los ensayos que puedan demostrar que una línea celular particular es pluripotente. Transmisión de línea germinal ha sido el estándar de oro para demostrar la pluripotence de células madre embrionarias de ratón (MESC) líneas 1,2,3. El uso de este ensayo, los investigadores pueden demostrar que una línea MESC puede hacer todos los tipos de células en el embrión incluidas las células germinales 4. Con la generación de líneas de CES 5,6 humana, el ensayo apropiado para demostrar pluripotence de estas células estaba claro desde el CES humanos no pueden ser probados para la transmisión de línea germinal. Como sustituto, el ensayo de teratoma se utiliza actualmente para demostrar la pluripottransparencia de las células madre pluripotentes (hPSCs) 7,8,9. Aunque este ensayo recientemente ha sido objeto de escrutinio y las nuevas tecnologías se están explorando activamente, el ensayo de teratoma es el actual estándar de oro 7. En este ensayo, las células en cuestión se inyectan en un ratón inmune comprometido. Si las células son pluripotentes, un teratoma eventualmente desarrollar y secciones del tumor se muestran los tejidos de las 3 capas germinales 10. En el ensayo de teratoma, hPSCs se puede inyectar en las diferentes áreas del ratón. Los sitios de inyección más comunes incluyen la cápsula testículo, la cápsula del riñón, hígado, o en la pata tanto por vía subcutánea o intramuscular 11. Aquí se describe un protocolo robusto para la generación de teratomas de hPSCs utilizando la cápsula testículo como el sitio para el crecimiento del tumor.
Protocolo
Nota: Todos los procedimientos con animales debe ser aprobado por el IACUC o equivalente.
Todo el equipo quirúrgico debe ser esterilizado antes de la cirugía. Guantes estériles, las cortinas de gasa y se debe utilizar.
1. Preparación antes de la cirugía
- Obtenga 6 semanas de edad Mus musculus CbySmn.CB17-Prkdc SCID / J ratones machos o otra cepa de ratón inmunodeficiente.
- Esterilice todos los instrumentos quirúrgicos, guantes y gasa.
- Disociar hPSCs ser inyectados con accutase.
- Contar las células y resuspender 1.000.000 células por 20-30 l en matrigel diluido 1:1 en DMEM/F-12. Mantener las células en hielo hasta que termine.
- Tenga en cuenta que a menudo es útil hacer una carrera a través del experimento en el que se inyecta azul de tripano. Esto ayudará a identificar cualquier problema potencial antes de que las células se pierden.
- En el vivero, anestesiar el puntero del ratón de acuerdo con los procedimientos aceptados en su institución. En nuestros experimentos, hemos utilizado un AnesthEIAS de la máquina con isoflurano. Los ratones fueron puestos inicialmente en una cámara de inducción con el oxígeno 1L/min y 3-4% isoflurano. Una vez anestesiado, un cono de la nariz con el oxígeno 1L/min e isoflurano al 2-3% se utilizó.
- El abdomen afeitado con maquinilla, y limpiar la pared anterior del abdomen del ratón, comenzando desde el centro del abdomen y de trabajo en sentido horario hacia el exterior. El primer uso solución de povidona yodada y luego lave con etanol al 70%. Repita 3 veces, el cambio de hisopos en cada ocasión. Traslado del animal a una compresa caliente para mantener al animal caliente dentro de un cultivo de tejido o una campana de disección.
- Hacer una incisión de 1 cm longitudinal a través de la piel y el peritoneo con tijeras quirúrgicas estériles justo por debajo del nivel de la articulación de la cadera.
- Mientras mantiene el peritoneo con una pinza, llegar hacia abajo, hacia la cadera derecha con otro forcept estéril y extraiga el tejido adiposo blanco, junto con los testículos adjuntos.
- Coloque los testículos en una gasa estéril.
- Llene una tuberculina o Hamilton (1 cc) jeringa de wiª los hPSCs a ser inyectado. Tenga en cuenta que es una buena idea incluir una línea de control hPSC que sabe que es pluripotente como WA09 (también conocido como H9). De esta manera usted tiene un control positivo que se puede utilizar para determinar si la inyección o la cirugía era defectuoso.
- Lentamente inyectar los hPSCs (20-30 l) en el centro de la cápsula testículo lejos de cualquier principales vasos sanguíneos, parando si la cápsula testicular comienza a hincharse.
- Retirar la aguja lentamente para evitar el reflujo de las células.
- Con unas pinzas, transfiera los testículos y la espalda tejido graso a su posición original en el abdomen.
- Cierre del peritoneo con 2 o 3 puntos de sutura reabsorbibles y cerrar la piel con autoclips.
- El ratón se debe mantener caliente hasta que se recupere y teniendo en cuenta algún tipo de analgésico (ver lo que es aceptado en el vivero) después de la cirugía dos veces al día durante 1-2 días.
Nótese que ni el anestésico ni el analgésico con interferir con el desarrollo del tumor. - Monitorear ºe animal para el crecimiento del tumor durante 6-12 semanas. Muy pocas veces, los tumores pueden crecer a 5 mm de tamaño anteriores a 6 semanas después de la inyección, por lo tanto es importante controlar los animales. Si esto sucede, los animales deben ser sacrificados y procesados y analizados los tumores como de costumbre.
- Una vez que el tumor es palpable y llega a aproximadamente 5 mm de tamaño, anestesiar el ratón y el sacrificio de acuerdo con los procedimientos aceptados animales de protocolo.
- Extirpar el tumor y el documento de acuerdo - Una fotografía tamaño, medida, peso.
- Cortar en trozos pequeños tumores y fijar en la solución de paraformaldehído al 4%. Almacenar en paraformaldehído al 4% hasta que las muestras se envían a un patólogo para su corte, coloración y el análisis.
2. Resultados representativos:
Cuando este protocolo se realiza como se ha descrito y la línea celular inyectado es pluripotentes, un palpable, visualmente evidente, tumor debe formar un plazo de 12 semanas a lo sumo. Para las líneas establecidas hPSC como WA09, vemos típicamentelos tumores dentro de 6 semanas. Para las líneas de IPSC no es raro ver a los tumores dentro de las 8-10 semanas. Es muy importante para inyectar ratones con una línea que es conocido por ser pluripotentes, como un control positivo, a fin de estar seguro de que el procedimiento se realizó correctamente. Los tumores por lo general un aspecto muy heterogéneo y tienen muchos quistes conectados (Figura 1). El análisis de las muestras tumorales de un patólogo debe mostrar los tejidos diferenciados de las tres capas germinales (Figura 2).
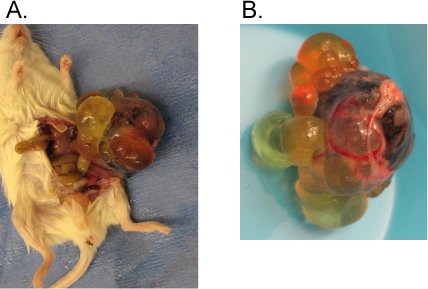
Figura 1. Típica teratoma hPSC deriva en la cápsula del testículo.
Siguiendo el protocolo descrito, un millón de WA09 células se inyectaron en la cápsula testículo de un ratón inmune comprometido. Seis semanas más tarde se observó un teratoma. A) Teratoma retirado del ratón. B) Acercar la imagen del teratoma. Tenga en cuenta la heterogeneidad de las estructuras y el quiste.

Figura 2. Hematoxilina y eosina tiñen secciones del teratoma muestran los tejidos de cada capa germinal.
Tras la fijación, el teratoma era seccionadas y teñidas con hematoxilina y eosina. Análisis por un patólogo reveló la presencia de células de cada una de las 3 capas germinales.
Discusión
El método que aquí se presenta ofrece una alta fiabilidad, los medios directos de la generación de los teratomas de hPSCs en la cápsula del testículo. Hay varios parámetros críticos en esta técnica. En particular, es importante para inyectar líneas hPSC celulares que se sabe que son pluripotentes como control. Otros parámetros importantes incluyen el intervalo de tiempo entre la inyección y la observación del tumor. Para las líneas celulares como WA09, los teratomas se deben observar en 6-8 semanas. Para las nuevas líneas de IPSC nos encontramos con que a menudo se requieren 10 semanas. Otra preocupación es el número de células inyectadas. Se inyecta un millón de células, pero el ensayo se puede hacer fácilmente con un menor número de células. Además, el medio de inyección es importante. Se encuentra que se obtienen los mejores resultados cuando las células se inyectan en una mezcla 1:1 de Matrigel y DMEM/F-12, en oposición a PBS o DMEM/F-12.
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Este trabajo fue financiado por becas CIRM # TR-1250, RT1-01108, y 00502-CL1.
Materiales
| Name | Company | Catalog Number | Comments |
| Nombre del reactivo | Empresa | Número de catálogo | |
| Accutase | Invitrogen | A1110501 | |
| DMEM/F-12 | Invitrogen | 113300-032 | |
| Matrigel | BD Biosciences | 354277 |
Referencias
- Bradley, A., Evans, M., Kaufman, M. H., Robertson, E. Formation of germ-line chimaeras from embryo-derived teratocarcinoma cell lines. Nature. 309, 255-255 (1984).
- Evans, M. J., Kaufman, M. H. Establishment in culture of pluripotential cells from mouse embryos. Nature. 292, 154 (1981).
- Martin, G. R. Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells. Proc. Natl. Acad. Sci. U. S. A. 78, 7634-7634 (1981).
- Downing, G. J., Battey, J. F. Technical assessment of the first 20 years of research using mouse embryonic stem cell lines. Stem Cells. 22, 1168-1168 (2004).
- Thomson, J. A. Embryonic stem cell lines derived from human blastocysts. Science. 282, 1145-1145 (1998).
- Reubinoff, B. E. Embryonic stem cell lines from human blastocysts: somatic differentiation in vitro. Nat Biotechnol. 18, (2000).
- Muller, F. J., Goldmann, J., Loser, P., Loring, J. F. A call to standardize teratoma assays used to define human pluripotent cell lines. Cell Stem Cell. 6, 412-412 (2010).
- Brivanlou, A. H. Stem cells. Setting standards for human embryonic stem cells. Science. 300, 913-913 (2003).
- Lensch, M. W., Schlaeger, T. M., Zon, L. I., Daley, G. Q. Teratoma formation assays with human embryonic stem cells: a rationale for one type of human-animal chimera. Cell Stem Cell. 1, 253-25 (2007).
- Gertow, K. Organized development from human embryonic stem cells after injection into immunodeficient mice. Stem. Cells. Dev. 13, 421-421 (2004).
- Gertow, K. Isolation of human embryonic stem cell-derived teratomas for the assessment of pluripotency. Curr Protoc Stem Cell Biol. Chapter 1, Unit1B 4-Unit1B 4 (2007).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados