Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Formulación de nanopartículas poliméricas mediante la técnica de dibloque Nanoprecipitation
En este artículo
Resumen
En este artículo se describe un método para sintetizar nanoprecipitation a base de polímeros con nanopartículas de copolímeros de bloque doble. Vamos a discutir la síntesis de copolímeros de bloque doble, la técnica nanoprecipitation, y sus posibles aplicaciones.
Resumen
La nanotecnología es una rama relativamente nueva de la ciencia que consiste en aprovechar las propiedades únicas de partículas que están en la escala de nanómetros (nanopartículas). Las nanopartículas pueden ser diseñados de una manera precisa en que la química puede ser su tamaño, la composición y la superficie cuidadosamente controladas. Esto permite una libertad sin precedentes para modificar algunas de las propiedades fundamentales de su carga, como la solubilidad, la difusividad, las características de liberación de biodistribución y la inmunogenicidad. Desde su creación, las nanopartículas se han utilizado en muchas áreas de la ciencia y la medicina, incluyendo la administración de fármacos, imágenes, y la biología celular 1-4. Sin embargo, no se ha utilizado plenamente fuera de "laboratorios de nanotecnología", debido a la barrera percibida técnica. En este artículo se describe un método simple para sintetizar una plataforma basada en nanopartículas de polímeros que cuenta con una amplia gama de aplicaciones potenciales.
El primer paso es sintetizar un copolímero de bloque doble que tiene tanto un dominio hidrofóbico y un dominio hidrofílico. Utilizando PLGA y PEG como polímeros modelo, que describe una reacción de conjugación con EDC / NHS química 5 (Fig. 1). También se discute el proceso de purificación del polímero. El bloque doble sintetizado co-polímero puede auto-ensamblan en las nanopartículas en el proceso de nanoprecipitation a través de interacciones hidrofóbicas hidrofílicos.
Las nanopartículas de polímeros se describe es muy versátil. El núcleo hidrofóbico de las nanopartículas pueden ser utilizadas para llevar a los medicamentos poco solubles para la administración de fármacos experiments6. Además, las nanopartículas pueden superar el problema de solventes tóxicos para los reactivos de biología molecular poco solubles, tales como wortmannin, que requiere un solvente como el DMSO. Sin embargo, el DMSO puede ser tóxico para las células e interferir con el experimento. Estos fármacos poco solubles y los reactivos pueden ser efectivamente entregados el uso de nanopartículas de polímeros con una toxicidad mínima. Nanopartículas de polímeros también se pueden cargar con un colorante fluorescente y se utilizan para los estudios de tráfico intracelular. Por último, estas nanopartículas de polímeros se pueden conjugar a la orientación a través de ligandos PEG superficie. Tales nanopartículas dirigidas pueden ser utilizados para etiquetar epítopos específicos en las células o en 7.10.
Protocolo
1. Síntesis de PLGA-PEG-b polímero
- Poli (D, L-láctico-co-glicólico) (PLGA) con grupos terminales carboxilato (PLGA-carboxilato) se disuelve en los disolventes de PLGA (como se menciona en la sección de materiales) a una concentración de 5 mm. PLGA puede ser disuelto en esta concentración con agitación suave.
- Ambos NHS (peso molecular 115,09) y el EDC (peso molecular 191,7) se disuelven en la solución de PLGA en una concentración de 25 mM. (Tanto la EDC y NHS se añaden en un exceso estequiométrico de 5 veces en comparación con PLGA). PLGA-carboxilato se convierte en PLGA-NHS mediante la adición de EDC y NHS de PLGA-carboxilato de solución con agitación suave durante 1 hora aproximadamente.
- El producto de reacción PLGA-NHS se precipita por la adición de metanol de la solución de lavado. Aproximadamente 10 veces el exceso de volumen de metanol, se añade a la solución. La solución se centrifuga a 2000 xg para precipitar el PLGA-NHS y descartar el sobrenadante (elimina los rastros de la EDC y NHS. Este procedimiento de lavado con metanol se repite al menos tres veces.
- El pellet de PLGA-NHS se seca al vacío durante 30 minutos para eliminar cualquier rastro de la solución de lavado.
- El pellet de PLGA-NHS está re-disuelto en el mismo disolvente a la misma concentración que se utilizó inicialmente para disolver PLGA. El PEG heterobifuncionales (amino-PEG-carboxilato), se añade a la solución de PLGA en una concentración de 5 mm (relación estequiométrica de 1:1). La solución se incuba durante 24 horas con agitación constante.
- Después de 24 horas, el producto de reacción PLGA-PEG-b de copolímero de bloque se precipita por la adición de la solución de lavado de metanol en exceso. Repita el proceso de lavado y centrifugación como se mencionó anteriormente en tres ocasiones. Esto eliminará todos los PEG exceso sin reaccionar.
- El copolímero de PLGA-PEG-b bloques se seca al vacío.
2. PLGA-PEG-b preparación de nanopartículas
Las nanopartículas con núcleo de PLGA cubiertos con PEG a la superficie se pueden preparar con estos copolímeros de bloque doble. Una variedad de diferentes fármacos hidrofóbicos pueden ser encapsulados en nanopartículas. Compuestos fluorescentes puede ser encapsulado en las nanopartículas, o puede ser conjugado con PLGA y por lo tanto estas nanopartículas se pueden utilizar para imágenes de fluorescencia.
Nanoprecipitation método se utiliza para hacer las nanopartículas sobre todo cuando la carga que se desea encapsular es altamente hidrofóbico en la naturaleza.
- El PLGA-PEG-b de copolímero de bloque y de la droga / de carga (a encapsular) son disueltos en cualquier disolvente que disuelve PLGA. PLGA puede ser disuelto por muchos solventes comunes, como acetonitrilo, DCM, tetrahidrofurano, acetona o acetato de etilo. La elección del disolvente es crucial, ya que influye en las propiedades de las nanopartículas. Por lo tanto, disolvente apropiado se debe utilizar en este paso.
- La mezcla de polímero / fármaco se añade gota a gota a 5.3 volúmenes de agua agitando dando una concentración de polímero final de alrededor de 3 mg / ml. (Fig. 2)
- Se mantiene la agitación durante 2 horas a presión reducida para permitir que las nanopartículas se forman por el auto-ensamblaje y eliminar los restos de disolvente orgánico.
- La recolección y purificación: Las nanopartículas son luego se concentró por centrifugación a 2.700 x g durante 10 minutos usando un filtro Amicon (MWCO 20 kDa), se lavan, y se reconstituyó en PBS. Esto elimina toda la carga sin atrapado drogas /. Caracterizaciones biofísicas básicas, tales como tamaño, carga superficial, y la eficiencia de carga de fármaco se puede realizar para comprender mejor las propiedades de las nanopartículas.
3. Almacenamiento
La liofilización es un método comúnmente utilizado para almacenar las nanopartículas 11. La liofilización se conservan las características físicas y químicas de las nanopartículas para la estabilidad a largo plazo 12. El proceso de secado por congelación puede causar la tensión en las partículas y desestabilizar a la formulación, por lo que la crio-protectores (protección contra el estrés de congelación) y lyo-protectores (protección contra el estrés de secado) se utilizan comúnmente. La elección de estos protectores está determinado por el tiempo deseado de almacenamiento 13.
- En el secado por congelación, no es la solidificación total de la muestra mediante la congelación por debajo de su Tg.
- En la etapa de secado, el hielo se elimina por sublimación. Temperatura y la presión debe ser optimizado para lograr un eficiente proceso de liofilización.
4. Los resultados representativos:
Caracterización de PLGA-PEG-b-Di copolímero de bloque
Diferentes técnicas se pueden utilizar para confirmar la conjugación exitosa de los polímeros. La composición de PLGA-PEG-b se puede caracterizar con un 400 MHz 1H resonancia magnética nuclear (RMN). Peso molecular del producto formado (PLGA-PEG-b) puede ser verificada por cromatografía de permeación en gel (GPC). El PLGA-b - PEG de peso molecular distribution la curva y el tiempo de elución debe ser diferente de PLGA y solo PEG. En combinación, estas técnicas deben caracterizar el producto formado y determinar si la reacción de conjugación se ha realizado correctamente.
Caracterización de PLGA-PEG-b nanopartículas
El tamaño de partícula y distribución de tamaño puede ser medido por dispersión de luz dinámica. Diferentes parámetros en el proceso de nanoprecipitation afectar el tamaño de las partículas. Pesos moleculares de los polímeros utilizados inicialmente (tanto PLGA y PEG) también afectan la distribución del tamaño de las partículas. Microscopía de transición de electrones (TEM) también se puede utilizar para confirmar la distribución del tamaño y la estructura de las nanopartículas como se ve en la figura 3. El rango de tamaño de partícula es generalmente en el rango nm. De gran tamaño de partículas con distribución de tamaño irregular podría indicar un error en la reacción de conjugación o la optimización del método nanoprecipitation necesidades. Además, la superficie potencial zeta puede ser medido por ZetaPALS.
La eficiencia de carga de fármaco / carga se puede cuantificar con el estándar de HPLC.
Las partículas se disuelven en disolventes orgánicos y HPLC se pueden realizar para medir la absorción de la droga / carga (Fig. 4). El estudio de cinética de liberación de fármacos se puede hacer cuando se conozca cantidades fijas de las nanopartículas se dializan en 30 Slide-A-Lyzer unidades de diálisis MINI. En intervalos de tiempo fijos, el contenido de la unidad de diálisis se recoge y el mismo volumen de disolvente orgánico, se añade la disolución de las nanopartículas. HPLC se lleva a cabo en estas muestras para cuantificar el contenido de drogas / carga.
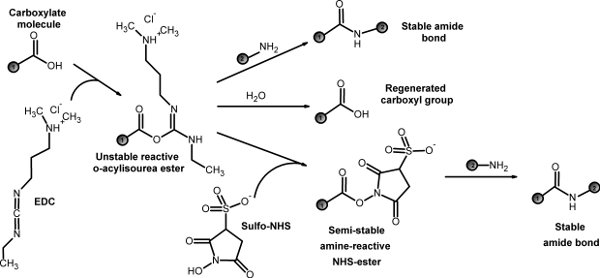
Figura 1. EDC / NHS química
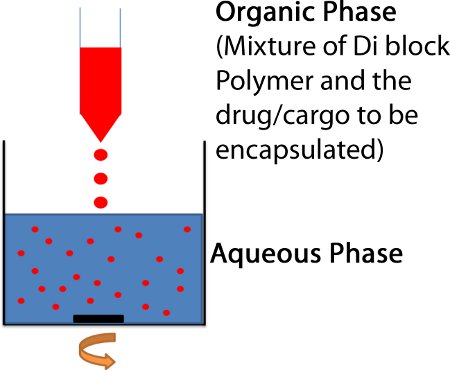
Figura 2. Nanoprecipitation método para la preparación de nanopartículas poliméricas. La solución orgánica de un disolvente (acetonitrilo o DCM) que contiene el bloque doble PEG-PLGA y la droga o la carga que se carga en la partícula se añade gota a gota a 5.3 mL de agitación H 2 O.

Figura 3. Microscopía Electrónica de Transmisión de nanopartices. Una imagen de TEM de PEG-PLGA nanopartículas que contienen wortamin. Ácido fosfotúngstico fue utilizado como un agente de contraste.
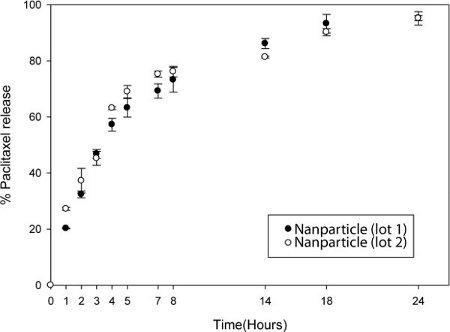
Figura 4. Liberación controlada de drogas a partir de nanopartículas. Liberación de paclitaxel a partir de nanopartículas después de la diálisis en PBS. En el momento señalado, las partículas fueron retirados de cassettes de diálisis y solubilizados en acetonitrilo. La solución se midió por HPLC. Dos lotes separados de las nanopartículas fueron comparados.
Discusión
El método nanoprecipitation con copolímeros de bloque doble representa un método sencillo, rápido para diseñar nanopartículas poliméricas. Las nanopartículas resultantes se componen de un núcleo hidrofóbico que puede ser utilizado para la entrega de los compuestos de baja solubilidad. La capa de superficie hidrofílica permite una excelente solubilidad en el agua mientras que proporciona una fracción de la conjugación más potencial a un ligando de orientación.
Hay muchas plataf...
Divulgaciones
No hay conflictos de interés declarado.
Agradecimientos
Este trabajo fue financiado por los jugadores de golf contra el cáncer, Carolina del Centro para la Nanotecnología piloto beca para la excelencia, la Universidad de Cancer Research Fund y el Instituto Nacional de Salud K-12 Premio de Desarrollo Profesional.
Materiales
| Name | Company | Catalog Number | Comments |
| Reactivo | Empresa | Número de catálogo | Comentarios |
| EDC | Thermo Scientific | 22980 | Conjugación del reactivo |
| NHS | Thermo Scientific | 24500 | Conjugación del reactivo |
| amino-PEG-carboxilato | Laysan Bio Inc. | NH2-PEG-CM-5000 | Polímero (se puede usar cualquier MW PEG, 5000 está en la lista) |
| PLGA-carbxylate | Lactel | B6013-2 | Polímero |
| Diclorometano (DCM) | Sigma-Aldrich | 34856 | Solvente |
| Acetonitrilo> 99% de pureza | Sigma-Aldrich | 34851 | Solvente |
| Metanol> 99% de pureza | Sigma-Aldrich | 34860 | Lavar |
Referencias
- Drotleffa, S., Lungwitz, U., Breuniga, M., Dennis, A., Blunk, T., Tessmarc, J., Goëpferich, A. Biomimetic polymers in pharmaceutical and biomedical sciences. European Journal of Pharmaceutics and Biopharmaceutics. 58, 385-407 (2004).
- Bulte, J. W. M. . Nanoparticles in Biomedical Imaging. 3, (2008).
- Omid, C., Farokhzad, R. L. Impact of Nanotechnology on Drug Delivery. ACS NANO. 3, 16-20 (2009).
- Li, Y. -. P., Pei, Y. -. Y., Xian-Ying, Z., Zhou-Hui, G., Zhao-Hui, Z., Wei-Fang, Y., Jian-Jun, Z., Jian-Hua, Z., Xiu-Jian, G. PEGylated PLGA nanoparticles as protein carriers: synthesis, preparation and biodistribution in rats. Journal of Controlled Release. 71, 203-211 (2011).
- Hermanson, G. T. . Bioconjugate techniques. , (2008).
- Jeong, B., Bae, Y. H., Lee, D. S., Kim, S. W. Biodegradable block copolymers as injectable drug-delivery systems. Nature. 388, 860-862 (1997).
- Yoo, H. S., Park, T. G. Folate receptor targeted biodegradable polymeric doxorubicin micelles. Journal of Controlled Release. 96, 273-283 (2004).
- Cheng, J., Teply, B. A., Sherifi, I., Sung, J., Luther, G., Gu, F. X., Levy-Nissenbaum, E., Radovic-Moreno, A. F., Langer, R., Farokhzad, O. C. Formulation of Functionalized PLGA-PEG Nanoparticles for In Vivo Targeted Drug Delivery. Biomaterials. 28, 869-876 (2007).
- Gu, F., Zhang, L. F., Teply, B. A., Mann, N., Wang, A., Radovic-Moreno, A. F., Langer, R., Farokhzad, O. C. Precise engineering of targeted nanoparticles by using self-assembled biointegrated block copolymers. Proceedings of the National Academy of Science. 105, 2586-2591 (2008).
- Sanna, V., Pintus, G., Roggio, A. M., Punzoni, A., Posadino, A. M., Arca, A., Marceddu, S., Bandiera, P., Uzzau, S., Sechi, M. Targeted Biocompatible Nanoparticles for the Delivery of (-)-Epigallocatechin 3-Gallate to Prostate Cancer Cells. J. Med. Chem. 54, 1321-1332 (2011).
- Abdelwahed, W., Degobert, G., Stainmesse, S., Fessi, H. Freeze-drying of nanoparticles: Formulation, process and storage considerations. Advanced Drug Delivery Reviews. 58, 1688-1713 (2006).
- Holzer, M., Vogel, V., Mäntele, W., Schwartz, D., Haase, W., Langer, K. Physico-chemical characterisation of PLGA nanoparticles after freeze-drying and storage. European Journal of Pharmaceutics and Biopharmaceutics. 72, 428-437 (2009).
- Lee, M. K., Kim, M. Y., Kim, S., Lee, J. Cryoprotectants for Freeze Drying of Drug Nano-Suspensions: Effect of Freezing Rate. Journal of Pharmaceutical Sciences. 98, 4808-4817 (2009).
- Wang, A. Z. Biofunctionalized targeted nanoparticles for therapeutic applications. Expert opinion on biological therapy. 8, 1063-1070 (2008).
- Jeong, B., Bae, Y. H., Kim, S. W. Drug release from biodegradable injectable thermosensitive hydrogel of PEG-PLGA-PEG triblock copolymers. J. Control Release. 63, 155-163 (2000).
- Gref, R. Biodegradable long-circulating polymeric nanospheres. Science. 263, 1600-1603 (1994).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados