Method Article
Biopolímeros Nano basados en ácido polimálico de Focalización de múltiples Marcadores tumorales: una oportunidad para la medicina personalizada?
En este artículo
Resumen
Un ejemplo de un fármaco de nano a base de ácido polimálico se presenta hacia el diseño racional de la medicina personalizada que es aplicable al cáncer. En él se describe la síntesis de un fármaco nano para tratar el cáncer de mama HER2-positivo humano en un ratón desnudo.
Resumen
Tumors with similar grade and morphology often respond differently to the same treatment because of variations in molecular profiling. To account for this diversity, personalized medicine is developed for silencing malignancy associated genes. Nano drugs fit these needs by targeting tumor and delivering antisense oligonucleotides for silencing of genes. As drugs for the treatment are often administered repeatedly, absence of toxicity and negligible immune response are desirable. In the example presented here, a nano medicine is synthesized from the biodegradable, non-toxic and non-immunogenic platform polymalic acid by controlled chemical ligation of antisense oligonucleotides and tumor targeting molecules. The synthesis and treatment is exemplified for human Her2-positive breast cancer using an experimental mouse model. The case can be translated towards synthesis and treatment of other tumors.
Introducción
En la era post-genómica en genomas de cáncer se han desentrañado (Centro Nacional de Biotecnología y el Atlas del Genoma del Cáncer), el tratamiento futuro del cáncer representará la diversidad genética de los tumores a menudo dentro del mismo tumor 1-4. Bioinformática y rápido, no es caro secuenciación de ADN permite la adquisición de genes / mutaciones malignas a nivel personal 2,4,5. Una vez que los genes han sido identificados, los pacientes serán tratados con la medicina personalizada para modificar o silenciar la expresión de genes malignos 6. La necesidad de dirigirse a las células cancerosas y liberar fármacos en estas células requiere de sistemas de entrega polifuncionales. Obviamente, las drogas nano pueden cumplir con este requisito 7.
En una ola creciente de descubrimientos nanopartículas han demostrado ser adecuado para llevar las cargas útiles de los fármacos quimioterapéuticos, proteínas y / o material genéticamente activa a las células cancerosas. Sin embargo, los efectos adversos siguen siendo advestida. Uno de ellos relacionado con la falta de biodegradabilidad puede causar la deposición de material en el tejido y órganos sanos con la probabilidad de provocar enfermedades. Para minimizar la deposición, se introdujo ácido polimálico no tóxico y no inmunogénico, que es de origen microbiano y biodegradable a H 2 O y CO 2 8. Utilizamos el polímero para sintetizar un tipo covalente todo-en-uno de la droga nano. Contiene agentes quimioterapéuticos unidos químicamente tales como temozolomida, doxorrubicina, o los oligonucleótidos antisentido y los grupos funcionales que sirven extravasación, la orientación del tejido, la entrega endosomolítico. Las drogas están intrínsecamente escinden de la plataforma nano cuando llegaron a la célula tumoral específica, regenerando así su actividad farmacéutica completa.
Se describe el método de producción microbiana de la plataforma nano polímero, su purificación, y la síntesis química de un fármaco que contiene nano Trastuzumab (Herceptin) para el cáncerfocalización y un oligonucleótido antisentido para la inhibición de HER2 sobreproducción. En la aplicación de la droga nano a xenogeneico cáncer de mama HER2-positivo humano en ratones desnudos, se demuestra una alta eficacia del tratamiento contra el cáncer. Los principios de la orientación del tumor y el silenciamiento de gen introducido aquí para medicamentos nano ácido polimálico se pueden aplicar en el tratamiento de otros casos de cáncer.
Protocolo
Todos los experimentos se ajustan a las disposiciones oficiales de los animales, incluidos los procedimientos quirúrgicos y no quirúrgicos realizados en vivo y están en plena conformidad con los protocolos del IACUC.
1. Bioproducción de ácido polimálico
- Haga crecer un cultivo de siembra de esférulas en agar y la transferencia de los plasmodios a 100 ml de medio de cultivo utilizando un 25 ° C Thermo declarado incubadora y medio de cultivo basal 8,9.
- Produce una cantidad de gravedad llena 500 ml plasmodios micro bajo la exclusión de la luz con el fin de evitar la esporulación.
- Preparar 80 g de CaCO 3 en suspensión en 8 L de medio basal en 10 L de recipiente biorreactor. Transferir los 500 ml envasados plasmodios micro en el recipiente de reacción montado y permitir que el bioproceso de 75 horas a 25 ° C, 10 L / min de flujo de aire filtrado y 150 rpm de agitación mediante un agitador segmento.
- Terminar cuando el caldo de cultivo tiene un pH de 4,8 que indica el final de la producción de MPLA y medir el contenido de MPLA por tque hidroxamato / Fe (III) de ensayo.
- Enfriar el caldo a 17 ° C y permiten que las células se asienten por gravedad.
- Se enfría a 4 ° C y ajustar el pH a 7,5, utilice 2 M NaOH. Bombear el sobrenadante a través de una columna llena con 1,5 l de DEAE-celulosa en la parte inferior dirección hacia arriba (DEAE grano grueso, equilibrada con 20 mM de Tris-HCl, pH 7.5 a 5 ° C).
- Lavar con 3 columnas de tampón que contiene NaCl 0,3 M después de cambiar la dirección de arriba a abajo y eluir PMLA en presencia de 0,7 M de NaCl.
- Ajuste a 0,1 M CaCl2 y precipitar PMLA-Calcio con 80% etanol helado. Fraccionar sobre Sephadex G25 en PMLA-calcio de 80 a 300 kDa, 50 - 80 kDa, y 10 - 50 kDa, utilizar agua en ausencia de tampón y sal.
- Pasar cada fracción sobre un 120H + columna de Amberlite IR, y congelar inmediatamente el ácido polimálico de flujo a través en nitrógeno líquido durante la liofilización.
- Disolver en acetona seca. Después de la filtración, el disolvente se retiraen la corriente de aire seco, se liofiliza y se almacena a -20 ° C.
2. Síntesis de a base de ácido polimálico Nano Drogas
- Activar grupos carboxilo de MPLA (P) mediante la mezcla de 116 mg (1 mmol unidades malyl) de PMLA-H en 1 ml de acetona anhidra y 1 mmol de N-hidroxisuccinimida y 1 mmol diciclohexil carbodiimida en 2 ml de dimetil formamida (DMF). Se agita a 20 ° C durante 3 h. Añadir 0,05 mmol de mPEG 5000-NH 2 (0,05% en moles de unidades malyl) en 1 ml de DMF seguido de 0,05 mmol de trietilamina (TEA).
- Añadir gota a gota disuelto en DMF 0,4 mmol de éster etílico de leucina (Loet) (40% en moles de unidades malyl), 0,1 mmol de ácido 2-tiol-1-etilamina (2-MEA) (10% en moles de unidades malyl) y 0,5 mmoles de TEA, todos disueltos en DMF. Después de cada adición, deje 1 hora y compruebe que no se completó la reacción de ninhidrina negativo de respuesta (capa-cromatografía fina, TLC).
- No retire los restos de éster NHS por hidrólisis espontánea con solución salina tamponada con fosfato (30 min, pH 6,8). Desalar más de PD-10 Columna, obtener "preconjugate" como un polvo blanco por liofilización. Seco tienda a menos 20 ° C.
- Disolver 30 mg de anticuerpo (mAb, IgG2a-κ) en 4,5 ml de fosfato de sodio 100 mM, NaCl 150 mM, pH 5,5.
- Reducir los enlaces disulfuro con Tris 5 mM (acetato de 2-carboxi) de clorhidrato de fosfina durante 30 min a 20 ° C y purificar sobre columna PD-10.
- Disolver Mal-PEG 3400-MAL en 2 ml del mismo tampón y añadir el mAb reducido a un volumen final de 10 ml y se agita durante la noche a 4 ° C. Se concentra hasta 2,5 ml durante Vivaspin 20, la exclusión de 30 kDa, y purificar a través de Sephadex G75. Verifique producto sobre sec-HPLC y medir la cantidad fotométrica a 280 nm de longitud de onda.
- Adjuntar Mal-PEG-MAL-mAb a "preconjugate" tioles obtención de P / PEG 5000 (5%) / Loet (40%) / mAb (0,2%) / 2-MEA (10%). Para ello, mezclar 5 ml de 200 nmol mAb-PEG 3400-Mal a 50 mg (p / mPEG 5000 / LOEt/2-MEA) en el pH por encima de 5,5, ajustar la concentración de sulfhyDryl a 2 mM y se incuba a 20 ° C durante 3 horas (rendimiento 98%).
- Solubilizar 3'-H 2 N-AON en DMF / PBS (pH 7,2) y reaccionar con N-succinimidil-3-(2-piridilditio) propionato (SPDP) en (01:01 v / v) de DMF / metanol (prueba de ninhidrina ) y purificar AON-PDP sobre Sephadex LH20-en metanol, y luego en agua y se liofiliza.
- Incubar 800 nmol AONs activados en el buffer de pH 5,5 con el Mal-PEG 3400-Mal-MAB-preconjugate anteriormente preparado durante toda la noche hasta que se termina la reacción de intercambio de disulfuro.
- Incorporar fluorescente Alexa Fluor 680-maleimida formando tioéter con polímero-2-MEA-SH. Bloquear el exceso de sulfhidrilos con 3-piridilditio-propionato (PDP) y purificar sobre Sephadex G75. Almacenar a 4 ° C o se congeló a -80 ° C hasta su uso posterior.
3. Ensayos y Propiedades
- Realizar pruebas para la pureza y la estabilidad en PBS y suero a 4 ° C y 37 ° C por análisis SEC-HPLC. Utilice sulfonato poliestireno como molecLos estándares de peso Ular. Mida distribución de tamaño nano y zeta potenciales. Utilice los sistemas comerciales.
- Añadir a 320 l muestra de 160 l de 10% (w / v) de cloruro de hidroxilamonio y 160 l de 10% (w / v) de NaOH. Después de 10-15 minutos, mezclar con 160 l de 5% (w / v) de Fe (III) Cl 3 en el 12% (v / v) de HCl y leer A 540 de hidroxamato / Fe (III). Calcular PMLA asumiendo 1 mg / ml PMLA corresponde a 2,5 A 540.
- Hidrolizar el fármaco de nano durante la noche en HCl 2 M a 110 ° C y ensayo de ácido málico en la cromatografía de fase inversa con referencia a las muestras cargadas con las normas de ácido málico. Cleave la droga nano con ditiotreitol 100 mM y medir Morpholino-AON por HPLC en fase reversa cuantitativa frente a estándares Morpholino AON.
- Tomar drogas nano sin escote y medir anticuerpos usando un kit de ensayo de proteínas. Cuantificar mPEG al permitir que su reacción con ferrothiocyanate amonio, a continuación, se extrae con cloroformo y leer la absorbencia a 510 nm de longitud de onda 10 .
- Realice ELISA con 5 l de drogas nano (1-10 mg MAB) por pocillo ensayar la actividad de anticuerpos y coligación. Utilice 0,5 mg / pocillo receptor de transferrina y HER2, respectivamente, como antígenos de placa recubierta y anticuerpos secundarios acoplados a peroxidasa.
- Calcular logrado% para AON, MPEG y mAb con respecto a ácido málico (100%) y comparar con el% previsto por diseño (ver ejemplos Tabla 1 y Tabla 2).
4. Pruebas in vitro
- Incubar el fármaco nano con células cancerosas cultivadas y medida de células supervivientes con el tiempo por su actividad para reducir reactivo amarillo [3 - (4,5-dimetiltiazol-2-il) -5 - (3-carboximetoxifenil) -2 - (4-sulfofenil )-2H-tetrazolio, sal interna] (MTS) a un colorante azul y leer la absorbancia relativa con un fotómetro. Siga las instrucciones del proveedor kit.
- Preparar extractos de células in vitro o ex vivo para la transferencia Western. Utilice helada extracción buffer que contiene SDS y cóctel inhibidor de la proteasa. Proteínas separadas por electroforesis en gel de reducción de SDS-poliacrilamida.
- Realice el Western Blot para las proteínas de interés en los extractos de la muestra. Utilice anticuerpos secundarios conjugados con fosfatasa alcalina.
- Uso de la microscopia confocal para demostrar la captación celular y co-localización de nano plataforma de polímero de drogas, AON y endosomas usando etiquetado de fluorescencia. Adjunte Alexa Fluor 680 a la plataforma conjugado nano y Lissamina a AONs como etiquetas fluorescentes. Utilice un microscopio 5X escáner espectral y células cancerosas vivas para visualizar la distribución de las moléculas marcadas
- Membranas endosoma mancha con tinte fluorescente Estiril Red y demuestran colocalización endosoma o liberación.
5. Ensayo in vivo
- Preparar el modelo de ratón de cáncer de mama positivo para HER2 humana (Tac de ratón desnudo: Cr: (MCR)-Foxnnm). Inserte un 0,72 mg liberando pellet 17β-estradiol (versión 90-días) subcutaneously en el cuello de cada ratón.
- Luego inyecte 1 x 10 7 células tumorales BT-474 por vía subcutánea en el flanco derecho y se dejó crecer el tumor.
- Iniciar el tratamiento cuando los tumores son 120 mm 3 en tamaño mediante la inyección en la vena de la cola 150 conjugado nano l que contiene 2,5 mg / kg de AON y / o 4,5 mg / kg de cada anticuerpo. Para el tratamiento inyectar dos veces por semana, total de seis veces.
- Mida el tamaño del tumor con calibres dos veces el débil y el cálculo de volúmenes utilizando la fórmula (longitud x profundidad x anchura) x (π / 6). La eutanasia a los animales 2 semanas después de la inyección final y después de la sedación con una solución de ketamina y dexmedetomidina seguido por dislocación cervical.
- Aislar los tumores y las secciones de tinción con H & E para la evaluación morfológica.
- Para la evaluación de la distribución de drogas a escala animal, utilizar un sistema de imágenes de fluorescencia. Inyectar la Alexa Fluor 680 drogas nano etiqueta e imagen a las 24 y 48 h.
- La eutanasia a los animales y detectar el fluorEscence en tumores y órganos aislados y perfundidos.
Resultados
La inhibición del cáncer de mama HER2-positivo humano silenciando la expresión del receptor HER2 y el bloqueo de la señalización de HER2-12
Estrategia
Entre las diferentes formas de cáncer de mama humano, los tumores HER2-positivos tienen el peor resultado clínico. Se presenta el tratamiento exitoso del cáncer de mama con sobreexpresión de HER2 humana en el modelo de ratón desnudo. La estrategia consiste en el fármaco activo tanto en el silenciamiento inmediata de la vía de señalización de HER2 empleando Herceptin y HER2-específica AON para el bloqueo de la síntesis depende de HER2-ARNm del receptor (Figura 1) nano. El conjugado nano plomo, que contiene Herceptin y anti-HER2 AON se muestra en la Figura 3, junto con dos controles que carecen de cualquiera de Herceptin o AON. El principal compuesto contenía anti-MsTfRmAb lograr extravasación activa de transcitosis through unión endotelial TfR de los vasos tumorales. Mucho menos la captación en el tumor se observó en ausencia del anticuerpo y se atribuyó a un tumor efecto EPR dependiente 13. Versiones fluorescentes de los conjugados que contienen nano Alexa Fluor 680 fueron sintetizados por los estudios de imagen.
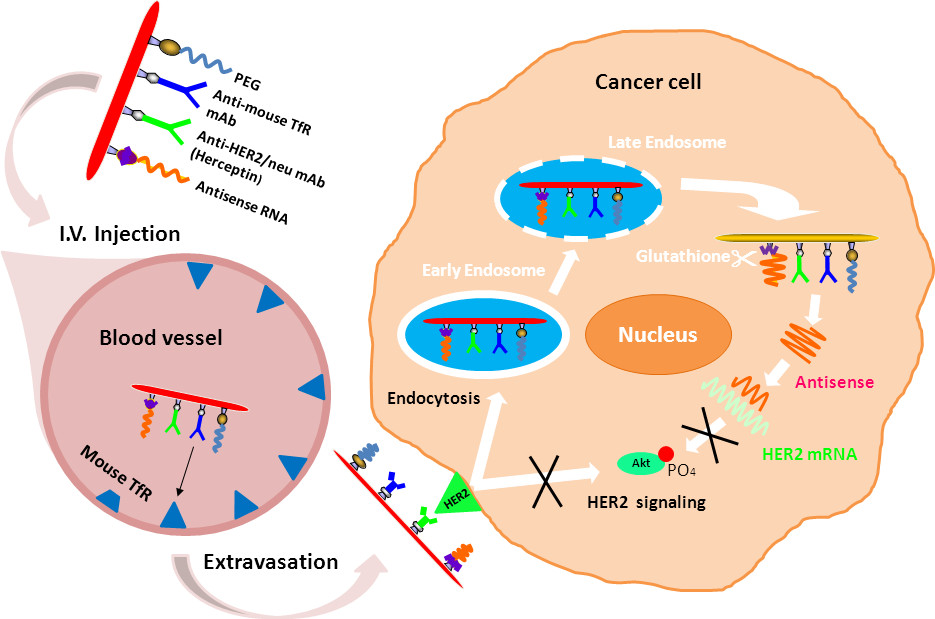
. Figura 1 Mecanismo de entrega AON en células de cáncer de mama HER2-positivo y la inhibición del crecimiento tumoral Esquina superior izquierda:. Nano conjugado una adaptación de la figura 3. Esquina inferior izquierda: vasos tumorales de ratón que expresan TfR en la superficie. El fármaco de nano se une al receptor y entra en el tumor por transcitosis. Además, cierto grado de acceso al tumor es posible a través de las capas endoteliales desordenados que participan en el tumor incremento de la absorción y retenti dependienteen (EPR) 13. A continuación, el nanodroga se une a HER2 expresado en las células de cáncer humano y internaliza en los endosomas tempranos. Encuadernación bloques también HER2 vía de señalización. Después de la maduración de los endosomas y su acidificación, se activa el mecanismo de escape del endosoma del fármaco de nano. Nanodroga de entrar en el citoplasma se libera de la plataforma de nano por escisión reductora del disulfuro de espaciador y se une a HER2-ARNm de bloqueo de HER2-síntesis. El bloqueo de la síntesis se extiende el bloqueo de la señalización de HER2-e induce la inhibición del crecimiento tumoral.
La producción microbiana de la plataforma ácido polimálico
La plataforma conjugado nano, ácido polimálico (PMLA), fue producido por microplasmodia culta de Physarum polycephalum y purificado del caldo como se describe en el Protocolo y se representa en la figura 2. Producción y purificación eran lisas y reproducible. Era importante para cont tiempo de rol, el pH y la temperatura para evitar la división espontánea del polímero. Se recomienda el lavado cuidadoso y la elución de DEAE-columna con el fin de eliminar el ADN, los carbohidratos, las toxinas y material de color. Extrema pureza se obtuvo después de disolver en acetona anhidra y la eliminación de material insoluble. Importe total del producido PMLA fue de 5 ± 1 g por campaña. Las cantidades de 1,5 ± 0,5 g altamente purificados PMPLA de M w 80.000-100.000 se lograron reproducible cuando se usa el biorreactor de 10 l. Perfiles de elución Sec-HPLC eran simétricos. Análisis de dispersión de luz dinámica de acuerdo con la distribución número indicaba un solo pico correspondiente a un diámetro hidrodinámico de 8 ± 1 nm y un índice de polidispersidad de PDI = 0,10 ± 0,02, calculado por el software del instrumento para partículas esféricas asumidos. Potencial Zeta fue de -22 ± 2 mV (pH 7,5).
/ 50668/50668fig2highres.jpg "width =" 500 "/>
Figura 2. Producción y purificación de ácido polimálico desde cultivadas plasmodios micro de Physarum polycephalum (adaptado de Lee et al. 9). Ácido polimálico (MPLA) se produce a partir de plasmodios de Physarum polycephalum en un biorreactor y se recogió del sobrenadante de cultivo mediante la unión de intercambiador de aniones (DEAE). El eluyente se precipitó-etanol como sal de calcio. Soluciones de la sal de calcio son Mw fraccionaron sobre Sephadex-G25-. Fracciones que contienen PMLA se convierten de la Ca-sal en el ácido sobre Amberlite IR-120H +. La libre PMLA finalmente se liofilizó para dar un polvo blanco seco.
La síntesis química del conjugado nano plomo
P / mPEG 5000 (5%) / Loet (40%) / AON (2,5%) / Herceptin (0,2%) / una nti-MsTfRmAb (0,2%)
Las estructuras esquemáticas de la droga nano plomo y de dos conjugados nano precursor se muestran en la Fig. 3 Ure. El cable contiene todos los constituyentes, mientras que los precursores fueron diseñados para carecer de cualquiera de AON HER2 o el anticuerpo Herceptin. Además de AON y mAb, los compuestos que contiene polietilenglicol, MPEG 5000, para minimizar la unión a las proteínas plasmáticas, el aclaramiento a través del sistema retículo-endotelial (RES), y la degradación por escisión enzimática. La secuencia antisentido 5'-CAT-GGT-GCT-CAC-TGC-GGC-TCC-GGC-3 'es complementaria a Her2 ARNm y ha sido cuidadosamente probado in vitro en varias líneas celulares que expresan HER2 para obtener una alta especificidad hacia el bloqueo de HER2 síntesis y no muestra los efectos fuera de la meta.
8/50668fig3highres.jpg "width =" 500 "/>
Figura 3. Nano conjuga para tratar el cáncer de mama HER2-positivo humano. Liderando drogas nano (estructura superior) contiene dos fármacos (Herceptin, AON HER2). Versiones 2 y 3 contienen sólo uno de los medicamentos. La absorción de 1 y 2 en las células tumorales que sobreexpresan HER2-humanos está gestionado por la unión de Herceptin. Nano conjugado 3, que no contiene Herceptin, recibió anti-HuTfRmAb para la absorción endosoma por las células humanas. La conjugación con Alexa Fluor 680 era opcional para los propósitos de formación de imágenes. La barra roja representa la plataforma conjugado nano PMLA / Loet (40%). % Indica la fracción de residuos de ácido málico consumidos en la unión del ligando indicado (cantidad total de residuos de ácido málico en el nanodroga = 100%).
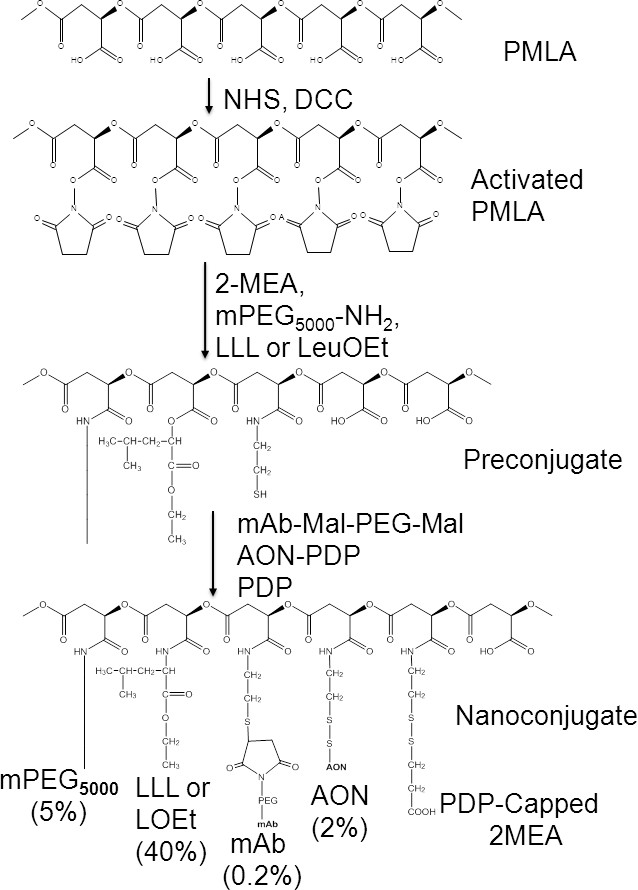
Figura 4. La síntesis química de nanoconjugados P / Loet / AON HER2 / anti-MsTfR/Herceptin De arriba a abajo:. Síntesis de succinimidiléster PMLA-N-hidroxi (PMLA-NHS) de carboxilatos colgante (activación química). Reemplazo de NHS por formación de amida con 2-mercapto-1-aminoethan (2-MEA), metil-PEG 5000-amina (mPEG 5000-NH 2), trileucina (LLL) o leucina éster etílico (Loet). Este "preconjugate" concede mAb-Mal-PEG-Mal por tioéter formación y AON por la formación de enlaces disulfuro escindibles. Restos de 2-MEA tiene un tope formando ácido amidoetil-ditio-propiónico. Sólo se muestra la unión de una sola mAb. Múltiples archivos adjuntos se gestionan mediante el uso de mezclas de mAbs. Porcentaje% denota fracciones de carboxilatos unidos a diversos ligandos (100% gratis PMLA).
Los conjugados de nanopartículas se sintetizaron como se indica en la figura 4 Ure. El peso molecular calculado de la ventajaconjugado era 719.000. El rendimiento global de la síntesis fue 45 ± 5% con respecto al contenido de ácido málico. En promedio, de las 862 unidades malyl (= 100%) de la plataforma 100 kDa de MPLA, 40% lleva a Loet, 5% de mPEG, 2% AON 2%, 0,2% y 0,2% Herceptin anti-MsTfR mAb. La cantidad para cada anticuerpo correspondió a un promedio de 1,7 moléculas por molécula de plataforma PMLA. El% diseñado y el% que se verificó mediante análisis de grupo eran los mismos dentro de ± 5%. Un ejemplo es el caso dado en la Tabla 1 para el cálculo del contenido experimental de ácido málico, AON, mAb y mPEG 5000 y en la Tabla 2 muestra la comparación con el contenido por diseño. La alta pureza de acuerdo con los criterios establecidos en la sección 3 se logró sobre la base de altos rendimientos de reacción y separación eficiente por exclusión de tamaño (por ejemplo, libre de mAb y mAb-nanoconjugate están separados por 1 min en sec-HPLC), y la solubilidad selectiva en disolventes. La actividad de los anticuerpos monoclonales fue se muestra para ser retenido a lo largo de la síntesis de drogas nano, y se confirmó que los dos tipos de anticuerpos fueron ensamblados en la misma plataforma de polímero. El resultado de atípico experimento de ELISA se muestra en la figura 5 Ure. En general, los ensayos para el análisis cuantitativo grupo para el ácido málico, AON, proteína, PEG y para ELISA fueron robusta, dando resultados reproducibles cuando se realiza por personal diferente y la instrumentación no sólo en el caso de la síntesis descrita, sino también cuando se utilizan para el análisis de otros nanoconjugados sintetizados.

Tabla 1. Cálculo de la composición nanodroga con referencia al contenido de ácido málico.
668table2.jpg "width =" 600 "/>
Tabla 2. Comparación de la composición de fármaco de nano experimental con composición diseñada.
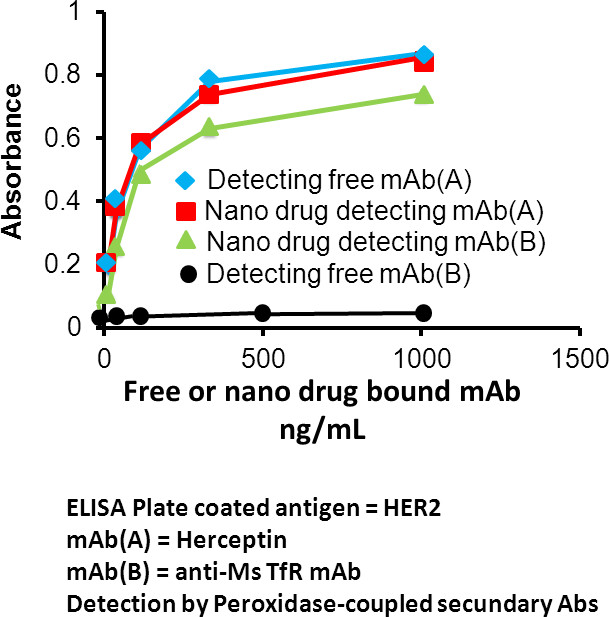
Figura 5. ELISA para la medición de la afinidad del anticuerpo después de la síntesis química, y para la demostración de unión múltiple de diferentes anticuerpos. El fármaco de nano contiene anticuerpo mAb (A) y anticuerpo mAb (B) contra los antígenos A y B, respectivamente. Las placas de ELISA se recubren con antígeno (A). Libre de mAb (A), el mAb libre (B), y drogas nano se aplican a placas de ELISA. Después del lavado, los anticuerpos se prueban con peroxidasa secundaria anticuerpos acoplados específicos para mAb (A) o mAb (B), mientras que sólo el mAb (A) se une a antígeno (A). Se ve que el fármaco libre y nano conjugado con mAb (A), e indirectamente anticuerpo monoclonal conjugado (B) de la misma molécula de fármaco de nano, pero no libre de mAb (B), Se conservan en el plato. La dependencia de la concentración muestra afinidades de unión comparables para el mAb libre y conjugada (A), lo que indica que la conjugación química no afectó a la actividad de unión del anticuerpo. Por otra parte, el co-ligación de mAb (B) con el mAb (A) en la misma entidad física (plataforma nano) resultados en mAb (B) la detección de anticuerpos. Los resultados experimentales mostrados aquí se refieren a TfRmAb anti-humano (A) y anti-ratón TfRmAb (B). Resultados similares se han demostrado para otras parejas de anticuerpos probados, tales como anti-MsTfR mAb y anti-HER2 MAB (Herceptin).
La investigación indicó fisicoquímica diámetro hidrodinámico 22,1 ± 2,3 nm para P / mPEG (5%) / Loet (40%) / AON (2%) / Herceptin (0,2%) / anti-MsTfRmAb (0,2%) (plomo, los dos- versión de drogas), 20,1 ± 2,4 nm para P / mPEG (5%) / Loet (40%) / AON (2%) / anti-MsTfRmAb (0,2%) / anti-HuTfRmAb (0,2%) (la versión de drogas AON) , y 15,1 ± 1,2 nm para P / mPEG (5%) / Loet (40%) / Herceptin (0,2%) (la versión de drogas Herceptin). Zeta-potenciales a pH 70.5 fueron en este orden -5,2 ± 0,4 mV, -5,7 ± 0,6 mV, y -4,1 ± 0,4 mV. Cabe mencionar que el diámetro hidrodinámico medido de conjugados nano no siguió la aditividad de los diámetros medidos para los componentes libres.
La entrega de la droga nano a través de la membrana de la célula tumoral y la liberación en el citoplasma después de 0 horas y 3h r
La entrega de fármaco de nano a través de la membrana celular por la absorción endosoma se muestra en la figura 6 Ure después de 0 horas y 3 horas. Etiquetas de fluorescencia están unidos a la plataforma nano de drogas (Alexa Fluor 680, verde) y para AON (lisamina, rojo). Su superposición se muestra en los paneles D y L y junto con la fluorescencia de endosomas marcados (azul) en los paneles de G & O. Coeficientes de correlación de Pearson (R (r) se calcula a partir de las imágenes en relación con la co-localización de la plataforma / endosomas, AON / endosomas, la plataforma / AON de 0 hy 3 h. Tque la imagen hr 3 indica la liberación de endosomas en el citoplasma y la disociación de AON de la droga nano por el glutatión dependiente de disulfuro de escisión en el citoplasma.

Figura 6. La microscopía confocal de la absorción de conjugado de nano por las células diana (adaptado de Ding et al. 11). Las células se incubaron durante 30 min a 37 ° C con drogas nano que había sido doblemente marcado con Alexa Fluor 680 (verde) en la plataforma de polímero y con lisamina (rojo) unido a AON. Además, los endosomas se tiñeron con FM1-43 (azul). La localización se muestra después de las 0 horas (A) y 3 horas (B) incubación. Los paneles A, AB, B y, ij muestran la tinción de los fluoróforos conjugados nano solo, ysu co-localización en A, cd & B, kl. Además, la tinción de endosomas se muestra en los paneles A, E y B, M y la colocalización de conjugado nano y paneles endosomesin A, fg & B, no. Los paneles A, h & B, contraste p espectáculo fase para paneles respectivos. (C) de correlación de Pearson coeficientes de R (r) para la colocalización de la plataforma-endosomas, AON-endosomas, plataforma-AON calculado para las 0 horas y 3 horas. Por favor, haga clic en aquí para ver una versión más grande de esta figura.
La inhibición de cáncer de mama humano in vitro e in vivo
En la inhibición del crecimiento in vitro de células que sobreexpresan HER2 línea BT-474 en comcomparación con una baja línea celular expresando MDA-MB-231 se muestra en la fig ure 7. Grado de inhibición es del 50% y 30%, respectivamente, por el plomo conjugado nano P / MPEG / Loet / AON HER2 / Herceptin / anti-MsTfRmAb. Inhibición por los otros compuestos es menor pero mayor para BT-474 que para MDA-MB-231 células. Línea celular BT-474 fue elegido para el tratamiento de cáncer de mama xenogeneico ratón.
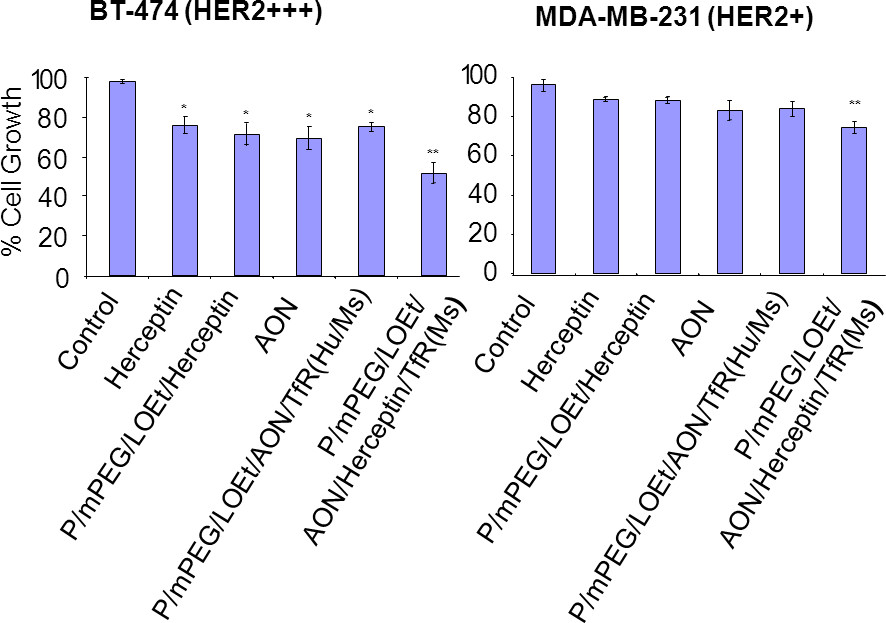
Figura 7. Inhibición del crecimiento in vitro de que sobreexpresan HER2 BT-474 células de cáncer de mama y de bajo expresando MDA-MB-231 células (adaptado de Inoue et al. 12). Comparación de la inhibición del crecimiento para que sobreexpresan HER2 BT-474 línea celular de cáncer de mama ( izquierda) y de HER2 bajo expresando línea celular de cáncer de mama MDA-MB-231 (a la derecha). TfR (s) denota anti-MsTfRmAb y TfR (Hu / Ms) marca el anti-HuTfRmAb y anti-MsTfRmAb. El fármaco de nano plomo, P / MPEG / Loet / AON HER2 / Herceptin / TfR (MS), y las drogas nano desprovistos de cualquiera de Herceptin o AON de HER2 se comparan con PBS, Herceptin y AON HER2. En la ausencia de Herceptin, anti-MsTfRmAb se conjugó para proporcionar la absorción de endosoma por las células tumorales. Las concentraciones fueron 40 g / ml con respecto a los anticuerpos, 4 M con respecto a AON HER2, 4 M endoporter (aplicación de AON). Importancia denota por *, P <0,05: **, P <0,02: ***, P <0,003 en comparación con PBS.
Los resultados del tratamiento in vivo en la Figura 8 se presentan para ratones portadores de BT-474 que sobreexpresan HER2 cáncer de mama humano. El crecimiento se inhibió> 95% por el nanodroga plomo que contiene Herceptin y HER2-específica AON en comparación con los controles tratados sólo con PBS (Fig. Ure 8). Inhibiciónera 60% o menos con Herceptin solo, P / MPEG / Loet / Herceptin o P / MPEG / Loet / AON / anti-MsTfRmAb / anti-HuTfRmAb. Western blot de extractos tumorales mostró inhibición tanto de la síntesis de HER2 y la fosforilación de Akt, pero ningún cambio de Akt total y la enzima GAPDH. PARP se escindió en correspondencia con un aumento del nivel de apoptosis. Imágenes de tumor después del tratamiento, y secciones de tejido teñidas con H & E que ilustra la regresión del tumor se muestran en la Fig. 9 Ure.
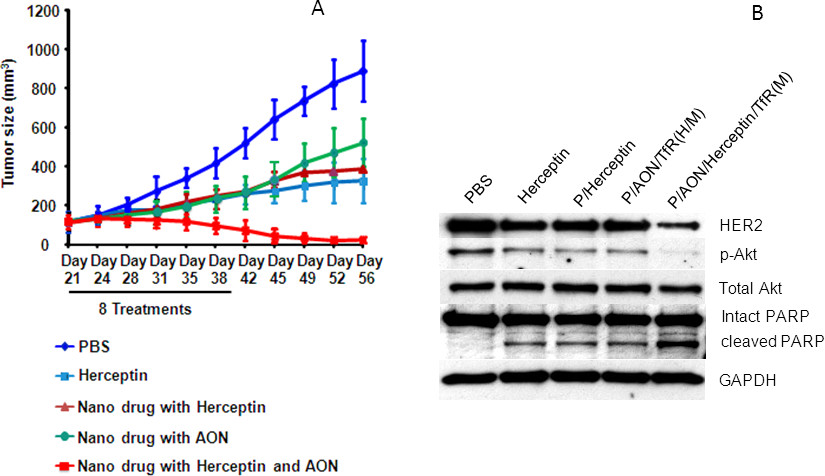
Figura 8. El tamaño del tumor y las proteínas durante el tratamiento con medicamentos nano de plomo y precursores (adaptado de Inoue et al. 12). Un tamaño del tumor. Para los distintos tratamientos (día 21 a día 42, total 8 inyecciones). Las barras indican estándardesviaciones de la media. El plomo conjugada con anti-Her2 AON y Herceptin fue superior a solas Herceptin o conjugados de fármacos que contienen nanopartículas individuales. B. Efecto de los distintos tratamientos sobre la expresión de HER2, fosforilados Akt, Akt total, PARB, PARB hendidas y GAPDH se muestran por el Western Blot. Por favor, haga clic aquí para ver una versión más grande de esta figura.
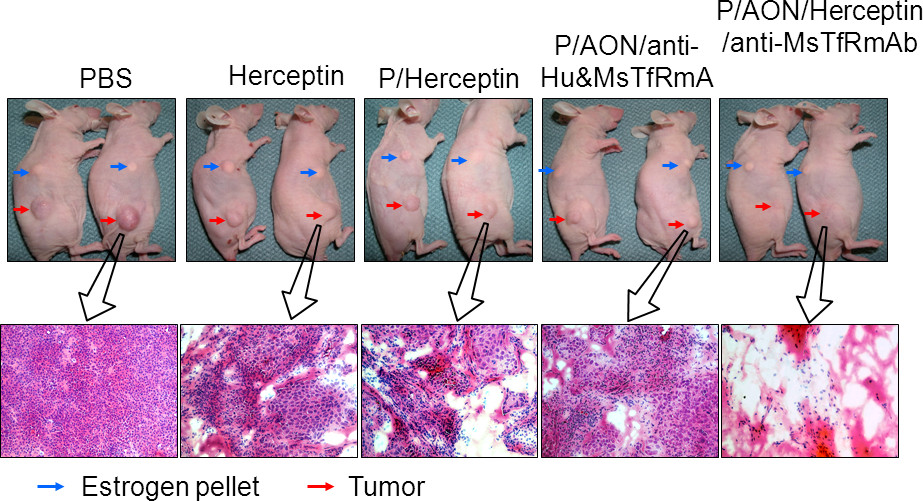
Figura 9. Tratamiento de BT-474 de cáncer de mama positivo para HER2 humano en ratones desnudos. La regresión del tumor y la necrosis / apoptosis en secciones de tejido (adaptado de Ionue et al. 12). Superior: reducción del tumor (flechas rojas). Indicación de la pastilla de estrógeno para apoyar el crecimiento del tumor (flecha azul). Lower: Hematoxilina y Eosina (H & E) tinción de secciones de tumores. La proliferación tumoral se muestra por el empaquetamiento denso de las células tumorales. El tejido necrótico es vista en que se han eliminado las células tumorales. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
La ruta experimental para la preparación de medicamentos nano de un polímero natural biodegradable se presentó que se puede utilizar en la síntesis de la medicina personalizada. La descripción comienza con la producción controlada y la purificación de ácido polimálico, que es una plataforma versátil para la síntesis de drogas nano. Utilizando técnicas reproducibles, el polímero se obtiene con alto peso molecular y en la pureza extrema adecuado para síntesis farmacéuticas. La síntesis se describe por un medicamento nano que se muestra para el tratamiento eficaz del cáncer de mama HER2-positivo. La descripción se puede traducir en la síntesis de la mayoría de otros fármacos nano para el tratamiento del cáncer. Orientación implica anticuerpos tales como Herceptin que se unen a un antígeno específico de tumor, tales como proteína HER2 o cualquier otro marcador tumoral que se internaliza de manera eficiente. El fármaco de nano ofrece una selección de oligonucleótidos antisentido y quimioterápicos que inhibe eficazmente el crecimiento del cáncer bajo Tretamiento. En el ejemplo, Herceptin vinculante para HER2 y la hibridación específica de oligonucleótidos antisentido con HER2-mRNA de codificación resultó en el bloqueo sostenido de HER2-señalización y reducción grave de cáncer de mama HER2-positivo. Basado en el principio subyacente de la focalización del tumor y la inhibición de la expresión génica mediante oligonucleótidos antisentido hemos actualizado sintetizado varias otras drogas nano y éxito inhibido glioblastoma humano preclínica y el cáncer de mama triple negativo 11,14-18.
El trabajo de síntesis comienza con la preparación de la plataforma de drogas nano altamente purificada, que es el ácido polimálico del sobrenadante del cultivo de Physarum polycephalum (una especie de la familia "moho de fango"). La preparación enfatiza altos pesos moleculares del polímero, en principio, lo que permite la unión de numerosos anticuerpos, péptidos, oligonucleótidos y otras moléculas que funcionan en la entrega de fármaco activo y la inhibición del crecimiento del tumor. Following el cultivo y la purificación controlada, calidad reproducible de polímero en rendimientos predecibles se ha producido. El polímero se almacena bajo condiciones convenientes para cualquier momento.
La síntesis de conjugados de nanopartículas PMLA que comienzan con la activación química de los carboxilatos polímero colgante se lleva a cabo en unos pocos pasos sintéticos. En entre los pasos, la síntesis se puede colocar opcionalmente en espera que permite la preparación de cantidades arbitrarias de intermedios y por lo tanto se puede utilizar en un escalado. El progreso de la síntesis se sigue por TLC y SEC-HPLC, y tanto la composición y la actividad del fármaco de nano se controla mediante ensayos específicos para el grupo químico cuantitativo, ELISA, y una variedad de mediciones físicas. Nuestra experiencia es que estas síntesis se han desarrollado sin contratiempos y de manera reproducible con excelentes rendimientos y pureza. Al optar por la especificidad de anticuerpos y oligonucleótidos antisentido cualquier variante de drogas nano se sintetiza favorablemente, según sea necesario en personalized medicamento.
Las modalidades del tratamiento exitoso del cáncer de mama HER2-positivo humano son interlocutores válidos para la preparación de modelos de cáncer de ratón, la aplicación de drogas nano, imágenes, y el análisis del crecimiento del tumor. Los resultados de las pruebas de viabilidad in vitro en son útiles en la selección de la línea celular y el fármaco que conduce a ser utilizada en el experimento con animales. En vivo de imágenes de Xenogen valida que el fármaco nano está entregado de hecho en el tumor. Resultados de Western Blot revela si el nivel de ciertas proteínas respondió de la manera prevista durante el tratamiento del cáncer. Medición del tamaño del tumor informa sobre el éxito del tratamiento, es decir, sobre la inhibición, la recesión o la regresión. El ejemplo descrito refleja nuestra experiencia con otros fármacos nano a base de ácido polimálico que indican un alto grado de previsibilidad, la reproducibilidad y la ausencia de toxicidad notables. Resultados recientes sobre la toxicidad y la eficacia de múltiples tconjugados de ácido polimálico argeted para el tratamiento triple negativo cáncer de mama se encuentran en un fuerte apoyo de esta noción 18. Una característica clave es que nuestro fármaco nano es capaz de penetrar barreras biológicas: la barrera endotelial por la extravasación en el intersticial del tumor, la membrana de las células tumorales por absorción endosoma, y la membrana del endosoma interrupción por la acción de los grupos de éster etílico de leucina o trileucina. La extravasación y la captación endosoma se llevan a cabo de forma fiable por los anticuerpos específicos vinculados a la droga nano. Anticuerpo receptor de transferrina anti-ratón de media afluencia eficiente en el tumor por transcitosis, probablemente debido a que el receptor se sobreexpresa en la mayoría de la vasculatura del tumor. Un anticuerpo diferente unido en las mismas funciones nano molécula conjugada en dirigir específicamente el fármaco nano en la célula tumoral receptor. La presencia de ambos anticuerpos, el uno para transcitosis y la otra para la absorción endosoma, es esencial para el funcionamiento óptimo. El análisis cuantitativo de mácido Alic y el anticuerpo es altamente recomendado para el control de la composición óptima del fármaco nano. Por último hay que señalar que el fármaco de nano covalente todo-en-uno administra el fármaco en forma unida químicamente en ruta a través de la vasculatura huésped en la célula tumoral receptor. La unión química hace que la mayoría de los fármacos inactivos (profármacos) hasta que se reconstituyen como medicamentos gratuitos por la escisión de la plataforma conjugado nano en el lugar de destino. Esto es importante porque la modalidad de reactivación proporciona un alto grado de seguridad durante el parto y una mínima posibilidad de evocar efectos secundarios dañinos. La versatilidad, eficacia y seguridad son atributos indispensables de una buena medicina personalizada.
Divulgaciones
Los autores Julia Y. Ljubimova, Keith L. Black, y Eggehard Holler son accionistas de Arrogene Technology Inc.
Agradecimientos
We greatly acknowledge financial support by NIH R01 CA123495, U01 CA151815, R01 CA136841, grants from the Department of Neurosurgery at Cedars-Cedars Medical Center and Arrogene Technology Inc.
Materiales
| Name | Company | Catalog Number | Comments |
| 2-Mercapto-1-ethylamine (Cysteamine; 2MEA) | Sigma-Aldrich | 30078-25G | |
| 4’,6-Diamidino-2-phenylindole (DAPI) | Vector Laboratories, Burlingame, CA | ||
| 90-Day release 17β-estradiol pellet | Innovative Research of America | ||
| Alexa Fluor 680 C2 maleimide | Invitrogen | A20344 | |
| Amberlite IR 120H | Sigma-Aldrich | 6428 | |
| Antifoam Y-30 Emulsion | Sigam-Aldrich | A5758 | |
| Anti-laminin-411 chain mAbs | Santa Cruz | SC-59980 | |
| Anti-pAkt mAb | Cell Signalling | 9271S | |
| Anti-PARB mAb | BD Biosciences | 556494 | |
| Anti-von Willebrand Factor antibody | Abcam | AB6994 | |
| Bacto Yeast Extract | Bacto, Dickinson/Sparks, MD | 212720 | |
| Beta-actin | Cell Signalling | 3700 | |
| BT-474 | ATCC | HTB-20 | |
| Calcium Carbonate | Alfa Aesar | 36337 | |
| Cell Proliferation Assay kit | Promega, Madison, WI, USA | PR-G3580 | |
| Centriplus 100 | Millipore | 4414 | |
| Dicyclohexylcarbodimide | Fluka | 36650 | |
| DMEM | Sigma-Aldrich | D5796 | |
| Eosin | Cardinal Health | S7439-4 | |
| Galardin (MMP-inhibitors) | Santa Cruz | SC-994 | |
| GAPDH | Cell Signalling | 2118 | |
| Hematoxilin | Cardinal Health | S7439-3 | |
| Hemin from porcine | Sigma-Aldrich | 51280 | |
| Herceptin | Genentech | 15534 | |
| Herceptin (Western blotting) | Cell Signalling | 2165S | |
| IgG2a-kappa murine malignoma | Sigma | M77695X5m | |
| Immun-Star AP Substrate Pack | Biorad | 170-5012 | |
| Immun-StarTM AP Substrate Pack | Biorad | 170-5012 | |
| LAL Reagent water | Lonza, MD | W50-1000 | |
| Laminin-411 mAbs | Abcam | ||
| Leucine ethyl ester (LOEt) | Sigma-Aldrich | 61850-10G-F | |
| Limulus Amebocyte Lysate (LAL) PYROGENT-5000 tests | Cambrex BioScience | N384 | |
| Lissamin-Morpholino AON | Gene Tools | Custom made | |
| L-malic acid | Sigma-Aldrich | M6413 | |
| Malate dehydrogenase | Sigma-Aldrich | M2634 | |
| Mal-PEG-Mal | Laysan | mal-PEG-mal-3400 | |
| Matrigel | BD Biosciences | 354248 | |
| Milk, nonfat powdered | Proteomics | M203-10G | |
| Morpholino oligonucleotides | GeneTools | custom made | |
| mPEG5000 | Lysan | mPEG-NH2-5000 | |
| N-hydroxysuccinimde (NHS) | ACROS Organics | 15727100 | |
| Ninhydrin | Merck | 1.06762.0100 | |
| Nitrocellulose Membrane Filter Paper Sandwich | Invitrogen | LC2001 | |
| Nitrocellulose Membrane Filter Paper Sandwich, 0.45 µm | Invitrogen | LC2001 | |
| Novex ® Tris-Glycine Transfer Buffer (25x) | Invitrogen | LC3675 | |
| Nude Mice [Tac:Cr:(MCr)-Foxnnm] | Taconic | ||
| PBS pH 7.2 10x | Gibco | 10010-49 | |
| PBS pH 7.2 1x | Gibco | 70013 | |
| PD-10 desalting columns | GE Healthcare | 17-0851 | |
| Physarum polycephalum M3CVII | ATCC | 204388 | |
| Pierce BCA protein assay | Thermo Scientific | 23225 | |
| Protease inhibitor cocktail | Roche | 1.18362E+11 | |
| Protein Detector ELISA Kit | KPL | 54-62-18 | |
| Sephadex G-25 superfine | GE Healthcare | 17-0031 | |
| Sephadex G-75 | GE Healthcare | 17-0050 | |
| Sephadex-LH20 | GE Healthcare | 17-0090 | |
| SKBR-3 | ATCC | HTB-30 | |
| SPDP | Proteochem | C1116 | |
| Streamline-DEAE | GE Healthcare | 17-0994 | |
| Styryl Red FM 1-43 | Life Technologies | T-3163 | |
| TBS 10x | Bio-Rad | 170-6435 | |
| TCEP | Sigma-Aldrich | C4706-2G | |
| TLC, silica coated aluminia sheets | Merck, Darmstadt, DE | 60F254 | |
| Trileucine (LLL) | Bachem | H-3915 | |
| Triton X-114 | Sigma-Aldrich | X114 | |
| Tween®20 | Sigma-Aldrich | P1379 | |
| Vivaspin 20 | VWR | 14005-302 | |
| DAPI | Vector Laboratories, Burlingame, CA | ||
| Dexmedetomidine | Pfizer | ||
| Atipamezole | Pfizer | ||
| Carprofen | Pfizer | ||
| Betadine | Foster and Smith, Wisconsin |
Referencias
- Koboldt, D. C., Fulton, R. S., McLellan, M. D. Comprehensive molecular portraits of human breast tumors. Cancer Genome Atlas Network. Nature. 490, 61-70 (2012).
- Kwong, L. N., Costello, J. C., et al. Oncogenic NRAS signaling differentially regulates survival and proliferation in melanoma. Nat. Med. 18, 1503-1510 (2012).
- Gerlinger, M., Rowan, A. J., Gerlinger, M., Rowan, A. J., et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N. Engl. J. Med. 366, 883-892 (2012).
- Yap, T. A., Workman, P. Exploiting the cancer genome: strategies for the discovery and clinical development of targeted molecular therapies. Annu. Rev. Pharmacol. Toxicol. 52, 549-573 (2012).
- Chatterjee, S. Cancer Biomarkers: Knowing the Present and Predicting the Future. Future Oncol. 1, 37-50 (2005).
- Suh, K. S., Sarojini, S., Youssif, M., et al. Tissue Banking, Bioinformatics, and Electronic Medical Records: The Front-End Requirements for Personalized Medicine. J. Oncology. , (2013).
- Ljubimova, J. Y., Holler, E. Biocompatible nanopolymers: the next generation of breast cancer treatment. Future Medicine, Nanomedicine. 7, 1-4 (2012).
- Lee, B. -. S., Vert, M., Holler, E., Steinbüchel, A. . Water-soluble aiphatic polyesters: poly(malic acid)s. Biopolymers 3a. , 75-103 (2002).
- Lee, B. -. S., Fujita, M., et al. Polycefin, a new prototype of multifunctional nanoconjugate based on poly(beta-L-malic acid) for drug delivery. Bioconjugate Chem. 17, 317-326 (2006).
- Nag, A., Mitra, G., et al. A colorimetric assay for estimation of polyethylene glycol and polyethylene glycolated protein using ammonium ferrothiocyanate. Analytical Biochem. 237, 224-231 (1996).
- Ding, H., Inoue, S., et al. Inhibition of brain tumor growth by intravenous poly(beta-L-malic) acid nanobioconjugate with pH-dependent drug release. Proc. Natl. Acad. Sci. USA. 107, 18143-18148 (2010).
- Inoue, S., Ding, H., et al. Nanobioconjugate inhibition of HER2/neu signaling and synthesis provides efficient mouse breast cancer treatment. Cancer Research. 71, 1454-1464 (2011).
- Maeda, H., Sawa, T., Konno, T. Mechanism of tumor-targeted delivery of macromolecular drugs, including the EPR effect in solid tumor and clinical overview of the prototype polymeric drug SMANS. J. Control. Release. 74, 47-61 (2001).
- Ljubimova, J. Y., Fujita, M., Ljubimov, Y. J., et al. Poly(malic acid) nanoconjugates containing various antibodies and oligonucleotides for multitargeting drug delivery. Nanomed. 3, 247-265 (2008).
- Inoue, S., Patil, R., Portilla-Arias, J., et al. Novel nanobioconjugate inhibiting EGFR expression in triple negative breast cancer. PLoS One. 7, 1-9 (2012).
- Patil, R., Portilla-Arias, J., Ding, H., et al. Cellular Delivery of Doxorubicin via pH-Controlled Hydrazone Linkage Using Multifunctional Nano Vehicle Based on Poly(β-L-malic Acid). Int. J. Mol. Sci. 13, 11681-11693 (2012).
- Patil, R., Portilla-Arias, J., Ding, H., et al. Temozolomide delivery to tumor cells by a multifunctional nano vehicle based on poly(β-L-malic acid). Pharm. Res. 27, 2317-2329 (2010).
- Ljubimova, J. Y., Portilla-Arias, J., Patil, R., et al. Toxicity and efficacy evaluation of multiple targeted polymalic acid conjugates for triple-negative breast cancer treatment. J. Drug Target. 21, 956-967 (2013).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados