Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Síntesis y caracterización de supramoleculares Coloides
En este artículo
Resumen
A protocol for the synthesis and characterization of colloids coated with supramolecular moieties is described. These supramolecular colloids undergo self-assembly upon the activation of the hydrogen-bonds between the surface-anchored molecules by UV-light.
Resumen
Control over colloidal assembly is of utmost importance for the development of functional colloidal materials with tailored structural and mechanical properties for applications in photonics, drug delivery and coating technology. Here we present a new family of colloidal building blocks, coined supramolecular colloids, whose self-assembly is controlled through surface-functionalization with a benzene-1,3,5-tricarboxamide (BTA) derived supramolecular moiety. Such BTAs interact via directional, strong, yet reversible hydrogen-bonds with other identical BTAs. Herein, a protocol is presented that describes how to couple these BTAs to colloids and how to quantify the number of coupling sites, which determines the multivalency of the supramolecular colloids. Light scattering measurements show that the refractive index of the colloids is almost matched with that of the solvent, which strongly reduces the van der Waals forces between the colloids. Before photo-activation, the colloids remain well dispersed, as the BTAs are equipped with a photo-labile group that blocks the formation of hydrogen-bonds. Controlled deprotection with UV-light activates the short-range hydrogen-bonds between the BTAs, which triggers the colloidal self-assembly. The evolution from the dispersed state to the clustered state is monitored by confocal microscopy. These results are further quantified by image analysis with simple routines using ImageJ and Matlab. This merger of supramolecular chemistry and colloidal science offers a direct route towards light- and thermo-responsive colloidal assembly encoded in the surface-grafted monolayer.
Introducción
Materiales coloidales mesoestructurados encuentra una amplia aplicación en la ciencia y la tecnología, como sistemas modelo para estudios fundamentales sobre los materiales atómicos y moleculares de 1,2, como materiales fotónicos 3,4, como sistemas de administración de fármacos 5,6, como revestimientos 7 y en la litografía para el patrón de superficie 8,9. Desde coloides liófobos son materiales metaestables que con el tiempo se agregan de forma irreversible debido a las interacciones de van der Waals omnipresente, su manipulación en las estructuras diana específicas es notoriamente difícil. Numerosas estrategias se han desarrollado para controlar el autoensamblaje coloidal incluyendo el uso de aditivos para sintonizar los electrostáticas 10,11 o 12,13 agotamiento de las interacciones, o desencadenantes externos tales como magnéticos o eléctricos 14 15 campos. Una estrategia alternativa sofisticada para lograr el control sobre la estructura, la dinámica y la mecánica de estos sistemas es su ingenio funcionalizaciónh moléculas que interactúan a través de fuerzas específicas y direccionales. La química supramolecular ofrece una caja de herramientas completa de pequeñas moléculas que exhiben específica del sitio, direccional y las interacciones fuertes aún reversibles, que pueden ser modulados por la fuerza en la polaridad del disolvente, la temperatura y la luz 16. Desde sus propiedades se han estudiado ampliamente a granel y en solución, estas moléculas son candidatos atractivos para estructurar materiales blandos en fases exóticas de una manera predecible. A pesar de la clara potencial de un enfoque integrado para orquestar el montaje coloidal a través de la química supramolecular, estas disciplinas rara vez han interconectado para adaptar las propiedades de los materiales coloidales mesoestructurados 17,18.
Una sólida plataforma de coloides supramoleculares debe cumplir tres requisitos principales. En primer lugar, el acoplamiento del resto supramolecular debe hacerse bajo suaves condiciones para evitar la degradación. En segundo lugar, las fuerzas de superficie en separaticomplementos más grande que el contacto directo debe estar dominado por los motivos atados, lo que significa que los coloides sin revestimiento casi exclusivamente a través de interacciones interactuar volumen excluido. Por lo tanto, las propiedades físico-químicas de los coloides deben adaptarse a suprimir otras interacciones inherentes a los sistemas coloidales, tales como van der Waals o fuerzas electrostáticas. En tercer lugar, la caracterización debe permitir una atribución inequívoca de la asamblea a la presencia de los restos supramoleculares. Para cumplir estos tres requisitos, una síntesis de dos etapas robusta de coloides supramoleculares fue desarrollado (Figura 1a). En una primera etapa, las partículas de sílice funcionalizado con NVOC hidrófobos están preparados para la dispersión en ciclohexano. El grupo NVOC puede escindirse fácilmente, produciendo partículas de amina-funcionalizado. La alta reactividad de las aminas permite post-funcionalización directa con el resto supramolecular deseado utilizando una amplia gama de condiciones de reacción suaves. Aquí, PRepare coloides supramoleculares por funcionalización de perlas de sílice con alcohol estearílico y un benceno-1,3,5-tricarboxamide (BTA) derivado 20. El alcohol estearílico desempeña varias funciones importantes: hace que el organofılica coloides e introduce repulsiones estéricas de corto alcance que ayuda a reducir la interacción específica entre coloides 21,22. las fuerzas de van der Waals se reducen aún más debido a la estrecha relación entre el índice de refracción de los coloides y el disolvente 23. De corto alcance atractivas las fuerzas de superficie de luz y termosensibles se generan mediante la incorporación de o-nitrobencilo protegida BTA 20. O nitrobencilo resto es una foto de grupo escindible que bloquea la formación de enlaces de hidrógeno entre BTA adyacentes cuando se incorporan en las amidas en las discotics (Figura 1b). Tras la fotoescisión por luz UV, la BTA en solución es capaz de reconocer e interactuar con moléculas idénticas a través de un BTA 3 veces hmatriz de bonos ydrogen, con una fuerza de unión que es fuertemente dependiente de la temperatura 17. Dado que los van der Waals son mínimos para las partículas de sílice recubiertas estearílico en ciclohexano, así como luz y la temperatura independiente, el conjunto de estímulos coloidal sensible observado debe ser mediada por la BTA.
Este video demuestra detallada cómo sintetizar y caracterizar los coloides supramoleculares y la forma de estudiar su autoensamblaje a irradiación UV por microscopía confocal. Además, un simple protocolo de análisis de imágenes para distinguir singletes coloidales de coloides agrupados y para determinar la cantidad de coloides por agrupaciones se informa. La versatilidad de la estrategia sintética permite variar fácilmente el tamaño de partícula, la cobertura de la superficie, así como el resto de unión introducido, lo que abre nuevas vías para el desarrollo de una gran familia de bloques de construcción coloidales de materiales avanzados mesoestructurados.
Protocolo
1. Síntesis de núcleo-corteza partículas de sílice
Nota: Las partículas de sílice se sintetizan de acuerdo con el siguiente procedimiento, que se basa en el método de Stöber 24,25.
- Síntesis de las semillas de sílice fluorescentes
- Disolver 105 mg (0,27 mmol) de isotiocianato de fluoresceína en 5 ml de etanol.
- Añadir 100 l de (3-aminopropil) trietoxisilano (APTES, 0,43 mmol) a la solución anterior.
- Sonicar la solución durante 5 min y se deja reaccionar durante la noche bajo una atmósfera de argón a temperatura ambiente mientras se agitaba. El complejo APTES colorante funcionalizado se usó sin purificación.
- En un 1 L de fondo redondo mezcla matraz 2,5 ml de las APTES colorante funcionalizado con 25 ml de amoniaco (25% en agua) y 250 ml de etanol.
- Añadir 10 ml de ortosilicato de tetraetilo (TEOS) bajo el menisco de la mezcla de reacción anterior con la ayuda de una pipeta de vidrio while agitaba con un agitador magnético.
- Del mismo modo, después de 5 h, añadir otro 1,75 ml de TEOS y se agita la mezcla durante la noche bajo una atmósfera de argón.
- Verter la dispersión en varias 45 ml tubos.
- Centrifugar los tubos (350 xg, 30 min), eliminar el sobrenadante y añadir 30 ml de etanol nuevo en cada tubo. Sonicar las nuevas dispersiones de 3 min, y se centrifuga de nuevo para eliminar el sobrenadante. Repita estos pasos de lavado 3 veces.
- Mantener las semillas fluorescentes en etanol en una concentración de aproximadamente 13,6 mg / ml y en la oscuridad (evitar la exposición a la luz).
- Preparar semillas no fluorescentes siguiendo el mismo procedimiento omitiendo la adición del colorante fluorescente.
Nota: Siguiendo este procedimiento, se obtienen semillas de alrededor de 100 nm de radio.
- Síntesis de partículas de sílice core-shell
- Llenar un 1 L matraz de fondo redondo con 51 ml de etanol, 17 ml de agua desionizada, 3,4 ml de amoníaco (25% en agua) y 4ml de la dispersión de semillas (54,4 mg de semillas fluorescentes aproximadamente).
- Llene una jeringa de plástico con 5 ml de TEOS y 10 ml de etanol.
- Llene una segunda jeringa de plástico con 1,34 ml de amoniaco (25% en agua), 3,4 ml de agua desionizada y 10,25 ml de etanol.
- Una los dos jeringas en el matraz de fondo redondo con un tubo de plástico.
- Equipar el matraz con un flujo de argón y un agitador magnético. La entrada de argón tiene que estar al lado de la salida de la segunda jeringa para evitar el contacto entre los gases de amoníaco a partir de las gotitas de TEOS para evitar la nucleación secundaria.
- Añadir el contenido de ambas jeringas al mismo tiempo a 1.7 ml / hr utilizando bombas peristálticas mientras se agitaba la mezcla. Asegúrese de obtener las gotitas que caen libres para evitar que se desliza en las paredes y, por tanto, la nucleación secundaria.
- Detener la adición después de 7 h para obtener partículas de núcleo-envuelta de aproximadamente 300 nm de radio.
- Verter el contenido del matraz en varias 45 ml tubos.
- Centrifugar los tubos (350 xg, 30 min), eliminar el sobrenadante y añadir 30 ml de etanol nuevo en cada tubo. Sonicar la nueva dispersión de 3 min, y se centrifuga de nuevo para eliminar el sobrenadante. Repita estos pasos de lavado 3 veces.
- Mantener las partículas de núcleo-envuelta en etanol y en la oscuridad (evitar la exposición a la luz).
- Preparar partículas de sílice no fluorescentes siguiendo el mismo procedimiento pero utilizando las semillas no fluorescentes.
2. La funcionalización de sílice Coloides
- Síntesis de coloides NVOC funcionalizado
- Dispersar 10 mg de partículas de sílice de núcleo-corteza en 1 ml de etanol junto con 12 mg (0,03 mmol) de la molécula de NVOC-C11-OH y 31 mg (0,11 mmol) de alcohol estearílico en un matraz de 50 ml de fondo redondo (resultante en un OH NVOC-C11-relación de 20/80 / alcohol estearílico molar).
- Sonicar la mezcla durante 10 minutos para asegurar que todas las moléculas se disuelven y las partículas están bien dispeRSED.
- Añadir a la mezcla de una barra de agitador magnético y se evapora el etanol con un flujo constante de argón a temperatura ambiente. Antes de continuar, asegúrese de que no hay etanol izquierda, si no que podría reaccionar con los grupos silanol de las partículas. Para comprobar si el etanol se evapora por completo prestar atención a la temperatura del fondo del matraz. Si se siente frío, el etanol no está todavía completamente evaporó.
- Calentar el matraz hasta 180 ° C durante 6 horas con agitación continua y bajo un flujo constante de argón 22.
- Deje que el matraz se enfríe a temperatura ambiente.
- Añadir 3 ml de CHCl 3 en el matraz y sonicar durante 5 min (o hasta que todo el contenido de sólidos se ha disuelto o dispersado).
- Se centrifuga la dispersión (2.600 xg, 4 min), eliminar el sobrenadante y añadir CHCl 3 fresco. Sonicar la nueva dispersión de 3 min, y se centrifuga de nuevo para eliminar el sobrenadante. Repita estos pasos de lavado 6 veces.
- Se secan las partículas a 70 ° C en vacío durante la noche y almacenarlos en un desecador.
- Síntesis de BTA-coloides
- Dispersar 10 mg de partículas funcionalizadas con una relación de 20/80 en moles de alcohol NVOC-C11-OH / estearílico en 3 ml de CHCl 3.
- Irradiar la dispersión en un UV-horno (λ max = 354 nm) durante 1 hora para escindir el grupo NVOC. Asegúrese de que la desprotección es homogénea en la superficie de las partículas por agitación de la dispersión suavemente con un agitador magnético, mientras que la desprotección. Esto produce las partículas de amina funcionalizada (Figura 1A).
- Disolver 9 mg del derivado de benceno-1,3,5-tricarboxamide (BTA, 0,01 mmol), 8,7 l de N, N-diisopropiletilamina (DIPEA, 0,05 mmol) y 5,2 mg de (benzotriazol-1-iloxi) tripirrolidinofosfonio hexafluorofosfato ( PyBOP, 0,01 mmol) en 1 ml de CHCl3.
- Añadir la solución de la amina p funcionalizadoartículo dispersión y se agita durante la noche a temperatura ambiente y bajo una atmósfera de argón.
- Se centrifuga la dispersión (2.600 xg, 4 min), eliminar el sobrenadante y añadir 3 ml de CHCl 3 fresco. Sonicar la nueva dispersión de 3 min, y se centrifuga de nuevo para eliminar el sobrenadante. Repita estos pasos de lavado 6 veces.
- Se secan las partículas a 70 ° C en vacío durante 48 horas y almacenarlos en un desecador.
3. Las mediciones de dispersión de luz estática (SLS)
Nota: Use partículas no fluorescentes, ya que el núcleo fluorescente absorbe la luz de la misma onda que la luz láser incidente de equipos de dispersión de luz convencional.
- Funcionalizar 10 mg de partículas de sílice no fluorescentes con el alcohol estearílico solamente (sin NVOC-C11-OH) siguiendo el procedimiento descrito en la sección 2.1.
- Preparar 500 l de una dispersión de 0,033 mg / ml de partículas no funcionalizado en agua y unaotra de 2 mg / ml de las partículas con el alcohol estearílico recubierto en ciclohexano.
- Sonicar dos dispersiones durante por lo menos 20 minutos para asegurar que las partículas se dispersan bien.
- Medir la intensidad dispersada de ambas dispersiones, los disolventes y el disolvente de referencia de 30 ° a 120 ° en pasos de 5 °.
- Trazar la intensidad de la muestra (muestra I) como una función de q
(Ecuación 1) q = 4π n sin disolvente (θ / 2) / λ o
con el θ ángulo de dispersión, el índice de refracción del disolvente n disolvente y la longitud de onda λ de la láser o. - Ajustar los datos a la siguiente ecuación usando software (por ejemplo, Origen)
(Ecuación 2) Muestreo la CP = (QR)
donde C es una constante y el factor de forma P (qR) está dada por
(Ecuación 3)
en el que el radio medio de los coloides esféricas es R. - Extracto de R a partir de los ajustes para cada dispersión.
- Calcular la proporción Rayleigh (R θ), que es una medida absoluta de la intensidad de la luz dispersada, de acuerdo con la siguiente ecuación, para cada θ.
(Ecuación 4)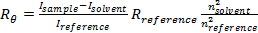
con la intensidad de la muestra, el disolvente y la referencia, que muestra, disolvente I y de referencia, respectivamente, el índice de refracción del disolvente y el disolvente de referencia n y n de referencia, de forma correspondiente, y la relación de Rayleigh de la referencia R de referencia. Aquí usar tolueno como referencia, De modo que n = agua 1.332, n = 1.497 tolueno, ciclohexano n = 1.426; R tolueno = 2.74x10 -3 m-1 26. - Calcular el índice de refracción promedio de los coloides (coloides n) de θ R y la ecuación 5.
(Ecuación 5)
con el número de partículas por volumen de N, el volumen de una partícula v partícula dada por v de partículas = 4/3 πR 3, y suponiendo que el factor de estructura S (q) ~ 1, que es el límite de las partículas que no interactúan.
4. Cuantificación del número de sitios activos por partícula
Nota: Use pequeñas partículas de 13 nm de radio (con una mayor superficie a-relación de volumen).
- Funcionalizar pequeñas partículas comercialmente disponibles con una relación de 20/80 en moles de NVOC-C11-OH / estearil alcohol siguiendo el procedimiento descrito en la Sección 2.1.
- Dispersar 20 mg de las partículas pequeñas, funcionalizados en 1 ml CHCl 3 y irradiar la dispersión en un UV-horno (λ max = 354 nm) durante 1 hora para escindir el grupo NVOC. Se agita la dispersión suavemente con una barra agitadora magnética, mientras que la desprotección. De esta manera, los coloides no se sedimentan y su superficie queda expuesta a la luz UV, garantizando así la desprotección homogénea.
- Centrifugar las partículas resultantes de amina funcionalizado (3.400 xg, 10 min) y eliminar el sobrenadante.
- Se secan las partículas a 70 ° C durante 2 hr.
- Disolver 0,50 mg de succinimidil 3- (2-piridilditio) propionato (SPDP, 0,0016 mmol) en 200 l de dimetilformamida (DMF).
- Añadir la solución de SPDP a la 20 mg de las partículas de amina funcionalizado secos y la vórticesistema de 30 min. Dentro de este tiempo, todas las aminas primarias disponibles en los coloides han reaccionado con el SPDP.
- Se lavan las partículas con 1 ml de DMF para 6 veces (o hasta que no SPDP libre se detecta en el sobrenadante mediante espectroscopía UV-Vis a λ = 375 nm). En la última etapa de lavado tratar de eliminar la mayor cantidad posible sobrenadante.
- Disolver 0,53 mg de ditiotreitol (DTT, 0,0034 mmol) en 50 l de DMF. Añadir la solución de DTT a las partículas y agitar la dispersión durante 30 minutos. Dentro de este tiempo se escinde el grupo piridina-2-tiona.
- Determinar la absorbencia de la libre piridina-2-tiona liberada en el sobrenadante a λ = 293 nm con un microvolumen UV-Vis espectrofotómetro.
- Construir una curva de calibración para determinar el coeficiente de extinción ɛ (~ 12.1x10 3 M -1 cm -1) de la piridina-2-tiona en DMF mediante la medición de la absorbancia de una serie de diluciones de diferentes cantidades conocidas de SPDP con un exceso de la TDT .
- Calcular la concentración de piridina-2-tiona, C P2T, que se escinde de las partículas utilizando la ley de Lambert-Beer:
(Ecuación 6) Abs = C p2t ε l
con la concentración molar de piridina-2-tiona C P2T, el coeficiente de extinción ɛ y la longitud de la trayectoria l. - Calcular el número de sitios activos (aminas) por partícula con la siguiente ecuación
(Ecuación 7)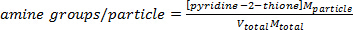
con la masa de una partícula de partículas M es decir partículas M = 4/3 3πR ρ, con ρ = 1,295 g / cm3, la masa total ponderada de partículas total M (20 mg) y el total del volumen total V (50 l). Esta ecuación supone que todos disponiblesaminas reaccionan con el SPDP y el TDT reduce todas las moléculas de SPDP unidos a las partículas.
5. Montaje del monitor coloidal por microscopía confocal
Nota: partículas de sílice Uso core-shell (con un núcleo fluorescente y una cáscara no fluorescente).
- Preparar 400 l de una dispersión de 0,1% en peso de partículas funcionalizadas-BTA en ciclohexano y sonicar la muestra durante 20 min.
- Irradiar el frasco de la muestra en el horno UV (λ max = 354 nm) para escindir el grupo nitrobencilo o de la BTA. Tomar 25 ml de alícuotas a diferentes tiempos de irradiación, por ejemplo de 0 hasta 30 min, para supervisar el proceso de agrupamiento.
- Colocar las diferentes alícuotas en diferentes láminas de vidrio con la ayuda de un espaciador y cerrar las cámaras con una hoja de cubierta (tamaño de la cámara es de 13 mm de diámetro x 0,12 mm de altura). Después de cerrar la cámara, gire la hoja de la cubierta al revés para que las partículas de sedimento y adsorb sobre el vidrio, lo que facilita la formación de imágenes.
- Tome varias imágenes de cada muestra con el microscopio confocal tan pronto como sea posible después de la preparación de la muestra para cada tiempo de irradiación.
Análisis 6. Imagen
- La cuantificación del número de singletes con ImageJ
Nota: Todos los comandos que se utilizan para escribir el guión, se describen en el manual de ImageJ:
http://imagej.nih.gov/ij/docs/guide/user-guide.pdf- Suavizar las imágenes confocal para eliminar píxeles aislados a partir de los bordes y rellenar pequeños orificios que ejecutan la función "Smooth".
- Dado que sólo los núcleos son fluorescentes, dilatar las áreas brillantes hasta que el borde de las partículas que pertenecen al mismo grupo de contacto y las partículas se funden. Para ello, utilice el filtro "Dilatar". Con partículas con grosor de la cáscara de aproximadamente 180 nm, y las imágenes con una resolución de 0,02 m / píxel, a dos pasos de dilatación son suficientes.
- Convertir las imágenesen una imagen binaria se ejecuta la función "Hacer binario".
- Establecer la escala mediante la ejecución de la función "" para fijar la escala ... ", distancia = 1 = 0,02 conocido píxel = 1 unidad = um" "para las fotografías tomadas con una resolución de 0,02 m / píxel por ejemplo.
- Aplicar un tamaño umbral para discriminar el ruido y las partículas fuera de foco a partir de partículas en desenfocadas. Por ejemplo, con imágenes tomadas con una resolución de 0,02 m / píxel, todas las áreas más pequeñas de 0,2 píxeles se descartan. Para ello, utilice el comando "Analizar partículas ...", "size = 0,2-Infinito".
- Crear una imagen y un archivo all.jpg all.txt con el tamaño de todas las áreas brillantes de la imagen (clusters y singletes) mediante el uso de los comandos "de" Resultados ", _all.txt" "y" "JPEG", "todos" ".
- Supongamos áreas que todos brillantes entre 0,2 y 0,7 píxeles de tamaño y con una circularidad (circularidad = 4 π área / perímetro 2) entre 0,7 y 1,0 sonsingletes que ejecutan el comando "Analizar partículas ...", "circularidad = 0,7-1,0".
- Crear una imagen y un archivo singlets.jpg singlets.txt con la información de todas las áreas brillantes que son singletes mediante el uso de los comandos "" Resultados ", _singlets.txt" "y" "", "interiores" JPEG ".
- Procesar la información con Matlab
- Lea el archivo .txt singlete y calcular el tamaño medio de un singlete por imagen (A singlete).
- Utilice el tamaño medio de un singlete para calcular el número de partículas por grupo (A = singlete doblete 2A, 3A Un triplete = singlete ...) y el número total de partículas en la imagen del otro archivo all.txt.
- Calcular la fracción de partículas en interiores para cada tiempo de exposición: singletes f = singletes número / partículas totales
- Calcular la fracción de dobletes, tripletes, etc.: F dobletes = 2 * Número de dobletes / partículas totales, etc.
Resultados
Dado que el procedimiento de dos etapas usado para sintetizar los coloides supramoleculares (figura 1A), acopla el BTA- derivados (Figura 1B) en una segunda etapa a temperatura ambiente y en condiciones de reacción suaves, se asegura su estabilidad.
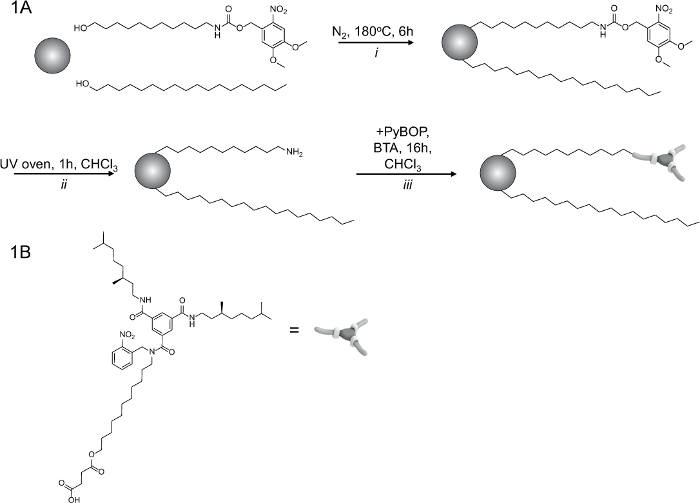
Figura 1. Esquema de la síntesis de coloides supramoleculares. A...
Discusión
Cuando ciclohexano, con un índice de refracción de 1,426, se usa como un disolvente para dispersar los BTA-coloides, interacciones de van der Waals son muy débiles, ya que los índices de refracción de los coloides y disolvente son casi los mismos. Tenga en cuenta que la concentración de coloides funcionalizados utilizados para los experimentos de SLS en ciclohexano es mucho más alta en comparación con los coloides de sílice desnudos en agua. Esto es necesario para obtener una dispersión suficientemente fuerte ...
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Los autores reconocen la Organización Holandesa para la Investigación Científica (NWO ECHO-CTPI subvención 717.013.005, NWO VIDI subvención 723.014.006) por el apoyo financiero.
Materiales
| Name | Company | Catalog Number | Comments |
| APTES | Sigma-Aldrich | ||
| FTIC | Sigma-Aldrich | ||
| TEOS | Sigma-Aldrich | ||
| LUDOX AS-40 | Sigma-Aldrich | Silica particles of 13 nm in radius | |
| MilliQ | --- | --- | 18.2 MΩ·cm at 25 °C |
| Ethanol | SolvaChrom | --- | |
| Ammonia (25% in water) | Sigma-Aldrich | --- | |
| Chloroform | SolvaChrom | --- | |
| Cyclohexane | Sigma-Aldrich | --- | |
| Dimethylformamide (DMF) | Sigma-Aldrich | --- | |
| Stearyl alcohol | Sigma-Aldrich | --- | |
| N,N-Diisopropylethylamine (DIPEA) | Sigma-Aldrich | --- | |
| Benzotriazol-1-yl-oxytripyrrolidinophosphonium hexafluorophosphate (PyBOP) | Sigma-Aldrich | --- | |
| Succinimidyl 3-(2-pyridyldithio)propionate (SPDP) | Sigma-Aldrich | --- | |
| Dithiothreitol (DTT) | Sigma-Aldrich | --- | |
| NVOC-C11-OH | Synthesized | --- | I. de Feijter, 2014 Responsive materials from adaptive supramolecular constructs, Doctoral thesis, Technical University of Eindhoven, The Netherlands |
| BTA | Synthesized | --- | I. de Feijter, 2014 Responsive materials from adaptive supramolecular constructs, Doctoral thesis, Technical University of Eindhoven, The Netherlands |
| Centrifuge | Thermo Scientific | Heraeus Megafuge 1.0 | |
| Ultrasound bath | VWR | Ultrasonic cleaner | |
| Peristaltic pumps | Harvard Apparatus | PHD Ultra Syringe Pump | |
| UV-oven | Luzchem | LZC-a V UV reactor equipped with 8x8 UVA light bulbs (λmax=354 nm) | |
| Stirrer-heating plate | Heidolph | MR-Hei Standard | |
| [header] | |||
| Light Scattering | ALV | CGS-3 MD-4 compact goniometer system, equipped with a Multiple Tau digital real time correlator (ALV-7004) and a solid-state laser (λ=532 nm, 40 mW) | |
| UV-Vis spectrophotometer | Thermo Scientific | NanoDrop 1000 Spectrophotometer | |
| Confocal microscope | Nikon | Ti Eclipse with an argon laser with λexcitation=488 nm | |
| Slide spacers | Sigma-Aldrich | Grace BioLabs Secure seal imaging spacer (1 well, diam. × thickness 13 mm × 0.12 mm) | |
| Syringes | BD Plastipak | 20 ml syringe | |
| Plastic tubing | SCI | BB31695-PE/5 | Ethylene oxide gas sterilizable micro medical tubing |
| Pulsating vortex mixer | VWR | Electrical: 120 V, 50/60 Hz, 150 W Speed Range: 500–3,000 rpm | |
Referencias
- Wang, Y., et al. Colloids with valence and specific directional bonding. Nature. 491 (7422), 51-55 (2012).
- Klinkova, A., Therien-Aubin, H., Choueiri, R. M., Rubinstein, M., Kumacheva, E. Colloidal analogs of molecular chain stoppers. PNAS. 110 (47), 18775-18779 (2013).
- Galisteo-Lõpez, J. F., et al. Self-assembled photonic structures. Adv. Mater. 23 (1), 30-69 (2011).
- Kim, H., et al. Structural colour printing using a magnetically tunable and lithographically fixable photonic crystal. Nat. Photonics. 3 (9), 534-540 (2009).
- Dinsmore, A. D., et al. Colloidosomes: Selectively permeable capsules composed of colloidal particles. Science. 298 (5595), 1006-1009 (2002).
- Destribats, M., Rouvet, M., Gehin-Delval, C., Schmitt, C., Binks, B. P. Emulsions stabilised by whey protein microgel particles: Towards food-grade Pickering emulsions. Soft Matter. 10 (36), 6941-6954 (2014).
- Prevo, B. G., Hon, E. W., Velev, O. D. Assembly and characterization of colloid-based antireflective coatings on multicrystalline silicon solar cells. J. Mater. Chem. 17 (8), 791-799 (2007).
- Kitaev, V., Ozin, G. A. Self-assembled surface patterns of binary colloidal crystals. Adv. Mater. 15 (1), 75-78 (2003).
- Plettl, A., et al. Non-Close-Packed crystals from self-assembled polystyrene spheres by isotropic plasma etching: adding flexibility to colloid lithography. Adv. Funct. Mater. 19 (20), 3279-3284 (2009).
- Yethiraj, A., Van Blaaderen, A. A colloidal model system with an interaction tunable from hard sphere to soft and dipolar. Nature. 421 (6922), 513-517 (2003).
- Spruijt, E., et al. Reversible assembly of oppositely charged hairy colloids in water. Soft Matter. 7 (18), 8281-8290 (2011).
- Kraft, D. J., et al. Surface roughness directed self-assembly of patchy particles into colloidal micelles. PNAS. 109 (27), 10787-10792 (2012).
- Rossi, L., et al. Cubic crystals from cubic colloids. Soft Matter. 7 (9), 4139-4142 (2011).
- Erb, R. M., Son, H. S., Samanta, B., Rotello, V. M., Yellen, B. B. Magnetic assembly of colloidal superstructures with multipole symmetry. Nature. 457 (7232), 999-1002 (2009).
- Vutukuri, H. R., et al. Colloidal analogues of charged and uncharged polymer chains with tunable stiffness. Angew. Chem. Int. Edit. 51 (45), 11249-11253 (2012).
- De Greef, T. F. A., Meijer, E. W. Materials science: Supramolecular polymers. Nature. 453 (7192), 171-173 (2008).
- De Feijter, I., Albertazzi, L., Palmans, A. R. A., Voets, I. K. Stimuli-responsive colloidal assembly driven by surface-grafted supramolecular moieties. Langmuir. 31 (1), 57-64 (2015).
- Celiz, A. D., Lee, T. C., Scherman, O. A. Polymer-mediated dispersion of cold nanoparticles: using supramolecular moieties on the periphery. Adv. Mater. 21 (38-39), 3937-3940 (2009).
- Cantekin, S., De Greef, T. F. A., Palmans, A. R. A. Benzene-1,3,5-tricarboxamide: A versatile ordering moiety for supramolecular chemistry. Chem. Soc. Rev. 41 (18), 6125-6137 (2012).
- Mes, T., Van Der Weegen, R., Palmans, A. R. A., Meijer, E. W. Single-chain polymeric nanoparticles by stepwise folding. Angew. Chem. Int. Edit. 50 (22), 5085-5089 (2011).
- van Blaaderen, A., Vrij, A. Synthesis and characterization of monodisperse colloidal organo-silica spheres. J. Colloid Interf. Sci. 156 (1), 1-18 (1993).
- Van Helden, A. K., Jansen, J. W., Vrij, A. Preparation and characterization of spherical monodisperse silica dispersions in nonaqueous solvents. J. Colloid Interf. Sci. 81 (2), 354-368 (1981).
- Israelachvili, J. Intermolecular and Surface Forces. Van der Waals forces between particles and surfaces. , 253-289 (2011).
- van Blaaderen, A., Vrij, A. Synthesis and characterization of colloidal dispersions of fluorescent, monodisperse silica spheres. Langmuir. 8 (12), 2921-2931 (1992).
- Giesche, H. Synthesis of monodispersed silica powders II. Controlled growth reaction and continuous production process. J. Eur. Ceram. Soc. 14 (3), 205-214 (1994).
- Wu, H. Correlations between the Rayleigh ratio and the wavelength for toluene and benzene. Chem. Phys. 367 (1), 44-47 (2010).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados