Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Observación y análisis de parpadear dispersión Raman de superficie mejorada
En este artículo
Resumen
Este protocolo describe el análisis de parpadear Raman de superficie mejorada dispersión debido a la caminata al azar de una sola molécula sobre una superficie de plata usando leyes de la energía.
Resumen
De una sola molécula en una ensambladura de plata nanoaggregate, parpadear superficie-realzada Raman (SERS) de dispersión se observa. Aquí, se presenta un protocolo de cómo preparar el SERS-activo nanoaggregate de plata, grabar un vídeo de ciertos puntos parpadeantes en la imagen microscópica y analizar las estadísticas intermitentes. En este análisis, una ley de potencia reproduce las distribuciones de probabilidad para eventos brillantes en relación a su duración. Las distribuciones de probabilidad para los eventos oscuros están equipadas por una ley de potencia con una función exponencial. Los parámetros de la ley de energía representan el comportamiento molecular en Estados luminosos y oscuros. Se pueden estimar el modelo de paseo aleatorio y la velocidad de la molécula a través de toda la superficie de plata. Es difícil estimar aun cuando estén usando promedios, las funciones de autocorrelación y proyección de imagen de súper-resolución SERS. En el futuro, análisis de ley de energía se deben combinar con la proyección de imagen espectral, porque los orígenes de parpadear no se puede confirmar por este método de análisis solo.
Introducción
Superficie-realzada Raman (SERS) de dispersión es altamente sensible Espectroscopía Raman de superficie de un metal noble. Puesto que el espectro de Raman provee información detallada sobre la estructura molecular basado en las posiciones de pico agudo, a través de los modos vibracionales de grupos funcionales en las moléculas, se puede investigar la información de una sola molécula sobre una superficie de metal usando SERS1,2,3. De un nanoaggregate de plata con un adsorbato en el nivel de una sola molécula, una señal intermitente se observa1,2,3,4,5,6, 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16y el espectro oscila1,2,3,4,5,6,7,8, 9,10,11,12,13,14. Intermitente puede ser inducida por una sola molécula que se mueve al azar dentro y fuera de un campo electromagnético mejorado de (EM) en un cruce de nanoaggregate de plata de nanómetro de tamaño. Por lo tanto, parpadeando se consideran pruebas simples para la detección de una sola molécula, en comparación con una técnica usando una distribución de Poisson de intensidades SERS y un bi-analito2,3,17. Sin embargo, los mecanismos detallados del espectro intermitente y fluctuante, que puede depender fuertemente de comportamiento molecular en la superficie del Ag, son todavía controvertidos.
En estudios previos, parpadeando SERS ha sido analizado utilizando la función de autocorrelación, que puede calcular el coeficiente de difusión y concentración de moléculas en movimiento dentro y fuera de un mejorado EM campo12,13,14 . Por otra parte, una puntuación de desviación estándar normalizada, que representa la inestabilidad de la intensidad total, se ha derivado por el perfil de tiempo de la señal15. Sin embargo, estos enfoques analíticos pueden basarse en el comportamiento de algunas moléculas. En cambio, en una imagen de súper-resolución de parpadear SERS, comportamiento de una sola molécula en un campo mayor de la EM puede ser identificados16. Sin embargo, estas técnicas pueden obtener estos parámetros solamente en un campo EM mejorado. El comportamiento aleatorio de una sola molécula en un amplio rango (por ejemplo, en parpadear SERS) puede ser representado como una ley de potencia en lugar de un promedio de4,5,6,7,8 ,9,10,11, similar a la intermitente de la fluorescencia de un semiconductor único quantum dot (QD)18,19. Mediante el uso de una energía ley análisis4,5,6,7,8,9,10,11, el comportamiento molecular puede estimarse en el brillante estado (en el campo EM mayor) y estado oscuro10; es decir, se puede estimar el comportamiento de la molécula sobre toda la superficie de plata.
Para esta técnica, plata coloidales nanoaggregates son usadas4,5,6,7,8,9,10,11. Estos nanoaggregates muestran varias bandas de resonancia (LSPR) plasmones localizados que afectan fuertemente mejoradas electromagnéticas cuando son excitados en ciertas longitudes de onda. Así, inmediatamente se puede obtener plata SERS-activo existen nanopartículas en suspensión coloidal y algunos datos. En el caso de nanoestructuras simple, que tienen acuerdos, formas y tamaños específicos, la dependencia LSPR de SERS parpadear puede ocultar otras dependencias7; es decir, si se utiliza la nanoestructura a LSPR buena o mala, los parámetros será constante, y por lo tanto, se ocultarán las otras dependencias. Análisis de ley de energía se ha utilizado para descubrir varias dependencias de lo SERS intermitente de plata coloidal nanoaggregates4,5,6,7,8, 9 , 10 , 11.
Access restricted. Please log in or start a trial to view this content.
Protocolo
1. preparación de la muestra
-
Preparación de nanopartículas coloidales de plata 20
- Para fabricar plata coloidales nanopartículas, disolver 0,030 g de nitrato de plata y 0,030 g de citrato trisódico dihidrato en 150 mL de agua en un matraz de fondo redondo de 200 mL.
- Combinar el matraz con un condensador de reflujo (Dimroth).
- Agitar la solución en el matraz con una barra magnética de agitador y agitar. Luego, calentar la solución de agitación en el matraz en baño de aceite a 150 ° C durante 60 min.
Nota: La solución convertirá luego lechoso, amarillo gris. - Enfríe la suspensión a temperatura ambiente y mantener la suspensión en el frasco cubierto con papel de aluminio en el refrigerador.
Nota: El protocolo puede ser una pausa en este punto. Uso de las nanopartículas coloidales, después de guardar en el refrigerador, dentro de un mes.
-
Preparación de muestra para varios colores parpadeando emisión 11
- Listo el portaobjetos de un microscopio, una placa de cristal con jabón de lavado a mano y enjuagar con agua.
- Añadir 0.1% soluciones acuosas del poly-L-lisina a la placa de cristal y retirar la solución con un soplador.
- Añadir la suspensión coloidal de plata a la placa de cristal y quitar la suspensión con un soplador.
- Incluya una zona de gota en el plato de cristal con un lápiz líquido bloqueador.
- Colocar agua destilada en el plato de cristal y cubrir con otra placa de vidrio para crear una diapositiva del microscopio y evitar que el agua se evapora.
-
Preparación de muestra para SERS intermitente color monótono 7 , 8 , 9 , 10
- Listo el portaobjetos de un microscopio, una placa de cristal con jabón de lavado a mano y enjuagar con agua.
- La plata coloidal suspensión la mezcla con el tinte thiacyanine o thiacarbocyanine (μm 25 ó 4, respectivamente) y una solución acuosa de NaCl (10 mM) en una proporción de volumen de 2:1:1.
- La suspensión de la muestra sobre la placa de vidrio de la gota y quitar la suspensión con un soplador.
- Incluya una zona de gota en el plato de cristal con un lápiz líquido bloqueador.
- La gota de una solución acuosa de NaCl (1 M) en la placa de vidrio para inmovilizar las nanopartículas de plata y cubrir con otra placa de vidrio para crear una placa portaobjetos de microscopio e impedir la evaporación de la solución.
2. observación de centelleo nanopartículas de plata
-
Iluminación de la muestra
- Coloque la placa de cristal de la muestra preparada con protocolo 1.2 o 1.3 en el escenario de un microscopio invertido.
- Iluminan la placa de vidrio la muestra utilizando luz blanca a través de un condensador de campo oscuro y un enfoque en varios puntos de color (azul, verdes, amarillos y rojos) en la placa de vidrio utilizando una lente de objetivo (60 X).
- Iluminan la placa de cristal de la muestra utilizando un haz atenuado, entregado en un ángulo de 30° con respecto a la superficie de la muestra, de un láser de onda continua (cw) bombeados de estado sólido (DPSS) de diodo a través de un filtro de interferencia.
- Para utilizar iluminación láser para observar la plata nanoaggregates como manchas de color monótonos en un mismo color, mueva el área de iluminación láser hacia el centro de la vista y centrarse en los puntos de la placa de vidrio mediante el ajuste de la etapa en la dirección z.
-
Observación de centelleo
- Inserte un filtro de paso de largo después de la lente del objetivo y se ilumina la placa de cristal de la muestra con un rayo de cw-láser DPSS entregado en un ángulo de 30° con respecto a la superficie de la muestra a través de un filtro de interferencia.
- Encontrar el parpadeo puntos como se muestra en la figura 1 (véase también Figura S1 en el material suplementario) moviendo el escenario en las direcciones x y y.
- Grabar el video de los puntos parpadeantes con el microscopio invertido, acoplado a una cámara de refrigerado digital dispositivo de carga acoplada (CCD), que tiene una resolución de tiempo de 120 61 ms, durante 20 minutos.
3. Análisis de parpadear SERS
-
Derivación de Perfil de tiempo de vídeo
- En el software que controla la cámara, abra el archivo de vídeo.
- Para seleccionar los puntos parpadeantes y zona oscura, arrastre las áreas que cubren por separado las regiones con y sin manchas en la imagen de vídeo.
- Para obtener perfiles de tiempo de intensidad de señal del intermitentes manchas y áreas oscuras en el video, seleccione Análisis Temporal en el análisisy haga clic en el cálculo en la ventana de Análisis Temporal .
- Guardar los datos como un archivo de texto.
-
Análisis del perfil de tiempo
- Acoplar una línea de base del perfil tiempo restando el perfil de tiempo de la zona oscura o ajuste con una función polinómica, como se muestra en la figuras 2A y 2B.
- Evaluar una intensidad promedio de la línea de base que consiste en aproximadamente 2.000 puntos, basey una desviación estándar de las intensidades de línea de base, σ, como se muestra en las figuras 2 y 2D.
- Distinguir eventos brillantes oscuros eventos con intensidades mayores a un umbral de base + 3σ y registrar la duración de cada evento. En la figura 3, por ejemplo, grabar el evento de 0 a 3.5476 s como el evento oscuro (con una duración de t = 3.5476 s) y grabar el evento de 3.5476 a 4.0981 s como el evento brillante (con una duración de t = 0.5505 s). Repita el procedimiento como se muestra en la tabla 1.
- Contar el número de acontecimientos brillantes y oscuras para cada duración, expresada en la primera y segunda línea del cuadro 2.
- Suma el número de eventos para cada duración, excepto para eventos de menos duración t. Como expresa en la segunda y tercera línea del cuadro 2, por ejemplo, suma el número de eventos para cada duración (excepto para los eventos de t = 0.0612 s) 41 + 18 + 9 +...; el resultado es igual a la sumatoria de t = 0.1223 s, es decir, 103.
- Divida las sumatorias por cada duración y normalizarlos. Tal como se expresa en la tabla 2, por ejemplo, dividir la suma de duración t = 0.0612 s por la s de duración 0.0612. El resultado es 3,351.5791. Luego, divida el resultado por el total de los resultados en la cuarta línea en la tabla 2. La distribución de probabilidad se deriva para ser 0.64494.
- Parcela las distribuciones de probabilidad para los eventos brillantes Pen(t) contra su duración t en un gráfico de logaritmo logaritmo y ajuste Log10Pa(t) por registro10 (
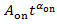 ) para deducir la ley exponente αen para un específico parpadeo punto. Si Pa(t) está ubicado por
) para deducir la ley exponente αen para un específico parpadeo punto. Si Pa(t) está ubicado por 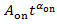 , la línea integral se desvía de las parcelas en pequeños valores de Pen(t), como se muestra por la línea punteada en la figura 4A.
, la línea integral se desvía de las parcelas en pequeños valores de Pen(t), como se muestra por la línea punteada en la figura 4A. - Parcela las distribuciones de probabilidad para eventos oscuro Poff(t) contra su duración t en un gráfico de logaritmo logaritmo y ajuste Log10Pde(t) por (10) registro
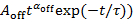 deducir la energía ley α exponenteoff y el truncamiento tiempo τ de la intermitencia del mismo punto. Si Poff(t) está equipado por
deducir la energía ley α exponenteoff y el truncamiento tiempo τ de la intermitencia del mismo punto. Si Poff(t) está equipado por 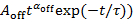 , la curva cabida se desvía de las parcelas en pequeños valores de Pde(t).
, la curva cabida se desvía de las parcelas en pequeños valores de Pde(t). - Repita 3.2.1 a 3.2.8 para los otros puntos parpadeantes en el video.
Access restricted. Please log in or start a trial to view this content.
Resultados
De la plata nanoaggregates con poli-l-lisina preparado por protocolo 1.2, se observan manchas multicoloras parpadeantes de SERS y superficie-realzada de la fluorescencia, tal como se muestra en la figura 111. En cambio, puntos parpadeando color monótonos de SERS fueron observados para la nanoaggregates de plata con las moléculas de tinte preparadas por protocolo 1.37,8,<...
Access restricted. Please log in or start a trial to view this content.
Discusión
Desde el cruce de nanoaggregate plata, SERS se emite. Así, tenemos que preparar nanoaggregates en lugar de nanopartículas coloidales, que se cubren con aniones citrato. Agregados de plata se forman a partir de la salazón efecto creado por la adición de poly-L-lisina, NH -3+ y es el origen del SERS, o cationes de Na+ de NaCl, como se muestra en la Figura S2 del material complementario. Por otra parte, para iluminar los lugares en la zona amplia, el rayo láser desenfoc...
Access restricted. Please log in or start a trial to view this content.
Divulgaciones
El autor no tiene nada que revelar.
Agradecimientos
El autor agradece su fructífera discusión de este trabajo Prof. Y. Ozaki (Universidad de Kwansei Gakuin) y Dr. T. Itoh (nacional del Instituto de Ciencia Industrial avanzada y tecnología). Este trabajo fue apoyado por KAKENHI (subvenciones para investigación científica) desde el Ministerio de educación, cultura, deportes, ciencia y tecnología (no. 16K 05671).
Access restricted. Please log in or start a trial to view this content.
Materiales
| Name | Company | Catalog Number | Comments |
| Silver nitrate, 99.8% | Wako | 194-00832 | |
| Trisodium citrate dihydrate, 99. % | Wako | 191-01785 | |
| Poly-L-lysine aqueous solution, 0.1% | Sigma-Aldrich | P8920 | |
| 3,3'-disulfopropylthiacyanine triethylamine | Hayashibara Biochemical Laboratories | NK-2703 | a kind of thiacyanine dyes |
| 3,3'-diethyl-5,5'-dichloro-9-methylthiacarbocyanine iodine salt | Hayashibara Biochemical Laboratories | SMP-9 | a kind of thiacarobocyanine dyes |
| Sodium chloride, 99.5% | Wako | 191-01665 | |
| Dimroth condenser | Iwaki | 61-9722-22 | perchased from AS ONE |
| Magnetic stirrer | Corning | DC-420D | |
| Oil bath | Advantech | OS-220 | |
| Glass plate | Matsunami | S-1112 | Microscope slide |
| Blower | Hozan | Z-288 | Air duster |
| Liquid blocker pen | Daido Sangyo | LIQUID BLOCKER (Super Pap Pen). Ready-to-use hydrophobic barrier pen designed for immunohistochemistry applications | |
| Inverted microscope | Olympus | IX-70 | |
| Objective lens | Olympus | LCPlanFl 60× | NA 0.7 |
| Dark field condenser | Olympus | U-DCD | NA 0.8–0.92 |
| Cooled digital CCD camera | Hamamatsu | ORCA-AG | controlled by software Aqua Cosmos |
| Software for the cooled digital CCD camera | Hamamatsu | AquaCosmos | used for also derivation of the time-profiles from the blinking spots in the video |
| Color CCD camera | ELMO | TNC-C920 | not used for analysis |
| DPSS laser | RGB laser system | NovaPro532-75 | λ = 532 nm; 60 mW (corresponds to a power density of 600 W/cm2) |
| Interference filter | Semrock | LL01-532-12.5 | |
| Long pass filter | Semrock | BLP01-532R-25 | |
| Software for the distinguishment and counting of the bright/dark events | home-maid | programmed by C++ | |
| Software for the fitting by a power law | LightStone | Origin6.1 |
Referencias
- Qian, X. M., Nie, S. M. Single-molecule and single-nanoparticle SERS: from fundamental mechanisms to biomedical applications. Chem. Soc. Rev. 37, 912-920 (2008).
- Pieczonka, N. P. W., Aroca, R. F. Single molecule analysis by surfaced-enhanced Raman scattering. Chem. Soc. Rev. 37, 946-954 (2008).
- Kneipp, J., Kneipp, H., Kneipp, K. SERS -a single-molecule and nanoscale tool for bioanalytics. Chem. Soc. Rev. 37, 1052-1060 (2008).
- Kitahama, Y., Ozaki, Y. Analysis of blinking SERS by a power law with an exponential function. Frontiers of Surface-Enhanced Raman Scattering: Single-Nanoparticles and Single Cells. , Wiley. Chichester. Chapter 6 (2014).
- Kitahama, Y. Truncated Power Law Analysis of Blinking SERS. Frontiers of Plasmon Enhanced Spectroscopy Volume 1 (ACS Symposium series Vol. 1245). , American Chemical Society. Washington DC. Chapter 4 (2016).
- Bizzarri, A. R., Cannistraro, S. Lévy Statistics of Vibrational Mode Fluctuations of Single Molecules from Surface-Enhanced Raman Scattering. Phys. Rev. Lett. 94, 068303(2005).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Power-law analysis of surface-plasmon-enhanced electromagnetic field dependence of blinking SERS of thiacyanine or thiacarbocyanine adsorbed on single silver nanoaggregates. Phys. Chem. Chem. Phys. 13, 7439-7448 (2011).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of excitation laser intensity dependence of blinking SERRS of thiacarbocyanine adsorbed on single silver nanoaggregates by using a power law with an exponential function. Chem. Commun. 47, 3888-3890 (2011).
- Kitahama, Y., Enogaki, A., Tanaka, Y., Itoh, T., Ozaki, Y. Truncated power law analysis of blinking SERS of thiacyanine molecules adsorbed on single silver nanoaggregates by excitation at various wavelengths. J. Phys. Chem. C. 117, 9397-9403 (2013).
- Kitahama, Y., Araki, D., Yamamoto, Y. S., Itoh, T., Ozaki, Y. Different behaviour of molecules in dark SERS state on colloidal Ag nanoparticles estimated by truncated power law analysis of blinking SERS. Phys. Chem. Chem. Phys. 17, 21204-21210 (2015).
- Kitahama, Y., Nagahiro, T., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of blinking from multicoloured SERS-active Ag colloidal nanoaggregates with poly-L-lysine via truncated power law. J. Raman. Spectrosc. 48, 570-577 (2017).
- Habuchi, S., et al. Single-Molecule Surface Enhanced Resonance Raman Spectroscopy of the Enhanced Green Fluorescent Protein. J. Am. Chem. Soc. 125, 8446-8447 (2003).
- Weiss, A., Haran, G. Time-Dependent Single-Molecule Raman Scattering as a Probe of Surface Dynamics. J. Phys. Chem. B. 105, 12348-12354 (2001).
- Emory, S. R., Jensen, R. A., Wenda, T., Han, M., Nie, S. Re-examining the origins of spectral blinking in single-molecule and single-nanoparticle SERS. Faraday Discuss. 132, 249-259 (2006).
- Itoh, T., Iga, M., Tamaru, H., Yoshida, K., Biju, V., Ishikawa, M. Quantitative evaluation of blinking in surface enhanced resonance Raman scattering and fluorescence by electromagnetic mechanism. J. Chem. Phys. 136, 024703(2012).
- Willets, K. A. Super-resolution imaging of SERS hot spots. Chem. Soc. Rev. 43, 3854-3864 (2014).
- Dieringer, J. A., Lettan, R. B., Scheidt, K. A., Van Duyne, R. P. A Frequency Domain Existence Proof of Single-Molecule Surface-Enhanced Raman Spectroscopy. J. Am. Chem. Soc. 129, 16249-16256 (2007).
- Cichos, F., von Borczyskowski, C., Orrit, M. Power-law intermittency of single emitters. Curr. Opin. Colloid Interface Sci. 12, 272-284 (2007).
- Tang, J., Marcus, R. A. Mechanisms of fluorescence blinking in semiconductor nanocrystal quantum dots. J. Chem. Phys. 123, 054704(2005).
- Lee, P. C., Meisel, D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J. Phys. Chem. 86, 3391-3395 (1982).
- Krichevsky, O., Bonnet, G. Fluorescence correlation spectroscopy: the technique and its applications. Rep. Prog. Phys. 65, 251-297 (2002).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and Chemical Applications of Fluorescence Correlation Spectroscopy: A Review. Biochemistry. 41, 697-705 (2002).
Access restricted. Please log in or start a trial to view this content.
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados