Method Article
Evacuación endoscópica mínimamente invasiva de hemorragia intracerebral
En este artículo
Resumen
En este trabajo se detalla el protocolo quirúrgico para la evacuación endoscópica mínimamente invasiva de la hemorragia intracerebral mediante la técnica SCUBA.
Resumen
La hemorragia intracerebral (ICH) es un subtipo de accidente cerebrovascular con alta mortalidad y malos resultados funcionales, en gran parte porque no hay opciones de tratamiento basadas en la evidencia para este proceso devastador de la enfermedad. En la última década, han surgido una serie de cirugías mínimamente invasivas para abordar este problema, una de las cuales es la evacuación endoscópica. La aspiración estereotáctica de sangre submarina ICH (SCUBA) es una novedosa técnica de evacuación endoscópica realizada en una cavidad llena de líquido utilizando un sistema de aspiración para proporcionar un grado adicional de libertad durante el procedimiento. El procedimiento SCUBA utiliza un dispositivo de succión, endoscopio y vasea y se divide en dos fases. La primera fase implica la aspiración máxima y la irrigación mínima para disminuir la carga de coágulos. La segunda fase implica aumentar el riego para la visibilidad, disminuir la fuerza de aspiración para la aspiración dirigida sin perturbar la pared de la cavidad y cauterizar cualquier vaso sangrante. Utilizando el endoscopio y la varita de aspiración, esta técnica tiene como objetivo maximizar la evacuación del hematoma al tiempo que minimiza el daño colateral al cerebro circundante. Las ventajas de la técnica SCUBA incluyen el uso de una funda endoscópica de bajo perfil que minimiza la interrupción cerebral y una visualización mejorada con una cavidad llena de líquido en lugar de una llena de aire.
Introducción
La hemorragia intracerebral es una hemorragia que se produce en el parénquima cerebral y es el subtipo de ictus más devastador en términos de mortalidad ydiscapacidad. La incidencia mundial de ICH es de aproximadamente 24.6 por cada 100,000 individuos, con 40,000 a 67,000 casos que ocurren cada año en los EE.UU.1,2. La hemorragia intracerebral es una emergencia médica que requiere un diagnóstico y manejo rápidos. Históricamente, los resultados han sido sombríos, con tasas de mortalidad del 40% a 1 mes, 51-54% a 1 año y 71% a los 5 años3,4,5,6. Una razón clave para un pronóstico tan pobre es que no hay tratamientos basados en la evidencia para este proceso de la enfermedad. Los ensayos clínicos previos (STICH I y II) no demostraron mejores resultados para la cirugía en comparación con el tratamiento médico conservador7,8. Una hipótesis propuesta para el fracaso de las craneotomías es que cualquier beneficio obtenido de la evacuación del coágulo es superado por el extenso trauma cerebral infligido por la naturaleza invasiva del procedimiento. Como resultado, en la última década, se han desarrollado una serie de técnicas mínimamente invasivas para intentar resolver este problema, cada una con ventajas y desventajas. Las técnicas se pueden agrupar en dos categorías: aspiración estereotáctica con trombólisis y evacuación activa. El primero consiste en aspirar el coágulo a través de un orificio de rebaba, administrar un agente trombolítico y drenar el coágulo residual a través de un catéter durante el período de varios días. Esta técnica se está probando actualmente en el ensayo clínico MISTIE y es utilizada por médicos en China con la aguja craneopuncture YL-19,10. La evacuación activa, por otro lado, implica aspirar todo el coágulo en un solo procedimiento sin la necesidad de un catéter drenante.
También se están llevando a cabo varios ensayos clínicos para esta técnica, incluido ENRICH, que utiliza el sistema NICO BrainPath para la evacuación transsalcal asistida por endoporte; el ensayo INVEST11, que es un estudio de viabilidad de un solo brazo que utiliza los sistemas Penumbra Apollo o Artemis para la evacuación endoscópica; y el ensayo MIND, que es un ensayo clínico aleatorizado multicéntrico que evalúa la evacuación endoscópica utilizando el dispositivo Artemis. La evacuación endoscópica es una técnica prometedora porque tiene el canal de trabajo de perfil más bajo para minimizar el trauma cerebral12. Este artículo describe una técnica endoscópica específica descrita como Stereotactic ICH Underwater Blood Aspiration (SCUBA)13. La primera fase se centra en la citorregulación del hematoma mediante aspiración máxima mientras se trabaja dentro del extremo de la hela. La segunda fase utiliza una alta tasa de irrigación para aspirar coágulos residuales y cauterizar cualquier vaso sangrante de una manera altamente dirigida.
Hay tres dispositivos utilizados en el procedimiento SCUBA: una vasea (6,33 mm), endoscopio y sistema de aspiración. El sistema de aspiración consiste en una varita quirúrgica (2,6 mm) diseñada para caber dentro del canal de trabajo de un endoscopio, que se inserta en la vaia. La varita es capaz de aspirar y, con solo presionar un botón en el mango, morcelación. El componente de morcelación del dispositivo es una bident giratoria en la punta del tubo de succión que gira al activarse. La succión se activa cubriendo el orificio en el pulgar en el mango, y el bident se activa presionando firmemente el botón. La activación por succión en este sentido es similar a los instrumentos de succión neuroquirúrgica comunes.
Protocolo
Previo a la realización de este protocolo, se obtuvo la aprobación institucional requerida y el consentimiento del paciente. Todos los procedimientos fueron aprobados por el Hospital Mount Sinai.
1. Criterios de inclusión
- Incluir pacientes que cumplan con todos los siguientes criterios: edad > 18 años, Escala de Rankin modificada al < 4, 4 de la Presente Escala de Coma de Glasgow (GCS) > 4, presentación de la Escala de Accidente Cerebrovascular de los NIH (NIHSS) ≥ 6, inicio de los síntomas < 24 horas antes de la tomografía computarizada inicial (la evacuación mínimamente invasiva de la ICH se puede realizar dentro de las 72 horas posteriores al ictus), localización supratentorial de ICH, volumen de ICH > 20 cm3,estabilidad en volumen de ICH medida en dos tomografías computarizadas con 6 horas de diferencia, presión arterial sistólica controlada a < 160 mmHg durante al menos 6 horas antes de la cirugía.
2. Criterios de exclusión
- Excluir a los pacientes que cumplan con uno o más de los siguientes criterios: la tomografía computarizada demuestra una hemorragia en expansión; signo puntual en las imágenes de CTA; lesión subyacente no asegurada(por ejemplo, malformación arteriovenosa, aneurisma, tumor); conversión hemorrágica de un accidente cerebrovascular isquémico agudo; ubicación infratentorial de ICH; hemorragia intraventricular grande que requiere tratamiento como resultado del efecto de masa o cambio; extensión de la hemorragia en el mesencéfalo; requisito absoluto de anticoagulación a largo plazo; coagulopatía; recuento de plaquetas < 100.000 células/mm3; inr> 1,4; tiempo de tromboplastina parcial activada (PTA) elevada; presentar GCS < 4, alto riesgo de accidente cerebrovascular isquémico; necesidad emergente de descompresión quirúrgica; incapacidad para dar su consentimiento para el procedimiento; está embarazada, amamantando o muestra una prueba de embarazo positiva; evidencia de infección activa; o cualquier enfermedad o afección comórbida que se espera que comprometa la supervivencia.
3. Posicionamiento y planificación
- Administrar anestesia general al paciente utilizando técnicas estándar.
- Mantenga las condiciones estériles durante todo el procedimiento preparando estérilmente la piel y cubriendo el área quirúrgica.
- Planifique la trayectoria de la evacuación mediante el uso de imágenes volumétricas preoperatorias para dibujar una línea a lo largo del eje largo del hematoma hasta la superficie externa del cráneo, de modo que la punta de la funda se sitúe de 1 a 2 cm desde el extremo distal del hematoma.
NOTA: Las cosas importantes a tener en cuenta al planificar la trayectoria son minimizar la interrupción del tejido cerebral (especialmente las estructuras elocuentes) y evitar cualquier vasculatura visible en imágenes no invasivas. La planificación de la trayectoria se realiza en un software de navegación estereotáctica, que varía según la institución. Una comparación de los sistemas de navegación comúnmente utilizados en la evacuación ICH está disponible en la literatura médica14. - Coloque al paciente en la posición anatómica correcta dependiendo de la ubicación del hematoma.
NOTA: La mayoría de los casos (80%) se realizan en decáno supino, y una minoría se realiza prona (15%) o supina con la cabeza girada (5%).
4. Apertura
- Haga una incisión lineal y horizontal de 2 cm a lo largo de la piel dentro de un pliegue natural de la piel.
- Abra el cráneo con una craniectomía de 1 a 1,2 cm de diámetro con un taladro de alta velocidad con una rebaba de corte de 5 mm. Intente alinear la craniectomía con el eje largo del hematoma, pero evite las estructuras de la línea media y los territorios cerebrales elocuentes.
NOTA: Un perforador es más grande de lo necesario, especialmente si el defecto está en la frente. - Si la trayectoria no es perfectamente perpendicular al cráneo, perfore un cilindro en el hueso a lo largo de la trayectoria planificada para garantizar una movilidad óptima de la vainela y el endoscopio dentro de la craniectomía, pero tenga en cuenta que la intersección con la duramadre no será perpendicular.
- Use cera ósea, espuma de gel en la trombina y cauterización bipolar para lograr la hemostasia.
- Visualice el hematoma subyacente usando ultrasonido para confirmar su tamaño y posición.
NOTA: La calidad del ultrasonido es más alta utilizando el transductor de orificio de rebaba en un campo húmedo antes de la durotomía. - Abra la duramadre de manera cruciada y cauterice las hojas durales hasta dentro de un milímetro del borde óseo.
NOTA: Evite las venas o arterias grandes. - Incise la piamadre 1 cm con una cuchilla #11 antes de cauterizar. Si se obtiene una biopsia cerebral, este es el momento ideal. Use pórceps tumorales o el extremo de la copa de un instrumento Penfield 1. Evite la cauterización hasta que se obtenga la biopsia.
- Cauterizar la incisión pial y la corteza subyacente con cauterización bipolar.
5. Fase 1 Evacuación
- Inserte la muestra introductora a lo largo de la trayectoria planificada con un estilista de navegación colocado dentro de la sheath. El estilo proporciona comentarios en vivo sobre la ubicación de la punta.
NOTA: Dado el pequeño tamaño de la craneectomía de 1 cm, a menudo no es posible un enfoque "transsalcal"; por lo tanto, la pia es incisa e ingresada en un espacio no vascular inmediatamente debajo de la craneectomía. - Si el coágulo es particularmente fibroso y se encuentra resistencia, haga un ligero ajuste en la valina para alcanzar el punto objetivo.
- Retire el introductor y la sonda de navegación una vez que se alcance el punto objetivo, a 1-2 cm del extremo distal del hematoma.
NOTA: Algunos operadores prefieren utilizar la navegación estereotáctica registrada en el endoscopio en lugar del introductor de la muestra para la navegación continua. - Observe la posición de la vasela marcándola a nivel de la piel.
NOTA: Si la presión dentro del hematoma es alta, el líquido puede fluir fuera de la vaina durante este paso. - Prepare el endoscopio activando los ajustes preferidos, incluidos el balance de blancos, el brillo, el filtro y la intensidad de la luz.
- Conecte el tubo de riego de una bolsa salina de 2 L a la altura del hombro al puerto de trabajo izquierdo y ajuste el caudal a aproximadamente el 25% en el endoscopio. Abra el puerto derecho del endoscopio todo el camino, lo que permite la salida del líquido de irrigación.
- Inserte el endoscopio en la heda. Inserte la varita dentro del canal de trabajo del endoscopio y sostenga la varita con la mano dominante.
NOTA: Para esta fase del procedimiento, mantenga el endoscopio y la varita dentro del extremo de la vase, aproximadamente de 0,5 a 2 cm desde el final de la vase. - Use el dedo puntero para amortiguar la distancia entre el endoscopio y el mango de la varita para mantener una conciencia constante de la ubicación de la punta del dispositivo dentro de la vaia.
- Establezca la fuerza de succión del sistema de aspiración al 100% y establezca el caudal de riego en bajo (~ 25%).
- Aspire cualquier hematoma líquido que se presente al final de la vaina manteniendo la varita dentro del distal 1 cm de la vaina.
NOTA: A medida que se aspira el hematoma, la cavidad colapsará hacia adentro debido al efecto de masa reducida. El riego constante mantiene la estructura de la cavidad durante la fase 2 de la evacuación. - Si se encuentra un coágulo sólido que no aspira solo con succión, active el bident dentro de la varita para digerir el coágulo.
- Si un trozo de coágulo es demasiado grande o fibroso para la succión y se adhiere a la punta de la varita, retire todo el endoscopio y la varita junto con el coágulo, teniendo cuidado de no desalojar el coágulo de la varita.
NOTA: Esto se llama la técnica ADAPT (A Direct Aspiration First Pass Technique), haciendo referencia a la práctica de extirpar el trombo intravascular durante la trombectomía para el accidente cerebrovascular isquémico agudo15. - Si la pieza de coágulo es particularmente grande con una cápsula fibrosa y las dos técnicas anteriores no funcionan, use el canal de trabajo del endoscopio como una succión adicional.
- Para lograr esto, conecte una succión quirúrgica convencional al segundo puerto del endoscopio (generalmente la vía de salida de riego) con la válvula cerrada pero lista para la activación. Dibuje el trozo grande de coágulo en el extremo de la vava con la varita. Cierre el puerto de entrada de riego y abra el puerto de salida para activar la succión quirúrgica máxima. El coágulo ahora está atascado en la punta de la varita, el endoscopio y la vasea. Retire la varita, el endoscopio, la vasea y coagule juntos.
NOTA: Esto se denomina técnica de doble ADAPTACIÓN.
- Para lograr esto, conecte una succión quirúrgica convencional al segundo puerto del endoscopio (generalmente la vía de salida de riego) con la válvula cerrada pero lista para la activación. Dibuje el trozo grande de coágulo en el extremo de la vava con la varita. Cierre el puerto de entrada de riego y abra el puerto de salida para activar la succión quirúrgica máxima. El coágulo ahora está atascado en la punta de la varita, el endoscopio y la vasea. Retire la varita, el endoscopio, la vasea y coagule juntos.
- Si el coágulo tiene una cápsula fibrosa y es difícil de separar del tejido cerebral, use la punta de la vaia como un disector romo.
NOTA: Esto se llama la técnica de disección de la vacia. - Después de aspirar, explore la cavidad a la misma profundidad girando suavemente la funda lateralmente hasta que no quede ningún coágulo residual a esa profundidad.
- Retire la valina 1 cm y repita los pasos de aspiración de la Fase 1 hasta que la vaila llegue a la pared proximal de la cavidad.
6. Fase 2 Evacuación
- Disminuir la succión de la varita al 25% y aumentar el riego al 100% para mejorar la visibilidad en la cavidad. Explore el hematoma residual e identifique las arterias sangrantes.
NOTA: Durante esta fase, es fundamental minimizar las fuerzas de succión en el tejido cerebral pericavity. - Aspire cualquier hematoma residual de manera específica con bajo poder de aspiración, teniendo cuidado de no dañar la materia cerebral circundante que puede incurrir en sangrado adicional o causar traumatismos en la pared de la cavidad.
NOTA: Los productos sanguíneos pueden interferir inicialmente con la visualización óptima, pero la cavidad se aclarará con el paciente, la irrigación continua. Si la cavidad no se aclara, identifique y cauterice los vasos sangrantes. - Monitoree cualquier vaso sangrante y diríjase a ellos en consecuencia con los siguientes pasos:
- Si los vasos sangrantes pequeños son difíciles de visualizar, dirija un flujo constante de riego hacia el vaso flotando inmediatamente sobre el sitio de sangrado con la funda y tirando del endoscopio hacia atrás desde la punta. Una vez que el recipiente esté mejor visualizado, cauterice el recipiente.
NOTA: Esto se llama la técnica de desplazamiento de la varica. - Irrigar la cavidad hasta que se logre la hemostasia
- Aplique presión usando el extremo de la vacia si el riego puro no funciona.
- Utilice la cauterización bipolar si los dos métodos anteriores no funcionan.
- Aspirar cualquier hematoma residual a lo largo de los lados o en las grietas de la cavidad.
NOTA: Este paso se vuelve más fácil una vez que se abordan los vasos sangrantes, lo que permite una visualización clara.
- Si los vasos sangrantes pequeños son difíciles de visualizar, dirija un flujo constante de riego hacia el vaso flotando inmediatamente sobre el sitio de sangrado con la funda y tirando del endoscopio hacia atrás desde la punta. Una vez que el recipiente esté mejor visualizado, cauterice el recipiente.
- Asegúrese de que la cavidad esté libre de todos los hematomas visibles y vasos sangrantes.
NOTA: Si hay una capa delgada de coágulo fresco por sangrado intraoperatorio, tenga cuidado de causar más sangrado en el intento de aspiración de esta capa delgada de sangre fresca. Aspire suavemente o deje la sangre fresca en su lugar. Diferenciar los coágulos de la pared de la cavidad es un desafío importante en el procedimiento.
7. Evaluación y cierre
- Retire el endoscopio y la funda lentamente, con el endoscopio en la punta de la funda para examinar las paredes del tracto al salir para controlar el sangrado adicional.
NOTA: Algunos operadores han abogado por infundir trombina en la cavidad en este punto, ya sea agregando trombina directamente al líquido de irrigación o inyectando gelatina mezclada con trombina a través del endoscopio. Esta es una opción razonable, pero inyectar gelatina mezclada con trombina hará que las imágenes de ultrasonido sean imposibles. - Use el ultrasonido de orificio de rebaba para evaluar si hay hematoma residual o sangrado activo.
NOTA: El ultrasonido es útil para resolver dudas sobre cualquier región cuestionable, así como para detectar grandes áreas de hematoma residual que puedan haberse perdido bajo visualización directa. - Realice una exploración Dyna-CT intraoperatoria si está disponible para evaluar el grado de evacuación.
NOTA: El objetivo del procedimiento es obtener al menos un 80% de evacuación. Si queda más del 20% del hematoma, reinicie la Fase 2 de la evacuación antes de continuar con los siguientes pasos. - Aplique espuma de gel hemostático en el orificio de rebabas sobre la superficie del cerebro.
- Cubra la craniectomía con una placa de titanio y asegúrela con tornillos de titanio.
- Cierre la galea y las capas subcutáneas con 3-0 suturas de poliglactina 910.
- Cierre la piel con 4-0 poliglicecrona 25 puntos subcuticulares, seguido de tiras de cinta quirúrgica de cierre de piel.
Resultados
La técnica de evacuación SCUBA se ha descrito en 47 pacientes sometidos a evacuación endoscópica de ICH entre diciembre de 2015 y septiembre de 2017. El volumen medio preoperatorio de ICH se notificó como 42,6 cm3 (desviación estándar = 29,7 cm3;volumen medio postoperatorio de ICH = 4,2 cm3, DE 6,6 cm3), lo que resultó en una tasa media de evacuación del 88,2% (DE 20,8%) (Tabla 1). Un ejemplo de tomografías computarizadas preoperatorias y postoperatorias se muestra en la Figura 1. En 23 (48,9%) casos, se detectaron vasos hemorrágicos activos, y en 12 (52,2%) de estos casos, el sangrado emanó de más de un vaso(Tabla 2). El sangrado se abordó utilizando solo irrigación en 5 casos (10,6%) y electrocauteridad en 18 casos (38,3%)(Tabla 2). El sangrado postoperatorio se aisló a un solo caso (2,1%) en el que la TC de cabeza de rutina realizada el día 1 postoperatorio demostró que la cavidad de evacuación se había rellenado con hemorragia que parecía originarse por un sangrado superficial de los vasos galeales en el tracto de acceso y la cavidad(Tabla 2). El examen de este paciente no empeoró y no requirió cirugía adicional.
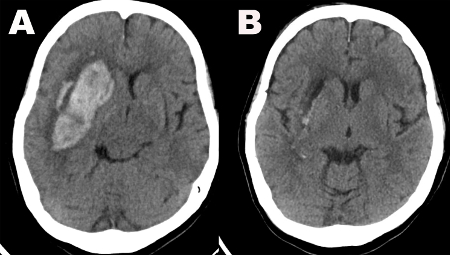
Figura 1: Tomografías computarizadas. (A) La imagen preoperatoria de la cabeza por TC muestra una gran hemorragia de los ganglios basales derechos. (B)La imagen de la cabeza por TC realizada en el día 1 postoperatorio demuestra una evacuación casi completa del hematoma. Haga clic aquí para ver una versión más grande de esta figura.
| Variable | Significar | Desviación estándar |
| Volumen preoperatorio | 42.6 | 29.7 |
| Volumen postoperatorio | 4.2 | 6.6 |
| Porcentaje de evacuación | 88.2% | 20.8% |
Tabla 1: Detalles de la evacuación. Volúmenes de ICH y tasas de evacuación para el procedimiento SCUBA.
| Variable | Número | Por ciento |
| Total de pacientes | 47 | - |
| Sangrado activo identificado | 23 | 48.9% |
| Buques individuales | 11 | 23.4% |
| Múltiples buques | 12 | 25.5% |
| Riego | 5 | 10.6% |
| Electrocauterización | 18 | 38.3% |
| Sangrado postoperatorio | 1 | 2.1% |
Cuadro 2: Detalles operativos. Detalles quirúrgicos (específicamente vasos sangrantes) encontrados durante el procedimiento de BUCEO.
Discusión
Existen varias mejores prácticas operativas para aprender e implementar durante la evacuación endoscópica de ICH. En primer lugar, es fundamental minimizar la interrupción del tejido cerebral siempre que sea posible. Lograr esto comienza con la optimización de la trayectoria quirúrgica para que la vaizante recorra el curso más corto posible evitando estructuras elocuentes. Para la ICH supratentorial, las estructuras elocuentes incluyen el área motora suplementaria, las cortezas motoras y sensoriales primarias, el giro temporal y angular superior izquierdo y la corteza visual primaria. Además, la trayectoria debe alinearse con el eje longitudinal del hematoma. Los beneficios de esta estrategia incluyen maximizar la visualización de la cavidad, minimizar la fuerza de torque en el cerebro adyacente al tracto de acceso, aumentar la probabilidad de poder ver los extremos de la cavidad y crear la trayectoria más corta posible hacia el coágulo, minimizando así el trauma cerebral.
Además de minimizar la interrupción del tejido cerebral, también es importante minimizar la distorsión de la cavidad del hematoma. La aspiración en una cavidad cerrada puede distorsionar la materia elástica del cerebro tanto como las fuerzas de compresión con el mismo daño. Para evitar esto, la fuerza de succión debe estar en el nivel mínimo posible necesario para la aspiración efectiva de coágulos sanguíneos. Esto es especialmente importante si la punta de la varita está avanzada más allá de la punta de la varita. La única vez que la fuerza de succión debe estar en alto es durante la Fase 1, cuando la punta está en contacto directo con el coágulo. La fuerza de succión debe disminuir a medida que avanza el procedimiento.
Se han reportado resultados desfavorables cuando la irrigación durante una evacuación endoscópica del hematoma intraventricular conduce a un aumento de la presión intracraneal16. El procedimiento SCUBA evita esto evacuando el hematoma en la Fase 1, que disminuye la presión dentro de la cavidad, y posteriormente irrigando en la Fase 2. En la Fase 2, el endoscopio tiene un segundo puerto de acceso que permite la salida de riego, evitando así la distensión excesiva de la cavidad del hematoma y la presión intracavidad elevada. Además, la vaia y el tracto no forman un sello estanco y el líquido de riego se pierde alrededor de la vaia.
Lograr y mantener la hemostasia durante la Fase 2 es un requisito crucial para una evacuación exitosa de SCUBA. Es importante monitorear meticulosamente cada pared de la cavidad para ver si hay vasos sangrantes y abordarlos en consecuencia con irrigación continua o cauterización bipolar. Lograr una hemostasia perfecta asegura que haya un riesgo mínimo de resangr sangrado postoperatorio.
Dado que la visualización clara y directa del hematoma residual dentro de la cavidad puede no ser siempre posible durante el procedimiento, es una buena práctica verificar la evacuación con imágenes intraoperatorias después de la Fase 2. Ha habido varios casos en los que el examen endoscópico directo sugirió que la cavidad estaba clara, pero se detectó hematoma residual en la ecografía intraoperatoria o en la TC DYNA, lo que llevó a otro paso con la vaina hacia la cavidad y a una evacuación adicional del hematoma.
En esta etapa temprana en el desarrollo de este procedimiento, hay evidencia lo suficientemente fuerte como para sugerir cuál debería ser el límite inferior del porcentaje de evacuación del volumen de coágulos residuales. Aunque actualmente no hay estudios que evalúen los resultados de los porcentajes de evacuación del procedimiento endoscópico, los modelos animales y el ensayo MISTIE sugieren que se prefiere una mayor evacuación9. En ratones inducidos por ICH, las moléculas en la sangre como el hierro tuvieron un efecto tóxico en el tejido cerebral circundante, mientras que los quelantes del hierro redujeron el daño17. El ensayo MISTIE II encontró que el volumen de edema perihematomal fue más pequeño cuando el porcentaje de evacuación superó el 65%, mayor cuando el porcentaje de evacuación varió de 20-65%, y mayor cuando el porcentaje de evacuación fue inferior al 20%18. Estos datos también sugieren que el resultado puede mejorar con un mayor porcentaje de evacuación, pero el estudio no fue impulsado para evaluar esta característica. Los ensayos MISTIE fase III, ENRICH, INVEST y/o MIND pueden arrojar luz sobre esta cuestión.
Un área que queda por resolver es el marco temporal del procedimiento. Muchos protocolos abogan por la evacuación dentro de las 72 horas y después de una exploración de estabilidad de 6 horas para garantizar que el hematoma esté estable. Muchos médicos eligen este curso de acción, ya que un pequeño estudio de 2004 informó complicaciones, resangrado y malos resultados en una pequeña serie de pacientes que se sometieron a craneotomía para cirugía ultra temprana19. Estudios más recientes sobre la evacuación endoscópica mínimamente invasiva han reportado buenos resultados con la evacuación ultra temprana20,21. Los manuscritos que informan sobre la evacuación endoscópica sugieren que el sangrado es identificable y controlable en evacuaciones ultra tempranas. El protocolo de estudio ENRICH requiere la evacuación dentro de las 24 horas posteriores al ictus y no exige un escaneo de estabilidad. La cirugía ultra temprana puede ser una opción en el futuro, pero se necesitan estudios adicionales para evaluar los riesgos y beneficios de la evacuación ultra temprana.
El procedimiento SCUBA es una técnica de evacuación de hemorragia intracerebral mínimamente invasiva que implica un endoscopio utilizando un sistema de aspiración. La evidencia preliminar sugiere que la técnica SCUBA se puede realizar de manera segura y confiable, lo que resulta en un alto porcentaje de evacuación. Se necesitan estudios adicionales para evaluar el impacto de este procedimiento en los resultados funcionales.
Divulgaciones
Christopher Kellner recibió una beca educativa de Penumbra para un curso de CME para enseñar la evacuación endoscópica de hemorragia intracerebral mínimamente invasiva. J Mocco es co-investigador principal del ensayo INVEST, que es un estudio de viabilidad para evaluar la evacuación endoscópica de hemorragia intracerebral mínimamente invasiva financiada por Penumbra. J Mocco es inversor y consultor de Rebound Therapeutics.
Agradecimientos
Esta investigación fue apoyada en parte por una subvención de Arminio y Lucyna Fraga y una subvención del Sr. y la Sra. Durkovic.
Materiales
| Name | Company | Catalog Number | Comments |
| Artemis Device 2.8mm | Penumbra Inc. | AP28 | Cannula Outer Diameter: 2.8mm. Cannula Length: 27cm. Aspiration Tubing Length: 9.5ft; The Food and Drug Administration (FDA) approved the Apollo System in 2014 for use in intraventricular hemorrhage (IVH) evacuation but its indication now includes ICH and the Artemis System was approved for the same IVH and ICH evacuation in 2017. |
| Artemis Device 2.1mm | Penumbra Inc. | AP21 | Cannula Outer Diameter: 2.1mm. Cannula Length: 26cm. Aspiration Tubing Length: 9.5ft |
| Artemis Device 1.5mm | Penumbra Inc. | AP15 | Cannula Outer Diameter: 1.5mm. Cannula Length: 27cm. Aspiration Tubing Length: 9.5ft |
| MAX Canister | Penumbra Inc. | APCAN2 | |
| Pump MAX 110V | Penumbra Inc. | PMX110 | |
| 19-French Sheath | Aesculap USA | FH604SU | Outer Diameter: 6.33mm |
| Storz Lotta 3-port Endoscope | Karl Stortz | 28164 LA / 28164 LS | Outer Diameter: 6.1mm. Two ports for irrigation/suction (1.6mm). One working channel (2.9mm) |
| Medtronic AxiEM | Medtronic | UC201403939 | An advantage of the Medtronic AxiEM system is it does not require pinning or line-of-site navigation. |
| High-speed drill with 5-mm cutting burr | Medtronic | 9BA60 | |
| Bone Wax | Ethicon | W31 | |
| Hemostatic Gel Foam with Thrombin | J&J Healthcare | 2994 | |
| Bipolar Cautery | State of the Art | 401102 | |
| Aloka burr hole ultrasound transducer | Aloka | UST-52114P | |
| 11-blade | Bard Parker | 372611 | |
| Penfield 1 instrument | Sklar Corp | 47-2255 | |
| AxiEM stylet | Medtronic | 9735428 | |
| Titanium plate | Depuy Synthes | 04503023/04503024 | |
| Titanium screws | Depuy Synthes | 0450310301/0450310401 | |
| DYNA CT on the Artis Q | Siemens Healthineers | A91AX-01343-33C1-7600 | |
| 3-0 Vicryl sutures | Ethicon | J416 | |
| 4-0 monocryl subcuticular stitches | Ethicon | Y426 | |
| Steri-Strips | 3M | R1547 |
Referencias
- van Asch, C. J. J., Luitse, M. J. A., Rinkel, G. J. E., vander Tweel, I., Algra, A., Klijn, C. J. M. Incidence, case fatality, and functional outcome of intracerebral haemorrhage over time, according to age, sex, and ethnic origin: a systematic review and meta-analysis. Lancet Neurology. 9 (2), 167-176 (2010).
- Qureshi, A. I., Mendelow, A. D., Hanley, D. F. Intracerebral haemorrhage. Lancet. 373 (9675), 1632-1644 (2009).
- Aguilar, M. I., Freeman, W. D. Spontaneous intracerebral hemorrhage. Seminars in Neurology. 30 (5), 555-564 (2010).
- Broderick, J., et al. Guidelines for the management of spontaneous intracerebral hemorrhage in adults: 2007 update: a guideline from the American Heart Association/American Stroke Association Stroke Council, High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group. Circulation. 116 (16), 391-413 (2007).
- Caceres, J. A., Goldstein, J. N. Intracranial hemorrhage. Emergency Medicine Clinics of North America. 30 (3), 771-794 (2012).
- Poon, M. T. C., Fonville, A. F., Al-Shahi Salman, R. Long-term prognosis after intracerebral haemorrhage: systematic review and meta-analysis. Journal of Neurology, Neurosurgery, and Psychiatry. 85 (6), 660-667 (2014).
- Mendelow, A. D., Gregson, B. A., Rowan, E. N., Murray, G. D., Gholkar, A., Mitchell, P. M. Early surgery versus initial conservative treatment in patients with spontaneous supratentorial lobar intracerebral haematomas (STICH II): a randomised trial. Lancet. 382 (9890), 397-408 (2013).
- Mendelow, A. D., et al. Early surgery versus. initial conservative treatment in patients with spontaneous supratentorial intracerebral haematomas in the International Surgical Trial in Intracerebral Haemorrhage (STICH): a randomised trial. Lancet Neurology. 365 (9457), 387-397 (2005).
- Hanley, D. F., et al. Safety and efficacy of minimally invasive surgery plus alteplase in intracerebral haemorrhage evacuation (MISTIE): a randomised, controlled, open-label, phase 2 trial. Lancet Neurology. 15 (12), 1228-1237 (2016).
- Wang, W. -. Z., et al. Minimally invasive craniopuncture therapy vs. conservative treatment for spontaneous intracerebral hemorrhage: results from a randomized clinical trial in China. International Journal of Stroke. 4 (1), 11-16 (2009).
- Fiorella, D., Arthur, A. S., Mocco, J. D. The INVEST Trial: A Randomized, Controlled Trial to Investigate the Safety and Efficacy of Image-Guided Minimally Invasive Endoscopic Surgery With Apollo vs ..... Neurosurgery. , (2016).
- Fiorella, D., Arthur, A., Bain, M., Mocco, J. Minimally Invasive Surgery for Intracerebral and Intraventricular Hemorrhage: Rationale, Review of Existing Data and Emerging Technologies. Stroke. 47 (5), 1399-1406 (2016).
- Kellner, C. P., et al. The Stereotactic Intracerebral Hemorrhage Underwater Blood Aspiration (SCUBA) technique for minimally invasive endoscopic intracerebral hemorrhage evacuation. Journal of NeuroInterventional Surgery. , (2018).
- Chartrain, A. G., et al. A review and comparison of three neuronavigation systems for minimally invasive intracerebral hemorrhage evacuation. Journal of NeuroInterventional Surgery. , (2017).
- Turk, A. S., et al. ADAPT FAST study: a direct aspiration first pass technique for acute stroke thrombectomy. Journal of NeuroInterventional Surgery. 6 (4), 260-264 (2014).
- Trnovec, S., Halatsch, M. -. E., Putz, M., Behnke-Mursch, J., Mursch, K. Irrigation can cause prolonged intracranial pressure elevations during endoscopic treatment of intraventricular haematomas. British Journal of Neurosurgery. 26 (2), 247-251 (2012).
- Wu, H., Wu, T., Xu, X., Wang, J., Wang, J. Iron toxicity in mice with collagenase-induced intracerebral hemorrhage. Journal of Cerebral Blood Flow & Metabolism. 31 (5), 1243-1250 (2011).
- Mould, W. A., et al. Minimally invasive surgery plus recombinant tissue-type plasminogen activator for intracerebral hemorrhage evacuation decreases perihematomal edema. Stroke. 44 (3), 627-634 (2013).
- Morgenstern, L. B., Demchuk, A. M., Kim, D. H., Frankowski, R. F., Grotta, J. C. Rebleeding leads to poor outcome in ultra-early craniotomy for intracerebral hemorrhage. Neurology. 56 (10), 1294-1299 (2001).
- Nishihara, T., et al. Newly developed endoscopic instruments for the removal of intracerebral hematoma. Neurocritical Care. 2 (1), 67-74 (2005).
- Nagasaka, T., Inao, S., Ikeda, H., Tsugeno, M., Okamoto, T. Inflation-deflation method for endoscopic evacuation of intracerebral haematoma. Acta Neurochirurgica. 150 (7), 685-690 (2008).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados