Method Article
Automatización de un protocolo de emisión de positrones la tomografía (PET) radiosonda síntesis de producción clínica
* Estos autores han contribuido por igual
En este artículo
Resumen
Emisión de positrones tomografía (PET) de los sitios que participan en múltiples ensayos de investigación clínica temprana necesitan capacidades de fabricación robusto y versátil del radiotrazador. Con la radiosonda [18F] clofarabina como ejemplo, ilustramos cómo automatizar la síntesis de un radiotrazador utilizando un radiosynthesizer flexible, basada en cassette y validar la síntesis para uso clínico.
Resumen
El desarrollo de nuevos trazadores de emisión de positrones la tomografía (PET) está permitiendo a los investigadores y los clínicos a una cada vez más amplia gama de objetivos biológicos y procesos de imagen. Sin embargo, el creciente número de marcadores diferentes crea desafíos para su producción en radiofarmacias. Mientras que históricamente ha sido práctico dedicar un radiosynthesizer personalizado configurado y celda caliente para la producción repetida de cada indicador individual, se hace necesario cambiar el flujo de trabajo. Radiosynthesizers comerciales reciente basados en cintas y kits desechables para cada trazador simplificar la producción de marcadores múltiples con un sistema de equipo eliminando la necesidad de modificaciones de trazador específico personalizados. Además, algunos de estos radiosynthesizers permiten al operador desarrollar y optimizar sus propios protocolos de síntesis además de comprar kits comercialmente disponibles. En este protocolo, describimos el procedimiento general de cómo se puede automatizar la síntesis manual de un nuevo trazador PET en uno de estos radiosynthesizers y validado para la producción de marcadores de tipo clínico. Por ejemplo, utilizamos el radiosynthesizer ELIXYS, una herramienta de radiochemistry cassette-basado flexible que puede soportar esfuerzos de desarrollo de trazadores PET, así como fabricación de sondeo clínico habitual en el mismo sistema, para producir [18F] clofarabina ([ 18 F] CFA), un trazador PET para medir la actividad enzimática en vivo desoxicitidina quinasa (dCK). Traducir una manual síntesis consiste en romper el protocolo sintético en los procesos de radioquímica básica que luego se traducen en química intuitiva "operaciones unitarias" soportadas por el software de sintetizador. Estas operaciones pueden rápidamente se convertirán en un programa de síntesis automatizada montando a través de la interfaz de arrastrar y colocar. Después de las pruebas básicas, el procedimiento de síntesis y purificación puede requerir optimización para lograr el rendimiento deseado y la pureza. Una vez que se obtiene el rendimiento deseado, una validación de la síntesis se lleva a cabo para determinar su idoneidad para la producción de la radiosonda para uso clínico.
Introducción
Una creciente variedad de objetivos biológicos se puede visualizar dinámicamente en la vida de los sujetos a través de la modalidad de proyección de imagen molecular PET. PET proporciona en vivo análisis de procesos biológicos, bioquímicos y farmacológicos específicos utilizando radiotrazadores específicos (marcadas con radionúclidos emisores de positrones de moléculas) que se inyectarán en el tema antes de la proyección de imagen1. El uso creciente del PET para el estudio de una amplia variedad de estos procesos en ciencia básica e investigación clínica2,3,4y en el descubrimiento, desarrollo y uso clínico de medicamentos en la atención al paciente5, 6, está llevando a una creciente demanda de diversos radiotrazadores7,8. Para evitar la exposición a la radiación para el quimico y asegurar una producción reproducible de los marcadores de breve duración, se fabrican típicamente con un radiosynthesizer automatizado de operación dentro de una "celda caliente". Radiosynthesizers recientes utilizan una arquitectura de cassette/kit de desechables para simplificar la tarea de cumplir con la fabricación del grado clínico mientras que también proporciona la flexibilidad para preparar varios tipos de radiotrazadores simplemente por intercambio de cassettes9 . Sin embargo, en etapas clínicas tempranas, no hay generalmente no casetes y kits comercialmente disponibles para llevar a cabo la radiosynthesis automatizado; en consecuencia, instalaciones de fabricación de drogas PET luchan para personalizar sistemas para implementar capacidades de la producción de cGMP-grado trazador dentro de un plazo de tiempo adecuado y a un costo razonable. Así, se han desarrollado radiosynthesizers que combinan la arquitectura de cassette/kit con características para facilitar el desarrollo y optimización de trazadores.
La ELIXYS FLEX/CHEM (ELIXYS) es un ejemplo de un radiosynthesizer flexible cassette-basado con una gran reacción, reactivo y disolvente temperatura compatibilidad10. Tiene tres reactores y utiliza un mecanismo robótico para configurar dinámicamente el camino flúido como exige cualquier síntesis particular protocolo11. El software de sintetizador permite la creación de programas de síntesis (secuencias) para diferentes marcadores arrastrando y soltando Operaciones a unitarias tales como Trampa isótopo Isótopos eluir, Añadir Reactivo, reacciona, y se evaporan12. Cada operación de la unidad tiene una variedad de parámetros programables disponibles para el operador, tales como duración, temperaturao gas inerte conducción de presión (presión). Mediante la comprensión de la naturaleza de cada operación de la unidad, una síntesis manual puede traducirse fácilmente en una secuencia de operaciones unitarias y luego modificarse durante la optimización del protocolo13. En combinación con el módulo ELIXYS/pura de la forma, el sistema integrado también puede realizar una purificación automatizado y formulación del trazador PET. Con este radiosynthesizer, hemos divulgado previamente la síntesis automatizada de 24 diferentes 18F etiquetado marcadores y grupos prostéticos11,14,15,16, como así como el radiofluorination enzimático automatizado de biomoléculas17, simplemente cambiando los reactivos y no la configuración del sistema. Otros han demostrado la síntesis automatizada de [18F] RO6958948 para la proyección de imagen de tau Neurofibrilar enredos18, la síntesis automatizada del grupo de prótesis [18F] F-Py-TFP con una etiqueta posterior de péptidos19 y la síntesis automatizada de [18F] AM580 para la proyección de imagen de la fosfodiesterasa 10a (PDE10A)20. Además, varios grupos han demostrado la producción de trazadores adecuados para uso clínico, incluyendo 4-[18F] fluorobencilo-triphenylphosphonium ([18F] FBnTP) para la proyección de imagen de la membrana mitocondrial potencial21, [ 18 F] DCFPyL para la proyección de imagen de membrana prostático específico antígeno (PSMA)22y [18F] THK-5351 para la proyección de imagen de tau23.
En este trabajo, utilizamos nuestra experiencia [18F] CFA para ilustrar cómo un procedimiento manual radiosynthetic puede ser traducido directamente y rápidamente en una síntesis automática conveniente para la producción rutinaria siguiendo pautas del cGMP. El rastreador [18F] CFA fue diseñada para la proyección de imagen de la actividad del dCK. El manual radiosynthesis [18F] CFA fue descrita originalmente por Shu et al. 24 como un procedimiento que utiliza dos reactores, purificación de cartucho silicona intermedia y una purificación final de HPLC paso (véase el Material suplementario, 1 sección para más detalles). Reciente en vitro y los estudios preclínicos han demostrado la especificidad excepcional de este trazador a dCK y estudios primero en humanos han demostrado biodistribución favorable25. Hay un interés inmediato en estudios clínicos de mayor escala para confirmar la sensibilidad [18F] mascota CFA a variaciones en la actividad de dCK y un interés a largo plazo en las potenciales aplicaciones clínicas de este trazador26. Puede ser un biomarcador útil para terapias que desencadenan la activación del T-cell, inducir daño en el ADN o dependen de prodrogas análogo nucleósido dCK-dependiente. En particular, [18F] CFA puede permitir la estratificación de los pacientes para una respuesta potencial al tratamiento con clofarabina. [18F] CFA también puede facilitar el estudio y desarrollo de inhibidores dCK que avanzan hacia los ensayos clínicos. Puesto que tradicionalmente han sintetizado este rastreador manualmente, avanzar en todos estos estudios requiere una síntesis automatizada, confiable de [18F] CFA conveniente para uso clínico.
Aunque hemos divulgado previamente una síntesis automatizada de [18F] CFA para estudios preclínicos16, este protocolo se basa más en estos esfuerzos y modificaciones necesarios para la producción clínica de este indicador, se describe incluyendo la integración de purificación totalmente automatizada y formulación, validación de protocolo y pruebas de control de calidad. Los procedimientos generales descritos aquí no se limitan a desarrollar una síntesis automatizada y clínicamente conveniente [18F] CFA pero se puede generalizar de una manera sencilla para desarrollar síntesis automáticas convenientes para el uso clínico de otras radiotrazadores marcados con flúor-18.
Protocolo
1. general procedimiento para la automatización y validación de un protocolo Radiosynthesis fabricación clínica
-
Analizar la elegibilidad del esquema síntesis manual para la fabricación clínica de
- Realizar análisis de riesgos de contaminación del producto con cualquier producto químico residual no deseado.
- Evitar clase 1 disolventes como benceno y reemplazarlos con disolventes alternativos adecuados (clase 2 o clase 3).
- Evite los productos químicos que pueden ser difíciles de detectar en la formulación final como posibles impurezas residuales.
- Elegir sólo productos químicos comercialmente disponibles en grado de alta pureza (el grado USP o Ph.Eur. deseado) y cuentan con un certificado de análisis.
- Refinar el esquema de síntesis si disolventes ni productos químicos indeseables son detectados por el análisis de riesgo y repetición sección 1.1 hasta que no queden.
- Realizar análisis de riesgos de contaminación del producto con cualquier producto químico residual no deseado.
-
Automatizar el protocolo de síntesis
- Si un protocolo automatizado para el trazador con el mismo sintetizador ya ha sido creado y subido a un repositorio en línea, descargar una copia del programa de síntesis.
- Si no existe un programa de síntesis automatizada, cree uno.
- Usando papel y lápiz, dividir la síntesis manual en pasos de alto nivel (p. ej., secado/activación de fluoruro [18F], calefacción para facilitar una reacción radioquímica, realizando un paso de purificación, etcetera.). Más romper los pasos en discretos, procesos básicos que se requieren. Por ejemplo, el esquema de la síntesis de [18F] CFA se muestra en la figura 1, la identificación de los pasos de alto nivel se muestra en la figura 2Ay figura 2Bmuestra la ruptura en los procesos.
- Usando papel y lápiz, mapa de cada proceso en las operaciones de la unidad individual proporcionadas por el software de sintetizador. Por ejemplo, un análisis de la cartografía de los procesos básicos en la síntesis de [18F] CFA a las operaciones de la unidad adecuada en el sintetizador software13 se muestra en la figura 2.
- Usando la interfaz de programación de radiosynthesizer, crear un programa en blanco y anexar cada una de las operaciones de la unidad identificada en la secuencia de clic en el botón de menú (arriba izquierda) y seleccionar secuencias, y haciendo clic en el nuevo Secuencia botón. Para el funcionamiento de cada unidad identificada en el paso 1.2.2.2, arrastre el funcionamiento de la unidad de las operaciones disponibles a la vista de tira de película y haga clic en o tipo para completar el valor deseado de cada parámetro de la operación de la unidad. La figura 3 muestra un ejemplo de la interfaz cuando todas las operaciones para sintetizar [18F] Franco han sido pobladas, y el usuario ha seleccionado la primera operación de unidad reaccionar para editar valores de parámetro. El programa de síntesis final [18F] CFA se describe en el Material adicional, Tablas S1 y S2.
- Verificar el programa de síntesis.
- Llevar a cabo una marcha en seco. Establecer y ejecutar el programa como en los pasos 2.1-2.3, usando todos los reactivos y solventes distintos de los radionucleidos (p. ej., flúor [18F]) para verificar su comportamiento.
- Si es necesario, ajuste los valores de parámetro de funcionamiento de unidad en el programa (por ejemplo, tiempo o presión conduce a transferir completamente un reactivo, el tiempo/temperatura para evaporar el solvente al nivel deseado, etc.) y vuelva a probar. Para ajustar valores de los parámetros, en primer lugar, volver al modo de Editar seleccionando secuencias en el menú principal (arriba izquierda) y seleccione el programa recién creado. A continuación, haga clic en la operación de la unidad deseada en la vista tira de diapositivas (parte inferior de la pantalla), desplácese hasta el parámetro deseado y seleccione o escriba el nuevo valor.
- Realice una prueba de baja actividad (< 370 MBq) para evaluar el programa.
- Optimizar la síntesis automatizada mediante el ajuste de valores de los parámetros para mejorar el rendimiento, tiempo de síntesis, capacidad de repetición, y cualquier otro deseado resultado mensurable.
-
Desarrollar procedimientos de análisis de control de calidad (QC)
- Usando una referencia no radiactivo del producto final y las muestras de posibles impurezas químicas, desarrollar un análisis HPLC de radio o radio-fino método de cromatografía (radio-TLC) capa con suficiente separación de especies para la determinación de pureza química, actividad molar, pureza radioquímica y radioquímica identidad. Validar los métodos analíticos para la repetibilidad y linealidad y determinar los límites de detección y cuantificación.
- Asimismo, desarrollar y validar un método de cromatografía de gases para analizar impurezas volátiles (por ejemplo, cantidades residuales de solventes que se utilizan durante la síntesis).
- Desarrollar y validar pruebas analíticas que permiten la detección y cuantificación de impurezas potenciales (p. ej., cryptand 222 mediante la prueba estándar del color).
- Utilice procedimientos estándar para la determinación de esterilidad, pH, radionucleídica identidad, pureza radionucleídica, concentración de radiactividad, volumen de producto y niveles de endotoxina.
-
Realizar la validación de la síntesis
- Establecer procedimientos operativos estándar (SOPs) para la síntesis y control de calidad procedimientos de prueba e integrar materiales y fabricación de sistema de seguimiento de equipos compatible con buena corriente requisitos de las prácticas (cGMP).
- Validar los procedimientos de síntesis a través de tres independientes y consecutivos producción funciona en los mismos niveles de radioactividad como destinados a la fabricación clínica siguiendo los PEOs. Documentar los resultados de las pruebas de control de calidad y el rendimiento de la síntesis.
- Todas las ejecuciones de validación consecutivos deben pasar los límites de control de calidad predefinidos. Si una validación funciona falla, repita el proceso de validación todo después de tratar adecuadamente la causa de la falta.
2. ejemplo: Automatizado síntesis de CFA [18F] para uso clínico
- Preparar la radiosynthesizer
- Poder en la radiosynthesizer.
- Garantizar el suministro de gas inerte se conectará con la suficiente presión y que las válvulas necesarias están abiertas para que el radiosynthesizer está conectado al suministro de gas.
- Instalar nuevos casetes desechables en el Reactor #1 y #2 posiciones y coloque los recipientes de reacción que contiene barras de agitación magnética. Asegúrese de que cada tubo de inmersión de transferencia de cassette está apuntado directamente hacia abajo.
- Preparar los frascos de reactivo e instalarlos en las cintas según el diagrama en la figura 4.
- Instalar un vacío [18O] frasco de recuperación H2O en la posición de W1 de Cassette #1.
- Activar un cartucho cuaternario methylammonium (QMA) por primer paso 12 mL de una solución de 1 M KHCO3 a través de él, seguido por 12 mL de agua desionizada. Condición de un cartucho Sep-Pak de sílice por pasar 5 mL de acetato de etilo a través de él.
- Conectar los cartuchos y hacer todas las conexiones de tubería de cinta como se muestra en la figura 5A. Verificar que ninguna tubería de cassette (incluidos tubos no utilizados) cuelga en el interior, donde pueden interferir con los movimientos robóticos.
- Conecte la tubería de suministro de fluoruro [18F] desde el ciclotrón a la línea entrada del fluoruro [18F] en la cinta #1.
- Asegúrese de que el recipiente está vacío. Lugar líneas de desechos desde el subsistema de purificación/formulación para el depósito de residuos (es decir, línea inútil del lazo 1 de muestra, HPLC subsistema residuos línea y la línea de residuos de la bomba de jeringa).
- Conecte las líneas de entrada de HPLC. Fase móvil HPLC lugar de entrada de línea "A" en un envase de acetato de amonio 25 mM y línea de entrada de fase móvil de HPLC "B" en un recipiente de EtOH.
- Equilibre la purificación/formulación subsistema y columna HPLC.
- Abra la página de control para el módulo de purificación/formulación del software seleccionando HPLC en el menú principal (arriba izquierda). De forma predeterminada, la ficha de purificación ya se seleccionarán. (Esta página se muestra en la figura 6).
- Fijar el caudal a 5,0 mL/min en la composición definida de solvente y elegir qué posición de la columna se instala la columna de purificación en. Encienda la bomba HPLC en el modo isocrática durante al menos 10 minutos.
- Enjuague la línea de productos y todas las líneas de colección de fracción con la fase móvil, cada uno durante 1 minuto.
- Enjuague cada bucle de muestra HPLC y HPLC muestra lazo transferencia tubo con 10 mL de la fase móvil utilizando una jeringa.
- Conecte las jeringa bomba purificación/formulación subsistema entrada líneas. Uso concentrado cloruro de sodio (90 mg/mL) para la línea de Elute y solución salina al 0.9% para la línea de reconstituir .
- Cebe el subsistema de formulación.
- Desplácese hasta la ficha de formulación de la página de control de purificación/formulación.
- Para preparar el cloruro de sodio concentrado (90 mg/mL), seleccione la ficha de Elute Pulse inicializar inicializar la bomba de jeringa. Pipetear 5 mL.
- Para preparar la solución salina al 0.9%, seleccione el reconstituir ficha dispensar 5 mL.
- Conecte las líneas de producto y Producto Final de la parte delantera del subsistema de depuración/formulación en una conexión de T. Conecte la salida de la T-conexión a un filtro estéril (0,22 μm) que, a su vez, está conectado al frasco de producto final estéril. Inserte una aguja de ventilación con un filtro estéril en el espacio superior del frasco de producto final. Una fotografía de la configuración final del sistema se muestra en la figura 5B.
- Añadir hielo seco y EtOH o MeOH a la trampa de frío.
- Ejecute el programa de síntesis
- Desplácese hasta la lista de programas seleccionando secuencias desde el botón de menú principal (arriba izquierda). Seleccione el programa CFA [18F] e inicie el programa presionando el botón Ejecutar .
- Con cuidado pasar por cada elemento en la lista de verificación de la ejecución y les como se completan. Parte de la pantalla de lista de verificación de la ejecución se muestra en la figura 7.
- Pulse continuar para confirmar que la instalación y causar la síntesis automatizada comenzar.
- Si lo desea, controlar la síntesis en tiempo real a través de información visual (cámaras de reactor), lecturas del sensor (p. ej., temperatura, presión, vacío, lectura de radiación, etc.) y cuentas regresivas. Una captura de pantalla representativa se muestra en la figura 8.
- Durante la operación de la unidad de depuración , seleccione el producto cuando el pico de producto ha comenzado a aparecer en el cromatograma del detector de radiación. Una captura de pantalla representante durante esta operación de la unidad (que contiene un cromatograma de la UV detector y detector de radiación de salida) se muestra en la figura 9.
- Una vez que el pico de cromatograma del detector de radiación vuelve a la línea de fondo, seleccionar residuos para desviar la trayectoria del flujo del subsistema HPLC para el depósito de residuos.
- Establecer y ejecutar el programa de formulación
- De la lista de programas (pantalla desecuencia ), abrir la [18F] formulación CFA programa.
- Ajustar los parámetros de la operación de la unidad de formulación.
- Calcular el volumen de la fracción de producto recogidas (Vfracción) basado en el caudal de la bomba HPLC y la duración de la colección de fracciones.
- Calcular el volumen adicional de cloruro de sodio (90 mg/mL) necesaria para lograr la isotonicity y calcular la cantidad de solución salina adicional necesaria para diluir la concentración de EtOH por debajo del 10%.
- Modificar el programa con estos valores. El volumen de cloruro de sodio (90 mg/mL) se ingresa por el paso de Elute y el volumen de solución salina se introduce para el paso de reconstituir . (Los cálculos se describen en el Material suplementario, Figura S2).
- Guardar el programa.
- Ejecute el programa. El sistema será diluir la fracción recogida producto purificado con cloruro de sodio y solución salina para asegurar la isotonicity de la formulación y entregar a través de un filtro de esterilización en el frasco del producto estéril.
- Recoge formulado [18F] CFA para control de calidad y envío
- Eliminar el producto CFA formulado [18F] de la célula caliente.
- Técnicas de trabajo estéril, retirar dos muestras (300 μL) para realizar las pruebas de control de calidad.
- Utilizar la primera muestra para prueba de esterilidad de la formulación final al inocular medios de cultivo tioglicolato y caldo de soja tríptica para 14 d sin observar ningún crecimiento.
- Utilice el segundo ejemplo para realizar control de calidad según los procedimientos desarrollados en el paso 1.3. A continuación se describen los procedimientos establecidos en las instalaciones biomédicas de ciclotrón UCLA Ahmanson según la farmacopea de los Estados Unidos.
- Evaluar la apariencia mediante inspección visual.
- Evaluar el pH con un papel indicador.
- Evaluar el contenido de endotoxina bacteriana mediante un cinético cromogénico bacteriana endotoxina prueba (BET).
- Evaluar radioquímico identidad con radio-HPLC analítico verificando la elución Co la muestra radiactiva y un compuesto no radiactivo.
- Determinar la pureza radioquímica con radio-HPLC analítico comparando el área bajo la curva (AUC) de impurezas radiactivas en el cromatógrama del detector gamma con la AUC correspondiente al producto deseado.
- Evaluar la pureza química con HPLC analítica mediante la determinación de las AUC en el cromatograma UV-detector de todas las impurezas de la UV-activa.
- Evaluar actividad molar y la masa de portador con radio-HPLC analítica mediante la determinación de la AUC correspondiente al producto deseado en el cromatograma UV-detector.
- Evaluar la vida media de la sonda midiendo su actividad en dos puntos diferentes de tiempo y ajuste una curva de decaimiento.
- Evaluar el contenido de solvente residual de la formulación por cromatografía de gases.
- Evaluar la energía de radionúclidos usando un espectrómetro gamma.
- Evaluar el contenido de cryptand 222 mediante una prueba basada en el TLC.
- Si pasan todas las pruebas, suelte la formulación de la sonda para su envío al sitio de proyección de imagen clínico.
- Funcionamiento posterior y sistema de cierre
- Enjuagar la columna de purificación de HPLC y todos los tubos utilizados para la recolección de productos con 70% EtOH en agua (v/v). Esto debe hacerse con la página de formulario de puro Control, similar al paso 2.1.12.
- Apaga la radiosynthesizer vía el botón de encendido en el software. Una ventana emergente le indicará cuando puede apagar la alimentación del sistema.
- Apague el suministro de aire comprimido y gas inerte por el cierre de las válvulas de cierre adecuado.
- Deje tiempo para la radiactividad residual en la celda caliente al decaimiento (normalmente durante la noche).
- Limpiar el radiosynthesizer
- Retire y deseche todos los casetes, cartuchos, viales de reactor y viales de los reactivos utilizados durante la síntesis.
- Vacíe el contenido de la trampa de frío.
- Limpiar los caminos fluidos del subsistema de purificación.
- Abra el programa de limpieza existente o crear un programa nuevo que contiene una operación de unidad de depuración en modo de limpieza (es decir, con la casilla de verificación de limpieza seleccionado). Ver Material suplementario, Figura S9 para obtener un ejemplo.
- En la página de configuración de parámetro, seleccione la columna que fue utilizada para la purificación y la línea de entrada de fase móvil HPLC conectado a una botella que contiene el 70% EtOH en el agua. Programa un caudal de 2 mL/min, una duración de lavado para cada bucle de inyección de 5 min y una duración de lavado para cada salida de producto y la fracción de 30 s. Seleccione Líneas secas y programa una duración de 30 s.
- Colocar las salidas de línea de fracción en un recipiente grande.
- Ejecute el programa.
- Después de la terminación, vacíe el depósito de residuos.
- Limpiar los caminos líquidos formulación subsistema.
- Abrir un programa ya existente o crear un programa nuevo que contiene una operación de unidad de formulación en modo de limpieza (es decir, con la casilla de verificación de limpieza seleccionada en la ficha limpiar ). Ver Material suplementario, S10 de figura para un ejemplo.
- Llene un reservorio de dilución limpia (en la parte delantera del subsistema de depuración/formulación) con 100 mL de EtOH.
- Coloque el subsistema de purificación/formulación Elute línea de entrada en un depósito de EtOH (contiene > 50 mL de EtOH).
- Coloque las líneas de entrada enjuague y reconstituir en un recipiente junto con la línea de salida de producto final.
- Ejecute el programa.
- Después de la terminación, vacíe el depósito de residuos.
Resultados
Un método para automatizar la producción de [18F] Franco fue desarrollado y se sintetizaron tres lotes de validación. Síntesis, purificación y formulación de [18F] CFA se logró en 90 ± 5 min (n = 3) y el rendimiento radioquímico no corregido por decaimiento 8.0 ± 1,4% (n = 3). Los rendimientos de la actividad de las tres carreras fueron 3.24 GBq, 2,83 GBq y 3.12 GBq, a partir de 34,3 GBq y GBq 41,8 41,1 GBq, respectivamente. Las formulaciones de CFA obtenidos [18F] pasan todas las pruebas de control de calidad (tabla 1). El protocolo automatizado actualmente se utiliza para la producción de grado clínico [18F] CFA para apoyar los ensayos clínicos.
| Datos de control de calidad | Validación de funcionamiento 1 | Validación run 2 | Validación de funcionamiento 3 |
| [requisito de "Pass"] | |||
| Aspecto | Pasar | Pasar | Pasar |
| [claro, incoloro, libre de partículas] | |||
| Concentración de radiactividad en EOS | 213 MBq/mL | MBq/mL 210 | 180 MBq/mL |
| [≤ 740 MBq/mL @ EOS] | |||
| pH | 6 | 5.8 | 6 |
| [5.0-8.0] | |||
| Half-Life | 115 min | 108 min | 112 min |
| [105-115 min] | |||
| Pureza radioquímica | 99% | 99% | 99% |
| [> 95%] | |||
| Identidad radioquímica por tiempo de retención relativo (RRT) | 1.01 | 1.01 | 1.01 |
| [1.00 < RRT < 1.10] | |||
| Actividad molar | 314 GBq/μmol | > 370 GBq/μmol | > 370 GBq/μmol |
| [≥ 3,7 GBq/μmol] | |||
| Masa total de la portadora en producto final | 3.1 μg | < 1 μg | < 1 μg |
| [≤ 50 μg/dosis] | |||
| Masa total de la impureza en el producto final | ND | ND | ND |
| [≤ 1 μg / dosis] | |||
| Volumen de inyección admisible máximo basado en portador total masa ≤ 50 μg/dosis y impureza total masa ≤ 1 μg/dosis | Toda la masa | Toda la masa | Toda la masa |
| Contenido residual de EtOH por cromatografía de gases | 8,90% | 9.50% | 9.60% |
| [≤ 10%] | |||
| Contenido EtOAc residual por cromatografía de gases | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ 5000 ppm] | |||
| Contenido de MeCN residual por cromatografía de gases | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ 410 ppm] | |||
| K222 residual por prueba de mancha de color | Pasar | Pasar | Pasar |
| [< 50 μg/mL] | |||
| Prueba de integridad de membrana de filtro | Pasar | Pasar | Pasar |
| [50 psi ≥ punto de burbuja] | |||
| Endotoxinas bacterianas | Pasar | Pasar | Pasar |
| [≤ 175 EU lote] | |||
| Pureza radionucleídica por espectroscopia gamma | Pasar | Pasar | Pasar |
| [> 99.5%] | |||
| Esterilidad | Pasar | Pasar | Pasar |
| [requisitos de USP < 71 >] |
Tabla 1: datos de prueba de control de calidad (QC) Resumen para los tres lotes de validación. EOB = final de bombardeo; EOS = fin de síntesis; ND = no detectado.
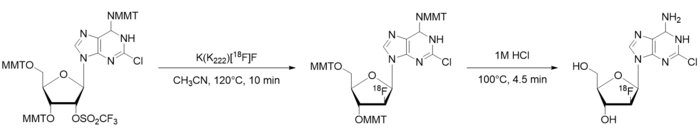
Figura 1: esquema de radiosynthesis CFA [18F]. TMM = Monomethoxytrityl. Haga clic aquí para ver una versión más grande de esta figura.
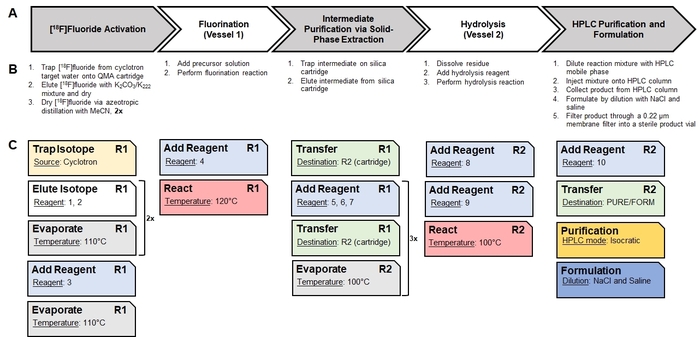
Figura 2: traducción de una manual síntesis en una secuencia automatizada de operaciones unidad. (A) este panel da una descripción de los pasos en la síntesis manual del [18F] CFA. (B) este panel muestra los procedimientos básicos necesitados para realizar cada uno de los pasos. (C) Radiosynthesizer-operaciones específicas de unidad utilizadas para realizar los procedimientos básicos se muestran como tarjetas. La operación de cada unidad tiene su propio conjunto de valores de parámetro (se muestra como subrayado) que se configuran mediante el software. La notación "R1" y "R2" indican los recipientes de reacción #1 y #2, respectivamente. Los reactivos correspondientes a los números de reactivo se identifican en la figura 4. La serie de operaciones unitarias se guarda como una secuencia y ejecutada por el software para realizar la síntesis automatizada. Haga clic aquí para ver una versión más grande de esta figura.
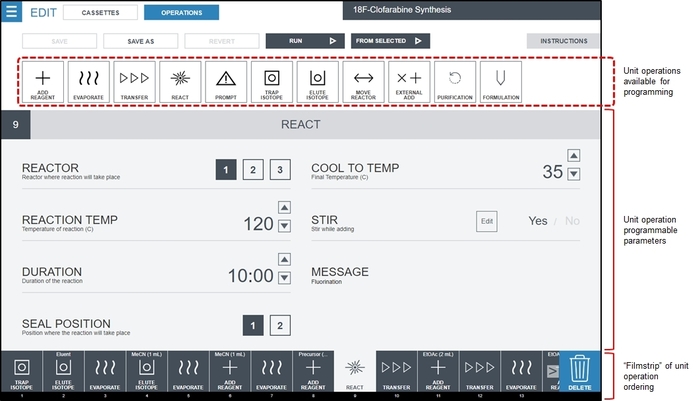
Figura 3: captura de pantalla de la interfaz de software radiosynthesizer (ELIXYS) para crear un programa de síntesis. Operaciones unitarias se colocan en el orden deseado en la tira de diapositivas mediante una interfaz de arrastrar y colocar. En esta captura de pantalla, se selecciona una operación de la unidad de reacción , y sus valores de parámetro editable se muestran en la parte principal de la pantalla. En este ejemplo, la reacción de fluoración se llevará a cabo en el recipiente de la reacción #1 (sellado) a 120 ° C por 10 min con agitación activa. El buque se haya enfriado a 35 ° C después de transcurrido el tiempo de reacción. Información de valores de los parámetros que pueden programarse para otras operaciones unitarias se muestra en el Material suplementario, sección 3. Haga clic aquí para ver una versión más grande de esta figura.
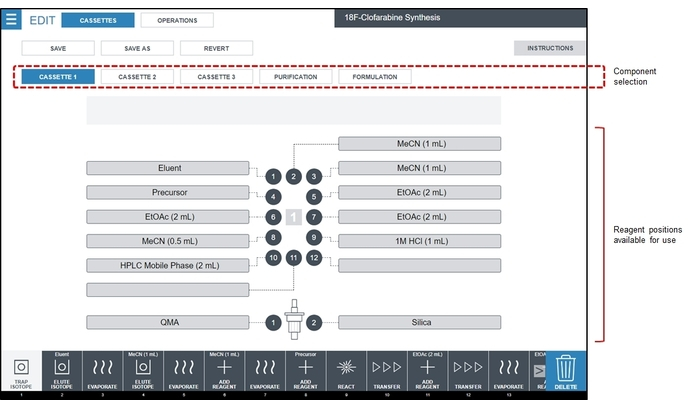
Figura 4: captura de pantalla de la pantalla de configuración de reactivos. Para la secuencia de síntesis CFA [18F], todos los reactivos se cargan en cartucho desechable #1, que se muestra resaltado en el área de selección de componente. Para la síntesis CFA [18F] descrita aquí, eluyente es de 1,0 mg de K2CO3 + 5,0 mg de K222 en 0,4 mL de H2O/0.5 de MeCN, Precursor es de 6 mg de precursor CFA en 0,6 mL de MeCN y Fase móvil de HPLC es 85:15 v acetato de amonio de 25 mM/v: etanol. Haga clic aquí para ver una versión más grande de esta figura.
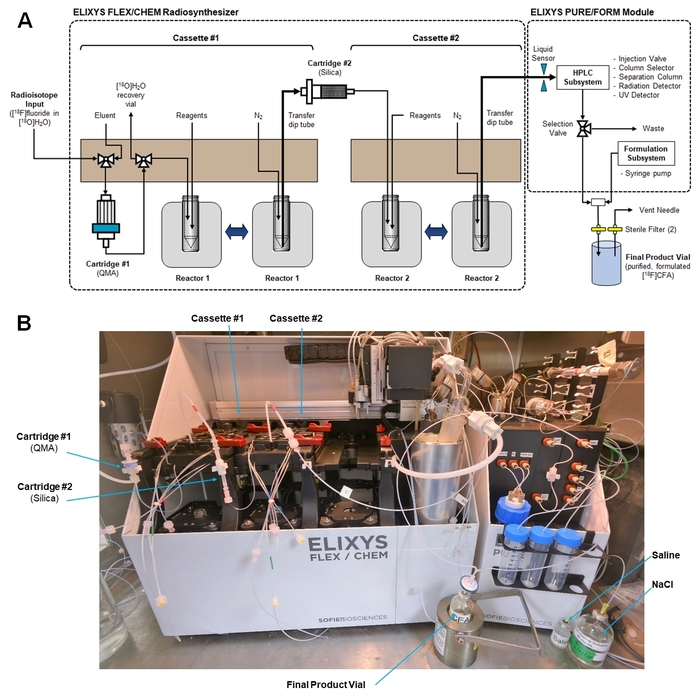
Figura 5: Configuración de Radiosynthesizer para la síntesis de [18F] CFA. (A) este es un esquema que muestra caminos fluidos cassette, las conexiones a los cartuchos y la conexión para transferir producto crudo final del módulo radiosynthesis al módulo de purificación/formulación. (Ambos módulos son controlados con una sola interfaz de computadoras y software). (B) esta es una fotografía de la radiosynthesizer dentro de una celda caliente después de la preparación para la síntesis CFA [18F]. Haga clic aquí para ver una versión más grande de esta figura.
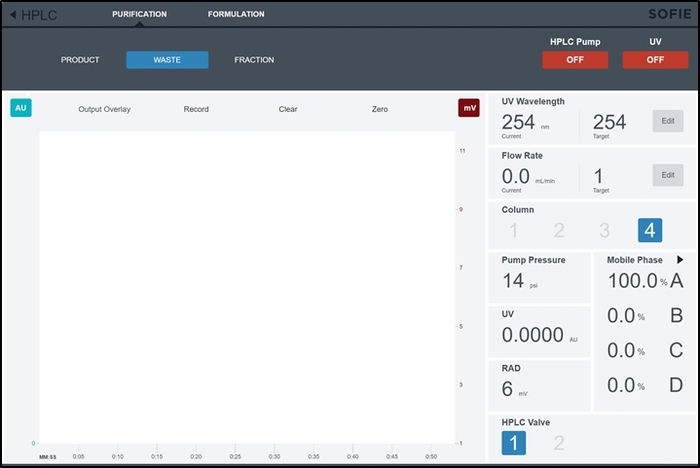
Figura 6: captura de pantalla de la interfaz de control del módulo de purificación/formulación. Esta pantalla es accesible por el operador para controlar manualmente los subsistemas HPLC y formulación durante la configuración de síntesis. Haga clic aquí para ver una versión más grande de esta figura.
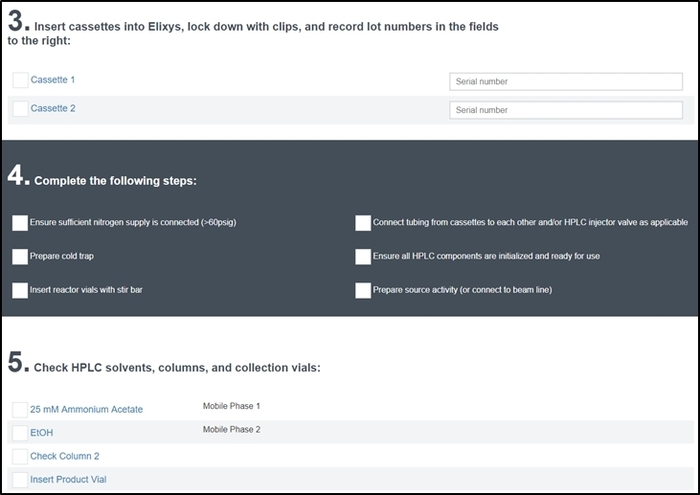
Figura 7: pantalla de lista de verificación pre-ejecución. El operador ingresa el número de serie de los cartuchos instalados en el sistema y debe marcar cada artículo para garantizar el sistema ha sido correctamente configurado y preparado para la síntesis. Además de estas secciones, el operador también se pedirá un nombre y una descripción de la síntesis de funcionan (sección 1) y números para todos los reactivos utilizados (sección 2) y se le pide que Verifique todos los feeds de reactor video están funcionando correctamente (sección 6). Haga clic aquí para ver una versión más grande de esta figura.
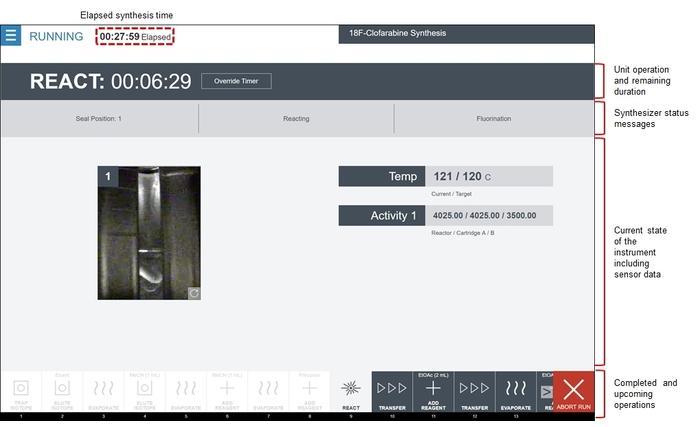
Figura 8: Captura de pantalla del software de radiosynthesizer mientras se ejecuta la secuencia de síntesis CFA [18F]. El software muestra el orden de las operaciones unitarias en la zona de la tira de película. Completadas las operaciones son en gris y resaltadas en blanco, la operación actual se resalta en gris y próximas operaciones se muestran en gris oscuro. La zona centro de la pantalla muestra el estado de la operación de la unidad de activo, incluyendo que subcomando está siendo ejecutado, así como el estado actual del sistema (reactor video feeds y los datos del sensor). Esta particular reacción funcionamiento de la unidad es la reacción de fluoración. En el área de temperatura , la temperatura del reactor se muestra junto a la temperatura deseada (programado). Debajo de este, el área de actividad muestra los valores del sensor de radiación de los tres sensores asociados con el paso de la reacción. Finalmente, un video en el de la izquierda muestra una vista en vivo de la cubeta del reactor. Haga clic aquí para ver una versión más grande de esta figura.
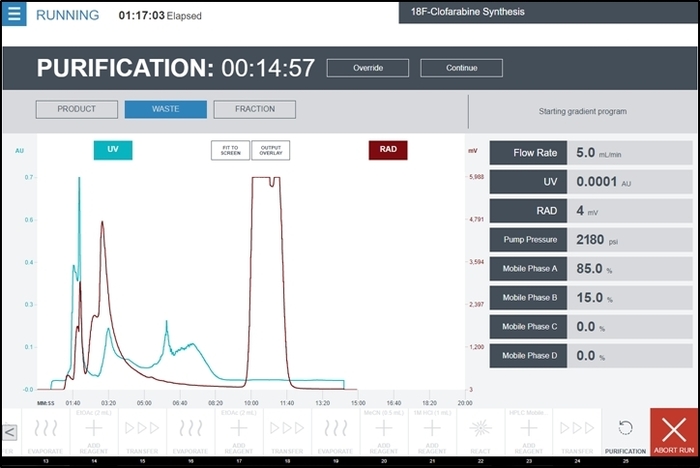
Figura 9: Captura de pantalla de la interfaz de usuario radiosynthesizer mientras se ejecuta la operación de la unidad de purificación durante la síntesis de [18F] CFA. La UV detector y detector de radiación salidas del módulo de purificación/formulación se muestran en el gráfico central en tiempo real. Comentarios adicionales de los detectores y la bomba HPLC se muestran a la derecha de la pantalla. El operador recoge el pico de producto temporalmente seleccionando el producto cuando el pico comienza a aparecer y luego cambiar a residuos después de que se ha visto el pico completo. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Este protocolo define los pasos básicos que deben tomarse al automatizar un protocolo de síntesis manual para lograr la producción de formulación de tracer grado clínico. El ciclo completo de desarrollo, incluyendo el desarrollo de control de calidad, es ejemplificado por la radiosonda [18F] CFA (para la proyección de imagen de la actividad de dCK). Se prestó especial atención a la modificación de la síntesis automatizada para asegurar la idoneidad del tracer para uso clínico. La síntesis implica procesos básicos tales como la activación de fluoruro [18F], radiofluorination de la molécula precursora, purificación cartucho intermedio, grupo de protección de retiro y semi-preparativa HPLC purificación y formulación para la inyección. Estos procesos básicos comprenden un repertorio estándar que es suficiente para la síntesis de la mayoría de marcadores 18PET F-labeled.
Diseño de la síntesis, la elección de los reactivos y su calidad es de particular importancia para el uso clínico. Garantizar la correcta programación y conexiones adecuadas mediante la realización de una síntesis simulacro (sólo disolventes) es imprescindible para eliminar errores inesperados cuando la síntesis se realiza con radiactividad. Las optimizaciones de síntesis posterior (solventes, volúmenes, cantidades, temperaturas, tiempos de reacción y las condiciones de purificación) dependen del trazador PET específico en el desarrollo. Durante estos experimentos, especial atención debe ser brilló en la pureza radioquímica y química del producto final que se logra, como estos deben cumplir con requisitos rigurosos para el uso clínico. Una síntesis que produce confiablemente un producto puro en rendimientos de actividad baja pero suficiente se prefiere normalmente un proceso de alto rendimiento que tiene un riesgo a fallar esporádicamente. Una vez que la síntesis se ha optimizado adecuadamente, el proceso final debe someterse a pruebas de validación (un requisito reglamentario) para asegurar la idoneidad clínica. El método de síntesis validados puede utilizarse entonces para producir el trazador PET para uso clínico. Al sintetizar un trazador PET según un método validado, los procedimientos de operación deben seguirse cuidadosamente. Para garantizar el cumplimiento, el software está programado para que el operador confirme la realización de pasos clave a través de una lista de verificación de la ejecución después de hacer clic en Ejecutar para iniciar la síntesis. Mientras que el sistema realizará la síntesis de una manera automatizada, el paso de purificación requiere intervención manual. El operador debe, por lo tanto, observar de cerca la pantalla cromatográfica durante la etapa de purificación de HPLC y entrada manualmente en tiempo real cuando al arranque y parada de recogida de la fracción producto.
Dentro de nuestros esfuerzos de optimización y automatización para la síntesis CFA [18F], hemos simplificado el método de purificación de HPLC semi-preparativa de la mezcla de producto utilizando un sistema solvente inyectable que consiste en solución de acetato de amonio y EtOH ; nuestro método anterior requiere un paso adicional al intercambio el solvente después de purificación16. Proceso de la formulación subsecuente, por lo tanto, necesidades solamente a reducir el contenido de la fracción recogida permite niveles y asegurar su isotonicity, que se pueden lograr mediante la dilución de EtOH. La etapa de formulación se realizó mediante un segundo programa consistiendo en una sola operación de unidad de formulación para permitir adiciones de volumen variable de soluciones de NaCl a la fracción de producto purificado mediante el módulo de formulación para tener en cuenta la variable volumen obtenido después de la purificación de HPLC. Si el volumen de la fracción de producto recogido se programó para ser constante, en cambio, la operación de la unidad de formulación podría incluirse en el programa principal de la síntesis, evitando la necesidad de un programa independiente. Sería una alternativa para evitar la intervención manual utilizar la funcionalidad completa del módulo de formulación (por ejemplo, diluir el palpador purificado con agua, trampa en un cartucho de extracción en fase sólida C18, lavarlo, eluir con un volumen fijo de EtOH y por último, diluye con un volumen fijo de solución salina).
La técnica presentada aquí para automatización y validación de un protocolo para el uso clínico de síntesis pretende ser bastante general. A través de la opción de radiosynthesizer (ELIXYS), una amplia gama de síntesis puede ser automatizada y validada. Esto incluye la complejas síntesis de 3-pot, o síntesis que implican temperaturas elevadas de solventes volátiles. Optimización de la síntesis se logra cambiando los parámetros del programa. El sintetizador tiene características para monitorear el impacto de los cambios, como la colocación de los recipientes de reacción para la extracción de muestras para el análisis de radio-TLC o HPLC de la radio. Sin embargo, sin modificaciones del sistema, el sistema actualmente no permite el manejo de volúmenes de reactivo muy baja (~ 5-20 μl), destilación del producto intermedio o el manejo de [18F] AlF, 68Ga, u otros radiometals. Si la síntesis manual a automatizarse contiene las medidas y no pueden eludirse, automatización y validación con otra plataforma de radiosynthesizer pueden ser apropiados.
Aunque este trabajo se ha centrado en el desarrollo de un protocolo para la producción automatizada de [18F] CFA para uso clínico, la síntesis de muchos otros trazadores PET podría automatizarse de manera conveniente para la producción clínica, siguiendo la misma lógica y métodos. Siguiendo el método presentado aquí, también hemos adaptado la síntesis automatizada de 9-(4-[18F] fluoro - 3-[hidroximetil] butil) guanina ([18F] FHBG) y validado para uso clínico. Protocolos establecidos por el usuario pueden cargarse y descargaron de la red de sonda de SOFIE, un portal para compartir programas de síntesis y asociados documentación entre diferentes Radiofarmacia sitios27. Esto puede evitar una duplicación de esfuerzos en la comunidad y facilitar estudios clínicos multicéntricos que implican proyección de imagen de PET.
Divulgaciones
Los regentes de la Universidad de California han licenciado la tecnología a SOFIE que fue inventado por Jeffrey Collins y R. Michael van Dam y han tomado acciones en SOFIE como parte de la operación de concesión de licencias. Además, R. Michael van Dam es un fundador y consultor de SOFIE. Los términos de este acuerdo han sido revisados y aprobados por la Universidad de California, Los Ángeles según sus políticas de conflicto de intereses. Eric Schopf y Christopher Drake son empleados y accionistas de SOFIE.
Agradecimientos
Este trabajo ha sido apoyado en parte por el Instituto Nacional del cáncer (R44 CA216539) y la Fundación de la UCLA a una donación realizada por Ralph y Marjorie Crump de la UCLA Crump Institute para la proyección de imagen Molecular.
Materiales
| Name | Company | Catalog Number | Comments |
| ELIXYS FLEX/CHEM | Sofie (Culver City, CA, USA) | 1010001 | Radiosynthesizer |
| Radiosynthesizer cassette | Sofie (Culver City, CA, USA) | 1861030400 | Cassette for ELIXYS FLEX/CHEM |
| ELIXYS PURE/FORM | Sofie (Culver City, CA, USA) | 1510001 | Radiosynthesizer purification module |
| [O-18]H2O | IBA RadioPharma Solutions (Reston, VA, USA) | IBA.SP.065 | >90% isotopic purity |
| [F-18]fluoride in [O-18]H2O | UCLA | N/A | Produced in a cyclotron (RDS-112; Siemens; Knoxville, TN, USA) by the (p,n) reaction of [O-18]H2O. Bombardment at 11 MeV using a 1 mL tantalum target with havar foil. |
| Deionized water | UCLA | N/A | Purified to 18 MΩ and passed through 0.1 µm filter |
| Acetonitrile (MeCN) | Sigma-Aldrich (St. Louis, MO, USA) | 271004 | Anhydrous, 99.8% |
| Ethanol (EtOH) | Decon Laboratories, Inc. (King of Prussia, PA, USA) | 2701 | Anhydrous, 200 proof |
| Sodium hydroxide (NaOH) solution | Merck (Burlington, MA, USA) | 1.09137.1000 | 1M solution |
| Hydrochloric acid (HCl) solution | Fisher Chemical (Hampton, NH, USA) | SA48-500 | 1M solution |
| Ethyl acetate (EtAc) | Fisher Chemical (Hampton, NH, USA) | E195SK-4 | HPLC grade |
| Sodium chloride (NaCl) | Fisher Chemical (Hampton, NH, USA) | S-640-500 | USP grade |
| Ammonium acetate | Fisher Chemical (Hampton, NH, USA) | A639-500 | HPLC grade |
| Potassium carbonate (K2CO3) | Fisher Chemical (Hampton, NH, USA) | P-208-500 | Certified ACS |
| CFA precursor | CalChem Synthesis (San Diego, CA, USA) | N/A | Custom synthesis |
| Cryptand 222 (K222; Kryptofix 2.2.2) | ABX Advanced Biochemical Compounds (Radeberg, Germany) | 800.1000 | >99% |
| Sodium chloride (NaCl) solution (saline) | Hospira (Lake Forest, IL, USA) | 0409-4888-02 | 0.9%, for injection, USP grade |
| Silica cartridge | Waters (Milford, MA, USA) | WAT051900 | Sep-pak Classic |
| Quaternary methylammonium (QMA) cartridge | Waters (Milford, MA, USA) | WAT023525 | Sep-pak Light Plus |
| Sterile syringe filter (0.22 µm) | Millipore Sigma (Burlington, MA, USA) | SLGSV255F | Millex-GV |
| Glass V-vial (5 mL) | Wheaton (Millville, NJ) | W986259NG | Used for reaction vessels |
| Septa | Wheaton (Millville, NJ) | 224100-072 | Used for reagent vials |
| Crimp cap | Wheaton (Millville, NJ) | 224177-01 | Used for reagent vials |
| Amber serum vial (2 mL) | Voigt (Lawrence, KS, USA) | 62413P-2 | Used for reagent vials |
| Magnetic stir bar | Fisher Scientific (Hampton, NH, USA) | 14-513-65 | Used for reaction vessels |
Referencias
- Phelps, M. E. Positron emission tomography provides molecular imaging of biological processes. Proceedings of the National Academy of Sciences. 97 (16), 9226-9233 (2000).
- Kitson, S., Cuccurullo, V., Ciarmiello, A., Salvo, D., Mansi, L. Clinical Applications of Positron Emission Tomography (PET) Imaging in Medicine: Oncology, Brain Diseases and Cardiology. Current Radiopharmaceuticalse. 2 (4), 224-253 (2009).
- Sengupta, D., Pratx, G. Imaging metabolic heterogeneity in cancer. Molecular Cancer. 15, 4 (2016).
- Rabinovich, B. A., Radu, C. G. Imaging Adoptive Cell Transfer Based Cancer Immunotherapy. Current Pharmaceutical Biotechnology. 11 (6), 672-684 (2010).
- Matthews, P. M., Rabiner, E. A., Passchier, J., Gunn, R. N. Positron emission tomography molecular imaging for drug development. British Journal of Clinical Pharmacology. 73 (2), 175-186 (2012).
- Hargreaves, R. The Role of Molecular Imaging in Drug Discovery and Development. Clinical Pharmacology & Therapeutics. 83 (2), 349-353 (2008).
- Keng, P. Y., Esterby, M., van Dam, R. M., Hsieh, C. -. H. Emerging Technologies for Decentralized Production of PET Tracers. Positron Emission Tomography - Current Clinical and Research Aspects. , 153-182 (2012).
- Lazari, M., Irribarren, J., Zhang, S., van Dam, R. M. Understanding temperatures and pressures during short radiochemical reactions. Applied Radiation and Isotopes. , 82-91 (2016).
- Lazari, M., et al. ELIXYS - a fully automated, three-reactor high-pressure radiosynthesizer for development and routine production of diverse PET tracers. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3 (1), 52 (2013).
- Claggett, S. B., Quinn, K., Lazari, M., Esterby, J., Esterby, M., van Dam, R. M. A new paradigm for programming and controlling automated radiosynthesizer. Journal of Nuclear Medicine. 53 (suppl. 1), 1471-1471 (2012).
- Claggett, S. B., Quinn, K. M., Lazari, M., Moore, M. D., van Dam, R. M. Simplified programming and control of automated radiosynthesizers through unit operations. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3, 53 (2013).
- Lazari, M., et al. Fully Automated Production of Diverse 18F-Labeled PET Tracers on the ELIXYS Multireactor Radiosynthesizer Without Hardware Modification. Journal of Nuclear Medicine Technology. 42 (3), 203-210 (2014).
- Lazari, M., et al. Fully-automated synthesis of 16β-18F-fluoro-5α-dihydrotestosterone (FDHT) on the ELIXYS radiosynthesizer. Applied Radiation and Isotopes. 103, 9-14 (2015).
- Collins, J., et al. Production of diverse PET probes with limited resources: 24 18F-labeled compounds prepared with a single radiosynthesizer. Proceedings of the National Academy of Sciences. 114 (43), 11309-11314 (2017).
- Drake, C., et al. Enzymatic Radiofluorination of Biomolecules: Development and Automation of Second Generation Prosthetic on ELIXYS Radiosynthesizer. Journal of Nuclear Medicine. 58 (supplement 1), 1 (2017).
- Gobbi, L. C., et al. Identification of Three Novel Radiotracers for Imaging Aggregated Tau in Alzheimer's Disease with Positron Emission Tomography. Journal of Medicinal Chemistry. 60 (17), 7350-7370 (2017).
- Ippisch, R., Maraglia, B., Sutcliffe, J. Automated production of [18F]-F-Py-peptides. Journal of Nuclear Medicine. 57, 275 (2016).
- Chen, H., et al. AMG 580: A Novel Small Molecule Phosphodiesterase 10A (PDE10A) Positron Emission Tomography Tracer. Journal of Pharmacology and Experimental Therapeutics. 352 (2), 327-337 (2015).
- Waldmann, C. M., et al. An Automated Multidose Synthesis of the Potentiometric PET Probe 4-[18F]Fluorobenzyl-Triphenylphosphonium ([18F]FBnTP). Molecular Imaging and Biology. 20 (2), 205-212 (2018).
- Ravert, H. T., et al. An improved synthesis of the radiolabeled prostate-specific membrane antigen inhibitor, [18F]DCFPyL. Journal of Labelled Compounds and Radiopharmaceuticals. 59 (11), 439-450 (2016).
- Betthauser, T. J., et al. Characterization of the radiosynthesis and purification of [18F]THK-5351, a PET ligand for neurofibrillary tau. Applied Radiation and Isotopes. 130, 230-237 (2017).
- Shu, C. J., et al. Novel PET probes specific for deoxycytidine kinase. Journal of Nuclear Medicine. 51 (7), 1092-1098 (2010).
- Kim, W., et al. [18F]CFA as a clinically translatable probe for PET imaging of deoxycytidine kinase activity. Proceedings of the National Academy of Sciences. 113 (15), 4027-4032 (2016).
- Barrio, M. J., et al. Human Biodistribution and Radiation Dosimetry of 18F-Clofarabine, a PET Probe Targeting the Deoxyribonucleoside Salvage Pathway. Journal of Nuclear Medicine. 58 (3), 374-378 (2017).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados