Method Article
Un ensayo de carga bacteriana molecular de la tuberculosis (TB-MBLA)
En este artículo
Resumen
Describimos una prueba de ensayo de carga bacteriana molecular de tuberculosis realizada después de la inactivación térmica del esputo. La inactivación del calor hace que las muestras de esputo no sean infecciosas y evita la necesidad de laboratorios de nivel 3 de contención para las pruebas moleculares de la tuberculosis.
Resumen
La tuberculosis es causada por Mycobacterium tuberculosis (Mtb), un patógeno clasificado por las Naciones Unidas (ONU) como sustancia biológica peligrosa de categoría B. En aras de la seguridad de los trabajadores, la manipulación de todas las muestras que se supone que llevan Mtb debe llevarse a cabo en un laboratorio de nivel de contención (CL) 3. La prueba de ensayo de carga bacteriana molecular de TB (TB-MBLA) es una prueba de reacción en cadena cuantitativa de la polimerasa de transcriptasa inversa (RT-qPCR) que cuantifica la carga de bacilla de Mtb utilizando imprimaciones y sondas de doble etiqueta para rRNA 16S. Describimos el uso de la inactivación de calor para hacer que las muestras de tuberculosis no sean infecciosas, preservando al mismo tiempo el ARN para el TB-MBLA. Una alícuota de 1 ml de la muestra de esputo en tubos centrífugos de 15 ml hervidos hervidos hervidos hervidos hervidos durante 20 minutos a 80 oC, 85 o C o 95 oC para inactivar los bacilos de Mtb. El cultivo de las muestras de calor inactivado y de control (en vivo) durante 42 días confirmó la muerte de la tuberculosis. La muestra inactivada se pincha con 100 ml del control de extracción y el ARN se extrae siguiendo el procedimiento de aislamiento de ARN estándar. No se observó crecimiento en los cultivos de muestras tratadas térmicamente. El ARN aislado está sujeto a RT-qPCR en tiempo real, que amplifica un objetivo específico en el gen Mtb 16S rRNA, dando resultados en forma de ciclos de cuantificación (Cq). Una curva estándar se utiliza para traducir Cq en carga bacteriana, o unidades formadoras de colonias estimadas por ml (eCFU/mL). Existe una relación inversa entre Cq y la carga bacteriana de una muestra. La limitación es que la inactivación de calor lide algunas células, exponiendo el ARN a los RNases que causan una pérdida de <1 log10eCFU/mL (es decir, <10 CFU/mL). Otros estudios determinarán la proporción de pacientes de muy baja carga que causan resultados falsos negativos debido a la inactivación del calor.
Introducción
Causado por Mycobacterium tuberculosis (Mtb), se registran más de 7 x 106 nuevos casos de tuberculosis (TB) en todo el mundo de los cuales más de 1 x 106 mueren por año1,2. Para invertir la tendencia, la Organización Mundial de la Salud (OMS) puso en marcha un enfoque de tres pilares que incluye el desarrollo de herramientas eficaces de diagnóstico y tratamiento3. Clasificado como una sustancia biológica peligrosa B por las Naciones Unidas, trabajar con muestras presuntamente positivas para Mtb requiere un nivel de contención (CL) de 3. Los laboratorios CL3 son caros de construir y mantener. En consecuencia, la mayoría de los países tienen servicios centralizados de cultura de la tuberculosis a nivel regional o nacional. Esto significa que la microscopía de frotis es la herramienta de diagnóstico más disponible en los centros sanitarios periféricos.
Existe la aprobación de la OMS para implementar pruebas moleculares rápidas como Xpert MTB/RIF en centros de salud de nivel 4, situados principalmente en los nivelesdedistrito4,5. Algunos distritos son bastante grandes y menos accesibles para algunas personas. Aunque es beneficioso, Xpert MTB/RIF funciona detectando el ADN de Mtb. El ADN es una molécula estable que sobrevive mucho después de que las células han muerto y por lo tanto no es un buen estándar para medir células viables críticas para monitorear la respuesta del tratamiento5,6. Los ensayos basados en ARN ofrecen una alternativa para la medición precisa de células viables7,8,9,10,11,12,13. El ARN existe en diferentes especies de estabilidad variable: ARN ribosomal (ARN r), ARN de transferencia (TRNA) y ARN mensajero (ARNm). El ARN mensajero está asociado con la expresión génica y, por lo tanto, el más estrechamente asociado con la actividad celular y la viabilidad14. Es importante tener en cuenta que la ausencia de expresión génica no es equivalente a la muerte celular porque se sabe que los patógenos como Mtb existen en estados inactivos (dormidos) pero viables15,16. Por lo tanto, las especies de ARN estables como el ARR son mejores marcadores de los estados activos e inactivos de las células viables.
Usando Escherichia coli,Sheridan demostró que 16S rRNA aumentó proporcionalmente con el crecimiento bacteriano medido por unidades formadoras de colonias (CFU) cuenta17. Hubo una disminución simultánea en el recuento de UFC y 16S rRNA cuando las bacterias E. coli fueron expuestas a antibióticos. La caída de rRNA después de la muerte celular fue un indicador de que podría ser utilizado como un marcador para la viabilidad celular13,17. A partir de este principio, el ensayo de carga bacteriana molecular de la tuberculosis (TB-MBLA) se desarrolló para apuntar a M. tuberculosis 16S rRNA para medir la carga bacilaria viable de tuberculosis como marcador de respuesta al tratamiento para pacientes en terapia antituberculosa11,18,19. Hemos desarrollado y optimizado aún más el TB-MBLA para incorporar un control de extracción celular que refleja la lisis de M. tuberculosis bacilos y es robusto en diferentes entornos ambientales20. El procedimiento TB-MBLA requiere que los primeros pasos del aislamiento de ARN de Mtb se lleven a cabo en un laboratorio CL3 hasta que las células de Mtb estén completamente lysed para garantizar la seguridad de los trabajadores. También incluye la preservación de muestras para el análisis retrospectivo por lotes que se mantendrá a -80 oC en el tiocianato de guanidina, una sustancia tóxica de nivel 4. Con este fin, hemos utilizado calor para inactivar Mtb y hacer que las muestras sean seguras para TB-MBLA que se realizarán en laboratorios de nivel de microscopía de frotis.
El uso de calor en aplicaciones clínicas y de laboratorio ha existido durante los siglos21,,22. Sin embargo, algunos microorganismos como Mtb son difíciles de matar, y la exposición más corta al calor es insuficiente para matar todas las células23,24. Un estudio reveló que 20 min de calentamiento de cultivos de tuberculosis a 80 oC mataron a todos los bacilos de Mtb sin destruir el ADN necesario para pcR25. Posteriormente, una serie de técnicas de extracción de ADN de laboratorio se calientan actualmente a 95 oC. Hemos aplicado el mismo principio para demostrar que la ebullición de muestras de tuberculosis a 80 oC, 85 o 95 oC inactiva Mtb, preservando al mismo tiempo el ARN suficiente para que se realice TB-MBLA. El cultivo o esputo inactivado se puede mantener en recipientes herméticamente cerrados a temperatura ambiente o refrigerados durante 7 días sin reducir la cantidad de ARNm cuantificable.
La TB-MBLA, que actualmente se utiliza como prueba de uso de investigación (RUO) es adaptable y se ha aplicado a diferentes tipos de muestras, incluyendo esputo, tejido pulmonar y líquido cefalorraquídeo. Todavía no se ha aplicado sobre el líquido alveolar bronquial, la sangre y otros tipos de muestras. Utilizando el esputo como muestra, los resultados de la evaluación multisitio en Africa (datos no publicados) y publicaciones anteriores18,26 muestran que la sensibilidad de MBLA es consistente con el cultivo líquido del tubo indicador de crecimiento de mycobacterium (MGIT). Sin embargo, TB-MBLA es más rápido, dando resultados en horas en lugar de días o semanas de cultivo, específico, no afectado por microorganismos no TB en la muestra, y da una medida cuantitativa de la gravedad de la enfermedad. La OMS ha reconocido recientemente a TB-MBLA como candidato para sustituir la microscopía de frotis y el cultivo para el seguimiento del tratamiento de la tuberculosis2.
En este artículo describimos en detalle la inactivación térmica y el protocolo TB-MBLA publicados en Sabiiti et al.27. Este protocolo detallado proporcionará un recurso visual integral para los usuarios de TB-MBLA en todo el mundo.
Protocolo
1. Preparación de muestras
-
Cultura
- Trabajando en un banco limpio o cabina de clase 1, cosecha 1 ml de alícuotas de fase exponencial Debacillus Calmette-Guérin (BCG) cultivo en tubos de centrífuga de plástico de 15 ml. Cierre bien los tubos.
NOTA: Para procesar una muestra completa de 5 ml, se requieren cinco tubos centrífugos de 15 ml.
ADVERTENCIA: Se requiere un gabinete de bioseguridad cuando se trabaja con cualquier cultivo de tuberculosis.
- Trabajando en un banco limpio o cabina de clase 1, cosecha 1 ml de alícuotas de fase exponencial Debacillus Calmette-Guérin (BCG) cultivo en tubos de centrífuga de plástico de 15 ml. Cierre bien los tubos.
-
Espécimen de esputo del paciente
- Trabajando en un espacio bien ventilado y usando una máscara nasal, abra cuidadosamente la taza de la muestra, pipetee 1 ml alícuotas en tubos centrífugos de plástico de 15 ml y cierre firmemente los tubos.
NOTA: Se recomienda una punta ancha en la boca para pipetear el esputo. Usando un par de tijeras, corta la parte fina de la boca de la punta de 1 ml para crear una boca más ancha.
- Trabajando en un espacio bien ventilado y usando una máscara nasal, abra cuidadosamente la taza de la muestra, pipetee 1 ml alícuotas en tubos centrífugos de plástico de 15 ml y cierre firmemente los tubos.
2. Inactivación de calor
- Antes de la preparación de la muestra, fije el baño de agua a 95 oC.
NOTA: La temperatura de 95 oC aumenta la posibilidad de reducir la actividad de RNase y, por lo tanto, preserva más ARN para TB-MBLA aguas abajo. - Transfiera los tubos de muestra a un estante de retención sumergido en el baño de agua. Asegúrese de que tres cuartas partes de cada tubo de muestra estén sumergidos en el agua.
- Hierva a 95 oC durante 20 minutos y, a continuación, transfiera los tubos al banco para enfriara a temperatura ambiente durante 5 minutos antes de iniciar la extracción de ARN.
NOTA: La inactivación completa del calor de los bacilos de M. tuberculosis y el BCG se verificó incubando muestras y controles inactivados por calor a 37 oC durante 42 días para verificar el crecimiento. Se tomó una medición de densidad óptica a 600 nm(600OD) al inicio y luego semanalmente durante el período de incubación de 42 días.
3. Extracción de ARN
NOTA: El proceso de extracción de ARN descrito aquí es para el kit de ARN enumerado en la Tabla de Materiales. Se pueden utilizar otros kits de extracción de ARN adecuados por diferentes fabricantes.
- Adición de control de extracción (EC)
- Transfiera 1 ml de alícuotas de las muestras inactivadas por calor a tubos de 1,5 ml. Espiga 100 s de la EC en cada muestra, cierre el tubo y mezcle invirtiendo el tubo al revés 3x.
NOTA: La CE se suministra con el kit de bacterias vitales TB-MBLA (Tabla de materiales).
- Transfiera 1 ml de alícuotas de las muestras inactivadas por calor a tubos de 1,5 ml. Espiga 100 s de la EC en cada muestra, cierre el tubo y mezcle invirtiendo el tubo al revés 3x.
- Sedimentación celular
- Con una microcentrífuga de sobremesa, centrifugar los tubos a 20.000 x g durante 10 minutos a temperatura ambiente. Pipetear el sobrenadante, dejando 50 l de sedimento.
- Suspenda el sedimento en 950 ml de tampón de lisis pipeteando hacia arriba y hacia abajo, y transfiera toda la suspensión al tubo de matriz de lising suministrado con el kit de extracción de ARN(Tabla de materiales). Asegúrese de que los tubos estén bien cerrados y etiquete tanto la tapa como el lado del tubo.
- Para la lisis celular, transfiera los tubos del paso 3.2.2 a un homogeneizador. Homogeneizar las muestras durante 40 s a 6.000 rpm.
- Purificación de ácido nucleico
- Centrifugar el lisado del paso 3.3 a 12.000 x g durante 5 min a temperatura ambiente.
- Preparar tubos frescos de 1 ml y añadir 300 ml de cloroformo en cada tubo.
- Usando una punta de 1 ml cuidadosamente pipeta fuera del sobrenadante sin tocar la matriz de lising.
- Transfiera el sobrenadante al cloroformo que contiene tubos y vórtice durante 5 s. Deje que el tubo se asiente durante 5 minutos o más hasta que tres fases (superior, media e inferior) sean claramente visibles.
- Centrífuga a 12.000 x g durante 5 min a temperatura ambiente. Pipetear cuidadosamente la fase superior y transferirla a tubos frescos de 1,5 ml.
- A los tubos del paso 3.4.5, añadir 500 ml de etanol 100% frío en frío, cerrar los tubos y mezclar invirtiendo suavemente al revés 3veces. Incubar los tubos a -80oC durante 15 min o -20oC durante 30 min y continuar la extracción, o dejar a -20oC durante la noche para completar la extracción al día siguiente.
- Poner la microcentrífuga a 4 oC y dejar enfriar a por lo menos 12 oC antes de iniciar la centrifugación. Cargue los tubos en la microcentrífuga y centrífuga durante 20 min a 13.000 x g. Deseche el sobrenadante, sustitúyalo con 70% de etanol helado y centrífuga durante otros 10 minutos a 13.000 x g.
NOTA: El 70% de etanol debe hacerse con agua libre de nucleasas de grado molecular. - Deseche todo el sobrenadante del paso 3.4.7 y transfiera los tubos a una incubadora a 50oC. Incubar durante 20 minutos para secar el pellet de ARN/ADN. Mantenga los tubos parcialmente abiertos para permitir la evaporación de todo el etanol.
- Añadir 100 l de agua libre de nucleasas al pellet seco e incubar durante 5 minutos a temperatura ambiente. Vórtice para 3 s para mezclar el contenido.
NOTA: En esta etapa, el extracto puede almacenarse de 2 a 3 días en el frigorífico o más a -80 oC hasta que se realice la sección 3.5.
- Eliminación de ADN
NOTA: Este paso es crucial porque la presencia de ADN en el extracto invalida el resultado de MBLA. Esta sección se basa en un kit de eliminación de ADN (Tabla de Materiales).- Preparar una mezcla de la enzima DNase I 10x tampón y la enzima DNase I para el número de muestras (10 l de tampón y 1 l de DNase por muestra) más un 10% adicional para cubrir cualquier pérdida de pipeteo. Mezclar por vórtice y luego pipetear 11 l en cada tubo que contenga el extracto de ARN.
- Mezclar por vórtice 3 s y luego girar brevemente (10 s a 13,000 x g) para eliminar cualquier gota en las paredes. Incubar a 37oC durante 30 min en el bloque caliente o incubadora. Añadir 1 l adicional de enzima DNase I directamente en cada tubo, mezclar bien por vórtice e incubar durante 30 minutos más a 37 oC.
- Descongelar el reactivo de inactivación de DNase 10 minutos antes del final de la incubación de DNase. Vortex 20 s para asegurar una suspensión homogénea y lechosa y luego añadir 10 l de reactivo de inactivación dNase en cada extracto de ARN del paso 3.5.2.
- Incubar la mezcla a temperatura ambiente durante 5 min. Vortex 3x durante el paso de incubación de 5 min.
- Centrifugar la mezcla a 13.000 x g durante 2 min. Transfiera cuidadosamente el sobrenadante a tubos libres de RNase de 1,5 ml sin tocar ninguna de las matrices de inactivación.
- Almacene el extracto de ARN en el refrigerador si está ejecutando el RT-qPCR en el mismo día o a -80 oC para su almacenamiento a largo plazo.
4. Reverso Transcriptasa qPCR
- Para muestras desconocidas, diluir todos los extractos de ARN que se utilizarán en una proporción de 1:10 en agua libre de RNase. Mezclar bien por vórtice durante 5 s y girar brevemente hacia abajo para eliminar las gotas o burbujas de aire.
- Para muestras estándar para una curva estándar, tome las normas de ARN Mtb y EC del congelador de -80 oC y descongele a temperatura ambiente. Realice siete y seis diluciones de 10 veces de las muestras estándar de Mtb y EC, respectivamente. Cambie las puntas antes de transferir la mezcla de un tubo a otro.
NOTA: Las muestras estándar se suministran con el kit TB-MBLA. -
Preparación de mezclas maestras
NOTA: Master mix (MM) es una solución de reactivos de PCR suficiente para amplificar todas las muestras, estándares y agua para un control sin plantilla (NTC). El agua utilizada como NTC debe ser la misma agua utilizada en la extracción y para preparar el MM. Asegúrese de que las normas, cada muestra de ARN y su dilución decimal se amplifican 2 veces para la reacción positiva de transcriptasa inversa (RT+) y 1x para la reacción negativa de transcriptasa inversa (RT-). La reacción RT- es un control para determinar la eficiencia de la eliminación de ADN (Tabla 1).- Transfiera 16 ml de MM a cada tubo de reacción PCR.
- Añadir 4 l de extracto de ARN en cada tubo de reacción RT+ y RT- y agua en los tubos de reacción NTC.
- Cargue los tubos de reacción en una máquina de PCR en tiempo real y ajuste las condiciones de PCR de la siguiente manera: 50 oC durante 30 min, 95 oC durante 15 min, ciclos de 40x a 94 oC para 45 s y 60 oC durante 1 min con adquisición con fluoróforos que se absorben en canales verdes y amarillos.
NOTA: El canal verde es el fluoróforo de detección Mtb y el amarillo es el fluoróforo de detección de control de extracción.
-
Interpretación de resultados
NOTA: Asegúrese de que las reacciones duplicadas de la misma muestra no difieran por más de 1 desviación estándar. Los valores Mtb y EC Cq superiores a 30 se consideran negativos. Véanse más detalles de interpretación en el Cuadro 2.- Para interpretar la respuesta al tratamiento, convierta los valores de Cq en carga bacteriana (eCFU/ml) utilizando la curva estándar. Lea la respuesta del tratamiento como el cambio en la carga bacteriana durante el período de seguimiento del tratamiento.
NOTA: La caída de la carga bacteriana después del tratamiento significa una respuesta positiva (es decir, medicamentos antituberculosos que matan a la bacteria de la tuberculosis) mientras que ningún cambio o aumento de la carga bacteriana implica una respuesta negativa, lo que puede significar resistencia de las bacterias de la tuberculosis a los medicamentos antituberculosos o que el paciente no se adhiere adecuadamente a su dosis de tratamiento. La caída de la carga bacteriana medida por TB-MBLA se correlaciona con el aumento del tiempo MGIT a la positividad del cultivo (TTP).
- Para interpretar la respuesta al tratamiento, convierta los valores de Cq en carga bacteriana (eCFU/ml) utilizando la curva estándar. Lea la respuesta del tratamiento como el cambio en la carga bacteriana durante el período de seguimiento del tratamiento.
5. Microscopía electrónica de transmisión
- Transfiera alícuotas de 2 ml de cultivos y controles inactivados por calor en tubos de microcentrífuga de 2 ml. Centrífuga durante 10 min a 20.000 x g.
- Deseche el sobrenadante y suspenda el pellet en 700 ml de tampón de fijación celular e incubar a temperatura ambiente durante 5 minutos para fijar las células.
- Centrifugar la suspensión durante 30 min a 16.000 x g para obtener un pellet duro. Deseche el sobrenadante y sustitúya con un 1% de sacarosa en solución salina con fosfato (PBS). Conservar los gránulos en sacarosa a 4oC hasta la sección para microscopía electrónica.
-
Seccionamiento y TEM
NOTA: El siguiente protocolo está adaptado de Griffiths et al.28.- Cryoprotect el pellet celular incrustándolo en sacarosa de 2,1 M en PBS durante la noche a 4oC. Lavar 3 veces con agua helada.
- Enfríe los gránulos celulares crioprotegidos en nitrógeno líquido y monte los talones de criomicrotomía. Usando el criomicrotome, corte las secciones ultrafinas a 90 nm.
- Recuperar las secciones cortadas utilizando los bucles de alambre de tungsteno de 1:1 mezcla de 2% metilcelulosa y 2.1 M sacarosa en PBS.
- Transfiera las secciones a soportes TEM (rejillas) de cobre hexagonal de 150 mallas recubiertos de pioloformo y almacene a 4 oC o proceda al paso 5.4.5.
- Contraste las rejillas en acetato de ursiel y seca al aire en una película de acetato de metilo. Lavar las rejillas con agua helada seguida de dos gotas de PBS durante 5 min y secar durante 15 a 30 minutos. Examine las secciones bajo TEM siguiendo las directrices del fabricante.
NOTA: Todas las etapas de etiquetado se realizaron a temperatura de hielo (temperatura líquida), excepto las etapas de lavado, que se realizaron a temperatura ambiente.
Resultados
El calor inactiva todos los bacilos de M. tuberculosis
La densidad óptica (OD) de los controles (células vivas) aumentó con el tiempo, (0,04OD–0,85OD)y no se observó ningún cambio de OD en las muestras inactivadas por calor, lo que significa crecimiento y ningún crecimiento respectivamente(Figura 1)27. Del mismo modo, el esputo clínico de control se volvió positivo para el día 3 en MGIT, mientras que las muestras clínicas inactivadas por calor no marcaron positivamente hasta el final de la incubación. El crecimiento de Mtb en MGIT fue confirmado por la microscopía de frotis Ziehl-Neelsen y el antígeno MPT6429.
El ARN en muestras inactivadas es estable a 37 oC durante 4 días
Las muestras inactivadas por calor se incubaron a 37 oC para determinar si el ARN se degrada tras la inactivación del calor de las células. No se encontró diferencia entre el ARN cosechado en el día (D) 0 inmediatamente después de la inactivación del calor y el ARN aislado en D1, 2, 3 y 4 en ambos cultivos BCG(Figura 2A-C)y esputo positivo de tbón(Figura 2D).
La RNase exógena aumenta la tasa de degradación del ARN en las fracciones inactivadas por calor
Para determinar por qué el ARN no se degradaba, la enzima RNase A se añadió exógenamente a 1.000 U/ml antes y/o después de la inactivación del calor. Esto causó una pérdida de ARN equivalente a la carga bacteriana de 1,5 a 0,3 a 0,3 , 1,8 a 0,2 y 1,3 a 0,1 – registrode 10 eCFU/ml a 80 oC, 85 oC y 95 oC respectivamente a lo largo de 4 días de incubación. Hubo una diferencia en el ARN degradado en las muestras donde rnase se añadió antes y/o después de la inactivación del calor(Figura 3A-C).
El ARN suficiente se conserva para TB-MBLA usando 16S rRNA como marcador de referencia
El efecto de la inactivación del calor en el ARR se midió en cultivos BCG y esputo de pacientes con VIH positivo. La carga bacteriana medida del cultivo BCG de control, 5,3 a 0,2 log10 eCFU/ml, fue de 0,2 a 0,1 log10 eCFU/ml superior al log combinado de 5,1 a 0,3oC 10 eCFU/ml de cultivo inactivado por calor (ANOVA p < 0,0001) a 80 oC, 85 oC y 95 oC (figura 47.27 Del mismo modo, la carga bacteriana del esputo del paciente de control, 7,1 log10 eCFU/ml, fue de 0,8 a 0,1 log10 eCFU/ml superior al registro combinado de 6,3 a 0,4110eCFU/ml a 80 oC, 85 oC y 95 oC(figura 4B)27. La reducción de la carga bacteriana fue <1log en los dos tipos de muestras analizadas.
La prueba de comparaciones múltiples de Sidak reveló una diferencia significativa entre la carga bacteriana a 95 oC frente a la de 80 oC y 85 oC (p a 0,001). No se ha encontrado ninguna diferencia en las muestras de tuberculosis a todas las temperaturas, p a 0,8.
La integridad de la pared celular no es destruida por el calor en la mayoría de las células mtb
Usando la microscopía electrónica de transmisión (TEM) investigamos si las células fueron lysed por inactivación de calor. Se hicieron secciones delgadas de pellets fijos de paraformaldehído de células e incrustados en un medio rico en electrones antes del examen por TEM. La inspección de las células con menor y mayor aumento reveló la pared celular intacta y los cuerpos de lípidos intracelulares visibles. Las células morfológicamente parecían alargadas pero no lysed. La Figura 5 ilustra la morfología de las células de mycobacterium en diferentes aumentos. Los dos paneles superiores revelan cuerpos de lípidos intracelulares y el cableado sin tapa, una característica morfológica típica de las especies de micobacterium. Los dos paneles inferiores son un aumento más alto que expande la vista de los cuerpos lipídicos y revela algunas estructuras microintracelulares.
La carga bacteriana medida por TB-MBLA se correlaciona inversamente con el tiempo de cultivo MGIT con la positividad
Para los pacientes que responden al tratamiento, la carga bacteriana cae a un promedio de 1 log10 eCFU/ml por semana durante el transcurso del tratamiento. Los respondedores rápidos se despejan más rápido, convirtiéndose en negativo (carga bacteriana cero) por 2 semanas de tratamiento. La caída de la carga bacteriana medida por TB-MBLA correspondió al aumento del tiempo de cultivo MGIT a la positividad (TTP). La Figura 6 demuestra la correlación inversa encontrada entre la carga bacteriana y el MGIT TTP. La diferencia, sin embargo, es que los resultados tb-MBLA están disponibles en 4 h y el tiempo de resultado es independiente del nivel de carga bacteriana. Esto contrasta con 5-25 días para las pruebas de cultivo MGIT. La contaminación con bacterias no TB compromete aún más los resultados de las pruebas de cultivo.
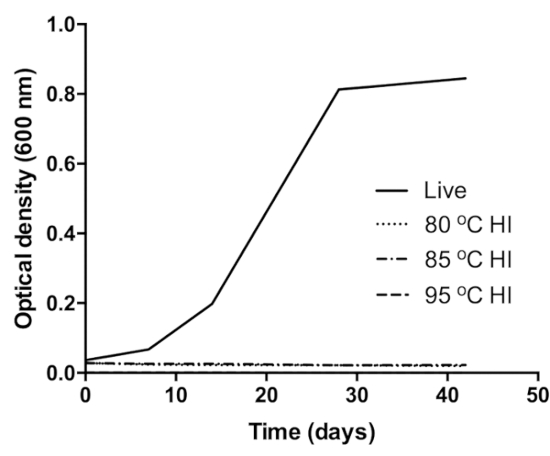
Figura 1: Verificación de la inactivación de BCG a 80 oC (curva de patrón de puntos), 85 oC (curva de patrón de punto-guión) y 95 oC (curva de patrón de guión). El control (curva negra) fue vivo (sin calefacción) cultura BCG inoculada en el mismo medio de crecimiento. El crecimiento del control se confirmó por el aumento de la DO del cultivo durante el período de incubación. Esta cifra fue modificada de Sabiiti et al.27. Haga clic aquí para ver una versión más grande de esta figura.
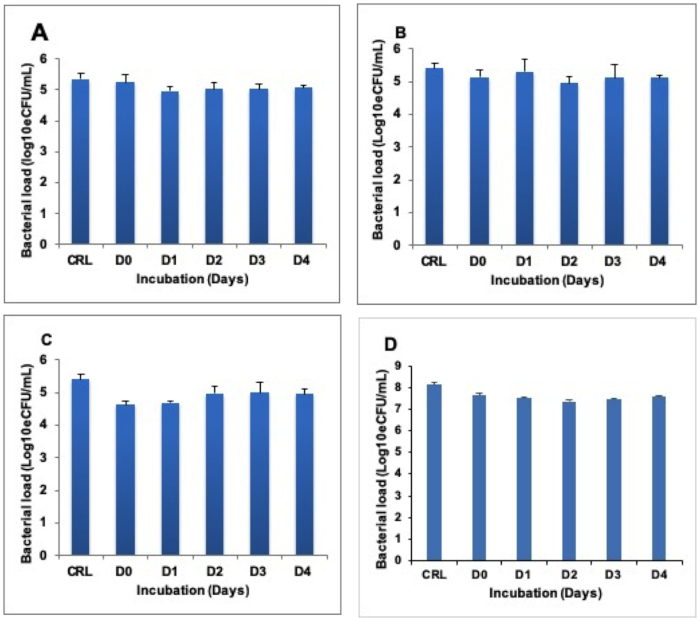
Figura 2: Estabilidad del ARN cuantificable en la muestra inactivada por calor incubada a 37 oC durante 4 días (D0–D4). (A), (B) y (C) muestran cultivos BCG inactivados a 80 oC, 85 oC y 95 oC, respectivamente. (D) muestra el esputo de TB inactivado a 80 oC. El control es la fracción no tratada (en vivo) de la misma muestra. Barras de error: desviación estándar. Tres repeticiones, nueve réplicas por carrera. Haga clic aquí para ver una versión más grande de esta figura.
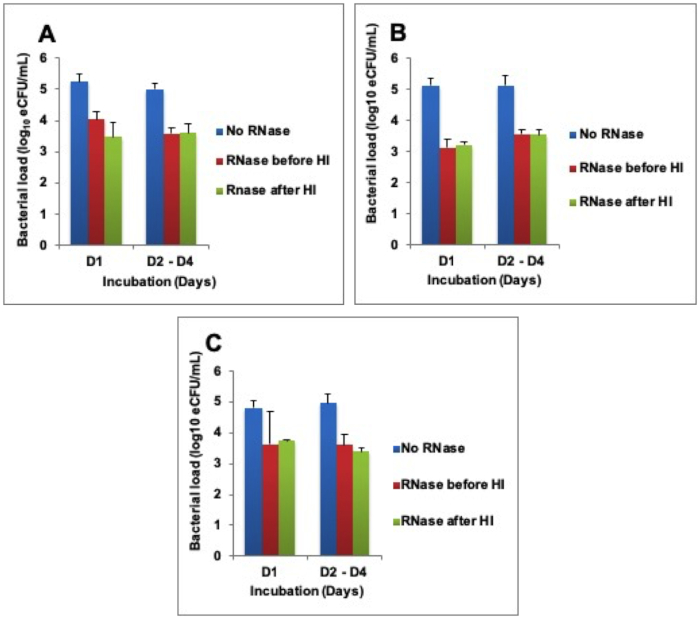
Figura 3: Mayor degradación del ARN después de la adición exógena de la enzima RNase A. (A) Inactivación por calor (HI) a 80oC, (B)HI a 85oC y (C)HI 95oC. Barras de error: error estándar de la media. Haga clic aquí para ver una versión más grande de esta figura.
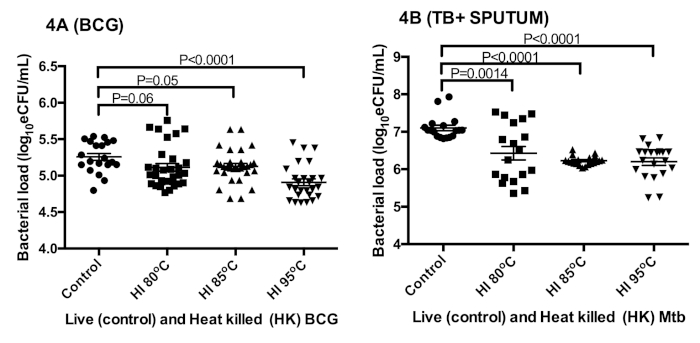
Figura 4: La preservación del ARN suficiente para la medición de la carga bacteriana TB-MBLA utilizando el ARNm 16S como marcador. (A) Carga bacteriana estimada a partir de cultivos BCG in vitro. (B) Carga bacteriana estimada a partir del esputo positivo de tuberculosis. Barras de error: error estándar de la media (n a 18 y 20 réplicas para A y B respectivamente). Esta cifra fue modificada de Sabiiti et al.27. Haga clic aquí para ver una versión más grande de esta figura.
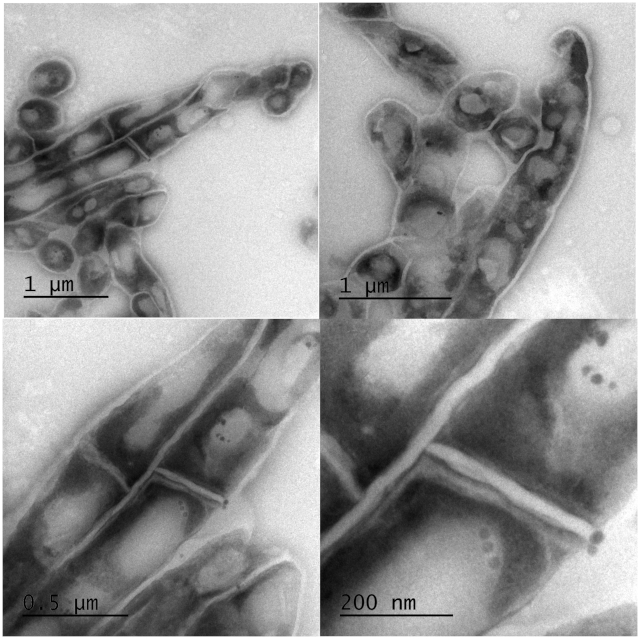
Figura 5: Micrografías electrónicas de bacilos Mtb intactos después de la inactivación a 95 oC durante 20 min. Se observaron paredes celulares intactas claras y cuerpos de lípidos enumerables con TEM. Parte superior: imágenes de bajo aumento de un grupo de células que revelan morfología de cordón de cuerda micobacteriana sin trabas y cuerpos lipídicos intracelulares. Parte inferior: aumento alto de los paneles superiores para ampliar la vista de los cuerpos lipídicos y revelar algunas estructuras microintracelulares. Haga clic aquí para ver una versión más grande de esta figura.
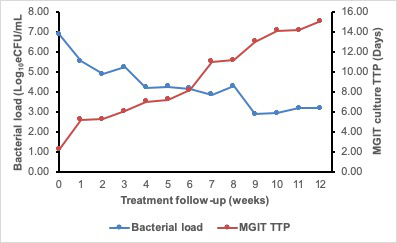
Figura 6: La curva de respuesta del tratamiento de 12 semanas de un paciente en terapia anti-TB que muestra una correlación inversa de la carga bacteriana medida por TB-MBLA y MGIT TTP. La carga bacteriana (curva azul) cae mientras que el TTP sube (curva roja) a medida que el paciente responde al tratamiento. Haga clic aquí para ver una versión más grande de esta figura.
| Mezcla maestra | Reacción positiva de RT | Reacción negativa RT |
| Volumen por reacción x no. de reacciones + 5 | Volumen por reacción x no. de reacciones + 5 | |
| Mezcla cuantitativa | 10,0 l | 10,0 l |
| Mezcla de imprimación Mtb16S (F + R) | 0,4 l | 0,4 l |
| Sonda Mtb16S | 0,2 l | 0,2 l |
| Mezcla de imprimación CE (F + R) | 0,4 l | 0,4 l |
| Sonda EC | 0,2 l | 0,2 l |
| Enzima RT | 0,2 l | ------- |
| Agua libre de RNase | 4,6 l | 4,8 l |
| Volumen total | 16 l | 16 l |
Tabla 1: Guía maestra de preparación de mezclas para el TB-MBLA qPCR.
| Tipo | Canal MTB | Canal EC | Interpretación |
| Muestra | Positivo | Positivo | Válido |
| Muestra | Positivo | Negativo | Indeterminado |
| Muestra | Negativo | Positivo | Válido |
| Muestra | Negativo | Negativo | No válido |
| MTB + Control | Positivo | Negativo | Válido |
| Control de extracción (EC) | Negativo | Positivo | Válido |
| Control del ADN | Negativo | Negativo | Válido |
| Control negativo (NTC) | Negativo | Negativo | Válido |
Tabla 2: Guía de interpretación de resultados TB-MBLA.
Discusión
Este artículo muestra que el tratamiento térmico durante 20 min a 80 oC, 85 oC y 95 oC inactiva eficazmente las muestras de tuberculosis, lo que permite realizar la TB-MBLA en una instalación que no sea DE CL3 sin riesgo de infección para los trabajadores de laboratorio. Los hallazgos confirman observaciones realizadas en estudios anteriores, al tiempo que contrastan con algunas sobre la eficacia de la inactivación térmica de Mtb25,30. Por ejemplo, algunos informes indican que la calefacción a 80 oC no es efectiva en muestras de carga de bacillario alta25,31,32,33. El efecto de inóculo de alta densidad se evitó en nuestro estudio asegurando que todos los cultivos de esputo y puros se calentaran a un volumen de 1 ml por tubo centrífugo de 15 ml que proporciona espacio adecuado para exponer cada parte de la muestra a ebullición27.
La preservación del ARN después de la inactivación del calor permite realizar TB-MBLA. Este hallazgo concuerda con dos estudios que demostraron la preservación del ARN después de la inactivación del calor12,34. Hemos demostrado que el ARN en muestras inactivadas por calor es estable a 37 oC durante 4 días, lo que implica que los laboratorios podrían realizar pruebas por lotes manteniendo muestras inactivadas a temperatura ambiente durante una semana. Mediante la aplicación de kits de extracción de ARN que requieren refrigeración o congelación, la capacidad de mantener muestras inactivadas por calor a temperatura ambiente evita la necesidad de que los laboratorios de cadena de frío y de categoría 3 realicen TB-MBLA en entornos limitados de recursos.
Se perdió menos de 1log de carga bacteriana usando el arnm 16S como marcador. Aunque hubo una diferencia entre la muestra en vivo y la muestra inactivada por calor, la cantidad perdida por la inactivación de calor es demasiado pequeña para comprometer los resultados aguas abajo. El aumento de la temperatura no aumentó la cantidad de ARN perdido, lo que implica que la pérdida observada es independiente del tratamiento térmico. El tratamiento térmico a altas temperaturas probablemente causa lisis celular, exponiendo el ARN a la degradación por RNases. De hecho, la adición exógena de RNase A a la fracción inactivada por calor aumentó la tasa de degradación del ARN. La ebullición no redujo la actividad de rnase, lo que implica que es una proteína muy resistente.
Es importante tener en cuenta que una degradación media del ARN de 1,5 log10 eCFU/mL no es una pérdida grande. Para ello, hipotetizamos que la calefacción aplica una pequeña proporción de bacilos de Mtb, exponiendo así una pequeña cantidad de ARN a RNase. Usando TEM mostramos que la morfología celular de Mtb y la integridad de las paredes celulares apenas se ve afectada por el calentamiento a 95 oC. Esto significa que puede requerir varios factores fisiológicos y el suministro suficiente de RNases como en el huésped para degradar significativamente el ARN35,36. Además, al ser un ribosoma estructural, 16S rRNA es potencialmente menos susceptible a RNase37,38. Una sola célula de Mtb contiene 700 ribosomas/0,1 mm3 de citoplasma37,lo que implica que hay cantidades más altas de ARN RRNA por celda. Por lo tanto, las cantidades más pequeñas de RNase pueden tener un impacto menor38. La existencia de un alto número de ribosomas da una ventaja a TB-MBLA en términos de sensibilidad y capacidad para detectar pacientes con tuberculosis de baja carga.
Hubo una fuerte correlación entre la carga bacteriana medida por TB-MBLA y el cultivo MGIT TTP. Esto confirma la carga bacteriana como el impulsor de la positividad del cultivo hasta cierto punto. Sin embargo, la ventaja de TB-MBLA es que cuantifica directamente la carga de bacillario presente en la muestra y no requiere proliferación de células Mtb antes de la detección. Esto contrasta con el cultivo cuyo tiempo de positividad depende del nivel de carga bacteriana y la tasa de proliferación de células Mtb. Estudios futuros evaluarán el flujo de trabajo TB-MBLA, incluida la inactivación de calor, en entornos clínicos de rutina. El estudio también explorará muestras con una gama de cargas bacterianas para entender el número que podría cambiar de positivo a negativo (es decir, aquellos con menos bacterias después de la inactivación del calor).
El protocolo TB-MBLA para la cuantificación molecular de la carga bacteriana es el primero de su tipo en bacteriología. El método cuantifica directamente la carga de bacillade Mtb del esputo del paciente y no requiere ningún cultivo para hacerlo. Esto lo hace más rápido y aumenta su potencial para informar una decisión clínica sobre el progreso del paciente. El paso de inactivación de calor reduce el riesgo de infección y aumenta la aplicabilidad de TB-MBLA en entornos que no tienen un laboratorio de categoría 3. Después de la inactivación de calor de la muestra, hay tres pasos de protocolo para lograr resultados TB-MBLA: extracción de ARN, transcriptasa inversa (RT)-qPCR y análisis de resultados qPCR.
Cuanto mayor sea la eficiencia del aisleo del ARN Mtb de una muestra de paciente, mayor será la calidad de los resultados. Es importante tener en cuenta que la calidad de la muestra de esputo afecta a la cantidad de ARN aislado. Por ejemplo, el esputo salival se considera de baja calidad y se ha asociado con una baja carga de bacillario. Esto significa que es importante capacitar al paciente para la expectoración de esputo de calidad. Para evaluar la eficiencia del proceso de extracción, se introduce un control de extracción (es decir, el número conocido de células no Mtb) en la muestra antes de la extracción de ARN. La recuperación del control de extracción confirma la eficiencia del proceso de extracción de ARN. El proceso de aislamiento de ARN no puede ser válido a menos que se haya recuperado el control de extracción. Dado el hecho de que Mtb es un organismo resistente hace que la lisis mecánica sea una parte crucial del proceso. La homogeneización de la muestra a alta velocidad (600 rpm) en presencia de cuentas (es decir, matriz de lising) lisa eficazmente las células. La purificación del lisado produce un extracto que contiene ARN y ADN. La eliminación del ADN es un último paso crucial de la extracción del ARN. TB-MBLA tiene como objetivo medir los bacilos viables mediante la cuantificación del ARN. Por lo tanto, la falta de eliminación del ADN genómico significa que los resultados tendrán una señal del ADN, que no es un buen marcador para la viabilidad celular6.
El RT-qPCR es un dúplex que ejecuta sondas etiquetadas duales para Mtb y control de extracción. Se trata de tres pasos: transcripción inversa de 30 minutos por transcriptasa inversa a 50oC, 15 min de desnaturalización a 95oC y 40 ciclos de amplificación a 94oC y 60oC. La adquisición de fluorescencia de las sondas se produce a 60 oC (es decir, la etapa de alargamiento del fragmento). Es importante tener en cuenta que el TB-MBLA se ha optimizado utilizando una máquina qPCR en particular, por lo que los operadores que utilizan otras plataformas qPCR deben optimizar las condiciones de sus equipos. La eficiencia de la eliminación de ADN se controla mediante la ejecución de una sola reacción por muestra en ausencia de RT. Un resultado positivo de esta reacción significa la eliminación incompleta del ADN. Las muestras de alta carga que tienen grandes cantidades de ADN pueden requerir el doble de la cantidad de enzima DNase para eliminar completamente el ADN. Afortunadamente, en muestras de alta carga de bacillario, la presencia de pequeñas cantidades de ADN es menos probable que afecte el resultado del ARN. El ARN ribosomal, el objetivo TB-MBLA, ocurre naturalmente en el doble de la cantidad de ADN37. En el PCR, un control sin plantilla (NTC), que es el agua utilizada para disolver los reactivos de PCR, controles para la contaminación cruzada con ADN exógeno o ARN. Una señal positiva en el NTC implica contaminación cruzada y el resultado se considera inválido. Esto significa que todas las soluciones constituidas con esta agua tienen que ser desechadas y las nuevas se hacen con un vial de agua fresca. Es aconsejable mantener el agua de PCR en alícuotas separadas para evitar la contaminación de toda el agua. Un control positivo (ARN Mtb) se utiliza para controlar la eficiencia general de la PCR.
El análisis de resultados implica la conversión de PCR Cqs en carga bacteriana (es decir, las unidades formadoras de colonias estimadas por ml) utilizando la curva estándar. Establecer y optimizar la curva estándar es crucial para este paso. Se recomienda una eficiencia de curva estándar de 0,95–1. Las curvas estándar para MTb y el control de extracción deben configurarse y optimizarse antes de que los pacientes u otras muestras de prueba se ejecuten en la máquina. Las muestras estándar se proporcionan con el kit TB-MBLA. Se recomienda una dilución de diez veces el extracto de ARN para PCR. Esto implica que el resultado de la carga bacteriana tiene que multiplicarse por un factor de 10 para obtener el resultado final de la carga bacteriana por ml. Es importante tener en cuenta que los Cqs por encima de 30 se consideran negativos para TB-MBLA. Se requiere un mínimo de dos posibles resultados de carga bacteriana medidos en diferentes puntos de tiempo para hacer una inferencia sobre la respuesta al tratamiento. Se recomienda encarecidamente que uno de los dos resultados sea basal, antes del inicio del tratamiento. Sin embargo, si la evaluación de la carga bacteriana iniciada por el paciente se produce a mitad del tratamiento, debe haber una medida de carga bacteriana de segundo punto de tiempo para evaluar la respuesta al tratamiento. TB-MBLA puede distinguir la carga bacteriana en un espacio de 3 días en el tratamiento, pero lo ideal son dos mediciones de carga bacteriana tomadas con 7 días de diferencia.
Si bien el protocolo genera resultados cuantitativos informativos para la respuesta al tratamiento, sigue siendo en gran medida manual y exige un tiempo considerable para la extracción de ARN. Es posible que los técnicos de los laboratorios ocupados no tengan este tiempo. Se están llevando a la organización de acuerdos para automatizar los procesos de extracción de ARN y PCR.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
El estudio fue posible gracias a la financiación de la Asociación Europea y de Países en Desarrollo de Ensayos Clínicos (EDCTP) – Subvención SP.2011.41304.008 del Programa Panafricano de Expansión de Biomarcadores (PanBIOME). También se obtuvo el apoyo de la universidad de St Andrews Escuela de Medicina beca de investigación. La publicación de este manuscrito y el protocolo TB-MBLA como recurso visual ha sido posible gracias a la financiación del Consejo De Financiación Escocés y del Fondo de Investigación de Desafíos Globales a la Universidad de St Andrews. Gracias al hospital materno de Maputo y al Centro de Salud de Mavalane, que proporcionó los especímenes clínicos de esputo, y al equipo de la Unidad de Tratamiento de la Tuberculosis de Maputo que ayudó con los experimentos de inactivación del calor de las muestras de esputo clínico.
Materiales
| Name | Company | Catalog Number | Comments |
| Heat inactivation: | |||
| 15 mL Centrifuge tubes | Fisher-Scientific | 10136120 | 50 mL tubes may be used if larger sample volumes are involved |
| 15 mL Wire Tube rack | Fisher-Scientific | 11749128 | Other brands with similar make can be used |
| Water bath | Fisher-Scientific | 15700619 | Other brands with similar make can be used |
| RNA extraction: | |||
| Chloroform | Sigma | 372978-1L | Not necessary in other RNA extraction kit brands |
| Ethanol, absolute 99-100% | Sigma | 51976-500ML-F | Larger volume available |
| Extraction control | SOI group St Andrews | VitalbacteriaEC | Supplied with the TB-MBLA Vitalbacteria kit |
| FASTRNA Pro blue Kit | MP Biomedicals | 116025050 | Supplied with lysing matrix tubes |
| Molecular grade water (RNase free) | Sigma | W4502-1L | Qiagen, Fisherscientific can also supply same product |
| Precellys 24 homogeniser | VWR | 432-3750 | FastPrep MP Biomedicals can be used too |
| Refrigerated micro-centrifuge, Fresco 21, Heraeus | Fisher-Scientific | 15352117 | Other brands with similar capacity can be used |
| Thermomixer | Eppendorf | BLD-455-010C | Works with 1-2 mL tubes |
| TURBO DNA-free | Fisher-Scientific | AM1907M | Takes longer but more effective than shorter DNA removal procedures. |
| RT-qPCR: | |||
| Primers and Taqman probes | SOI group St Andrews | VitalbacteriaPP | Supplied with the TB-MBLA Vitalbacteria kit. Probe fluorophores are FAM (green) for Mtb and HEX (yellow) for Extraction control (EC). Applied Biosystems qPCR platforms use VIC instead of HEX. |
| QuantiTect Multiplex RT-PCR NR Kit | Qiagen | 204845 | PCR mix plus the RT enzyme |
| RotorGene Q 5plex machine | Qiagen | 9001580 | Other qPCR machines: Vii7, Quantistudio, Steponelus etc. can be used |
| Strip Tubes and Caps, 0.1 mL | Qiagen | 981103 | Other tube sizes available depending on the rotor size. For other PCR platforms 96 well PCR plates are needed. |
| Non-heat inactivation Sample preservation materials | |||
| 1 M Tris-HCl pH 7.5 | Sigma | 93313 | Supplied ready to use |
| 2-Mercaptoethanol | Sigma | 63689 | Many competent suppliers |
| Guanidine thiocyanate (GTC) | Promega | V2791 | Promega brand recommended for quality |
| Molecular grade water (RNase free) | Sigma | W4502-1L | Ensures that GTC solution is free of nucleases |
| General materials (used but not specific to TB-MBLA) | |||
| 500 mL plastic containers | 734-5087 | Nalgene brand recommeded | |
| Biological waste discard jars | Many competent suppliers | ||
| Chemical waste discard jars | Many competent suppliers | ||
| Disposable gloves, chemical resistant | Many competent suppliers | ||
| Freezer (-20 °C) | Many competent suppliers | ||
| Freezer (-80 °C) | Many competent suppliers | ||
| Fridge (0-8 °C) | Many competent suppliers | ||
| Fume hood | For safe handling of toxic reagents | ||
| Laboratory scales | For accurate measurement of reagents | ||
| Measuring cylinders, plastic | To ensure accurate measurement of reagents | ||
| PCR reaction tubes | Should be suitable to the PCR instrument used | ||
| Pipettes and matching sterile filtered pipette tips, | DNAse and RNAse-free, range: P1000, P200, P10, P2 recommended | ||
| Qiagility loading plates | Qiagen | 5-well master mix plate, 16-well reagent plate, 32-well sample plate, 72-well and 96-well reaction plates | |
| QIAgility Pipetting Robot | Qiagen | Important for high throughput pipetting | |
| Racks for 1.5 mL and 2 mL microtubes and for 15 mL and 50 mL Falcon tubes | Chemical-resistant and autoclavable recommended | ||
| RNase Away (Removes RNases enzymes from working space) | Fisher Scientific | 10666421 | Important to ensure services and devices are free from RNase enzyme |
| Safety goggles, chemical resistant | Fisher Scientific | Can also be got from Sigma. Protect eyes from toxic reagents. | |
| Sterile Pasteur pipettes, 1.5-3 mL | Many competent suppliers | ||
| Sterile RNAse-free microtubes | 1.5 mL tubes suitable for freezing at -80 °C recommended | ||
| TB disinfectant, e.g. Tristel Fuse | Ensure it is freshly prepared or prepared within a week | ||
| Vortex | Genie 2 brand recommended | ||
| Transmission electron microscopy | |||
| Glutaldehyde (8%) | Sigma | G7526-10ML | Part of the Cell fixation buffer (HEPES buffer) |
| HEPES (pH 7.4, 100 mM) | Sigma | H4034-25G | Part of the Cell fixation buffer (HEPES buffer) |
| Leica FCS ultracryo | Leica | Cryomicrotome for tissue sectioning | |
| Methyl cellulose | Agar Scientific | AGG6425 | Cold mounting resin |
| Paraformaldehyde (4% in PBS) | Sigma | P6148-500G | Part of the Cell fixation buffer (HEPES buffer) |
| Sucrose | Sigma | 84097-250G | Preservation and mounting medium |
| Uranyl acetate | Agar Scientific | AGR1260A | Universal Electron microscopy stain |
Referencias
- World Health Organization. END TB Global Tuberculosis Report 2017. World Health Organization. , (2017).
- World Health Organization. Global tuberculosis report 2018. World Health Organization. , (2018).
- World Health Organization. TB Elimination in Low-Incidence Countries. World Health Organization. , (2014).
- Boehme, C. C., et al. diagnostic accuracy, and effectiveness of decentralised use of the Xpert MTB/RIF test for diagnosis of tuberculosis and multidrug resistance: a multicentre implementation study. The Lancet. 377, 1495-1505 (2011).
- World Health Organization. Xpert MTB/RIF assay for the diagnosis of pulmonary and extrapulmonary TB in adults and children. World Health Organization. , (2010).
- Friedrich, S. O., et al. Assessment of the sensitivity and specificity of Xpert MTB/RIF assay as an early sputum biomarker of response to tuberculosis treatment. The Lancet Respiratory Medicine. 1, 462-470 (2013).
- Desjardin, L. E., et al. Measurement of Sputum Mycobacterium tuberculosis Messenger RNA as a Surrogate for Response to Chemotherapy. American Journal of Respiratory Critical Care Medicine. 160, 203-210 (1999).
- Hellyer, T. J., et al. Detection of Viable Mycobacterium tuberculosis by Reverse Transcriptase-Strand Displacement Amplification of mRNA. Journal of Clinical Microbiology. 37, 518-523 (1999).
- Honeyborne, I., et al. Molecular Bacterial Load Assay , a Culture-Free Biomarker for Rapid and Accurate Quantification of Sputum Mycobacterium tuberculosis Bacillary Load during Treatment. Journal of Clinical Microbiology. 49, 3905-3911 (2011).
- Li, L., et al. Sputum Mycobacterium tuberculosis mRNA as a Marker of Bacteriologic Clearance in Response to Antituberculosis Therapy. Journal of Clinical Microbiology. 48, 46-51 (2010).
- Honeyborne, I., et al. The Molecular Bacterial Load Assay Replaces Solid Culture for Measuring Early Bactericidal Response to Antituberculosis Treatment. Journal of Clinical Microbiology. 52, 3064-3067 (2014).
- Hellyer, T. J., Jardin, L. E. D. E. S., Hehman, G. L., Cave, M. D. Quantitative Analysis of mRNA as a Marker for Viability of Mycobacterium tuberculosis. Journal of Clinical Microbiology. 37, 290-295 (1999).
- Aellen, S., Que, Y., Guignard, B., Haenni, M., Moreillon, P. Detection of Live and Antibiotic-Killed Bacteria by Quantitative Real-Time PCR of Specific Fragments of rRNA. Antimicrobial agents chemotherapy. 50, 1913-1920 (2006).
- Deutscher, M. P. Degradation of RNA in bacteria: Comparison of mRNA and stable RNA. Nucleic Acids Research. 34, 659-666 (2006).
- Gupta, R. K., Srivastava, R. Resuscitation Promoting Factors: A Family of Microbial Proteins in Survival and Resuscitation of Dormant Mycobacteria. Indian Journal of Microbiology. 52, 114-121 (2012).
- Mukamolova, G. V., Turapov, O., Malkin, J., Woltmann, G., Barer, M. R. Resuscitation-promoting factors reveal an occult population of tubercle bacilli in sputum. American Journal of Respiratory Critical Care Medicine. 181, 174-180 (2010).
- Sheridan, G. E. C., Masters, C. I., Shallcross, J. A., Mackey, B. M. Detection of mRNA by Reverse Transcription-PCR as an Indicator of Viability in Escherichia coliCells Detection of mRNA by Reverse Transcription-PCR as an Indicator of Viability in Escherichia coli Cells. Applied Environment Microbiology. 64, 1313-1318 (1998).
- Honeyborne, I., et al. Molecular bacterial load assay, a culture-free biomarker for rapid and accurate quantification of sputum Mycobacterium tuberculosis bacillary load during treatment. Journal of Clinical Microbiology. 49, 3905-3911 (2011).
- Sabiiti, W., et al. Molecular Bacterial Load Assay: a Fast and Accurate Means for Monitoring Tuberculosis Treatment Response. BMJ Global Health. 2, 1-8 (2017).
- Gillespie, H., Stephen, S. W., Oravcova, K., Bishop, A. K. Mybacterial Load Assay. Diagnostic Bacteriology. Methods and Protocols. , 89-105 (2017).
- Juffs, H., Deeth, H. Scientific Evaluation of Pasteurisation for Pathogen Reduction in Milk and Milk Products. Food Standards Australia New Zealand. , (2007).
- Holmes, C. J., Degremont, A., Kubey, W. Effectiveness of Various Chemical Disinfectants versus Cleaning Combined with Heat Disinfection on Pseudomonas Biofi lm. Blood Purification. 22, 461-468 (2004).
- Chedore, P., et al. Method for inactivating and fixing unstained smear preparations of Mycobacterium tuberculosis for improved laboratory safety. Journal of Clinical Microbiology. 40, 4077-4080 (2002).
- Cardoso, C. L., et al. Survival of Tubercle Bacilli in Heat-fixed and Stained Sputum Smears. Memórias do Instituto Oswaldo Cruz. 96, 277-280 (2001).
- Doig, C., Seagar, A. L., Watt, B., Forbes, K. J. The efficacy of the heat killing of Mycobacterium tuberculosis. Journal of Clinical Pathology. 55, 778-779 (2002).
- Honeyborne, I., et al. The molecular bacterial load assay replaces solid culture for measuring early bactericidal response to antituberculosis treatment. Journal of Clinical Microbiology. 52, 3064-3067 (2014).
- Sabiiti, W., et al. Heat Inactivation Renders Sputum Safe and Preserves Mycobacterium tuberculosis RNA for Downstream Molecular tests. Journal of Clinical Microbiology. , 1-8 (2019).
- Griffiths, G., McDowall, A., Back, R., Dubochet, J. On the preparation of cryosections for immunocytochemistry. Journal of Ultrasructure Research. 89, 65-78 (1984).
- Kumar, V. G., Urs, T. A., Ranganath, R. R. MPT 64 Antigen detection for Rapid confirmation of M. tuberculosis isolates. BMC Research Notes. 4, 79 (2011).
- Zwadyk, P., Down, J. A., Myers, N., Dey, M. S. Rendering of mycobacteria safe for molecular diagnostic studies and development of a lysis method for strand displacement amplification and PCR. Journal of Clinical Microbiology. 32, 2140-2146 (1994).
- Blackwood, K. S., et al. Viability testing of material derived from Mycobacterium tuberculosis prior to removal from a Containment Level-III Laboratory as part of a Laboratory Risk Assessment Program. BMC Infectious Diseases. 5, 3-9 (2005).
- Somerville, W., Thibert, L., Schwartzman, K., Behr, M. A. Extraction of Mycobacterium tuberculosis DNA: a Question of Contaiment. Journal of Clinical Microbiology. 43, 2996-2997 (2005).
- Bemer-Melchior, P., Drugeon, H. B. Inactivation of Mycobacterium tuberculosis for DNA typing analysis. Journal of Clinical Microbiology. 37, 2350-2351 (1999).
- McKillip, J. L., Jaykus, L. A., Drake, M. rRNA stability in heat killed and UV-irradiated enterotoxigenic Staphylococcus aureus and Escherichia coli O157:H7. Journal of Appied Environmental Microbiology. 64, 4264-4268 (1998).
- Blank, A., Dekker, C. A. Ribonucleases of Human Serum, Urine, Cerebrospinal Fluid, and Leukocytes. Activity Staining following Electrophoresis in Sodium Dodecyl Sulfate-Polyacrylamide Gels. Biochemistry. 20, 2261-2267 (1981).
- O'Leary, T. J. Reducing the impact of endogenous ribonucleases on reverse transcription-PCR assay systems. Clinical Chemistry. 45, 449-450 (1999).
- Yamada, H., Yamaguchi, M., Chikamatsu, K., Aono, A., Mitarai, S. Structome analysis of virulent Mycobacterium tuberculosis, which survives with only 700 ribosomes per 0.1 fl of cytoplasm. PLoS One. 10, 1-14 (2015).
- Yang, K., et al. Structural insights into species-specific features of the ribosome from the human pathogen Mycobacterium tuberculosis. Nucleic Acids Research. 45, 10884-10894 (2017).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados