Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
RGBradford: Cuantificación de proteínas con la cámara de un teléfono inteligente
En este artículo
Resumen
Este artículo proporciona un protocolo para la cuantificación de proteínas utilizando el ensayo Bradford y un teléfono inteligente como dispositivo analítico. Los niveles de proteínas en las muestras se pueden cuantificar utilizando datos de color extraídos de una imagen de una microplaca tomada con un teléfono inteligente.
Resumen
La cuantificación de proteínas es un procedimiento esencial en la investigación en ciencias de la vida. Entre otros métodos, el ensayo de Bradford es uno de los más utilizados. Debido a su amplia difusión, se han informado exhaustivamente las limitaciones y ventajas del ensayo de Bradford, incluyendo varias modificaciones del método original para mejorar su rendimiento. Una de las alteraciones del método original es el uso de la cámara de un teléfono inteligente como instrumento analítico. Aprovechando las tres formas del colorante Coomassie Brilliant Blue que existen en las condiciones del ensayo de Bradford, este artículo describe cómo cuantificar con precisión la proteína en muestras utilizando datos de color extraídos de una sola imagen de una microplaca. Después de realizar el ensayo en una microplaca, se toma una imagen con la cámara de un teléfono inteligente y se extraen datos de color RGB de la imagen utilizando una aplicación de software de análisis de imágenes gratuita y de código abierto. A continuación, se utiliza la relación entre la intensidad azul y verde (en la escala RGB) de muestras con concentraciones desconocidas de proteína para calcular el contenido de proteína en función de una curva estándar. No se observan diferencias significativas entre los valores calculados utilizando datos de color RGB y los calculados utilizando datos de absorbancia convencionales.
Introducción
Independientemente del uso posterior (por ejemplo, ELISA, cinética enzimática, Western blot, purificación de proteínas y espectrometría de masas), la cuantificación de proteínas es crucial para un análisis preciso en los laboratorios de ciencias de la vida. Además de su uso como lecturas secundarias (es decir, para calcular los niveles relativos de analitos por masa de proteína), los niveles de proteína en una muestra también pueden ser el resultado deseado en sí mismo. Por ejemplo, uno puede estar interesado en los niveles de proteínas en los recursos alimenticios1 o en la orina2. Hay muchos métodos disponibles para medir la concentración de proteínas en las muestras3, incluidas las lecturas directas de absorbancia UV4, la quelación proteína-cobre 5,6, los ensayos colorimétricos de unión proteína-colorante7 y los ensayos fluorescentes de unión proteína-colorante8. La relevancia de la cuantificación de proteínas se evidencia por la presencia de dos artículos que describen métodos de medición de proteínas 5,7 en el top-3 de la literatura más citada 9,10. A pesar del hecho de que muchos autores descuidan su cita real citando referencias no primarias o no citando nada en absoluto, los artículos originales que describen el ensayo de proteína de Lowry y el ensayo de proteína de Bradford suman >200,000 citas cada10.
La popularidad del ensayo Bradford se debe a su asequibilidad, simplicidad, velocidad y sensibilidad. El ensayo se basa en la interacción entre las proteínas y el colorante Coomassie Brilliant Blue G en condiciones ácidas. En las condiciones del ensayo (es decir, pH bajo), el colorante existe en tres formas: una forma catiónica roja con λmax a 470 nm; una forma neutra verde con λmax a 650 nm; y una forma aniónica azul con λmax a 590 nm11,12 (Figura 1). La forma catiónica predomina en ausencia de proteínas. A medida que las proteínas interactúan con el colorante, estabilizan la forma aniónica azul, lo que provoca un cambio notable en el color de la solución, de marrón a azul. Por lo general, el cambio en la concentración de la forma azul del colorante se cuantifica espectrofotométricamente, cuya absorbancia a 590-595 nm es proporcional a la cantidad de proteína en el ensayo.
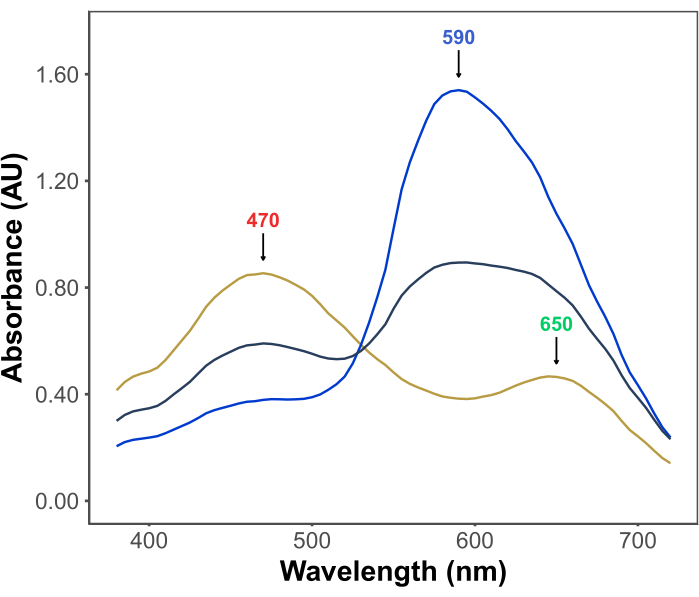
Figura 1: Espectros de absorción G azul brillante de Coomassie bajo las condiciones del ensayo Bradford. Los tres picos principales están marcados con flechas que indican el λmax de las formas roja (470 nm), verde (650 nm) y azul (590 nm) del tinte. Los espectros se registraron en ausencia de proteína (línea amarilla) y en presencia de 3 μg (línea gris) y 10 μg (línea azul) de albúmina sérica bovina. Haga clic aquí para ver una versión más grande de esta figura.
El uso generalizado del ensayo de Bradford ha llevado a la identificación de varias limitaciones (p. ej., respuestas variables a diferentes proteínas11 e interferencia de lípidos13 y detergentes7) y al desarrollo de modificaciones para mejorar su rendimiento (p. ej., la adición de detergentes 14,15, alcalinización14,16 y el uso de la relación de absorbancias17). Además de las modificaciones en el propio ensayo, también se ha descrito el uso de dispositivos alternativos, como teléfonos inteligentes o cámaras, para capturar señales analíticas 18,19,20. De hecho, el desarrollo de métodos que hacen uso de teléfonos inteligentes como analizadores químicos portátiles ha sido un área activa de investigación. La motivación para el uso de teléfonos inteligentes se deriva de la asequibilidad, portabilidad, facilidad de uso y amplia disponibilidad de estos dispositivos.
Este artículo proporciona un protocolo para la cuantificación de proteínas utilizando el ensayo RGBradford20, que utiliza un teléfono inteligente como dispositivo analítico. A diferencia de la publicación original de RGBradford20, aquí se ha introducido un procedimiento que agiliza el proceso de extracción de color. Implica la utilización de una aplicación de software disponible gratuitamente para extraer automáticamente la información de color de cada pocillo de una imagen de microplaca, lo que ahorra mucho tiempo y esfuerzo. Esta es una alternativa al método anterior de adquirir manualmente los datos de color de cada pocillo uno por uno utilizando una aplicación de software de edición de gráficos20. En última instancia, los niveles de proteínas en las muestras se pueden cuantificar utilizando datos de color extraídos de una imagen de una microplaca tomada con un teléfono inteligente.
Protocolo
1. Preparación del reactivo de ensayo de proteínas Bradford
- Disolver 100 mg de Coomassie Brilliant Blue G en 50 ml de etanol al 95% (p/v). Mezclar hasta que Coomassie Brilliant Blue G se disuelva por completo.
PRECAUCIÓN: El etanol es inflamable y causa irritación en los ojos. Evite las llamas y use gafas. - A la solución anterior, agregue 100 ml de ácido fosfórico al 85% (p/v) con cuidado.
PRECAUCIÓN: El ácido fosfórico es corrosivo para los metales y causa corrosión en la piel, daños oculares graves y toxicidad oral aguda. Use guantes y gafas. - Agregue lentamente la solución que contiene Coomassie Brilliant Blue G, etanol y ácido fosfórico a 600 ml de agua desionizada.
- Diluir la solución hasta un volumen final de 1.000 ml. Escale hacia arriba o hacia abajo según el número de muestras a analizar. Como se describe en el método original7, las concentraciones finales en el reactivo Bradford de trabajo deben ser 0,01% (p/v) de azul brillante Coomassie G, 4,7% (p/v) de etanol y 8,5% (p/v) de ácido fosfórico.
- Elimine cualquier material insoluble que se filtre a través del papel de filtro (papel Whatman # 1 o equivalente).
- El reactivo es estable durante varias semanas cuando se almacena a temperatura ambiente (RT) y se protege de la luz. Filtre según sea necesario, ya que pueden formarse precipitados con el tiempo.
NOTA: Alternativamente, los reactivos Bradford listos para diluir y usar están disponibles comercialmente. Siga las instrucciones del fabricante para preparar el reactivo y continúe con el siguiente paso.
2. Preparación de soluciones estándar de proteínas
- Preparar una solución madre (véase el paso 2.4) de una proteína aislada para utilizarla como estándar. Una proteína asequible y de uso común es la albúmina sérica bovina (BSA). Otras opciones son la ovoalbúmina y la gammaglobulina bovina.
- Si se conoce la absorción molar de la proteína utilizada como patrón, comprobar la concentración de la solución madre en un espectrofotómetro.
- Para BSA, una fórmula comúnmente utilizada es BSA (mg/mL) = (A280/6.6) × 10, donde A280 es la absorbancia a 280 nm con una longitud de trayectoria de 1 cm leída contra un blanco apropiado (es decir,ε 2801% = 6.6)7. Por ejemplo, 0,8 mg/ml de BSA tiene una absorbancia de 0,528 a 280 nm.
- Para generar la curva estándar, prepare varias diluciones de BSA dentro de 0,025 mg/mL y 1,0 mg/mL. Esto dará como resultado 0,25-10 μg de BSA por pocillo después de agregar un volumen de muestra de 10 μL por pocillo.
NOTA: Las soluciones patrón proteicas deben prepararse en un medio con la misma composición (concentración final) del medio utilizado para preparar las muestras.
3. Ensayo
- Diluir las muestras para lograr una concentración de proteína dentro del rango de la curva estándar de 0,025-1,0 mg/mL. Tener varias (al menos 3) diluciones de muestra dentro del rango.
NOTA: Las muestras se pueden diluir con solución salina tamponada con fosfato (PBS) o cualquier otra composición de medio/tampón compatible con el reactivo Bradford. La concentración final de los componentes del medio no debe diferir entre el estándar y las muestras. - Agregue 10 μL de cada solución estándar de proteína a tres pocillos (es decir, por triplicado) de una microplaca de 96 pocillos. Para el punto 0 (cero) de proteína, añadir 10 μl del tampón/medio utilizado para preparar las soluciones patrón y las diluciones de la muestra.
- A otro conjunto de pocillos, agregue 10 μL de cada dilución de muestra a tres pocillos (es decir, por triplicado) de la misma microplaca de 96 pocillos. Un enfoque consiste en añadir diferentes volúmenes de una muestra y completar con un medio de hasta 10 μL por pocillo (por ejemplo, 0,5 μL, 1 μL, 2 μL, 4 μL y 8 μL de la muestra más 9,5 μL, 9 μL, 8 μL, 6 μL y 2 μL de medio).
- Agregue 250 μL de reactivo de ensayo de proteína Bradford a todos los pocillos. En la Figura 2 se muestra una configuración típica de microplacas. En este ejemplo, se incluyó un conjunto de pozos en blanco que contenían 260 μL (el volumen final por pozo) de agua para que sirvieran como blanco en un lector de microplacas (paso 4.5). Esto solo es necesario si también se van a recopilar datos de absorbancia.
NOTA: Prepare una curva estándar en la misma microplaca de muestras cada vez que se realice el ensayo. En otras palabras, si el número de muestras requiere otra placa, prepare otra curva estándar en la segunda placa, y así sucesivamente. - Registre los resultados (sección 4) en un plazo de 5 a 15 minutos.
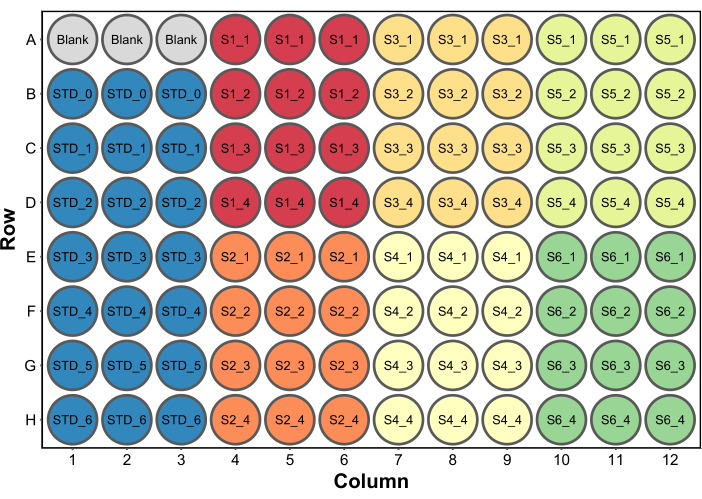
Figura 2: Un diseño típico de la placa para el ensayo de proteína de Bradford. En blanco se refiere a tres pocillos que contienen 260 μL de agua para ser utilizados como blanco en un lector de microplacas. Las ETS se refieren a los estándares de proteínas. S1-S6 son seis muestras diferentes. SX_1-SX_4 son cuatro diluciones de muestra diferentes para cada muestra. Haga clic aquí para ver una versión más grande de esta figura.
4. Registro de resultados
- En una habitación bien iluminada, sostenga la microplaca paralela al banco contra un fondo blanco uniforme (por ejemplo, una hoja de papel) con una mano. Asegure una alineación precisa colocando un nivel de burbuja en la placa.
- Con la otra mano, sostenga el teléfono inteligente en paralelo (algunas aplicaciones de la cámara indican útilmente la inclinación del dispositivo) al banco y a la microplaca y tome una o varias fotografías de toda la microplaca (Figura 3). En dispositivos iOS, active el indicador de nivel de la cámara en la configuración de la cámara habilitando la opción Cuadrícula . En dispositivos Android, active el indicador de nivel de cámara en la configuración de la cámara habilitando Sugerencias de encuadre.
- No se requiere ningún aparato de iluminación especial, pero tenga cuidado de evitar sombras y reflejos. Por ejemplo, evite sombrear la placa o el fondo con el teléfono inteligente y evite sombrear el fondo con la microplaca. Los pequeños reflejos en los bordes del área del pozo no son un problema; Los datos de color se pueden extraer de un área muy pequeña en el centro de cada pocillo.
- Compruebe brevemente la uniformidad del fondo, las sombras y los reflejos de la imagen. Además, eche un vistazo al ángulo de los pozos; El centro de cada pozo debe ser directamente visible (es decir, no detrás de las paredes del pozo).
- Si se desea comparar entre las lecturas de absorbancia de la microplaca y los datos de color de la imagen, lea la microplaca a 590 nm y 450 nm en un lector de microplacas21.

Figura 3: Captura de los resultados del ensayo de proteínas de Bradford. En una habitación bien iluminada, la microplaca se coloca paralelamente al banco sobre un fondo uniforme con una mano. Con la otra mano, el smartphone se sujeta en paralelo al banco y a la microplaca. Haga clic aquí para ver una versión más grande de esta figura.
5. Extracción automática de datos de color
- Descargue ImageJ y ReadPlate22, un complemento de ImageJ está disponible en https://imagej.nih.gov/ij/plugins/readplate/index.html (este es un archivo .txt).
- Abra ImageJ, haga clic en Plugins > Instalar y seleccione el archivo descargado en el paso 6.1.
- Establezca los parámetros de medición haciendo clic en Analizar > Establecer medidas y marque las siguientes opciones: Área; Desviación estándar; Valor de gris mínimo y máximo; Valor medio de gris; Valor de gris modal. En la parte inferior de la ventana, establezca Redirigir a: Ninguno y Decimales (0-9): 3.
- Vaya a Archivo > Abrir y seleccione la imagen de la microplaca tomada en el paso 4.
- Ve a Plugins > ReadPlate. Lea las instrucciones y, a continuación, haga clic en Aceptar.
- Seleccione el número de pozos: 96.
- Usando la herramienta de selección rectangular cargada automáticamente por el complemento, haga un rectángulo que comience en el centro del pozo A1 y termine en el centro del pozo H12. A continuación, haga clic en Aceptar.
- Seleccione el canal azul y haga clic en Aceptar.
- Confirme los parámetros predeterminados haciendo clic en Aceptar.
- Compruebe si el software delineó un área dentro de cada pozo y si las áreas seleccionadas no cubren áreas con sombras o reflejos anormales. Haga clic en Aceptar.
- Guarde los resultados y repita los pasos 5.8-5.10 para el canal verde.
- Calcule la relación azul-verde utilizando el modo de cada color.
NOTA: El cálculo se puede realizar manualmente o utilizando el software de preferencias del lector, como R, Microsoft Excel o GraphPad Prism.
6. Extracción manual de datos de color
- Descarga Inkscape, un editor de gráficos gratuito y de código abierto.
NOTA: Se puede utilizar cualquier software con la herramienta de selección de color (generalmente representada como un cuentagotas) para identificar el color y extraer datos RGB. - Abra Inkscape, vaya a Archivo > Abrir. Seleccione la imagen de la microplaca tomada en el paso 4.
- Elija la herramienta Seleccionar y transformar objetos (S), que se representa como una flecha en la parte superior izquierda, y haga clic en la imagen. Un borde de línea discontinua indicará la selección.
- Seleccione la herramienta Seleccionar colores de la imagen (D), que se representa como un cuentagotas en el lado izquierdo.
- Haga clic en el centro de un pozo. El color en el panel inferior ("Relleno:") cambiará en consecuencia. Haz clic en el color y aparecerá una pestaña de Relleno y Trazo en el lado derecho.
- Cambia el menú desplegable Color plano a RGB. Registre los valores mostrados para los canales azul y verde de cada pocillo.
- Calcule la relación azul-verde utilizando los valores registrados.
NOTA: El cálculo se puede realizar manualmente o utilizando el software de preferencias del lector, como R, Microsoft Excel o GraphPad Prism.
7. Construcción de curvas estándar y extrapolación de incógnitas
- Grafique la relación de intensidad promedio entre el verde y el azul en función de la concentración estándar de proteínas.
NOTA: Trace los datos manualmente o utilizando el software de las preferencias del lector, como R, Microsoft Excel o GraphPad Prism. - Calcule la relación media de intensidad verde-azul para cada muestra y dilución.
- Compruebe si la señal obtenida para la muestra se encuentra dentro del rango lineal del patrón de proteína.
- Ignore cualquier valor por debajo o por encima de los valores mínimo o máximo de la curva estándar.
- Utilice la ecuación lineal que describe la curva estándar para extrapolar la cantidad de proteína en la muestra. Multiplique los valores calculados por el factor de dilución en consecuencia.
Resultados
La Figura 4 es una imagen de una microplaca de la que se extrajeron datos de color y se registró la absorbancia a 450 nm y 590 nm. Los datos de color RGB reportados aquí como representativos se obtuvieron automáticamente como se describe en la sección 5. Un patrón típico de datos de color es un aumento en los valores de azul y una disminución en los valores de rojo y verde (Figura 5). Tenga en cuenta que, a pesar de la reflexión evidente en todos los poc...
Discusión
Este artículo describe RGBradford, un método que utiliza la cámara de un teléfono inteligente para registrar datos de un ensayo de proteína de Bradford, extraer datos de color y cuantificar con precisión los niveles de proteína en muestras biológicas, como se describióoriginalmente recientemente. Una diferencia con el método RGBradford original es que aquí se utilizó un procedimiento para obtener datos de color automáticamente con un complemento ImageJ22 . La p...
Divulgaciones
El autor no tiene conflictos de intereses que declarar.
Agradecimientos
Este trabajo fue financiado por el Consejo Nacional de Desarrollo Científico y Tecnológico (CNPq, Brasil) [números de beca 428048/2018-8 y 402556/2022-4] y la Universidad de Brasilia (Brasil). El autor agradece al Dr. Duarte Nuno Carvalho y a la Dra. Evelyn Santos (i3s, Oporto, Portugal) por proporcionar acceso a sus teléfonos inteligentes utilizados en esta investigación.
Materiales
| Name | Company | Catalog Number | Comments |
| 96-well flat-bottom polystyrene microtiter plates | Jet Biofil, Guangzhou, China | TCP011096 | Any flat-bottom microplate compativle with optical reading will suffice. |
| Bovine serum albumin | Sigma-Aldrich, St. Louis, MO | A2153 | |
| Coomassie Brilliant Blue G | Sigma-Aldrich, St. Louis, MO | B0770 | |
| Ethyl alcohol | |||
| iPhone 11 | Apple | MWM02BR/A | Can be substituted with other smartphone equiped with a camera |
| iPhone 14 Pro | Apple | N/A | |
| Phosphoric acid | Sigma-Aldrich, St. Louis, MO | 695017 | |
| Redmi Note 9 Pro | XIAOMI | N/A | |
| S22 Ultra | Samsung | N/A | |
| SpectraMax 384 Plus. Microplate reader. | Molecular Devices, San Jose, CA | PLUS 384 | Any microplate reader capable of reading at 450 nm and 590 nm will work. This is optional. The method was actually created to dismiss the need of a microplate reader. |
Referencias
- Zaguri, M., Kandel, S., Rinehart, S. A., Torsekar, V. R., Hawlena, D. Protein quantification in ecological studies: A literature review and empirical comparisons of standard methodologies. Methods in Ecology and Evolution. 12 (7), 1240-1251 (2021).
- Koga, T., et al. Mild electrical stimulation and heat shock ameliorates progressive proteinuria and renal inflammation in mouse model of Alport syndrome. PLoS One. 7 (8), e43852 (2012).
- Peterson, G. L. Determination of total protein. Methods in Enzymology. 91, 95-119 (1983).
- Goldfarb, A. R., Saidel, L. J., Mosovich, E. The ultraviolet absorption spectra of proteins. The Journal of Biological Chemistry. 193 (1), 397-404 (1951).
- Lowry, O. H., Rosebrough, N. J., Farr, A. L., Randall, R. J. Protein measurement with the Folin phenol reagent. The Journal of Biological Chemistry. 193 (1), 265-275 (1951).
- Smith, P. K., et al. Measurement of protein using bicinchoninic acid. Analytical Biochemistry. 150 (1), 76-85 (1985).
- Bradford, M. M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry. 72 (1-2), 248-254 (1976).
- Datki, Z., et al. Application of BisANS fluorescent dye for developing a novel protein assay. PLoS One. 14 (4), e0215863 (2019).
- Van Noorden, R., Maher, B., Nuzzo, R. The top 100 papers. Nature. 514 (7524), 550-553 (2014).
- . Scopus Available from: https://www.scopus.com/ (2022)
- Compton, S. J., Jones, C. G. Mechanism of dye response and interference in the Bradford protein assay. Analytical Biochemistry. 151 (2), 369-374 (1985).
- Chial, H. J., Thompson, H. B., Splittgerber, A. G. A spectral study of the charge forms of Coomassie Blue G. Analytical Biochemistry. 209 (2), 258-266 (1993).
- Pande, S. V., Murthy, M. S. R. A modified micro-Bradford procedure for elimination of interference from sodium dodecyl sulfate, other detergents, and lipids. Analytical Biochemistry. 220 (2), 424-426 (1994).
- Gogstad, G. O., Krutnes, M. -. B. Measurement of protein in cell suspensions using the Commassie brilliant blue dye-binding assay. Analytical Biochemistry. 126 (2), 355-359 (1982).
- Friedenauer, S., Berlet, H. H. Sensitivity and variability of the Bradford protein assay in the presence of detergents. Analytical Biochemistry. 178 (2), 263-268 (1989).
- Stoscheck, C. M. Increased uniformity in the response of the Coomassie blue G protein assay to different proteins. Analytical Biochemistry. 184 (1), 111-116 (1990).
- Zor, T., Selinger, Z. Linearization of the Bradford protein assay increases its sensitivity: Theoretical and experimental studies. Analytical Biochemistry. 236 (2), 302-308 (1996).
- Gee, C. T., Kehoe, E., Pomerantz, W. C. K., Penn, R. L. Quantifying protein concentrations using smartphone colorimetry: A new method for an established test. Journal of Chemical Education. 94 (7), 941-945 (2017).
- de Camargo, C., Vicentini, M., Gobbi, A., Martinez, D., Lima, R. Smartphone for point-of-care quantification of protein by Bradford assay. Journal of the Brazilian Chemical Society. 28 (4), 689-693 (2016).
- Moreira, D. C. RGBradford: Accurate measurement of protein concentration using a smartphone camera and the blue to green intensity ratio. Analytical Biochemistry. 655, 114839 (2022).
- Ernst, O., Zor, T. Linearization of the Bradford Protein Assay. Journal of Visualized Experiments. (38), 1918 (2010).
- Angelani, C. R., et al. A metabolic control analysis approach to introduce the study of systems in biochemistry: the glycolytic pathway in the red blood cell: Metabolic control analysis and the glycolytic pathway. Biochemistry and Molecular Biology Education. 46 (5), 502-515 (2018).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados