Técnica quirúrgica del implante de cadera personalizado impreso en 3 dimensiones para el tratamiento de la displasia de cadera canina
En este artículo
Resumen
En este trabajo se describe una nueva técnica quirúrgica para la implantación extracapsular de un implante personalizado, impreso en 3 dimensiones y que preserva la articulación. Este novedoso tratamiento tiene como objetivo restaurar la estabilidad de la cadera en perros adultos jóvenes que sufren de displasia de cadera con laxitud mediante la reproducción única de la forma anatómica del borde acetabular de la articulación de la cadera.
Resumen
La displasia de cadera causa una discapacidad importante en los perros. Las opciones de tratamiento se limitan al tratamiento paliativo (p. ej., alivio del dolor, ejercicio físico, cambios en el estilo de vida y control de peso) o cirugías invasivas como osteotomías pélvicas y artroplastia total de cadera. Por lo tanto, existe una fuerte necesidad insatisfecha de una solución eficaz y amigable con los perros que mejore la calidad de vida del mejor amigo del hombre. Llenamos este vacío de tratamiento al ofrecer un implante de cadera (3DHIP) mínimamente traumático y extraarticular, específico para perros, impreso en 3 dimensiones que restaura la estabilidad de la articulación de la cadera. El tratamiento quirúrgico con un implante 3DHIP es menos invasivo que las osteotomías y puede realizarse bilateralmente en una sola sesión quirúrgica. El implante 3DHIP extiende el borde acetabular dorsal de la articulación displásica de la cadera, aumentando así la cobertura de la cabeza femoral e inhibiendo la subluxación articular con una recuperación rápida. Un acceso suficiente al borde acetabular dorsal y ventral del cuerpo ilíaco, junto con un ajuste y fijación óptimos del implante, son pasos clave para un implante exitoso de 3DHIP e implican la necesidad de un abordaje específico. El presente artículo tiene como objetivo mostrar esta innovadora técnica quirúrgica con consejos y trucos como manual quirúrgico para la implantación del implante 3DHIP en perros afectados por displasia de cadera.
Introducción
La displasia de cadera (EH) en perros se manifiesta debido a un mal ajuste entre la cavidad de la cadera (acetábulo) y la cabeza femoral, lo que resulta en una subluxación de la articulación de la cadera. Afecta principalmente a perros jóvenes de razas medianas a grandes, lo que resulta en el deterioro del cartílago articular y, en última instancia, en la osteoartritis (OA) severa que conduce a dolor crónico y baja calidad de vida 1,2. La prevalencia global de displasia de cadera en perros es del 15,56%, que varía ampliamente según la raza y los sistemas de clasificación 3,4.
Además de los cambios en el estilo de vida, los pacientes con perro con displasia de cadera son tratados con fármacos antiinflamatorios y analgésicos para controlar el dolor y mantener la movilidad4. En caso de laxitud de la cadera en perros adultos jóvenes, el único recurso quirúrgico es la osteotomía pélvica doble (DPO) o triple (TPO), un procedimiento que implica dos o tres cortes completos de los huesos pélvicos para ampliar la cobertura de la cabeza femoral. Sin embargo, las complicaciones después de las osteotomías son comunes y aún se observa la progresión de la OA 5,6,7,8,9. Una vez que se han desarrollado la artrosis grave y el dolor crónico, solo quedan las cirugías complejas de alto impacto, como la artroplastia total de cadera (THR) o la ostectomía femoral de cabeza y cuello (FHO)de rescate 10. Sin embargo, la FHO presenta resultados menos favorables en perros de razas grandes y requiere fisioterapia prolongada para la restauración de la función de las extremidades11. Además, la THR es técnicamente desafiante e inherentemente asociada con complicaciones graves 12,13,14. Por lo tanto, se requiere un tratamiento eficaz para la displasia de cadera que solo requiera una cirugía de bajo impacto y con un menor riesgo de complicaciones antes de alcanzar esta etapa final.
El implante de cadera personalizado impreso en 3D (3DHIP) es el primer tratamiento de su tipo para la displasia de cadera canina desarrollado con la intención de ofrecer un implante traumático mínimo específico para perros que restaura la estabilidad de la articulación de la cadera. La técnica consiste en un implante de titanio para tratar principalmente a pacientes perros adultos jóvenes (de 6 meses a 2 años) con una articulación de cadera disfuncional que muestra una laxitud de la cadera de grado B (limítrofe) a D (moderada) según la Fédération Cynologique Internationale (FCI)15. Después de la tomografía computarizada (TC) de la articulación displásica, se diseña un implante siguiendo la anatomía específica de la articulación de la cadera de manera personalizada para extender el reborde acetabular dorsal, evitando así la subluxación de la articulación de la cadera y restaurando la estabilidad de la articulación de la cadera.
Un estudio previo de cadáveres caninos reveló que el implante mejoró la cobertura de la cabeza femoral y demostró fallas bajo una fuerza de impacto de 1.330 ± 320 Newtons16. Posteriormente, un estudio piloto con perros experimentales demostró una mayor cobertura de la cabeza femoral, una menor laxitud de la cadera y un aumento de la carga de peso mediante el análisis de la placa de fuerza. Además, el examen de las caderas intervenidas a los 6 meses después de la implantación reveló un volumen normal y una superficie lisa tanto de la cabeza femoral como del cartílago acetábulo, acompañada de hipertrofia de la cápsula articular basada en evaluaciones macroscópicas e histológicas17. Tras la confirmación de la eficacia y seguridad del implante y del concepto de tratamiento, se llevó a cabo una investigación clínica en perros de clientes que sufrían de displasia de cadera. El estudio a corto plazo reveló que los beneficios del implante de extensión de borde acetabular impreso en 3D son un buen ajuste personalizado del implante al acetábulo que restaura la estabilidad de la articulación de la cadera, una disminución de las actividades relacionadas con el dolor y un procedimiento quirúrgico de bajo impacto18. La aplicación del implante requiere el acceso a la cara ventrocaudal del cuerpo ilíaco y a la cara craneodorsal de la articulación de la cadera. En este artículo, describimos nuestra planificación quirúrgica y procedimiento quirúrgico con un abordaje craneodorsal modificado de la articulación de la cadera como manual para la implantación del 3DHIP en perros afectados por displasia de cadera.
Protocolo
Este estudio se consideró una práctica veterinaria clínica no experimental según lo mencionado en el artículo 1 - 5 (b) de la Directiva 2010/63/UE y fue aprobado por los Comités de Estudios Clínicos Veterinarios (VCSC) de la Universidad de Utrecht, Utrecht, Países Bajos. Este estudio involucró el tratamiento de perros propiedad de clientes, y todos los perros continuaron bajo el cuidado de sus respectivos dueños. A todos los dueños de perros se les proporcionó una carta informativa en la que se detallaba el protocolo del estudio, todas las posibles complicaciones (por ejemplo, infección, fallo del implante, déficits neurológicos y otros) y tratamientos alternativos como la osteotomía pélvica. Además, en este formulario, se explicaron los aspectos de privacidad y la gestión de datos inherente. Todos los clientes firmaron un formulario de consentimiento informado. Todo el protocolo de este estudio se divide en los siguientes pasos principales: selección del paciente, diseño y producción del implante 3DHIP, manejo preoperatorio y anestesia, procedimiento quirúrgico y manejo postoperatorio.
1. Selección del paciente
- Identifique a los perros de los 6 meses de edad > los que tengan signos clínicos relacionados con la EH y que tengan un signo positivo de subluxación de Ortolani (Figura 1) y evidencia radiográfica de EH con FCI grado B a D (Figura 2).
NOTA: La prueba de subluxación de Ortolani es una maniobra diagnóstica utilizada en medicina veterinaria para evaluar la estabilidad de la articulación de la cadera en perros. Durante la prueba de Ortolani en perros, el examinador coloca al animal boca arriba y flexiona las caderas a 90° mientras estabiliza la pelvis. Cada extremidad trasera se abduce suavemente, con el objetivo de desplazar la cabeza femoral del acetábulo para evaluar la estabilidad de la articulación de la cadera. Un signo positivo de Ortolani, indicado por un "chasquido" o movimiento característico, sugiere displasia de cadera y la posibilidad de inestabilidad de la articulación de la cadera. - Excluya a los perros con una placa de crecimiento acetabular abierta, caderas luxoides o cirugía previa de cadera.
- Realizar una tomografía computarizada de las caderas para excluir perros con cambios osteoartríticos moderados a graves en las caderas y para el diseño del implante.
NOTA: Se excluyen los perros que tengan cuello femoral y/o osteofitos del borde acetabular craneal y caudal > 2 mm (Figura 3).
2. Diseño y producción de implantes 3DHIP
- Diseñar el implante 3DHIP (patente número EP3463198B119) a partir de imágenes DICOM de TC DICOM preoperatorias de la pelvis completa según lo descrito por Willemsen et al.16 y Kwananocha et al.18 en el laboratorio (consulte la Tabla de Materiales).
- Segmente el hueso pélvico y el fémur de cada perro candidato a partir de la TC preoperatoria y cree un modelo 3D utilizando un software especializado (consulte la Tabla de Materiales y la Figura 4A).
- Cree un sistema de coordenadas local para la pelvis, basado en el plano pélvico posterior inclinado.
- Mida el ángulo nativo de Norberg (NA) de las caderas de cada perro candidato en el modelo 3D (Figura 4B).
- Utilice el software especializado (consulte la Tabla de materiales) para diseñar el implante 3DHIP en el modelo 3D de la pelvis. Utilice la NA nativa para determinar la cantidad de extensión del borde acetabular dorsal que se necesita; el implante 3DHIP aumenta el NA en 25-35 grados (Figura 4C y Figura 4D).
- Asegúrese de que el implante 3DHIP conste de dos subsecciones: la parte de fijación y la parte de extensión de la llanta. Diseñe la pieza de fijación para que conste de una carcasa interior porosa e incorpore cuatro orificios para tornillos de bloqueo y una brida de ilion ventral adicional para facilitar y precisar el posicionamiento. Diseñe la parte de extensión del borde para extender el borde acetabular dorsal con un desplazamiento interno de 1,5 mm que permita la fijación sin obstáculos de la cápsula articular (Figura 5A y Figura 5B).
- Imprima el implante 3DHIP creado (Figura 5C) a partir de una aleación de titanio de grado médico (Ti6AI4V ELI grado 23) utilizando tecnología de fusión selectiva por láser con una máquina de impresión directa de metal, operada por el fabricante del implante (consulte la Tabla de materiales).
- Posprocesamiento del implante 3DHIP impreso, incluida la liberación de tensión (recocido al vacío), el pulido manual del espejo y la limpieza ultrasónica, operado por el fabricante del implante (consulte la Tabla de materiales).
- Realice la limpieza final en la unidad de esterilización del hospital para eliminar cualquier polvo metálico residual que quede del proceso de fabricación.
- Lave manualmente el implante 3DHIP con champú de povidona y yodo (consulte la Tabla de materiales) y agua estéril.
- Limpie el implante 3DHIP con la lavadora higiénica (consulte la Tabla de materiales) a una temperatura de 94 °C durante 90 min.
- Encierre el implante 3DHIP en laminados de esterilización transparentes dobles (consulte la Tabla de materiales) y selle cada laminado por separado.
- Esterilizar el implante mediante autoclave con vapor (consulte la Tabla de materiales) a una temperatura de 134 °C durante 80 min.
3. Manejo preoperatorio y anestesia
- Realizar un examen general del perro del cliente antes de la anestesia y categorizar el riesgo de la anestesia utilizando la escala del paciente de la Sociedad Americana de Anestesiólogos (ASA) (escala 1-5)20.
NOTA: La escala de pacientes de la Sociedad Americana de Anestesiólogos (ASA, por sus siglas en inglés) se emplea para categorizar el riesgo de anestesia de los perros y ayuda a los veterinarios a determinar los protocolos anestésicos apropiados para cada perro. Clasifica a los perros en diferentes clases en función de su estado de salud, que van desde la Clase I para perros sanos hasta la Clase V para aquellos en condiciones críticas que no se espera que sobrevivan a la cirugía. Los perros categorizados en ASA 1 (perro sano normal) y ASA 2 (perros con enfermedad sistémica leve) se consideran candidatos adecuados para este tratamiento quirúrgico. Por lo general, estos perros no tienen enfermedades sistémicas subyacentes o tienen enfermedades sistémicas subyacentes leves, gozan de buena salud general y exhiben funciones fisiológicas normales. Se consideran candidatos de bajo riesgo para cirugía y anestesia. El animal debe estar en ayunas durante al menos 6 h antes de la hora programada para la inducción. - Anestesiar al perro siguiendo la categorización ASA según las necesidades individuales del paciente.
- Administrar dexmedetomidina intravenosa a una dosis de 2 μg/kg y clorhidrato de metadona a una dosis de 0,3 mg/kg para la premedicación en el perro. (consulte la Tabla de Materiales).
NOTA: La selección de premedicamentos y la vía de administración pueden diferir según la preferencia del anestesiólogo y el estado de salud y comportamiento del perro. - Administrar propofol intravenoso a una dosis de 2-4 mg/kg (consultar la Tabla de Materiales) para la inducción de la anestesia.
- Intubar al perro y mantener la anestesia con isoflurano inhalado (consulte la Tabla de materiales) y oxígeno.
- Administrar dexmedetomidina intravenosa a una dosis de 2 μg/kg y clorhidrato de metadona a una dosis de 0,3 mg/kg para la premedicación en el perro. (consulte la Tabla de Materiales).
- Monitorear continuamente y garantizar la estabilidad de los signos vitales, que abarcan la frecuencia cardíaca, la frecuencia respiratoria, los niveles de dióxido de carbono al final de la espiración, la saturación percutánea de oxígeno arterial, la presión arterial no invasiva, la temperatura esofágica y la electrocardiografía.
- Realizar analgesia epidural mediante técnica estéril.
- Coloque al perro en decúbito esternal y flexione suavemente las extremidades traseras hacia adelante para crear más espacio entre la última vértebra lumbar y el sacro.
- Identifique el sitio de inyección ubicado justo caudal a la séptima apófisis espinal dorsal, donde se puede palpar un "hoyuelo".
- Realice un lavado estéril y póngase guantes estériles utilizando técnicas asépticas.
- Inserte la punta de la aguja espinal en el espacio epidural y verifique su correcta colocación mediante la técnica de "gota colgante". Brevemente, introduzca una gota de solución salina en el centro de la aguja espinal. Cuando la punta de la aguja espinal penetra en el ligamento flavum y entra en el espacio epidural, la solución salina dentro del cubo migrará del cubo a la aguja21.
- Inyecte los fármacos (morfina 0,1 mg/kg diluida con levobupivacaína 1 mL/5 kg) (consulte la Tabla de Materiales) a un ritmo lento y constante para asegurar una distribución uniforme del fármaco cuando se confirme la colocación correcta.
- Coloque un catéter urinario Foley permanente (consulte la Tabla de materiales) en la vejiga utilizando una técnica estéril y déjelo en su lugar durante 12-24 h.
- Asegurar un ambiente limpio y estéril para el procedimiento de cateterismo; Recorta el pelo del prepucio en los perros machos y la bóveda vaginal ventral circundante en las hembras.
- Limpie el área con una solución de povidona yodada (consulte la Tabla de materiales) y enjuague el prepucio/bóveda vaginal con 2-12 ml de solución diluida de povidona yodada (el volumen varía según el tamaño del perro).
- Lávese bien las manos y use guantes estériles para minimizar el riesgo de contaminación.
- Aplique gelatina lubricante estéril en el extremo distal del catéter Foley y emplee una técnica aséptica durante la inserción del catéter Foley.
- Una vez que el catéter esté correctamente colocado en la vejiga, infle el balón con agua estéril de acuerdo con el volumen especificado en el paquete. Esto asegura el catéter en su lugar y evita el desplazamiento accidental.
- Conecte el puerto de drenaje del catéter Foley al puerto receptor de una bolsa de recolección de orina.
- Corta toda la extremidad circunferencialmente, comenzando desde la columna vertebral hasta justo distal al corvejón. En el caso de la implantación bilateral de 3DHIP en una sola etapa, corte la otra extremidad de manera similar y conecte los lados izquierdo y derecho en el dorso lumbosacro.
- Envuelva la parte distal de la extremidad con un vendaje cohesivo no estéril. Seleccione un ancho y largo apropiados de vendaje cohesivo no estéril, comenzando ligeramente por debajo del sitio quirúrgico y envolviéndolo en espiral por la extremidad, cubriendo la pata y las uñas.
- Administrar cefazolina inyectable a una dosis de 20 mg/kg (consultar la Tabla de Materiales) por vía intravenosa 30 min antes de la incisión cutánea y repetir cada 90 min hasta el final de la cirugía.
- Coloque al perro en una mesa de operaciones estándar en decúbito lateral y coloque la extremidad afectada en posición colgante. Asegure al paciente en esta posición usando un posicionador de bolsas de frijoles al vacío
- Realice el último exfoliante quirúrgico estéril en la extremidad en preparación para la cirugía. Frote la piel 2 veces con gluconato de clorhexidina al 4% y termine con dos aplicaciones de etanol en aerosol al 70% (v/v) (consulte la Tabla de materiales).
- Coloque cuatro paños quirúrgicos impermeables alrededor del sitio quirúrgico. Indique a un asistente que libere la extremidad distal de su posición suspendida, mientras el cirujano asegura y cubre la extremidad distal con un calcetín impermeable estéril. Agregue una capa de envoltura cohesiva estéril para mayor protección.
- Cubra la piel expuesta de toda el área quirúrgica con un paño impregnado de yodo (consulte la Tabla de materiales) y luego asegúrelo con pinzas para toallas.
4. Procedimiento quirúrgico
- Identificar la punta del trocánter mayor, el borde craneal del fémur proximal y el ala ilíaca a través de la palpación para establecer la orientación.
- Incidir la piel con un bisturí quirúrgico desde la espina ilíaca dorsal craneal comenzando 6-10 cm craneal hasta el trocánter mayor. Luego, gire ligeramente ventralmente a lo largo del borde craneal del fémur proximal. Detenga la incisión 2-5 cm distal al trocánter mayor. La longitud de la incisión es de aproximadamente 8-15 cm (dependiendo del tamaño del perro; Figura 6A).
NOTA: Este abordaje quirúrgico fue modificado a partir del abordaje craneodorsal de la articulación de la cadera previamente reportado por Johnson22. - Realizar una incisión a través de la grasa subcutánea hasta la fascia para establecer una disección anatómica siguiendo los planos anatómicos (Figura 6B).
- Separe y haga una incisión aguda en la hoja superficial del músculo fascia lata a lo largo del borde craneal del músculo bíceps femoral. Retrae el músculo bíceps femoral caudalmente.
- Identifica el triángulo graso, que está bordeado por el músculo tensor de la fascia latea, el músculo glúteo y el músculo bíceps femoral. Separe el triángulo graso con una tijera de disección de punta roma y el dedo índice, lo que proporcionará acceso a las capas más profundas.
- Incidir el tabique intermuscular entre el músculo glúteo superficial, el músculo glúteo medio y el músculo tensor de la fascia lata con un bisturí quirúrgico (Figura 7A y Figura 7E).
- Use un retractor de mano para separar y retraer los músculos glúteos superficiales y medios dorsalmente, lo que expondrá la inserción del músculo glúteo profundo.
- Socava el músculo glúteo profundo cerca del trocánter mayor con tijeras de disección de punta roma.
- Colocar una sutura de estancia en el tendón glúteo profundo aproximadamente 1-1,5 cm proximal de su inserción en el trocánter mayor.
- Realizar una tenotomía glútea profunda completa cerca del hueso (aproximadamente a 0,5-1 cm de distancia de su inserción) utilizando un bisturí quirúrgico (Figura 7B y Figura 7F).
- Realice una disección roma con tijeras de disección de punta roma para liberar el músculo glúteo profundo de la cápsula articular subyacente, después de lo cual se puede elevar subperiósticamente desde el ilion usando un elevador perióstico y un dedo índice.
- Utilice la electrocauterización bipolar para la hemostasia de pequeños vasos entre el músculo glúteo profundo y la cápsula articular. Luego, retraiga el músculo glúteo profundo dorsalmente reemplazando los retractores Amry Navy.
- Liberar parcialmente el músculo ilíaco del borde caudoventral de la diáfisis ilíaca mediante un elevador perióstico e identificar la inserción del músculo recto femoral (Figura 7C y Figura 7G).
- Utilice un elevador perióstico para eliminar todo el tejido blando restante del eje ilíaco expuesto para prepararse para el posicionamiento preciso del implante 3DHIP y rasque el periostio para estimular el crecimiento óseo para la fijación secundaria del implante.
- Identificar el músculo articular coxae caudal al músculo recto femoral que recubre la cápsula articular.
NOTA: El músculo articularis coxae puede liberarse de su inserción si interfiere con la posición del implante. - Coloque el implante 3DHIP en su posición designada con el brido del implante de la parte de fijación enganchada debajo del borde ventral del eje ilíaco caudoventral expuesto, justo craneal a la prominencia ósea que marca la inserción del músculo recto femoral (Figura 7D y Figura 7H).
- Compruebe que la parte de extensión del borde del implante se superpone a la parte craneodorsal de la cápsula articular de la cadera sin interferir con la fijación de la cápsula articular en el borde acetabular y que no se captura ningún músculo glúteo profundo debajo de la parte de extensión.
NOTA: La exposición adecuada para el posicionamiento del implante y la inserción del tornillo se puede lograr mediante la abducción continua, la rotación externa y la flexión de la articulación de la cadera por un asistente para liberar la tensión en el complejo muscular glúteo que facilita la exposición quirúrgica. - Compruebe la posición ideal del implante visualizando y sondeando con la cánula de succión para obtener un stock óseo perfecto en los cuatro orificios de los tornillos expuestos y sondeando la ausencia de espacio entre el reborde ilial y el eje ilíaco caudoventral.
- Fije temporalmente el implante en la posición deseada con un tornillo de bloqueo autorroscante de titanio (2,4 mm, 2,7 mm o 3,5 mm) (consulte la Tabla de materiales), que no está completamente apretado para permitir ajustes mínimos de rotación en el implante al colocar el segundo tornillo.
NOTA: La secuencia de colocación de los cuatro tornillos se puede adaptar de acuerdo con su conveniente accesibilidad (Figura 5C). - Realice fluoroscopia intraoperatoria (consulte la Tabla de materiales) en vistas laterales (Figura 8A) y latero-oblicuas (Figura 8B) para evaluar de manera integral la posición y alineación del implante. Compare las imágenes fluoroscópicas obtenidas con la planificación preoperatoria para asegurarse de que el implante está posicionado de acuerdo con el plan quirúrgico.
- Comprobar que la curvatura de la parte de extensión del borde del implante es exactamente congruente con la curvatura de la cabeza femoral y del reborde acetabular caudal y craneal visible que no están cubiertos por el implante.
NOTA: Si es necesario, se pueden realizar ajustes. Se retira el primer tornillo, se reemplaza el implante y se fija temporalmente con un tornillo en un nuevo material óseo, y se repite la fluoroscopia. - Inserte tres tornillos de bloqueo autorroscantes de titanio (2,4 mm, 2,7 mm o 3,5 mm) en los orificios de los tornillos restantes para fijar el implante al eje ilial. Después de colocar el segundo tornillo, apriete completamente el primer tornillo.
- Realice una comprobación final de que todos los tornillos estén apretados a mano en el mecanismo de bloqueo.
- Realizar la flexión, extensión y abducción de la articulación de la cadera, así como la prueba de subluxación de Ortolani para excluir el pinzamiento de la cabeza/cuello femoral y garantizar que se revierta la laxitud de la cadera.
- Vuelva a unir los extremos cortados del tendón de inserción del músculo glúteo profundo utilizando un patrón de sutura de bucle de bloqueo y 1-2 suturas de colchón con material de sutura de monofilamento absorbible sintético (consulte la Tabla de materiales) que están destinadas a la aproximación del tejido durante períodos prolongados. Extienda y rote internamente la articulación de la cadera para disminuir la tensión en el tendón de inserción del músculo glúteo profundo mientras se sutura.
- Repare la fascia glútea y la fascia tensora lata con sutura absorbible de monofilamento sintético en un patrón interrumpido simple.
- Cierre el tejido subcutáneo con una sutura absorbible de monofilamento sintético en un patrón interrumpido simple y cierre la piel con una sutura no absorbible de monofilamento sintético en un patrón interrumpido simple (consulte la Tabla de materiales).
NOTA: Si se planea un procedimiento bilateral de una sola etapa, gire al perro hacia el otro lado con la extremidad no tratada en posición colgante. Después de la preparación aséptica, los pasos 3.10-4.27 del procedimiento quirúrgico se realizan de manera similar. - Realizar imágenes postoperatorias que consisten en una tomografía computarizada de las caderas o radiografías ortogonales de cadera en vistas latero-oblicuas y ventrodorsales para la evaluación final de la posición del implante y la colocación del tornillo (Figura 9).
5. Manejo postoperatorio
- Proporcionar atención hospitalaria durante la noche y manejo del dolor (p. ej., con infusiones de tasa continua [CRI] de ketamina HCl 2-10 mcg∙kg-1∙min-1 o citrato de sufentanilo 0.1 mcg∙kg-1∙h-1 con metadona (IV, 0.2 mg/kg cada 6 h, carprofeno (IV, 4 mg/kg una vez al día) y gabapentina (PO, 10 mg/kg cada 8 h) (consulte la Tabla de materiales).
- Permitir el postoperatorio directo con correa corta caminar según sea necesario para orinar y defecar en el suelo no resbaladizo al día siguiente (ver Video Complementario S1).
NOTA: En caso de inestabilidad de las extremidades traseras o problemas para levantarse, use un cabestrillo de soporte o una toalla debajo del vientre para sostener las extremidades traseras. - Permitir el alta domiciliaria el día después de la cirugía, después de retirar el catéter de Foley y cuando se observe micción voluntaria.
- Recetar medicamentos para el manejo del dolor en el hogar (p. ej., medicamentos orales como carprofeno 2 mg/kg dos veces al día y gabapentina 10 mg/kg cada 8 h durante 14 días) (consulte la Tabla de materiales).
NOTA: En perros hiperactivos, se puede administrar clorhidrato de trazodona 2-5 mg/kg dos veces al día (consulte la Tabla de Materiales), por vía oral. Esto se puede continuar durante 1-2 semanas después de la operación para garantizar una rehabilitación segura sin actividades de alto impacto. - Prohíba las actividades de alto impacto (p. ej., saltar, correr, subir escaleras, correr con otras mascotas o "vivienda brusca") durante 6 semanas después de la operación. En casa, saque a los perros lentamente y anímelos a usar las extremidades traseras operadas de acuerdo con un esquema de ejercicio semanal. Dentro de las 6 semanas posteriores a la operación, permita que el paciente perro camine con correa de 4 a 6 veces al día, inicialmente durante 5 a 10 minutos cada una en las primeras 2 semanas, y luego extienda la duración en 5 minutos cada 2 semanas.
- Aconsejar fisioterapia profesional y/o hidroterapia a partir de la segunda semana después de la cirugía, cuando la cicatrización de las heridas cutáneas esté completa.
Resultados Representativos
Los resultados a corto plazo de la extensión del reborde acetabular se han publicado previamente, derivados de un estudio observacional en curso en el Departamento de Ciencias Clínicas de la Universidad de Utrecht18. De diciembre de 2019 a marzo de 2022, se incluyeron en el estudio un total de 61 caderas de 34 perros. La cohorte estuvo formada por 24 hombres y 10 mujeres, con una mediana de edad de 12 meses (entre 7 y 38 meses) y un peso corporal medio de 27,3 kg (entre 12 y 86 kg). Siete perros se sometieron a cirugía de cadera unilateral, mientras que veinte perros se sometieron a cirugía bilateral de cadera en una sola sesión. Además, siete perros fueron operados en ambas caderas, realizada en dos sesiones separadas.
El estudio previo encontró un aumento significativo en el ángulo de Norberg (NA), el porcentaje lineal de cobertura de la cabeza femoral (LFO) y el porcentaje de cobertura de la cabeza femoral (PC) inmediatamente después de la implantación (Tabla 1). Además, el signo de subluxación de Ortolani postoperatorio fue negativo en el 96,7% de las extremidades operadas, lo que indica que el implante de extensión del reborde acetabular restauró la congruencia de la cadera y disminuyó la laxitud de las caderas displásicas18. En particular, la capacidad de aumentar la cobertura de la cabeza femoral sin realizar ninguna osteotomía redireccional permitió la retención fisiológica de la geometría pélvica. La técnica mínimamente invasiva resultó en una baja incidencia de complicaciones (4,9%) a corto plazo, favoreció la movilización precoz y disminuyó el dolor relacionado con la actividad (Tabla 1).
Además, esta técnica permitió la colocación de implantes bilaterales de 3DHIP en una sola etapa. Las extremidades tratadas soportaron peso sin soporte pélvico dentro de las 12 a 24 horas posteriores a la cirugía. Durante el período de seguimiento de 12 meses, 3 perros requirieron cirugía de revisión debido a la falla del implante (2 perros) o a un avance significativo de la osteoartritis (1 perro). Utilizando el abordaje quirúrgico presentado simultáneamente con los movimientos sugeridos de la articulación de la cadera (abducción, flexión y rotación externa), se obtuvo una mejor exposición de la cara ventrocaudal de la diáfisis ilíaca y de la cara craneodorsal de la articulación de la cadera, lo que facilitó el posicionamiento del implante 3DHIP. Además, la fluoroscopia intraoperatoria aumentó la precisión de la posición del implante.
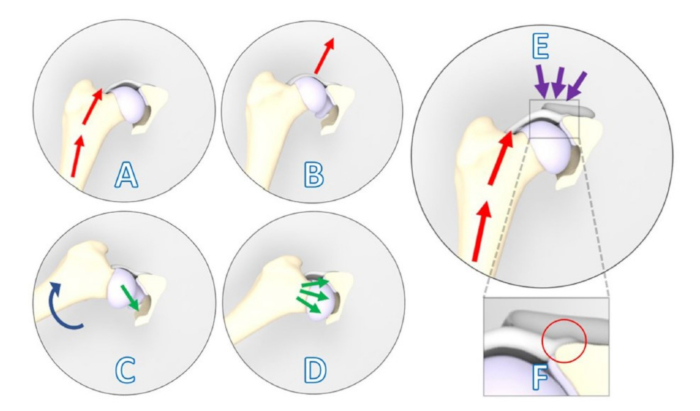
Figura 1: Ilustraciones esquemáticas que muestran un signo positivo de subluxación Ortolani contrarrestado por el implante 3DHIP. (A-D) Signo positivo de subluxación Ortolani. (A) La extremidad del perro se coloca en flexión y aducción neutras, y se ejerce una fuerza (flechas rojas) hacia el dorso del perro a lo largo del eje femoral que causa (B) subluxación dorsal de la articulación displásica de la cadera. (C) La abducción gradual de la extremidad (flecha azul) se realiza mientras se mantiene la presión sobre el fémur. (D) Dependiendo de la deficiencia del reborde acetabular, la cabeza femoral subluxada vuelve a caer en la cavidad (flechas verdes). (E) El implante 3DHIP se introduce para mejorar la estabilidad de la articulación displásica de la cadera al reforzar la cápsula de la cadera y el labrum, que sirven como superficies estabilizadoras y de soporte de peso (flechas moradas). (F) Al aumentar el área rectangular, el desplazamiento interno de 1,5 mm del implante es visible en el círculo rojo, lo que garantiza que la fijación de la cápsula no se vea afectada. Esta figura fue modificada a partir de Willemsen et al.17. Abreviatura: 3DHIP = implante de cadera impreso en 3 dimensiones. Haga clic aquí para ver una versión más grande de esta figura.
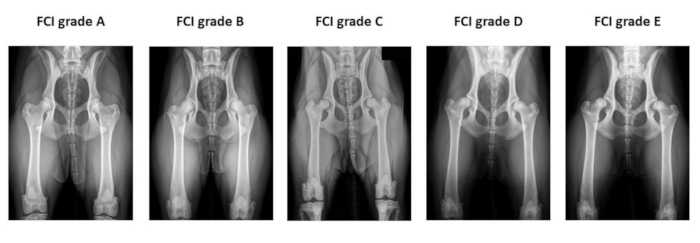
Figura 2: Ejemplo de las radiografías preoperatorias de cadera utilizadas para la clasificación de la displasia de cadera de la Fédération Cynologique Internationale . Las radiografías se toman en la posición extendida de la cadera ventro-dorsal. De izquierda a derecha, la FCI clasifica la displasia de cadera en cinco categorías diferentes: A (normal), B (limítrofe), C (displasia leve de cadera), D (displasia moderada de cadera) y E (displasia grave de cadera). Abreviatura: FCI = Fédération Cynologique Internationale. Haga clic aquí para ver una versión más grande de esta figura.
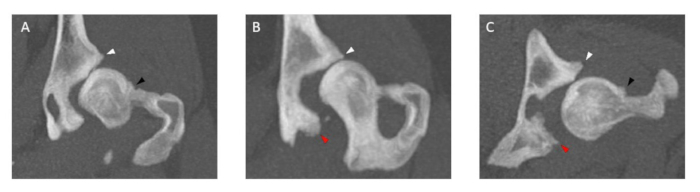
Figura 3: Imágenes de exámenes de TC de la articulación de la cadera que ilustran osteofitos de diferentes tamaños. El grosor de todos los osteofitos se mide en los planos coronales (A,B) y transversales (C) en el borde acetabular craneal (punta de flecha blanca) y caudal (punta de flecha roja) y en el cuello femoral (punta de flecha negra). Se excluyen los perros que tengan cuello femoral y/o osteofitos de reborde acetabular craneal y caudal > 2 mm. El grosor del corte del examen CT es de 5 mm. Haga clic aquí para ver una versión más grande de esta figura.
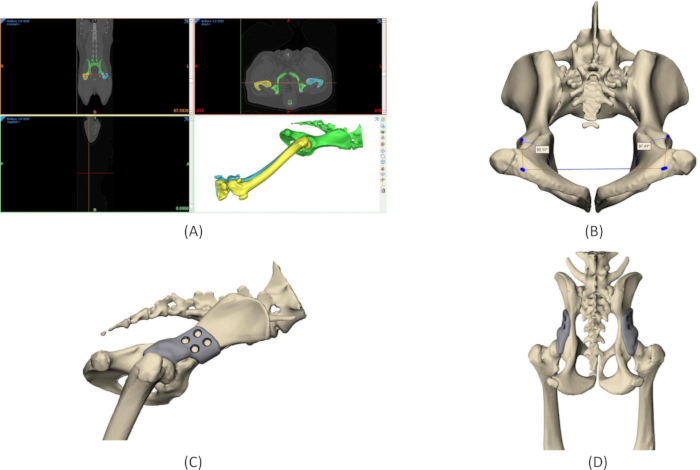
Figura 4: Proceso de diseño del implante 3DHIP. (A) Segmentación de la región de interés a partir de datos CT DICOM. (B) Mediciones de los ángulos nativos de Norberg en el modelo 3D de la pelvis. (C) Representación de un implante 3DHIP en la cadera derecha, vista lateral. (D) Representación de implantes bilaterales 3DHIP, vista dorsal-ventral. Abreviatura: 3DHIP = implante de cadera impreso en 3 dimensiones. Haga clic aquí para ver una versión más grande de esta figura.
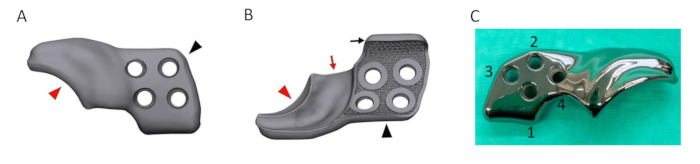
Figura 5: Representación de un implante 3DHIP diseñado. (A) Imagen renderizada del lado lateral/exterior del implante 3DHIP. (B) Imagen renderizada de la superficie interna del implante que muestra la superficie porosa que permite el crecimiento óseo para la osteointegración. La parte de fijación ósea (punta de flecha negra) del implante renderizado que incorpora 4 orificios de tornillo de bloqueo y la brida ventral de ilion (flecha negra) para ayudar en el posicionamiento y estabilización correctos del implante. La parte de extensión del borde (punta de flecha roja) del implante renderizado con un desplazamiento interno de 1,5 mm (flecha roja) que permite la fijación sin obstáculos de la cápsula articular. (C) Fotografía de un implante de titanio 3DHIP que muestra 4 orificios para tornillos dispuestos en la secuencia para la inserción del tornillo. Abreviatura: 3DHIP = implante de cadera impreso en 3 dimensiones. Haga clic aquí para ver una versión más grande de esta figura.
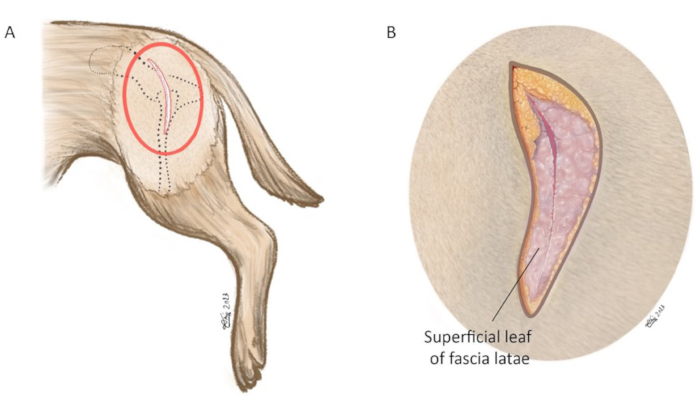
Figura 6: Ilustración esquemática de la incisión en la piel. (A) El óvalo rojo marca el área en la que se realiza la incisión en la piel. (B) Aumento del círculo rojo en (A). La incisión en la piel se realiza utilizando una cuchilla #10 centrada en la punta del trocánter mayor, apuntando a la espina ilíaca dorsal craneal. La longitud de la incisión es de aproximadamente 8-15 cm. En la imagen ampliada, la hoja superficial de la fascia lata está incisa a lo largo del borde del músculo craneal del músculo bíceps femoral. Orientación: a la izquierda es craneal, la superior es dorsal. Haga clic aquí para ver una versión más grande de esta figura.
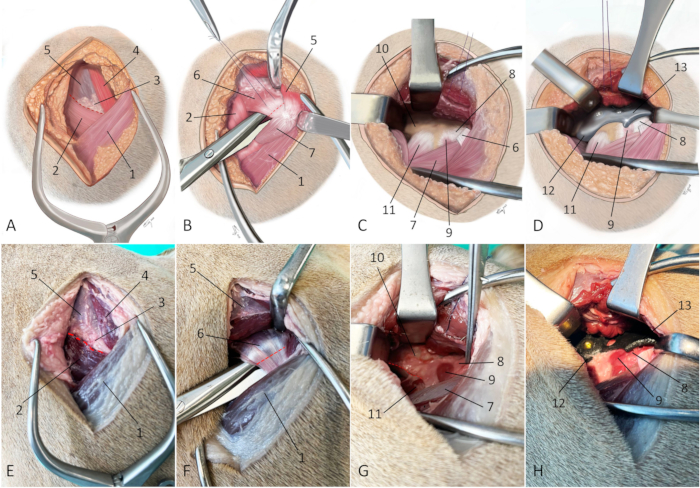
Figura 7: Ilustraciones esquemáticas y fotografías de un cadáver embalsamado que representan el enfoque quirúrgico para la implantación de 3DHIP. (A-D) Las ilustraciones esquemáticas y las fotografías (E-H) de un cadáver embalsamado representan el enfoque quirúrgico para la implantación de 3DHIP. (A y E) La línea punteada roja marca la línea de la incisión a través del tabique intermuscular entre el músculo glúteo superficial, el músculo glúteo medio y el músculo tensor de la fascia lata. (B y F) La línea punteada roja marca el sitio de la tenotomía. Los músculos glúteos superficiales y medios se retraen dorsalmente para exponer el músculo glúteo profundo. Las tijeras de disección se utilizan para socavar el músculo glúteo profundo cerca de su inserción en el trocánter mayor. La tenotomía se realiza cerca (a 0,5-1 cm) de su inserción en el hueso. (C y G) La exposición adecuada para la colocación del implante 3DHIP requiere la liberación del músculo glúteo profundo de la cápsula articular y la superficie lateral del cuerpo ilíaco y la liberación parcial del músculo ilíaco y los músculos recto femoral del borde caudoventral de la diáfisis ilial (línea punteada roja). (D y H) El implante 3DHIP se coloca fuera de la cápsula de la articulación de la cadera. Para mayor precisión y facilidad de colocación, la brida de ilion de la parte de fijación del implante se coloca debajo del borde ventral del eje ilíaco caudoventral expuesto. Orientación: a la izquierda es craneal, la superior es dorsal. 1) músculo bíceps femoral, 2) músculo tensor de la fascia lata, 3) triángulo graso, 4) músculo glúteo superficial, 5) músculo glúteo medio, 6) músculo/tendón glúteo profundo, 7) músculo vasto lateral, 8) cápsula articular de la articulación, 9) músculo articular coxae, 10) parte caudal del cuerpo ilíaco, 11) músculo recto femoral, 12) brida ilion del implante y 13) parte de extensión del borde del implante. Haga clic aquí para ver una versión más grande de esta figura.
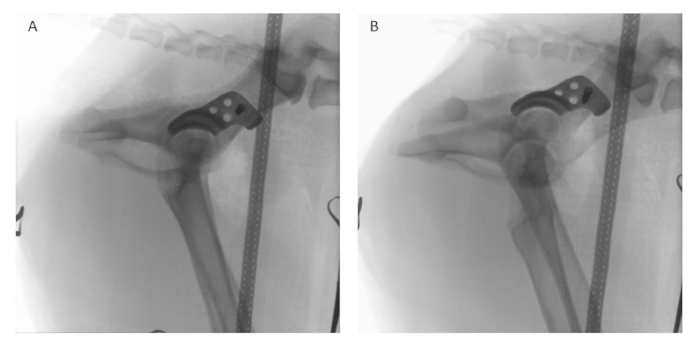
Figura 8: Fluoroscopia intraoperatoria. Después de la colocación del implante y la fijación temporal con un tornillo de bloqueo, la fluoroscopia intraoperatoria se realiza en (A) vistas laterales y (B) latero-oblicuas utilizando un intensificador de imagen digital para evaluar y comparar la posición del implante con la planificación preoperatoria. Haga clic aquí para ver una versión más grande de esta figura.

Figura 9: Ejemplos de radiografías postoperatorias en tres planos y TAC postoperatoria después de una cirugía bilateral de implante 3DHIP en un solo ciclo en un perro. (A) Vista ventrodorsal de la radiografía; (B) radiografía latero-oblicua derecha; (C) radiografía latero-oblicua izquierda. Reconstrucción 3D a partir de TAC postoperatorio en vista lateral que muestra la (D) cadera derecha y (E) vista dorso-ventral. (F) TAC postoperatorio de ambas caderas en el plano transversal con un grosor de corte de 5 mm. Los implantes 3DHIP se fijaron con cuatro tornillos de bloqueo a cada lado. Haga clic aquí para ver una versión más grande de esta figura.
| Mediciones de resultados | Preoperatively | Postoperatorio inmediato | 1,5 meses | 3 meses | Valor p |
| NA (◦) | 87 ± 13A | 134 ± 19ter | - | 131 ± 20ter | <0,001* |
| LFO (%) | 22 ± 15A | 81 ± 16ter | - | 76 ± 19ter | <0,001* |
| PC (%) | 33 ± 17bis | 79 ± 21ter | - | 77 ± 20ter | 0.002* |
| HCPI (%) | 31,44 ± 11,9A | - | 20,39 ± 10,09b | 17,69 ± 10,8b | <0,001** |
Tabla 1: Resultados a corto plazo (media ± DE) de las mediciones radiográficas mediante TC coronal y cuestionario del propietario relacionado con el dolor utilizando el Índice de Dolor Crónico de Helsinki en perros con displasia de cadera sometidos a implante de 3DHIP. Esta tabla fue modificada de Kwananocha et al.18. HCPI (%) = 100% × puntuación total del índice/máxima puntuación posible del índice de las preguntas respondidas. a,bvalor p < 0,05 de Bonferroni, p-valor* del análisis de medidas repetidas, p-valor** del modelo mixto lineal generalizado. Abreviaturas: NA = ángulo de Norberg; LFO = porcentaje lineal de superposición de la cabeza femoral; PC = porcentaje de cobertura de la cabeza femoral; DE = desviación estándar; HCPI = Índice de Dolor Crónico de Helsinki.
Video complementario S1: Se permite el soporte de peso postoperatorio directo con solo caminatas cortas con correa sobre un piso antideslizante a partir del día después de la cirugía. Haga clic aquí para descargar este video.
Discusión
La extensión del reborde acetabular mediante el implante 3DHIP proporciona ventajas sobre las terapias quirúrgicas convencionales para la displasia de cadera canina y ha mostrado resultados prometedores para aumentar la cobertura de la articulación displásica de la cadera y revertir la laxitud de la cadera en el seguimiento a corto plazo17,18. Esta publicación tuvo como objetivo mostrar la técnica quirúrgica con consejos y trucos como manual quirúrgico para la implantación del implante 3DHIP en perros afectados por displasia de cadera.
Selección de candidatos para la colocación de implantes 3DHIP: los perros jóvenes de entre 6 y 24 meses de edad con displasia clínica de cadera marcada por laxitud de la cadera (FCI grado B-D) con una prueba de subluxación de Ortolani positiva son candidatos adecuados. La placa de crecimiento acetabular triradiada debe estar cerrada y, preferiblemente, no hay osteoartritis en las imágenes de TC, aunque se aceptan osteofitos menores de hasta 2 mm. Los perros con caderas luxoides con luxación casi completa de la cabeza femoral no son aceptados para la colocación de implantes 3DHIP debido a la rápida progresión de la osteoartritis, la incapacidad de la cabeza femoral para moverse hacia el acetábulo y la conversión temprana esperada a un reemplazo total de cadera.
Hay algunos pasos críticos dentro de la técnica quirúrgica.
Diseño de implantes
Dado el diseño individualizado de los implantes 3DHIP, es absolutamente obligatoria una valoración preoperatoria de la articulación displásica de la cadera mediante un TAC. Además de la determinación del tamaño y la posición correcta del implante del reborde ilial ventral, se puede determinar en particular la cantidad de extensión del borde acetabular necesaria para proporcionar una cobertura suficiente de la cabeza femoral.
Abordaje quirúrgico
Un paso crítico durante la cirugía es la exposición suficiente del borde acetabular dorsal y el borde ventral del cuerpo ilíaco caudal para la colocación del implante. El abordaje quirúrgico del cuerpo ilíaco y de los aspectos craneodorsales de la articulación de la cadera en el implante de 3DHIP difiere de los abordajes convencionales22. En la técnica presentada, se omitió la osteotomía trocantérea y se realizó una tenotomía glútea profunda mientras se conservaban los músculos glúteo superficial y medio. De esta forma, se evitó el riesgo de complicaciones asociadas a las osteotomías trocantéreas 23,24,25, como la consolidación tardía o no consolidada y se aceleró el proceso de recuperación. Además, este enfoque craneodorsal modificado se puede emplear en una variedad de edades, razas y tamaños de perros sin necesidad de modificaciones. Cabe destacar que no se reportaron complicaciones asociadas al abordaje quirúrgico presentado.
Colocación correcta del implante
A pesar de que el implante de cadera impreso en 3D a medida está diseñado para adaptarse perfectamente a la anatomía acetabular única de cada perro, se observó una colocación imperfecta del implante con una desviación craneocaudal de 4-5 mm con respecto a la posición objetivo planificada en la primera cohorte de perros, posiblemente relacionada con la curva de aprendizaje con la técnica18. El reborde ilial ventral de la parte de fijación ósea del implante 3DHIP permite un posicionamiento más preciso, especialmente en la dirección dorsoventral. Sin embargo, debido a la localización extracapsular del implante, todavía es difícil lograr un posicionamiento perfecto del implante; El borde interno del acetábulo está oscurecido por la membrana sinovial. Además, la formación de osteofitos durante el tiempo de producción del implante puede influir en el posicionamiento adecuado del implante. Para garantizar la colocación precisa del implante de acuerdo con el plan preoperatorio, actualmente se requiere la verificación mediante fluoroscopia intraoperatoria. También se espera que con una mayor experiencia, la precisión del posicionamiento del implante disminuya aún más a menos de 1-2 mm de precisión en la colocación. En el futuro, la cirugía guiada con guías de fresado quirúrgico impresas en 3D puede obviar la necesidad de fluoroscopia.
Esta técnica también tiene algunas limitaciones. Los resultados previos a corto plazo sugieren una amplia gama de diferentes anatomías de cadera que pueden tratarse con implantes 3DHIP. Si bien los hallazgos del estudio a largo plazo aún no están disponibles, se recomienda considerar la implantación de 3DHIP para perros que no muestran signos de osteoartritis (OA) o que solo tienen un grado leve de OA en las articulaciones de la cadera. La colocación de implantes 3DHIP tiene como objetivo ralentizar eficazmente la progresión del deterioro de la articulación de la cadera. Se deben excluir los perros con caderas luxoides y degeneración de cadera de moderada a grave, según lo determinado en la evaluación preoperatoria.
En comparación con el implante de 3DHIP, las cirugías convencionales para tratar la displasia de cadera canina, como la DPO/TPO, presentan más desafíos, especialmente en un procedimiento bilateral en una sola etapa y/o en perros gigantes debido a su naturaleza invasiva que involucra dos o tres osteotomías pélvicas 5,6,7,26. Por lo tanto, los perros con EH bilateral pueden beneficiarse de una extensión del borde acetabular mediante un implante 3DHIP; Proporciona un procedimiento bilateral de una sola etapa eficaz y poco invasivo. Además, el implante de 3DHIP ayuda a ahorrar un tiempo valioso y puede prevenir el desarrollo posterior de la artrosis que podría ocurrir en procedimientos bilaterales de doble etapa.
Para concluir, la utilización del implante 3DHIP presentado para extender el borde acetabular dorsal es muy prometedora como tratamiento quirúrgico alternativo para la displasia de cadera en caninos. Especialmente, la opción de ofrecer un procedimiento bilateral de una sola etapa eficaz y poco invasivo para perros con displasia bilateral de cadera y laxitud es una enorme ventaja con respecto a los tratamientos alternativos actuales. Es obligatorio un seguimiento adicional de esta nueva técnica a medio y largo plazo.
Divulgaciones
Los autores no tienen conflictos de intereses que declarar. BM es uno de los cinco inventores del método de fabricación de un implante para extender el reborde acetabular dorsal (2021) cuya patente (EP3463198B1) ha sido licenciada a Rita Leibinger.
Agradecimientos
El presente estudio fue apoyado financieramente principalmente por la fundación Vrienden Diergeneeskunde Universiteit Utrecht; MT ha recibido financiación a largo plazo de la Sociedad Holandesa de Artritis (LLP22); FV y JM están financiados por el Proyecto Eurostars E115515 - 3DHIP. IK es titular de una beca de la Facultad de Medicina Veterinaria de la Universidad de Kasetsart, Tailandia.
Materiales
| Name | Company | Catalog Number | Comments |
| The laborotory for implant design | |||
| 3D Lab | University Medical Center Utrecht 3D, Utrecht, Netherlands | The laboratory responsible for designing the 3DHIP implant. [https://www.umcutrecht.nl/nl/3d-lab/] | |
| Software | |||
| 3-Matic software version 17 | Materialise, Leuven, Belgium | CT DICOM data processing | |
| Materialise Mimics software version 25.1 | Materialise, Leuven, Belgium | Software to design the 3DHIP implant on the 3D model of the pelvis | |
| Implant manufacturer | |||
| Amnovis | Amnovis, Aarschot, Belgium | Printing and postprocessing of the 3DHIP implant. [https://www.amnovis.com/] | |
| Instrument and machine | |||
| 2.4 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-224 | Titanium self tapping locking screw 2.4 mm. |
| 2.7 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-227 | Titanium self tapping locking screw 2.7 mm. |
| 3.5 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-235 | Titanium self tapping locking screw 3.5 mm. |
| BLUE SEAL 100 x 360 mm | Interster, Wormerveer, Netherlands | 3FKFB210819 | The transparent sterilization laminate size 100 x 360 mm |
| ETHILON 3-0 with FS-1 needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | 669H | Polyamide 6 3-0 (non-absorbable suture material) with 24 mm 3/8c reverse cutting needle using for skin closure |
| Fluoroscopy model NZS 229 | Philips, Eindhoven, Netherlands | Fluoroscopy | |
| Foley Catheter 10 fr x 90 cm (36") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC1036 | Foley urine catheter size 10 fr |
| Foley Catheter 6 fr x 60 cm (24") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC624 | Foley urine catheter size 6 fr |
| Foley Catheter 8 fr x 90 cm (36") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC836 | Foley urine catheter size 8 fr |
| Ioban 2 | 3M, MN, USA | 6640EU | Iodine-impregnated surgical drape |
| Miele professional G 7826 | Miele Nederland B.V., Vianen, Netherlands | The hygienic washing machine | |
| MMM sterilizer OB10643 | MMM Group, Planegg, Germany | Steam autoclave | |
| MONOCRYL 2-0 with SH Plus needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | MCP3170H | Poliglecaprone 25 plus antibacterial 2-0 (absorbable suture material) with 26 mm 1/2c taperpoint needle using for subcutaneous tissue closure |
| MONOCRYL 3-0 with SH Plus needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | MCP3160H | Poliglecaprone 25 plus antibacterial 3-0 (absorbable suture material) with 26 mm 1/2c taperpoint needle using for subcutaneous tissue closure |
| PDS 0 with CP needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | PDP485H | Polydioxanone plus antibacterial 0 (absorbable suture material) with 40 mm 1/2c reverse cutting needle using for muscle fascia and tendon closure |
| PDS 2-0 with CP-1 needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | PDP466H | Polydioxanone plus antibacterial 2-0 (absorbable suture material) with 36 mm 1/2c reverse cutting needle using for muscle fascia and tendon closure |
| ProX DMP320 | 3D systems, South Carolina, USA | Direct metal printing machine using selective laser melting technology | |
| Medications | |||
| Betadine oplossing | Mylan B.V., Amstelveen, Netherlands | RVG 01331 | Povidone-iodine solution 100 mg/mL (500 mL) |
| Betadine shampoo | Mylan B.V., Amstelveen, Netherlands | RVG 08943 | Povidone-iodine 75 mg/mL (120 mL) |
| Carporal 20 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 101766 | Carprofen 20 mg/tablet |
| Carporal 40 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 115715 | Carprofen 40 mg/tablet |
| Carporal 50 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 101767 | Carprofen 50 mg/tablet |
| Cefazolin Mylan 1 g | Mylan B.V., Amstelveen, Netherlands | RVG 16532 | Cefazolin powder 1 g for injection |
| Chlorhexidine 0.5% in alcohol 70% spray | Orphi Farma BV, Lage Zwaluwe, Netherlands | 8711407672906 | Chlorhexidine 0.5% in alcohol 70% spray (250 mL) |
| Dexdomitor 0.5 mg/mL | Orion Corporation, Espoo, Finland | EU/2/02/033/001-002 | Dexmedetomidine hydrochloride 0.5 mg/mL for injection (20 mL) |
| Gabapentin Sandoz 300 mg | Sandoz B.V., Almere, Netherlands | RVG 33681 | Gabapentin 300 mg/capsule |
| GABAPENTINE TEVA 100 mg | Teva B.V., Haarlem, Netherlands | RVG 31980 | Gabapentin 100 mg/capsule |
| HiBiScrub | Mölnlycke Health Care AB., Utrecht, Netherlands | RVG 10156 | Chlorhexidine digluconate 40 mg/mL (500 mL) |
| Insistor 10 mg/mL | Richter pharma AG, Oostenrijk, Netherlands | REG NL 121166 | Methadone hydrochloride 10 mg/mL for injection (10 mL) |
| Isoflutek 1000 mg/g | Laboratorios Karizoo S.A., Barcelona, Spain | REG NL 118938 | Isoflurane 1000 mg/g (250 mL) |
| Levobupivacaine Fresenius Kabi 2.5 mg/mL | Fresenius Kabi Nederland b.v., Huis ter Heide, Netherlands | AWA 0611 | Levobupivacaine 2.5 mg/mL solution for injection (10 mL) |
| Morfine HCI CF 10 mg/mL | Centrafarm B.V., Breda, Netherlands | RVG 50836 | Morphine hydrochloride 10 mg/mL (1 mL) |
| Narketan 10 | Vetoquinol B.V., Breda, Netherlands | vm08007/4090 | Ketamine 10 mg/mL (10 mL) |
| Propofol 10 mg/mL | Fresenius Kabi Nederland b.v., Huis ter Heide, Netherlands | RVG 110627 | Propofol 10 mg/mL emulsion for injection or infusion (50 mL) |
| Rimadyl | Zoetis B.V., Capelle a/d Ijssel, Netherlands | REG NL 10101 | Carprofen 50 mL/mL for injection (20 mL) |
| Sufentanil-hameln 50 mcg/mL | Hameln pharma gmbh, Hameln, Germany | 4260016653249 | Sufentanil citrate 50 mcg/mL for injection |
| Trazadone EG 100 mg | EG (Eurogenerics) NV Heizel, Brussel, Belgium | BE439607 | Trazadone hydrochloride 100 mg/tablet |
Referencias
- King, M. D. Etiopathogenesis of canine hip dysplasia, prevalence, and genetics. Vet Clin North Am Small Anim Pract. 47 (4), 753-767 (2017).
- Akis, I., et al. The association of genetic polymorphisms of bone formation genes with canine hip dysplasia. Iran J Vet Res. 21 (1), 40-45 (2020).
- Loder, R. T., Todhunter, R. J. The demographics of canine hip dysplasia in the United States and Canada. J Vet Med. 2017, 1-15 (2017).
- Schachner, E. R., Lopez, M. J. Diagnosis, prevention, and management of canine hip dysplasia: a review. Vet Med (Auck)l. 6, 181-192 (2015).
- Vezzoni, A., Boiocchi, S., Vezzoni, L., Vanelli, A. B., Bronzo, V. Double pelvic osteotomy for the treatment of hip dysplasia in young dogs). Vet Comp Orthop Traumatol. 23 (6), 444-452 (2010).
- Tavola, F., Drudi, D., Vezzoni, L., Vezzoni, A. Postoperative complications of double pelvic osteotomy using specific plates in 305 dogs. Vet Comp Orthop Traumatol. 35 (1), 47-56 (2022).
- Koch, D. A., Hazewinkel, H. A. W., Nap, R. C., Meij, B. P., Wolvekamp, W. T. C. Radiographic evaluation and comparison of plate fixation after triple pelvic osteotomy in 32 dogs with hip dysplasia. Vet Comp Orthop Traumatol. 06 (01), 09-15 (1993).
- Rose, S. A., Bruecker, K. A., Petersen, S. W., Uddin, N. Use of locking plate and screws for triple pelvic osteotomy. Vet Surg. 41 (1), 114-120 (2012).
- Remedios, A. M., Fries, C. L. Implant complications in 20 triple pelvic osteotomies. Vet Comp Orthop Traumatol. 06 (04), 202-207 (1993).
- Moses, P. A. Alternative surgical methods for treating juvenile canine hip dysplasia. Aust Vet J. 78 (12), 822-824 (2000).
- Harper, T. A. M. Femoral head and neck excision. Vet Clin North Am Small Anim Pract. 47 (4), 885-897 (2017).
- Forster, K. E., et al. Complications and owner assessment of canine total hip replacement: a multicenter internet based survey. Vet Surg. 41 (5), 545-550 (2012).
- Volstad, N. J., Schaefer, S. L., Snyder, L. A., Meinen, J. B., Sample, S. J. Metallosis with pseudotumour formation: Long-term complication following cementless total hip replacement in a dog. Vet Comp Orthop Traumatol. 29 (4), 283-289 (2016).
- Nesser, V. E., Kowaleski, M. P., Boudrieau, R. J. Severe polyethylene wear requiring revision total hip arthroplasty in three dogs. Vet Surg. 45 (5), 664-671 (2016).
- Verhoeven, G., Fortrie, R., Van Ryssen, B., Coopman, F. Worldwide screening for canine hip dysplasia: where are we now. Vet Surg. 41 (1), 10-19 (2012).
- Willemsen, K., et al. Patient-specific 3D-printed shelf implant for the treatment of hip dysplasia: Anatomical and biomechanical outcomes in a canine model. J Orthop Res. 40 (5), 1154-1162 (2021).
- Willemsen, K., et al. Patient-specific 3D-printed shelf implant for the treatment of hip dysplasia tested in an experimental animal pilot in canines. Sci Rep. 12 (1), 3032 (2022).
- Kwananocha, I., et al. Acetabular rim extension using a personalized titanium implant for treatment of hip dysplasia in dogs: short-term results. Front Vet Sci. 10, 1160177 (2023).
- Van Der Wal, B. C. H., Sakkers, R. J. B., Meij, B. P., Evers, L. A. M., Weinans, H. H. . Method of manufacturing an implant. EP3463198B1. , (2021).
- Brainard, B. M., Hofmeister, E. H. Anesthesia principles and monitoring. Small Animal Surgery. , (2012).
- Martinez-Taboada, F., Redondo, J. I. Comparison of the hanging-drop technique and running-drip method for identifying the epidural space in dogs. Vet Anaesth Analg. 44 (2), 329-336 (2017).
- Johnson, K. A. Approach to the craniodorsal aspect of the hip joint through a craniolateral incision in the dog. Piermattei's Atlas of Surgical Approaches to the Bones and Joints of the dog and cat. , (2014).
- Whitelock, R. G., Dyce, J., Houlton, J. E. Repair of femoral trochanteric osteotomy in the dog. J Small Anim Pract. 38 (5), 195-199 (1997).
- Silveira, C. J., Saunders, W. B. Greater trochanter osteotomy as a component of cementless total hip replacement: Five cases in four dogs. Vet Surg. 51 (2), 303-310 (2022).
- Archibeck, M. J., Rosenberg, A. G., Berger, R. A., Silverton, C. D. Trochanteric osteotomy and fixation during total hip arthroplasty. J Am Acad Orthop Surg. 11 (3), 163-173 (2003).
- Vezzoni, A. Complications of double and triple pelvic osteotomies. Complications in Small Animal Surgery. , (2016).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados