Estandarización de un novedoso software semiautomático para la medición del crecimiento de neuritas
* Estos autores han contribuido por igual
En este artículo
Resumen
Los ensayos de excrecencia de neuritas proporcionan un valor cuantitativo sobre los procesos neuronales regenerativos. La ventaja de este software semiautomático es que segmenta los cuerpos celulares y las neuritas por separado mediante la creación de una máscara y mide varios parámetros, como la longitud de las neuritas, el número de puntos de ramificación, el área del grupo de cuerpos celulares y el número de grupos celulares.
Resumen
Las técnicas efectivas de imagen en vivo son cruciales para evaluar la morfología neuronal con el fin de medir el crecimiento de neuritas en tiempo real. La medición adecuada del crecimiento de neuritas ha sido un desafío de larga data a lo largo de los años en el campo de la investigación en neurociencia. Este parámetro sirve como piedra angular en numerosas configuraciones experimentales in vitro , que van desde cultivos disociados y cultivos organotípicos hasta líneas celulares. Al cuantificar la longitud de la neurita, es posible determinar si un tratamiento específico funcionó o si se potencia la regeneración axonal en diferentes grupos experimentales. En este estudio, el objetivo es demostrar la robustez y precisión del software de análisis de crecimiento de neuritas Incucyte Neurotrack. Este software semiautomático está disponible en un sistema de microscopía de lapso de tiempo que ofrece varias ventajas sobre las metodologías comúnmente utilizadas en la cuantificación de la longitud de la neurita en imágenes de contraste de fase. El algoritmo enmascara y cuantifica varios parámetros en cada imagen y devuelve métricas de células neuronales, incluida la longitud de las neuritas, los puntos de ramificación, los grupos de cuerpos celulares y las áreas de grupos de cuerpos celulares. En primer lugar, validamos la robustez y precisión del software correlacionando sus valores con los del manual NeuronJ, un plug-in de Fiji. En segundo lugar, utilizamos el algoritmo que es capaz de trabajar tanto en imágenes de contraste de fase como en imágenes de inmunocitoquímica. Utilizando marcadores neuronales específicos, validamos la viabilidad del análisis de crecimiento de neuritas basado en fluorescencia en neuronas sensoriales en cultivos in vitro . Además, este software puede medir la longitud de las neuritas en diversas condiciones de siembra, que van desde células individuales hasta redes neuronales complejas. En conclusión, el software proporciona una plataforma innovadora y eficaz en el tiempo para los ensayos de crecimiento de neuritas, allanando el camino para cuantificaciones más rápidas y fiables.
Introducción
En los nervios ciáticos, es posible medir la regeneración axonal1. Además, estudios in vitro han demostrado la viabilidad de monitorizar el crecimiento axonal 2,3 para comprender sus diversas fases, desde la brotación axonal hasta la degeneración axonal, tanto en neuronas sanas como lesionadas. Mediante el seguimiento de estos procesos, es posible medir parámetros como la polaridad axonal, la iniciación, la estabilidad y la ramificación. Este último parámetro es crucial para entender la percepción del dolor neuropático 4,5,6. Del mismo modo, la degeneración axonal puede ser monitorizada in vivo7 o in vitro 8,9. Durante el crecimiento de las neuritas, las redes de citoesqueletos de actina y microtúbulos se estabilizan o cambian de acuerdo con las necesidades de la célula10. El citoesqueleto de actina se reorganiza para permitir la formación del cono de crecimiento axonal, y los microtúbulos se realinean en haces para estabilizar la neurita en crecimiento11. Con el fin de estudiar el crecimiento de las neuronas centrales y periféricas in vitro, se cuantifican tres parámetros comunes: longitud axonal total, distancia máxima y puntos de ramificación. Estos parámetros se utilizan para estudiar la respuesta de crecimiento neuronal al tratamiento (i.e., neurotrofinas, compuestos, inhibidores, ácido retinoico, siRNA, shRNA) o en animales modificados genéticamente 12,13,14. Para evaluar si las neuronas tienen neuritas más alargadas y/o más ramificadas, estos tres parámetros permiten evaluar la morfología de una neurona. La medición de la longitud de las neuritas es el parámetro de mayor interés en varios montajes experimentales in vitro. A partir de los ganglios de la raíz dorsal, se realizan principalmente dos tipos de cultivos: cultivo in vitro disociado o cultivo organotípico de explantes enteros de DRG. En cualquier caso, la longitud de la neurita es un parámetro de oro para evaluar el resultado del experimento. En una línea celular similar a una neurona motora (NSC-34), se mide el crecimiento axonal y la ramificación después de la diferenciación inducida por el ácido retinoico15,16. De hecho, al medir el crecimiento de las neuritas, es posible determinar si un tratamiento específico ha funcionado17, la tasa de crecimiento18 o la capacidad de regeneración después de un procedimiento de lesión19.
La forma de evaluar adecuadamente el crecimiento de las neuritas ha planteado un número significativo de desafíos a lo largo de los años en el campo de la investigación. Sin embargo, no existe una estandarización de las mediciones de la longitud de las neuritas. Algunos de los métodos más utilizados para el cultivo celular in vitro son, por ejemplo, el plug-in manual NeuronJ en Fiji18,20 o MetaMorph21,23 y el semiautomático Neurolucida23,24. Además de las metodologías manuales, también existen métodos automáticos, como el plug-in NeuriteTracer en Fiji25, el software HCA Vision26,27 o WIS-NeuroMath 2,28. Otras metodologías menos precisas se basan en la medición de la dimensión general de las neuronas. Estos métodos incluyen la medición de la distancia vectorial desde el cuerpo de la célula hasta la punta del axónmás largo 29 o el análisis de Sholl30. Sin embargo, estos métodos de medición son adecuados para cultivos de muy baja densidad o neuronas individuales. Además, todas estas metodologías se utilizan principalmente en neuronas teñidas o neuronas que expresan fluoróforos codificados genéticamente (es decir, GFP, Venus, mCherry). El tipo de neurona y la densidad del cultivo celular afectan profundamente a la elección de la metodología de medición. Por ejemplo, segmentar manualmente neuronas con morfologías muy intrincadas y complicadas, como las neuronas DRG, puede convertirse fácilmente en una tarea imposible. Si las neuronas enrevesadas ya son un desafío para segmentar, las redes neuronales están completamente fuera del alcance de los enfoques manuales debido a su organización altamente compleja.
Por un lado, la segmentación manual es muy precisa porque la realizan los ojos y la inteligencia humanos; Por otro lado, lleva mucho tiempo. El elevado gasto de tiempo requerido por los métodos manuales es el principal inconveniente. Por esta razón, solo se adquieren unas pocas neuronas para el análisis, lo que lo hace menos preciso y costoso en términos de tiempo. Los enfoques automáticos o semiautomáticos, por otro lado, reducen parcialmente el gasto de tiempo. Sin embargo, también tienen algunas desventajas. Los métodos automáticos necesitan ser entrenados para que funcionen correctamente, y si el software no es lo suficientemente interactivo con el usuario, la segmentación puede ser incorrecta.
Además de la medición del crecimiento de neuritas, el número de puntos de ramificación también es información valiosa. Con la segmentación manual, se puede calcular el número de puntos de bifurcación, mientras que esto no es posible con una distancia vectorial. Con los métodos automáticos, generalmente se proporciona el número de puntos de bifurcación, mientras que con el análisis de Sholl, debe calcularse con una fórmula matemática.
En este artículo de métodos, nuestro objetivo es describir la funcionalidad y efectividad de este software semiautomático en la medición de la longitud axonal total y otros parámetros. La máquina permite la adquisición automática de imágenes en puntos de tiempo definidos o para la realización de estudios a largo plazo (días, semanas, meses), preservando un entorno fisiológico para las células vivas. La medición del crecimiento de las neuritas mediante imágenes de lapso de tiempo de contraste de fase tiene la ventaja de permitir un monitoreo continuo de la cinética y el crecimiento de las neuritas. Además, también es posible monitorear la muerte celular a través de la adición en los medios de colorantes específicos que se dirigen a las células muertas 31,32,33. Aunque el software se lanzó en 2012, somos los primeros en estandarizar esta metodología de forma reproducible e imparcial para la cuantificación precisa del crecimiento de neuritas. Sin embargo, es importante tener en cuenta que el software no está incluido con la compra de la máquina. A pesar de este gasto adicional, su uso ofrece ventajas significativas en la medición de la longitud axonal total y otros parámetros, contribuyendo así a la investigación en el campo de la neurociencia.
Protocolo
1. Escaneo del recipiente en la máquina
NOTA: La detección se realiza mediante la cámara Basler Ace 1920-155 μm incorporada.
- Abra el programa haciendo clic en Conectar al dispositivo y seleccionando Programar - Adquirir. A continuación, haga clic en el signo + .
- Especifique si el buque se escaneará repetidamente o solo 1 vez eligiendo la opción Escanear a tiempo o Escanear una vez ahora, respectivamente.
- Seleccione Nuevo para crear un recipiente completamente nuevo para escanear. Si no se agrega un nuevo recipiente, cree un nuevo escaneo utilizando una de las opciones que se describen a continuación.
- Seleccione Copiar actual para crear una nueva embarcación copiando una embarcación de la programación actual. Seleccione Copiar anterior para crear una nueva embarcación copiando una embarcación escaneada anteriormente.
- Seleccione Agregar escaneo para restaurar un recipiente escaneado previamente para escaneos adicionales.
- Seleccione el tipo de escaneo en función del ensayo y la aplicación. Para el análisis, seleccione Estándar.
- Especifique la configuración de análisis. Elija una de las opciones Célula por célula, ya sea Ninguna, Célula adherente por célula o Célula por célula no adherente, y especifique los canales de imagen en función de las moléculas fluorescentes utilizadas. Seleccione la opción Ninguno para cultivos de neuronas sensoriales adultas y embrionarias. En las líneas de celda, seleccione las opciones Ninguno o Célula por celda adherente .
- Seleccione el objetivo del microscopio (4x, 10x, 20x). Se adquieren con el aumento más alto (20x) en cultivos primarios, mientras que en líneas celulares, 10x es suficiente.
- Seleccione el tipo de recipiente que desea escanear de las opciones proporcionadas. Indique la ubicación de la embarcación en el cajón seleccionando su posición en el mapa virtual del cajón.
- Especifique el patrón de escaneo para la adquisición de imágenes seleccionando los pocillos que desea escanear. Seleccione el número deseado de imágenes por pocillo. Aparecerá una estimación de la duración del escaneo.
- Proporcione información sobre el buque escribiendo el nombre y especifique el mapa de la placa haciendo clic en el signo + .
- Haga clic en Siguiente. Elija el Tipo de análisis y haga clic en Siguiente. Aparecerá una pantalla de resumen de las opciones seleccionadas. Si es correcto, haga clic en Escanear ahora y se iniciará el escaneo.
2. Configuración para el análisis de imágenes de contraste de fase
NOTA: El análisis de Neurotrack solo se puede realizar en imágenes previamente adquiridas por la máquina.
- Seleccione el recipiente escaneado que desea analizar. Seleccione Iniciar análisis. Seleccione Crear nueva definición de análisis.
- Selecciona Neurotrack. Seleccione Canales de imagen. Seleccione un conjunto representativo de imágenes para realizar el análisis. Seleccione todas las imágenes de cada pozo para entrenar el algoritmo.
- Refine la configuración de Definición de análisis ajustando los siguientes parámetros.
NOTA: De forma predeterminada, las neuritas están segmentadas en magenta, mientras que los cuerpos celulares en amarillo. Es posible modificar los colores como se desee.- Para la segmentación de clústeres de cuerpos de celdas, ajuste lo siguiente como se describe a continuación.
- Modo de segmentación: La segmentación de las imágenes se realiza para distinguir los cuerpos celulares del fondo y las neuritas. Elige entre Brillo y Textura. Para cultivos primarios y líneas celulares, seleccione el modo de brillo.
- Ajuste de segmentación: Utilice el control deslizante para ajustar la sensibilidad de segmentación hacia más fondo o más celdas. Oscila entre 0 (Fondo) y 2 (Celdas). Aumenta o disminuye el tamaño de la mascarilla amarilla. Mueva el control deslizante hacia 0 (Fondo) para que el tamaño de la máscara amarilla se reduzca gradualmente, dejando espacio para la máscara magenta. Lo contrario ocurre si el control deslizante se mueve hacia 2 (celdas).
- Para la limpieza, ajuste lo siguiente como se describe a continuación.
- Relleno de agujero (μm2): Ajústelo para eliminar cualquier agujero en la máscara del cuerpo de la célula más pequeño que el área especificada por el usuario.
- Ajustar tamaño (píxeles): Aumente (si es positivo) o reduzca (si es negativo) la máscara amarilla en el número especificado de píxeles. Oscila entre -10 y +10. Ajuste esto para agregar o eliminar la segmentación amarilla en los objetos de alto contraste, como las células muertas y los desechos celulares.
- Ancho mínimo de la célula (μm): elija un valor para definir el tamaño en el que los cuerpos de las células se considerarán como neuritas.
- En el caso de los filtros de clúster de cuerpo de celda, ajuste lo siguiente como se describe a continuación.
- Área (μm2): Establezca un valor mínimo y máximo del área del cuerpo de la célula. Los valores por encima y por debajo de los valores establecidos no se considerarán cuerpos de celda.
- Para los parámetros de neurita, ajuste lo siguiente como se describe a continuación.
- Filtrado: Reduce el enmascaramiento de pequeñas imperfecciones y residuos de vasos. Elija entre las opciones Ninguno, Mejor y Mejor. Elija Ninguno solo para cultivos y recipientes muy limpios. Elija Mejor para un procesamiento más rápido a expensas de perder la detección de neuritas muy finas. Puede ser suficiente para células con neuritas gruesas o de alto contraste; Además, puede ser útil para embarcaciones con muchas imperfecciones o desechos. Elija Mejor para un tiempo de procesamiento más prolongado, pero es la configuración de filtro más sensible para garantizar la detección de neuritas muy finas.
- Sensibilidad de las neuritas: Se utiliza para ajustar la sensibilidad de detección. Aumente la sensibilidad para detectar neuritas más finas. Oscila entre 0,25 (menos) y 0,75 (más).
NOTA: Aumenta o disminuye la sensibilidad del software para reconocer neuritas. Si el control deslizante se mueve hacia 0,25 (menos), el software será más estricto en su reconocimiento de neuritas. En cambio, si el control deslizante se mueve hacia 0.75 (Más), el software será menos estricto en esta detección y, por lo tanto, más imperfecciones (es decir, restos de celdas, suciedad) se considerarán neuritas. - Ancho de la neurita (μm): Utilícelo para ajustar la detección al tamaño de las neuronas. Puede ser 1, 2 o 4. Al aumentarlo, no se considerarán las neuritas más delgadas. Establézcalo en 1 para cultivos de neuronas sensoriales adultas primarias y 2 para líneas celulares y cultivos de neuronas sensoriales embrionarias.
- Para la segmentación de clústeres de cuerpos de celdas, ajuste lo siguiente como se describe a continuación.
- Haga clic en Vista previa actual para visualizar la imagen segmentada. Se proporcionarán las siguientes medidas para cada imagen: Longitud de la neurita (mm/mm2), Puntos de ramificación de la neurita (pormm2), Grupos de cuerpo celular (pormm2) y Área del grupo de cuerpo celular (mm2/mm2).
- Repita los pasos 2.3 y 2.4 para todas las imágenes seleccionadas. Haga clic en Siguiente.
- Seleccione el tiempo de escaneo y el pozo para analizar. Asigne un Nombre de Definición y, si es necesario, Notas de Análisis. Haga clic en Siguiente > Finalizar.
3. Configuración para el análisis de imágenes de inmunocitoquímica (ICC)
- Siga los mismos pasos que se ilustran de la versión 2.1 a la 2.4. Seleccione los canales de imagen para neuritas y núcleos. Seleccione el Conjunto de imágenes; seleccione Todas las imágenes de cada pozo para entrenar el algoritmo.
- Perfeccione la configuración de Definición de análisis ajustando los siguientes parámetros, tal y como se describe a continuación.
NOTA: De forma predeterminada, las neuritas están segmentadas en azul, mientras que los cuerpos celulares son morados. Sin embargo, los colores se pueden modificar como se desee.- Segmentación de clústeres de cuerpos celulares: utilícela para segmentar la imagen en objetos de interés. Calcule el brillo del fondo en cada píxel de la imagen. Una vez encontrado el fondo, realice una de las siguientes opciones.
- Sin sustracción de fondo: Utilícelo para segmentar sin alterar la imagen original. Elija entre Umbral adaptable o Fijo. Adaptativo: el fondo se utiliza para encontrar objetos, pero no se resta explícitamente; con esta opción, es posible establecer el ajuste de umbral (GCU). Umbral fijo: los objetos que son más brillantes que este umbral se detectan en la imagen original; con esta opción, es posible establecer el umbral (GCU).
- Resta de fondo: usa esta opción para restar el fondo de la imagen mediante una transformación de Top-Hat y, a continuación, aplicarle un umbral. Con esta opción, establezca Radio y Umbral. Radio: se utiliza un disco de este radio; El disco debe ser lo suficientemente grande como para que no quepa completamente dentro de ningún objeto de la imagen. Umbral: los objetos que son más brillantes que este umbral se detectan en la imagen sustraída por el fondo.
- Limpieza: Utilice la siguiente opción para realizar esto.
- Relleno de agujeros (μm2): Utilícelo para eliminar los agujeros de la máscara del cuerpo de la célula que sean más pequeños que el área especificada.
- Ajustar tamaño (píxeles): Utilícelo para aumentar (si es positivo) o reducir (si es negativo) la máscara púrpura en el número especificado de píxeles. El rango es de -10 a +10. Agrega o elimina el púrpura en objetos de alto contraste, como células muertas y desechos celulares.
- Ancho mínimo de la célula (μm): Utilícelo para definir el tamaño en el que los cuerpos de las células se considerarán como neuritas.
- Filtros de clúster de cuerpo de celda: utilice la siguiente opción para aplicar los filtros.
- Área (μm2): Establezca un valor mínimo y máximo del área del cuerpo de la célula. Los valores por encima y por debajo de los valores establecidos no se considerarán cuerpos de celda.
- Parámetros de Neurite: Utilice la siguiente opción para establecerlos.
- Sensibilidad gruesa de la neurita: Utilícela para ajustar el brillo de la neurita. La sensibilidad debe aumentarse si la intensidad de fluorescencia de las neuritas es baja. Va de 0 (Menos) a 10 (Más). Aumenta o disminuye la sensibilidad del software para reconocer neuritas menos brillantes. Los valores óptimos oscilan entre 7 y 10; Tenga en cuenta que si se establece en 10, es muy probable que también se considere el fondo en la medición de la neurita.
- Sensibilidad fina de la neurita: Utilícela para ajustar la sensibilidad de detección. Se debe aumentar la sensibilidad para detectar neuritas más finas. Oscila entre 0,25 (menos) y 0,75 (más). Aumenta o disminuye la sensibilidad del software para reconocer neuritas finas y menos brillantes. Si el control deslizante se mueve hacia 0,25 (menos), el software no tendrá en cuenta las neuritas débiles. En cambio, si el control deslizante se mueve hacia 0.75 (Más), el software detectará también neuritas muy tenues (casi de fondo).
- Anchura de la neurita (μm): Utilícela para ajustar la detección al tamaño de las neuronas. Puede ser 1, 2 o 4. Al aumentarlo, no se considerarán las neuritas más delgadas. Configúrelo en 1 para cultivos de neuronas sensoriales adultas primarias, en 2 para líneas celulares y cultivos de neuronas sensoriales embrionarias.
- Segmentación de clústeres de cuerpos celulares: utilícela para segmentar la imagen en objetos de interés. Calcule el brillo del fondo en cada píxel de la imagen. Una vez encontrado el fondo, realice una de las siguientes opciones.
4. Exportación de datos
- Abra el análisis. Haga clic en Métricas gráficas.
- Seleccione la métrica, los puntos de tiempo y los pozos de interés.
- Seleccione la opción de agrupación entre Todo, Ninguno, Columnas, Filas y Réplicas de mapa de placas.
- Haga clic en Exportar datos y seleccione la carpeta de destino y, si es necesario, otras opciones. Se creará un archivo .txt.
NOTA: La máquina proporcionará un único valor promedio de la métrica elegida para cada pozo. Se requiere una anotación manual durante el análisis para recuperar valores de imagen individuales.
5. Exportación de imágenes
- Abra el recipiente. Haga clic en Exportar imágenes y películas.
- Seleccione el tipo de exportación para las imágenes.
- Seleccione Como se muestra para exportar las imágenes tal como se muestran. Haga clic en Siguiente y seleccione las imágenes de interés para exportar. Haga clic en Siguiente.
- Seleccione el Tipo de secuencia entre una sola película o serie de imágenes y los puntos de tiempo de interés. Haga clic en Siguiente.
- Ajuste las opciones de exportación según sea necesario y haga clic en Siguiente. Establezca la carpeta de salida, el formato de archivo y el nombre del archivo y, a continuación, haga clic en Exportar.
- Seleccione Como almacenado para exportar imágenes en formato RAW. Seleccione el tipo de imagen.
- Seleccione los puntos de tiempo y los pozos de interés. Haga clic en Siguiente. Establezca la carpeta de salida, el formato de archivo y el nombre del archivo y, a continuación, haga clic en Exportar.
- Seleccione Como se muestra para exportar las imágenes tal como se muestran. Haga clic en Siguiente y seleccione las imágenes de interés para exportar. Haga clic en Siguiente.
- Exportación de imágenes con las máscaras de segmentación
- Abra el análisis. Haga clic en el icono de Capas de imagen. Seleccione las máscaras de canales deseadas (Fase Neurita y Fase Célula de Agrupación de Cuerpos). Siga el paso 5.2.
Resultados
El algoritmo de medición del crecimiento de neuritas es robustamente capaz de detectar neuritas tanto en redes neuronales como en neuronas individuales. Genera una máscara amarilla que segmenta objetos con alto contraste, como cuerpos celulares, restos celulares, células muertas, explantes de tejido y sombras. Además, aparece una máscara magenta en neuritas de varios grosores. Los valores de longitud de la neurita se proporcionan en mm/mm2, lo que indica que la longitud axonal se ha dividido por el área de la imagen, que es 0,282739 mm2 y constante para cada condición de escaneo. Por lo tanto, para obtener valores puros de la longitud de la neurita en mm, los números proporcionados por el software deben multiplicarse por el área de la imagen.
Método semiautomático frente a manual
El software utilizado es una metodología semiautomática para medir la longitud axonal total. Para evaluar la precisión del software, realizamos mediciones en las mismas neuronas utilizando el método manual con el complemento NeuronJ. Como se muestra en la Figura 1, la máscara de segmentación en las neuronas es muy similar entre los dos métodos (Figura 1A).
Además, se realizó un análisis estadístico de los valores obtenidos para examinar su correlación. El análisis de correlación de Spearman arrojó un alto coeficiente r de 0,8526, lo que proporciona una fuerte evidencia de la exactitud y precisión del algoritmo (Figura 1B). La medición automática requiere altos estándares de calidad del cultivo basados en su limpieza, densidad y pureza. Los resultados obtenidos con la segmentación semiautomática son reproducibles y no se ven afectados por el juicio individual. La reproducibilidad imparcial es un problema para las metodologías manuales.
A veces, pueden ocurrir errores de segmentación semiautomáticos debido a diferentes causas. En las imágenes de contraste de fase, la suciedad en el cultivo pudo ser detectada como neuritas por la segmentación semiautomática. Además, la presencia de diferentes tipos de células puede perturbar el proceso de segmentación. Estos problemas no surgen con la segmentación manual porque la realizan los ojos humanos. No obstante, si surgen estos problemas, pueden superarse mediante el uso de imágenes inmunocitoquímicas como control.
Segmentación de neuritas
En el caso de los cultivos primarios de neuronas DRG adultas, el punto de partida óptimo para un análisis de fase fiable es tener las neuronas colocadas uniformemente en el pozo y limpiarlas. Si se producen errores durante la siembra y las células se concentran en un punto, como se ilustra en la Figura 2A-B, los valores serán más una estimación que un reflejo cercano de la realidad. En tales situaciones, la máscara amarilla cubrirá la mayoría de las neuritas entre las células (Figura 2A-B), lo que resultará en la pérdida de longitud de la neurita. Además, el software estará significativamente sesgado en el reconocimiento de neuritas, y es muy probable que aparezca una máscara magenta en objetos que no son neuritas (Figura 2D). En una imagen óptima, debe haber hasta 15 neuronas con un aumento de 20x.
Cuando las neuronas están correctamente plateadas y el cultivo está limpio, como se ilustra en la Figura 3A-B, es aconsejable ajustar el control deslizante de segmentación hacia el fondo (0,5 - 0,7; Figura 3C). Esto ayuda a reducir el componente amarillo que aparecerá en los objetos de alto contraste de la imagen, como los puntos de ramificación que deberían estar en magenta. Además, si las neuritas son negritas, una sensibilidad de las neuritas entre 0,4 y 0,5 debería ser suficiente para cubrir la mayoría de ellas (Figura 3C-D).
Otra situación común que puede surgir es un cultivo sucio con muchos restos celulares y células muertas, como se muestra en la Figura 4A-B. En tales condiciones, hay muchos objetos de alto contraste. Por lo tanto, es aconsejable aumentar el tamaño de la máscara amarilla ajustando el control deslizante de segmentación hacia la celda o aumentando el parámetro ajustar tamaño (+1, +2, etc.; Figura 4C). No obstante, también sería útil disminuir ligeramente la sensibilidad de las neuritas para evitar que el software identifique incorrectamente como neuritas objetos que no son neuritas como tales. (Figura 4C-D).
A veces, las neuritas pueden parecer muy delgadas y pálidas, como se muestra en la Figura 5A-B, lo que plantea desafíos para que el software las segmente con precisión (Figura 5D). En este caso, es aconsejable aumentar la sensibilidad de las neuritas al menos a 0,6 (Figura 5C). Sin embargo, hay que tener en cuenta que cuanto mayor sea la sensibilidad, mayor será la probabilidad de que el software marque incorrectamente los objetos que no son neuritas como tales (Figura 5D). Se pueden tomar algunas precauciones para evitar que el sesgo de sensibilidad aumente demasiado, por ejemplo, ajustando el control deslizante de segmentación hacia las celdas. Sin embargo, si las neuritas son demasiado delgadas para ser detectadas por el software, los valores de longitud de las neuritas estarán sesgados independientemente.
En el caso de las imágenes de inmunocitoquímica, el problema principal está en el fondo. Aparte de las condiciones de siembra para las que se aplican las reglas antes mencionadas, la principal fuente de sesgo es la propia fluorescencia. El software reconoce eficazmente las neuritas muy brillantes, mientras que las neuritas más delgadas y menos intensas se quedan atrás (Figura 6A-B). Para evitar la pérdida de longitud de la neurita, la sensibilidad fina de la neurita se puede aumentar hasta 0,75 (Figura 6C). Sin embargo, es muy recomendable reducir la sensibilidad gruesa de la neurita al menos a 8-9 para evitar un sesgo de detección excesivo considerando las neuritas en el fondo (Figura 6C-D). Si este último no se reduce, todo el fondo se segmentará, como se muestra en la Figura 7.
Un problema común con la adquisición de fluorescencia es la dispersión de la luz. A menudo, las imágenes de inmunocitoquímica presentan linternas en la imagen, lo que afecta significativamente la calidad y precisión del análisis (Figura 8A-B). En tal situación, no se puede hacer mucho para mejorar el análisis, y los valores serán más una estimación. La dispersión de la luz interfiere con el reconocimiento de las neuritas, por lo que solo se detectarán las neuritas muy brillantes (Figura 8C-D). Otro problema en las imágenes de inmunocitoquímica es la calidad de la tinción per se. Con frecuencia, debido a errores humanos, los axones pueden romperse (Figura 9A) y los cuerpos celulares pueden ser arrancados durante los lavados (Figura 9B). Estos errores plantean un problema crítico, ya que los valores de longitud de las neuritas pierden precisión y exactitud. En consecuencia, se altera la interpretación de los datos biológicos, lo que lleva a conclusiones erróneas.
En el caso de los cultivos embrionarios, la situación es diferente. En este tipo de cultivo predomina la presencia de células gliales. En consecuencia, los errores aumentan significativamente ya que el software también detecta los revestimientos de las células gliales (Figura 10A-B). Para minimizar este problema, el control deslizante de segmentación debe moverse hacia las celdas, normalmente alrededor de valores de 1,7-2 (Figura 10C-D). Este enfoque asegura que la mayoría de las células gliales estén cubiertas por la máscara amarilla y, por lo tanto, no se consideren en la medición de la longitud de la neurita. Otro consejo útil es mantener la anchura de la neurita en 2, ya que las neuronas embrionarias en cultivo suelen presentar formas bipolares o unipolares con neuritas gruesas (Figura 10C-D). Esta precaución filtra la mayoría de los revestimientos de las células gliales que suelen ser muy finos. Por último, tenga cuidado de no aumentar demasiado la sensibilidad de las neuritas; De lo contrario, lo que se ha filtrado por el parámetro de ancho de neurita se incluirá nuevamente en la medición de longitud de neurita.
En el caso de los cultivos embrionarios, donde predomina el componente de las células gliales, la inmunocitoquímica podría ser la mejor opción. Al teñir específicamente las neuronas, se resuelve el problema de la segmentación de la glía, ya que la glía no se tiñe, lo que hace que el análisis sea mucho más fácil y preciso (Figura 11).
Por último, el software también puede ser explotado para evaluar el programa de diferenciación de líneas celulares y/o iPSCs para evaluar su estado de crecimiento. Por lo tanto, la aplicación de parámetros y precauciones similares se puede utilizar para diferentes objetivos.
En cuanto al proceso de diferenciación, se ha demostrado la robustez del software en la línea celular NSC-34 (línea celular híbrida constituida por células de neuroblastoma de ratón y motoneuronas derivadas de la médula espinal de embriones de ratón) durante la maduración en células similares a las motoneuronas. En cuanto a los cultivos primarios de DRG, el punto de partida óptimo para un buen análisis es la siembra celular uniforme. Las células indiferenciadas y diferenciadas, tras el tratamiento con ácido retinoico, pueden seguirse mediante adquisiciones durante todo el período de cultivo o, como se muestra en la Figura 12, en el último punto de tiempo.
De hecho, además de la longitud de la neurita, el algoritmo también proporciona el parámetro del punto de bifurcación. Sin embargo, es importante tener en cuenta que el parámetro de punto de bifurcación no representa el número exacto de puntos de bifurcación; más bien, indica la densidad de ramificación en la imagen tal como se expresa en mm/mm2. Esta medición está significativamente influenciada por los residuos en el cultivo y la concentración de siembra. Por lo tanto, la densidad de neuronas en la imagen y la limpieza del cultivo son factores cruciales para obtener valores fiables. Si el cultivo presenta muchos restos celulares, no filtrados por la máscara amarilla, se incluirán en la longitud de la neurita, así como en la medición del punto de ramificación.
En consecuencia, se recomienda normalizar estos valores para el recuento de células, ya que el número de neuronas en la imagen influye en las mediciones de la longitud de las neuritas y el punto de ramificación.
Segmentación de cuerpos celulares
Entre todos los parámetros proporcionados por el sistema, se encuentran el grupo de células y el área de grupos de cuerpos células. Sin embargo, estos dos parámetros no son fiables para utilizarlos como valores para el recuento de células. Como se ilustra en la Figura 4, el software segmenta los objetos de alto contraste en la máscara amarilla, incluidas las sombras causadas por el movimiento medio en el pozo. Además, también segmenta las células muertas y los desechos celulares (Figura 4). Para obtener un recuento celular confiable de las neuronas en crecimiento, se puede utilizar un método manual, como la herramienta Cell Counter en Fiji (Figura 13).
En la Tabla 1 para las imágenes de fase y en la Tabla 2 para las imágenes de inmunocitoquímica se proporciona un resumen de los parámetros de análisis sugeridos por tipo de cultivo. Además, en la Tabla 3 se proporciona un resumen de los parámetros de análisis sugeridos para resolver problemas específicos.
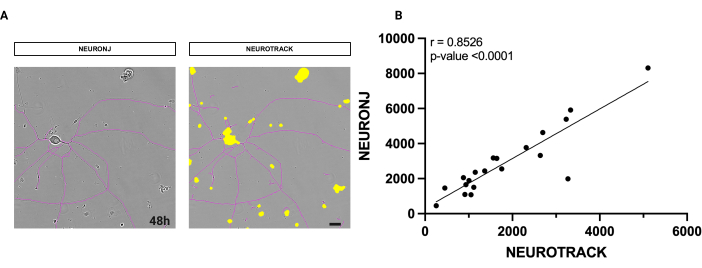
Figura 1: Análisis de correlación entre la segmentación manual y semiautomática de neuritas. (A) A la izquierda, una imagen de fase representativa de una neurona segmentada con el plug-in NeuronJ en Fiji. A la derecha, una imagen de fase representativa de una neurona está segmentada con el software semiautomático. (B) Se analizó una regresión lineal simple ejecutada en 20 neuronas con métodos manuales y semiautomáticos. Coeficiente de correlación de Spearman r = 0,8526, p**** < 0,0001. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
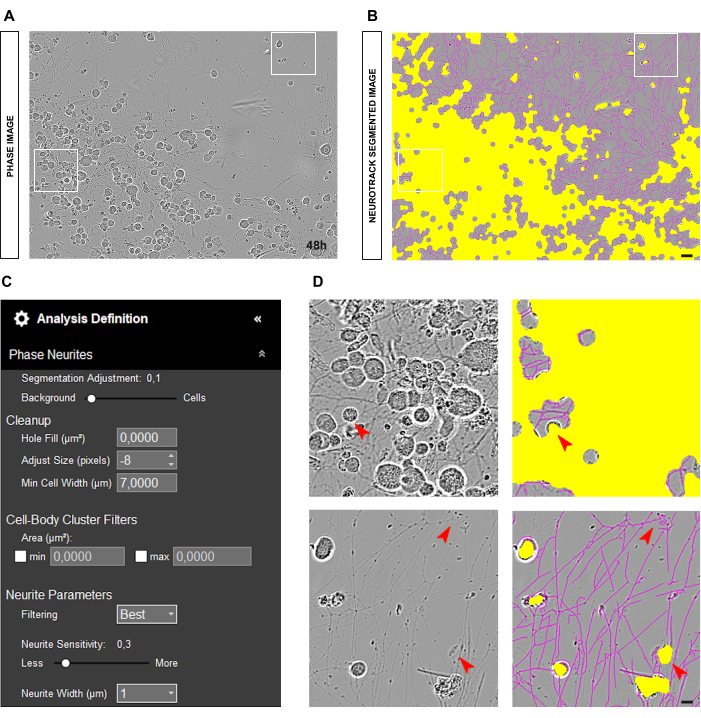
Figura 2: Error de siembra en cultivo de neuronas sensoriales adultas. (A) Imagen de fase representativa del error de siembra. (B) Imagen representativa segmentada automáticamente. La máscara amarilla segmenta los cuerpos celulares, la máscara magenta segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Panel superior: zoom en el error de segmentación del cuerpo celular (máscara amarilla) debido a la agrupación de cuerpos celulares. Panel inferior: zoom sobre el error de segmentación de las neuritas (máscara magenta) debido a los desechos celulares. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
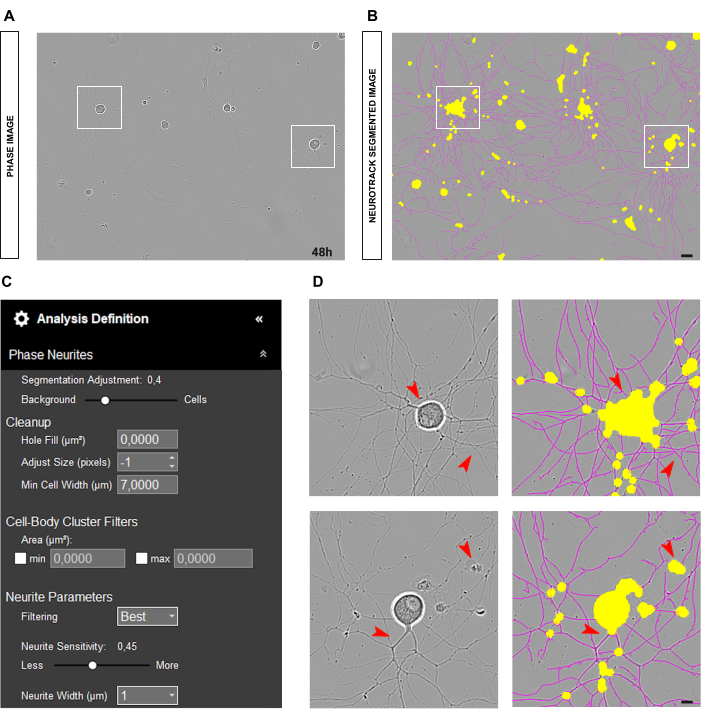
Figura 3: Cultivo ideal de neuronas sensoriales adultas para el análisis de crecimiento de neuritas. (A) Imagen de fase representativa de una condición de siembra ideal para el análisis de crecimiento de neuritas. (B) Imagen representativa segmentada automáticamente. La máscara amarilla segmenta los cuerpos celulares, la máscara magenta segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Zoom en la segmentación del cuerpo celular (máscara amarilla) y en la segmentación de neuritas (máscara magenta). Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
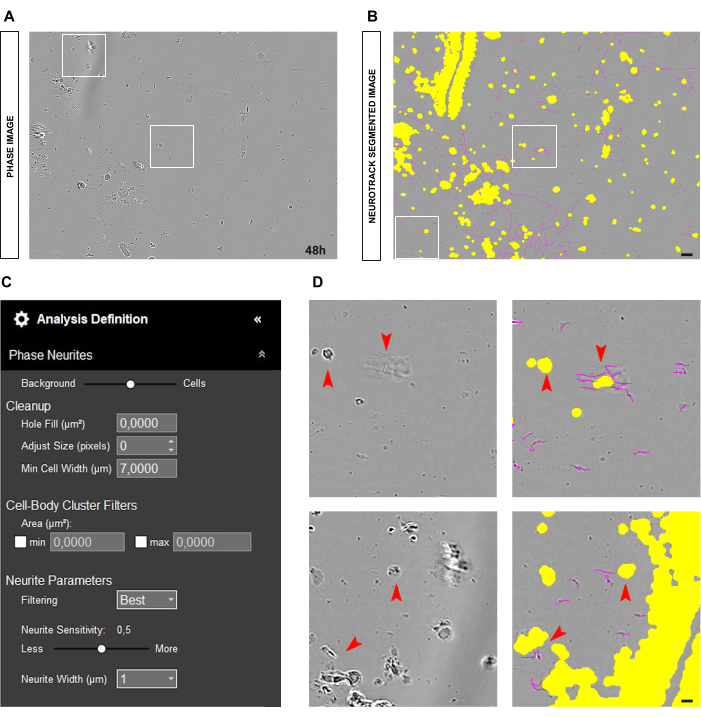
Figura 4: Elementos perturbadores en el análisis del crecimiento de neuritas en el cultivo de neuronas sensoriales adultas. (A) Imagen de fase representativa de desechos celulares y sombras debidas a movimientos medios. (B) Imagen representativa segmentada automáticamente. La máscara amarilla segmenta los cuerpos celulares, la máscara magenta segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Amplíe el error de segmentación del cuerpo celular (máscara amarilla) y la segmentación de neuritas (máscara magenta) debido a los desechos celulares y las sombras del medio en movimiento. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
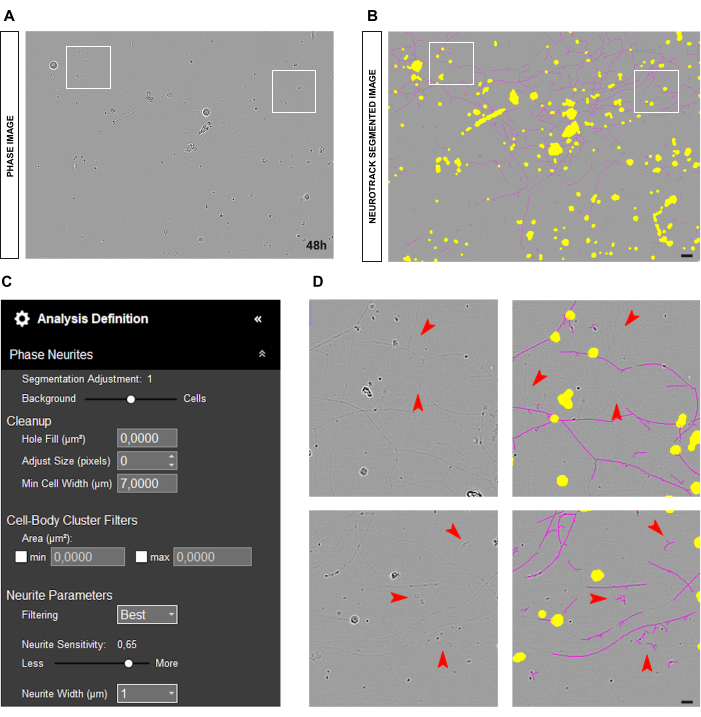
Figura 5: Neuritas delgadas en análisis de crecimiento de neuritas en cultivo de neuronas sensoriales adultas. (A) Imagen representativa de fase de neuronas caracterizadas por neuritas muy delgadas. (B) Imagen representativa segmentada automáticamente. La máscara amarilla segmenta los cuerpos celulares, la máscara magenta segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Panel superior: zoom sobre la pérdida de longitud de la neurita debido a los límites de detección de la segmentación de las neuritas (máscara magenta). Panel inferior: zoom sobre el error de segmentación de neuritas (máscara magenta) en objetos extraños. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
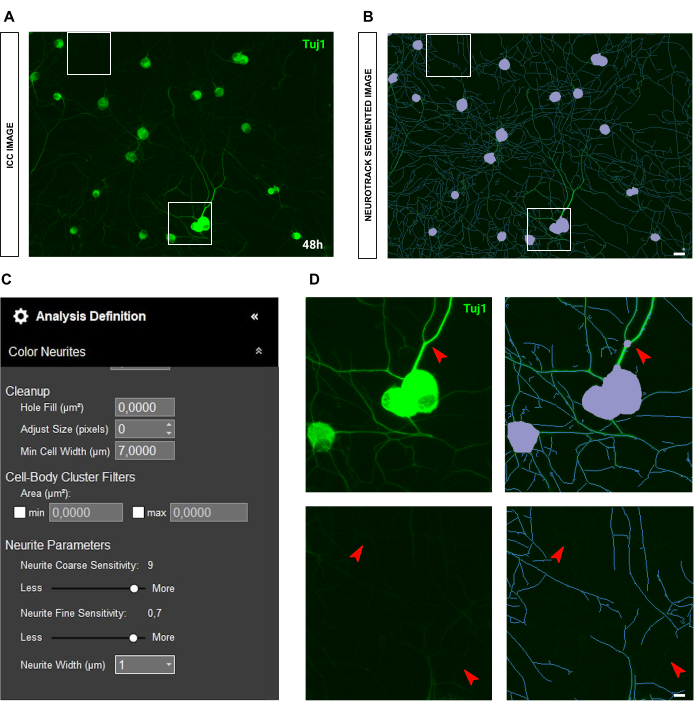
Figura 6: Brillo de las neuritas en el análisis del crecimiento de las neuritas en el cultivo de neuronas sensoriales adultas. (A) Imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de neuronas caracterizadas por neuritas muy brillantes y gruesas. (B) Imagen representativa segmentada automáticamente. La máscara púrpura segmenta los cuerpos celulares, la máscara azul segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Panel superior: zoom en el error de segmentación del cuerpo celular (máscara púrpura) debido al grosor de las neuritas. Panel inferior: zoom sobre la pérdida de longitud de las neuritas debido al intenso brillo de fluorescencia de las neuritas gruesas. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
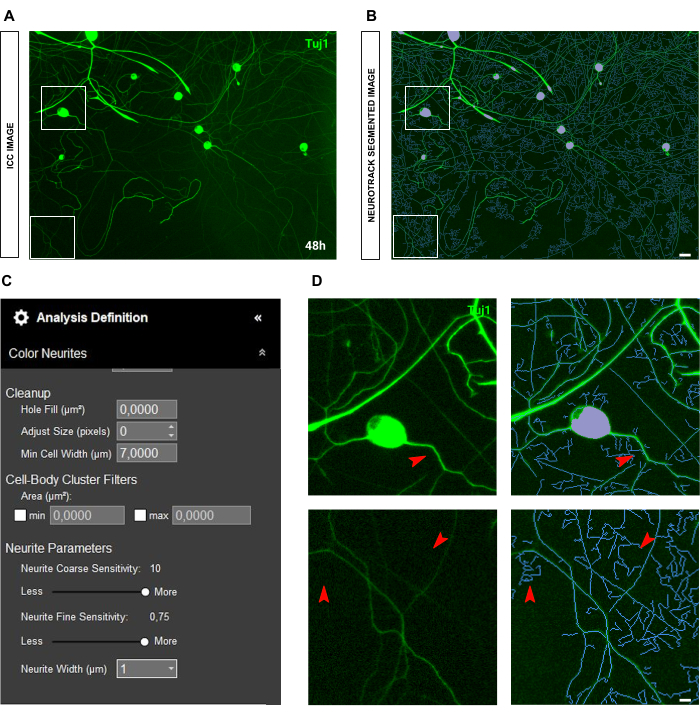
Figura 7: Fluorescencia de fondo en el análisis de crecimiento de neuritas en cultivo de neuronas sensoriales adultas. (A) Imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de alto ruido de fluorescencia de fondo. (B) Imagen representativa segmentada automáticamente. La máscara púrpura segmenta los cuerpos celulares, la máscara azul segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Zoom en el error de segmentación de neuritas (máscara azul) debido a la interferencia de la fluorescencia de fondo. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
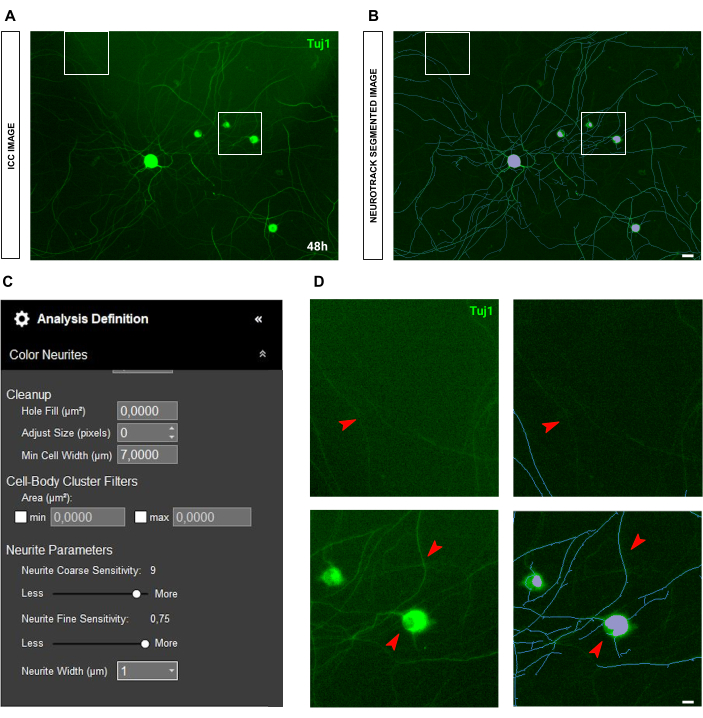
Figura 8: Dispersión de la luz en el análisis del crecimiento de neuritas en el cultivo de neuronas sensoriales adultas. (A) Imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de la dispersión de la luz. (B) Imagen representativa segmentada automáticamente. La máscara púrpura segmenta los cuerpos celulares, la máscara azul segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Panel superior: zoom sobre la pérdida de longitud de la neurita debido a la interferencia de la dispersión de la luz. Panel inferior: zoom en el error de segmentación del cuerpo de la célula (máscara morada). Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
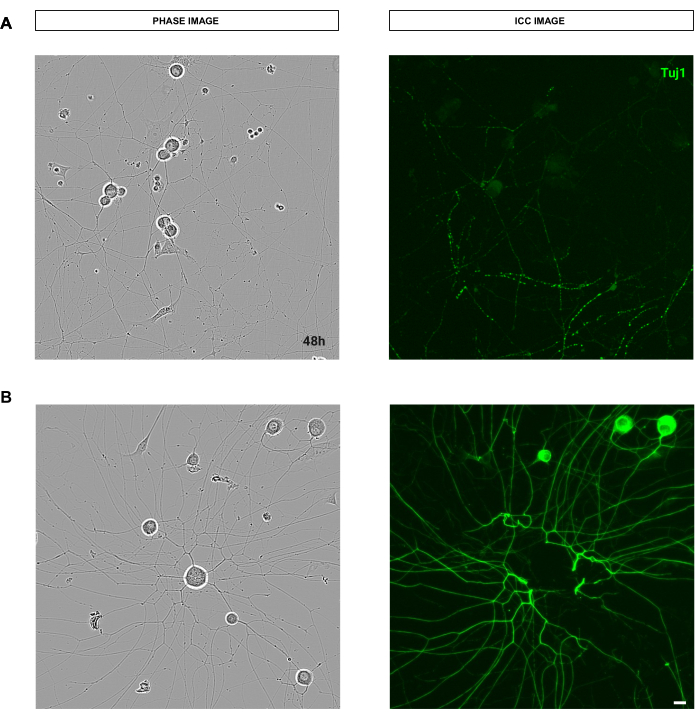
Figura 9: Errores que afectan la calidad del procedimiento de tinción que interfieren con el análisis de crecimiento de neuritas en el cultivo de neuronas sensoriales adultas. (A) A la izquierda, una imagen representativa de fase de neuronas sensoriales adultas. A la derecha, una imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de neuritas rotas debido al lavado en el procedimiento de tinción. (B) A la izquierda, una imagen representativa de fase de neuronas sensoriales adultas. A la derecha, una imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de la remoción del cuerpo celular debido a los lavados del procedimiento de tinción. Las imágenes se adquirieron 48 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
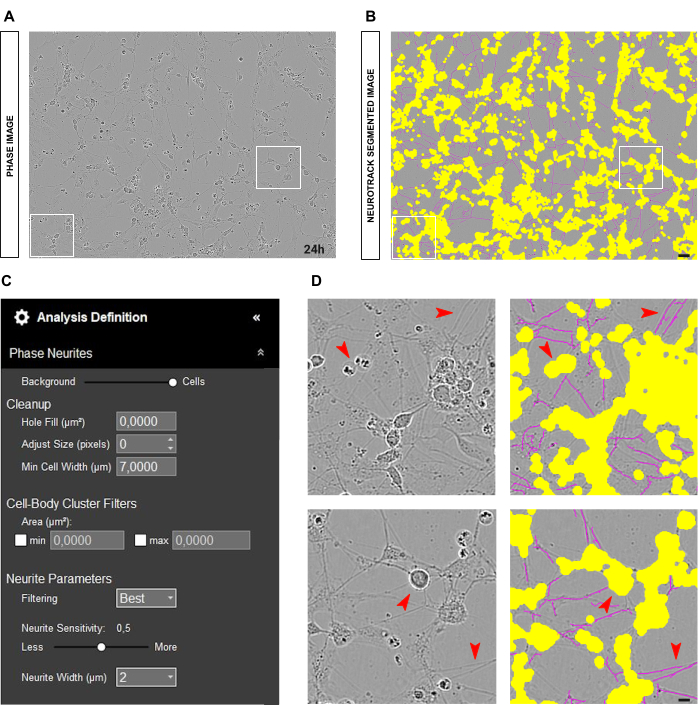
Figura 10: Cultivo de neuronas sensoriales embrionarias (E13.5) ideal para el análisis de crecimiento de neuritas. (A) Imagen de fase representativa de una condición de siembra ideal para el análisis de crecimiento de neuritas en cultivo de neuronas sensoriales embrionarias. (B) Imagen representativa segmentada automáticamente. La máscara amarilla segmenta los cuerpos celulares, la máscara magenta segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Zoom en la segmentación del cuerpo celular (máscara amarilla) y en la segmentación de neuritas (máscara magenta). Las imágenes se adquirieron 24 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
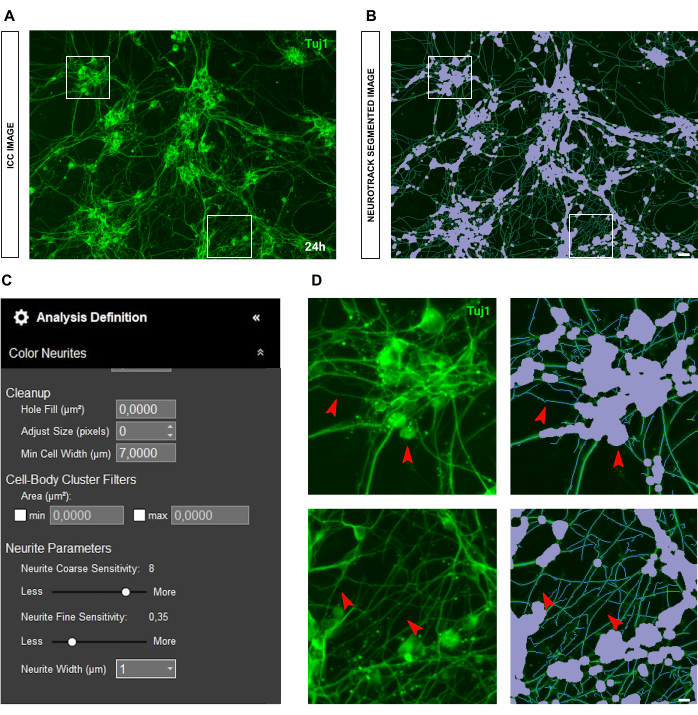
Figura 11: Cultivo ideal de neuronas sensoriales embrionarias (E13.5) para el análisis de crecimiento de neuritas. (A) Imagen inmunocitoquímica representativa (marcador neuronal Tuj1) de un cultivo de neuronas sensoriales embrionarias ideal para el análisis de crecimiento de neuritas. (B) Imagen representativa segmentada automáticamente. La máscara púrpura segmenta los cuerpos celulares, la máscara azul segmenta las neuritas. (C) Parámetros ilustrativos de definición de análisis de crecimiento de neuritas. (D) Zoom en la segmentación del cuerpo celular (máscara morada) y en la segmentación de neuritas (máscara azul). Las imágenes se adquirieron 24 h después de la siembra. Aumento 20x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.

Figura 12: Las células NSC-34 diferenciadas tienen más neuritas y ramificaciones en comparación con los controles indiferenciados. Imágenes representativas de células NSC-34. Panel superior: células NSC-34 indiferenciadas (control). Panel inferior: células NSC-34 diferenciadas después de 96 horas de tratamiento con ácido retinoico. En el lado izquierdo de ambos paneles, imágenes de contraste de fase, mientras que en el lado derecho de ambos paneles, imágenes segmentadas automáticamente (soma en amarillo, neuritas en magenta). Las imágenes se adquirieron 96 h después de la siembra. Aumento 10x. Barra de escala, 50 μm. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
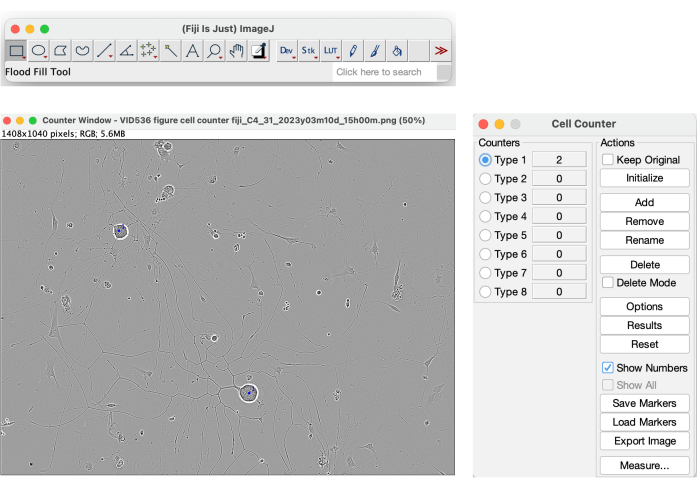
Figura 13: Herramienta de contador de celdas en Fiji. Recuento manual de células realizado en una imagen de fase de una condición de siembra ideal para el análisis de crecimiento de neuritas. Aumento 20x. La figura fue creada con BioRender. Haga clic aquí para ver una versión más grande de esta figura.
| Tipo de cultura | Cultivo de DRG adulto (Fase) | Cultivo embrionario de DRG (Fase) | NSC-34 (Fase) |
| Magnificación | 20 veces | 20 veces | 10 veces |
| Modo de segmentación | Brillo | Brillo | Brillo |
| Ajuste de segmentación | 0.5 - 0.7 | 1.7 - 2 | 1 |
| Ajustar tamaño (píxeles) | 0, +1, +2 | 0, +1 | 0 |
| Filtrado | Mejor | Mejor | Mejor |
| Sensibilidad a las neuritas | 0.4 - 0.5 | 0.25 - 0.4 | 0.3 - 0.5 |
| Anchura de la neurita | 1 | 2 | 2 |
Tabla 1: Resumen de los parámetros de definición de análisis sugeridos para cultivos de neuronas sensoriales adultas, cultivos de neuronas sensoriales embrionarias (E13.5) y cultivos de NSC-34 en imágenes de contraste de fase.
| Tipo de cultura | Cultura de GRD para adultos (ICC) | Cultivo embrionario de DRG (ICC) |
| Magnificación | 20 veces | 20 veces |
| Modo de segmentación | Brillo | Brillo |
| Ajuste de segmentación | 0.5 - 0.7 | 1.7 - 2 |
| Ajustar tamaño (píxeles) | 0, +1, +2 | 0, +1 |
| Filtrado | Mejor | Mejor |
| Sensibilidad gruesa de la neurita | 8 - 9 | 8 - 9 |
| Neurita Sensibilidad Fina | hasta 0,75 | 0.5 - 0.75 |
| Anchura de la neurita | 1 | 2 |
Tabla 2: Resumen de los parámetros de definición de análisis sugeridos para cultivos de neuronas sensoriales adultas, cultivos de neuronas sensoriales embrionarias (E13.5) y cultivos de NSC-34 en imágenes de inmunocitoquímica.
| EMITIR | SUGERENCIAS |
| Cultura sucia | Ajuste el control deslizante de segmentación hacia las celdas |
| Aumentar el parámetro de ajuste de tamaño (+1,+2...) | |
| Disminuir ligeramente la sensibilidad de las neuritas | |
| Neuritas pálidas/delgadas | Aumentar la sensibilidad de las neuritas (al menos 0,6) |
| Ajuste el control deslizante de segmentación hacia las celdas. | |
| Neuritas finas en ICC | Aumentar la sensibilidad de las neuritas finas (hasta 0,75) |
| Reducir la sensibilidad áspera de las neuritas (al menos a 8-9) | |
| Células gliales | Ajuste el control deslizante de segmentación hacia las celdas (1.7-2) |
| Anchura de la neurita a 2 |
Tabla 3: Resumen de los parámetros de definición de análisis sugeridos para resolver problemas específicos en diferentes tipos de culturas.
Discusión
Medir con precisión cómo crecen las neuronas en condiciones sanas, lesionadas y enfermas es un parámetro crítico en muchas configuraciones experimentales dentro del campo de la neurociencia. Ya sea que se trabaje con cultivos organotípicos de explantes enteros de DRG o cultivos disociados, la medición adecuada del crecimiento axonal ha sido un desafío importante en los últimos 20 años. Sin una cuantificación fiable y precisa del crecimiento de neuritas, es imposible evaluar si un tratamiento específico, como el ácido retinoico (durante 4 días) para las células NSC-3434 o las neurotrofinas (durante 1-2 días) para las neuronas DRG embrionarias 14,35, ha sido eficaz. Las neuronas suelen exhibir un crecimiento continuo cuando están sanas; sin embargo, después de una lesión, la tasa de crecimiento axonal aumenta12,13. El tiempo es crucial cuando se mide el crecimiento axonal; Por lo tanto, antes de comenzar un experimento, es esencial realizar una prueba de prueba para determinar el momento óptimo para fijar las células en función de su curva de meseta de tasa de crecimiento.
La elección del método, manual o automático, marca un hito en términos de gasto de tiempo y precisión. Algunos de los métodos manuales más comunes incluyen NeuronJ18,20 y Metamorph (Visitron)2,22,28. Los métodos manuales requieren que los usuarios rastreen manualmente las neuritas, lo que requiere mucho tiempo y imágenes de una sola célula. Con la segmentación manual de neuritas, las redes neuronales están completamente fuera de su alcance. Por lo general, estas metodologías miden solo el axón más largo o utilizan la medición de distancia vectorial, perdiendo así información importante como el número de puntos de ramificación y la longitud axonal total. Algo de mejora es proporcionada por el análisis de Sholl30, que de todos modos se limita a condiciones de una sola célula. El análisis de una sola célula presenta varios desafíos, comenzando con la siembra de células. Las neuronas deben estar sembradas en una concentración muy baja, lo que puede no ser la condición de crecimiento más adecuada para cada tipo de célula. Otro problema surge de la adquisición de imágenes. Por lo general, el microscopio confocal se utiliza para la obtención de imágenes, lo que requiere usuarios capacitados y neuronas fluorescentes y no es eficiente ni en tiempo ni costo. Con el microscopio confocal se obtienen imágenes de alta resolución, pero muy pocas neuronas se obtienen imágenes de cada experimento. Esto representa una limitación, ya que se necesitan más réplicas biológicas para llegar a un número adecuado de neuronas.
Algunas metodologías automáticas, como NeuroMath 2,28, resuelven el problema de la segmentación de neuritas, que requiere mucho tiempo, y que se realiza de forma automática.
Sin embargo, debido a las limitaciones de tiempo, este módulo de medición del crecimiento de neuritas proporciona resultados más rápidos al adquirir imágenes en la máquina de microscopía de lapso de tiempo. Este último, junto con este software, mejora significativamente la eficiencia de tiempo y costes tanto para los estudiantes como para los investigadores principales.
La máquina de adquisición permite la creación de un mapa bastante completo del pozo, adquiriendo un número variable de imágenes en función del diámetro del pozo. Esto representa una ventaja significativa, ya que se obtienen imágenes de varias neuronas al mismo tiempo. Sin embargo, alcanzar solo un aumento de 20x es suficiente y adecuado para analizar las imágenes con el software. Su potencia radica en su capacidad para entrenar con un conjunto de imágenes y realizar una medición semiautomática de la longitud axonal total. Además, el software puede trabajar tanto en neuronas individuales como en redes neuronales. El software es capaz de segmentar neuritas y cuerpos celulares con dos máscaras diferentes. Una máscara amarilla segmenta todos los objetos de alto contraste de la imagen, como cuerpos de celda, restos de celda y sombras. Una máscara magenta, en cambio, segmenta las neuritas. La precisión y exactitud del software se demostraron mediante la segmentación de las mismas neuronas tanto con el software como con NeuronJ. Desde el punto de vista del análisis estadístico, los valores de las longitudes de las neuritas se correlacionaron bien con un alto coeficiente de correlación de Spearman.
Después de evaluar la confiabilidad del método, pasamos al análisis de varias condiciones de prueba. Para un análisis óptimo, se requieren algunas precauciones. En primer lugar, las neuronas tienen que sembrarse uniformemente en el pozo, evitando los puntos con alta concentración de células. La agrupación de neuronas hace que el software pierda precisión en la detección de las neuritas. Otra variable que influye en la exactitud y precisión del análisis es la limpieza del cultivo. Es preferible un cultivo limpio con pocos residuos celulares y células muertas. Sin embargo, el software es capaz de compensar estos problemas mediante la modulación de la sensibilidad de la neurita y la máscara de segmentación del cuerpo celular. Como se mencionó anteriormente, la máscara amarilla segmenta objetos de alto contraste, entre los que también hay sombras causadas por el movimiento del medio en el pozo. Las sombras pueden cubrir las neuritas, lo que resulta en la pérdida de la longitud de la neurita. Sin embargo, este problema se resuelve fácilmente permitiendo que el medio se asiente antes de la adquisición de la imagen.
El algoritmo es capaz de realizar la cuantificación de la longitud de las neuritas tanto en imágenes de contraste de fase como en imágenes de inmunocitoquímica. Cuando se trata de fluorescencia, se deben tomar otras precauciones para obtener un análisis confiable. En primer lugar, la calidad de la tinción influye profundamente en el resultado del análisis. Si las neuritas se rompen o segmentan y los cuerpos celulares se arrancan durante los lavados, el análisis pierde resistencia y fiabilidad. Además, la fluorescencia en sí misma representa un elemento potencialmente perturbador para el análisis. Dado que el enfoque es realizado automáticamente por la máquina, el objetivo enfoca objetos muy brillantes como artefactos, cuerpos celulares o neuritas gruesas. Como resultado, quedan neuritas más delgadas y menos brillantes, lo que dificulta que el usuario mida correctamente la longitud de la neurita.
Como consecuencia, el análisis de las imágenes de fase podría estar mejor fundamentado en comparación con el análisis de las imágenes de inmunocitoquímica. El software es capaz de trabajar en muchas morfologías neuronales diferentes, desde las más intrincadas y elaboradas hasta las más simples, ya sea como células individuales o en redes neuronales. Por lo tanto, es utilizable en muchos campos de investigación diferentes, que van desde cultivos primarios de neuronas provenientes del sistema nervioso central o periférico de varias etapas de desarrollo hasta neuronas derivadas de iPSC y líneas celulares como NSC-34.
A pesar del importante potencial del software, se pueden señalar algunas limitaciones. En primer lugar, la precisión de la segmentación del cuerpo celular no es óptima. En consecuencia, parámetros como el grupo de cuerpos celulares y el área del grupo de cuerpos celulares no se pueden utilizar de manera confiable para el recuento de células. En segundo lugar, además de las precauciones necesarias para una segmentación óptima de las neuritas, los axones insuficientemente gruesos pueden excluirse de la medición de la longitud de las neuritas, lo que provoca la pérdida de datos.
El parámetro de punto de bifurcación encuentra problemas relacionados con ambos tipos de segmentación. Las sombras, las células muertas o los desechos en el cultivo que se localizan en los puntos de ramificación los oscurecen a medida que se cubren por la segmentación del cuerpo celular. Además, en el caso de las neuritas delgadas, la fiabilidad del parámetro del punto de ramificación vuelve a verse gravemente comprometida.
Además, el enfoque automático durante la adquisición de imágenes a veces puede ser subóptimo. El aumento máximo de la máquina está limitado a 20x, lo que puede ser inadecuado para observar detalles más finos o fluorescencia en estructuras delgadas como neuritas. Además, la máquina funciona mejor con sustratos plásticos homogéneos. Si se inserta un cubreobjetos de vidrio en el pozo, el enfoque en el vidrio puede fallar, lo que resulta en imágenes parcialmente borrosas. Sin embargo, este software no solo se aplica a las neuronas, sino también a campos de investigación completamente diferentes, como el crecimiento de hongos36.
A fin de cuentas, creemos que este módulo de medición del crecimiento de neuritas es una herramienta fiable para medir las neuritas de forma rápida, imparcial y eficiente.
Divulgaciones
Los autores declaran que la investigación se llevó a cabo sin ninguna relación comercial o financiera que pudiera crear un conflicto de intereses.
Agradecimientos
Queremos agradecer a Alessandro Vercelli por los comentarios críticos y el apoyo técnico de Sartorius por la ayuda. Nuestra investigación sobre estos temas ha sido generosamente apoyada por la Beca Rita-Levi Montalcini 2021 (MIUR, Italia). Esta investigación fue financiada por el Ministero dell'Istruzione dell'Università e della Ricerca MIUR project Dipartimenti di Eccellenza 2023-2027 al Departamento de Neurociencia Rita Levi Montalcini. La investigación de D.M.R. se ha llevado a cabo durante y con el apoyo del curso nacional de doctorado interuniversitario italiano en Desarrollo Sostenible y Cambio Climático (enlace: www.phd-sdc.it).
Materiales
| Name | Company | Catalog Number | Comments |
| Collagenase A | Merck / Roche | 10103586001 | |
| Dispase II (neutral protease, grade II) | Merck / Roche | 4942078001 | |
| Dulbecco's modified eagle's medium | Merck / Sigma | D5796 | |
| Fetal bovin serum | Merck / Sigma | F7524 | |
| Ham's F-12 Nutrient Mix (1X) | ThermoFisher Scientific | 21765029 | |
| Ham's F12 w/ L-Glutamine | Euroclone | ECM0135L | |
| Hanks' Balanced Salt Solution | Euroclone | ECM0507L | |
| HBSS (10X), no calcium, no magnesium, no phenol red | ThermoFisher Scientific | 14185045 | |
| HyClone Characterized Fetal Bovine Serum (U.S.) | Cytiva | SH30071.03 | |
| Incucyte, Neurotrack Analysis Software | Sartorius | 9600-0010 | |
| L-15 Medium (Leibovitz) | Millipore/Sigma | L5520 | |
| Laminin Mouse Protein, Natural | ThermoFisher Scientific | 23017015 | |
| L-Cysteine | Merck / Sigma | C7352 | |
| Leibovitz's L-15 medium w/o L-glutamine | Euroclone | ECB0020L | |
| mouse NGF 2.5S (>95%) | Alomone Labs | N-100 | |
| Neurobasal Medium [-] Glutamine | ThermoFisher Scientific | 21103049 | |
| NSC-34 | CELLutions Biosystems Inc (Ontario, Canada) | CLU140 | |
| Papain from papaya latex | Sigma | P4762 | |
| Penicillin-Streptomycin (5,000 U/mL) | ThermoFisher Scientific | 15070063 | |
| Percoll (Density 1.130 g/mL) | Cytiva | 17089101 | |
| Poly-D-Lysine Solution (1mg/mL) | EMD Millipore/Merck | A-003-E | |
| Poly-L-Lysine Solution (0-01%) | Sigma | P4832 | |
| Recombinant Human NT-3 | PeproTech | 450-03 | |
| Retinoic Acid | Merck / Sigma | R2625 | |
| Trypsin-EDTA solution | Sigma | T3924 | |
| β-Tubulin III (Tuj1) antibody | Merck / Sigma | T8660 |
Referencias
- Terenzio, M., et al. Locally translated mTOR controls axonal local translation in nerve injury. Science. 359, 1416-1421 (2018).
- Marvaldi, L., et al. Enhanced axon outgrowth and improved long-distance axon regeneration in sprouty2 deficient mice. Dev Neurobiol. 75, 217-231 (2015).
- Kalinski, A. L., et al. Deacetylation of Miro1 by HDAC6 blocks mitochondrial transport and mediates axon growth inhibition. J Cell Biol. 218, 1871-1890 (2019).
- Marvaldi, L., et al. Importin α3 regulates chronic pain pathways in peripheral sensory neurons. Science. 369, 842-846 (2020).
- Gangadharan, V., et al. Neuropathic pain caused by miswiring and abnormal end organ targeting. Nature. 606, 137-145 (2022).
- Testa, L., Dotta, S., Vercelli, A., Marvaldi, L., et al. Communicating pain: emerging axonal signaling in peripheral neuropathic pain. Front Neuroanat. 18, (2024).
- Thongrong, S., et al. Sprouty2 and -4 hypomorphism promotes neuronal survival and astrocytosis in a mouse model of kainic acid induced neuronal damage. Hippocampus. 26, 658-667 (2016).
- Yaron, A., Schuldiner, O. Common and divergent mechanisms in developmental neuronal remodeling and dying back neurodegeneration. Curr Biol. 26, R628-R639 (2016).
- Maor-Nof, M., et al. Axonal degeneration is regulated by a transcriptional program that coordinates expression of pro- and anti-degenerative factors. Neuron. 92, 991-1006 (2016).
- Bromberg, K. D. Regulation of neurite outgrowth by Gi/o signaling pathways. Front Biosci. 13, 4544-4557 (2008).
- Girouard, M. P., et al. Collapsin response mediator protein 4 (CRMP4) facilitates wallerian degeneration and axon regeneration following Sciatic nerve injury. eNeuro. 7, 0479-0419 (2020).
- van Erp, S., et al. Age-related loss of axonal regeneration is reflected by the level of local translation. Exp Neurol. 339, 113594 (2021).
- Wang, X., et al. Driving axon regeneration by orchestrating neuronal and non-neuronal innate immune responses via the IFNγ-cGAS-STING axis. Neuron. 111, 236-255.e7 (2023).
- Kaselis, A., Treinys, R., Vosyliūtė, R., Šatkauskas, S. DRG axon elongation and growth cone collapse rate induced by Sema3A are differently dependent on NGF concentration. Cell Mol Neurobiol. 34, 289-296 (2014).
- Maier, O., et al. Differentiated NSC-34 motoneuron-like cells as experimental model for cholinergic neurodegeneration. Neurochem Int. 62, 1029-1038 (2013).
- Nango, H., et al. Highly efficient conversion of motor neuron-like NSC-34 cells into functional motor neurons by Prostaglandin E2. Cells. 9, 1741 (2020).
- Kim, H. W., Caspar, T., Shah, S. B., Hsieh, A. H. Effects of proinflammatory cytokines on axonal outgrowth from adult rat lumbar dorsal root ganglia using a novel three-dimensional culture system. Spine J. 15, 1823-1831 (2015).
- Frey, E., et al. An in vitro assay to study induction of the regenerative state in sensory neurons. Exp Neurol. 263, 350-363 (2015).
- Zhang, Z., et al. Cerebellar injury and impaired function in a rabbit model of maternal inflammation induced neonatal brain injury. Neurobiol Learn Mem. 165, 106901 (2019).
- Pemberton, K., Mersman, B., Xu, F. Using ImageJ to assess neurite outgrowth in mammalian cell cultures: Research data quantification exercises in undergraduate neuroscience lab. J Undergrad Neurosci Educ. 16, A186-A194 (2018).
- Marvaldi, L., Hausott, B., Auer, M., Leban, J., Klimaschewski, L. A Novel DRAK inhibitor, SC82510, promotes axon branching of adult sensory neurons in vitro. Neurochem Res. 39, 403-407 (2014).
- Quarta, S., et al. Peripheral nerve regeneration and NGF-dependent neurite outgrowth of adult sensory neurons converge on STAT3 phosphorylation downstream of neuropoietic cytokine receptor gp130. J Neurosci. 34, 13222-13233 (2014).
- Woitke, F., et al. Adult hippocampal neurogenesis poststroke: More new granule cells but aberrant morphology and impaired spatial memory. PLoS One. 12, e0183463 (2017).
- Xiao, X., et al. Automated dendritic spine detection using convolutional neural networks on maximum intensity projected microscopic volumes. J Neurosci Meth. 309, 25-34 (2018).
- Pool, M., Thiemann, J., Bar-Or, A., Fournier, A. E. NeuriteTracer: A novel ImageJ plugin for automated quantification of neurite outgrowth. J Neurosci Meth. 168, 134-139 (2008).
- Wang, D., et al. HCA-Vision: Automated neurite outgrowth analysis. SLAS Disc. 15, 1165-1170 (2010).
- Whitlon, D. S., et al. Novel high content screen detects compounds that promote neurite regeneration from cochlear spiral ganglion neurons. Sci Rep. 5, 15960 (2015).
- Rishal, I., et al. WIS-neuromath enables versatile high throughput analyses of neuronal processes. Dev Neurobiol. 73, 247-256 (2013).
- Smith, D. S., Pate Skene, J. H. A Transcription-dependent switch controls competence of adult neurons for distinct modes of axon growth. J Neurosci. 17, 646-658 (1997).
- Gardiner, N. J., et al. Preconditioning injury-induced neurite outgrowth of adult rat sensory neurons on fibronectin is mediated by mobilisation of axonal α5 integrin. Mol Cell Neurosci. 35, 249-260 (2007).
- Hauck, J. S., et al. Heat shock factor 1 directly regulates transsulfuration pathway to promote prostate cancer proliferation and survival. Commun Biol. 7, 9 (2024).
- Zhu, Y., et al. Loss of WIPI4 in neurodegeneration causes autophagy-independent ferroptosis. Nat Cell Biol. 26, 542-551 (2024).
- Reggiani, F., et al. BET inhibitors drive Natural Killer activation in non-small cell lung cancer via BRD4 and SMAD3. Nat Commun. 15, 2567 (2024).
- Ackerman, H. D., Gerhard, G. S. Bile acids induce neurite outgrowth in NSC-34 cells via TGR5 and a distinct transcriptional profile. Pharmaceuticals. 16, 174 (2023).
- Tuttle, R., Matthew, W. D. Neurotrophins affect the pattern of DRG neurite growth in a bioassay that presents a choice of CNS and PNS substrates. Development. 121, 1301-1309 (1995).
- Wurster, S., et al. Live monitoring and analysis of fungal growth, viability, and mycelial morphology using the IncuCyte NeuroTrack processing module. mBio. 10 (3), e00673-e00619 (2019).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados