Method Article
שיטת ניטור משתלמת HIV-1 תרופות התנגדות להגדרות משאב מוגבלת
In This Article
Summary
בדיקת עמידות לתרופות ל-HIV-1 אנשים נגועים נכשלו טיפול תרופתי (ART) יכולה להדריך את הטיפולים בעתיד ולשפר את תוצאות טיפול. תוצאות בריאותיות אופטימיזציה של פרט ואוכלוסייה בשכיחות איידס גבוהה, אך משאב מוגבל הגדרות סופו של דבר תדרוש גנוטיפ עמידות לתרופה במחיר סביר ונגיש ושיטות פרשנות.
Abstract
יש עמידות לתרופות של HIV-1 את הפוטנציאל לסכן את היעילות והשפעה של טיפול תרופתי (ART) ברצינות. כתוכניות לאמנות באפריקה שמדרום לסהרה להמשיך ולהרחיב, יחידים באמנות צריכים להיות תחת פיקוח הדוק להופעתה של עמידות לתרופה. מעקב של עמידות לתרופות מועברת כדי לעקוב אחר שידור של זני נגיפים כבר עמידים לאמנות הוא גם קריטי. למרבה הצער, בדיקת עמידות לתרופות היא עדיין אינה נגישה בקלות בהגדרות מוגבלות של משאבים, כי גנוטיפ זה יקר ודורש מעבדה משוכללת ותשתיות ניהול הנתונים. שיטת ניטור עמידות לתרופת genotypic גישה פתוחה לניהול אנשים ולהעריך את העמידות לתרופה מועברת מתוארת. השיטה משתמשת בתוכנת קוד פתוח חופשית לפרשנות של דפוסי עמידות לתרופות והדור של דוחות חולה בודדים. יש פרוטוקול גנוטיפ שיעור הגברה של יותר מ 95% עבור דגימות פלזמה עם avעומס iral> 1,000 HIV-1 RNA עותקים / מיליליטר. הרגישות פוחתת באופן משמעותי לעומס נגיפי <עותקי RNA 1,000 HIV-1 / מיליליטר. השיטה המתוארת כאן הייתה תוקף כנגד שיטה של עמידות לתרופות של HIV-1 בדיקות שאושרה על ידי ארצות הברית מנהל המזון והתרופות אמריקניות (FDA), שיטת גנוטיפ Viroseq. מגבלות של השיטה המתוארת כאן כוללות את העובדה שזה לא אוטומטי ושזה גם לא הצליח להגביר את CRF02_AG צורה רקומביננטי במחזור מפנל אימות של דגימות, למרות שזה מוגבר תת A ו-B מאותו הפנל.
Introduction
מגפת האיידס בדרום אפריקה כבר מתפתחת במהירות 1 עם עלייה במקביל מעריכי באנשים בטיפול תרופתי (ART), ובמיוחד בדרום אפריקה 2, 3. כראיה על ההשפעה אפידמיולוגיים של תוכניות טיפול בקנה מידה גדולה בהפחתת שכיחות 4 והגדלת תוחלת חיים במשאב מוגבל הגדרות (RLS) 5 ממשיך לצבור, המאמצים להגדיל את כיסוי ART יהיו מוגברים. האבולוציה של הנחיות לשימוש בטיפול ככלי למניעה 6, 7 מתחת לבדיקה והטיפול בתוכניות אומרת שהמספר המוחלט של אנשים בטיפול יהיה להגביר עוד יותר. מספרים גדולים של אנשים יהיו על אמנות לתקופות זמן ארוכות יותר כפי שתוחלת החיים הממוצעת של אנשים באמנות מתקרבת זה של האוכלוסייה נגוע ב-HIV 8. הפיתוח וההעברה של עמידות לתרופת HIV יש alwaי"ש נחשב איום על ההישגים של ART 9-12. לפיכך, יש צורך במעקב וניטור של עמידות לתרופות קפדניים יותר ככל שיותר אנשים הם יזמו על אמנות.
עמידות לתרופות Genotypic הבדיקה (GRT) שמשה בהצלחה במדינות מפותחות, הן למעקב, כמו גם ניטור של עמידות לתרופות של HIV-1 באנשים שקיבלו לאמנות. בהגדרות אלה, GRT כבר משולב לתוך הרצף של טיפול ל-HIV-1 אנשים נגועים. רוב ההנחיות הבינלאומיות ממליצים GRT למבוגר או מטופלי ילדים שלא הצליחו ART (קו ראשון וקו שני) 13-15, מטופלי ילדים שנחשפו למניעת העברת אמא לילד משטרים (PMTCT) אבל נגועים לאחר מכן 16, ובהגדרות עם רמות גבוהה של עמידות לתרופות מועברת בין אנשים שנדבקו בחריפות 13-15. עם זאת, דרישות העלות, טכנולוגיה ותשתיות מוגבלות implemenסימטרייה של גישות דומות לניטור עמידות לתרופה בRLS.
הטיפול בדרום אפריקה ב-HIV והנחיות ניטור בשלב זה אינו ממליצים על השימוש בGRT בבחירה מנחה של אמנות עבור אנשים שלא הצליחו קו הראשון משטר 17. אנשים מופעלים מבוססים בעיקר על virological פרמטרים (עומס הנגיפי RNA HIV-1). עם זאת ב2012, אגודת האיידס בדרום אפריקה הרופאים פרסמה הנחיות לבדיקת עמידות לתרופות ARV דרום האפריקאי הראשונות 18. הנחיות אלה ממליצים על בדיקות GRT לכל המבוגרים שלא הצליחו קו ראשון וART קו שני ועבור תינוקות נגועים וילדים שנחשפו לPMTCT 18. עם זאת, GRT אינו מומלץ 18 לאנשים שנדבקו בחריפות, משום שאין ראיות הנוכחיות לרמות גבוהות של עמידות לתרופות מועברת בדרום אפריקה 19-29. צפוי כי חלק מההמלצות אלה ישולב לאורך זמן ולטיה הלאומיתהנחיות atment וניטור של המדינות השונות באזור. כבר עכשיו, ב2013 הנחיות טיפול בדרום אפריקה יש כרגע היא המלצת GRT בזמן של כישלון קו השני למבוגרים ובזמן של כישלון טיפול המבוסס על PI הראשון או קו שני לילדים 30.
הוכח כי שילוב GRT להנחיות טיפול בדרום אפריקה יהיה פוטנציאל העלות ניטראלית. בהתחשב בעלות של תרופות משטר הקו השניה שהם יחסית יקרים יותר מאשר תרופות הקו הראשונות, תוך שימוש בGRT לזהות חולים שבאמת צריך להיות מופעל לטיפול קו שני לא תביא כל עלות נוספת לתכנית. בנוסף, GRT יכול גם לזהות סיבות אחרות לכישלון, לשמר את אפשרויות טיפול והפקת מידע על דפוסי התנגדות מתעוררים ביום 31. לכן, יש צורך להפחית את העלות של שיטות ניטור עמידות לתרופה עוד יותר על מנת לשפר את הגישה, איכות טיפולתוצאות ד.
כאן, אנו מציגים שיטת GRT תוכננה להשתמש פריימרים כלליים (קוד פתוח) לשעתוק לאחור, תגובת שרשרת פולימרז (PCR) ורצף (טבלה 1), כמו גם תוכנות קוד פתוח בעיקר לפרשנות עמידות לתרופה. לניהול קליני, הפרוטוקול הוא החמיא על ידי שיטת ביקורת ודיווח מקיפה עם פרשנות מומחה של דו"ח עמידות לתרופה במעבדה עם קרוב דבקות בהנחיות הטיפול הלאומית. הפרוטוקול מחולק לארבעה מרכיבים שונים: 1) ה-HIV ריבונוקלאית חומצה (מיצוי RNA), 2) הפוך תמלול ותגובת שרשרת פולימרז (PCR הגברה) של מטרות נגיפיות, 3) רצף ו4) שיטות ביואינפורמטיקה לניתוח של chromatograms, יישור, אוצרות ופרשנות של נתונים ברצף.
Protocol
1. Ethylenediaminetetraacetic חומצה (EDTA) עיבוד דם מלא
הערה: דם יכול להיות מעובד באופן מיידי לאחר איסוף יכול להיות מאוחסן על 4 מעלות צלזיוס למשך לא יותר מ 24 שעות.
- העבודה בארון בטיחות ביולוגית, תאפשר כל דגימת דם EDTA כדי להגיע לטמפרטורת חדר.
- עבור כל דגימה, תווית מספיק cryovials עם זיהוי המדגם (ID), אחסון חומר (פלזמה), ותאריך.
- צנטריפוגה הדגימות 10 דקות ב 1,000 x גרם. אל תשתמשו בבלמים כדי לעצור צנטריפוגות. זו תניב שלוש שכבות (מלמעלה למטה): פלזמה, leucocytes (מעיל באפי) - שכבה דקה מאוד - ואריתרוציטים, כולל טסיות דם.
- בזהירות לשאוב supernatant (הפלזמה) וaliquot 500 מיליליטר לכל cryovial. יש להיזהר שלא לשבש את שכבת התאים (מעיל באפי) או להעביר את כל תאים.
- אחסן ב-80 ° C עד צורך להפקת RNA או להמשיך למיצוי RNA באופן מיידי.
- הכן גיליון עבודה חילוץ עם תעודות הזהות של הדגימות להיעקר לרבות בקרות פלזמה חיוביות ושליליות.
- עבור כל דגימה להיעקר, תווית צינור microcentrifuge סטרילי 1.5 מיליליטר עם זיהוי המדגם, תאריך הפקה ו" RNA ". גם תווית צינור טור והאוסף התאסף כמו גם צינור microcentrifuge 2 מיליליטר מכיל פתרון תמוגה עבודה עם מספרים מקביל מגיליון עבודת החילוץ.
- עבודה בממשלה ביו הבטיחות, להוסיף מדגם μl 200 לצינור microcentrifuge 2 מיליליטר המקביל של פתרון תמוגה עובד.
- גם וורטקס ו דגירה של 10 דקות בטמפרטורת חדר.
- לאחר 10 דקות, צנטריפוגות הצינור לזמן קצר.
- הוספת 800 מיליליטר של אתנול מוחלט לכל אחד מהצינורות.
- מערבבים על ידי vortexing דופק ו צנטריפוגות לזמן קצר.
- העבר 600 μl של פתרון זה להרכבת צינור עמודה / אוסף המקביל. צנטריפוגה ב 6,000 xגרם במשך דקות 1.
- העבר את העמודה לצינור אוסף חדש וזורקים את צינור האיסוף הישן המכיל התסנין. חזור על השלב מעל 2.8 (לעיל) פעמיים נוספות.
- הוספת AW1 לשטוף חיץ 500 μl לכל עמודה ו צנטריפוגות ב 6,000 XG דקות 1.
- מחק את צינור התסנין ואוסף ולהעביר את העמודה לצינור איסוף חדש.
- הוסף 500 μl היה AW2 חיץ ו צנטריפוגות ב XG 20,000 במשך 3 דקות. חזור על שלב 2.11.
- צנטריפוגה בצינור אוסף חדש ב20,000 XG במשך 2 דקות נוספות.
- מחק עמודת תסנין ומקום ב1.5 מיליליטר צינור microcentrifuge.
- הוסף 60 μl הצפת AVE (מים RNase ללא) לאמצע הטור להבטיח כי אתה לא לוותר על הנוזל בצד של הטור.
- דגירה בטמפרטורת חדר למשך דקות 1.
- צנטריפוגה ב 6,000 XG במשך 2 דקות.
- מחק את העמודה וכובע 1.5 מיליליטר microcentrifuge הצינורות.
- הדגימות מוכנות כעת לreverשעתוק se.
- אם בדיקה היא שיש לבצע באופן מיידי, לאחסן ב 4 מעלות צלזיוס למשך עד 6 שעות. עם זאת, אם בדיקה היא להתעכב ואז למקם ב -80 ° C באופן מיידי. נ.ב.: לא להקפיא / להפשיר את הדגימות יותר מ 3x.
3. הכנה מגיב לשעתוק לאחור
- לפני שמתחיל, לחשב את הכמויות של כל אחד מהחומרים הכימיים הנדרשים למספר הדגימות בטיפול כולל, בקרות פלזמה החיוביות ושליליות. כמו כן להוסיף פקד מגיב.
- שימוש בכמויות מחושבת משלב 3.1 (לעיל), להכין אדנוזין deoxyribonucleotide התמהיל (dNTP) פריימר בצינור נקי, סטרילי 200 μl PCR ואחריו vortexing דופק לזמן קצר. כל דגימה צריכה 0.5 μl של פריימר RT21 ההפוך ו0.5 μl של dNTP, ראה טבלה 2.
- μl 1.0 aliquot של תמהיל dNTP-פריימר ל200 צינורות PCR μl.
- הכן טרנסקריפטאז ההפוך (RT) תערובת אנזים על ידי הוספת 1 μ; ליטר של חיץ השעתוק לאחור 10x, 1 μl של 0.1M DTT ו2 μl של 25mm MgCl 2 לצינור סטרילי ואחריו vortexing ובקצרה צנטריפוגה, ראו לוח 3.
- הוסף 0.5 μl כל אחד מהאנזימים RNAseOUT והכתב עילי III לאחור transcriptase לצינור תערובת אנזים לאחר מכן הקש על הצינור בעדינות לתערובת.
- שמור את הצינורות עם תערובות dNTP-פריימר ותערובת אנזים על גוש קר ותעבור לתחנת RNA.
4. שעתוק לאחור
- הוסף 6 μl של מדגם RNA לצינור תמהיל dNTP-פריימר ואחריו vortexing בקצרה לערבב.
- לאחר התוספת של RNA, לעבור לחדר PCR עם שתי dNTP / פריימר / תמהיל RNA ואנזים RT לערבב צינורות על גוש קרח או קרים.
- בקצרה צנטריפוגות צינורות dNTP / תערובת פריימר / RNA (משלב 4.2) ולמקם אותם לתוך thermocycler.
- חום ב-C ° 65 במשך 5 דקות כדי לפגל-RNA.
- במהירות מגניב 4 ° C, להחזיק למשך 2דקות.
- השהה thermocycler ועדיין על 4 מעלות צלזיוס; להוציא את הצינורות.
- להוסיף במהירות 5 μl של תערובת האנזים תוך שמירה על הצינורות על גוש קר.
- מערבבים בעדינות על ידי הקשה על הצינור אז צנטריפוגות בקצרה את הצינורות ולחזור לthermocycler.
- החזק את הצינורות ב50 מעלות צלזיוס למשך 60 דקות כדי להפוך לתמלל RNA אחרי denaturation אנזים ב85 מעלות צלזיוס למשך 5 דקות כדי לעצור את השעתוק לאחור.
- מגניב 37 ° C. ברגע שהטמפרטורה מגיעה ל37 מעלות צלזיוס, להשהות ולקחת את הצינור מתוך thermocycler.
- מהירות להוסיף 0.5 μl של RNAse H לצינורות ולחזור לthermocycler.
- החזק על 37 מעלות צלזיוס למשך 20 דקות ולאחר מכן לצנן עד 4 ° C.
- ה-DNA משלימה (cDNA) ניתן להשתמש מייד או יכולה להיות מאוחסנת ב -20 מעלות צלזיוס או יותר קר עד צורך. עם זאת, האחסון לטווח הארוך של cDNA צריך להיות ב -80 ° C.
5. מגיב הכנה לPCR
- Befoמתחיל מחדש, לחשב את הכמויות של כל אחד מהחומרים הכימיים הנדרשים למספר הדגימות בטיפול וקבוצת הביקורת. בנוסף לשלושה פקדים (חיובי, שלילי, ומגיבים), אתה יכול גם להוסיף פקד PCR (HIV-DNA). ניתן להכין תערובות PCR הסיבוב הראשונות ושנייה בו זמנית ואת תערובת מאסטר השנייה מאוחסנת ב -20 ° C עד צורך. תערובות יכולות להיות מאוחסנות במשך כ -8 שעות.
- הוספת 18.4 מים μl, 2.5 μl חיץ 10x, 1.0 μl MgCl 2, 0.5 dNTPs μl, ו0.25 μl של כל אחד מצבעי היסוד, כפי שמוצג בטבלה 4 ומערבולת.
- הוסף 0.1 μl של פולימראז פלטינום תקי (5U/μl) ולערבב בעדינות את הצינור על ידי הקשה עליו.
- 23 μl aliquot של מיקס מאסטר 200 צינורות PCR μl.
- עם צינורות תערובת הורים על גוש קר או מהלך קרח לחדר ה-PCR.
6. מקונן PCR
- הוסף 2 μl של cDNA ל23 μl של maste PCR סיבוב 1r לערבב.
- לסגור את הצינורות, לשים את הדגימות בthermocycler ולהשתמש בתנאים הבאים PCR רכיבה על אופניים: 94 מעלות צלזיוס למשך 2 דקות, 30 מחזורים של 95 מעלות צלזיוס במשך 30 שניות, 58 מעלות צלזיוס במשך 20 שניות, ו72 מעלות צלזיוס למשך 2 דקות, אחריו extention סופי 72 מעלות צלזיוס למשך 10 דקות כפי שמוצג באיור 1.
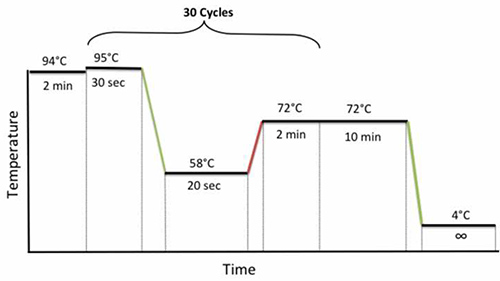
איור 1. תנאי רכיבה על אופניים המקוננים PCR. לחצו כאן לצפייה בתמונה גדולה יותר.
- המשך שלב PCR סיבוב 2 או לאחסן את מוצרי ה-PCR סיבוב 1 ב -20 מעלות צלזיוס או יותר קר עד נדרש בשלב מאוחר יותר.
- לPCR סיבוב 2, להוסיף 2 μl של המוצר ה-PCR סיבוב 1 ל23 μl של תערובת ההורים PCR סיבוב 2ד להשתמש באותה תכנית ה-PCR באיור 1.
7. ג'ל אלקטרופורזה
- הכנת ג'ל
- הוספה גרם 0.5 של לוח agarose בבקבוק זכוכית מיליליטר 250 ולהוסיף 50 מיליליטר של חיץ 1x TBE לבקבוק.
- מחממים במיקרוגל רותח; מערבולת בתדירות גבוהה (בערך כל 30 שניות) עד solubilized לחלוטין. השתמש אחיזת סיליקון או סיליקון תנור כפפה לתפוס את הבקבוק החם. פתרון agarose יכול להרתיח את של הבקבוק בקלות רבה כל כך מקרוב לפקח על התהליך הזה.
- לקרר בטמפרטורת חדר למשך כ 10 דקות.
- יוצקים agarose לתוך מגש ליהוק ג'ל המכיל מסרק גודל מתאים; ג'ל מוכן לשימוש בכ 20-30 דקות.
- הנח ג'ל אלקטרופורזה בחדר ולהפעיל כפי שהומלץ על ידי היצרן.
- ג'ל אלקטרופורזה וויזואליזציה.
- מיץ רומן ורטקס עבור 10 שניות לפני השימוש.
- לדלל 1 μl של מיץ רומן עם 5 μl של Dמדגם NA ולערבב.
- למהול 3 μl של מיץ רומן עם 3 μl של סמן משקל מולקולרי ומערבבים.
- טען את תערובות מסעיפי 7.2.2 ו 7.2.3 (לעיל) ולהפעיל את הג'ל על 100 V ו400 mA ל40 דקות כדי להעריך את ההגברה PCR.
- הגברה חיובית ניתן דמיינו תחת אור UV כ1,315 בר נ"ב, איור 2.
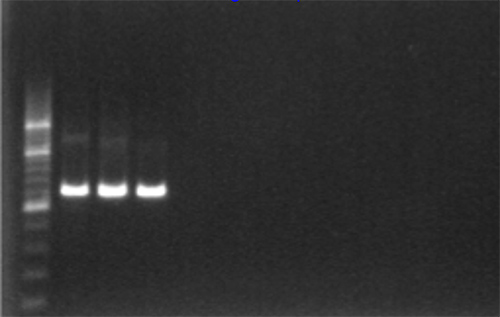
איור 2. אישור ג'ל של ההגברה PCR באמצעות 1% ג'ל אלקטרופורזה agarose וסולם נ"ב 200. לחץ כאן לצפייה בתמונה גדולה יותר.- לא צריך להיות שום הגברה בבקרות שליליות ומגיבות, ובכך מצביע על העדרו של זיהום.
8. ניקוי מוצרי ה-PCR
- כהכנה לתגובת רצף, מוצרי ה-PCR סיבוב השני חיוביים ניקו באמצעות ערכת טיהור PureLink ה-PCR.
- הוסף 80 μl של העבודה חיץ עקידה גבוהה Cutoff (B3) ל20 μl של מוצר ה-PCR ותמהיל פיפטה.
- הוסף את המדגם מעורב עם חיץ המחייב לעמודת ספין בצינור איסוף.
- צנטריפוגה העמודה ב 10,000 XG דקות 1. העבר את העמודה לתוך צינור אוסף חדש.
- לשטוף את העמודה עם 650 μl של הצפת לשטוף עם אתנול.
- צנטריפוגה העמודה ב 10,000 XG דקות 1. העבר את העמודה לתוך צינור אוסף חדש.
- צנטריפוגה עמודה במהירות המרבית למשך 2-3 דקות כדי להסיר כל חיץ לשטוף שיורית.
- מניחים את טור הספין בצינור 1.7 elution מיליליטר נקי מסופק עם הערכה.
- הוסף 40 μl של חיץ elution למרכז של העמודה ודגירת העמודה בtemperatur החדרדואר דקות 1.
- צנטריפוגה העמודה במהירות המרבית למשך 2 דקות (> XG 10,000).
- צינור elution מכיל המוצר ה-PCR מטוהר שלך מוכן לסידור. מחק את העמודה.
- קבע את הריכוז ואיכות של ה-DNA באמצעות Nanodrop.
- אם אין מתקני רצף בבית זמינים, ניתן לשלוח את מוצרי ה-PCR המטוהרים למעבדה רצף מסחרית בשלב זה.
9. תגובות רצף
- מוצרי ה-PCR הם רצף משתמשים בגרסה הגדולה ערכת שליחות קטלנית לצבוע 3.1 ו4 פריימרים עבור כל דגימה (שני קדימה ושתיים לאחור). רצפי פריימר מוצגים בטבלה 2. לכן, לאחר ריצת רצף, כל דגימה תהיה ארבעה רצפים שהתאספו לתוך contig.
- הגדר את תגובות רצף כפי שמצוין בטבלה 5 עבור כל אחד מארבעת צבעי יסוד.
- מערבבים את חיץ רצף ופריימרים ידי vortexing לפני השימוש.
- מערבבים אתמים, חיץ ופריימר לפני התוספת של רצף הצבע הגדול. מערבבים על ידי vortexing.
- בעדינות מערבב את תערובת ההורים לאחר הוספת תערובת רצף צבע הגדולה על ידי צינור היפוך או הקשה עליו בעדינות.
- Aliquot 9 μl של מיקס מאסטר לתוך צלחת אופטית 96 היטב.
- כדי להפעיל 24 דגימות / צלחת, להגדיר את הצלחת כמפורטת להלן איור 3.
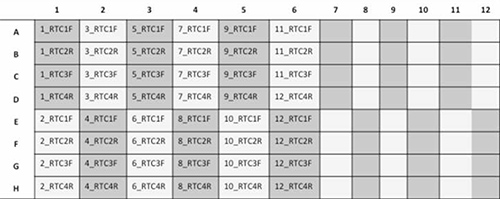
איור 3. ייצוג ערכה של צלחת 96 היטב עם 12 דגימות מטופל להיות רצף עם 4 צבעי יסוד כל אחד (RTC1F, RTC2R, RTC3F, וRTC4R). לחץ כאן לצפייה בתמונה גדולה יותר.
- הוספת 1.0 μl של דגימת DNA (~ ng 20-40), מכסה את הצלחת עםn דבק כיסוי אלומיניום ואז בעדינות מערבב אותו.
- צנטריפוגה ב 3,000 XG דקות 1. הסר את כיסוי האלומיניום ולהוסיף מזרן גומי איטום.
- מניחים את הצלחת על thermocycler ולהפעיל את תכנית רכיבה על אופניים הבאים מוצגת באיור 4.
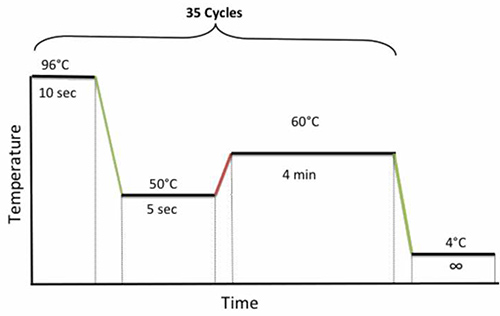
איור 4. תנאי רכיבה על אופניים ה-PCR עבור סידור. לחצו כאן לצפייה בתמונה גדולה יותר.
- כאשר מסיים PCR, לנקות את מוצר רצף באופן מיידי.
10. ניקוי רצף
- עבור כל תגובת רצף, לערבב 50 אתנול מוחלט μl ו5 μl 3 נתרן אצטט M.
- בעזרת פיפטה רבה, להוסיף 55 &# 956; ליטר של תמיסת נתרן אצטט / EtOH היטב כל אחד.
- לאטום בארות עם כיסוי אלומיניום דביק, על מנת להבטיח שכל אחד גם הוא חתום כראוי.
- צנטריפוגה ב 3,000 XG עבור 20 דקות.
- אחרי 20 דקות, להסיר כיסוי ולהפוך את הצלחת, בתנועה אחת חלקה, על רקמות במעבדה מקופלות (לא דופקים להיפטר supernatant כמו זה יהיה לעקור את גלולה!).
- צנטריפוגה את הצלחת ההפוכה על אותו הרקמה ב XG 150 למשך 2 דקות.
- מייד להוסיף 150 70% קרים μl EtOH. אל תתמהמהו תוספת של אתנול בשלב זה.
- חותם עם אותה עטיפת האלומיניום הדבקה ומערבולת.
- צנטריפוגה ב 3,000 XG במשך 5 דקות.
- הפוך צלחת על גבי רקמה חדשה מקופלת וצנטריפוגות ההפוכה ב XG 150 דקות 1.
- לאחר צנטריפוגה, המקום שנחשף בthermocycler ולייבש אותו ב-C ° 50 למשך 2 דקות.
- לאחר הצלחות היא יבשות, לאטום אותו עם מכסה נייר דבק, לעטוף בנייר כסף ולאחסן ב -20 C ˚ עד מוכן להמשיך wiה אלקטרופורזה רצף.
- כאשר מוכן רצף, לפזר מוצרי רצף ניקו ב10 מיליליטר פוראמיד Hi-Di, לפגל ועומס אלקטרופורזה.
11. ביואינפורמטיקה
- רצף עצרת
- הפעל את תכנית Geneious.
- צור תיקיית עבודה כדי לאחסן את הרצפים.
- ייבא את הקבצים שנוצרו על ידי ABI המכונה רצף לתיקיית העבודה שימוש באפשרות היבוא. Geneious יקצה ציון איכות אחוז עבור כל רצף המיובא.
- רצפים פתוחים עם ציוני איכות> 70% על ידי לחיצה כפולה עליהם.
- כל קובץ צריך לפתוח בחלון חדש. התוכנה תציין את האיכות בכל עמדת נוקלאוטיד של chromatogram של איכות הרצף באמצעות סורגים כחולים בהירים. שהפס גבוה יותר, טוב יותר את איכות שיחת הבסיס.
- באמצעות הסמן, בחר את הקטע באמצע של הרצף והשאיר את הקצוות, שהן בדרך כלל באיכות ירודה.
- לחץ על כפתור התמצית כדי לחלץ את האזור עם רצף באיכות טובה.
- בחר את כל ארבעת הרצפים שחולצו עבור כל דגימה ולהרכיב אותם נגד רצף התייחסות.
- בדוק את הרצף התאסף כדי לוודא שאתה נמצא במסגרת הקריאה הנכונה. אם אתם נמצאים במסגרת הקריאה הנכונה, תחילת פרוטאז צריכה להתחיל עם חומצות אמינו הבאות: PQITLW. תחילת RT תתחיל עם PISPIE.
- חלץ את אזור contig מכסה את תחילתו של יחסי הציבור לRT קודון 300th. במהלך תהליך זה, גם לבדוק לתוספות או השמטות.
- לעבור את רצף הקונצנזוס של contig חילוץ, זיהוי כל אי בהירויות ולאמת עמדות מעורבים בסיסים ידי בדיקת איכות (סימטריה, גובה, רקע וכתפיים של אזורי איגוף) של שיחות הבסיס.
- בחר את רצף הקונצנזוס ולחץ על לחצן התמצית ליצור קובץ נפרד של רצף הקונצנזוס מארבעה צבעי יסוד וLabel אותו כראוי.
- לייצא את הרצף לתיקיית גיבוי ואחסון במחשב או בתיקיית רשת.
- רצף הערכת איכות (HIVDB)
- לנתח את הרצף באמצעות תכנית HIVDB בhttp://hivdb.stanford.edu.
- הגעה למחיקות והוספות בנתוני הסיכום ולהבטיח כי הרצף מכסה את כל 99 פרוטאז קודונים (PR) ו300 קודונים RT 1.
- בדוק עבור כל מודגש אבטחת איכות נושאים (QA) בשני אזורי יחסי הציבור וRT, כגון קודונים הפסקה, משמרות מסגרת, עמדות מעורפלות ושאריות יוצאות דופן.
- בקרת איכות רצף
- הפיצוץ הרצף החדש מול מסד נתוני רצף מקומי קודמים ארוך.
- אם הרצף החדש הוא> 97% דומים לרצף כלשהו במסד הנתונים, את כל השלבים של הפרוטוקול צריכים להיבדק, החלו בניתוח הרצף וחוזרים למיצוי RNA לensurדואר שלא היו קופצים תמהיל (מיתוג מדגם, ואבחון לא נכון) או זיהום.
- אם אין בעיות מזוהות, לחזור על הניתוח של שתי דוגמאות הישנות וחדשים מהשלב מיצוי RNA.
- אם הרצפים עדיין> 97% דומים, לסקור את ההיסטוריה המטופל להעריך עבור כל הצמדה אפידמיולוגיים בין יחידים.
- ניתוח פילוגנטי
- יישר את כל הרצפים מבסיס הנתונים באמצעות תכנית ClustalW בGeneious.
- באופן ידני לבדוק את היישור לרצפים שאינם מיושרים כהלכה, מחיקות והוספות ולערוך בהתאם.
- לבנות עץ פילוגנטי באמצעות PHYML, בונה עץ Geneious או בוני עץ אחרים בGeneious.
- לבחון את העץ עבור דגימות עם אורכי סניף קצר.
- סקור את הדגימות עם אורכי סניף קצרים לזיהום אפשרי.
12. מידענות DB REGA
- הרצף Upload
- היכנס לRegaDB באמצעות שם משתמש וסיסמא ייחודיים.
- בתפריט הנפתח, תחת זהות של חולה, בחר "מתחילה עם".
- הוסף את קוד זיהוי המטופל ובחר את הפרט גנוטיפ הוא להיות נטען.
- בתפריט בצד השמאל, בחר באפשרות "לבודד נגיפי".
- מהאפשרויות תחת בודד נגיפי בחר "להוסיף".
- הזן את התאריך לדוגמא, מזהה לדוגמא, זיהוי הרצף ותאריך רצף.
- בחר באפשרות "לבחור קובץ", ולאחר מכן נווט לקובץ fasta של הרצף להיות נטען.
- לאחר בחירת קובץ fasta לצורך טעינה, לחץ על העלאה.
- ברגע שהרצף שהועלה מופיע בתיבת נוקלאוטיד תחת מזהה הרצף ותאריכים, לחץ על כפתור OK בפינה הימנית התחתונה של החלון.
- הגעה ליישור חלבון יחסי הציבור וRT על ידי לחיצה על כפתור החלבון ובחירה או יחסי ציבור או RT.
- בדקו את המוטציה עמידות לתרופה על ידי לחיצה על כפתור ההתנגדות. זה נותן ליאתה פרופילי התנגדות משלושה אלגוריתמים: ANRS, סטנפורד HIVDB וRegaDB.
- דו"ח ייצור באמצעות REGA
- היכנס לRegaDB באמצעות שם המשתמש הייחודי שלך ואת הסיסמה.
- בתפריט הנפתח, תחת זהות של חולה, בחר "מתחילה עם".
- הוסף את קוד זיהוי המטופל ובחר את האדם שהדו"ח שלה הוא להיות שנוצר.
- בתפריט בצד הימין, בחר לבודד נגיפי.
- מהאפשרויות תחת בודד נגיפי לחץ על "תצוגה".
- לחץ לחיצה כפולה על הבודד הנגיפי עבורו ברצונך ליצור דוח.
- על חלון הבודד הנגיפי, לחץ על כרטיסיית דו"ח בודד נגיפית.
- בחר את האלגוריתמים לפרשנות של גנוטיפ מתפריט הנפתח ולאחר מכן בחר תבנית דוח לשימוש.
- ברגע שהאלגוריתם והתבנית שנבחרו, לחץ על הכפתור "צור".
- הורד את מסמך rtf שנוצר.
- פתח את rtf לעשותcument כמסמך Word.
- שינוי הגודל של תרשים ההיסטוריה טיפול.
- לאחר התרשים, להוסיף את הסעיף "תרשים קליני ופרשנות התנגדות".
- תוך שימוש בנתונים על שולחן ההתנגדות והתרשים הקליני, להוסיף תיאור של פרופיל ההתנגדות של המטופל מתחיל עם היסטוריית הטיפול של החולה, והתרופות שלבודד הנגיף הוא עמידה. גם להוסיף תיאור של העומס הנגיפי של החולה ופרופילי ספירת תאי CD4 + מהתרשים.
- לשלוח את הדוח למחלות זיהומיות מומחה (ID) לביקורת והמלצות על ניהול מטופל בעתיד. תהליך זה הוא גם שלב בקרת איכות חשובה מאוד. כל שגיאות בגנוטיפ או inconsistences בהיסטוריה הטיפול, ניתן לזהות פרופילי virological והחיסוניים ובדיקה לפני דו"ח סופי נשלח, עם כל ההמלצות, למטפל ניהול המטופל.
תוצאות
שיטת תוקף הייתה שינוי של שיטה שדווחה בעבר 20. שיטת גנוטיפ Viroseq, אשר אושרה על ידי ה-FDA, הייתה בשימוש כשיטת ההתייחסות באימות. פנל של דגימות בדיקת מיומנות המתקבלות מהסוכנויות הלאומיות הצרפתית למחקר באיידס וצהבת נגיפית (ANRS) שימש בהשוואה העיקרית בין שתי השיטות. שתי שיטות genotyping היו 100% concordant בזיהוי כל המוטציות הקשורים עמידות לתרופה החשובה קליני כפי שפורש על ידי תכנית HIVDB לדגימות שהיו מוגבר בהצלחה על ידי שני השיטות. כפי שניתן לראות בטבלה 6, רצפי נוקליאוטידים של שלושה הזוגות היו 99.5% זהים. רצפי חומצות אמינו חזו היו 100% זהים. דגימה אחת מתוך חמישה לא יכולה להיות מוגברת בהצלחה על ידי Viroseq. בנוסף למדגם לא מוגבר על ידי Viroseq, השיטה בתוך הבית לא הצליחה להגביר דגימה שנייה שהוצגהכדי להיות וירוס במחזור רקומביננטי (CRF02_AG) על ידי Viroseq. שלוש הדגימות שמוגברות עם שני מתודולוגיות היו תת סוג B (שתי דוגמאות) ותת (מדגם אחד).
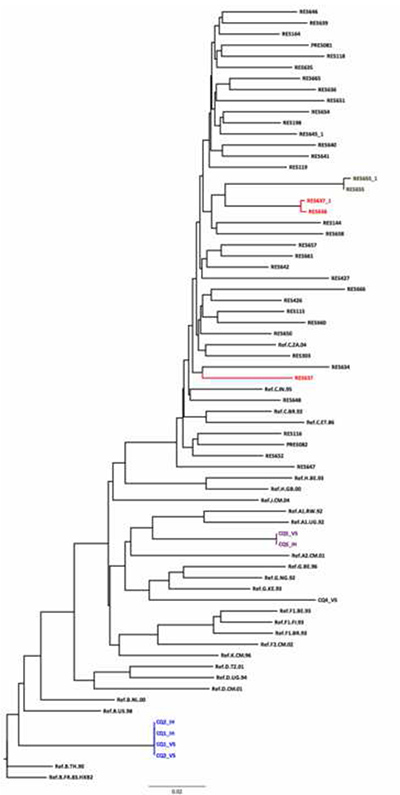
איור 5. שימוש בעץ השכן הצטרפות HKY נעשה כחלק מהבטחת איכות רצף. ישנם ארבעה זוגות / אשכולות של רצף עם מרחקים גנטיים קצרים מאוד. המרחק הגנטי בין RES655 וRES655_1 (דגימות אותו הרצף בימים שונים) הוא 0.003. היא טעות פוטנציאלית עם זוג RES637_1/RES638 כמרחק הגנטי שלהם הוא קצר מדי (0.075) לדגימות מאנשים epidemiologically לא צמודים שונים. יש RES637 אחר על העץ עם מרחק של 0.075 בהשוואה לRES638_1. אשכול CQ01/CQ02 עולה כי שתי דגימותמלוח הן כפילויות של המדגם זהה. הם מתקבצים יחד עם רצף ההתייחסות תת הסוג B המאשר את תת הוקצה על ידי כלי REGA Subtyping. CQ05 וCQ04 התקבצו עם תת ו-G בהתאמה, ואילו כלי subtyping REGA סיווג אותם וכCRF02_AG בהתאמה. כלי שימושי נוסף לsubtyping HIV ורקומבינציה הוא SCUEL, אשר זמין בhttp://www.datamonkey.org. לחץ כאן לצפייה בתמונה גדולה יותר.
פנל של חמש דגימות שימש כדי להעריך את רמת הדיוק של שיטת in-house. עשרה גנוטיפים לשכפל נוצרו לכל אחד מחמש הדגימות. באמצעות המנתח הגנטי 16 נימי 3130xl, 48 של 50 גנוטיפים נוצרו מ24 ריצות, שהוכנו באותו היום. לכל חמש דגימות, רצפי חומצות אמינו חזו היו 100% concordant בין משכפל. לרצפי חומצות, ה הגרעיןפה היה> 99% דמיון pairwise.
בשנתיים הראשונות של השימוש בשיטה זו, דגימות שישים חזרו על עצמם באופן אקראי ממיצוי RNA רצף. לא היו הבדלים משמעותיים סטטיסטי בין ציון איכות הרצף ובמספר מעורבים בסיסים בין משכפל. השוואות pairwise שני נוקליאוטידים וחומצות אמינו לזוגות שישים היו גדולים יותר מ99% זהות. לכן מוטציות עמידות לתרופות לכל הזוגות היו 100% תואמות.
הפחתת עלויות
כרכי התגובה לRT, PCR וסדר הופחתו בחצי לפחות, ביחס לשיטה המקורית 20, 32, מבלי להתפשר על האיכות של הרצפים שנוצרו. זה אפשר הפחתה בעלות של 50% לשלבי RT וה-PCR.
השיטה החדשה תוכננה במקור לעבודה עם שישה פריימר רצף רצף כל 99 קודונים של גן פרוטאז ו300 קודונים הראשונים של הגן ההפוך טרנסקריפטאז 20, 32. שיטות דומות גם להשתמש בשש עד שמונה פריימרים 33, 34. כמה שיטות שפורסמו לאחרונה השתמשו בפחות משישה צבעי יסוד, לפעמים למרות רצף פרוטאז וגני RT seprately 35, 36. אנחנו ביקשנו לצמצם את מספר פריימרים רצף 6-4, (איור 6)
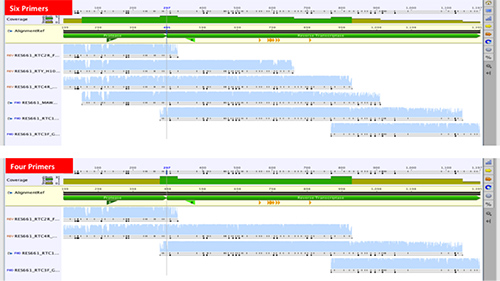
איור 6. השוואה של רצפים רציפים משישה לעומת ארבעה פריימרים רצף לדור של רצף Pol 1197 נ"ב המכסה את כל 99 קודונים פרוטאז ה-HIV-1 ו300 קודונים הראשונים של גן reverse transcriptase.242/51242fig6highres.jpg "target =" _blank "> לחץ כאן לצפייה בתמונה גדולה יותר.
רצפים מסט של 17 דגימות שנוצרו משישה פריימרים הושוו לרצפים שנוצרו לאחר ההרחקה של שני פריימרים (MAW46 וrty). תת היו 14 C תת, שני תת סוג B, וא 'תת סוג אחד לא היו הבדלים משמעותיים בציוני איכות רצף. שוב, את זהות pairwise הממוצעת בין 17 הזוגות של חומצות גרעין הייתה 99% ו100% ברמת חומצת אמינו. לפיכך, הפחתת פריימרים רצף 6-4 הביאה לירידה בעלות רצף בכמעט שליש.
כלי תוכנת הקניינית רק בשימוש בפרוטוקול זה היה Geneious להרכבת רצף. כלי פרשנות עמידות לתרופות, כמו גם את הדו"ח יצירת כלים כל כלים חופשיים, פתוחים גישה. פעולה זו מפחיתה את העלות נוספת על ידי ביטול את העלויות כרוכות בשימוש בתוכנת קניינית. יתר על כן, collectivמשא ומתן דואר אפשר ריאגנטים לפרוטוקול זה להיות ארוז בערכה לגישה קלה מחיים טכנולוגיים וזמין כטכנולוגיות שבתאי / החיים genotyping שיטה 37. יתר על כן, חברי שבתאי יכולים לגשת לחומרים כימיים במחיר מוזל.
הגדרה קלינית
הפרוטוקול המתואר יושם בניטור והמעקב של עמידות לתרופות בקהילה כפרית בקוואזולו נטאל. כולל של 604 גנוטיפים נוצרו מדגימות קליניות בין דצמבר 2010 ומאי 2013 בקצב הגברה של 95% לדגימות עם עומס נגיפי> 1,000 RNA עותקים / מיליליטר. מחקר עמידות לתרופה זו קלינית HIV אושר על ידי ועדת המחקר ביו רפואת האתיקה של אוניברסיטת קוואזולו נטאל (BF052/10 אסמכתא) והוועדה לחקר הבריאות של מחלקת קוואזולו נטאל לבריאות (מס 'אסמכתא HRKM 176/10). דיווחי חולה בודדים שהופקו ונשלחו בחזרה למרפאותלניהול מטופל.
שבעים ושניים (72) גנוטיפים גם נוצרו כחלק ממעקב של מחקר עמידות לתרופות משודר, מקוננים בתוך מחקר גדול המבוסס על אוכלוסייה פוטנציאלי HIV מעקב. הדגימות ראשוניות היו דם כל זין מחט שנאסף בmicrotubes EDTA. בגנוטיפ היה שיעור הגברה של 79% 19. אישור אתי לגנוטיפ של דגימות ממחקר המעקב הושג מאוניברסיטת ועדת המחקר ביו קוואזולו נטאל אתיקה (BE066107 אסמכתא).
| שם פריימר | רצף | משך | הוראה | תפקיד HXB2 | |
| לוע-26 | TTGGAAATGTGGAAA GGAAGGAC | 23 | קדימה | 2028-2050 | סיבוב 1 PCR |
| RT-21 | CTGTATTTCAGCTATC AAGTCCTTTGATGGG | ביום 31 | הפוך | 3539-3509 | סיבוב 1 PCR |
| Pro-1 | TAGAGCCAACAGCCC CACCA | 20 | קדימה | 2147-2166 | PCR סיבוב 2 |
| RT-20 | CTGCCAATTCTAATTC TGCTTC | 22 | הפוך | 3462-3441 | PCR סיבוב 2 |
| RTC1F | ACCTACACCTGTCAA CATAATTG | 23 | קדימה | 2486-2508 | רצף |
| RTC2R | TGTCAATGGCCATTG TTTAACCTTTGG | 27 | הפוך | 2630-2604 | רצף |
| RTC3F | CACCAGGGATTAGAT ATCAATATAATGTGC | 30 | קדימה | 2956-2994 | רצף |
| RTC4R | CTAAATCAGATCCTAC ATACAAGTCATCC | 29 | הפוך | 3129-3101 | רצף |
| RT-y | GTGTCTCATTGTTTAT ACTAGG | 22 | הפוך | 2967-2946 | רצף |
| לוע-46 | TCCCTCAGATCACTC TTTGGCAACGAC | 27 | קדימה | 2251-2277 | רצף |
טבלת 1. שעתוק הפוך, PCR, ופריימרים מותאמים אישית רצף בשימוש בדורו של שבר 1197 Pol נ"ב המכסה את כל 99 קודונים פרוטאז ה-HIV-1 ו300 קודונים הראשונים של גן trascriptase ההפוך.
| RT21 (5pmol/ml) | 0.5 | 0.2 |
| dNTP (10 מ"מ) | 0.5 | 0.4 |
| סך הכל | 1 |
טבלה 2. dNTP / פריימר לערבב לתגובת השעתוק ההפוכה.
| מגיב | נפח / תגובה (מיליליטר) | ריכוז / תגובה |
| הראשון סטרנד חוצץ (10x) | 1 | 1 |
| MgCl 2 (25 מ"מ) | 2 | 4 |
| DTT (0.1 ז) | 1 | 0.008 |
| RNaseOUT (40 U / ml) | 0.5 | 16 |
| כתב עילי III הפוך transcriptase (200U/ml) | 0.5 | 8 |
| סך הכל | 5 |
לוח 3. אנזים לערבב לתגובת השעתוק ההפוכה.
| מגיב | נפח / תגובה (מיליליטר) | ריכוז סופי / תגובה |
| מים שטופלו DEPC | 18.4 | - |
| PCR חוצץ (10x) | 2.5 | 1 |
| MgCI 2 (50 מ"מ) | 1 | 2 |
| תמהיל dNTP (10 מ"מ) | 0.5 | 0.2 |
| פריימר froward (5 pmol / ml) | 0.25 | 0.05 |
| פריימר ההפוך (5 pmol / ml) | 0.25 | 0.05 |
| פלטינום תקי פולימראז (5 U / ml) | 0.1 | 0.02 |
| סיכום ביניים | 23 | - |
לוח 4. תערובת אב PCR המקונן.
| מגיב | נפח / תגובה (מיליליטר) | ריכוז / תגובה |
| מים שטופלו DEPC | 6.1 | |
| רצף חוצץ (5x) | 2 | 1 |
| פריימר (3.2 pmol / ml) | 0.5 | 0.16 |
| תמהיל רצף גדול דיי שליחות קטלנית | 0.4 | - |
| סך הכל | 9 |
לוח 5. מיקס מאסטר לתגובות רצף.
| Viroseq | Inhouse | % דמיון NA | |||||||
| מזהה לדוגמה | סוג משנה | ציון איכות | מוטציות יחסי הציבור | מוטציות RT | סוג משנה | ציון איכות | מוטציות יחסי ציבור | מוטציות RT | |
| CQ01 | ב ' | 99.9 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | ב ' | 99.2 | M46L, I54L, V82, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | 100 |
| CQ02 | ב ' | 99.5 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | ב ' | 99.5 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | 100 |
| CQ03 | NA | NA | NA | NA | NA | NA | |||
| CQ04 | CRF02_AG | 98.4 | I54V, V82F, I84V | M41L, L74I, L210W, T215Y, V108I, Y181C | NA | NA | NA | NA | NA |
| CQ05 | 99.7 | K103N | 93 | K103N | 100 | ||||
לוח 6. resul השוואתיts מניתוח קבלה בין שיטת גנוטיפ Viroseq והשיטה בבית באמצעות פנל של דגימות הניתן על ידי ANRS.
Discussion
שיטות בבית כמה עלות הנמוכה תוארו במאמצים כדי לנסות להפוך את גנוטיפ עמידות לתרופות HIV זול יותר 33, 34, 36. אין ספק בצורך לשלב בדיקת עמידות לתרופות לרצף של טיפול עבור אנשים בטיפול תרופתי במשאב מוגבל הגדרות. עם זאת, רוב השיטות דיווחו להתמקד ביישום של גנוטיפ עמידות לתרופה במעקב של עמידות לתרופות ברמת אוכלוסייה. שיטת גנוטיפ שבתאי / חיים טכנולוגיות היא פרוטוקול משולב במלואם למעקב וניטור של עמידות לתרופות. שיטה זו נועדה להיות פרוטוקול סביר יישום בעיקר קוד פתוח ומשאבים ביואינפורמטיקה הגישה פתוחים לפרשנות של עמידות לתרופות והפקת דוחות לניהול קליני.
זה היה הראה באמצעות השוואה עם שיטת גנוטיפ Viroseq אישרה ה-FDA להיותמדויק בזיהוי מוטציות עמידות לתרופות מפנל של דגימות בדיקת מיומנות ANRS, בפנל של דגימות מעבדה שהיו מוגברות בהצלחה 100%. הדיוק הוערך גם על דגימות קליניות של וירוסי C תת סוג, תת הסוג הדומיננטי ביותר בדרום אפריקה. השיטה הייתה מדויקת כעל דגימות C תת כפי שהיה בתת הסוג A ו-B עם זאת, אם השיטה הייתה בשימוש בחלקים אחרים של העולם שבו CRF02_AG נפוץ, יש צורך בשינוי של פריימרים מאז השיטה לא הצליח להגביר את אחד המדגמים הפנל שהוצג לי CRF02_AG. לחלופין, סט מנוון של פריימרים רגישים לכל הקבוצה M וירוסי 33, 36 יכולים לשמש באזורים שבם החלוקה תת הסוג היא יותר הטרוגנית 38.
הרגישות של השעתוק לאחור וPCR יכולה להיות מוגברת על ידי מיצוי RNA מכמויות גבוהות יותר של פלזמה, כמו 500 מיליליטר. הפלזמה ניתן centrifuged ב21,000 XG במשך 90 דקות להתרכז חלקיקים נגיפיים לפני שתמשיך עם הפרוטוקול כפי שתואר על ידי ערכת מיני מיצוי RNA QIAamp נגיפית.
כפי שניתן לראות, יש לו את השיטה החדשה יתרון נוסף שהיא מייצרת דו"חות מקיפים לניהול מטופל. דוחות אלה הם איחוד של גנוטיפ, חיסוני ונתוני ניטור virologic כמו גם היסטוריה קלינית וטיפול מRegaDB. זו מלווה בפרשנות מעבדה מפורטת של פרופיל ההתנגדות ואחריו ביקורת באותה מידה מפורטת של ההיסטוריה הקלינית של המטופל, כמו גם המלצות לטיפול. השימוש ברופאים מומחה כדי לבדוק את הדיווחים ולספק המלצות לטיפול בחולים מספק הדרכה נחוצה עבור מתרגל אחות, כמו גם רופאים לא מנוסים, שיותר ויותר לספק לאמנות בדרום אפריקה כחלק מהמלצות ארגון הבריאות העולמי להסטת משימה. אלה קלינייםדיווחים הוכחו להיות עזרי הוראה יעילים לרופאים עם מעט או ללא ניסיון בניהול עמידות לתרופה. מנקודת מבט של מטופל, השיטה שלנו מקטינה את הצורך לנסוע לאתרים מרכזיים לגישה לשירותי HIV מומחה.
לפיכך, הפרוטוקול המתואר כמכלול מספק פלטפורמה טובה שדרכו ניתן לשלב בניהול עמידות לתרופות ב-HIV, במחיר סביר, לרצף של טיפול לאמנות שלא הצליחו אנשים נגועים ב-HIV. נתונים שנוצרו יכולים לשמש למטרות אפידמיולוגיים על מנת להעריך את ההתפתחות והעברה של עמידות לתרופות בקהילה. גודלו של הבר לקים שנוצר הוא מספיק טוב לניתוח פילוגנטי מורכב יותר אשר ייצר הבנה טובה יותר של המגיפה ברמת אוכלוסייה.
Disclosures
עבודה זו נתמכה על ידי קרן Wellcome (082384/Z/07/Z), האיחוד האירופי (סנטה 2007 147-790), המרכז האמריקאי למחלות לשלוט באמצעות CAPRISA (כותרת פרויקט: מערכות בריאות חיזוק וכישלון הטיפול ב-HIV (איידס TFC)), ושויצרי דרום אפריקאי משותפת תכנית מחקר (SSJRP) "השוויצרית Prot / דרום אפריקה: חלבון ביואינפורמטיקה פיתוח משאבים לפתוגנים חשובים הקשורים לבריאות" מענק מחקר שכותרתו (090,999 / ת מספר מענק RL נתמך על ידי קרן Wellcome. / 09 / ת). הממנים לא היו תפקיד בעיצוב מחקר, איסוף נתונים וניתוח, החלטה לפרסם, או הכנה של כתב היד. המחברים מצהירים שום אינטרסים כלכליים מתחרים.
Acknowledgements
המחברים מבקשים להודות לכל העמיתים שעשו את עבודה זה אפשרי, במיוחד מאיה Balamane, אליזבת לבנה ג'ונסטון, שרון Sjoblom, גרג Ording Zakhona Gumede, Xolile Kineri, Phindile Mabaso, Lungisa Ndwandwe, ג'יימס גארווי, גאווין קוב, Senzo Maphanga, Terusha Chetty , Kevi Naidoo, אנדרו Skingsley, קתרין סטוט, וLungani Ndwandwe. המחברים רוצים גם להודות לכל אנשים של מחלקת בריאות ומרכז אפריקה אנשים שעובדים Hlabisa HIV הטיפול וטיפוח לתכנית.
Materials
| Name | Company | Catalog Number | Comments |
| Superscript III 1st strand Synthesis kit | Life Technologies | 18080051 | Reverse Transcription |
| SATURN/LiFE Technologies Custom Primers | Life Technologies | 4473517 | PCR |
| Platinum Taq | Life Technologies | 10966026 | PCR |
| PureLink QUICK PCR Purification Kit | Life Technologies | K310002 | PCR |
| Viroseq | ABBOTT | 4J94-20 | Reverse Transcription and PCR |
| Agarose Tablets (Dnase/Rnase free) | BIOLINE | BIO-41027 | PCR |
| TBE Buffer | MERCK | 1.06177.2500 | PCR |
| O'Range Ruler 200 bp DNA Ladder | Fermentas | FE SM0633 | PCR |
| Novel Juice | GeneDireX | LD001-1000 | PCR |
| MiniBis Bioimaging System | DNR Bioimaging Systems Ltd | Gel Documentation | |
| Power Pac 300 | BIORAD | Gel Electrophoresis | |
| Big Dye Terminator Kit version 3.1 | Life Technologies | 4337456 | Sequencing |
| Arrays | Life Technolgies | 4319899 | Sequencing |
| PoP | Life Technologies | 4363785 | Sequencing |
| 10x EDTA Buffer | Life Technologies | 402824 | Sequencing |
| Formamide | Life Technologies | 4311320 | Sequencing |
| 5x Sequencing Buffer | Life Tecgnologies | 4336697 | Sequencing |
| 3130 xl Genetic Analyzer | Life Technologies | Sequencing | |
| GeneAmp PCR System 9700 | Life Technologies | RT/PCR/Sequencing | |
| Centrifuge 5804 | EPPENDORF | Sample Processing | |
| Centrifuge 5415R | EPPENDORF | RNA Extraction | |
| Centrifuge 5415R | EPPENDORF | RT and PCR | |
| Centrifuge 5415D | EPPENDORF | PCR Product Clean up | |
| Centrifuge 5810 | EPPENDORF | Sequencing Clean up | |
| Picofuge | BIORAD | C1301-230V | RT and PCR |
| Vortex Genius 3 | IKA | RNA extraction and reagent preparation | |
| Vortex mixer | IKA | Sequencing Cleanup | |
| NanoDrop 2000 UV/VIS spectrophotometer | ThermoScientific | DNA quantification | |
| 3 M Sodium Acetate | MERCK | 567422 | Sequencing Clean up |
| Absolute Ethanol | MERCK | SAAR2233540LP | Sequencing Cleanup |
| 1.5 ml SARSTEDT Tubes | BIODEX | 72.692.005 | RNA Extraction |
| 2 ml SARSTEDT Tubes | BIODEX | 72.693.005 | RNA Extraction |
| 2 ml Collection tubes | SCIENTIFIC GROUP | MCT-200-NC/S | RNA Extraction |
| Optical MicroAmp 96-well reaction plates | Life Technologies | N8010560 | Sequencing |
| 200 µl 8 Strip StarPCR Tubes with attached flat caps | STAR Lab - supplied by CELTIC | A1402-3700 | RT and PCR |
| 200 µl PCR individual tubes | Scientific Group | CR/3745 | RT and PCR |
| Geneious | Biomatters | Sequence analysis | |
| Internet Access | Preferrably high speed | ||
| Web resources | |||
| hivdb.stanford.edu | Stanford University | Drug reistance analysis | |
| http://bioafrica.mrc.ac.za:8080/regadb-ui/RegaDB | SATuRN | database | |
| http://bioafrica.mrc.ac.za/tools/pppweb.html | SATuRN | Sequence quality tool | |
References
- Shao, Y., Williamson, C. The HIV-1 epidemic: low- to middle-income countries. Cold Spring Harbor Persp. Med. 2, (2012).
- Mutevedzi, P. C., et al. Scale-up of a decentralized HIV treatment programme in rural KwaZulu-Natal, South Africa: does rapid expansion affect patient outcomes. Bull. World Health Organ. 88, 593-600 (2010).
- Houlihan, C. F., et al. Cohort profile: Hlabisa HIV treatment and care programme. Int. J. Epidemiol. 40, 318-326 (2011).
- Tanser, F., Barnighausen, T., Grapsa, E., Zaidi, J., Newell, M. L. High coverage of ART associated with decline in risk of HIV acquisition in rural KwaZulu-Natal. South Africa. Science. 339, 966-971 (2013).
- Bor, J., Herbst, A. J., Newell, M. L., Barnighausen, T. Increases in adult life expectancy in rural South Africa: valuing the scale-up of HIV treatment. Science. 339, 961-965 (2013).
- Montaner, J. S., et al. The case for expanding access to highly active antiretroviral therapy to curb the growth of the HIV epidemic. Lancet. 368, 531-536 (2006).
- Granich, R. M., Gilks, C. F., Dye, C., De Cock, K. M., Williams, B. G. Universal voluntary HIV testing with immediate antiretroviral therapy as a strategy for elimination of HIV transmission: a mathematical model. Lancet. 373, 48-57 (2009).
- Johnson, L. F., et al. Life expectancies of South african adults starting antiretroviral treatment: collaborative analysis of cohort studies. PLoS Med. 10, (2013).
- Blower, S., Ma, L., Farmer, P., Koenig, S. Predicting the impact of antiretrovirals in resource-poor settings: preventing HIV infections whilst controlling drug resistance. Curr. Drug Targets. 3, 345-353 (2003).
- Geretti, A. M. Epidemiology of antiretroviral drug resistance in drug-naive persons. Curr. Opin. Infect. Dis. 20, 22-32 (2007).
- Larder, B. A., Darby, G., Richman, D. D. HIV with reduced sensitivity to zidovudine (AZT) isolated during prolonged therapy. Science. 243, 1731-1734 (1989).
- Erice, A., et al. Brief report: primary infection with zidovudine-resistant human immunodeficiency virus type 1. N. Engl. J. Med. 328, 1163-1165 (1993).
- Williams, I., et al. British HIV Association guidelines for the treatment of HIV-1-positive adults with antiretroviral therapy. HIV Med. 13 Suppl 2, 1-85 (2012).
- DHHS, . US Panel on Antiretroviral Guidelines for Adults and Adolescents. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. , (2012).
- Vandamme, A. M., et al. European recommendations for the clinical use of HIV drug resistance testing: 2011 update. AIDS Rev. 13, 77-108 (2011).
- DHHS, . US Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children. Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection. , (2012).
- . Department of Health. Clinical guidelines for the management of HIV & AIDS in adults and adolescents. , (2010).
- Conradie, F., et al. The 2012 southern African ARV drug resistance testing guidelines. S. Afr. J.HIV Med. 13, 162-167 (2012).
- Manasa, J., et al. Primary Drug Resistance in South Africa: Data from 10 Years of Surveys. AIDS Res. Hum. Retroviruses. 28, 558-565 (2012).
- Tshabalala, M., et al. Surveillance of transmitted antiretroviral drug resistance among HIV-1 infected women attending antenatal clinics in Chitungwiza, Zimbabwe. PLoS ONE. 6, (2011).
- Bartolo, I., et al. Antiretroviral drug resistance surveillance among treatment-naive human immunodeficiency virus type 1-infected individuals in Angola: evidence for low level of transmitted drug resistance. Antimicrob. Agents Chemother. 53, 3156-3158 (2009).
- Bartolo, I., et al. HIV-1 genetic diversity and transmitted drug resistance in health care settings in Maputo, Mozambique. J. Acquir. Immune Defic. Syndr. 51, 323-331 (2009).
- Hamers, R. L., et al. HIV-1 drug resistance in antiretroviral-naive individuals in sub-Saharan Africa after rollout of antiretroviral therapy: a multicentre observational study. Lancet Infect. Dis. 11, 750-759 (2011).
- Hamers, R. L., et al. HIV-1 Drug Resistance Mutations Are Present in Six Percent of Persons Initiating Antiretroviral Therapy in Lusaka, Zambia. J. Acquir. Immune Defic. Syndr. , (2010).
- Nwobegahay, J., Selabe, G., Ndjeka, N. O., Manhaeve, C., Bessong, P. O. Low prevalence of transmitted genetic drug resistance in a cohort of HIV infected naive patients entering antiretroviral treatment programs at two sites in northern South Africa. J. Med. Virol. 84, 1839-1843 (2012).
- Iweriebor, B. C., et al. Molecular epidemiology of HIV in two highly endemic areas of northeastern South Africa. Arch. Virol. 157, 455-465 (2012).
- Parboosing, R., Naidoo, A., Gordon, M., Taylor, M., Vella, V. Resistance to antiretroviral drugs in newly diagnosed, young treatment-naive HIV-positive pregnant women in the province of KwaZulu-Natal South Africa. J. Med. Virol. 83, 1508-1513 (2011).
- Nwobegahay, J. M., et al. Prevalence of antiretroviral drug resistance mutations and HIV-I subtypes among newly-diagnosed drug-naive persons visiting a voluntary testing and counselling centre in northeastern South Africa. J. Health Popul. Nutr. 29, 303-309 (2011).
- Nwobegahay, J., et al. Prevalence of drug-resistant mutations in newly diagnosed drug-naive HIV-1-infected individuals in a treatment site in the waterberg district, limpopo province). S. Afr. Med. J. 101 (2011), 335-337 (2011).
- Rosen, S., Long, L., Sanne, I., Stevens, W. S., Fox, M. P. The net cost of incorporating resistance testing into HIV/AIDS treatment in South Africa: a Markov model with primary data. J. Int. AIDS Soc. 14, 24 (2011).
- Dalai, S. C., et al. Evolution and molecular epidemiology of subtype C HIV-1 in Zimbabwe. AIDS. 23, 2523-2532 (2009).
- Chen, J. H., et al. In-house human immunodeficiency virus-1 genotype resistance testing to determine highly active antiretroviral therapy resistance mutations in Hong Kong. Hong Kong Med. 18, 20-24 (2012).
- Lee, C. K., et al. An in-house HIV genotyping assay for the detection of drug resistance mutations in Southeast Asian patients infected with HIV-1. J. Med. Virol. 84, 394-401 (2012).
- Aitken, S. C., et al. A Pragmatic Approach to HIV-1 Drug Resistance Determination in Resource-Limited Settings by Use of a Novel Genotyping Assay Targeting the Reverse Transcriptase-Encoding Region Only. J. Clin. Microbiol. 51, 1757-1761 (2013).
- Zhou, Z., et al. Optimization of a low cost and broadly sensitive genotyping assay for HIV-1 drug resistance surveillance and monitoring in resource-limited settings. PLoS One. 6, (2011).
- , Life Technologies. Life Technologies and SATuRN Collaborate to Increase Access to HIV Testing in Africa. , (2012).
- Lihana, R. W., Ssemwanga, D., Abimiku, A., Ndembi, N. Update on HIV-1 diversity in Africa: a decade in review. AIDS Rev. 14, 83-100 (2012).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved