A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
שיטה כללית לגילוי Nitrosamide היווצרות בחילוף החומרים במבחנה של Nitrosamines מאת ציטוכרום P450s
In This Article
Summary
Α-hydroxylation של nitrosamines מסרטנים מאת ציטוכרום P450s הוא מסלול מטבולי מקובל שמייצר מזיקות-DNA intermediates, לגרום מוטציות. עם זאת, נתונים חדשים מציין עוד חמצון כדי nitrosamides יכול להתרחש. אנו מתארים גנרל שיטה לגילוי nitrosamides המופק במבחנה ציטוכרום P450 מזורז מטבוליזם של nitrosamines.
Abstract
N-nitrosamines הם קבוצת חומרים מסרטנים סביבתי, אשר דורשים ציטוכרום P450 חמצון להפגין פעילות ומבוססת. המנגנון המקובל של הפעלת מטבולית כרוך היווצרות α-hydroxynitrosamines המפרקות באופן ספונטני לסוכנים החומר הדנ א. הצטברות של נזק לדנ א של מוטציות וכתוצאה מכך יכול בסופו של דבר להוביל לסרטן. ראיות חדשות מציין כי α-hydroxynitrosamines יכול להיות עוד יותר מחומצן כדי nitrosamides processively על-ידי ציטוכרום P450s. מאחר nitrosamides הם בדרך כלל יציבים יותר α-hydroxynitrosamines אפשר גם alkylate ה-DNA, nitrosamides עשוי לשחק תפקיד carcinogenesis. בדו ח זה, אנו מתארים פרוטוקול כללי עבור הערכת ייצור nitrosamide מ במבחנה ציטוכרום P450 מזורז חילוף החומרים של nitrosamines. פרוטוקול זה מנצל הגישה הכללית של הסינתזה בין את nitrosamides הרלוונטי של במבחנה ציטוכרום P450 חילוף החומרים assay באמצעות ספקטרומטר מסה של טנדם יינון שגובהו ברזולוציה של כרומטוגרפיה נוזלית-nanospray לצורך זיהוי. שיטה זו מתגלה N′- nitrosonorcotinine כמו מטבוליט מינור של N′- nitrosonornicotine במחקר דוגמה. השיטה יש רגישות גבוהה וזיהוי המוני בשל באופן סלקטיבי מדויק. יישום השיטה הזאת למגוון רחב של מערכות nitrosamine-ציטוכרום P450 יעזרו לקבוע את הכלליות של השינוי הזה. הבנה טובה יותר של היווצרות nitrosamide יכול לסייע מכיוון ציטוכרום P450s הן רב-צורתיות משתנות בפעילות, להערכת הסיכון לסרטן בודדים.
Introduction
N-nitrosamines הם קבוצה גדולה של חומרים מסרטנים נמצאו הדיאטה, מוצרי טבק, ואיכות הסביבה הכללית; הם יכולים גם להיות הקימו endogenously גוף האדם1. יותר מ-300 N -nitroso תרכובות נבדקו, > 90% הוערכו מסרטנים כמו בחיה מודלים2,3. להפגין את carcinogenicity שלהם, תרכובות אלו צריך קודם להיות מופעל על ידי ציטוכרום P450s1,2,3. מחקרים מראים כי ציטוכרום P450s ברצון נישחק nitrosamines כדי α-hydroxynitrosamines (איור 1), אשר הם תרכובות תגובתי עם מחצית החיים של ~ 5 s לפני נרקב באופן ספונטני כדי alkyldiazohydroxides. האחרון יכול alkylate דנ א לאחר ההפסד של H2O ו- N2. ה-DNA שנוצר adducts, אם לא מתוקן, יכול לגרום מוטציות, במקרה של onco קריטי - או גנים משתיק קול של גידול, להוביל לפיתוח סרטן1. מסיבה זו, יש כבר שהושקעו מאמצים להשיג הבנה מלאה מסלולים מטבוליים, אן adducts, ואת הזרם מטבוליטים של ציטוכרום P450 חמצון של nitrosamines מסרטנים. הידע הזה יש פוטנציאל היישום הערכת סיכון סרטן בודדים4.
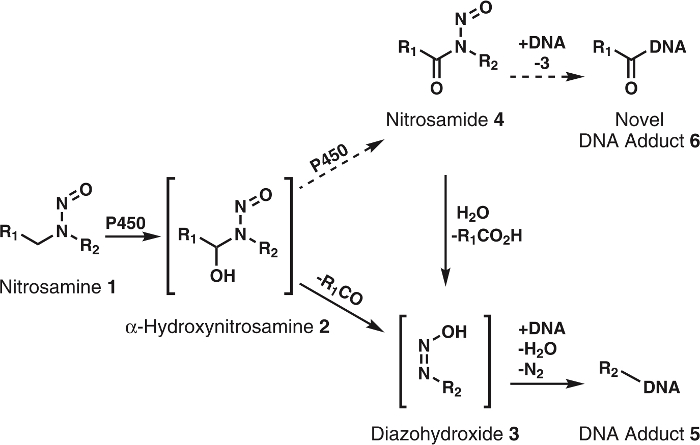
איור 1: גנרל וחילוף החומרים המוצע של nitrosamines.
Nitrosamines (1) הם תחמוצת על-ידי P450s כדי α-hydroxynitrosamines (2) המפרקות באופן ספונטני כדי alkyldiazohydroxides (3). תרכובות אלו יכולים לאגד הדנ א על טופס שה-DNA adducts. זה המשוערות הזה 2 יש נוספת תחמוצת על-ידי P450s nitrosamides 4. אלה ניתן ישירות לאגד ל- DNA טופס DNA הרומן adducts או להיות הידרוליזה ל 3 לטופס ש-DNA הידוע adducts. R1 ו- R2 מייצגים כל אלקיל קבוצה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של הדמות הזאת.
למרות ההנחה α-hydroxynitrosamine נתמך באופן יציב על ידי נתונים מקיפים, יש כמה סתירות; אחד גדול הוא זמן מחצית החיים הקצר של α-hydroxynitrosamines5,6. ידוע כי תרכובות אלו מיוצרים בחברת קרום רשתית תוך-פלזמית, אחר כך alkylate DNA גרעיני. בהתחשב חייהם של כמה שניות, זה הוא תמוה איך intermediates האלה לשרוד המסע הנדרש אבל את ציטוזול. אחת ההשערות היא כי חלק של α-hydroxynitrosamines הם processively מחומצן nitrosamides7,8, אשר יציבים למדי השוואה9. זה ככל הנראה להתרחש דרך השמירה של α-hydroxynitrosamines ציטוכרום P450 פעילה באתר. כבר ראיתי תקדים עבור סוג זה של חמצון עם ניקוטין10, כהלים11ו12,alkylnitrosamines פשוט13. בנוסף, nitrosamides הם ישיר אקטינג מסרטנים2,3. על סמך שלהם תגובתיות9, תרכובות אלו הם האמינו להפקת DNA adducts זהים לאלו הנובעות α-hydroxynitrosamines יחד עם חדש, ה-DNA נחקרו adducts (איור 1). לכן, השערה זו לא רק מסביר התחבורה באמצעות ציטוזול, אלא גם היווצרות של ה-DNA נזק מוצרים.
בנייר זה, מתואר פרוטוקול כללי להערכת במבחנה ציטוכרום P450 בתיווך המרה של nitrosamines ל- nitrosamides. ההמרה שדווחה בעבר של N′- nitrosonornicotine (NNN) N′- nitrosonorcotinine (NNC) על ידי ציטוכרום P450 2A6 הצור דוגמה14. יישום של פרוטוקול זה על מגוון רחב של מערכות אנזים-סובסטרט יעזרו לקבוע את החשיבות של nitrosamides בחילוף החומרים nitrosamine הכללית.
Access restricted. Please log in or start a trial to view this content.
Protocol
1. חומרים, שגרות כלליות
- Synthesize NNN כאמור תיאר 15. להשיג norcotinine, P450 2A6 Baculosomes, nadph ל התחדשות מערכת, 0.5 x תגובת מאגר וכל כל כימיקלים אחרים או ממיסים ממקורות מסחריים בכיתה ריאגנט.
- ספקטרום NMR רשומה על ספקטרומטר 500 מגה-הרץ. דוח כימית משתנה בהתאם חלקים למיליון (ppm). כדי להשתמש פסגות הממס שיורית הפניות פנימיות 1 H-NMR (7.26 ppm CDCl 3) 13 C-NMR (77.2 ppm CDCl 3).
הערה: שיא פיצול להשתמש בקיצורים הבאים: s = גופיה, d = כפיל, dd = כפיל של doublets, dt = כפיל של שלישייה, dq = כפיל של רביעיות, ddd = כפיל של כפיל של doublets ו- m = multiplet. - לבצע ספקטרומטר מסה ברזולוציה גבוהה (HRMS) עבור תרכובות שנבחרו על LTQ Orbitrap Velos ונתונים ח כ מ/z.
- שימוש polygram מראש מצופה לוחות סיליקה ג'ל TLC (40 מ מ x 80 מ מ, בעובי 0.2 מ מ) 254 ננומטר מחוון פלורסנט עבור שכבת דק כרומטוגרפיה (TLC). דמיינו TLC צלחות על ידי הקרנת מנורת UV.
- לבצע כרומטוגרפיה פלאש על 60, 70-150 רשת סיליקה ג'ל באמצעות עמודה זכוכית 1.5 ס"מ על 15 ס"מ.
2. הכנת בקרה חיובית nitrosamide (N ′-nitrosonorcotinine, NNC)
- יבש, בתנור למשך הלילה (16 h, ~ 140 ° C), 25 מ ל, סיבוב המדרגה הבקבוק המכילה בר מערבבים מגנטי. בבוקר, מגניב. הבקבוק תחת זרם של N 2 תוך שימוש bubbler שמן להמשיך להזרים 2 N קצב בועה אחת מתחת לשניה.
הערה: לאחר קירור, אין אמצעי זהירות כדי לשמור את הבקבוק תחת N 2 נדרשים. - בשכונה fume, להוסיף norcotinine (31.8 מ ג, 0.196 mmol) אנהידריד אצטי (5 מ"ל), חומצה אצטית (1 מ"ל) הבקבוקון מקורר. מוסיפים את תערובת זו ברציפות תוך כדי קירור עד 0 ° C עם אמבט קרח-מים-
התראה: אנהידריד אצטי וחומצה אצטית הם מאכל. - ננו להוסיף 2 (33.3 מ"ג, 0.483 mmol) באחד בחלק ומערבבים ברציפות את התערובת עבור 2.5 ח' צג התקדמות התגובה לפי TLC (100% EtOAc, R f = 0.19, ראה שלב 1.4).
הערה: במשך הזמן הזה, התערובת יהיה יותר ויותר צהוב עם בעבוע ומדי פעם. - להרוות את התגובה על ידי לשפוך את התערובת אל תוך קר כקרח H 2 O (18 מ ל). מיד לחלץ את תמיסה מימית 18 מ של CH 2 Cl 2 משפך 100 מ. לחלץ את השכבה המימית לפחות 2 פעמים נוספות עם CH 2 Cl 2 (9 מ ל כל אחד).
- יבש של אורגניקס במאגר מעל ~ 100 מ"ג של MgSO 4 עבור 2 דק מסנן ולרכז את הפתרון על ידי אידוי רוטרי להניב תשואה של נפט גולמי, צהוב. מחממים את המים הרותחים עד 30 מעלות צלזיוס במהלך אידוי כדי להסיר את שאריות חומצה אצטית.
הערה: הפרוטוקול ניתן להשהות כאן אם המתחם הוא מומס CH 2 Cl 2 והפתרון מאוחסנים בחושך-2-8 ° C. - לטהר את המתחם גולמי על ידי טור כרומטוגרפיה (ראה שלב 1.5) באמצעות סיליקה ג'ל שלב נייח ו- 100% EtOAc כמו ה-eluent 16.
התראה: NNC, nitrosamides נלווים שצריך לנהוג בזהירות כפי הם מנועות להיות מסרטנים אנושי. - לפזר את המתחם טהור CDCl 3 ולהשתמש NMR (ראה שלב 1.2) כדי לאשר את המבנה ולקבוע את molarity של פתרון זה 17. לאחסן פתרון זה בחושך-2-8 ° C עד הצורך.
הערה: פתרון זה ישמש בתור פקד חיובי במבחנה וזמינותו (שלב 3.5). ספקטרום NMR משמרות כימי זמינים מידע תמיכה. - עם פתרון NNC טהור, לאשר המדויקת הורה המוני ולקבוע ההמונים יון המוצר על ידי אינפוזיה ישירה בספקטרומטר ברזולוציה גבוהה (HRMS) תחת פרמטרים שתואר בשלבים 1.3 ו- 4.3.
הערה: המוצר ההמונים ישמש לגילוי המתחם הזה ב במבחנה חילוף החומרים וזמינותו (שלב 4.3).
3. Nitrosamine-P450 דוגמה במבחנה דגירה
- להסיר P450 2A6 Baculosomes חיים-nadph להתחדשות מערכת, 10 מ מ NADP + מניות פתרון מקפיא-80 ° C ולתת להם להפשיר על קרח. ברגע הקרת, לדלל את Baculosomes ואת nadph להתחדשות מערכת 1:10 ו- 1:50, בהתאמה, לתוך צינור יחיד 1 מ"ל עם X 0.5 תגובת מאגר. באופן דומה, להוסיף 3 μL של NADP + מניות פתרון כדי μL 97 של 0.5 X תגובת מאגר.
הערה: NADP + הוא רגיש אור. לשמור על פתרון זה מוגן על-ידי גלישת המכיל שלו בנייר אלומיניום. אנזים פתרונות רגישים מחזורים ההקפאה-הפשרה; להגביל זה לא יותר מ 2 מחזורים. להכין aliquots לפי הצורך לניסויים עתידיים. - עבור כל דגירה, להוסיף 50 μL של פתרון אנזים (מכיל 5 pmol P450) 1 מ"ל צינור המכיל 40 μL של 4 פתרון NNN μM עשה עם מאגר התגובה. דגירה מראש תערובת חדשה זו למשך 2 דקות ב 37 מעלות צלזיוס שימוש באמבט מים ולאחר מכן להוסיף 10 μL של פתרון NADP + מדולל. דגירה מערכת מלאה עבור 1-30 דקות ב- 37 מעלות צלזיוס.
הערה: באמצעות 5-מין במרווחי זמן דגירה פעמים (למשל 5, 10, 15 דקות, וכו) תספק קורס מספיק זמן היווצרות nitrosamide. - לאחר זמן הדגירה הרצוי, להרוות הראשון μl 10 הוספת N ZnSO 3.0 4 ו-10 μL של 3.0 N Ba(OH) 2- מערבולת פתרון זה, של התמיסה לבן יהוו. Centrifuge הדגימה ב 8000 g x במשך 4 דקות על גלולה את התמיסה.
הערה: ההליך עלי לא לעשות הפסקה בשלב זה כמו nitrosamides יצרו מוגבלת יציבות בפתרונות מימית. השהיית זמן עלולה לגרום התשלילים שווא. - מיד pipette את תגובת שיקוע ולנתח 2 μL באמצעות ספקטרומטר מסה tandem ברזולוציה גבוהה nanoelectrospray חיובי-יינון כרומטוגרפיה נוזלית (LC-NSI +-HRMS/MS, צעדים 4.1-4.3).
- עבור שליטה חיובית incubations, להתאדות aliquot המכיל 100 fmol של פתרון NNC מסונתז לתוך צינור 1 מ"ל תחת זרם של N 2. הבקבוקון, להוסיף מערכת אנזימים מלא משלב 3.2, המשך כמתואר עבור שלבי 3.3-3.4.
- עבור שליטה שלילי incubations, עריכת הניסוי המתואר (צעדים 3.2-3.4) מלבד להחליף ה-50 μL האנזים פתרון עם 0.5 X תגובת מאגר.
4. דוגמה פרמטרים עבור זיהוי nitrosamide על ידי LC-NSI +-HRMS/MS
- עבור LC רכיב, החל את המילוי ההדרגתי צעד מרובת הבאים בשלב 4.2 למערכת UPLC באמצעות מסחרי, נארזו ידנית 18 סי18 (5 μm), מ מ x 75 100 μm, עמודות נימי דיזה μm 15.
- באמצעות 5 מ"מ NH 4 OAc של הממס, MeCN כ- B הממס, לטעון את הדגימה אל העמודה על-ידי הפעלת ב-5% B בμl 1/דקה בין 0 - 5 דקות ולאחר מכן האטה את קצב הזרימה כדי μL 0.3/דקה לאחר מכן. הבא, להפעיל הדרגתי בין 5 ל-20% B יותר מ- 4 דקות, כבש 55% B מעל 10 דקות, ולאחר מכן equilibration מחדש ל- 5% ב'
- לבצע את LC-NSI +-HRMS/MS על Orbitrap LTQ. צג עבור NNC על ידי סריקה מלאה והן פיצול 2 MS. לבצע סריקה מלאה ברזולוציה של 60,000 ולחלץ את המסה האב מדויק (192.07670)-סובלנות המונית של 5 עמודים לדקה. פיצול 2 MS שימוש לבודד האב יונים (אמו 2.0), שבר על ידי התנגשות-induced דיסוציאציה (CID) עם אנרגיית התנגשות של eV 25, ברזולוציה של 15,000, ולסרוק הזמן של גב' 30 לחלץ את ההמונים מדויק עבור המוצר יונים של NNC (מ/z 192 מ/z 134.04739 ו- 162.07874)-סובלנות המונית של 5 ppm.
Access restricted. Please log in or start a trial to view this content.
תוצאות
מבוסס על העבודה של לבן ואח. 19, norcotinine היה nitrosated כדי NNC נקיה, תשואה גבוהה (80-92%) כדי לייצר תקן לניסוי במבחנה . ראיות מבניות לתגובה מוצלחת הושג מניתוחי spectroscopic כולל 1H-NMR, 13C-NMR, נעים ו- HSQC (מידע תמיכה) יחד עם HRMS אשר אישר את המסה האב [M + H]+ בתוך 5 pp...
Access restricted. Please log in or start a trial to view this content.
Discussion
שחקרתי את חילוף החומרים של nitrosamines הוא מרכיב קריטי להבנת carcinogenicity שלהם. מאז ציטוכרום מעורב P450s, אנזימים מטבוליים אחרים רב-צורתיות, יישום של ידע זה יכול באופן פוטנציאלי לזהות בסיכון גבוה-יחידים-1,-4. נתונים חדשים המציין את חמצון נוסף של α-hydroxynitrosamines, מטבוליטים הג...
Access restricted. Please log in or start a trial to view this content.
Disclosures
המחברים אין לחשוף.
Acknowledgements
מחקר זה נתמך על ידי מענק אין. CA-81301 מן המכון הלאומי לסרטן. אנו מודים בוב קרלסון לסיוע העריכה, ד ר פיטר Villalta, מינג Xun לסיוע ספקטרומטר מסה אנליטי ביוכימיה משותפים משאב של מרכז הסרטן הבונים החופשיים, ואת ד ר אדם טי Zarth ד ר אנה ק מישל לדיונים החשובים שלהם קלט. למשאב משותף ביוכימיה אנליטי נתמכת באופן חלקי על ידי נבחרת סרטן המכון סרטן מרכז תמיכה גרנט CA-77598
Access restricted. Please log in or start a trial to view this content.
Materials
| Name | Company | Catalog Number | Comments |
| Norcotinine | AKoS GmbH (Steinen, Germany) | CAS 17708-87-1, AKoS AK0S006278969 | |
| Acetic acid | Sigma-Aldrich | 695092 | |
| Acetic Anhydride | Sigma-Aldrich | 242845 | |
| Ammonium Acetate | Sigma-Aldrich | 431311 | |
| Barium Hydroxide | Sigma-Aldrich | 433373 | |
| D-Chloroform | Sigma-Aldrich | 151823 | |
| HPLC Acetonitrile | Sigma-Aldrich | 34998 | |
| Magnesium Sulfate | Sigma-Aldrich | M7506 | |
| Methylene Chloride | Sigma-Aldrich | 34856 | |
| Sodium Nitrite | Sigma-Aldrich | 237213 | |
| ViVid CYP2A6 Blue Screening Kit | Life Technologies | PV6140 | |
| Zinc Sulfate | Sigma-Aldrich | 221376 | |
| 0.5 mL tubes | Fisher | AB0533 | |
| 100 mL round bottom flask | Sigma-Aldrich | Z510424 | |
| 125 mL Erlenmeyer flask | Sigma-Aldrich | CLS4980125 | |
| 125 mL Separatory Funnel | Sigma-Aldrich | Z261017 | |
| 25 mL round bottom flask | Sigma-Aldrich | Z278262 | |
| 500 MHz NMR Spectrometer | Bruker | ||
| Allegra X-22R Centrifuge | Beckman-Coulter | ||
| LC vials | ChromTech | CTC–0957–BOND | |
| LTQ Orbitrap Velos | Thermo Scientific | ||
| Magnetic Stir bar | Sigma-Aldrich | Z127035 | |
| NMR tube | Sigma-Aldrich | Z274682 | |
| P1000, P200, and P10 pipettes | Eppendorf | ||
| Rotary evaporator | Sigma-Aldrich | Z691410 | |
| RSLCnano UPLC system | Thermo Scientific | ||
| Shaking Water Bath | Fisher | FSSWB15 | |
| Stir plate | Sigma-Aldrich | CLS6795420 | |
| PicoFrit Column | New Objective | PF3607515N5 | |
| Luna C18, 5 um | Phenomenex | 535913-1 |
References
- Rom, W. N., Markowitz, S. Environmental and Occupational Medicine. , 4th ed, Wolters Kluwer/Lippincott Williams & Wilkins. 1226-1239 (2007).
- Preussmann, R., Stewart, B. W. Chemical Carcinogens, ACS Monograph 182. Searle, C. E. 2, 2nd ed, American Chemical Society. 643-828 (1984).
- Magee, P. N., Montesano, R., Preussmann, R. Chemical Carcinogens. ACS monograph 173. Searle, C. E. , American Chemical Society. 491-625 (1976).
- Zhu, A. Z., et al. Alaska Native smokers and smokeless tobacco users with slower CYP2A6 activity have lower tobacco consumption, lower tobacco-specific nitrosamine exposure and lower tobacco-specific nitrosamine bioactivation. Carcinogenesis. 34 (1), 93-101 (2013).
- Mesić, M., Revis, C., Fishbein, J. C. Effects of structure on the reactivity of alpha-hydroxydialkynitrosamines in aqueous solutions. J. Am. Chem. Soc. 118, 7412-7413 (1996).
- Mochizuki, M., Anjo, T., Okada, M. Isolation and characterization of N-alkyl-N- (hydroxymethyl)nitrosamines from N-alkyl-N- (hydroperoxymethyl)nitrosamines by deoxygenation. Tetrahedron Lett. 21, 3693-3696 (1980).
- Guttenplan, J. B. Effects of cytosol on mutagenesis induced by N-nitrosodimethylamine, N-nitrosomethylurea and à-acetoxy-N-nitrosodimethylamine in different strains of Salmonella:evidence for different ultimate mutagens from N-nitrosodimethylmine. Carcinogenesis. 14, 1013-1019 (1993).
- Elespuru, R. K., Saavedra, J. E., Kovatch, R. M., Lijinsky, W. Examination of a-carbonyl derivatives of nitrosodimethylamine in ethylnitrosomethyamine as putative proximate carcinogens. Carcinogenesis. 14, 1189-1193 (1993).
- Chow, Y. L. ACS Symposium Series. 101, American Chemical Society. 13-37 (1979).
- von Weymarn, L. B., Retzlaff, C., Murphy, S. E. CYP2A6- and CYP2A13-catalyzed metabolism of the nicotine delta5'(1')iminium ion. J. Pharmacol. Exp. Ther. 343 (2), 307-315 (2012).
- Bell-Parikh, L. C., Guengerich, F. P. Kinetics of cytochrome P450 2E1-catalyzed oxidation of ethanol to acetic acid via acetaldehyde. J Biol Chem. 274 (34), 23833-23840 (1999).
- Chowdhury, G., Calcutt, M. W., Nagy, L. D., Guengerich, F. P. Oxidation of methyl and ethyl nitrosamines by cytochrome P450 2E1 and 2B1. Biochemistry. 51 (50), 9995-10007 (2012).
- Chowdhury, G., Calcutt, M. W., Guengerich, F. P. Oxidation of N-nitrosoalkylamines by human cytochrome P450 2A6: sequential oxidation to aldehydes and carboxylic acids and analysis of reaction steps. J Biol Chem. 285 (11), 8031-8044 (2010).
- Carlson, E. S., Upadhyaya, P., Hecht, S. S. Evaluation of nitrosamide formation in the cytochrome P450-mediated metabolism of tobacco-specific nitrosamines. Chem Res Toxicol. 29 (12), 2194-2205 (2016).
- Amin, S., Desai, D., Hecht, S. S., Hoffmann, D. Synthesis of tobacco-specific N-nitrosamines and their metabolites and results of related bioassays. Crit. Rev. Toxicol. 26, 139-147 (1996).
- Clark, A. G., Wong, S. T. A rapid chromatographic technique for the detection of dye-binding. Anal Biochem. 89 (2), 317-323 (1978).
- Pauli, G. F., et al. Importance of purity evaluation and the potential of quantitative (1)H NMR as a purity assay. J Med Chem. 57 (22), 9220-9231 (2014).
- van der Heeft, E., et al. A microcapillary column switching HPLC-electrospray ionization MS system for the direct identification of peptides presented by major histocompatibility complex class I molecules. Anal Chem. 70 (18), 3742-3751 (1998).
- White, E. H. The Chemistry of the N-Alkyl-N-nitrosoamides. I. Methods of Preparation. J. Am. Chem. Soc. 77, 6008-6010 (1955).
- Patten, C., et al. Evidence for cytochrome P450 2A6 and 3A4 as major catalysts for N'-nitrosonornicotine alpha-hydroxylation by human liver microsomes. Carcinogenesis. 18, 1623-1630 (1997).
- Wong, H. L., Murphy, S. E., Hecht, S. S. Cytochrome P450 2A-catalyzed metabolic activation of structurally similar carcinogenic nitrosamines: N'-nitrosonornicotine enantiomers, N-nitrosopiperidine, and N-nitrosopyrrolidine. Chem. Res. Toxicol. 18, 61-69 (2004).
- Hecht, S. S. Biochemistry, biology, and carcinogenicity of tobacco-specific N-nitrosamines. Chem. Res. Toxicol. 11, 559-603 (1998).
- von Weymarn, L. B., Zhang, Q. Y., Ding, X., Hollenberg, P. F. Effects of 8-methoxypsoralen on cytochrome P450 2A13. Carcinogenesis. 26 (3), 621-629 (2005).
Access restricted. Please log in or start a trial to view this content.
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved