Method Article
קיבוע מהיר ב- Vivo ובידוד מתחמים תרגומיים מתאי אוקריוטיים
* These authors contributed equally
In This Article
Summary
אנו מציגים טכניקה לייצוב מהיר של מתחמים תרגומיים (ביוסינטזה של חלבונים) עם קשרים צולבים פורמלדהידים בתאי שמרים ויונקים חיים. הגישה מאפשרת לנתח מתווכים ארעיים ואינטראקציות דינמיות של RNA:חלבון. ניתן להשתמש במתחמים המקושרים ביישומים מרובים במורד הזרם, כגון בשיטות פרופיל מבוססות רצף עמוק, מיקרוסקופיה וספקטרומטריית מסה.
Abstract
תגובות מהירות הכוללות חלוקה מחדש מהירה של RNA שליחים ושינויים בתרגום mRNA רלוונטיים להתאמות הומיאוסטטיות מתמשכות של התאים. התאמות אלה הן קריטיות לשרידות תאים אאוקריוטיים ו'בקרת נזקים ' במהלך רמות חומר מינון ומליחות משתנות, טמפרטורה ולחצים כימיים וקרינה שונים. בשל האופי הדינמי ביותר של התגובות ברמת הרנ"א, וחוסר היציבות של רבים מתווכים RNA:RNA ו- RNA:protein, קבלת תמונה משמעותית של מצב ה- RNA הציטופלסמי אפשרית רק עם מספר מוגבל של שיטות. ניסויי פרופיל ריבוזום מבוססי רנ"א הם בין מקורות הנתונים האינפורמטיביים ביותר לשליטה בתרגום. עם זאת, היעדר ייצוב ביניים אחיד של RNA ו-RNA:חלבון עלול להוביל להטיות שונות, במיוחד במסלולי התגובה התאית המהירה. במאמר זה, אנו מספקים פרוטוקול מפורט של קיבעון מהיר החל על תאים אאוקריוטים של חמינות שונה, כדי לסייע RNA ו RNA: ייצוב ביניים חלבון. אנו מספקים דוגמאות לבידוד של מתחמי ה- RNA: חלבון המיוצבים בהתבסס על משקעים משותפים שלהם עם שברים סומליים ריבוזומליים ופוליבו. ניתן להשתמש בחומר המיוצב המופרד כחלק מניסויים מסוג ריבוזום פרופיל, כגון בגישה של ריצוף פרופיל מורכב תרגום (TCP-seq) ונגזרותיו. רב-תכליתיות של שיטות בסגנון TCP-seq הוכח כעת על ידי היישומים במגוון אורגניזמים וסוגי תאים. ניתן גם לטוהר ולדמות את המתחמים המיוצבים באמצעות מיקרוסקופיית אלקטרונים, מופרדים לשברים סומליים שונים של פולי(ריבו) ונבדקים לרצף RNA, בשל קלות היפוך הקישור הצולב. לכן, שיטות המבוססות על קיבוע snap-chilling ופורמלדהיד, ואחריו מבוסס משקעים או סוג אחר של העשרה מורכבת RNA: חלבון, יכול להיות עניין מיוחד בחקירת פרטים עדינים יותר של דינמיקה מורכבת RNA: חלבון מהיר בתאים חיים.
Introduction
אורגניזמים חיים נתונים לשינויים פנים-תאיים דינמיים לאורך תוחלת החיים שלהם, הדורשים תגובות מהירות כדי לשמור על הומאוסטזיס ולהבטיח הישרדות. כדי לאפשר הסתגלות סביבתית, תאים אאוקריוטים להתאים את חילוף החומרים שלהם באמצעות בקרת ביטוי גנים. ניתן להפעיל בקרת ביטוי גנים במהלך תמלול ו/או תרגום; עם תגובות תרגומיות המתרחשות בדרך כלל מהר יותר1,2,3,4. לדוגמה, שינויים תרגומיים בדרך כלל להתעורר בתוך 1-30 דקות של תחילת הלחץ, בעוד שינויים ברמת שעתוק לאחר שעות לאחרחשיפהללחץ 3,4,5. שינויים בתפוקת התרגום מושגים מהר יותר בשל הזמינות המתמשכת של מולקולות RNA שליח (m) בציטופלסמה. לעומת זאת, ברמת התמלול, מולקולות mRNA חדשות חייבות להיות מסונתזות, ובאאוקריוטים, מעובדים ומיוצאים מהגרעין, ומייצרים עיכובים נרחבים בזמן התגובה2,4,6,7,8.
תגובה תרגומית חריפה ללחץ מאופיינת בדרך כלל בירידה כוללת בתפוקת התרגום, עם עלייה סלקטיבית של חלבונים הדרושים להישרדות התא1,3,4,9. הפחתת תפוקת ייצור החלבון נחשבת חיונית בשל הוצאות האנרגיה הגבוהות של התהליך3,7. כדי להקל על העיכוב הסלקטיבי ועליית, תגובות תרגומיות מוגשות על ידי מגוון של מנגנוני רגולציה מורכבים. ניתן להפעיל רגולציה בכל שלבי התרגום: חניכה, התארכות, סיום ביוסינתזה של פוליפפטיד ומיחזור ריבוזומלי10,11,12,13אבל מוצג בצורה החזקה ביותר בשלב החניכה,5,7,9,10,13. במהלך החניכה, תת-unit ריבוזומלי קטן (SSU), בסיוע גורמי חניכה אאוקריוטיים (eIFs), נקשר לאזור הלא מתועד של 5' (UTR) עד לזיהוי קודון התחלה2,5,6,8,11,12,13. מנגנוני רגולציה מתמקדים לעתים קרובות במזיפים אלקטרוניים המשפיעים על התקשרות, סריקה והפעלה של זיהוי קודון. לדוגמה, גורם החניכה eIF2, גורם תרגום חיוני המסייע בגיוס של יזם Met-tRNAiMet לSSU, הוא לעתים קרובות ממוקד אאוקריוטים בתנאי לחץ4,6,11. בשמרים, זרחן של גורם זה יכול להיות מושרה תחת חסך תזונתי ומתח אוסמוטי1,4,11,14,15ובתאי יונקים, רעב בחומצות אמינו, לחץ רטיקולום אנדופלסמי (ER), מתח UV, זיהום ויראלי ורמות חמצן משתנות עלולים לעורר תגובה זו.8,9,11. עלייה מהירה בתרגום mRNA ספציפי ניכרת בתגובת תאי היונקים להיפקסיה, המציגה עיכוב תרגום מהיר גלובלי וערעור סלקטיבי של ביוסינתזה של גורמים היפוקסיה-בלתי ניתנים לערעור (HIFs). HIFs הם גורמי שעתוק, אשר לאחר מכן לעורר תכנות סלולרי לטווח ארוך יותר ברמת שעתוק DNA8,9,16. תגובות דומות נצפו בשמרים תחת לחץ חום, עם ביטוי תרגום מהיר של חלבוני הלם חום (HSPs) ואחריו תגובות מושהות ברמת שעתוק17,18. בנוסף למחסור בחומרים מזינים והלם חום, תגובות תרגומיות בשמרים נחקרו תחת חמצן משתנה8,19מליחות,5פוספט, גופרית,20,21 וחנקן22,23 רמות. למחקר זה השלכות נרחבות על השימושים התעשייתיים של שמרים, כגון אפייה ותסיסה24,25. תגובות תרגומיות עשויות גם להיות אינסטרומנטליות בקידום ההבנה של מחלות כגון הפרעות ניווניות ומחלות לב, המאופיינות בלחצים תאיים כמו עקה חמצונית. בסך הכל, תגובות תרגומיות הן חלק בלתי נפרד מהבקרה בביטוי הגנים ומאפשרות הסתגלות מהירה למגוון רחב של תנאי לחץ באורגניזמים אאוקריוטים.
כדי ללמוד תגובות תרגומיות, נדרשות שיטות המספקות תמונות מעוותות מינימליות של נוף התרגום. פרופיל פוליזום הוא גישה קלאסית המשמשת בחקר התרגום על פני mRNA, הכוללת הפרדה של שברים סומליים פולי (ריבו) של mRNA באמצעות אולטרה צנטריפוגה באמצעות שיפועי סוכרוז26,27. הגישה עשויה לשמש כדי לחקור רמות תרגום עבור mRNAs בודדים (עם שיטות הזיהוי כגון שעתוק הפוך ותגובת שרשרת פולימראז, RT-PCR26), או ברחבי העולם בשילוב עם טכניקות תפוקה גבוהה (microarray או RNA-seq28,29). גישה מפותחת יותר היא פרופיל ריבוזום, המאפשר לחקור עמדות של ריבוסומים מוארכים לאורך מולקולת mRNA בקנה מידה רחב גנום, כמו גם את המסקנה של יעילות התרגום על פני transcriptome וניצול של אתרי ההתחלה העיקריים והאלטרנטיביים30,31. פרופיל ריבוזום כרוך בבידוד ורצף של שברי mRNA המוגנים על ידי נוכחות ריבוזומלית עליהם. פרופיל ריבוסום סיפק תובנה ניכרת על דינמיקת התרגום על פני מספר תנאים, כולל מתח היפוקסי, הלם חום ומתח חמצוני31,32. הטכניקה הותאמה לסוגי חומרי מקור מרובים, כולל שמרים ותאי יונקים.
בעוד פרופיל polysome ו ribosome היו בסיסיים בהרחבת יכולות המחקר בתרגום, תהליך התרגום כולל מתווכים תרגומיים שונים ומתחמים שקשה ללכוד בשיטות אלה11,13. מגבלה נוספת נובעת מהיעדר יכולת לחקור סוגי תגובה מהירים, שכן מתחמי תרגום מתייצבים ב- vivo על ידי תוספת של מעכבי תרגום ספציפיים (אנטיביוטיקה), מה שמוביל לממצאי הפצה מסוימים של ריבוזום, או ex vivo על תמוגה התא במיוחד (אנטיביוטיקה) או באופן לא ספציפי (יונים מלח או מגנזיום גבוהים), מה שמוביל למחסור במתווכים קצרי מועד או פחות יציבים33, 34,35.
פורמלדהיד נמצא בשימוש נרחב כדי לקשר בין חומצות גרעין וחלבונים, כגון במחקרים אימונופרציפיטציה של כרומטין (ChIP) וקישור אימונופרציפיטציה (CLIP). גודלו הקטן וחמידות התאים המצוינת שלו מאפשרים פעולה מהירה ב- vivo 36. בהתבסס על קישור מהיר פורמלדהיד, הגישה ליצירת פרופיל ריבוזום הורחבה עם ריצוף הפרופיל המורכב של התרגום (TCP-seq)10,36,37,38,39,40. TCP-seq, שפותח לראשונה בשמרים, מאפשר לכידה של כל מתווכים תרגום, כולל סריקה או לאחר סיום מתחמי SSU ותצורות ריבוזומליות מרובות37,38,41,42. השיטה נוצלה במספר מחקרים10,38,39,41,42, שחלקם משתמשים בגישה קומבינטורית של מעכבי תרגום וקישורים פורמלדהיד כדי להקל על מעצר התרגום. גירסה שונה נוספת של הטכניקה, סלקטיבי TCP-seq39, הועסק לאחרונה כדי לכלול אימונופורציה של מתחמים crosslinked, הרחבת היקף יישומי TCP-seq. האופי המהיר, היעיל והה הפיך של קישור צולב פורמלדהיד הופך גישות אלה מתאים לחקר mRNA ארעי: אינטראקציות מורכבות תרגום, במיוחד בהקשר של מסלולי תגובה דינמיים מאוד ברמת התרגום.
כאן אנו מפרטים את התהליכים של קישור צולב של in vivo פורמלדהיד לצורך ייצוב ובידוד מורכבים של תרגום מקיף. אנו מספקים פרוטוקולים נפרדים לניואנסים עבור שמרים ותאי יונקים(איור 1). אנו מתארים דוגמאות נוספות לשימוש הבא בחומר המיוצב באמצעות קישור מקושר(איור 1),כגון לזיהוי גורמי חלבון מטוהרים באמצעות אימונובלוטינג (סופג מערבי), טיהור בסיוע אימונו (או 'אימונו-פחת'; IP) והעשרה של מתחמים תרגומיים המכילים גורמי עניין ספציפיים, מיקרוסקופיית אלקטרונים ורצף RNA.
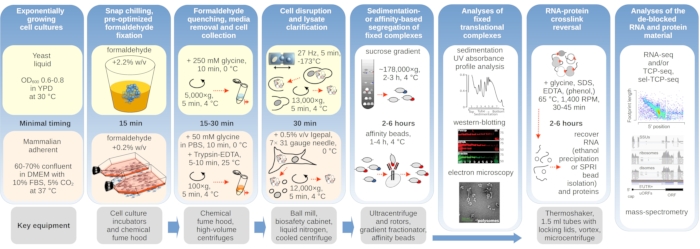
איור 1: תרשים המתאר סקירה כללית של ההתקנה הניסיונית הטיפוסית. השלבים העיקריים של ייצוב פורמלדהיד in vivo של מתחמים תרגומיים מתוארים כתרשים זרימה, בתוספת מידע על המכשירים העיקריים הדרושים. יישומים פוטנציאליים במורד הזרם של החומר המקושר מפורטים, כולל דוגמאות אשר הועסקו בהצלחה אך לא כוסו ישירות בפרוטוקול זה, כגון טיהור חרוזים SPRI של RNA, ריצוף RNA וספקטרומטריית מסה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
Protocol
1. פרוטוקול תא שמרים
- תרבית תאי שמרים וקבעון
הערה: קיבוע וקציר תאים מותאמים מ10,38עם שינויים.- הגדרת 1 L תרבית תא שמרים (סוג בר (WT) BY4741 ניתנים כדוגמה) בשייקר מסלולית עם צפיפות אופטית התחלתית של לא יותר מ 0.05 AU ב 600 ננומטר (OD600)במדיה מתאימה (1% w / v של תמצית שמרים, 2% w / v של פפטון, 2% w / v של דקסטרוז (גלוקוז), 40 מ"ג / ליטר של אדנין סולפט (YPD) המשמש כדוגמה) בתנאים הרצויים (30 °C המשמשים זה ניסוי).
- הקימו צנטריפוגה מוכנה עם רוטור תואם ובקבוקי צנטריפוגה לתרבית ההשעיה הנוזלית של תאי שמרים. לניסויי רעב לגלוקוז, גלולה את התאים פעם אחת הצפיפות האופטית של 0.6-0.8 AU ב 600 ננומטר (OD600)הוא הגיע, באמצעות צנטריפוגה קצרה ב 30 °C (5,000 x גרם עבור 1 דקות.
הערה: שמור תיעוד של OD של התאים הגדלים ולתת לתאים לגדול עד OD600 מגיע 0.6-0.8 AU, אם שלב הצמיחה המעריכי הוא עניין. - resuspend הכדור מיד בחום (30 °C) YP מדיה המכילה לא או נמוך (0.25% w /v) הוסיף גלוקוז ודגרה את התרבות במשך 10 דקות נוספות ב 30 °C (50 °F) בשייקר מסלול-אינקובטור.
הערה: הרכב המדיה עשוי להשפיע על יעילות הקישורים הבאים. פרוטוקול זה נבדק באמצעות YPD בלבד. בעת ביצוע ניסויי רעב, דבקות בתזמון ומזעור העיכובים בין ההליכים היא קריטית. - ברגע התאים מוכנים, להגדיר קופסת קרח בתוך מכסה המנוע אדים עם המכילה 250 גרם של קרח מים כתוש נקי. ודאו ש-25 מ"ל סטריפטיות ופתרון פורמלדהיד מיוצב טרי של מתנול 37% נגישים בתוך מכסה המנוע. יוצקים את תרבית 1 L לתוך המכילה 25% w / v של קרח מים כתוש.
הערה: שמור את התאים על קרח לאורך כל הפעולות הבאות עד התאים קפואים, אלא אם צוין אחרת. - מוסיפים 75 מ"ל של 37% w/v של תמיסת פורמלדהיד לריכוז סופי של 2.2% w/v ומערבבים בעוצמה את התערובת עד שהקרח נמס.
- ברגע שהקרח נמס, הגדירו שעון זמן למשך 10 דקות.
הערה: דבק בתזמונים המומלצים ובמשטר הטמפרטורה כדי להשיג תוצאות קיבעון לשחזור. - לאחר הדגירה במשך 10 דקות, להעביר את התרבות לתוך בקבוקי צנטריפוגה מכווצים מראש גלולה את התאים על ידי צנטריפוגה ב 4 °C (5 °F), 5,000 x g במשך 5 דקות. בזמן ספין זה הוא על, precool צינור 50 מ"ל ולשמור על חיץ מוכן טרי A (המכיל גליצין לנטרל כל פורמלדהיד שנותר) על קרח.
הערה: עיין בטבלה שסופקה עבור קומפוזיציות המאגר המדויקות. - לאחר צנטריפוגה, מניחים את צינורות הצנטריפוגה על קרח עם צד הכדור במגע עם הקרח. מכניסים את הצינורות למכסה המנוע של האדים ומשליכים את הסופר-נט למיכל פסולת פורמלדהיד.
- resuspend גלולה התא מכל הצינורות ב 20 מ"ל של חוצץ A באמצעות סטריפט 25 מ"ל והעברה לצינור 50 מ"ל.
הערה: שטיפה זו היא קריטית למניעת קישור צולב בלתי יתורגם ותוספת המאגר לא תעלה על 20 דקות זמן מקציר התאים. - הפוך את הנפח עד 40 מ"ל עם חוצץ A ולאסוף את התאים שטף על ידי צנטריפוגה ב 4 °C (5 °F), 5,000 x g במשך 5 דקות.
- להשליך את supernatant ו resuspend את גלולה התא ב 40 מ"ל של חוצץ A1, שהוא חוצץ A לא מכיל גליצין, כדי להסיר כל זיהום גליצין.
- תאי גלולה שוב על ידי צנטריפוגה ב 4 °C (5 °F), 5,000 x g במשך 5 דקות.
- חזור על הכביסות עם חוצץ A1 פעם נוספת. להשליך את supernatant ומניחים את גלולה התא על קרח. שקול את הצינור עם הכדור (מסת תא רטוב צריך להיות ~ 1 גרם לכל 1 ליטר של תרבית התא).
- הפרעה לתאי שמרים ואיסוף ציטוסול
- מלאו קופסת קצף פוליסטירן מרופדת בנייר אלומיניום עם חנקן נוזלי לעומק של כ-3 ס"מ. מניחים צינור 50 מ"ל זקוף בקופסה.
- resuspend הכדור (~ 1 g מסת תא רטוב) ב 550 μL של חוצץ A2 על ידי pipetting ומערבולת עבור 10 s. הוסף 10 μL של 40 U /μL של מעכב RNase ומערבולת שוב עבור 10 s.
אזהרה: ללבוש ציוד מגן מתאים, כגון כפפות מבודדות תרמית, בעת טיפול חנקן נוזלי. ודא כי כל מיכל המשמש להחזקת חנקן נוזלי אינו דולף, וכי מתלה הצינור בפנים לא יצוף או ייפול על צידו. עבוד באזור מאוורר היטב כדי למנוע דלדול חמצן. - באמצעות פיפטה 1 מ"ל, לטפטף את השעיית התא לתוך צינור 50 מ"ל המכיל את החנקן הנוזלי.
הערה: יש לבצע את הטפטוף לאט ובזהירות כדי למנוע צבירה של הטיפות. ודא שהטיפה קופאת לפני הצגת טיפות חדשות. - מעבירים את צינור 50 מ"ל עם טיפות השעיית התא הקפוא לטמפרטורת החדר וממתינים עד שהחנקן הנוזלי מתאדה לחלוטין. לאטום את הצינור עם המכסה שלה ולאחסן את כדורי התא ב -80 °C (80 °F) או מיד להמשיך הלאה.
אזהרה: ודא כי החנקן הנוזלי מתאדה לחלוטין לפני איטום הצינור. שאריות חנקן נוזלי בצינור אטום עלולות לגרום להצטברות לחץ מסוכנת. - כדי להתכונן לשלב הבא, precool 1.5 מ"ל צינורות ללא נוקלאז ו 10 מ"ל צנצנות שחיקה נירוסטה על קרח יבש.
- מעבירים את טיפות השעיית התא הקפואות לצנצנות באמצעות מרית נקייה וסטרילית.
אזהרה: ודא כי צנצנות הטחינה אטומות היטב. - שקועים בצנצנות הטחינה בחנקן הנוזלי למשך דקה אחת ומבטיחים שהשלב הנוזלי יישאר מתחת לצומת. הגדר טחנת מערבל קריו ב 27 הרץ עבור תסיסה במשך 1 דקות.
הערה: תמיד לאזן את מיכל הטחינה עם עוד אחד מאותו דגם גם אם המדגם דורש רק מיכל אחד לעיבוד. - להסעיר את צנצנות הטחינה האטומות ב 27 הרץ במשך 1 דקות בטחנת המיקסר.
- מצננים מחדש את צנצנות הטחינה בחנקן נוזלי כבעבר ומנערים במהירות של 27 הרץ למשך דקה נוספת בטחנת המיקסר.
- מעבירים את הצנצנות לקופסת הקרח המכילה קרח יבש יחד עם צינורות 1.5 מ"ל ללא נוקלאז. באמצעות מרית פלדה קטנה, להעביר את דגימת אבקת התוצאה לתוך הצינורות ~ 100 aliquots מ"ג, ולאחסן את הצינורות ב -80 °C (70 °F).
הערה: מומלץ להשתמש ~ 600 מ"ג של המדגם לכל ניסוי הכולל ניתוח פרופיל מטען polysome, הפרדת הציטוסול לשברים מתורגמים ולא מתורגמים, והפרדה נוספת של השבר המתורגם ל- SSU, ריבוזום ושברים disome על עיכול RNase.
- הפרדת המתחמים הריבוזומליים הקבועים (פולי) מהשברים הלא מתורגמים של הציטוסול
הערה: ההליך שנקבע קודם לכן10,38בדרך כלל אחריו הוא העשרת RNA מתורגם בהתבסס על משקעים משותפים שלה עם (פולי) ריבוזומים. גישה מעודנת יותר להפרדת שברי הציטוסול המתורגמים והלא מתורגמים מוצגת כאן, ומבטלת את הצורך לזרז ולאחר מכן לשאוב מחדש את החומר.- הכן 2.5 מ"ל ליניארי 10%-20% עם שיפועי סוכרוז עם חוצץ B בשיטת הפשרת ההקפאה43 בצינורות אולטרה-צנטריפוגה דקים בקיר (5 מ"ל, 13 x 51 מ"מ).
הערה: שיטת הפשרת ההקפאה מבוצעת על ידי תוספת רציפים והקפאה של שכבות סוכרוז חוצץ עם ריכוזים רגרסיים ליניאריים על גבי זה. ראה טבלה משלימה 1 לקבלת פרטים. - כדי ליצור כרית סוכרוז 50% w /v רצירה, על שיפועים ליניאריים מפשירים ומייצבים, לאט לאט לוותר 0.5 מ"ל של 50% סוכרוז חוצץ B ישירות על החלק התחתון של הצינורות באמצעות מזרק 1 מ"ל מחובר מחט 19 G x 1.5 " או נימי זכוכית של ממדים דומים / מתאימים. לפני חלוקה, בזהירות ובאיטיות לנהוג את קצה המחט או נימי מלמעלה למטה של שיפועי סוכרוז שנוצרו מראש, הימנעות כל הפרעה, עד שהוא מגיע לתחתית הצינור.
הערה: ראה טבלה משלימה 1 לקבלת הוראות להכנת מאגר B. - בזהירות לאזן את מעברי הצבע על ידי הסרת החלקים העליונים או שכבות יותר 10 w /v של סוכרוז במאגר B ולשמור אותם קר כקרח או ב 4 °C (70 °F).
הערה: שיפוע רנציף עם שכבת סוכרוז 50% התחתונה נדרש כדי לאסוף חומר עם שיעור משקעים גבוה יותר מבלי לזרז אותו על קיר הצינור. - להפשיר ~ 100 מ"ג של דגימת אבקת התא הקפוא בטמפרטורת החדר ומיד להניח על קרח. מערבבים 150 μL של חוצץ A2 על ידי pipetting, להוסיף מעכב RNase ל 1 U / μL ומערבבים על ידי מערבולת (למנוע קצף מוגזם ערבוב עם שלב הגז) עבור 10 s.
הערה: המשך את כל הפעולות תוך שמירה על החומר על הקרח, אלא אם צוין אחרת. - גלם את פסולת התא על ידי centrifuging הצינורות ב 4 °C (5 °F), 13,000 x g במשך 5 דקות לשחזר את supernatant המובהק (~ 150 μL) חדש 1.5 מ"ל חלבון כריכה צינור.
- טען את התערובת המובהרת על צינורות הדרגתי סוכרוז רשלני החל מהשלב 1.3.3 ומאזן אותם בקפידה.
- Ultracentrifuge הצינורות בנפח בינוני נדנדה דלי רוטור ב 4 °C (5 °F), עם כוח G ממוצע 287,980 x g (k-factor 49) במשך 1 שעות 30 דקות.
הערה: תנאים אלה עברו אופטימיזציה מראש (באמצעות ניתוח מעקב ספיגת UV הדרגתי לאחר אולטרה-צנטריפוגה) כדי לשמור על ה- SUS וה- LUS (50%) - השתמש מזרק סטרילי חדש 1 מ"ל מצויד מחט 19 G x 1.5 " כדי לאסוף את שבר ציטסול מתורגם. מקם את שיפוע 5 מ"ל על מתלה יציב המבטיח את תחתית הצינור גלוי.
- מהחלק העליון של הצינור, לתקוע את המחט ישר לתוך החלק התחתון של השיפוע (מבלי לנקב את הצינור) ובעדינות, מבלי ליצור בועות, לצייר בדיוק 0.5 מ"ל של הפתרון התחתון המכיל את בריכת RNA מתורגמת.
הערה: ודא שלב זה מבוצע בחדר קר ואת הצינור מוחזק בחוזקה. מומלץ לצייר את כל 0.5 מ"ל בתנועה upstroke יחיד כדי למנוע הפרעה של השיפוע. - אשר את הנוכחות ריבוזומלית (פולי) ואת דלדול SSU, LSU ושברים קלים יותר בתערובת התוצאה על ידי קריאת ספיגה של מעבר צבע סוכרוז על הפעלת אולטרה צנטריפוגה.
- מרכז את מאגר הרנ"א המתורגם שנאסף מהשלב הקודם ל- 100 μL באמצעות סינון אולטרה-סינון בהתקן מיקרו-ריכוז עם קרום תאית מתחדשת 10 kDa מנותק.
הערה: יש לשטוף מראש את הממברנה של התקן ריכוז המיקרו עם 0.5 מ"ל של חוצץ 1 (ראה איור 2a)ולהשתמש בתנאי ספין (g) המומלצים על ידי היצרן. - עוד לדלל את החומר מהשלב הקודם חמש פעמים (להוסיף 400 μL) עם חוצץ 1 ולהתרכז בחזרה 200 μL, כדי לאפשר נפח קטן יותר, כמו גם הסרה חלקית של סוכרוז.
הערה: מומלץ לאחסן את התערובות המתקבלות ב- -80 °C (80 °F) למשך עד 6 חודשים ולהשתמש כחומר קלט לבניית ספריית הרנ"א-רנ"א בתרגום הכולל, או לשלב העיכול של RNase של בניית ספריית TCP-seq. ניתן לשחזר את שבר הציטוסול 'שאינו מתורגם' מראש השיפוע באמצעות שגרה דומה ולאחסן אותו ב- -80 °C (80 °F).
- הכן 2.5 מ"ל ליניארי 10%-20% עם שיפועי סוכרוז עם חוצץ B בשיטת הפשרת ההקפאה43 בצינורות אולטרה-צנטריפוגה דקים בקיר (5 מ"ל, 13 x 51 מ"מ).
- RNase העיכול של קבוע (פולי) ריבוסומלי מורכב והפרדה של חומר מעוכל לתוך subunit ריבוזומלי קטן (SSU), monoribosomal (ריבוזומים, RS), ו diribosomal (disomes, DS) שברים
הערה: ההליך בדרך כלל עוקב אחר גישה שתוארה בעבר10,38אבל סוג הדרגתי שונה, זמן הפרדה, תאוצה ותנאי עיכול RNase מועסקים, כדי להשיג את הרזולוציה הטובה ביותר על פני כל שלושת השברים המבודדים.- הכן מאוזן בקפידה 12.5 מ"ל ליניארי 10%-40% עם שיפועי סוכרוז w /v שנעשו עם חוצץ 1 ב 13 מ"ל צינורות פוליפרופילן קיר דק, 14 x 89 מ"מ, באמצעות שיטת הפשרת ההקפאה43 כמתואר בשלב 1.3.1 ולשים לב בו.
- מפשירים בטמפרטורת החדר ומעבירים מיד את הדגימות על הקרח או לוקחים את שבר הציטוסול המרוכז והמדולדל מסוכרוז מהשלב 1.3.12.
הערה: המשך את כל ההליכים על קרח אלא אם צוין אחרת. - לעכל את שבר ציטוסול מתורגם על ידי ערבוב ב 4.5 U של E. coli RNase I לכל 1 OD260 יחידה של השבר במשך 30 דקות ב 23 °C (70 °F). מיד להוסיף ולערבב על ידי pipetting מעכב RNase מסוגל לנטרל RNase I ל 0.25 U / μL לתערובת, כדי לנטרל RNase I.
הערה: השתמש מעכב RNase מסוגל לעכב RNase I. להפיק AU260 באמצעות AU260 = (ספיגה ב 260 ננומטר מתוקננת ליחידות צפיפות אופטית שווה ערך ל 1 ס"מ נתיב אופטי x נפח של lysate ב μL) / 1,000. - מעבירים מיד את הדגימות לקרח.
זהירות: חשוב לדבוק בתנאים המומלצים של העיכול ולמדוד בזהירות את כמות RNase I הנוסף. יחידת RNase I המכונה כאן מוגדרת כמות האנזים הנדרש כדי לייצר 1 מיקרוגרם של חומר מסיס בחומצה מ RNA כבד העכבר ב 30 דקות ב 37 °C. קבוצות RNase I עשוי להיות וריאציות מתועדות בפעילות ועשויים לדרוש ניסויים כדי להשיג תנאי עיכול אופטימליים. אם מלאי האנזים מרוכז מדי, מומלץ לדלל אותו עם חוצץ 1 כדי למנוע צינורות כמויות קטנות מאוד של הפתרון. - טען את תערובות התגובה על מעברי הצבע של 10%-40% w/v סוכרוז מהשלב 1.4.1.
הערה: השתמש באמצעי אחסון סופיים בטווח של 150-300 μL לכל מעבר צבע. כל טיהור דורש שני מעברי צבע מינימליים. השתמש באמצעי אחסון קלט שונים של החומר (AU נמוך יותר260, 10-11 AU260, עבור DS ו גבוה יחסית AU260, 13-14 AU260, עבור SSU או RS) כדי להשיג הפרדה אופטימלית. - Ultracentrifuge הצינורות בנפח בינוני נדנדה דלי רוטור ב 4 °C (5 °F) עם כוח G ממוצע 178,305 x g (k-factor 143.9) במשך 3 שעות 30 דקות.
זהירות: אם יש צורך בצינורות איזון רזרביים, השווה את התפלגות המסה והמסה שלהם עם הצינורות המכילים מדגם. השתמש בשיפועים סוכרוז חילוף על כיסוי עם כמות של חוצץ שווה לזה של שכבת העל מדגם ולא צינורות עם ריכוז סוכרוז אחיד. - הגדר התקן שבר הדרגתי לפחות 30 דקות לפני השלמת ספין ultracentrifugation, כולל מילוי פתרון מרדף כבד מסונן 0.2 מיקרומטר (למשל, 60% סוכרוז במים deionized כפי שנעשה כאן) לתוך משאבת עקירה.
הערה: מומלץ לטהר את הקווים והצינורות של השבר באמצעות מים דהויוניזציה, ואחריו 1%-2% פתרון SDS במים deionized, מים deionized, ולבסוף 80% אתנול בתמיסת מים deionized לפני ואחרי ריצות. - התאם את בסיס הקריאה של ספיגה על ידי מילוי המערכת במים דה-יוניים ואיפוס האופטיקה בהתאם להמלצות היצרן, ולאחר מכן פיצוי המשמרת הבסיסית באמצעות שיפוע סוכרוז 14 x 89 מ"מ רזרבי שנעשה עם חוצץ זהה לצינורות הדגימה (לדוגמה, חיץ 1).
הערה: השתמש באותה מהירות תזוזה כדי לבצע את ההתאמות כמו עבור קריאת המדגם, כגון 1.5 מ"ל/דקה. - מדוד את נפח המת של מערכת ההעתקה על-ידי ספירה מדויקת של הזמן בין הפתרון שנכנס לראשונה לנתיב האופטי של הגלאי לבין הופעתו הראשונה בפלט של מלקט השברים.
הערה: עם המהירות המומלצת של 1.5 מ"ל / דקה, השבר יכול להתבצע בטמפרטורת החדר. מומלץ להעביר באופן מיידי את השברים שנאספו על קרח. - בצע פירוק באמצעות קריאת ספיגה חיה ב- 254 ננומטר, מהירות תזוזה של 1.5 מ"ל /דקה וזיהוי שבר בשורה בהתבסס על מיקום השיתוך הצפוי ופרופיל הספיגה של הדגימות. השתמש במעבר צינור אספן עם עיכוב זמן המתאים לנפח המת כפי שנמדד בעבר.
- לבודד שברים המתאימים למיקומים ולניידות של מתחמי SSU, RS ו- DS ולאסוף אותם לצינורות מיקרוצנטריפוגה חדשים בעלי חלבון נמוך 1.5 מ"ל; מעבירים מיד את השברים המבודדים על הקרח ומקפיאים אם לא מעובדים הלאה מיד.
הערה: מומלץ להקפיא באופן מיידי את השברים שנאספו בקרח יבש או בחנקן נוזלי ולאחסן בטמפרטורה של -80 °C (70 °F) ומטה למשך עד 6 חודשים.
- ביטול הצלבה של מתחמי ריבוזומליים ובידוד ה-RNA לבניית ספריות RNA-seq
- כדי לבטל חסימה/להפוך את הקישורים הצולבים ולבודד את ה-RNA הרחק מהחלבונים הקשורים, העבירו כמחצית מכל שברי ההדרגה של סוכרוז לחומצת גרעין נמוכה חדשה המחייבת פוליפרופילן 1.5 מ"ל מיקרוצנטריפוגה (350 μL לכל צינור) עם התקני בטיחות/נעילה של המכסה.
- להשלים את התערובות עם 40 μL של פתרון עצירה 100% (10% SDS w /v ו 100 mM EDTA), 4 μL של 1 M טריס-HCl pH 2 ב 25 °C (ל 10 mM), 1.6 μL של 2.5 M גליצין (ל 10 mM) ומים ללא נוקלאז deionized כדי להשיג את הנפח הסופי של 400 μL.
- מערבבים את התוכן של הצינורות על ידי צנרת ולהעביר את הצינורות בטמפרטורת החדר.
- הוסף נפח שווה של פנול חומצי:כלורופורם:איזואמיל אלכוהול 125:24:1 (pH 4.0-5.0) תערובת לכל צינור. לנער במרץ את התערובות במשך 2 דקות באמצעות מערבל מערבולת להגדיר למהירות מקסימלית.
זהירות: פנול וכלורופורם הם מאכלים ורעילים. יש להימנע ממגע פיזי עם הנוזלים ולעבוד באזור מאוורר היטב או מתחת למכסה המנוע. השתמש תמיד כפפות, חלוק מעבדה ומשקפי מגן או מגן פנים בעת עבודה עם פנול או כלורופורם. - מניחים את הצינורות בתרמוסקר ומנערים ברציפות ב 65 °C (65 °F), 1,400 סל"ד במשך 30 דקות.
- להקל על צבירת פאזה על ידי צנטריפוגה התערובת ב 12,000 x גרם במשך 10 דקות בטמפרטורת החדר.
- לאסוף את השלבים מימיים העליונים ולהעביר אותם לתוך חומצת גרעין נמוכה טרי מחייב 1.5 mL צינורות.
הערה: כדי למנוע זיהום צולב, אל תנסה לשחזר את השלבים מימיים לחלוטין. נפח שחזור סביר הוא 300-350 μL. - להשלים את השלבים מימיים שנאספו עם 0.1 כרכים של 3 M נתרן אצטט (pH 5 ב 25 °C ), 20 מיקרוגרם של גליקוגן (באמצעות 5 מיקרוגרם / μL מלאי) ו 2.5 כרכים של אתנול מוחלט. מערבבים בזהירות את הפתרונות על ידי מערבולת הצינורות במשך 1 דקות.
- לזרז את הרנ"א על ידי דגירה של הדגימות ב -20 °C (20 °F) לפחות 2 שעות (מומלץ לילה).
- מחממים את הצינורות לטמפרטורת החדר ומערבבים על ידי מערבולת.
הערה: התחממות מוקדמת של הצינורות וצנטריפוגה לאחר מכן בטמפרטורת החדר (ללא צינון כפוי) מסייעים להפחית את המשקעים וההחזקה המשותפת של המלח והפנול. תנאים אלה לא אמורים לגרום לאובדן חומר או חוסר יעילות של אוסף RNA אם מבוצע כמתואר ושימוש באתנול טהור מספיק. - פלט את הרנ"א לזרז על ידי צנטריפוגה הצינורות ב 12,000 x g במשך 30 דקות בטמפרטורת החדר.
- השליכו את הסופר-נט ושטפו את הכדור פעמיים עם 80% v/v אתנול, ואוספים אותו בכל פעם על ידי צנטריפוגה ב 12,000 x גרם במשך 10 דקות בטמפרטורת החדר.
- יבש את כדורי הרנ"א על ידי פתיחת מכסי הצינור והנחת הצינורות הפתוחים בתנור בלוק יבש להגדיר 45 °C (75 °F) למשך 10 דקות. להמיס את הכדור היבש התוצאה ב 20 μL של חיץ 1x HE.
- להעריך את ריכוז RNA התוצאה באמצעות מדידת ספקטרום סופג UV.
הערה: ניתן להעריך עוד יותר את אורך שבר הרנ"א ואת הכמות הכוללת באמצעות ג'ל-אלקטרופורזה דנטורינג, כגון במנגנון אלקטרופורזה ג'ל נימי אוטומטי המבוסס על פלואורסצנטיות.
- אימונופורציה משותפת סלקטיבית של SSU על ידי eIFs מתויג וניתוח כתם מערבי של העשרת SSU סלקטיבית
הערה: השתמש ~15 AU (260 ננומטר) של שבר SSU מעוכל מופרד משקעים מהשלב 1.4.11 כדי לבצע טיהור זיקה באמצעות חרוזי IgG מגנטיים. שמור ~ 5% מהשבר SSU כפקד קלט (שבר קלט, I). eIF4A מתויג (TIF1-TAP; תג טיהור זיקה טנדם) זן שמרים שימש אשר גם מאפשר לזהות eIF4A על ידי בדיקה עבור תג TAP באמצעות נוגדן אנטי TAP.- העברה 100 μL של השעיית חרוזים IgG מגנטי (1 מ"ג של החרוזים שימשו עבור כל 15 AU (260 ננומטר) של ליסאט או שבר) לתוך חלבון נמוך חדש מחייב 1.5 mL צינור; לאסוף את החרוזים באמצעות מתלה מגנטי ולשאף אותם.
- לשטוף את החרוזים המגנטיים פעמיים עם 1 מ"ל של חוצץ 1 באמצעות resuspension רציף על ידי pipetting ואיסוף באמצעות המתלה המגנטי.
- לאחר הכביסה, לאסוף ולקבע את החרוזים, תוך שמירה אותם על המדף המגנטי.
- מוסיפים את שבר SSU לחרוזים שנשטפו ודגר את התערובת במשך 4 שעות עם סיבוב ב 4 °C (75 °F) ב cyclomixer להגדיר ~ 20 סל"ד.
- לאסוף את החרוזים באמצעות מתלה מגנטי ב 4 °C (4 °C) ולשמור את supernatant (שבר זרימה דרך, FT).
- לשטוף את החרוזים פעמיים ב 4 °C (55 °F) עם חוצץ 1 בתוספת 4 mM DTT, בכל פעם מסתובב במשך 10 דקות cyclomixer ואיסוף ו decanting החרוזים על המדף המגנטי. שמור את הכביסות (שברי W1 ו- W2).
- עבור יישום אנליטי כגון סופג מערבי, לחמוק החומר הכרובל תחת denaturing והפחתת תנאים על ידי הוספת LDS (ליתיום דודסיל סולפט) polyacrylamide ג'ל אלקטרופורזה (PAGE) חוצץ מדגם עם pH 8.5 עד 1x ו- DTT ל 2 mM.
- מחממים את התערובת ב 95 °C (5 דקות) בבלוק תרמי כדי לסיים את ההעמלה.
- לאסוף את החרוזים באמצעות המדף המגנטי ולשחזר את eluate denatured (שבר E) בחלבון נמוך טרי מחייב 1.5 מ"ל מיקרוצנטריפוגה צינור.
- השתמש בשבר E מהשלב הקודם כדי להפעיל דף נתרן דודסיל סולפט (SDS) מיד, או לאחסן את שבר E ב -20 °C (70 °F).
הערה: עבור אוסף הכנה של מתחמי תרגום מועשר TAP-תג עבור כל יישום הבא, להשתמש בגישה חלופית elution באמצעות טבק חרוט וירוס (TEV) פרוטאז. עיין בטבלה המשלימה 1 לקבלת פרטים נוספים. - כדי לרכז את שברי FT, W1 ו- W2 לדלל, לזרז את החומר שלהם על ידי הוספת 3x כמויות של אצטון קר כקרח. לדגור את תערובת אצטון מדגם ב -20 °C (50 °F) במשך 3 שעות.
- גלולה את המשקעים על ידי centrifuging הצינורות ב 13,000 x g במשך 10 דקות ב 4 °C (70 °F).
- להשליך את supernatant ואוויר לייבש את הכדור בצינורות הפתוחים בטמפרטורת החדר במשך 30 דקות.
- להמיס את הכדור ב 7 μL של 1x LDS טעינת חוצץ בתוספת 2 mM DTT. מחממים את הדגימות בבלוק תרמי להגדיר 95 °C (5 דקות).
- טען את כל דגימות I, FT, W1, W2 ו- E על 4%-12% w /v של שיפוע אקרילאמיד, ג'ל denaturing polyacrylamide ביס-טריס. הפעל את הג'ל באמצעות 1x MES SDS (2- [N-mopholino]חומצה אתנסולפונית, נתרן דודסיל סולפט) חוצץ ריצה ב 80 V, עד סמן החלבון (10-250 kDa) נפתר היטב וצבע העופרת מגיע לתחתית הג'ל.
הערה: מומלץ לטעון דילול טורי של WCL (תא שלם ליסאט) (2-10 מיקרוגרם) על הג'ל כפקד. זה עשוי לקחת כמה ניסיונות להשיג טעינה דומה של הג'ל על פני חומר השבר. - העבר את תכולת החלבון של הג'ל על קרום דיפלואוריד פוליווינילידן (PVDF) בשיטת העברה רטובה ב 100 V עבור 1 שעה בחדר קר כפי שהומלץ על ידי יצרן ציוד סופג מערבי.
- לחסום את הממברנה באמצעות חוצץ חסימה מתאים (פוספט חוצץ מלוח מבוסס) בטמפרטורת החדר במשך 1 שעות תחת רעד מתמיד.
- בעקבות הוראות היצרן לדילול נוגדנים, יש לבדוק את הממברנה עם נוגדן אנטי-TAP לאיתור חלבון eIF4A מתויג, נוגדן אנטי-Pab1p או נוגדן אנטי-β-אקטין (או כל מטרה רצויה אחרת) על ידי דגירה לילית של הממברנה עם נוגדן מדולל של Buffer חסימה (PBS) (1:1,000 דילול) בציקלומיקסר בחדר קר.
הערה: 1:1,000 דילול נוגדנים הוא נקודת התחלה טובה. - לשטוף את הממברנה שלוש פעמים עם 1x פוספט חוצץ מלוח, 0.2% v / v Tween 20 (PBST) במשך 10 דקות כל אחד.
- לחקור את הממברנה עם נוגדנים משניים שכותרתו פלואורסצנטית בעקבות הוראות היצרן על ידי דגירה בציקולם בטמפרטורת החדר במשך 1 שעות.
הערה: 1:20,000 דילול נוגדנים הוא נקודת התחלה טובה. - לשטוף את הממברנה שלוש פעמים עם 1x PBST במשך 10 דקות כל אחד. לשטוף בקצרה את הממברנה עם מים deionized, ולאחר מכן עם מתנול מוחלט. יבש ודמיין את הממברנה במערכת הדמיה פלואורסצנטית בהתאם להוראות היצרן.
הערה: כתמים עבור חלבונים אחרים ניתן להשיג באמצעות נוגדנים משניים עם צבעים התואמים ערוצים פלואורסצנטיים שונים (כגון eIF4A-TAP לעומת זוג β-actin המשמש כאן), על ידי כתמים רציפים או הפשטה והכתמה של אותה קרום או חיתוך הממברנה מג'ל טעון עם דפוס חוזר של שברים ובחינת כל חתיכה בנפרד עם נוגדנים בהתאמה (כמו בדוגמה Pab1p המשמש כאן).
2. פרוטוקול תא יונקים
- תרבית תאים של יונקים קיבעון
- ב 2 T-175 צלוחיות, לגדל HEK293 תאים ל 60%-70% מפגש בינוני נשר שונה של Dulbecco ו 10% v / v סרום בקר עוברי ב 37 °C ו 5% v / v פחמן דו חמצני.
הערה: המדיה המלאה נעשית על ידי הוספת 55 מ"ל של FBS מסחרי לתוך 500 מ"ל של DMEM שנרכש מסחרית עם גלוקוז גבוה, המכיל L-גלוטמין, פנול אדום ונתרן ביקרבונט, אבל לא HEPES או נתרן פירובט. ספירת תאים לכל בקבוק T-175 ב 70% מפגש צריך להיות בטווח של 1.7-2.0 x 107. - לפחות 3 שעות לפני זמן הקיבעון הרצוי, החלף את המדיה של צלוחיות T-175 בדיוק עם 30 מ"ל של מדיה מלאה מחוממת מראש ולהחליף את הבקבוקונים בחממה תא.
הערה: ודא שהמדיה הטרייה מועברת לצד הנגדי של הבקבוקון אל שכבת התא כדי למנוע ניתוק תאים. ניסיון לנהל את חילופי התקשורת מהר ככל האפשר, החדרת הפרעה מינימלית של גז ואיזון טמפרטורה. - לאחר החלפת המדיה הסלולרית, הכין מאגרים וכימיקלים הדרושים עבור קיבעון. הכן את מלאי הפוספט-מלוח של Dulbecco עם גליצין של 50 מ"ר על ידי הוספת 10.2 מ"ל של מלאי גליצין 2.5 M לבקבוק 500 מ"ל של DPBS וערבוב.
- הכן בקבוק DMEM בתוספת 10% FBS כמו בשלב 2.1.1 לשימוש בתנאים לא סטריליים ו 100 מ"ל aliquot של 0.25% טריפסין-EDTA. מקור בקבוק נוסף של DPBS מסחרי מראש מנוסח עם סידן כלורי (CaCl2)ומגנזיום כלוריד (MgCl2).
הערה: ניתן לאחסן את הפתרונות ב- 4 °C (4 °F) למשך עד שבועיים. - הכן קופסת קרח עד הקצה עם קרח מים כתוש, כך בקבוק T-175 יכול להתאים באופן שווה על גבי ולשמור על מכסה המנוע אדים יחד עם חוצצים מוכנים, גם על קרח.
הערה: בשל התגובות המהירות של תרגום לכל שינוי סביבתי, יש למזער את כל התזמונים בין הסרת צלוחיות התא מהחממה לבין הוספת פתרון הפורמלדהיד. - כדי לצנן את התאים, להסיר את בקבוקון T-175 מן החממה ולחץ אותו בחוזקה על הקרח הבטחת מגע משטח מקסימלי. בתוך מכסה המנוע של האדים הכימיים, הטה את הבקבוקון על צידו כך שהתקשורת תאסוף בצד שממול לתאים. Pipette 168 μL של 37% w /v פורמלדהיד ישירות לתוך המדיה המאובזרת (לריכוז סופי של 0.2% w/v). מערבבים מיד על ידי נדנדה עדינה של הבקבוקון קדימה ואחורה, סוגרים וממקמים מחדש את הבקבוק על הקרח, ומבטיחים שהוא אופקי והתאים מכוסים באופן שווה.
זהירות: פורמלדהיד הוא חומר מזיק עם תופעות לוואי פוטנציאליות לטווח ארוך וגם גירוי הן למערכת הנשימה והן לעור. זה צריך להיות מטופל רק במכסה אדים כימי מתאים. מיכלים של פורמלדהיד חייב תמיד להיות אטום כאשר מחוץ למכסה המנוע אדים.
הערה: ודא כי פורמלדהיד מתווסף ישירות למדיה התא ולא לקיר הבקבוק. שלב 2.1.6 אמור להימשך פחות מדקה אחת. - לדגור את הבקבוקונים על הקרח במשך 10 דקות נוספות. יוצקים את המדיה לתוך מיכל פסולת מתאים דרך הצד הבקבוקון מול התאים.
- בעזרת סטריפט, פיפטה ב-30 מ"ל של תמיסת מלח מכווצת פוספט של דולבק ללא יוני סידן ומגנזיום, ובנוסף מכילה גליצין של 50 מ"ר, בעדינות בצד שממול לתאים. מערבבים על ידי נדנדת הבקבוק; מחזירים את הבקבוק למיקום אופקי ודגרה במשך 10 דקות נוספות על הקרח.
- יוצקים את התמיסה דרך הצד הבקבוקון מול התאים ולהוסיף בעדינות 7 מ"ל של פתרון טריפסין-EDTA סטנדרטי 0.25% w /v כדי לנתק מחדש את התאים. לדגור על הבקבוק בטמפרטורת החדר במשך 5-10 דקות.
הערה: ודא פתרון טריפסין-EDTA מכסה את כל התאים באופן שווה. יש להשתמש בהטיה ונדנדה עדינה תקופתית כדי לקדם ניתוק תאים. - מעבירים את הבקבוק אנכית ובאמצעות פסים אוספים את התאים המנותקים על ידי שטיפת כל התאים הנותרים מקירות הבקבוקון. מעבירים את המתלים לצינור 50 מ"ל על קרח.
הערה: תאים קבועים יכולים להיות שבירים יותר; אין להנחית בעוצמה או יותר ממה שנדרש כדי לנתק את התאים מקיר הבקבוקון. - מיד להשלים את השעיית התא שנאסף עם 20 מ"ל של מדיה מלאה (מדיה קר קרח לא סטרילי עם 10% FBS) ומערבבים על ידי היפוך עדין של הצינור.
הערה: המדיה תרבית התא המלאה (כולל 10% FBS) מתווספת כדי לנטרל את טריפסין, מניעת נזק נוסף קרום התא והתפוררות התא. - גלולה את התאים על ידי centrifuging הצינור ב 100 x g במשך 5 דקות ו 4 °C (75 °F). גלולה תא חייב להיות גלוי בבירור.
- יוצקים את המדיה בעדינות resuspend את גלולה התא ב 10 מ"ל של DPBS קר כקרח עם Ca2 +, מ"ג2 +, וללא גליצין.
- חזור על שלב 2.1.12.
- יוצקים את מאגר הכביסה ומניחים מחדש בעדינות את גלולה התא ב-800 מיקרו-אל של DPBS קר כקרח עם Ca2+, מ"ג2+, ללא גליצין, על קרח. העבר את התאים resuspended לתוך חלבון נמוך חדש מחייב 1.5 מ"ל צינור microcentrifuge.
- צנטריפוגות הצינור ב 100 x גרם במשך 3 דקות ו 4 °C (5 °F). בזהירות להשליך את supernatant באמצעות pipettor 1 מ"ל. בשלב זה, כדור התא יכול להיות קפוא ב -80 °C (80 °F) או להמשיך לשלב תמותת התא.
הערה: כדורי תאים קפואים ניתן לאחסן ב -80 °C (80 °F) עד שנה אחת. מצאנו כי הקפאת כדורי התא מקלה על תמה לאחר מכן וממליצה להקפיא גם אם אחסון לטווח ארוך אינו מתוכנן.
- ב 2 T-175 צלוחיות, לגדל HEK293 תאים ל 60%-70% מפגש בינוני נשר שונה של Dulbecco ו 10% v / v סרום בקר עוברי ב 37 °C ו 5% v / v פחמן דו חמצני.
- שיבוש תאי יונקים ואיסוף ציטוסול
- בארון בטיחות ביולוגית, להוסיף 300 μL של מאגר תמוגה מבוסס על חומר ניקוי לא,חד-תכליתי ו 7 μL של מעכב RNase 40 U/μL. מערבבים היטב על ידי צנרת באמצעות קצה 1 מ"ל.
- בזהירות לצרף מחט 25 G למזרק 1-3 מ"ל ו pipette במרץ את התערובת, באמצעות לפחות שבע צריכת איטי כלפי מעלה ומשיכות פליטה במהירות כלפי מטה.
- להשליך את המזרק ואת המחט לתוך פח חדה ולחזור על ההליך באמצעות מזרק 0.3 מ"ל מצויד מחט 31 G.
- להשליך את המזרק ואת המחט לתוך פח חדה. צנטריפוגות הצינורות ב 4 °C (5 °F), 12,000 x g במשך 5 דקות כדי גלולה את פסולת התא.
- העבר את supernatant לתוך חלבון נמוך חדש מחייב 1.5 מ"ל צינור microcentrifuge. לאחסן את שניהם, את פסולת התא (למטרות בקרה) ואת lysate התא המובהק כתוצאה ב -80 °C (70 °F).
הערה: הצפיפות האופטית של lysate נע בין 25-30 AU260 כאשר שני צלוחיות T-175 משולבים ואת אמצעי האחסון המומלצים אחריו. ניתן לאחסן את ריסטים ופסולת התא ב -80 °C (80 °F) עד שנה אחת.
- הפרדת המתחמים הריבוזומליים הקבועים (פולי) מהשברים הלא מתורגמים של הציטוסול
- הכן שיפועים ליניאריים 15%-45% עם סוכרוז בצינורות פוליפרופילן דקים בקיר 13 מ"ל, 14 x 89 מ"מ, בשיטת הפשרת ההקפאה בדרך כלל כמתואר בשלב 1.3.1 של פרוטוקול השמרים, אך באמצעות חיץ 2 (איור 2a).
הערה: להפשיר את השיפועים לילה בחדר קר בשעה 4 °C (70 °F) בלילה שלפני השבר. - טען 150-250 (מקסימום 300) μL של lysate התא מהשלב הקודם 2.2.5 אל מעברי הצבע מאוזנים. יש לאחסן את ה- lysate הנותר ב- -80 °C (70 °F) ולהשתמש למטרות בקרה.
הערה: כאן דוגמה של הפרדה מבוססת משקעים לשברים פוליסומליים, ריבוזומליים ו' חופשיים 'SSU מסופקת. עיין בטבלה המשלימה שסופקה 1 לקבלת גישה חלופית. - Ultracentrifuge הצינורות בנפח בינוני נדנדה דלי רוטור ב 4 °C (5 °F), כוח G ממוצע 178,305 x g (k-factor 143.9) במשך 1 שעות 45 דקות.
- 30 דקות לפני השלמת הסיבוב, להגדיר ולנקות את שבר מעבר הצבע, כמתואר בשלבים פרוטוקול שמרים 1.4.7-1.4.9.
- חלק את מעברי הצבע בדרך כלל כמתואר בשלבי פרוטוקול שמרים 1.4.10-1.4.11.
הערה: שלב זה יפריד בין שברי SSU פוליזומליים, ריבוזומליים ו'חופשיים'. ניתן להשתמש בשברים פוליזומליים בניסויי פרופיל פוליזום. - העבר מיד את השברים שנאספו על קרח ואם לא מעובד נוסף, יש לאחסן ב-80 מעלות צלזיוס עד 6 חודשים.
הערה: אם שינוי צינור מלקט השבר מסונכרן עם זיהוי שבר מקוון הפרדה, אנו ממליצים להשתמש עד 800 שברי μL (זמן איסוף של 32 s לשבר ב 1.5 מ"ל / דקה). אם השבר מבוצע מבלי להשתמש בקריאת הספיגה בשורה, מומלץ להשתמש בשברים של 250-500 μL (10-20 s לשבר ב- 1.5 מ"ל/דקה). לאחר ההפרדה, השברים יכולים לשמש עבור אימונופורציה, מיקרוסקופיית אלקטרונים, denaturing PAGE וכתם מערבי מיד, או נתון היפוך crosslink עבור ניתוחי RNA ו / או פרוטאומיים הבאים.
- הכן שיפועים ליניאריים 15%-45% עם סוכרוז בצינורות פוליפרופילן דקים בקיר 13 מ"ל, 14 x 89 מ"מ, בשיטת הפשרת ההקפאה בדרך כלל כמתואר בשלב 1.3.1 של פרוטוקול השמרים, אך באמצעות חיץ 2 (איור 2a).
תוצאות
מתחמי תרגום רגישים להרכב היוני של המאגרים, וזה חשוב במיוחד במהלך ultracentrifugation שבו תכונות משקעים מוערכים. לכן בדקנו מספר מאגרי משקעים באמצעות ליסאט מובהר המופק מחומר שמרים לא קבוע הקרקע, על מנת לבחור תנאים המתאימים ביותר לפתרון מתחמי תרגום ואיחודי משנה ריבוזומליים נפרדים (SSU, LSU), מונוזומים (RS) ופוליוזומים מעבר למעבר. כל המאגרים התבססו על הרכב הליבה המכיל 25 mM HEPES-KOH pH 7.6 ו- 2 mM DTT. הריכוזים של KCl, MgCl2, CaCl2ו- EDTA שונו עוד יותר על פני המאגרים (איור 2a), ורכיבים אלה נוספו לליסטים לפני טעינה הדרגתית ולמאגרי מעברי הדוע של סוכרוז לפני יציקת הדרגתיות, בהתאם.
במאגרים 1 ו -2 מתחמי תרגום שנפתרו היטב הושגו. חוצץ 1 הביא להפרדה טובה יותר של תת-units ריבוזומליים קטנים (SSUs) (איור 2a). אומיטנס של MgCl2 ותוספת של EDTA (מאגרים 3,4) גרמו לאובדן תכונות המשקעים הגבוהות עבור רוב הפוליוזומים וסביר להניח שהפירוק החלקי שלהם(איור 2a). בעוד תוספת של 2.5 מ"מ CaCl2 הביאה לפסגות פוליזומליות קצת יותר הומוגניות, השיפור היה שולי והכמות הכוללת של החומר הפוליזומלי ירדה במקרה זה (איור 2a) בהשוואה למאגרים 1 ו -2. לכן בחרנו במאגר 1 כחוצץ העבודה של בחירה.
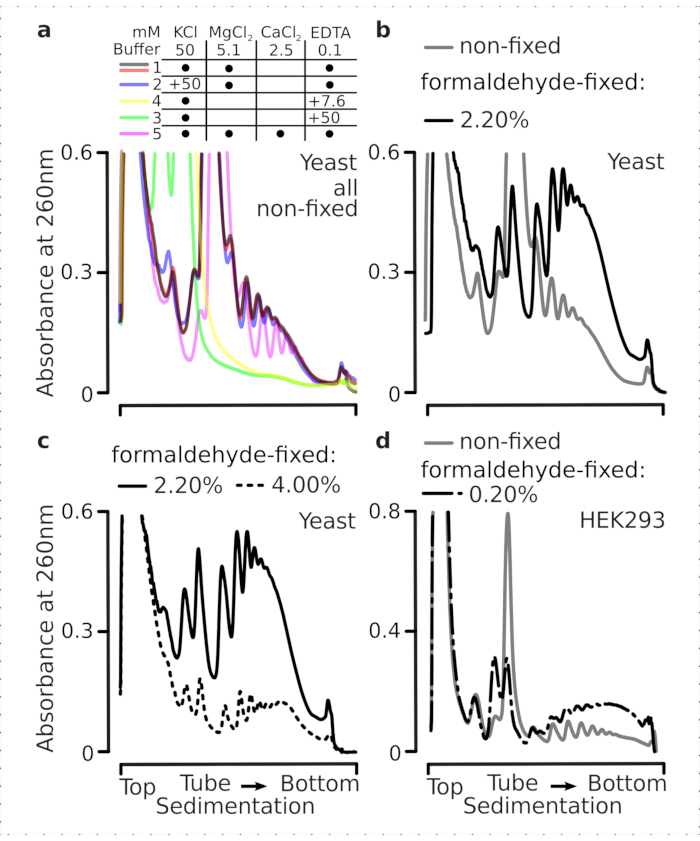
איור 2: תנאי חיץ לחילוץ מורכב תרגום והערכה של ההשפעה המייצבת של הקיבעון. מוצגים פרופילי ספיגת UV שנאספו ב 260 ננומטר עבור סך תאי שמרים ליסאט מופרדים 10%-40% w / v סוכרוז הדרגתיים. (א)השפעות של מלחים חד- וחלוקתיים ובדל יוני מגנזיום על משקעים של חומר המופק מתאי שמרים שאינם קבועים. קווים אדומים ואפורים מייצגים שכפול טיפוסי. (ב,ג) השוואה של ליסאטים הנגזרים מתאי שמרים לא קבועים (קו אפור), 2.2% (קו שחור) ו-4.4% (קו מנוקד שחור) עם /v של תאי שמרים קבועים בפורמלדהיד. (ד)ייצוב של פוליזומים על ידי 0.2% ממוטב w /v של קיבוע פורמלדהיד (קו מקווקו ומנוקד שחור) של תאי HEK 293T, בהשוואה לחומר מאותם תאים שאינם קבועים (קו אפור). אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
לאחר מכן בדקנו את ההשפעה של ייצוב פוליזומלי על ידי קיבעון עם ריכוזי פורמלדהיד שונים. באמצעות אותם גישות של חומר תא, מאגרים, טיפול בתאים ותזמון, השווינו בין חומר המופק מתאים ותאים לא קבועים קבועים עם 2.2% ו-4% w/v של פורמלדהיד(איור 2b,c). מצאנו כי 2.2% w / v של פורמלדהיד היה מתאים יותר לקיבעון כמו בעוד זה שמר מצוין polysomes כפי שניתן לשפוט על ידי יחס polysome-למונום(איור 2b),זה לא להפחית את התשואה הכוללת של החומר ריבוזומלי לעומת 4% w / v של פורמלדהיד, אשר הפגין סימנים ברורים של קיבוע יתר(איור 2c).
עבור החומר הנגזר מתאי יונקים, בשל יחס נפח מאגר-לתא של תמוגה גדול יותר הנדרש על-ידי החילוץ מבוסס הניקוי, נעשה שימוש במאגר 2 (איור 2a). זה יצר מתחמי תרגום שנפתרו היטב עם משקעים בשיפועים סוכרוז(איור 2d). ראוי לציין, ריכוז נמוך בהרבה של פורמלדהיד של 0.2% w / v שימש, כמו ריכוזים גבוהים יותר הביא לאובדן חומר פוליזומלי וריבוזומלי משמעותי (נתונים לא הראו). בדמיון לתוצאות שהושגו עם תאי שמרים, חומר מיוצב crosslink הפגין שימור טוב יותר של הפוליזומים ויחס פוליזום-מונוסום גבוה יותר (איור 2d).
לאחר מכן בדקנו אם תנאי קיבוע הפורמלדהיד שנבחרו יעילים מספיק כדי לייצב mRNA מתורגם באופן פעיל בתוך השברים הפוליזומליים כתוצאה של crosslinking, ואת התשואה הפויזומלית המשופרת היא לא רק תוצאה של עיכוב תפקוד האנזים והתקדמות התארכות התרגום. השתמשנו ב- EDTA ובמלח מונובלנטי גבוה (KCl) כדי לערער את היציבות בפוליוזומים ובריבוזומים. ריאגנטים אלה נוספו ליסאטים תא שמרים מובהר, ונכללו בכל המאגרים הבאים מעברי צבע סוכרוז על גבי הרכב המאגר 1, בהתאמה.
ואכן, 15 מ"מ EDTA הציג אפקט פחות מערער על השברים הפוליזומליים הנגזרים מהתאים הקבועים (איור 3a),המאשרים כי המתחמים המקושרים חזקים יותר. ניתן להתגבר במידה מסוימת על ההשפעות המערערות של EDTA על ידי הגדלת הריכוז של פורמלדהיד, שכן חומר מ-4% מהתאים הקבועים בפורמלדהיד התנגד להתפתחות טובה יותר(איור 3a). עם זאת, הגדלת ריכוז EDTA ל-50 מ"מ הביאה לערעור היציבות של רוב מתחמי התרגום בתנאים קבועים ולא קבועים, כפי שניתן להסיק מהמשבעים האיטיים יותר של החומר והיעדר פסגות מעוצבות היטב (איור 3b). זה יכול להיות מוסבר על ידי התגלגלות חלקית של מבנים ואובדן הכולל של קומפקטיות, ולא על ידי ניתוק מלא של רכיבים פוליזומליים מן mRNA. גם במקרה זה, החומר המקושר הפגין משקעים מהירים יותר (איור 3b).
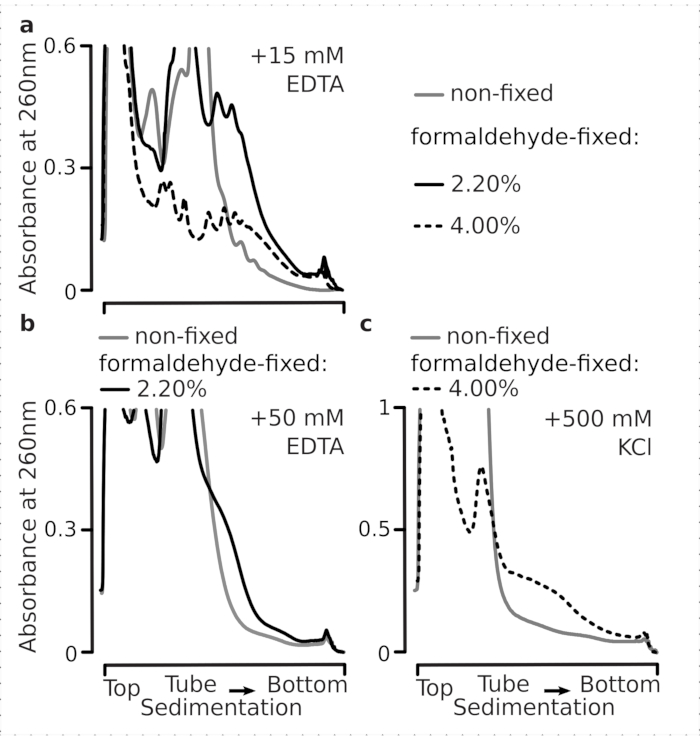
איור 3: ההשפעות של קיבעון פורמלדהיד שמרים in vivo על היציבות של פוליזומים. חוצץ 1 (ראה טקסט ואיור 2a) שימש בכל הניסויים. סוג נתונים והתווייה כמתואר במקרא איור 2. (א)השוואה של תוספת של 15 mM EDTA לתא lysates ומאגרים הבאים על היציבות של polysomes נגזר לא קבוע (קו אפור), 2.2% (קו שחור) ו 4% (קו מנוקד שחור) w / v של תאים קבוע פורמלדהיד. (ב)זהה (( א), אך לתוספת של 50 mM EDTA ולא כולל 4% w /v של תאים קבועים פורמלדהיד. (ג)זהה (( ),אך עבור תוספת של 500 mM KCl ולא כולל 2.2% w /v של תאים קבועים פורמלדהיד. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
בדומה להשפעות EDTA, ב 500 mM KCl, מצאנו שיפור משמעותי של היציבות עם 4% w / v של קיבוע פורמלדהיד (איור 3c). אובדן הקומפקטיות לכאורה במקרה זה יכול להיות מוסבר גם על ידי ניתוק חלקי של המרכיבים של מתחמי ריבוזומליים, ולא ניתוק מוחלט שלהם מן ה- RNA. בסך הכל, פוליזומים הנגזרים מתאים קבועים פורמלדהיד הפגינו עמידות גבוהה יותר להתפתחות ולערעור מבני, בקנה אחד עם יצירת קשרים קוולנטיים נוספים בתוך מתחמים אלה.
במהלך מגרה תנאי גדילה, mRNAs יכול להיות יזם במהירות וכתוצאה מכך הצטברות של ריבוזומים מרובים על אותן מולקולות mRNA, אשר יוצרים מבנים המכונה polyribosomes, או polysomes. ניתן להפריד בין פוליזומים על-ידי אולטרה-צנטריפוגה בשיפועים של סוכרוז, שם הם משקעים על סמך הסדר שלהם (מספר ריבוזומים המחוברים בו זמנית ב- mRNA). כאשר התרגום מודחק, ריבוזומים אינם עוסקים בסבב תרגום נוסף בקרוב, וכתוצאה מכך (חלקי) 'פירוק' של פוליזומים, אשר מוצג כמעבר מודאלי לכיוון הפוליוזומים מסדר נמוך יותר והצטברות של מונוזומים4,26.
מודל של תגובה תרגומית שניתן לדמיין ברמת התפלגות הסדר הפוליזום יכול להיות מסופק על ידי רעב גלוקוז. דלדול גלוקוז מעורר את אחת ההשפעות המעכבות התרגומיות הדרמטיות והמהירות ביותר על שמרים1,3,40. מחקרים קודמים הוכיחו כי בתוך 1 דקות של דלדול גלוקוז, אובדן polysomes, הצטברות של monosomes ועיכוב של חניכת התרגום יכול להתרחש4. בתוך 5 דקות של תוספת גלוקוז מחדש, התרגום משוחזר במהירות עם עלייה ניכרת polysomes3,4. כמו כן נצפתה כי התרגום היה מעוכב כאשר תאים נחשפו למדיה המכילה גלוקוז של 0.5% (w/ v) או נמוך יותר ולא נראתה השפעה ברמות הגלוקוז של 0.6% (w/v) ומעלה.
לכן ביקשנו לקבוע אם תנאי הקיבעון שלנו מתאימים לשימור ההבדלים התרגומיים בתוך הדינמיקה של תגובת לחץ גלוקוז, כפי שניתן להעריך על ידי יחס פוליsome-למונוסום. השווינו את החומר מהתאים הגדלים בשלב בינוני מעריכי על גלוקוז גבוה (2.00% w/v הוסיף) עם אלה שהועברו במשך 10 דקות למדיה עם לא או נמוך הוסיף (0.00% או 0.25% w / v, בהתאמה) גלוקוז. הקיבעון בוצע באמצעות 2.2% w/v של פורמלדהיד במקביל לבקרה (לא מורעב; החלפת מדיה מהירה עם אותה מדיה סטנדרטית המכילה 2% w / v הוסיף גלוקוז, ואחריו דגירה במשך 10 דקות קיבעון) ו 10 דקות מורעב (החלפת מדיה מהירה עם מדיה זהה אבל נמוך 0.25 w / v או לא גלוקוז נוסף, ואחריו דגירה במשך 10 דקות קיבעון) תאים.
בהתאם לממצאים הקודמים, ראינו שתאי שמרים מדכאים במידה רבה את התרגום על לחץ רעב לגלוקוז(איור 4a). שניהם, ללא תוספת ותנאי גלוקוז נמוכים גרמו לפירוק פוליזום, עם מעט אך ככל הנראה יותר פוליזומים שנשמרו במקרה של תוספת גלוקוז נמוכה. לכן, התגובה להסרת גלוקוז שמרים עשוי להיות לא מסוג all-on או all-off והוא מכוון בהדרגה. אישור הציפיות לפעולה מייצבת של קישור פורמלדהיד, חומר פוליזומלי מהתאים הקבועים הפגין הבחנה גבוהה יותר בין התאים הרעבים והלא מורעבים, וניתן לטעון כי שמר על טווח דינמי גבוה יותר של התגובה (איור 4b). באופן מסקרן, במקרה של חומר מהתאים הקבועים, ריכוז גלוקוז נמוך נוסף הביא לשפע הפוליזומלי הספציפי המובחן הרבה יותר ממצב הגלוקוז ללא תוספת, בהשוואה לתאים הלא קבועים (איור 4a). זוהי אינדיקציה חזקה להתאמת גישת קיבוע פורמלדהיד בשימור ולכידת הבדלים דקה וחולפים יחסית בשיווי המשקל של תהליכים דינמיים מאוד, כגון במהלך תגובות תרגומיות.

איור 4: לכידת שינויים מהירים בתרגום השמרים לאחר הרעבת גלוקוז. חוצץ 1 (ראה טקסט ואיור 2a) שימש בכל הניסויים. סוג נתונים והתווייה כמתואר במקרא איור 2. (א)ליסאטים של תאים המתקבלים מ- non-starved (קו אפור), מורעבים לגלוקוז מוגבל (0.25% w/v הוסיף גלוקוז במשך 10 דקות; קו חום) ורוקנו גלוקוז (ללא תוספת גלוקוז במשך 10 דקות; קו אדום) תאי שמרים לא קבועים. (ב)זהה ל- (a), אך עבור 2.2% w/v תאים קבועים פורמלדהיד. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
ניטור מצב תרגום על ידי ריבוזומים הקשורים לתרגום פעיל mRNA באמצעות משקעים הדרגתיים סוכרוז ('פרופיל polysome') היא טכניקה מיושמת נרחבת26,27,28. בשילוב עם ניתוח microarray כמותי ולאחרונה עם רצף תפוקה גבוהה28,44, פרופיל polysome מספק מידע על mRNAs הקשורים ריבוזום תמלול רחב. עם מספר הנחות, נטען באופן מסורתי בתחום המחקר ביוסינתזה חלבון כי נוכחות פוליזומלית היא אינדיקציה למעורבות פעילה בתרגום של mRNAs בהתאמה. מסקנה נוספת היא לעתים קרובות (אך לא תמיד) מוצדקת, כי ריבוזומים יותר נוכחים על mRNA באורך נתון (גבוה יותר את הסדר של polysomes), פעיל יותר כי mRNA מעורב בתרגום. לכן, הפרדת השבר הפוליזומלי משאר החומר יכולה להיות שימושית מנקודת המבט של בידוד הרנ"א המתורגם באופן פעיל. בתוך גישות פרופיל טביעת הרגל, ובמיוחד TCP-seq10,38,39 המייצר אוכלוסייה נפרדת של יחידות SSUs המשוחררות הנגזרות מהסריקה, התחלה והפסקה של מתחמי קודון, ייתכן שיהיה תובנה נוספת להסיר תת-יחידות ריבוזומליות שאינן משקעות משותפות עם המונוזומים המלאים או הפוליוזומים.
לכן השתמשנו בהפרדה של mRNPs 'לא מתורגמים' כגון SSU חינם (mRNA מאוגד SSU יחיד או SSU ללא mRNA מצורף) הרחק ממאגר 'תרגום פעיל' של mRNAs. כדי להשיג זאת, הנחנו כי mRNAs המעורבים באינטראקציות עם אחד (מונו)או מספר ריבוזומים (polysomes) ניתן לתרגם באופן פעיל. מתחמים כאלה יכולים להיות מופרדים מהאחרים על ידי מקדם המשפך הגבוה שלהם. הצענו גם להפריד את מאגר ה- mRNAs 'המתורגם באופן פעיל' לכרית סוכרוז (50% w /v של סוכרוז) במקום גלולה ישירה של החומר על קיר הצינור. צנטריפוגה של מתחמי משקעים מהירים לתוך הכרית אפשרה לנו לפקח על ההפרדה באמצעות קריאת פרופיל ספיגה ולהשיג תפוקה גבוהה יותר של החומר solubilized, לא צבור ולא denatured, לעומת גלולה מחדש solubilization10,38.
בסך הכל, כדי לטהר את SSUs בודדים, ריבוזומים, disomes, ו polysomes דחוסים באופן קומפקטי בסדר גבוה יותר, ליסאטים מובהרים קבועים היו נתונים לתהליך אולטרה-צנטריפוגה דו-שלבי (איור 5). בשיפוע הסוכרוז הראשון, האולטרה-צנטריפוגה הביאה להפרדה של SUS ו- LSUs בחינם בחלק העליון (10%-20% w/v של סוכרוז) של מעבר הצבע, ואילו המאגר המתורגם עם הצלבה כולל פוליזומים ו- mRNAs הקשורים לריבוזום שלם אחד התרכז בתחתית (50% w/v של סוכרוז) של השיפוע (איור 5a ). 50% התחתונים של שכבת סוכרוז המכילה את מאגר ה- mRNA המתורגמת התרכזו אז וה- RNA שלה מתעכל עם RNase I, ואחריו אולטרה-צנטריפוגה הדרגתית שנייה של סוכרוז כדי להשיג SSU נפרד, LSU, RS, דיסומים עמידים בפני RNase (DS) וחלק קטן של פוליזומים עמידים בפני גרקלאז מסדר גבוה יותר(איור 5b). כתמים שליליים עם אצטט אורניל והדמיה עם מיקרוסקופ אלקטרונים שידור אישרו את זהות המתחמים המבודדים בכל שלב משקעים (איור 5).

איור 5: בידוד של שברי הרנ"א המתורגמים הכוללים הרחק מהרנ"א הלא מתוורגם. (a,c)סכמטית (משמאל) והתוצאות הייצוגיות המתאימות (מימין; סוג נתונים ותווית כמתואר במקרא איור 2) של (א)הפרדה הדרגתית ראשונה של סוכרוז של שברי הציטסול שאינם מתורגמים כולל SSUs בחינם ומאגר ה- mRNA המתורגם שזוהה על ידי משקעים משותפים עם ריבוזומים ופוליזומים, ותבר(ג)הפרדה בין מתחמי ריבוזומליים בודדים ששוחררו ממאגר ה- mRNA המתורגם על ידי עיכול RNase I מבוקר ועיכול אולטרה-צנטריפוגה באמצעות שיפוע סוכרוז ליניארי שני ל- SSU, LSU, ריבוזומלי (RS) ושברים לא-סומליים (DS) עמידים בפני נוקלאז. כמויות גבוהות (15 AU260)ונמוכה (8 AU260)של החומר שאינו מורעב עוכל נכללו כדי להדגים אפשרות להגדיל את עומסי האולטרה-צנטריפוגה כאשר שברים קטנים הם עניין. ניתן לזהות גם פוליזומים עמידים בפני נוקלאז מסדר גבוה יותר (למשל, טריזומים בדוגמאות שסופקו). (ב,ד) תמונות TEM מייצגות של שברים מנוגדים לאורניל אצטט מ- (a,c), בהתאמה כמתויגים. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
על מנת לבדוק את ההתאמה של משטר הקיבעון לשמירה על חלבונים ארעיים הקשורים לריבוזום (במיוחד, eIFs), בדקנו את ההשתתפות העצמית של eIF4A, eIF מעבדה הקשורה באופן דינמי לריבוזום, על פני שברי ריבוזומליים. ניצלנו את טיהור הזיקה של eIF4A Tandem (TAP) מתויג זן שמרים (TIF1-TAP) וחקרנו נוכחות eIF4A בחומר הנגזר מהתאים הקבועים לעומת לא קבועים באמצעות נוגדן אנטי TAP, בהשוואה לשפע של Pab1p כבקרה נוספת של כריכת RNA, באמצעות SDS-PAGE ואחריו סופג מערבי(איור 6).
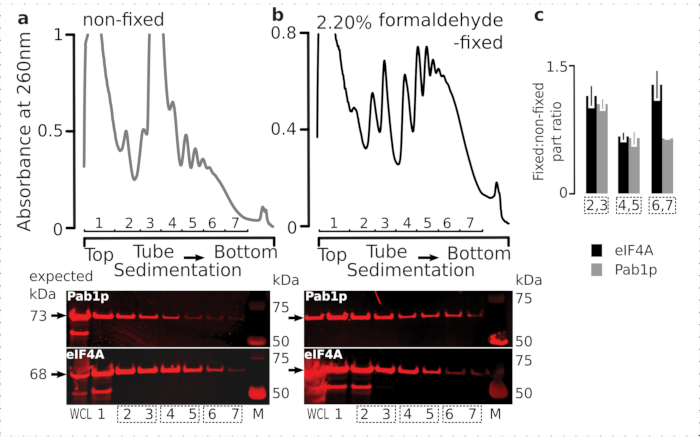
איור 6: ייצוב חלבונים ארעיים במתחמי התרגום על קיבוע פורמלדהיד בוויו. (a,b)(חלקות עליונות) ליסייט תא שלם (WCL) של (א)לא קבוע ו- (ב)2.2% תאי שמרים קבועים פורמלדהיד המופרדים על-ידי אולטרה-צנטריפוגה ומדמיינים כמתואר באגדת איור 2. (חלקות תחתונות) הדמיית כתם מערבי של שברי מעברי הצבע סוכרוז בהתאמה עם הפרדת החומר שנותח במעברי הצבע המתאימים (התוויות העליונות) ו- WCL כפקד. (ג)יחס ממוצע בין השפע eIF4A או Pab1p בשברים של חומר קבוע ולא קבוע. פרופורציות יחסיות (מנורמלות לאות של כל 2-7 השברים) של eIF4A (פסים שחורים) ו- Pab1p (פסים אפורים) חושבו על-פני 2,3 (SSU, LSU), 4,5 (RS, polysomes קל) ו- 6,7 (פוליזומים כבדים) מהנתונים של (a,b) (חלקות תחתונות) והיחס הקבוע שלהם ללא קבוע נלקח. קווי שגיאה מציינים סטיית תקן של היחס מהממוצע כאשר השברים המאוגדים (תיבות מנוקד) מטופלים כשכפולים. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
בהתאם לשפע הגבוה שלהם בתאים, ראינו בעוצמה גבוהה של האות משני החלבונים בכל התא (WCL) ושברים משקעים איטיים יותר שמקורם בתאים לא קבועים(איור 6a,לוח תחתון). זיהינו גם כמויות משמעותיות של חלבונים אלה ב- WCL המופקים מהתאים הקבועים ומרגיעים את היעילות של מיצוי החומר המקושר והיעדר הפסדים בלתי צפויים(איור 6b, לוח תחתון). עם זאת, בניגוד לתאים הלא קבועים, חומר מהתאים הקבועים הדגים נוכחות יחסית גבוהה של eIF4A בשברים ריבוזומליים המשתילים מהר יותר, בהשוואה ל- Pab1p (איור 6c). תוצאה זו מצביעה על כך eIF4A נשאר קשור יותר עם polysomes בחומר פורמלדהיד crosslinked.
לאחר שאישרנו את אפקט הייצוב החיובי והספציפי של קישור צולב על נוכחות eIF4A בשברים ריבוזומליים, השתמשנו בחומר הקבוע מזן שמרים מתויג eIF4A (TIF1-TAP) כדי ללכוד ולהעשיר מתחמים המכילים eIF4A על ידי טיהור זיקה עם חרוזים IgG מגנטיים. יש לנו שברי WCL מועשרים זיקה, SSU חינם ופוליזומלי (מאגר mRNA מתורגם) לאחר המשקעים הראשונים באמצעות הדרגתי סוכרוז (למשל, סעיף 1.3 של פרוטוקול שמרים), כמו גם SSU, LSU ו RS שברים מן המשקעים השניים עם פירוק הבריכה המתורגמת למתחמים בודדים עם RNase I (למשל, סעיף 1.4 של פרוטוקול שמרים) (איור 7 ). בכל המקרים, למעט שבר LSU, הצלחנו לצפות העשרה סלקטיבית של eIF4A בשברים המטוהרים (eluate, E), בהשוואה לנוכחות של β-אקטין בחומר המקור (קלט, I) (איור 7).
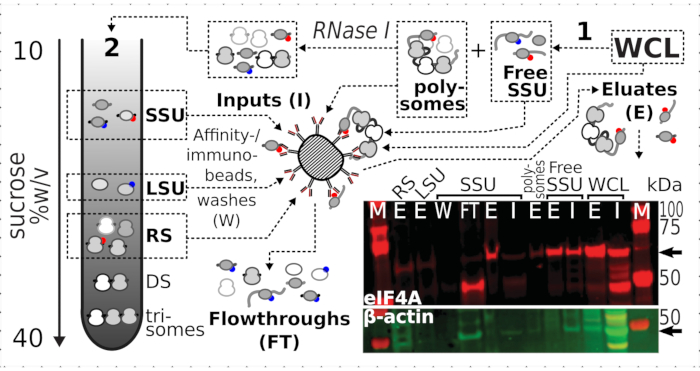
איור 7: אימונופורציה סלקטיבית של מתחמי תרגום המיוצבים על ידי in vivo פורמלדהיד על ידי eIF4A הקשורים באופן חולף. השרטוט ממחיש את המקור של מתחמי תרגום שונים ואפיטופ eIF4A, כולל WCL המובהק ללא חלק של תאי שמרי eIF4A-TAP; SSUs חינם ובריכת RNA מתורגמת (polysomes) מופרדים ב- ultracentrifugation הראשון; SSU, LSU ו- RS שברים שוחררו מן ה- RNA המתורגם על ידי RNase I עיכול מופרד באמצעות ultracentrifugation השני (ראה טקסט). תמונת כתם מערבית מספקת הדמיה של שפע eIF4A בשברים בהשוואה לשפע של בקרת β-אקטין מוכתמת בו זמנית. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
טבלה משלימה 1. נא לחץ כאן כדי להוריד טבלה זו.
Discussion
קיבוע פורמלדהיד הוא שיטה נוחה ופופולרית להשגת קישור מהיר של ויוו של ביומולקולס10,36,45,46,47,48. בהשוואה ליעדים הביו-מולולקוליים הפוטנציאליים האחרים, לכידה מוצלחת של מתחמים תרגומיים מחייבת קיבעון מיידי במהלך צינון הצמדה של התאים או חומר אחר. ללא התייצבות לא מוצהרת, קיים פוטנציאל לתהליכים שונים הקשורים לתרגום להמשיך, ולהסיט את ההתפלגות המורכבת הרחק מהמצב הלא מעורער של vivo 49. בהשוואה לשיטות האחרות של מעצר תרגום וייצוב מורכב ריבוזומלי, המהירות של פעולת פורמלדהיד על פני קרום התא והאופי חסר ההשעיה של הקישורים המבטיחים שימור של המגוון המקסימלי של מתחם התרגום המתווכים קרוב יותר למצבם המבוזר במקור50.
הגישה המוצגת כאן נקבעה ומותאמת הן בתאי שמרים והן בתאי יונקים, ושיטות נגזרו כעת על ידי קבוצות אחרות לשימוש על פני חומר ביולוגי מגוון יותר, כגון בחולייתנים שלמים (למשל, עוברים של דגי זברה)10,38,39,49,51,52 . למרות שעבודות אלה מרגיעות באופן קולקטיבי את הרבגוניות ואת הישימות הרחבה של הגישה, קישור מהיר של פורמלדהיד של מתחמי תרגום יכול להיחשב מעט קשה להחליף סוגים חדשים של חומר ביולוגי בשל הצורך של אופטימיזציות והתאמות.
דרישה בראש ובראשונה להצלחת השיטה היא אופטימיזציה מחדש של ריכוז הפורמלדהיד וטכניקת איסוף התאים וההפרעה. פחות חדיר, תאי שמרים קטנים ועגולים דורשים ריכוז פורמלדהיד גבוה בהרבה (לפחות פי 10) ושיבוש פיזי של התאים הקבועים. לעומת זאת, תאי יונקים חסידים גדולים ושטחיים בתרבית יכולים להיות קבועים יתר על המידה ודורשים טיפול עדין על קיבעון, בעוד החילוץ של מתחמים קבועים יכול להתבצע כימית עם הפרעה ממברנה באמצעות דטרגנטים. קישור תת-מוצלב עשוי לאפשר למתווכים פחות יציבים או קצרי מועד יותר לנתק או לדלוף למצב מאוחר יותר. קישור יתר עלול להשפיע לרעה על היכולת לבודד וללמוד שברים ריבוזומליים ויכול ליצור הטיות סלקטיביות כגון דלדול עמוק יותר של מתחמים כבדים. בהתבוננות שלנו, אפילו שינויים קלים, כגון סוג התאים האנושיים החסידים המשמשים, יכולים להשפיע על התשואה של מתחמי crosslinked התאושש ועשויים לדרוש אופטימיזציה מחדש של גדוד crosslinking. אנו יכולים גם לצפות כי תאים עם תכונות חדורות שונות באופן משמעותי, כגון תאים צמחיים, ידרשו אופטימיזציה נרחבת נוספת של תנאי הקיבעון52. עם זאת, קשה לדמיין סוג של חומר ביולוגי שלא יהיה תואם לחלוטין את הגישה.
שיקול אחד הנוגע לפרוטוקול קיבוע היונקים הוא הצפיפות וכמות החומר התאי המשמש כקלט. מומלץ כי התאים יגדלו ללא הרף מבלי לזרוע מחדש או הפרעות אחרות למשך יומיים לפחות, כדי למנוע השפעות חיצוניות על דינמיקת התרגום התאי. ישים עבור רוב סוגי התאים, אבל עבור רוב התאים החסידים השיג בעקביות רמות מפגש של לא יותר מ 70% יבטיח היעדר השפעות עיכוב מגע גדול שיכול להשפיע לרעה ובלתי צפוי על שיעורי התרגום.
מאפיין מעניין נוסף, ואולי נוח במיוחד, של קיבעון פורמלדהיד הנובע מהתגובה חסרת ההפלות שלו הוא השפעת הייצוב על מתחמי תרגום במערכות של טקסונומיה מעורבת. חיידקים, ועוד יותר מכך מתחמים תרגומיים של המיטוכונדריה, כלורופלסטים וטפילים תאיים שונים, היו ידועים לשמצה כקשים למיקוד עם מעכבי תרגום ספציפיים. לעומת זאת, בנתוני TCP-seq, מיפוי טביעות רגליים למיטרוטרן ניתן להבחין בקלות בנתונים38,39,50. התפתחות מעניינת לאחר מכן יכולה להיות שימוש בגישה לחקור תרגום במיקרו-קומוניזם שלם, כגון בדגימות קרקע, מים או מעיים, שבהן מעצר תרגום מהיר ואמין וייצוב מורכב בכל אמצעי אחר יהיו בעייתיים.
כמו כן יש לציין כי עבור החומר המסובך ביותר (כגון רקמות קשות ו / או מגושם), שום דבר לא מונע את השימוש בייצוב פורמלדהיד מיד עם הפרעה לתא הומוגניזציה חומרית. גישה זו כבר משמשת לעתים קרובות כדי להסיר את עיכוב הכניסה לתא בעת ייצוב מתחמי תרגום עם מעכבי מולקולה קטנה ספציפית33,53,54,55. בהתחשב בכך קיבוע פורמלדהיד שימש באופן מסורתי עם תוצאות מצוינות עבור ייצוב מדגם ex vivo / in vitro ביישומים כגון מיקרוסקופיה אלקטרונית45,56,57,58, אנו יכולים לצפות אפילו פחות השפעות שליליות במקרה זה, במיוחד אלה הקשורים להפקה לקויה של מתחמי התרגום מהתאים הקבועים ביסודיות.
הממצאים שלנו מאשרים את השימושיות של קיבוע פורמלדהיד מהיר לייצב מתחמים ארעיים מאוד, כגון אלה הכוללים eIF4A. ראוי לציין כי בניגוד ליונקים, שמרים eIF4A קשורה הרבה יותר חלש עם מתחם כריכת המכסה eIF4F, וכתוצאה מכך, מתחמים תרגומיים בכלל. eIF4A הולך לאיבוד בדרך כלל במהלך כל טיהור נרחב של החומר ריבוזומלי בשמרים29,59,60,61,62,63. עם זאת, בחומר שמרים קבוע in vivo,ניתן להשיג העשרה אמינה של eIF4A בכל שברי מתחמי התרגום שבהם נוכחותו הייתה צפויה. נתוני Sel-TCP-seq שפורסמו בעבר הדגימו את ההעשרה של eIF2 ו- eIF3 המקשרים ביתר שאת לריבוזומים (אך גם חשפו הרכבה מורכבת מורכבת של חלבונים תרגומיים משותפים)39. לפיכך, השיטה מתאימה לאיתור שניהם, מרכיבים מחוברים חזקים וחלשים יותר של מתחמי התרגום.
לסיכום, הצגנו גישה שימושית כדי לקבל תובנות בעיקר על השינויים המתרחשים בשלב החניכה של התרגום וכאשר נדרשת התפלגות ריבוזומלית מינימלית על ה- mRNA. חשוב לציין, הגישה מתאימה לייצוב של רכיבים ערמומיים ודינמיים יחסית של מתחמי תרגום, כגון eIF4A, וניתן להשתמש בה באופן נרחב בכפוף לאופטימיזציות הדרושות. סיפקנו גם ראיות לתועלת של קיבעון פורמלדהיד בתרחישים של שינוי דינמי מהיר של תרגום, פתיחת תחומי חקירה כגון תגובות תאיות בקצב מהיר לשינויים סביבתיים או תנאי לחץ.
Disclosures
המחברים אינם מצהירים על ניגודי עניינים.
Acknowledgements
עבודה זו נתמכה על ידי מענק פרויקט דיסקברי של מועצת המחקר האוסטרלית (DP180100111 ל- T.P. ו- N.E.S), מענק החוקר הלאומי לבריאות ומחקר רפואי (GNT1175388 ל- N.E.S) ומלגת מחקר (APP1135928 ל- T.P.). המחברים מכירים במתקני מיקרוסקופיה אוסטרליה במרכז למיקרוסקופיה מתקדמת, האוניברסיטה הלאומית האוסטרלית, מתקן הממומן על ידי האוניברסיטה והממשלה הפדרלית.
Materials
| Name | Company | Catalog Number | Comments |
| Yeast extract | Merck, Sigma-Aldrich | 70161 | |
| Peptone | Merck, Sigma-Aldrich | 70178 | |
| D-Glucose (Dextrose) | Merck, Sigma-Aldrich | 49139 | |
| Adenine sulphate | Amresco | 0607-50G | |
| Formaldehyde solution | Merck Sigma-Aldrich | F11635-500ML | ACS reagent, 37 wt. % in H2O, contains 10-15% Methanol as stabiliser (to prevent polymerisation) |
| RNaseOUT™ Recombinant Ribonuclease Inhibitor | Invitrogen™ byThermo Fischer Scientific | 10777019 | |
| cOmplete™, EDTA-free Protease Inhibitor Cocktail | COEDTAF-RO Roche by Merck | 11873580001 | |
| Magnesium chloride solution | (Merck/Sigma-Aldrich) | M1028 | |
| Ethylenediaminetetraacetic acid solution | (Merck/Sigma-Aldrich) | E7889 | |
| Ambion™ RNase I, cloned, 100 U/µL | Ambion | AM2294 | |
| SUPERase•In™ RNase Inhibitor (20 U/μL) | Invitrogen™ by Thermo Fisher Scientific | AM2694 | |
| Acidic phenol:chlorophorm:isoamyl alcohol 125:24:1 (pH 4.0-5.0) | (Merck/Sigma-Aldrich) | P1944-100ML | |
| Dynabeads™ Goat Anti-Mouse IgG | Invitrogen™ by Thermo Fisher Scientific) | 11033 | |
| Sodium Acetate (3 M), pH 5.5 | Invitrogen™ by Thermo Fisher Scientific) | AM9740 | |
| Glycogen (5 mg/ml) | Invitrogen™ by Thermo Fisher Scientific) | AM9510 | |
| Ethyl alcohol, Pure | Merck; Sigma Aldrich | E7023 | |
| Amersham™ Hybond® P Western blotting membranes, PVDF | Merck | GE10600023 | PVDF membrane for western blotting |
| Bolt™ 4 to 12%, Bis-Tris, 1.0 mm, Mini Protein Gel | Invitrogen™ by ThermoFischer Sientific | NW04120BOX | Protein gel |
| 4X Bolt™ LDS Sample Buffer | Invitrogen™ by ThermoFischer Sientific | B0007 | LDS sample loading buffer |
| Precision Plus Protein™ Kaleidoscope™ Prestained Protein Standards | BioRad | 1610375 | Protein ladder |
| 20X Bolt™ MES SDS Running Buffer | ThermoFischer Scientific | B0002 | PAGE runninjg buffer |
| Intercept® (PBS) Blocking Buffer | LI-COR | 927-70001 | Odyssey Blcoking buffer (PBS) |
| IRDye® 800CW Goat anti-Mouse IgG Secondary Antibody | LI-COR | 92632210 | |
| IRDye® 800CW Goat anti-Rabbit IgG Secondary Antibody | LI-COR | 92632211 | |
| TAP Tag Polyclonal Antibody | Invitrogen™ by ThermoFischer Sientific | CAB1001 | |
| Anti-beta Actin antibody | Abcam | ab8227 | |
| Sucrose | (Merck/Sigma-Aldrich) | 84097 | BioUltra, for molecular biology, ≥99.5% (HPLC) |
| DL-Dithiothreitol solution | (Merck/Sigma-Aldrich) | 43816 | BioUltra, for molecular biology, ~1 M in H2O |
| Terumo Syringe 1CC/mL | Terumo Syringe | 878499 | |
| Potassium chloride | (Merck/Sigma-Aldrich) | 60128 | |
| HEPES | (Merck/Sigma-Aldrich) | H3375 | |
| Dulbecco's Modified Eagle's Medium - high glucose | Sigma Aldrich | D5796 | |
| Fetal Bovine Serum | Sigma Aldrich | 12003C | |
| Trypsin-EDTA (0.05%), phenol red | Gibco | 25300062 | |
| Dulbecco's Phosphate Buffered Saline with Calcium and magnesium | Sigma-Aldrich | D8662 | |
| Glycine | Sigma-Aldrich | G7126 | |
| Tris hydrochloride | Merck/Sigma-Aldrich | 10812846001 | |
| Sodium dodecyl sulfate | Merck/Sigma-Aldrich | 436143 | |
| IGEPAL CA-630 | Merck/Sigma-Aldrich | I3021 | |
| Rnasin Ribonuclease Inhibitor | Promega | N2111 | |
| Stainless steel grinding jar | Retsch | 02.462.0059 | |
| MM400 mixer mill | Retsch | 20.745.0001 | |
| Gradient Fractionator | Brandel | BRN-BR-188 | |
| Thermomixer R | Eppendorf | Z605271 | |
| Nanodrop spectrophotometer | Thermo Fisher Scientific | ND-2000 | |
| 0.5-ml microcentrifuge tubes with locking devices | Eppendorf Safe-Lock | 30121023 | |
| Mini Gel Tank | (Thermo Fisher Scientific) | A25977 | PAGE running tank |
| 5 mL, Open-Top Thinwall Ultra-Clear Tube, 13 x 51mm | Beckman-Coulter | 344057 | |
| 13.2 mL, Certified Free Open-Top Thinwall Polypropylene, 14 x 89mm - 50Pk | Beckman-Coulter | 331372 | |
| Amicon Ultra-0.5 ultrafiltration devices | Merck | UFC5030 | Ultracel-30 regenerated cellulose membrane, 0.5 mL sample volume |
| Thermo Sorvall Evolution RC Floor Super Speed Centrifuge | Cambridge Scientific | 15566 | |
| Beckman Coulter Optima L-90K | GMI | 8043-30-1191 | |
| Nunc EasYFlask 175cm2 | Thermofisher Scientific | 159910 | |
| Falcon 50 mL Conical Centrifuge Tubes | Thermofisher Scientific | 14-432-22 | |
| 25 mL Serological Pipette | Sigma-Aldrich | SIAL1250 | |
| 10 mL Serological Pipette | Sigma-Aldrich | SIAL1100 | |
| DNA lobind tubes | Eppendorf | 30108051 | |
| Cold Centrifuge 5810 R | Eppendorf | EP022628188 | for 50 mL tubes |
| Orbital Shaking Incubator | Ratek | OM11 | |
| Frezco 17 Microcentrifuge | Thermofisher Scientific | 75002402 | |
| Eppendorf DNA lo-bind tubes | Merck/Sigma-Aldrich | EP0030108051 | |
| Eppendorf® Protein LoBind tubes | Merck/Sigma-Aldrich | EP0030108116 | |
| SW 41 Ti Swinging bucket rotor | Beckman-Coulter | 331362 | |
| Heracell™ 150i CO2 Incubator, 150 L | Thermofisher Scientific | 51026282 | |
| 0,3 mL ultra-fine II short insulin syringe | BD Medical | 328822 | |
| 3 mL syringe with Luer Lok tip | BD Medical | 302113 | |
| 25 G x 16 mm Hypodermic Needle | Terumo | TUAN2516R1 |
References
- Janapala, Y., Preiss, T., Shirokikh, N. E. Control of translation at the initiation phase during glucose starvation in yeast. International Journal of Molecular Sciences. 20 (16), 4043 (2019).
- Masvidal, L., Hulea, L., Furic, L., Topisirovic, I., Larsson, O. mTOR-sensitive translation: Cleared fog reveals more trees. RNA Biology. 14 (10), 1299-1305 (2017).
- Ashe, M. P., De Long, S. K., Sachs, A. B. Glucose depletion rapidly inhibits translation initiation in yeast. Molecular Biology of the Cell. 11 (3), 833-848 (2000).
- Crawford, R. A., Pavitt, G. D. Translational regulation in response to stress in Saccharomyces cerevisiae. Yeast. 36 (1), 5-21 (2019).
- Melamed, D., Pnueli, L., Arava, Y. Yeast translational response to high salinity: global analysis reveals regulation at multiple levels. RNA. 14 (7), 1337-1351 (2008).
- Hershey, J. W., Sonenberg, N., Mathews, M. B. Principles of translational control: An overview. Cold Spring Harbor Perspectives in Biology. 4 (12), 011528 (2012).
- Mata, J., Marguerat, S., Bähler, J. Post-transcriptional control of gene expression: a genome-wide perspective. Trends in Biochemical Sciences. 30 (9), 506-514 (2005).
- Spriggs, K. A., Bushell, M., Willis, A. E. Translational regulation of gene expression during conditions of cell stress. Molecular Cell. 40 (2), 228-237 (2010).
- Liu, B., Qian, S. B. Translational reprogramming in cellular stress response. Wiley Interdisciplinary Reviews RNA. 5 (3), 301-315 (2014).
- Archer, S. K., Shirokikh, N. E., Beilharz, T. H., Preiss, T. Dynamics of ribosome scanning and recycling revealed by translation complex profiling. Nature. 535 (7613), 570-574 (2016).
- Hinnebusch, A. G., Ivanov, I. P., Sonenberg, N. Translational control by 5'-untranslated regions of eukaryotic mRNAs. Science. 352 (6292), 1413-1416 (2016).
- Dever, T. E., Green, R. The elongation, termination, and recycling phases of translation in eukaryotes. Cold Spring Harbor Perspectives in Biology. 4 (7), 013706 (2012).
- Shirokikh, N. E., Preiss, T. Translation initiation by cap-dependent ribosome recruitment: Recent insights and open questions. Wiley Interdisciplinary Reviews RNA. 9 (4), 1473 (2018).
- Jiménez-Díaz, A., Remacha, M., Ballesta, J. P., Berlanga, J. J. Phosphorylation of initiation factor eIF2 in response to stress conditions is mediated by acidic ribosomal P1/P2 proteins in Saccharomyces cerevisiae. PLoS One. 8 (12), 84219 (2013).
- Sonenberg, N., Hinnebusch, A. G. Regulation of translation initiation in eukaryotes: mechanisms and biological targets. Cell. 136 (4), 731-745 (2009).
- Majmundar, A. J., Wong, W. J., Simon, M. C. Hypoxia-inducible factors and the response to hypoxic stress. Molecular Cell. 40 (2), 294-309 (2010).
- Barraza, C. E., et al. The role of PKA in the translational response to heat stress in Saccharomyces cerevisiae. PLoS One. 12 (10), 0185416 (2017).
- Richter, K., Haslbeck, M., Buchner, J. The heat shock response: Life on the verge of death. Molecular Cell. 40 (2), 253-266 (2010).
- Jamar, N. H., Kritsiligkou, P., Grant, C. M. The non-stop decay mRNA surveillance pathway is required for oxidative stress tolerance. Nucleic Acids Research. 45 (11), 6881-6893 (2017).
- Chen, Z., et al. The complete pathway for thiosulfate utilization in Saccharomyces cerevisiae. Applied and Environmental Microbiology. 84 (22), (2018).
- Marzluf, G. A. Molecular genetics of sulfur assimilation in filamentous fungi and yeast. Annual Review of Microbiology. 51, 73-96 (1997).
- Miller, D., Brandt, N., Gresham, D. Systematic identification of factors mediating accelerated mRNA degradation in response to changes in environmental nitrogen. PLoS Genetics. 14 (5), 1007406 (2018).
- Zhang, W., Du, G., Zhou, J., Chen, J. Regulation of sensing, transportation, and catabolism of nitrogen sources in Saccharomyces cerevisiae. Microbiology and Molecular Biology Reviews. 82 (1), (2018).
- Tokpohozin, S. E., Fischer, S., Becker, T. Selection of a new Saccharomyces yeast to enhance relevant sorghum beer aroma components, higher alcohols, and esters. Food Microbiology. 83, 181-186 (2019).
- Walker, G. M., Stewart, G. G. Saccharomyces cerevisiae in the production of fermented beverages. Beverages. 2 (4), 30 (2016).
- Chassé, H., Boulben, S., Costache, V., Cormier, P., Morales, J. Analysis of translation using polysome profiling. Nucleic Acids Research. 45 (3), 15 (2017).
- Jin, H. Y., Xiao, C. An integrated polysome profiling and ribosome profiling method to investigate in vivo translatome. Methods in Molecular Biology. 1712, 1-18 (2018).
- Arava, Y., et al. Genome-wide analysis of mRNA translation profiles in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences of the United States of America. 100 (7), 3889-3894 (2003).
- Lackner, D. H., et al. A network of multiple regulatory layers shapes gene expression in fission yeast. Molecular Cell. 26 (1), 145-155 (2007).
- Ingolia, N. T., Ghaemmaghami, S., Newman, J. R. S., Weissman, J. S. Genome-Wide Analysis in Vivo of Translation with Nucleotide Resolution Using Ribosome Profiling. Science. 324 (5924), 218-223 (2009).
- Ingolia, N. T., Hussmann, J. A., Weissman, J. S. Ribosome Profiling: Global Views of Translation. Cold Spring Harbor Perspectives in Biology. 11 (5), (2019).
- Gerashchenko, M. V., Lobanov, A. V., Gladyshev, V. N. Genome-wide ribosome profiling reveals complex translational regulation in response to oxidative stress. Proceedings of the National Academy of Sciences of the United States of America. 109 (43), 17394-17399 (2012).
- Hussmann, J. A., Patchett, S., Johnson, A., Sawyer, S., Press, W. H. Understanding biases in ribosome profiling experiments reveals signatures of translation dynamics in yeast. Proceedings of the National Academy of Sciences Genetics. 11 (12), 1005732 (2015).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Hoffman, E. A., Frey, B. L., Smith, L. M., Auble, D. T. Formaldehyde crosslinking: A tool for the study of chromatin complexes. Journal of Biological Chemistry. 290 (44), 26404-26411 (2015).
- Kage, U., Powell, J. J., Gardiner, D. M., Kazan, K. Ribosome profiling in plants: What is not lost in translation. Journal of Experimental Botany. 71 (18), 5323-5332 (2020).
- Shirokikh, N. E., Archer, S. K., Beilharz, T. H., Powell, D., Preiss, T. Translation complex profile sequencing to study the in vivo dynamics of mRNA-ribosome interactions during translation initiation, elongation and termination. Nature Protocols. 12 (4), 697-731 (2017).
- Wagner, S., et al. Selective translation complex profiling reveals staged initiation and co-translational assembly of initiation factor complexes. Molecular Cell. 79 (4), 546-560 (2020).
- Zlotorynski, E. Profiling ribosome dynamics. Nature Reviews Molecular Cell Biology. 17 (9), 535-535 (2016).
- Sen, N. D., Gupta, N., S, K. A., Preiss, T., Lorsch, J. R., Hinnebusch, A. G. Functional interplay between DEAD-box RNA helicases Ded1 and Dbp1 in preinitiation complex attachment and scanning on structured mRNAs in vivo. Nucleic Acids Research. 47 (16), 8785-8806 (2019).
- Zhao, J., Qin, B., Nikolay, R., Spahn, C. M. T., Zhang, G. Translatomics: The global view of translation. International Journal of Molecular Sciences. 20 (1), 20010212 (2019).
- Luthe, D. S. A simple technique for the preparation and storage of sucrose gradients. Analytical Biochemistry. 135 (1), 230-232 (1983).
- Wang, Z., Gerstein, M., Snyder, M. RNA-Seq: A revolutionary tool for transcriptomics. Nature Review Genetics. 10 (1), 57-63 (2009).
- Orlando, V. Mapping chromosomal proteins in vivo by formaldehyde-crosslinked-chromatin immunoprecipitation. Trends in Biochemical Sciences. 25 (3), 99-104 (2000).
- Schmiedeberg, L., Skene, P., Deaton, A., Bird, A. A Temporal Threshold for Formaldehyde Crosslinking and Fixation. PLoS One. 4 (2), 4636 (2009).
- Solomon, M. J., Varshavsky, A. Formaldehyde-mediated DNA-protein crosslinking: A probe for in vivo chromatin structures. Proceedings of the National Academy of Sciences. 82 (19), 6470-6474 (1985).
- Solomon, M. J., Larsen, P. L., Varshavsky, A. Mapping proteinDNA interactions in vivo with formaldehyde: Evidence that histone H4 is retained on a highly transcribed gene. Cell. 53 (6), 937-947 (1988).
- Bohlen, J., Fenzl, K., Kramer, G., Bukau, B., Teleman, A. A. Selective 40S footprinting reveals cap-tethered ribosome scanning in human cells. Molecular Cell. 79 (4), 561-574 (2020).
- Shirokikh, N. E. Translation complex stabilization on messenger RNA and footprint profiling to study the RNA responses and dynamics of protein biosynthesis in the cells. Critical Reviews in Biochemistry and Molecular Biology. , (2021).
- Giess, A., et al. Profiling of small ribosomal subunits reveals modes and regulation of translation initiation. Cell Reports. 31 (3), 107534 (2020).
- Firmino, A. A. P., et al. Separation and paired proteome profiling of plant chloroplast and cytoplasmic ribosomes. Plants (Basel). 9 (7), (2020).
- Gerashchenko, M. V., Gladyshev, V. N. Translation inhibitors cause abnormalities in ribosome profiling experiments. Nucleic Acids Research. 42 (17), 134 (2014).
- Santos, D. A., Shi, L., Tu, B. P., Weissman, J. S. Cycloheximide can distort measurements of mRNA levels and translation efficiency. Nucleic Acids Research. 47 (10), 4974-4985 (2019).
- Schneider-Poetsch, T., et al. Inhibition of eukaryotic translation elongation by cycloheximide and lactimidomycin. Nature Chemical Biology. 6 (3), 209-217 (2010).
- Plénat, F., et al. Formaldehyde fixation in the third millennium. Annales De Pathologie. 21 (1), 29-47 (2001).
- Salic, A., Mitchison, T. J. A chemical method for fast and sensitive detection of DNA synthesis in vivo. Proceedings of the National Academy of Sciences. 105 (7), 2415-2420 (2008).
- Wang, N. S., Minassian, H. The formaldehyde-fixed and paraffin-embedded tissues for diagnostic transmission electron microscopy: A retrospective and prospective study. Human Pathology. 18 (7), 715-727 (1987).
- Grifo, J. A., et al. Characterization of eukaryotic initiation factor 4A, a protein involved in ATP-dependent binding of globin mRNA. Journal of Biological Chemistry. 257 (9), 5246-5252 (1982).
- Li, Y. Commonly used tag combinations for tandem affinity purification. Biotechnology and Applied Biochemistry. 55 (2), 73-83 (2010).
- Blum, S., et al. ATP hydrolysis by initiation factor 4A is required for translation initiation in Saccharomyces cerevisiae. Proceedings of the National Academy of Sciences. 89 (16), 7664-7668 (1992).
- Merrick, W. C. eIF4F: A Retrospective. Journal of Biological Chemistry. 290 (40), 24091-24099 (2015).
- Rogers, G. W., Komar, A. A., Merrick, W. C. eIF4A: The godfather of the DEAD box helicases. Progress in Nucleic Acid Research and Molecular Biology. 72, 307-331 (2002).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved