A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
אופטימיזציה של טכנולוגיית עיבוד עבור Tiebangchui עם Zanba מבוסס על CRITIC בשילוב עם שיטת Box-Behnken Response Surface
In This Article
Summary
הפרוטוקול הנוכחי מתאר שיטת עיבוד יעילה וסטנדרטית לניקוי רעלים עבור טיבנגצ'וי מוקפץ זנבה באמצעות CRITIC בשילוב עם שיטת משטח התגובה Box-Behnken.
Abstract
השורש המיובש של מטוטלת Aconitum Busch., המכונה Tiebangchui (TBC) בסינית, הוא אחת התרופות הטיבטיות המפורסמות ביותר. זהו צמח נפוץ בצפון מערב סין. עם זאת, מקרים רבים של הרעלה התרחשו בגלל הרעילות האינטנסיבית של TBC ובגלל שהמינונים הטיפוליים והרעילים שלה דומים. לכן, מציאת שיטה בטוחה ויעילה כדי להפחית את הרעילות שלה היא משימה דחופה. חיפוש בקלאסיקות הרפואה הטיבטית מראה כי שיטת העיבוד של הקפצה של TBC עם זנבה נרשמה ב"מפרט עיבוד של הרפואה הטיבטית של מחוז צ'ינגהאי (2010)". עם זאת, פרמטרי העיבוד הספציפיים עדיין אינם ברורים. לפיכך, מחקר זה נועד לייעל ולתקנן את טכנולוגיית העיבוד של TBC מוקפץ זנבה.
ראשית, נערך ניסוי חד-גורמי על ארבעה גורמים: עובי הפרוסה של TBC, כמות זנבה, טמפרטורת עיבוד וזמן. עם תכולת אלקלואיד מונואסטר ודיסטר ב-TBC מוקפץ-זנבה כאינדקסים, נעשה שימוש ב-CRITIC בשילוב עם שיטת משטח התגובה Box-Behnken כדי לייעל את טכנולוגיית העיבוד של TBC מוקפץ זנבה. תנאי העיבוד האופטימליים של TBC מוקפץ זנבה היו עובי פרוסת TBC של 2 ס"מ, פי שלושה יותר זנבה מאשר TBC, טמפרטורת עיבוד של 125 מעלות צלזיוס ו-60 דקות של טיגון מוקפץ. מחקר זה קבע את תנאי העיבוד האופטימליים והסטנדרטיים לשימוש ב-TBC מוקפץ זנבה, ובכך סיפק בסיס ניסיוני לשימוש קליני בטוח ולייצור תעשייתי של TBC מוקפץ זנבה.
Introduction
השורש המיובש של מטוטלת Aconitum Busch ו- A. flavum Hand.-Mazz., אחת התרופות הטיבטיות המפורסמות ביותר, נקרא Tiebangchui (TBC) בסינית 1,2. השורשים המיובשים של TBC עוזרים להפיג קור ורוח, להפחית כאב ולהרגיע זעזועים. הוא נרשם בכרך הראשון של "תקני תרופות (רפואה טיבטית) של משרד הבריאות של הרפובליקה העממית של סין", הקובע כי השורשים המיובשים של TBC משמשים בדרך כלל לטיפול בדלקת מפרקים שגרונית, חבורות ומחלות הצטננות אחרות3. עם זאת, המינון הטיפולי הקליני של TBC דומה למינון הרעיל שלו, ומקרים של הרעלה או מוות דווחו לעתים קרובות עקב שימוש לא נכון4. לכן, הפחתת הרעילות ושימור היעילות של TBC הפכו עם השנים למוקד מחקרי.
ברפואה הטיבטית, עיבוד הוא אחת השיטות היעילות ביותר להחלשת הרעילות של TBC. על פי "מפרט עיבוד של הרפואה הטיבטית של מחוז צ'ינגהאי (2010)", יש להניח את עשבי התיבול המקוריים (TBC) בסיר ברזל ולהקפיץ עם זנבה עד שהזנבה הופכת צהובה, ולאחר מכן זנבה מוסרת ועשבי התיבול מיובשים באוויר 5,6. עם זאת, לא תועדו פרמטרים ספציפיים של תהליך, מה שמקשה על השליטה בטכנולוגיית העיבוד ובאיכות ה-TBC המוקפץ של זנבה. שיטת CRITIC היא שיטת משקל אובייקטיבית שיכולה למנוע ערפול וסובייקטיביות, ולהגביר את האובייקטיביות של שקילה7. שיטת משטח התגובה Box-Behnken יכולה לשקף ישירות את האינטראקציה בין כל גורם באמצעות התאמת פולינום8. השילוב של משטח התגובה Box-Behnken ושיטת CRITIC משמש בדרך כלל לאופטימיזציה של טכנולוגיית העיבוד כדי לרכוש את פרוטוקול העיבוד הממוטב 9,10. במאמר זה, אלקלואיד מונואסטר-דיטרפנואיד (MDA) (בנזואילקוניטין) ושני אלקלואידים דיאסטר-דיטרפנואידים (DDAs) (אקוניטין, 3-דאוקסיאקוניטין) שימשו כמדדי הערכה. CRITIC בשילוב עם שיטת משטח התגובה Box-Behnken יושמה כדי לייעל את טכנולוגיית העיבוד של TBC מוקפץ זנבה ולבסס שיטת עיבוד סטנדרטית לשימוש קליני בטוח.
Protocol
שיטת עיבוד TBC מוקפצת זנבה עברה אופטימיזציה ותקינה על ידי CRITIC בשילוב עם שיטת משטח התגובה Box-Behnken. Benzoylaconitine, aconitine, ו 3-deoxyaconitine שימשו כמדדי הערכה במהלך הליך זה.
1. הכנת פתרון לדוגמה
- הכן את תמיסת מלאי חומרי הייחוס. לשקול בדיוק 9.94 מ"ג של benzoylaconitine, 8.49 מ"ג של aconitine, ו 6.25 מ"ג של 3-deoxyaconitine (טבלה של חומרים) על איזון אנליטי אלקטרוני ומניחים אותם בתוך בקבוק נפח 10 מ"ל. לאחר מכן, להוסיף 0.05% חומצה הידרוכלורית מתנול פתרון להמיס את המוצקים לפצות את נפח ל 10 מ"ל. לבסוף, נערו היטב את התערובת כדי לקבל את תמיסת מלאי חומרי הייחוס עם ריכוזי מסה של 0.9940 מ"ג / מ"ל בנזואילקוניטין, 0.8490 מ"ג / מ"ל אקוניטין, ו 0.6250 מ"ג / מ"ל של 3-deoxyaconitine.
זהירות: חומצה הידרוכלורית היא חומר מאכל מאוד11. השתמשו בהגנה מתאימה, כגון כפפות, מעיל מעבדה, משקפי מגן ומכסה אדים. - הכן את הפתרון לדוגמה לבדיקה.
- שוקלים 2 גרם אבקת TBC מוקפצת זנבה בצלוחית חרוטית.
- מכינים TBC מוקפץ זנבה במשקל 30 גרם TBC (2 ס"מ) ו-90 גרם זנבה ומוסיפים אותם למכונה המוקפצת שחוממה מראש. הגדר את הזמן והטמפרטורה של מכונת הטיגון המוקפץ ל - 40 דקות ו - 140 מעלות צלזיוס, בהתאמה. הגדר את ההתקן להשלמת העיבוד.
- השתמשו במכונת ריסוק מהירה כדי לטחון את ה-TBC המוקפץ של זנבה בנפרד לדגימות אבקה שיכולות לעבור דרך מסננת של 50 רשת (0.355 מ"מ).
- הוסף 3 מ"ל של תמיסת אמוניה ו 50 מ"ל של תמיסה מעורבת של אלכוהול איזופרופיל ואתיל אצטט (יחס של 1: 1 v/v) לתוך הצלוחית החרוטית לעיל, בהתבסס על מחקרים קודמים12,13.
הערה: להכנת תמיסת האמוניה, יש להוסיף 40 מ"ל של תמיסת אמוניה מרוכזת לבקבוק נפחי של 100 מ"ל ולמלא במים מטוהרים לקו המדידה. נקוט אמצעי הגנה מתאימים בעת שימוש בתמיסת אמוניה מרוכזת מכיוון שיש לה ריח חזק. - לשקול את הדגימה לעיל ואת בקבוק חרוטי ולרשום את המשקל. Ultrasonicate במשך 30 דקות (מתח: 220 V, תדר: 40 kHz).
הערה: אלקלואידים Aconitine מתפרקים בקלות על ידי חום. לכן, הטמפרטורה של מיצוי קולי חייב להיות מתחת 25 °C (75 °F). - שוקלים את הדגימה ואת בקבוק חרוטי לאחר מיצוי קולי.
- לפצות על המשקל האבוד על ידי הוספת תערובת של אלכוהול איזופרופיל ואתיל אצטט (יחס של 1: 1 v/v).
- סנן את הפתרון לדוגמה. יש לאדות 25 מ"ל מהתסנין ליובש באמצעות מאייד סיבובי בטמפרטורה של 40°C.
- להמיס את השאריות על ידי הוספת 5 מ"ל של תמיסת מתנול 0.05% חומצה הידרוכלורית, לסנן את התמיסה דרך מסנן מזרק 0.2 מיקרומטר, ולנתח אותו על ידי ביצוע כרומטוגרפיה נוזלית בעלת ביצועים גבוהים (HPLC).
- שוקלים 2 גרם אבקת TBC מוקפצת זנבה בצלוחית חרוטית.
- הכינו תמיסת ייחוס מעורבת המכילה 0.1988 מ"ג/מ"ל בנזואילקוניטין, 0.0509 מ"ג/מ"ל אקוניטין, ו-0.0938 מ"ג/מ"ל 3-דאוקסיאקוניטין.
הערה: כל תקן (0.9940 מ"ג בנזואילקוניטין, 0.2545 מ"ג אקוניטין, ו-0.4690 מ"ג 3-דאוקסיאקוניטין) מומס בבקבוק נפחי של 5 מ"ל במתנול חומצה הידרוכלורית 0.05% כמדיום המסה. - הכן חיץ אמוניום אצטט 0.04 M על ידי המסת 6.16 גרם של אמוניום אצטט (טבלה של חומרים) ב 2 L של מים טהורים במיוחד (שלב A נייד). התאם את ה- pH ל- 8.50 באמצעות אמוניה.
זהירות: אמוניה היא חומר מסוכן. השתמשו בהגנה מתאימה, כגון כפפות, מעיל מעבדה, משקפי מגן ומכסה אדים. - מסננים 2 ליטר של 100% אצטוניטריל אולטרה-טהור (שלב B נייד) ומנטרלים אותו.
זהירות: אצטוניטריל הוא חומר מסוכן13. השתמשו בהגנה מתאימה, כגון כפפות, מעיל מעבדה, משקפי מגן ומכסה אדים.
2. מצב כרומטוגרפי
- הזריקו 10 μL של תמיסות הדגימה שטופלו מראש למערכת HPLC עם משאבות בינאריות. השתמש במערכת HPLC המשתמשת בטור ODS-3 (5 מיקרומטר x 4.6 מ"מ x 250 מ"מ; עבודה ב- 30 ° C) עם שלבים ניידים A ו- B להפרדת מד"א ו- DDA. הזריקו כל דגימה שלוש פעמים לצורך שכפול טכני.
- תכנת את השיטה כפי שמוצג בטבלה 1 עבור העמודה ODS-3. הגדר קצב זרימה של 1.0 מ"ל/דקה ואת אורך גל הגילוי כ- 235 ננומטר.
- תעד את אזורי השיא של כל מתחם יעד.
הערה: פרטים על המכשירים ניתן למצוא בטבלת החומרים.
3. בדיקת הסתגלות המערכת
הערה: עיין בסעיף 2 לקבלת התנאים הכרומטוגרפיים לביצוע שלבים 3.1-3.5.
- לחקור את הקשר הליניארי בין הריכוז לאזור השיא.
- הכינו ריכוזים שונים - 19.88, 39.76, 59.64, 159.04, 198.80 ו- 497.00 מיקרוגרם/מ"ל - של תמיסת בנזואילקוניטין.
- הכינו ריכוזים שונים - 8.49, 16.98, 25.47, 33.96, 50.94 ו- 169.80 מק"ג/מ"ל - של תמיסת אקוניטין.
- הכינו ריכוזים שונים - 1.875, 12.50, 37.50, 62.50, 93.75 ו- 125.00 מיקרוגרם/מ"ל - של תמיסת 3-דאוקסיאקוניטין.
- הזריקו את תמיסות הייחוס הנ"ל מריכוז מסה נמוך לריכוז מסה גבוה ותיעדו את אזורי השיא.
- קבל שלוש משוואות רגרסיה ליניארית מתרשים ריכוז תמיסת הייחוס (μg/L) כנגד שטח השיא.
הערה: ודא שהריכוזים של בנזואילקוניטין, אקוניטין, ו- 3-deoxyaconitine נמצאים בטווח הליניארי של עקומה סטנדרטית זו.
- בצע בדיקות מדויקות על ידי הזרקה רציפה של שש חזרות של 10 μL של תמיסת הדגימה למערכת HPLC והפעל את הדגימות תחת אותם תנאי HPLC המתוארים בסעיף 2. רשום את אזורי השיא של בנזואילאקוניטין, אקוניטין, ו 3-deoxyaconitine.
- בצע ניסויים בבדיקת יציבות על ידי הזרקת 10 μL של תמיסת הדגימה שהוכנה וקבע את אזורי השיא לאחר 0 שעות, 2 שעות, 4 שעות, 8 שעות, 12 שעות ו- 24 שעות.
הערה: אזורי השיא נרשמים באופן אוטומטי על-ידי מערכת HPLC שאליה מתבצעת הפניה. נקודות זמן אלה התבססו על ספרות רלוונטית15,16,17. - בצע את בדיקת השחזור על ידי לקיחת אותה אצווה של TBC מוקפץ זנבה כדי להכין שש תמיסות מדגם בדיקה במקביל בהתאם לשיטה בשלב 1.2. הזריקו 10 μL מכל דגימה למערכת HPLC והפעילו את הדגימות כמתואר בסעיף 2.
הערה: יכולת השחזור הוערכה על ידי השוואת הבדלי הריכוז בין שש הדגימות. - בצע את ניסוי השחזור על ידי הכנת שש מנות של אותה אצווה של TBC מוקפץ זנבה עבור פתרון הבדיקה. לאחר מכן, הוסף ~ 100% מחומר הייחוס של כל רכיב מדד לשישה חלקים של פתרון הבדיקה כדי לחשב את שיעור ההתאוששות. הזריקו דגימות אלה (10 μL) למערכת HPLC באותם תנאים המתוארים בסעיף 2 וחשבו את קצב ההחלמה באמצעות משוואה (1):
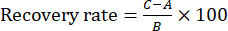 (1)
(1)
הערה: ב-Eq. (1), A הוא כמות הרכיב שיש למדוד בתמיסת הבדיקה, B הוא כמות חומר הייחוס שנוספה ו-C הוא הערך הנמדד של התמיסה המכילה את חומר הייחוס ואת דגימת TBC המוקפצת של זנבה.
4. ניסויים בגורם יחיד
- השוואה בין עובי הפרוסה
- הכינו חמש קבוצות לבדיקות, כל אחת עם 30 גרם TBC, כאשר עובי ה-TBC הוא 0.5, 1, 2, 3 ו-4 ס"מ, בהתאמה. שוקלים כמות זנבה שהיא פי שלושה מזו של TBC (90 גרם).
הערה: TBC רעיל. השתמשו בהגנה מתאימה, כגון כפפות, מעיל מעבדה, משקפי מגן ומכסה אדים, והיזהרו בתהליך החיתוך. באמצעות הניסוי המקדים נמצא כי כמות גדולה פי שלושה של זנבה נדרשה למגע מלא בין TBC לזנבה. לכן, בתכנון הניסוי הפורמלי, המחקר בחר פי שלושה מכמות הזנבה כאשר בחן את עובי הפרוסה. - כוונו את הטמפרטורה ואת הזמן של מכונת ההקפצה האוטומטית ל-140 °C ול-40 דקות, בהתאמה.
- הוסף ~ 30 גרם TBC ו 90 גרם זנבה למכונה לאחר שמכונת המוקפץ האוטומטית התחממה לטמפרטורה שנקבעה.
- הכן את הפתרונות לדוגמה על-ידי ביצוע שלב 1.2. חישוב תכולת מד"א ומד"א במוצרי עיבוד שונים בהתאם לעקומת התקן (טבלה 2). חשב את הציון המקיף בהתבסס על התוצאות באמצעות שיטת CRITIC בסעיף 6.
- בדרך זו, להשוות את כמויות זנבה, כמו גם טמפרטורות עיבוד וזמנים לאופטימיזציה של התנאים.
- הכינו חמש קבוצות לבדיקות, כל אחת עם 30 גרם TBC, כאשר עובי ה-TBC הוא 0.5, 1, 2, 3 ו-4 ס"מ, בהתאמה. שוקלים כמות זנבה שהיא פי שלושה מזו של TBC (90 גרם).
- השוואה בין כמות זנבה
- בצע חמש קבוצות של בדיקות, כל אחת עם 30 גרם TBC (2 ס"מ), כאשר כמות זנבה היא פי אחד, שניים, שלושה, ארבעה וחמישה מאשר TBC, בהתאמה.
- הפעל את מכונת ההקפצה לעיבוד. כוונו את השעה והטמפרטורה של מכונת הטיגון המוקפץ ל-40 דקות ו-140°C.
- הכן את הפתרונות לדוגמה על-ידי ביצוע שלב 1.2. חישוב תכולת מד"א ו-DDAs במוצרי עיבוד שונים בהתאם לעקומת התקן (טבלה 2). חשב את הציון המקיף בהתבסס על התוצאות באמצעות שיטת CRITIC בסעיף 6.
- השוואה בין טמפרטורת העיבוד
- בצע חמש קבוצות של בדיקות, כל אחת עם 30 גרם TBC (2 ס"מ) ו 90 גרם של זנבה.
- הפעל את מכונת ההקפצה לעיבוד. הגדר את טמפרטורת העיבוד ל- 100°C, 120°C, 140°C, 160°C ו- 180°C. הגדר את זמן העיבוד כ- 40 דקות.
הערה: באמצעות ניסויים מקדימים, נמצא כי מהירות הצהבת זנבה נמוכה מאוד כאשר טמפרטורת העיבוד נמוכה מ- 100 מעלות צלזיוס, וזנבה קלה לצריבה ולהשחרה אם הטמפרטורה גבוהה מדי (מעל 180 מעלות צלזיוס). לכן, 100 °C ו 180 °C נקבעו להיות ערכי המינימום והמקסימום של הטמפרטורה במהלך העיבוד, בהתאמה. - הכן את הפתרונות לדוגמה על-ידי ביצוע שלב 1.2. תעד את אזורי השיא של מד"א ומד"א. חישוב תכולת מד"א ו-DDAs במוצרי עיבוד שונים בהתאם לעקומת התקן (טבלה 2). חשב את הציון המקיף בהתבסס על התוצאות באמצעות שיטת CRITIC בסעיף 6.
הערה: הניסוי כולל טמפרטורות גבוהות של 160 ° C ו 180 ° C. שימו לב לבטיחות במהלך הניסוי, על פי קוד הבטיחות של המעבדה.
- השוואה בין זמן עיבוד
- בצע חמש קבוצות של בדיקות, כל אחת עם 30 גרם TBC (2 ס"מ) ו 90 גרם של זנבה.
- הפעל את מכונת ההקפצה לעיבוד. הגדר את זמן העיבוד ל- 20, 40, 60, 80 ו- 100 דקות. הגדר את הטמפרטורה ל 140 °C.
- הכן את הפתרונות לדוגמה על-ידי ביצוע התיאור בשלב 1.2. תעד את אזורי השיא של מד"א ומד"א. חישוב איכות מד"א ו-DDAs במוצרי עיבוד שונים בהתאם לעקומת התקן (טבלה 2). חשב את הציון המקיף בהתבסס על התוצאות באמצעות שיטת CRITIC בסעיף 6.
5. אופטימיזציה של טכנולוגיית עיבוד של TBC מוקפץ זנבה באמצעות מתודולוגיית משטח תגובה (RSM)
- עיצוב משטח תגובה Box-Behnken
- קבע את טווח עובי הפרוסה (A, 1-3 ס"מ), כמות הזנבה (B, 2-4x), טמפרטורת העיבוד (C, 100-140 ° C) וזמן העיבוד (D, 40-80 דקות) על ידי ניסויים ראשוניים באמצעות בדיקות גורם יחיד (שלב 4.1-4.4).
הערה: הערכים המקודדים של ארבעה משתנים ורמתם מוצגים בטבלה 3. שלוש רמות של כל משתנה קודדו כ- -1, 0 ו- 1.
- קבע את טווח עובי הפרוסה (A, 1-3 ס"מ), כמות הזנבה (B, 2-4x), טמפרטורת העיבוד (C, 100-140 ° C) וזמן העיבוד (D, 40-80 דקות) על ידי ניסויים ראשוניים באמצעות בדיקות גורם יחיד (שלב 4.1-4.4).
- השתמש בתוכנה כדי ליצור את המטריצה ולנתח את מודלי משטח התגובה.
הערה: צילומי המסך עבור השימוש בתוכנה מוצגים בקובץ משלים 1.- השתמש בתכנון Box-Behnken בן שלושה שלבים וארבעה גורמים המורכב מ-24 ניסויים (כפי שנעשה במחקר זה), ומדוד חמישה עותקים משוכפלים (סדר הפעלה 1, 9, 14, 16 ו-25) כדי לחשב את סכום השגיאה הטהור של ריבועים (טבלה 4). הגדר את הציון הכולל (Y) כתגובה (שלבים 1-4, קובץ משלים 1).
- בדף הבית, לחץ על עיצוב חדש (שלב 1, קובץ משלים 1), ובחלונית השמאלית של דף העיצוב, לחץ על משטח תגובה | Box-Behnken ולהגדיר את הפרמטרים של ארבעת הגורמים בטבלה (שלב 2, קובץ משלים 1).
- לחץ על הבא (שלב 2, קובץ משלים 1), הגדר את שמות התגובות ולחץ על סיום (שלב 3, קובץ משלים 1).
- צור את עיצוב משטח התגובה באמצעות הפעולה לעיל (שלב 4, קובץ משלים 1).
- השתמש בתכנון Box-Behnken בן שלושה שלבים וארבעה גורמים המורכב מ-24 ניסויים (כפי שנעשה במחקר זה), ומדוד חמישה עותקים משוכפלים (סדר הפעלה 1, 9, 14, 16 ו-25) כדי לחשב את סכום השגיאה הטהור של ריבועים (טבלה 4). הגדר את הציון הכולל (Y) כתגובה (שלבים 1-4, קובץ משלים 1).
- השלם את הניסוי בהתבסס על 29 התרחישים המיועדים למשטח התגובה.
- הכן את הפתרונות לדוגמה על-ידי ביצוע שלב 1.2.
- תעד את אזורי השיא של מד"א ומד"א.
הערה: אזורי השיא נרשמים באופן אוטומטי על-ידי מערכת HPLC שאליה מתבצעת הפניה. - חישוב איכות מד"א ומד"א במוצרי העיבוד השונים.
- חשב את הציון המקיף בהתבסס על התוצאות באמצעות שיטת CRITIC בשלב 6.
הערה: השיטה הספציפית מודגמת בשלב 6. - הזן את הציון המקיף שהתקבל של 29 ניסויים למחשב ונתח אותו באמצעות התוכנה המוזכרת (שלב 5, קובץ משלים 1).
- לבצע את התיקוף הסטטיסטי של משוואות הפולינום וניתוחי משטחי התגובה המשורטטים בגרפים תלת-ממדיים באמצעות התוכנה (שלבים 6-8, קובץ משלים 1).
- בחלונית הניווט השמאלית , תחת ניתוח ( +), לחץ על Y ולאחר מכן לחץ על התחל ניתוח בחלון קביעת תצורה (שלב 6, קובץ משלים 1).
- לחץ על ANOVA בתפריט העליון והתבונן בטבלת התוצאות המציגה ניתוח שונות (שלב 7, קובץ משלים 1).
- בתפריט העליון, לחץ על Model Graphs ולאחר מכן על 3D Surface כדי לקבל את חלקות משטח התגובה המשקפות את ההשפעות של פרמטרי עיבוד על הציונים הסינתטיים (שלב 8, קובץ משלים 1).
- בצע את האימות של מודל משטח התגובה בשילוש בתנאים האופטימליים החזויים (שלב 9, קובץ משלים 1) כדי לאמת את יציבות טכנולוגיית העיבוד. בחלונית הניווט השמאלית , תחת אופטימיזציה, לחץ על מספרי לאחר מכן, בתפריט העליון, לחץ על פתרונות. שימו לב לתנאים האופטימליים החזויים.
6. הערכת מודל
הערה: שלב זה יבוצע לאחר השלמת כל ניסוי גורם יחיד או ניסוי משטח תגובה. לאחר השלמת כל ניסוי (למשל, השוואת עובי הפרוסה), נמדדת תכולת מד"א ומד"א בדגימות השונות לקבלת חמישה מערכי נתונים, לפי שלב 1.2 וסעיף 2. הנתונים מוצגים בטבלה משלימה S1.
- עיבוד חסר ממד של האינדקס
הערה: שלב זה ממיר את הערך הנמדד (Xij) לערך יחסי חסר ממד, כך שהערך של כל מדד יהיה באותה רמת כמות. פעולה זו יכולה להקל על ניתוח מקיף והשוואת אינדיקטורים ביחידות שונות או בסדרי גודל18. לצורך המחשה, נעשה שימוש בערכי עובי הפרוסה לצורך החישובים המוצגים להלן (טבלה משלימה S1).- לתקנן את התוכן של מד"א (להשיג yMDA; מד"א מתייחס לבנזואילקוניטין) באמצעות הנוסחה ב- Eq. (2).
הערה: המדד "i" מייצג אחד מארבעה גורמים, ועובי הפרוסה הוא הגורם הראשון שנחקר. לפיכך, הערך של i שווה ל- 1. המדד "j" מייצג כל רמה של גורמים; לפיכך, כאשר עובי הפרוסה הוא הרמה הראשונה (0.5 ס"מ), J שווה ל -1; כאשר עובי הפרוסה הוא הרמה החמישית (4 ס"מ), j שווה ל-5. תכולת מד"א (Xij) ב-TBC המעובד בעובי של 0.5, 1, 2, 3 ו-4 ס"מ הייתה 0.9693, 1.0876, 1.3940, 1.4185 ו-1.3614 מ"ג/גרם, בהתאמה. לפיכך, x j,max הוא 1.4185 ו- xj, min הוא 0.9693.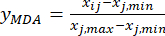 (2)
(2)
כך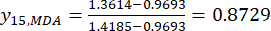
כאן, Xij הוא התוכן הנמדד של מד"א של הניסוי בפקטור i-th וברמה j-th; xj, min הוא התוכן המינימלי של מד"א בקבוצת ניסויים זו; ו- xj, max הוא התוכן המרבי של מד"א בקבוצת ניסויים זו. לפיכך, i = 1, 2, ..., m ו - j = 1, 2, ..., n.
הערה: לפיכך, הערכים המתוקננים של מד"א הם 0.0000, 0.2634, 0.9455, 1.0000 ו- 0.8729 באמצעות Eq. (2). - סטנדרטיזציה של התוכן הכולל של DDAs (להשיג yDDAs; DDAs מתייחס aconitine ו 3-deoxyaconitine) באמצעות הנוסחה Eq. (3).
הערה: i הוא אחד מארבעה גורמים, ו-j הוא כל רמה של הגורמים; Xij הוא התוכן הנמדד של ה-DDAs של הניסוי בפקטור i-th וברמת j-th; xj, min הוא התוכן המינימלי של DDAs בניסוי קבוצתי זה של נתונים; ו- xj, max הוא התוכן המרבי של DDAs בניסוי קבוצתי זה של נתונים. בדרך זו, i = 1, 2, ..., m, ו - j = 1, 2, ..., n. תכולת ה-DDAs (Xij) ב-TBC המעובד בעובי של 0.5, 1, 2, 3 ו-4 ס"מ הייתה 0.3492, 0.2692, 0.2962, 0.5354, 0.5124 מ"ג/גרם, בהתאמה. לפיכך, x j,max הוא 0.5354 ו- xj, min הוא 0.2692.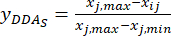 (3)
(3)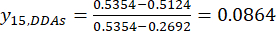
הערה: הערכים המתוקננים הם 0.6995, 1.0000, 0.8986, 0.0000 ו- 0.0864 באמצעות Eq. (3).
- לתקנן את התוכן של מד"א (להשיג yMDA; מד"א מתייחס לבנזואילקוניטין) באמצעות הנוסחה ב- Eq. (2).
- חשב את עוצמת הניגודיות המתאימה (S i), קונפליקט (δ i), מידע (C i) ומשקל אינדקס (W i) לפי Eqs. (4) עד (7), בהתאמה19,20.
הערה: i = 1, 2, ..., m. yij הוא הנתונים הסטנדרטיים של תוכן MDA או DDAs של הניסוי בגורם i-th וברמת j-th.- כדי להעריך את עוצמת הניגודיות, חשב תחילה את ערך מד"א הממוצע.
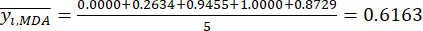
כאשר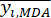 הוא הערך הממוצע של מד"א.
הוא הערך הממוצע של מד"א.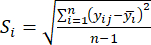 (4)
(4)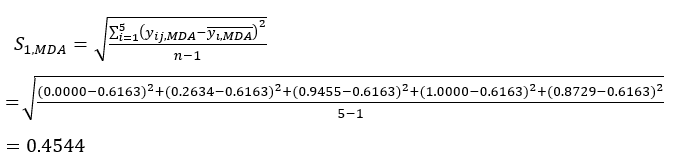
- כדי לחשב את ערך ההתנגשות, הערך תחילה את מקדם המתאם γ-ij באמצעות הפונקציה CORREL ב- Excel21.
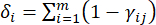 (5)
(5)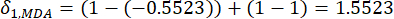
- חשב ערכי מידע באופן הבא.
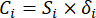 (6)
(6)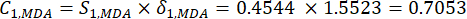
הערה: באופן דומה, C1, DDAS = 0.7210 - חשב את משקל המדד באופן הבא.
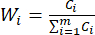 (7)
(7)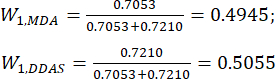
הערה: לפיכך, מקדמי המשקל של מד"א ומד"א בהשוואה לעובי הפרוסה נקבעו כ-0.4945 ו-0.5055, בהתאמה.
- כדי להעריך את עוצמת הניגודיות, חשב תחילה את ערך מד"א הממוצע.
- חשב את הציונים המקיפים של עובי הפרוסה.
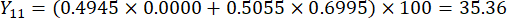
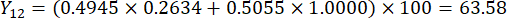
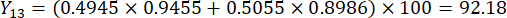
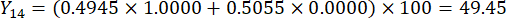
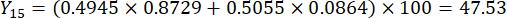
הערה: Y13 הוא הערך המרבי. לכן, הפרמטר הטוב ביותר של עובי חיתוך הוא הרמה השלישית - 2 ס"מ.
תוצאות
במחקר זה, לשיפוע האלוציה שבו השתמשו הייתה רזולוציה טובה (איור 1) עבור שלושת מרכיבי האינדקס ב-TBC מוקפץ זנבה, כפי שנקבע לאחר ניפוי באגים חוזר. לשלושת מרכיבי האינדקס ב-TBC מוקפץ-זנבה היה קשר ליניארי טוב בטווח ריכוזים מסוים (טבלה 2). הדיוק (טבלה 5), היציבות (טבלה 6), ה?...
Discussion
TBC היא תרופה טיבטית חשובה עם השפעות של הפגת קור והקלה על כאב. הוא משמש בעיקר לטיפול בפציעות טראומטיות ובארתרלגיה שגרונית בסין במשך אלפי שנים24,25,26. אלקלואידים דיטרפנואידים הם מרכיבים פעילים ורעילים של TBC27,28,29
Disclosures
למחברים אין ניגודי עניינים לחשוף.
Acknowledgements
עבודה זו נתמכה כספית על ידי הקרן הלאומית למדעי הטבע של סין (מס '82130113), הקרן למדע פוסט-דוקטורט בסין (מס '2021MD703800), קרן המדע לנוער של מדע וטכנולוגיה, המחלקה במחוז סצ'ואן (מס '2022NSFSC1449), ותוכנית קידום המחקר "מלגות Xinglin" של אוניברסיטת צ'נגדו לרפואה סינית מסורתית (לא. BSH2021009).
Materials
| Name | Company | Catalog Number | Comments |
| 3-Deoxyaconitine | Chengdu Desite Biotechnology Co., Ltd. | DST221109-033 | |
| Aconitine | Chengdu Desite Biotechnology Co., Ltd. | DSTDW000602 | |
| Ammonium acetate | Tianjin Kermel Chemical Reagent Co., Ltd | Chromatographic grade | |
| Benzoylaconitine | Chengdu Desite Biotechnology Co., Ltd. | DSTDB005502 | |
| Design-Expert software | Stat-Ease, Inc., Minneapolis, MN, USA | version 13.0 | |
| Electronic analytical balance | Shanghai Liangping Instruments Co., Ltd. | FA1004 | |
| High performance liquid chromatography | SHIMADZU Co., Ltd. | LC-20A | |
| High-speed smashing machine | Beijing Zhongxing Weiye Instrument Co., Ltd. | FW-100 | |
| Millipore filter | Tianjin Jinteng Experimental Equipment Co., Ltd | φ13 0.22 Nylon66 | |
| stir-Fry machine | Changzhou Maisi Machinery Co., Ltd | Type 5 | |
| Tiebangchui | Gannan Baicao Biotechnology Development Co., Ltd | 20211012 | |
| Ultra pure water systemic | RephiLe Bioscience, Ltd. | Genie G | |
| Ultrasonic cleansing machine | Ningbo Xinyi Ultrasonic Equipment Co., Ltd | SB2200 | |
| Zanba | 27 Chuanzang Road, Ganzi County | - |
References
- Li, C. Y., et al. Aconitum pendulum and Aconitum flavum: A narrative review on traditional uses, phytochemistry, bioactivities and processing methods. Journal of Ethnopharmacology. 292, 115216 (2022).
- Wang, J., Meng, X. H., Chai, T., Yang, J. L., Shi, Y. P. Diterpenoid alkaloids and one lignan from the roots of Aconitum pendulum Busch. Natural Products and Bioprospecting. 9 (6), 419-423 (2019).
- Yu, L., et al. Traditional Tibetan medicine: therapeutic potential in rheumatoid arthritis. Frontiers In Pharmacology. 13, 938915 (2022).
- Zhao, R., et al. One case of ventricular arrhythmia caused by poisoning of traditional Chinese medicine Aconitum pendulum Busch. Journal of People's Military Medical. 61 (4), 346-348 (2018).
- Qinghai Medical Products Administration. Processing specification of Tibetan medicine of Qinghai province. Qinghai Nationalities Publishing House. , 96-97 (2010).
- Li, J., et al. Comparison of three objective weighting methods to optimize the extraction process of Jianwei Chupi granules. Journal of Guangdong Pharmaceutical University. 38 (6), 91-97 (2022).
- Feng, Z. G., et al. Processing methods and the underlying detoxification mechanisms for toxic medicinal materials used by ethnic minorities in China: A review. Journal of Ethnopharmacology. 305, 116126 (2023).
- Hsu, Y. T., Su, C. S. Application of Box-Behnken design to investigate the effect of process parameters on the microparticle production of ethenzamide through the rapid expansion of the supercritical solutions process. Pharmaceutics. 12 (1), 42 (2020).
- Cheng, F., et al. Optimization of the baked drying technology of Cinnamomi Ramulus based on CRITIC combined with box-behnken response surface method. Journal of Chinese Medicinal Materials. 2022 (8), 1838-1842 (2022).
- Huang, X., et al. Optimization of microwave processing technology for carbonized Gardenia jasminoides by Box-Behnken response surface methodology based on CRITIC weighted evaluation. Chinese Herbal Medicines. 48 (6), 1133-1138 (2017).
- Elling, U., et al. Derivation and maintenance of mouse haploid embryonic stem cells. Nature Protocols. 14 (7), 1991-2014 (2019).
- Gu, J., Wang, Y. P., Ma, X. Simultaneous determinnation of three diester diterpenoid alkaloids in the toots of Aconiti flavi et penduli by HPLC method. Chinese Pharmaceutical Affairs. 28 (6), 618-621 (2014).
- Zhang, Y., Fu, X. UPLC simultaneous determination of six esteric alkaloids components in Aconitum Flaram Hand.Mazz. Asia-Pacific Traditional Medicine. 16 (5), 62-65 (2020).
- Rumachik, N. G., Malaker, S. A., Paulk, N. K. VectorMOD: Method for bottom-up proteomic characterization of rAAV capsid post-translational modifications and vector impurities. Frontiers In Immunology. 12, 657795 (2021).
- Wang, Y. J., Tao, P., Wang, Y. Attenuated structural transformation of aconitine during sand frying process and antiarrhythmic effect of its converted products. Evidence-Based Complementary and Alternative Medicine. 2021, 7243052 (2021).
- Wang, H. P., Zhang, Y. B., Yang, X. W., Zhao, D. Q., Wang, Y. P. Rapid characterization of ginsenosides in the roots and rhizomes of Panax ginseng by UPLC-DAD-QTOF-MS/MS and simultaneous determination of 19 ginsenosides by HPLC-ESI-MS. Journal of Ginseng Research. 40 (4), 382-394 (2016).
- vander Leeuw, G., et al. Pain and cognitive function among older adults living in the community. Journals of Gerontology Series A. Biological Sciences and Medical Sciences. 71 (3), 398-405 (2016).
- Lao, D., Liu, R., Liang, J. Study on plasma metabolomics for HIV/AIDS patients treated by HAART based on LC/MS-MS. Frontiers in Pharmacology. 13, 885386 (2022).
- Li, Y., et al. Evaluation of the effectiveness of VOC-contaminated soil preparation based on AHP-CRITIC-TOPSIS model. Chemosphere. 271, 129571 (2021).
- Zhong, S., Chen, Y., Miao, Y. Using improved CRITIC method to evaluate thermal coal suppliers. Scientific Reports. 13 (1), 195 (2023).
- Lewis, N. S., et al. Magnetically levitated mesenchymal stem cell spheroids cultured with a collagen gel maintain phenotype and quiescence. Journal of Tissue Engineering. 8, (2017).
- Chinese Pharmacopoeia Committee. . Pharmacopoeia of the People's Republic of China. 4, (2020).
- Li, G., et al. Effect of response surface methodology-optimized ultrasound-assisted pretreatment extraction on the composition of essential oil released from tribute citrus peels. Frontiers in Nutrition. 9, 840780 (2022).
- Liu, X. F., et al. Hezi inhibits Tiebangchui-induced cardiotoxicity and preserves its anti-rheumatoid arthritis effects by regulating the pharmacokinetics of aconitine and deoxyaconitine. Journal of Ethnopharmacology. 302, 115915 (2023).
- Smolen, J. S., et al. Rheumatoid arthritis. Nature Reviews.Disease Primers. 4, 18001 (2018).
- Wang, F., et al. C19-norditerpenoid alkaloids from Aconitum szechenyianum and their effects on LPS-activated NO production. Molecules. 21 (9), 1175 (2016).
- Wang, B., et al. Study on the alkaloids in Tibetan medicine Aconitum pendulum Busch by HPLC-MSn combined with column chromatography. Journal of Chromatographic Science. 54 (5), 752-758 (2016).
- Liu, S., et al. A review of traditional and current methods used to potentially reduce toxicity of Aconitum roots in Traditional Chinese Medicine. Journal of Ethnopharmacology. 207, 237-250 (2017).
- Qiu, Z. D., et al. Online discovery of the molecular mechanism for directionally detoxification of Fuzi using real-time extractive electrospray ionization mass spectrometry. Journal of Ethnopharmacology. 277, 114216 (2021).
- El-Shazly, M., et al. Use, history, and liquid chromatography/mass spectrometry chemical analysis of Aconitum. Journal of Food and Drug Analysis. 24 (1), 29-45 (2016).
- Chan, T. Y. K. Aconitum alkaloid poisoning because of contamination of herbs by aconite roots. Phytotherapy Research. 30 (1), 3-8 (2016).
- Guo, L., et al. Exploring microbial dynamics associated with flavours production during highland barley wine fermentation. Food Research International. 130, 108971 (2020).
- Guo, T. L., Horvath, C., Chen, L., Chen, J., Zheng, B. Understanding the nutrient composition and nutritional functions of highland barley (Qingke): A review. Trends in Food Science & Technology. 103, 109-117 (2020).
- Wu, H., et al. Anti-myocardial infarction effects of Radix Aconiti Lateralis Preparata extracts and their influence on small molecules in the heart using matrix-assisted laser desorption/ionization-mass spectrometry imaging. International Journal of Molecular Sciences. 20 (19), 4837 (2019).
- Huang, G., et al. Study on cardiotoxicity and mechanism of "Fuzi" extracts based on metabonomics. International Journal of Molecular Sciences. 19 (11), 3506 (2018).
- Li, S. L., et al. An insight into current advances on pharmacology, pharmacokinetics, toxicity and detoxification of aconitine. Biomedicine & Pharmacotherapy. 151, 113115 (2022).
- Xie, Y., et al. Optimization of processing technology of braised Rehmanniae Raidx based on multiple indexes and response surface technology and correlation between components and color. Journal of Chinese Traditional Medicine. 47 (18), 4927-4937 (2022).
- Yang, X. Q., Xu, W., Xiao, C. P., Sun, J., Feng, Y. Z. Study on processing technology of Atractylodes chinensis with rice water and its pharmacodynamics of anti-diarrhea. Chinese Herbal Medicines. 53 (1), 78-86 (2022).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved