A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
טכניקה אוסף טורי של הנוזל השדרתי מן צ'יסטרנה מגנה על עכבר
Summary
טראנסגנטי (TG) מודלים העכבר לספירה לספק הזדמנות מצוינת לחקור כיצד ומדוע רמות Aβ או טאו בשינוי CSF התקדמות המחלה בחולים אנושיים. כאן, אנו מדגימים מעודן צ'יסטרנה magna טכניקה לנקב הדגימה CSF סדרתי של העכבר.
Abstract
מחלת אלצהיימר (AD) היא מחלה ניוונית מתקדמת מאופיינת על ידי פתולוגית בתצהיר של תאי β עמילואיד פפטיד (Aβ) והצטברות intraneuronal של חלבון טאו hyperphosphorylated. בגלל נוזל המוח והשדרה (CSF) נמצא בקשר ישיר עם המרחב תאי המוח, הוא מספק השתקפות של שינויים ביוכימיים במוח בתגובה תהליכים פתולוגיים. CSF מחולים לספירה מראה ירידה בצורת חומצה אמינית 42 של Aβ (Aβ42), ועלייה טאו טאו סך hyperphosphorylated, אם כי המנגנונים האחראים שינויים אלה עדיין אינם מובנים במלואם. טראנסגנטי (TG) מודלים העכבר לספירה לספק הזדמנות מצוינת לחקור כיצד ומדוע רמות Aβ או טאו בשינוי CSF עם התקדמות המחלה. כאן, אנו מדגימים מעודן צ'יסטרנה magna טכניקה לנקב הדגימה CSF מן העכבר. טכניקה זו מאפשרת דגימה עדין מאוד סדרתי דגימות CSF להיות המתקבל עכבר באותו חודש 2-3 במרווחים אשר מאוד מצמצם את ההשפעה של השתנות מבלבלים בין העכבר ברמות Aβ או טאו, כך שניתן לזהות שינויים עדינים לאורך זמן. בשילוב עם Aβ ו טאו ELISA, טכניקה זו יהיה שימושי עבור מחקרים שנועדו לבחון את היחס בין רמות של CSF Aβ42 ו טאו, חילוף החומרים שלהם במוח במודלים של העכבר לספירה. מחקרים בעכברים Tg יכול לספק אימות חשוב לגבי הפוטנציאל של Aβ CSF או רמות טאו לשמש סמנים ביולוגיים על התקדמות המחלה ניטור, כדי לפקח על ההשפעה של התערבויות טיפוליות. כמו עכברים אפשר להקריב את המוח ניתן לבחון שינויים ביוכימיים או היסטולוגית, המנגנונים שבבסיס השינויים CSF ניתן להעריך טוב יותר. נתונים אלה צפויים להיות אינפורמטיבי לפרשנות של שינויים CSF האדם לספירה.
Protocol
משיכת צינור זכוכית נימי
- צינור זכוכית נימי היא לרכוש את המכשיר סאטר Inc (בורוסיליקט זכוכית, B100-75-10).
- משוך את צינורות נימי על סאטר P-87 Flaming micropipette חולץ, עם מדד חום להגדיר 300 ומדד הלחץ נקבע על 330.
- חתוך את קצה צינור זכוכית נימי במספריים, כך קצה קוני בעל קוטר פנימי של כ - 0.5 מ"מ.
צ'יסטרנה magna לנקב טכניקה CSF
דגימות CSF לקוחים צ'יסטרנה magna (איור 1) בשיטה התפרסם בעבר 1. 
איור 1
1. עכברים הם anesthesized ידי קטמין (100mg/kg) ו xylazine (10mg/kg), intraperitoneally מנוהל. במהלך תקופה של אינדוקציה הרדמה, העכברים מוחזקים 37 מעלות צלסיוס חממה.
2. העור של הצוואר הוא מגולח, ואת העכבר ממוקם אז נוטה על המכשיר stereotaxic עם מגע ישיר של כרית חימום. בדיקה רקטלית טמפרטורה מוכנס לתוך פי הטבעת, כך החום המיוצר על ידי כרית חימום מותאם בתגובה לשינויים בטמפרטורת הגוף. ראש מאובטח עם מתאמי הראש. האתר כירורגית הוא ניקה עם יוד povidone 10%, ואחריו אתנול 7 0% (חוזר 3 פעמים), וכן חתך sagittal של העור נעשה נחות העורף.
3. תחת המיקרוסקופ לנתיחה, הרקמה התת עורית והשרירים (מ biventer cervicis ומ rectus capitis dorsalis הגדולות) מופרדים באמצעות דיסקציה קהה עם מלקחיים. צמד של microretractors משמש להחזיק את השרירים בנפרד.
4. העכבר הוא הניח כך שהראש יוצר זווית כמעט 135 o עם הגוף.
5. תחת המיקרוסקופ לנתיחה, מאטר הדורה של צ'יסטרנה magna מופיע משולש הפוך נוצצים ברור שדרכו הלשד המוארך וכלי הדם הגדולים (arteria spinalis dorsalis), ואת החלל CSF גלויים (איור 2). 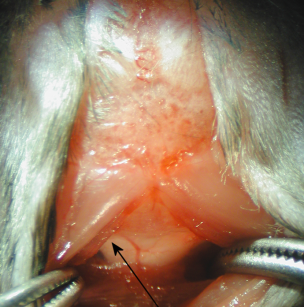
איור 2
6. מאטר הדורה נמחקת יבש עם מטלית כותנה סטרילי. לחדור לתוך צינור נימי citerna magna דרך מאטר דורה, לרוחב spinalis dorsalis arteria (איור 2). בעקבות שינוי ניכר התנגדות החדרת צינור נימי, CSF זורם לתוך צינור נימי.
7. הסר בזהירות את צינור נימי, ולחבר אותו מזרק 3 מ"ל דרך צינורות פוליאתילן בעל קוטר 1 מ"מ פנימי. להזריק את CSF לתוך צינור מראש המסומנים Eppendorf 0.5 מ"ל, ולהקפיא את הצינור מיד על קרח יבש ולאחר מכן להעביר אותו למקפיא -80 מעלות צלזיוס.
8. CSF לאחר הדגימה, את השרירים מחדש מיושר, והעור הוא sutured (4-0, Ethicon, חברת Johnson & Johnson). אודות 1 מ"ל של 0.9% NaCl מוזרק מתחת לעור כדי למנוע דה הידרציה. העכבר הוא שמר על האינקובטור כדי לשמור על טמפרטורת הגוף עד שהוא מתאושש; את משקל העכבר מנוטר 1 יום, 1 שבוע לאחר הניתוח.
תוצאות ודיון
אנו תיאר פרוטוקול אמין הדגימה הסידורי של CSF מעכברים ללא זיהום פלזמה לזיהוי.
1. ההליך כולו אורך בדרך כלל 10 דקות לכל עכבר (כולל הרדמה). נפח CSF שהושגו תלויה זנים העכבר. בעכברים PS / APP Tg כפול השתמשנו 2, הנפח הממוצע הוא כ - 5 μl (3-7 μl), ואילו (JNPL3) עכברים P301L 3 נותן תשואה של כ μl μl-15 10. עבור דגימה סדרתי, לכל היותר 7-8 μl יכול להילקח בבטחה כל פעם בהפרש של 2-3 חודשים.
2. במהלך הניתוח, חשוב למקם את הראש ואת הגוף של העכבר כראוי על המסגרת stereotaxic כך מאטר הדורה של צ'יסטרנה magna יכולים להיחשף מספיק. בזהירות למנוע את כלי הדם, כאשר חודר מאטר הדורה עם צינור נימי על מנת למנוע זיהום של חלבונים פלזמה, אשר ניתן לנטר במדגם CSF על ידי immunoblotting עבור ApoB 4.
3. צמצום נזק לרקמות במהלך הניתוח כל חשוב, כמו conglutination רקמות יכולים להגדיל את הקושי על ידי דימום predisposing הדגימה הבאה.
4. טמפרטורת הגוף צריך להיות מטופח במהלך הניתוח כי היפותרמיה הנגרמת על ידי הרדמה יכולים להשפיע משמעותית על רמות טאו phosphorylated במוח במהירות רבה 5.
5. ELISA Ab פרוטוקול נוגדנים השתמשנו תוארו בפירוט Refolo et al. 6. שני μl של CSF מעכברים PS / APP ייתן תוצאות משביעות רצון כאשר בדילול 1:50-1:60. עבור ELISA טאו, 4-5 CSF μl מ P301L (JNPL3) בעכברים יהיה מספיק עבורזיהוי מוחלט של טאו, או טאו זרחן ylated ב תראונין 231 (ערכות נרכשים מן המקור-Bio).
6. טכניקה זו ניתן ליישם מודלים העכבר אחרים של מחלות נוירולוגיות, אשר נפח קטן של CSF היא משביעת רצון עבור מבחני הרצוי.
Discussion
אנו תיאר פרוטוקול אמין הדגימה הסידורי של CSF מעכברים ללא זיהום פלזמה לזיהוי.
1. ההליך כולו אורך בדרך כלל 10 דקות לכל עכבר (כולל הרדמה). נפח CSF שהושגו תלויה זנים העכבר. בעכברים PS / APP Tg כפול אנו used2, הנפח הממוצע הוא כ - 5 μl (3-7 μl), ואילו (JNPL3) עכברים P301L 3 נותן תשואה של ...
Acknowledgements
העבודה שלנו היא נתמכת על ידי NIH מענקים NS048447 ו AG017216to KD. לי ליו רוצה להודות לד"ר הייקי Tanila (מאוניברסיטת קופיו, Kuopio, פינלנד) על הפיקוח שלו ואת התמיכה במהלך הפיתוח של הפרוטוקול המקורי.
References
- Liu, L., et al. Longitudinal observation on CSF Abeta42 levels in young to middle-aged amyloid precursor protein/presenilin-1 doubly transgenic mice. Neurobiol Dis. 17, 516 (2004).
- Holcomb, L., et al. Accelerated Alzheimer-type phenotype in transgenic mice carrying both mutant amyloid precursor protein and presenilin 1 transgenes. Nat Med. 4, 97 (1998).
- Lewis, J., et al. Neurofibrillary tangles, amyotrophy and progressive motor disturbance in mice expressing mutant (P301L) tau protein. Nat Genet. 25, 402 (2000).
- DeMattos, R. B., et al. Plaque-associated disruption of CSF and plasma amyloid-beta (Abeta) equilibrium in a mouse model of Alzheimer's disease. J Neurochem. 81, 229 (2002).
- Planel, E., et al. Anesthesia leads to tau hyperphosphorylation through inhibition of phosphatase activity by hypothermia. J Neurosci. 27, 3090 (2007).
- Refolo, L. M., et al. A cholesterol-lowering drug reduces beta-amyloid pathology in a transgenic mouse model of Alzheimer's disease. Neurobiol Dis. 8, 890 (2001).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved