このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
非対称受容体のパターンでセルローリング軌道を勉強
要約
我々は、非対称受容体柄の基板上にセルローリング軌跡を観察し、分析するためのプロトコルについて説明します。結果のデータは、ラベルフリー細胞分離と解析のための受容体柄の基板のエンジニアリングするのに便利です。
要約
非対称受容体パターン上を転動することによりフロー流に直交するセルの横方向変位は、セル1のラベルフリーの分離および分析用の新しいデバイスの開発のための機会を提供します。このようなデバイスは、連続フロー分離、または異なる細胞表現型または受容体の発現のレベルを区別するために接着を調節する受容体のパターンの横変位を使用することができます。受容体-パターニング基板上に軌跡を圧延細胞の性質を理解することは、基板とそのようなデバイスの設計のエンジニアリングが必要である。
ここでは、セルローリング接着2をサポートしている非対称の受容体のパターンでセルローリング軌道を研究するためのプロトコルを示す。 P -セレクチン受容体の明確に定義された、ミクロンスケールのパターンは、フローチャンバー内に組み込まれた金被覆スライド上にマイクロコンタクトプリントを作製した。 PSGL - 1リガンド3を発現HL60細胞がパターン化された行のフィールドを越え流れと逆の明視野顕微鏡で視覚化した。細胞は横方向のたわみ1で、その結果、パターンの傾斜縁部に沿ってロールバックして追跡。各セルは、一般的に、パターンのエッジに沿って一定の距離(エッジ追跡の長さとして定義される)のためにロール端から剥離し、下流のパターンに再接続。この剥離が困難フローチャンバーに終了するには、入り口から細胞の全体の軌跡を追跡することになりますが、粒子追跡のソフトウェアは、それらが単一の受容体に移動された時に細胞のローリング軌跡を分析し、生成するために使用されていました柄のライン。軌道は、セルの圧延速度と異なるパターンの各セルのエッジ追跡の長さの分布を得るために検討した。
このプロトコルは、受容体のパターンでセルローリング軌跡を定量化し、パターンの角とせん断応力などのこれらの工学的パラメータを関連づけるのに便利です。そのようなデータは、ラベルフリー細胞の分離および分析用マイクロ流体デバイスの設計に有効になります。
プロトコル
1。 HL60細胞のローリング
1.1。加工基板の作製。
- 金でコーティングされたガラススライド上にPEG分子の自己組織化単分子膜を(SAM)が交互にするマイクロコンタクトプリンティング(μCP)4-7を使用する:α= 10の傾斜角度で受容体のパターンを定義したマイクロコンタクトプリンティングポリジメチルシロキサン(PDMS)スタンプの作製SU - 8の成形プロセスによる°。 20分間ピラニア溶液(30%過酸化水素に硫酸の3:1混合物)で、金表面を清掃し、使用する° Cより前の24.5で、大量のDI水で表面を洗う。エタノール5mmのPEG溶液とインクPDMSスタンプを。 20分間空気中のタイムスタンプを乾かします。ゆっくりと40秒のために金表面にスタンプを置き、金表面とスタンプ間の良好な接触があることを確認してください。過剰な圧力は必要ありません。エタノールで表面をリンスし、N 2気流下でそれを乾燥させてください。
- ° Cパターンの24.5で3時間灌流室(電子顕微鏡の科学)を用いて、P -セレクチン溶液(DPBS 15μg/ mLの)P -セレクチンとの残りの領域内の基板をインキュベートする。大量のDPBSで表面を洗浄します。
- 埋め戻しの非特異的相互作用をブロックするために1時間BSA(DPBSで1 mg / mL)で表面。大量のDPBSで表面を洗浄します。
1.2。フローチャンバーで実験をローリング細胞。
- 長方形のフローチャンバーにパターン化表面上にHL60細胞(〜10 5細胞/ mL)(; 幅 w = 1.0センチメートル、長さ= 6センチメートル、Glycotech、株式会社高さh = 0.0127センチメートル)の懸濁液を流す24.5℃で0.5 DYN / cm 2と (〜0.05 Pa)の周りの対応するせん断応力と、75μL/ minの流量を生成するためのシリンジポンプ(世界の精密機器、SP230IW)を使用してください。 τ平面ポアズイユ流の方程式体積流量Qは、μは動粘度(0.001002 PaのS)であるτは=6μQ/wh2を 、使用して、せん断応力を計算し、wはフローチャンバーの幅であり、hは高さです。フローチャンバー。
- 300の期間については、通常、1秒あたり1フレームの速度で、4を用いて接着剤P -セレクチン基質との相互作用をローリングHL60細胞を記録するために設置されたカメラ(アンドールIXON 885)×目標と倒立顕微鏡(ニコンTE2000 - U)を使用してくださいS.それぞれのせん断応力の大きさとパターンの傾斜角の3つの独立した実験を、実行します。各実験から得られた平均値の平均と標準偏差として存在するデータ。
- データ解析。
パターニングされた線のエッジに沿ってトラックを生成するフリーウェア8を追跡粒子を利用したカスタマイズされたMatlabの(MathWorks社)プログラムによって画像のシーケンスを分析する。 P -セレクチンバンドの終わりまで拡張するトラックを選択し、2本の直線の線分が備わっています - 流れに沿った一つのパターンのエッジに揃え、他。これら2つのセグメントは、次にエッジで速度を圧延し、平野地域で速度を圧延、エッジ追跡の長さを計算するために使用されています。
2。代表的な結果:
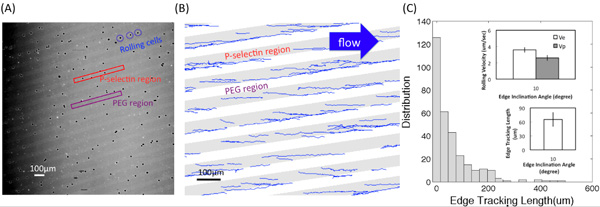
図(A)は 4 ×の対物レンズを用いて接着剤P -セレクチン基質とHL60ローリング相互作用のビデオから変換した顕微鏡画像の一つを示しています。明るい領域と暗い領域はそれぞれ、P -セレクチン受容体とPEGの地域に対応しています。 図(B)は、カスタマイズされたMatlabのプログラムを使用して得られたトラックを示しています。エッジの傾斜角度は10 °であり、せん断応力は、0.5 DYN / cm 2であった。エッジ追跡の長さ、L E、変位、D、およびエッジ上やバンド内の圧延速度は、それぞれV、EとV のp、、 図(C - 1)に記載されている。 図(C - 2)を示しエッジ追跡の長さの分布(記録されたセルの数)。インセットは、L Eの平均値とエッジの圧延速度(V、E)を示し、傾斜角のバンド(V P)内部のα= 10 °および0.5 DYN / cm 2と周りの流体せん断応力の大きさ。エラーバーは、各条件の1つの標準偏差、n = 3の複製実験を(3回の反復面)を表します。
ディスカッション
我々は、マイクロコンタクトプリンティング2を用いて作製した非対称受容体柄の表面にセルローリング軌跡を調べるために、プロトコルを記述している。 PEGとP -セレクチンの領域の間に明確なコントラストを示すパターン化表面の光学顕微鏡像は、スタンピングが成功したかどうかを確認するために使用することができます。シャープ、ストレートエッジは刻印がよく実行されると...
開示事項
謝辞
このプロジェクトは、MITの技術革新のためのデシュパンデセンター(RKとJMK)と化学と生物学的分離プログラムを通じてRKにNSFのキャリア賞0952493によってサポートされていました。我々は兵士のナノテクノロジー(ISN)とその施設の使用のためのMITのマイクロ技術研究所(MTL)のための研究所に感謝する。
資料
| Name | Company | Catalog Number | Comments |
| Human promyelocytic leukemia cells | ATCC | CCL-240 | HL60 cells |
| Gold-coated glass slides | EMF | TA134 | Gold slides |
| (1-Mercaptoundec-11-yl)tetra(ethylene glycol) | Sigma-Aldrich | 674508 | PEG |
| Recombinant human P-selectin | R&D Systems | ADP3-050 | P-selectin |
| Bovine serum albumin | Rockland Immunochemicals | BSA-50 | BSA |
| Dulbecco’s phosphate buffered saline | Mediatech, Inc. | 21-030 | DPBS |
| Sulfuric acid | Sigma-Aldrich | 339741 | |
| Hydrogen peroxide | Sigma-Aldrich | 316989 |
参考文献
- Karnik, R., Hong, S., Zhang, H., Mei, Y., Anderson, D. G., Karp, J. M., Langer, R. Nanomechanical control of cell rolling in two dimensions through surface Patterning of receptors. Nano Lett. 8 (4), 1153-1158 (2008).
- Lee, C. H., Bose, S., Van Vliet, K. J., Karp, J. M., Karnik, R. Examining Lateral Displacement of HL60 Cells Rolling on Asymmetric P-selectin Patterns. Langmuir. 27 (1), 240-249 (2011).
- Norman, K. E., Moore, K. L., McEver, R. P., Ley, K. Leukocyte rolling in-vivo is mediated by p-selectin glycoprotein ligand-1. Blood. 86 (12), 4417-4421 (1995).
- Bernard, A., Delamarche, E., Schmid, H., Michel, B., Bosshard, H. R., Biebuyck, H. Printing patterns of proteins. Langmuir. 14 (9), 2225-2229 (1998).
- James, C. D., Davis, R. C., Kam, L., Craighead, H. G., Isaacson, M., Turner, J. N., Shain, W. Patterned protein layers on solid substrates by thin stamp microcontact printing. Langmuir. 14 (4), 741-744 (1998).
- Mrksich, M., Whitesides, G. M. Using self-assembled monolayers to understand the interactions of man-made surfaces with proteins and cells. Annual Review of Biophysics and Biomolecular Structure. 25, 55-78 (1996).
- Tan, J. L., Tien, J., Chen, C. S. Microcontact printing of proteins on mixed self-assembled monolayers. Langmuir. 18 (2), 519-523 (2002).
- Lee, D., King, M. R. Microcontact Printing of P-Selectin Increases the Rate of Neutrophil Recruitment Under Shear Flow. Biotechnology Progress. 24 (5), 1052-1059 .
- Greenberg, A. W., Hammer, D. A. Cell separation mediated by differential rolling adhesion. Biotechnol. Bioeng. 73 (2), 111-124 (2001).
- Higuchi, A., Tsukamoto, Y. Cell separation of hepatocytes and fibroblasts through surface-modified polyurethane membranes. J. Biomed. Mater. Res. Part A. 71A (3), 470-479 (2004).
- Alexeev, A., Verberg, R., Balazs, A. C. Patterned surfaces segregate compliant microcapsules. Langmuir. 23 (3), 983-987 (2007).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved