このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
の調製と評価
要約
Here, we describe a protocol for radiolabeling and in vivo testing of tridentate 99mTc(I) chelate-tetrazine derivatives for pre-targeting and bioorthogonal chemistry.
要約
Pre-targeting combined with bioorthogonal chemistry is emerging as an effective way to create new radiopharmaceuticals. Of the methods available, the inverse electron demand Diels-Alder (IEDDA) cycloaddition between a radiolabeled tetrazines and trans-cyclooctene (TCO) linked to a biomolecule has proven to be a highly effective bioorthogonal approach to imaging specific biological targets. Despite the fact that technetium-99m remains the most widely used isotope in diagnostic nuclear medicine, there is a scarcity of methods for preparing 99mTc-labeled tetrazines. Herein we report the preparation of a family of tridentate-chelate-tetrazine derivatives and their Tc(I) complexes. These hitherto unknown compounds were radiolabeled with 99mTc using a microwave-assisted method in 31% to 83% radiochemical yield. The products are stable in saline and PBS and react rapidly with TCO derivatives in vitro. Their in vivo pre-targeting abilities were demonstrated using a TCO-bisphosphonate (TCO-BP) derivative that localizes to regions of active bone metabolism or injury. In murine studies, the 99mTc-tetrazines showed high activity concentrations in knees and shoulder joints, which was not observed when experiments were performed in the absence of TCO-BP. The overall uptake in non-target organs and pharmacokinetics varied greatly depending on the nature of the linker and polarity of the chelate.
概要
99m Tc では、世界的に年1、2、3ごとに行わ億50以上の撮像法で、核医学診断に使用される支配的な放射性同位元素のまま。臨床的に使用される99m Tc での薬剤の大部分は、灌流型放射性医薬品です。 99m Tc では、ターゲティング構築物への連結を介して、特定のバイオマーカーを結合するのに向いている積極的に標的とする化合物の数は限られています。対象と99m Tc での放射性医薬品の作成は、多くの場合、目的のバイオマーカー、または同位元素の半減期と結合するターゲッティング分子の能力に99m Tc で -リガンド複合体の影響により阻害される高分子量の生体分子と共に使用するための十分な長さではありません抗体など。後者は、典型的には、画像が非標的TISSからクリアする生体分子のためのために取得されるまでに数日を要します UE。プレターゲッティングは、これらの課題を克服するための代替的なアプローチを提供しています。
バイオ直交化学と組み合わせたプレターゲッティングの両方蛍光および放射性イメージング4、5、6、7、8のための新たな分子イメージングプローブを開発するための有効な方法であることが示されています。 1,2,4,5-テトラジン(Tzの)およびトランス -cyclooctene(TCO)誘導体の間の逆電子需要ディールス-アルダー(IEDDA)反応、 図1に示すように、6特に有効であることが示されました。これらのコンポーネントとのIEDDA反応は、高選択性、in vivoでプレターゲッティングアプリケーション9、10にも最適です(2≈6000 M -1 s -1のk)をPBSに速い反応速度を示すことができます。
e_content 11 C、18 Fに基づく">使用される最も一般的なアプローチは、TCO由来ベクターを標的にし、十分な遅延期間の後、放射性標識されたテトラジンが投与さを投与することを含む。放射性標識テトラジン、64のCu、89 Zrおよび111 Inがされています11、12、13、14、15に報告された。対照的に、in vivoでの結合タンパク質および分解を防止するために、共リガンドの使用を必要とHYNIC系配位子を用いて調製したの99mのみ報告Tc標識Tzのは、あります16。別の方法として、ここでは99m Tc で (I)の合成を報告し、[99m Tc で (CO)3] +コアで安定した三座複合体を形成するリガンドのファミリーを使用して、テトラジンを標識しました。 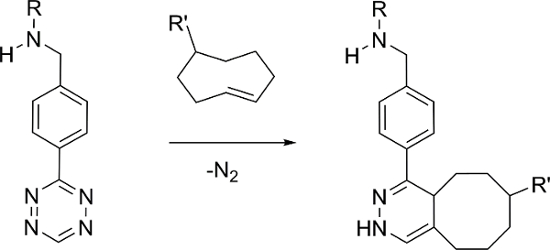
図1:テトラジンとトランス -cyclooctene間のバイオ直交IEDDA反応。 この図の拡大版をご覧になるにはこちらをクリックしてください。
準備リガンドのファミリーは、極性および金属結合領域とTzを( 図2)との間のリンカー基の性質に変化する三座キレートを含んでいます。目標は、結合していないときに効果的に高い標的対非標的比を得るために、局在化およびin vivoでの TCO標識部位と反応し、速やかにクリアできた99m Tc でテトラジン構築物を同定することでした。リガンドをテストするには、ビスホスホネートのTCO-誘導体(TCO-BP)が17を使用しました。私たちは、TCO-BPは、アクティブな骨代謝の領域に局在することが以前に示されているとと反応することができます生体内 18 で放射性標識されたテトラジン。それは、単一の工程で調製することができ、実験は局在が主に関節(膝、および肩)で発生する通常のマウスで行うことができるので、新たなテトラジンをテストするための便利な試薬です。
プロトコル
動物実験は、動物ケアに関するカナダ評議会(CCAC)のガイドラインに従ってマクマスター大学の動物研究倫理委員会によって承認されました。
99m Tc でとTZ-三座配位子の1放射性標識
警告:以下の手順は、放射性化合物の使用を必要とします。仕事は、安全性と廃棄規制の遵守とライセンス実験室で行われるべきです。マイクロ波反応は、特に、化学合成のために設計されたマイクロ波中で行うべきです。
- 合成[99m Tc で (CO)3(H 2 O)3] + 19、20
- マイクロ波バイアルに、結合8mgのK 2 [BH 3 CO 2] 15mgののNa 2 CO 3、20ミリグラムのNa 2 B 4 O 7・10H 2 O、及び25mgのKOCO [CH(OH)]2 COONa・4H 2 Oをパージアルゴンガスで10分間バイアル。
- バイアルに0.9%生理食塩水で(〜1100 MBqで、〜30 MCI) - 99メートルのTcO 4の4 mLを加え。
- 試薬の十分な混合を確実にするために攪拌し、10秒後、110℃で3.5分間マイクロ波中の反応を加熱します。
- 〜400μLの1 M HClを用いて3.5から4に、溶液のpHを調整します。 pH試験紙を使用して確認してください。
- テトラジンの放射性標識は、1-5のリガンド
- 250μLのMeOH 21内の各リガンドの2mgの(化合物1-5)を溶解します。
- 各ソリューションに[99m Tc で (CO)3(H 2 O)3] +(〜74 MBqで、〜2 MCI)の250μLを追加します。
- 60℃で20分間マイクロ波を用いて反応混合物を加熱します。
注:この手順は、すべての5テトラジンため同一でした。 - 化合物2-5の場合は、溶媒および再dissolを蒸発させます1(v / v)のDCM:TFA 1の1mLに得られる生成物をまし。
- 6分(2-4)または10分(5)マイクロ波で60℃で溶解させた反応生成物(2-5)を加熱します。
- 室温に冷却した後、エバポレーター(36℃、8ミリバール、3分、6,000 rpm)を用いて溶媒を蒸発させ、1で乾燥させ、化合物溶解:1 ACN:H 2 Oまたは1:1のMeOH:H 2 OをHPLC精製の前に。
- HPLC(C 18逆相)を用いて、未標識テトラジンリガンドで標識された生成物を分離するなどの99m Tc で標識した化合物(1-5)を 、精製します。 H 2 O 20を超える分(18分)、C 18分析4.6×100 mmカラム:40:60 ACNにH 2 O(0.1%TFAとの両方):通常、30:70 ACNの溶出勾配を使用します。 UV(254 nm)で、ガンマ検出の両方を使用してください。
- 各標識生成物の少量のサンプルを取り、共同INJのそれにそのHPLC保持時間を比較します(20%メタノール-H 2 O中の0.125 mg)をected、非放射性、Re標識標準。 Re標識標準は、UV HPLCトレースで識別され、γ-HPLCトレース中の99m Tc で標識化合物と同時に溶出します。この共注射は99m Tc で標識された化合物の正体を確認し、同程度の保持時間でピークを示しています。
- 蒸発器(36℃、8ミリバール、3分、6,000 rpm)を用いたHPLC画分から溶媒を蒸発させます。
- 0.5%BSAおよび0.01%のTween-80を含む、7.4 kBq / PBS中μLの濃度で精製された化合物を策定します。
- 標識された化合物が安定であることを確認するために、in vitroでの安定性試験を行います。安定性を評価するために、各時点でのHPLCに混合物の少量(3.7 MBqの)を注入し、1、4、6時間37℃で製剤化化合物をインキュベートします。
2.事前標的バイオ分布研究
- 動物の i>の準備
- 7-9週齢の雌のBALB / cマウスを用いて(n = 3)を、尾静脈注射を介して、TCO-BPは、生理食塩水(20ミリグラム/キログラム)(5μgの/μL)中に処方管理。
- 物理的な拘束装置にマウスを置き、尾の側面に位置する静脈を識別し、アルコール綿棒で拭いてください。尾の先端から約2cmで、静脈に浅い角度、並列で30ゲージの針を挿入します。ゆっくりと、注射針を削除し、出血が止まるまでのわずかな圧力で、注射部位で清潔なガーゼスポンジを適用するプランジャーを押し下げます。
- TCO-BPの1時間後の注射では、尾静脈注射を介して、PBS中の0.5%BSAの100μLで処方さ99m Tc でテトラジンの〜0.74 MBqの(20マイクロCi)、0.01%のTween-80を投与します。
- 生体分布研究
- 所望の時点(T = 6時間)、3%イソフルラン2%酸素の混合ガスを使用してマウスanaesthetize。に実証eは、麻酔の外科的平面の下であることを確認するために麻酔をかけたマウスの撤退をつまみます。
- シリンジヘパリンで前処理を使用して、心臓穿刺により血液(1ミリリットル)を収集します。継続的な麻酔のためのノーズコーンで鼻との背中の上に置いてマウスや動物に剣状突起の位置を確認します。
- 20°の角度で、少し剣状突起下の動物の正中線の左に、25 G針を挿入します。完全に針を挿入し、ゆっくりと心を穿刺した場合、針ハブに血を見るために、プランジャーに引き戻します。必要に応じて、心臓を穿刺し、プランジャーを保持しながら、わずかに針を再調整。ゆっくりとシリンジに血液を描画します。
- 麻酔下ながら、頸椎脱臼により動物を安楽死させます。
- ビニール袋に各動物を置き、全身の活動レベルを測定するために、投与量キャリブレータ(99m Tc で設定)を使用します。
- 前計量で、次の組織および体液を収集(内容を)(内容の)血液、骨(膝と肩)、胆嚢、腎臓、肝臓、胃、(内容で)小腸、大腸と盲腸、甲状腺および気管、尿と膀胱:チューブをカウント編、および尾。
- 適切な計数管に組織を置く前に血液を除去し、乾燥ブロットをPBS中(血液、胆嚢、および膀胱を除く)は、適切な組織をすすいでください。
- ビニール袋に動物の死体を置き、投与量キャリブレータを使用して残留全身活性を測定。
- 組織サンプルを含む各チューブを秤量します。チューブの減算初期重量は、組織の塊を得ました。
- 各マウスについての注射の時に試験サンプル(100μL)で活性の量を測定するために、投与量キャリブレータ(99m Tc で設定)を使用します。
注:この試験サンプルは、したがって、注射時に活動カウントを与え、注入量に等しいです。 - 組織の測定時に、A以前に使用した試験サンプルのliquot 5μL。マルチ検出器ガンマカウンター(99m Tc で設定)を使用し、5μLの試験サンプル毎分のカウント(CPM)を得ることがカウントされます。
- 換算係数(CPMマイクロCi -1)を得るために、式1を使用して活動し、CPMの関係を計算するために、2.2.9と2.2.10で得られた2つの値を使用してください。
(1)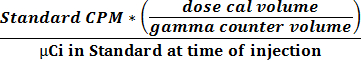
- 各組織または液体サンプル中の放射能の量を測定するために、ガンマカウンターを使用してください。
- 総注射量の測定の相対的な時に各組織または体液中の活動量を算出するための式1を使用してください。この値は、臓器重量によって正規化し、組織のグラム当たりのパーセント注射用量( すなわち、%のID / g)と報告されています。
- 手順に従ってくださいabsenにおける99m Tc で標識テトラジンリガンドを使用して、負の対照実験を行うために2.2.13に2.1.2TCO-BPのCE。犠牲マウス(n = 3)0.5、1、4及び6時間後の注射で、上述したように、組織または流体を得ました。
結果
リガンドは、商業的に入手可能なテトラジン22、23製品のカップリング、続いて単純な還元的アミノ化戦略( 図2)を介して、異なるリンカーおよびキレート剤を用いて合成しました。放射性標識は、全ての化合物のための同様の方法を使用して実行し、高度に再現可能でした。 83%(1)、45%(2)?...
ディスカッション
変化する極性のテトラジン結合三座キレートのコレクションを調製し、in vivoでの TCO誘導体とIEDDA反応におけるそれらの99m Tc での複合体の有用性を評価しました。効果的かつ再現性の99m Tc で標識法は、リガンド濃度はラベリング工程(化合物2-5) のt-ブチル基の脱保護を行った10 -3 Mであった。5テトラジンキレート、のため?...
開示事項
The authors declare they have no competing financial interests.
謝辞
This work supported by research grant funding from the Natural Sciences and Engineering Research Council (NSERC) of Canada, the Ontario Institute for Cancer Research (OICR, #P.SI.015.8), and the Canadian Cancer Society (CCS, #703857). The authors acknowledge the contributions of Dr. Denis Snider who provided assistance in preparing the manuscript.
資料
| Name | Company | Catalog Number | Comments |
| Argon gas | Alphagaz | --- | --- |
| Na2CO3 | EMD Millipore | 106395 | --- |
| Na2B4O7·10H2O | Anachemia | S9640 | --- |
| KNaC4H4O6·4H2O | Anachemia | 217255 | --- |
| Technelite 99mTc generator | Lantheus medical imaging | --- | Source of 99mTcO4- |
| 0.9% Saline | Lantheus medical imaging | --- | To elute generator |
| 1 M HCl | Lab Chem | --- | --- |
| MeOH | Caledon | --- | --- |
| ACN | Caledon | --- | HPLC grade |
| Millipore H2O | Thermo Fisher Scientific | Barnstead Nanopure | --- |
| DCM | Caledon | --- | --- |
| TFA | Caledon | --- | --- |
| PBS | Thermo Fisher Scientific | 10010023 | pH 7.4 1x |
| BSA | Sigma Aldrich | A7906 | --- |
| Tween80 | Sigma Aldrich | P8047 | --- |
| Isoflurane | CDMV | 108737 | Supplier: Fresenius Kabi Animal Health |
| HPLC | Waters | 1525 Binary Pump, 2998 Photodiodde Array Detector, E-SAT/IN, Bioscan Flowcount PMT detector (item # 15590) | --- |
| HPLC column for analysis and purification of compounds 2-4 | Phenomenex | 00G-4435-E0 | Gemini® 5 µm C18 110 Å, LC Column 250 x 4.6 mm |
| HPLC column for analysis and purification of compounds 1 and 5 | Waters | 186003115 | XBridge BEH C18 Column, 130 Å, 5 µm, 4.6 mm x 100 mm |
| Microwave Reactor | Biotage | Initiator 8 | --- |
| Biotage V10 Evaporator | Biotage | Serial # V1041 | --- |
| Dose calibrator | Capintec, Inc. | CRC-25R | --- |
| Gamma counter | Perkin Elmer | Wizard 1470 Automatic Gamma Counter | --- |
| Animal room scale | Mettler Toledo | XP105 Delta Range | --- |
| Microwave vials | Biotage | 355629 | 0.5-2 mL |
参考文献
- Jurisson, S. S., Lydon, J. D. Potential Technetium Small Molecule Radiopharmaceuticals. Chem. Rev. 99 (9), 2205-2218 (1999).
- Kluba, C. A., Mindt, T. L. Click-to-chelate: Development of Technetium and Rhenium-Tricarbonyl Labeled Radiopharmaceuticals. Molecules. 18, 3206-3226 (2013).
- Amato, I. Nuclear Medicines Conundrum. Chem. Eng. News. 87 (36), 58-70 (2009).
- Hnatowich, D. J., Virzi, F., Rusckowski, M. Investigations of Avidin and Biotin for Imaging Applications. J. Nucl. Med. 28 (8), 1294-1302 (1987).
- Blackman, M. L., Royzen, M., Fox, J. M. Tetrazine Ligation: Fast Bioconjugation Based on Inverse-Electron-Demand Diels-Alder Reactivity. J. Am. Chem. Soc. 130 (41), 13518-13519 (2008).
- Devaraj, N. K., Weissleder, R., Hilderbrand, S. A. Tetrazine-Based Cycloadditions: Application to Pretargeted Live Cell Imaging. Bioconjugate Chem. 19 (12), 2297-2299 (2008).
- Rossin, R., et al. In Vivo Chemistry for Pretargeted Tumor Imaging in Live Mice. Angew. Chem., Int. Ed. 49 (19), 3375-3378 (2010).
- Zeglis, B. M., et al. Optimization of a Pretargeted Strategy for the PET Imaging of Colorectal Carcinoma via the Modulation of Radioligand Pharmacokinetics. Mol. Pharmaceutics. 12 (10), 3575-3587 (2015).
- Rossin, R., et al. Highly Reactive trans-Cyclooctene Tags with Improved Stability for Diels-Alder Chemistry in Living Systems. Bioconjugate Chem. 24 (7), 1210-1217 (2013).
- Rossin, R., Robillard, M. S. Pretargeted Imaging Using Bioorthogonal Chemistry in Mice. Curr. Opin. Chem. Biol. 21, 161-169 (2014).
- Denk, C., et al. Development of a 18F-Labeled Tetrazine with Favorable Pharmacokinetics for Bioorthogonal PET Imaging. Angew. Chem., Int. Ed. 53 (36), 9655-9659 (2014).
- Herth, M. M., Andersen, V. L., Lehel, S., Madsen, J., Knudsen, G. M., Kristensen, J. L. Development of a 11C-labeled Tetrazine for Rapid Tetrazine-Trans-Cyclooctene Ligation. Chem. Commun. 49 (36), 3805-3807 (2013).
- Li, Z., et al. Tetrazine-Trans-Cyclooctene Ligation for the Rapid Construction of 18F Labeled Probes. Chem. Commun. 46 (42), 8043 (2010).
- Nichols, B., Qin, Z., Yang, J., Vera, D. R., Devaraj, N. K. 68Ga Chelating Bioorthogonal Tetrazine Polymers for the Multistep Labeling of Cancer Biomarkers. Chem. Commun. 50 (40), 5215-5217 (2014).
- Zeglis, B. M., et al. A Pretargeted PET Imaging Strategy Based on Bioorthogonal Diels-Alder Click Chemistry. J. Nucl. Med. 54 (8), 1389-1396 (2013).
- García, M. F., et al. 99mTc-Bioorthogonal Click Chemistry Reagent for In Vivo Pretargeted Imaging. Bioorg. Med. Chem. 24 (6), 1209-1215 (2016).
- Russell, R. G. G. Bisphosphonates: The First 40 Years. Bone. 49 (1), 2-19 (2011).
- Yazdani, A., et al. A Bone-Seeking Trans-Cyclooctene for Pretargeting and Bioorthogonal Chemistry: A Proof of Concept Study Using 99mTc and 177Lu-Labeled Tetrazines. J. Med. Chem. , (2016).
- Alberto, R., et al. A Novel Organometallic Aqua Complex of Technetium for the Labeling of Biomolecules: Synthesis of [99mTc(OH2)3(CO)3]+ from [99mTcO4]- in Aqueous Solution and its Reaction with a Bifunctional Ligand. J. Am. Chem. Soc. 120 (31), 7987-7988 (1998).
- Alberto, R., Ortner, K., Wheatley, N., Schibli, R., Schubiger, A. P. Synthesis and properties of boranocarbonate: A convenient in situ CO source for the aqueous preparation of [99mTc(OH2)3(CO)3. J. Am. Chem. Soc. 123 (13), 3135-3136 (2001).
- Lu, G., et al. Synthesis and SAR of 99mTc/Re-labeled Small Molecule Prostate Specific Membrane Antigen Inhibitors with Novel Polar Chelates. Bioorg. Med. Chem. Lett. 23 (5), 1557-1563 (2013).
- Maresca, K. P., et al. Small Molecule Inhibitors of PSMA Incorporating Technetium-99m for Imaging Prostate Cancer: Effects of Chelate Design on Pharmacokinetics. Inorg. Chim. Acta. 389, 168-175 (2012).
- Bartholomä, M. D., et al. Insight into the Mode of Action of Re(CO)3 Thymidine Complexes. ChemMedChem. 5 (9), 1513-1529 (2010).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved