このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
点滅表面増強ラマン散乱の観測と解析
要約
このプロトコルを記述する点滅表面増強ラマン分析発電法を用いた銀表面の単一分子のランダム ・ ウォークによる散乱します。
要約
銀 nanoaggregate 接合部での単一分子から点滅表面増強ラマン散乱 (SERS) が観察されます。SERS 活性を準備する方法のプロトコルを表示するここでは、銀の nanoaggregate、顕微鏡画像の特定の点滅しているスポットのビデオを記録し、点滅の統計情報を分析します。この分析では、べき乗則はその期間を基準にして明るいイベントの確率分布を再現します。暗いイベントの確率分布は、指数関数との力法律によって取り付けられています。べき乗則のパラメーターは、明るいと暗い状態での分子の挙動を表します。ランダムウォーク モデルおよび銀表面全体に分子の速度を見積もることができます。それは平均、自己相関関数、および超解像 SERS のイメージングを使用する場合でもを見積もるは困難です。将来は、点滅の起源は、単独でこの分析法による確認ができないため電力法解析スペクトル イメージングを組み合わせる必要があります。
概要
表面増強ラマン散乱 (SERS) は、機密性の高い貴金属表面ラマン分光です。金属表面上の単一分子の情報を調べることができますラマン スペクトル、分子内の機能グループの振動モードを鋭いピークの位置に基づく分子の構造に関する詳細情報を提供しますのでSERS1,2,3を使用しています。分子レベルで吸着と銀 nanoaggregate から点滅信号が観察される1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16、およびスペクトル変動1,2,3,4,5,6,7,8、 9,10、11,12,13,14。点滅は、ナノサイズの銀 nanoaggregate ジャンクションで強化された電磁 (EM) フィールドがランダムに出入りする単一分子誘起することができます。したがって、点滅と、表面増強ラマン散乱強度および bi 検体2,3,17のポアソン分布を用いた手法と比較して、単一分子検出のための簡単な証拠と見なされます。ただし、Ag 表面上の分子の挙動に依存が強く、点滅と変動のスペクトルの詳細なメカニズムはまだ論争を呼びます。
従来、SERS の点滅が分析されて拡散係数と、強化された EM フィールド12,13,14 出入りする分子の濃度を計算することができます自己相関関数を使用して.さらに、全磁力の不安定性を表す、正規化された標準偏差のスコアは、信号15時間プロファイルから派生しています。ただし、これらの分析方法は、いくつかの分子の挙動に基づく可能性があります。対照的に、SERS の点滅の超解像イメージング、強化された電磁界での単一分子の挙動は、識別された16をすることができます。ただし、これらのテクニックは、強化された EM 分野のみでこのようなパラメーターを取得できます。平均4,5,6,7,8 よりもむしろ力法律として (例えば、SERS の点滅) の広い範囲での単一分子のランダムな動作を表現できます。 ,9,10,11, 半導体単一量子ドット (QD)18,19から点滅蛍光に似ています。電力法分析4,5,6,7,8,9,10,11, 分子の挙動を使用して(強化された電磁界) で明るい状態と暗い状態10; の両方に推定することができます。つまり、全体の銀表面上の分子の挙動を推定できます。
この技は、銀コロイド ハイパーラマンが使用される4,5,6,7,8,9,10,11。これらハイパーラマンは、ある特定の波長で興奮しているとき強く強化された電磁界に影響を与える各種の局在表面プラズモン共鳴 (LSPR) バンドを示します。したがって、SERS 活性銀ナノ粒子コロイド懸濁液といくつかのデータに存在するがすぐに得られます。単純なナノ構造、ある特定のサイズ、形状、および手配の場合点滅 SERS の LSPR の依存性は、他の依存の7; を隠すことができます。すなわち、LSPR に良し悪しのナノ構造を使用する場合、パラメーターは定数になります、他の依存したがって隠されています。銀コロイド ハイパーラマン4,5,6,7,8,から点滅 SERS の様々 な依存症を発見するパワー法解析が使用されています9,10,11。
プロトコル
1. サンプル準備
-
銀コロイドのナノ粒子の作製20
- 銀コロイドのナノ粒子を作製するには、0.030 g 硝酸銀と 0.030 g 200 mL 丸底フラスコに水 150 mL にクエン酸ナトリウム二水和物を溶かします。
- (ジムロート) 還流凝縮器とフラスコを組み合わせます。
- 磁気スターラー、攪拌棒でフラスコ内でソリューションをかき混ぜます。60 分 150 ° C で油浴中でフラスコの攪拌溶液を熱し。
注: ソリューションは、黄色、乳白色、グレーになります。 - 室内の温度の懸濁液を冷却し、冷蔵庫にアルミ箔で覆われたフラスコの懸濁液を維持します。
注: プロトコルをこの時点で一時停止できます。コロイド状ナノ粒子を使用して、1 ヶ月以内、冷蔵庫で保存した後。
-
マルチカラーのサンプルの調製点滅発光11
- 顕微鏡のスライドを準備ができて、石鹸でガラス板を手で洗って水ですすいでください。
- ガラス板に 0.1% ポリ L リジン水溶液を追加し、送風機とソリューションを削除します。
- ガラス板に銀コロイド懸濁液を追加および送風機を懸濁液を削除します。
- 液体ブロッカー ペンでガラス板のドロップ領域を囲みます。
- ガラス板に蒸留水をドロップし、顕微鏡スライドを作成し、水が蒸発するを防ぐ別のガラス板でそれをカバーします。
-
単調な色点滅 SERS のサンプルの調製7,8,9,10
- 顕微鏡のスライドを準備ができて、石鹸でガラス板を手で洗って水ですすいでください。
- 銀コロイド懸濁液の thiacyanine または thiacarbocyanine の色素を混ぜて (25 または 4 μ M、それぞれ)、塩化ナトリウム (10 mM) の水溶液 2 の容積比で: 1:1。
- ガラス プレート上にサンプル サスペンションをドロップし、送風機とサスペンションを削除します。
- 液体ブロッカー ペンでガラス板のドロップ領域を囲みます。
- 銀ナノ粒子を固定化するガラス板に塩化ナトリウム (1 M) の水溶液をドロップし、顕微鏡スライド プレートを作成し、ソリューションを蒸発から防ぐために、別のガラス板でそれをカバーします。
2. 点滅銀ナノ粒子の観察
-
サンプルの照明
- 倒立顕微鏡のステージ上の 1.2 または 1.3 プロトコルを使用したサンプルのガラス プレートを配置します。
- 様々 な色の斑点 (青、緑、黄、および赤) 対物レンズ (60 X) を使用してガラス板上に暗視野コンデンサーとフォーカスを白色光を使用してサンプルのガラス プレートを照らします。
- ダイオード励起固体 (DPSS) 連続波 (cw) レーザー干渉フィルターを通してから試料表面に対して 30 ° の角度で配信、弱毒ビームを用いたサンプル ガラス板を照らします。
- 周辺の同じ色に単調な色の斑点として銀ハイパーラマンを観察するレーザ光を照射して、レーザー照射面積をビューの中央に移動、z 方向の段階を調整することによってガラス プレート上のスポットに焦点を当てます。
-
点滅の観察
- ロングパス ・ フィルターを対物レンズの後に挿入し、試料表面に対して 30 ° の角度で干渉フィルターを通して配信 DPSS cw レーザー光を用いたサンプル ガラス板を照らします。
- 図 1に示すように、点滅してスポットを見つける (また見なさい図 S1補足資料で) x 方向と y 方向でステージを移動することによって。
- 20 分間の 61-120 ms の時間分解能を持っている冷却デジタル電荷結合素子 (CCD) カメラに結合、倒立顕微鏡で点滅している地点のビデオを記録します。
3 点滅表面増強ラマン散乱の解析
-
時間プロフィール ビデオからの導出
- CCD カメラを制御するソフトウェア、ビデオのファイルを開きます。
- 点滅スポット、暗い領域を選択すると、別にビデオ イメージのスポットとの領域をカバーする領域をドラッグします。
- 点滅スポットやビデオの暗い部分から信号強度の時間分布を導出するには、分析、時系列解析を選択し、時系列解析] ウィンドウで[計算] をクリックします。
- テキスト ファイルとしてデータを保存します。
-
時間プロファイルの解析
- 時間プロファイルのベースラインは、暗い領域および/または図 2 aと2 bに示すように、多項式関数でフィッティングから時間プロファイルを引いて平らにします。
- 図 2と2 Dに示すように約 2000 点、私基本基準強度の標準偏差は、σ, から成る平均基準強度を評価します。
- 私基本+ 3 σ、しきい値よりも大きい強度を使用してイベントを暗いから明るいイベントを区別し、各イベントの存続期間を記録します。図 3、たとえば、3.5476 を 0 からイベント記録暗いイベントとして s (持続時間t = 3.5476 s)、4.0981 に 3.5476 からイベントを記録および明るいイベントとして s (持続時間t = 0.5505 s)。表 1に示すように、手順を繰り返します。
- 表 2の最初と 2 番目の行で表さ各期間の明るい部分と暗いイベントの数をカウントします。
- 期間tよりも短い間隔でイベントを除いて、各期間のイベントの数を合計します。各期間のイベントの数をたとえば、合計表 2の 2 番目と 3 番目の行に示された、( tのイベントを除いて 0.0612 = s) 41 + 18 + 9 +...;その結果tの総和に等しい = 0.1223 s、すなわち103。
- 各期間合計で割ります、正規化します。表 2に示された、たとえば、分割期間tの合計 = 0.0612 期間 0.0612 s で s。結果は 3,351.5791 です。次に、表 2の 4 行目の結果の合計で結果を分割します。確率分布は、0.64494 に派生します。
- 明るいイベントP、上(t) 対数-対数グラフで自分の時間tに対して確率分布をプロットし、ログ10Pの(t)10 のログ(
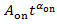 )、電源法指数 αに特定のスポットで点滅を推測します。Pの(t) が取り付けられている場合
)、電源法指数 αに特定のスポットで点滅を推測します。Pの(t) が取り付けられている場合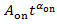 、近似直線は、図 4Aの点線で示すように、 Pの(t) の小さな値でプロットから逸脱。
、近似直線は、図 4Aの点線で示すように、 Pの(t) の小さな値でプロットから逸脱。 - 暗いイベントPオフ(t) 対数-対数グラフではtの期間に対する確率分布をプロットし、ログ10(ログ10Pから(t) に合わせてください
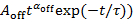 電源法指数 α のオフと、切り捨て時間τ同じ点滅からスポットを推測します。Pオフ(t) が取り付けられている場合
電源法指数 α のオフと、切り捨て時間τ同じ点滅からスポットを推測します。Pオフ(t) が取り付けられている場合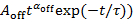 、 Pオフ(t) の小さな値でプロットから逸脱する近似曲線。
、 Pオフ(t) の小さな値でプロットから逸脱する近似曲線。 - ビデオで他の点滅しているスポットを 3.2.1 に 3.2.8 を繰り返します。
結果
プロトコル 1.2 により作製したポリ L リジンと銀のハイパーラマンからは、 1 図11に示すように SERS と表面増強蛍光から色とりどりの点滅しているスポットを観察します。対照的に、表面増強ラマン散乱から単調な色の点滅の斑点は、プロトコル 1.37,8,9,
ディスカッション
銀 nanoaggregate ジャンクションからセールが出力されます。したがって、我々 はコロイド状ナノ粒子、クエン酸アニオンで覆われているよりもむしろハイパーラマンを準備する必要。銀の集計は、ポリ-L-リジン、NH3+し、サールの起源の付加によって作成されるエフェクトを塩漬けから形成されているまたは塩化ナトリウム、補足資料の図 S2のようにから Na+
開示事項
著者は、何を開示します。
謝辞
著者は、この作品の実りある議論するため尾崎幸洋教授 (関西学院大学)、伊藤哲夫博士 (国立科学研究所の高度な産業と技術) をありがちましょう。この作業は、教育省、文化、スポーツ、科学および技術 (第 16 K 05671) から科研費 (費補助金科学研究 C) によって支えられました。
資料
| Name | Company | Catalog Number | Comments |
| Silver nitrate, 99.8% | Wako | 194-00832 | |
| Trisodium citrate dihydrate, 99. % | Wako | 191-01785 | |
| Poly-L-lysine aqueous solution, 0.1% | Sigma-Aldrich | P8920 | |
| 3,3'-disulfopropylthiacyanine triethylamine | Hayashibara Biochemical Laboratories | NK-2703 | a kind of thiacyanine dyes |
| 3,3'-diethyl-5,5'-dichloro-9-methylthiacarbocyanine iodine salt | Hayashibara Biochemical Laboratories | SMP-9 | a kind of thiacarobocyanine dyes |
| Sodium chloride, 99.5% | Wako | 191-01665 | |
| Dimroth condenser | Iwaki | 61-9722-22 | perchased from AS ONE |
| Magnetic stirrer | Corning | DC-420D | |
| Oil bath | Advantech | OS-220 | |
| Glass plate | Matsunami | S-1112 | Microscope slide |
| Blower | Hozan | Z-288 | Air duster |
| Liquid blocker pen | Daido Sangyo | LIQUID BLOCKER (Super Pap Pen). Ready-to-use hydrophobic barrier pen designed for immunohistochemistry applications | |
| Inverted microscope | Olympus | IX-70 | |
| Objective lens | Olympus | LCPlanFl 60× | NA 0.7 |
| Dark field condenser | Olympus | U-DCD | NA 0.8–0.92 |
| Cooled digital CCD camera | Hamamatsu | ORCA-AG | controlled by software Aqua Cosmos |
| Software for the cooled digital CCD camera | Hamamatsu | AquaCosmos | used for also derivation of the time-profiles from the blinking spots in the video |
| Color CCD camera | ELMO | TNC-C920 | not used for analysis |
| DPSS laser | RGB laser system | NovaPro532-75 | λ = 532 nm; 60 mW (corresponds to a power density of 600 W/cm2) |
| Interference filter | Semrock | LL01-532-12.5 | |
| Long pass filter | Semrock | BLP01-532R-25 | |
| Software for the distinguishment and counting of the bright/dark events | home-maid | programmed by C++ | |
| Software for the fitting by a power law | LightStone | Origin6.1 |
参考文献
- Qian, X. M., Nie, S. M. Single-molecule and single-nanoparticle SERS: from fundamental mechanisms to biomedical applications. Chem. Soc. Rev. 37, 912-920 (2008).
- Pieczonka, N. P. W., Aroca, R. F. Single molecule analysis by surfaced-enhanced Raman scattering. Chem. Soc. Rev. 37, 946-954 (2008).
- Kneipp, J., Kneipp, H., Kneipp, K. SERS -a single-molecule and nanoscale tool for bioanalytics. Chem. Soc. Rev. 37, 1052-1060 (2008).
- Kitahama, Y., Ozaki, Y. Analysis of blinking SERS by a power law with an exponential function. Frontiers of Surface-Enhanced Raman Scattering: Single-Nanoparticles and Single Cells. , (2014).
- Kitahama, Y. Truncated Power Law Analysis of Blinking SERS. Frontiers of Plasmon Enhanced Spectroscopy Volume 1 (ACS Symposium series Vol. 1245). , (2016).
- Bizzarri, A. R., Cannistraro, S. Lévy Statistics of Vibrational Mode Fluctuations of Single Molecules from Surface-Enhanced Raman Scattering. Phys. Rev. Lett. 94, 068303 (2005).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Power-law analysis of surface-plasmon-enhanced electromagnetic field dependence of blinking SERS of thiacyanine or thiacarbocyanine adsorbed on single silver nanoaggregates. Phys. Chem. Chem. Phys. 13, 7439-7448 (2011).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of excitation laser intensity dependence of blinking SERRS of thiacarbocyanine adsorbed on single silver nanoaggregates by using a power law with an exponential function. Chem. Commun. 47, 3888-3890 (2011).
- Kitahama, Y., Enogaki, A., Tanaka, Y., Itoh, T., Ozaki, Y. Truncated power law analysis of blinking SERS of thiacyanine molecules adsorbed on single silver nanoaggregates by excitation at various wavelengths. J. Phys. Chem. C. 117, 9397-9403 (2013).
- Kitahama, Y., Araki, D., Yamamoto, Y. S., Itoh, T., Ozaki, Y. Different behaviour of molecules in dark SERS state on colloidal Ag nanoparticles estimated by truncated power law analysis of blinking SERS. Phys. Chem. Chem. Phys. 17, 21204-21210 (2015).
- Kitahama, Y., Nagahiro, T., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of blinking from multicoloured SERS-active Ag colloidal nanoaggregates with poly-L-lysine via truncated power law. J. Raman. Spectrosc. 48, 570-577 (2017).
- Habuchi, S., et al. Single-Molecule Surface Enhanced Resonance Raman Spectroscopy of the Enhanced Green Fluorescent Protein. J. Am. Chem. Soc. 125, 8446-8447 (2003).
- Weiss, A., Haran, G. Time-Dependent Single-Molecule Raman Scattering as a Probe of Surface Dynamics. J. Phys. Chem. B. 105, 12348-12354 (2001).
- Emory, S. R., Jensen, R. A., Wenda, T., Han, M., Nie, S. Re-examining the origins of spectral blinking in single-molecule and single-nanoparticle SERS. Faraday Discuss. 132, 249-259 (2006).
- Itoh, T., Iga, M., Tamaru, H., Yoshida, K., Biju, V., Ishikawa, M. Quantitative evaluation of blinking in surface enhanced resonance Raman scattering and fluorescence by electromagnetic mechanism. J. Chem. Phys. 136, 024703 (2012).
- Willets, K. A. Super-resolution imaging of SERS hot spots. Chem. Soc. Rev. 43, 3854-3864 (2014).
- Dieringer, J. A., Lettan, R. B., Scheidt, K. A., Van Duyne, R. P. A Frequency Domain Existence Proof of Single-Molecule Surface-Enhanced Raman Spectroscopy. J. Am. Chem. Soc. 129, 16249-16256 (2007).
- Cichos, F., von Borczyskowski, C., Orrit, M. Power-law intermittency of single emitters. Curr. Opin. Colloid Interface Sci. 12, 272-284 (2007).
- Tang, J., Marcus, R. A. Mechanisms of fluorescence blinking in semiconductor nanocrystal quantum dots. J. Chem. Phys. 123, 054704 (2005).
- Lee, P. C., Meisel, D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J. Phys. Chem. 86, 3391-3395 (1982).
- Krichevsky, O., Bonnet, G. Fluorescence correlation spectroscopy: the technique and its applications. Rep. Prog. Phys. 65, 251-297 (2002).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and Chemical Applications of Fluorescence Correlation Spectroscopy: A Review. Biochemistry. 41, 697-705 (2002).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved