JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
힘에 민감한 요소에 대한 나노 역학 측정을 위한 고속 자기 핀셋
* 이 저자들은 동등하게 기여했습니다
요약
여기에서는 최대 1.2kHz의 속도로 힘에 민감한 생체 분자에 대한 나노기계적 측정을 수행하는 고속 자기 핀셋 설정에 대해 설명합니다. 우리는 모델 시스템으로 DNA 헤어핀과 SNARE 복합체에 대한 적용을 소개하지만 기계 생물학적 사건에 관여하는 다른 분자에도 적용 할 수 있습니다.
초록
단일 분자 자기 핀셋(MT)은 핵산 및 단백질과 같은 생체 분자를 강력하게 조사하는 강력한 도구 역할을 하므로 기계 생물학 분야에서 유용할 태세입니다. 이 방법은 일반적으로 마그네틱 비드의 이미지 기반 추적에 의존하기 때문에 이미지 기록 및 분석의 속도 제한과 비드의 열 변동으로 인해 표적 분자의 작고 빠른 구조적 변화를 관찰하는 데 오랫동안 적용이 방해를 받았습니다. 이 글에서는 생체 분자 및 그 복합체의 나노 단위, 밀리초 역학을 해결할 수 있는 고분해능 MT 설정의 구성 및 작동에 대한 자세한 방법을 설명합니다. 응용 사례로서, DNA 헤어핀과 SNARE 복합체 (막 융합 기계)를 사용한 실험이 시연되며, 피코 네톤 규모의 힘이있을 때 일시적인 상태와 전이를 어떻게 감지 할 수 있는지에 초점을 맞 춥니 다. 우리는 고속 MT가 세포에서 힘을 감지, 전송 및 생성하는 분자에 대한 고정밀 나노 역학 측정을 계속 가능하게 하여 기계 생물학에 대한 분자 수준의 이해를 심화할 것으로 기대합니다.
서문
세포는 기계적 자극을 능동적으로 감지하고 반응합니다. 그렇게 함으로써 많은 생체 분자는 역동적인 구조적 변화를 가능하게 하는 힘 의존적 특성을 나타냅니다. 잘 알려진 예로는 세포에 주변 환경의 주요 기계적 정보를 제공하는 기계에 민감한 이온 채널과 세포골격 요소가 있습니다.
또한, 독특한 힘을 지닌 성질을 나타내는 분자는 더 넓은 의미에서 기계에 민감한 것으로 간주 될 수 있습니다. 예를 들어, 핵산 이중가닥의 국소 형성 및 용융뿐만 아니라 G-사중가닥과 같은 고차 구조는 복제, 전사, 재조합, 그리고 최근에는 게놈 편집에서 중요한 역할을 합니다. 또한, 시냅스 통신에 관여하는 일부 신경 단백질은 일반적인 분자간 상호 작용 수준을 초과하는 물리적 힘을 생성하여 기능을 수행합니다. 어떤 예를 연구하든, 높은 시공간 정밀도로 관련된 생체 분자의 나노 역학을 조사하는 것은 관련 기계 생물학적 과정 1,2,3의 분자 메커니즘을 밝히는 데 매우 유용하다는 것을 증명할 것입니다.
단일분자 힘 분광법은 생체분자 2,4,5,6의 기계적 성질을 조사하는 강력한 도구로 사용되어 왔다. 그들은 힘의 적용과 동시에 핵산과 단백질의 구조적 변화를 모니터링하여 힘 의존적 특성을 조사할 수 있습니다. 잘 알려진 두 가지 설정은 광학 핀셋과 자기 핀셋(MT)으로, 미크론 크기의 비드를 사용하여 분자 5,6,7,8을 조작합니다. 이러한 플랫폼에서 폴리스티렌(광학 핀셋용) 또는 마그네틱 비드(MT용)는 일반적으로 이중 가닥 DNA(dsDNA)의 짧은 단편으로 구성된 분자 "핸들"을 통해 표적 분자(예: 핵산 및 단백질)에 연결됩니다. 그런 다음 비드를 움직여 힘을 가하고 이미지를 작성하여 표적 분자의 구조적 변화를 보고하는 위치를 추적합니다. 광학 핀셋과 자기 핀셋은 응용 분야에서 크게 상호 교환할 수 있지만 힘을 제어하는 접근 방식에는 중요한 차이점이 있습니다. 광학 핀셋은 본질적으로 비드를 제자리에 가두는 위치 클램프 도구로, 대상 구조물이 모양 변화를 겪을 때 가해지는 힘이 변동하기 때문입니다. 펼침과 같은 확장 증가는 밧줄을 느슨하게 하고 장력을 감소시키며 그 반대의 경우도 마찬가지입니다. 광학 핀셋의 힘을 제어하기 위해 능동 피드백을 구현할 수 있지만, MT는 환경 섭동에도 견딜 수 있는 영구 자석에 의한 안정적인 원거리 자기력을 활용하여 자연스럽게 힘 클램프 장치로 작동합니다.
오랜 역사와 단순한 설계에도 불구하고 MT는 고속 비드 추적의 기술적 문제로 인해 고정밀 측정에 대한 응용 분야에서 광학 핀셋에 비해 뒤쳐져 있습니다. 그러나 최근 여러 그룹이 공동으로 MT 기기 2,9,10,11,12,13,14,15,16,17,18,19의 하드웨어와 소프트웨어의 다각적인 개선을 주도하고 있습니다 . 이 연구에서는 1.2kHz에서 실행되는 이러한 설정의 예를 소개하고 이를 사용하여 힘에 민감한 생체 분자에 대한 나노역학적 측정을 수행하는 방법을 설명합니다. 모델 시스템으로서 우리는 DNA 헤어핀과 뉴런 SNARE 복합체를 사용하고 피코네톤 체계에서 빠르고 구조적인 변화를 조사합니다. DNA 헤어핀은 잘 정의된 힘 범위20,21에서 간단한 2-상태 전이를 나타내므로 핀셋 설정의 성능을 검증하기 위한 장난감 모델 역할을 합니다. SNARE 단백질이 막 융합을 구동하는 힘에 민감한 복합체로 조립됨에 따라(22), 이들은 또한 단분자 힘 분광법(single-molecule force spectroscopy)에 의해 광범위하게 연구되었다 14,23,24,25. 데이터를 분석하고 열역학 및 동역학에 대한 유용한 정보를 추출하는 표준 접근 방식이 제시됩니다. 우리는 이 기사가 기계생물학 연구에서 고정밀 MT의 채택을 촉진하고 독자들이 자신의 힘에 민감한 관심 시스템을 탐색하도록 동기를 부여할 수 있기를 바랍니다.
프로토콜
이 프로토콜에 설명 된 모든 재료와 장비는 재료 표에 나열되어 있습니다. 아래에 설명된 고속 MT 설정을 작동하기 위한 LabVIEW 소프트웨어와 샘플 데이터를 분석하기 위한 MATLAB 스크립트는 GitHub (https://github.com/ShonLab/Magnetic-Tweezers)에 보관되어 공개적으로 사용할 수 있습니다.
1. 장치의 구성
참고: 고속 MT 구조의 일반적인 원리는 고속 CMOS(Complementary Metal Oxide Semiconductor) 카메라와 고출력 코히어런트 광원을 사용한다는 점을 제외하면 기존의 표준 MT 시스템과 유사합니다(그림 1). 표준 MT 기기 5,26,27에 대한 자세한 설명은 다른 출처를 참조하십시오.
- 진동 방지 광학 테이블에 도립 현미경을 설치합니다. 고속 CMOS 카메라와 프레임 그래버를 설치합니다.
- 자석을 3D로 조작하기 위한 변환 스테이지를 구축합니다. 전동 리니어 스테이지 장착(>20mm 트래블) 수동 XY s 위에 수직으로 stag이자형.
알림: 수직 이동은 힘을 제어하는 반면 XY stage는 설정의 초기 구성을 위해 자석을 광축에 수동으로 정렬하기 위한 것입니다. - 회전식 스테퍼 모터와 회전 자석용 벨트 및 풀리 시스템을 설치합니다.
알림: 벨트는 모터 샤프트와 몇 센티미터 떨어진 자석 사이의 회전 운동을 전달합니다. 자석의 회전은 병진 조작 내부에 있습니다. - 자석을 장착합니다. 자석 사이에 1mm의 간격이 잘 정의된 두 개의 동일한 자석을 병렬로 단단히 고정할 수 있는 아크릴 홀더(제조 회사에서 주문, 보충 그림 S1 참조)를 사용합니다(그림 1B). 주어진 한 쌍의 자석으로 얻을 수 있는 최대 힘을 활용하려면 병진 단계의 수직 위치를 조정하여 자석이 가장 낮은 위치로 이동할 때 샘플 평면과 정렬되도록 합니다.
알림: Lipfert et al. 자석28의 홀더 설계 및 구성에 대한 자세한 내용은 자석의 높이와 방향은 데이터 수집과 함께 LabVIEW 소프트웨어에 의해 제어됩니다. - View저배율 대물 렌즈로 자석을 시야의 중심에 맞춥니다. 자석을 회전시켜도 자석 쌍의 중심이 크게 변위되지 않는지 확인하십시오.
알림: 자석 사이의 중간점이 회전축을 중심으로 회전하면 불완전한 홀더로 인해 자석이 중심에서 벗어날 수 있습니다. 갭 크기에 비해 작은 수준의 정렬 불량은 자석 회전이 특정 응용 분야에서 밧줄을 확인하고 토크를 적용하기 위한 것이기 때문에 견딜 수 있습니다. - 비드 조명을 위한 초발광 다이오드(SLD)를 설치합니다. 두 자석 사이의 1mm 간격을 통해 빔을 통과시킵니다. 빔이 간격에 맞도록 적절하게 시준되고 조명이 자석에 의해 가려지지 않는지 확인하십시오.
- 노즈피스에 피에조 렌즈 스캐너를 설치하고 비드 트래킹을 위해 100x 오일 이멀젼 대물 렌즈(개구수[NA]: 1.45)를 장착합니다. 추적 결과에서 아티팩트가 발생할 수 있는 가능성을 방지하려면 자석을 움직일 때 조명이 균일하게 유지되는지 확인합니다. 마지막으로 픽셀을 포화시키지 않고 조명 수준을 최대 밝기로 조정합니다.
참고: 비드의 고속 추적을 위한 다양한 광원의 비교는 Dulin et al.29를 참조하십시오.
2. 자기력의 교정
- 중합효소연쇄반응(PCR; 표 1 참조)을 사용하여 한쪽 끝(표면 부착용)에 비오틴(표면 부착용)으로 표지되고 다른 쪽 끝(비드 부착용)에 아지드로 표지된 5kbp dsDNA 단편(프라이머 B, 프라이머 Z_5k 및 λ-DNA 사용)을 준비합니다.
- 섹션 6에 이어, 5 kbp 분자를 갖는 유동 셀을 준비한다.
- 섹션 7에 따라 확장 및 회전을 확인하여 좋은 비드-테더 구조를 식별합니다. 특히, 중심에서 벗어난 부착물(30, 31)로 인한 비드 높이 오프셋을 최소화하기 위해 최소 회전 궤적(즉, 반경 <200nm)을 갖는 비드를 선택해야 합니다. 좋은 밧줄이 확인되면 섹션 9를 참조하여 비드 추적을 시작합니다.
- 설정이 새로운 경우 신뢰할 수 있는 고분해능 측정을 위해 노이즈와 안정성을 특성화하십시오. 유동 셀 표면에서 ~3mm 떨어진 곳에 자석을 배치하고(>10pN을 적용하고 비드의 브라운 운동을 억제하기 위해), 1.2kHz에서 비드의 z 위치를 추적하고, z 좌표 시계열32,33에서 앨런 편차(AD)를 계산합니다(그림 2C). 고속 영역(<0.1초)에서 수 나노미터의 AD 값을 달성할 수 있는지, 차등 추적(기준 비드에 대한 자기 비드 위치)이 더 긴 시간 척도에서 AD를 감소시키는지 확인합니다.
참고: 일반적으로 최대 속도(1.2kHz 또는 0.83ms 분해능)에서 <3nm의 AD를 얻으며 AD는 최소 10초까지 계속 감소하여 최소 드리프트를 의미합니다. 다른 사람들은 유사한 설정 9,10,11,12,34에서 유사한 값을 보고했습니다. - 정지 위치(F ~ 0pN)에 자석을 두고 테더링된 비드의 x 및 y 좌표를 1.2kHz로 기록합니다. 충분히 긴 기간 동안(즉, 변동의 특징적인 이완 시간(35)보다 충분히 긴) 위치를 기록하여, 브라운 운동이 충분히 샘플링되도록 한다.
참고: 여기서 x 방향은 자기장의 방향을 따르는 반면 y 의 움직임은 자기장에 수직인 횡방향 운동을 나타냅니다. - 자석을 플로우 셀에 더 가깝게 이동하고 자석이 플로우 셀의 상단에 부드럽게 닿을 때까지 비드 위치 측정을 반복합니다. 자석이 샘플 평면에서 7mm 이상 떨어져 있을 때 큰 단계(예: 1-2mm)로 이동하지만(적용된 힘은 자석의 원거리 필드에서 천천히 증가하기 때문에) 더 높은 힘 수준에서 더 미세한 보정을 위해 가까이 접근함에 따라 스텝 크기를 점진적으로(예: 0.1-0.5mm) 줄입니다(그림 2B).
- 두 가지 대체 방법 중 하나를 사용하여 각 자석 위치 d에서의 힘을 계산합니다(두 방법을 모두 포함하는 MATLAB 스크립트 "force calibration.m"이 제공됨, 보충 파일 1 참조).
- 비드의 y 좌표
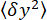 (그림 2D)의 분산과 가장 낮은 위치에 대한 비드의 평균 z-위치
(그림 2D)의 분산과 가장 낮은 위치에 대한 비드의 평균 z-위치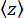 (그림 2B, 하단)를 측정합니다. 그런 다음 방정식 (1)7,27,36을 사용하여 힘을 추정합니다(고정 비드 반경 R = 1,400nm 및 열 에너지 k RT = 4.11pN∙nm).
(그림 2B, 하단)를 측정합니다. 그런 다음 방정식 (1)7,27,36을 사용하여 힘을 추정합니다(고정 비드 반경 R = 1,400nm 및 열 에너지 k RT = 4.11pN∙nm).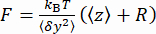 (1개)
(1개) - 또는 y 좌표 Sy의 전력 스펙트럼 밀도(PSD)를 계산합니다(그림 2E). 이중 로렌치안 모델(37)을 식 (2)를 사용하여 측정된 Sy에 피팅함으로써 인가된 힘 F를 결정한다.
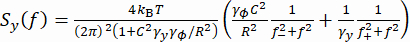 (2개)
(2개)
여기서, R은 비드 반경, γy및 γ φ는 각각 병진 및 회전 항력 계수(스톡스-아인슈타인 방정식으로부터 추정)이고, kRT는 열에너지 이고,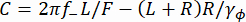 f+ 및 f-는 수학식 3을 사용하여 구한 두 가지 특성 주파수이다.
f+ 및 f-는 수학식 3을 사용하여 구한 두 가지 특성 주파수이다.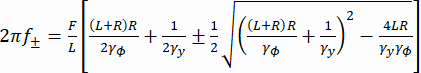 (3)
(3)
참고: 테더 확장 L은 잘 확립된 WLC(worm-like chain) 모델을 따르는 힘의 함수이므로 위의 표현식은 F를 유일한 피팅 매개변수로 남겨둡니다(모든 힘 수준에서 공유되고 정확한 값이 결과에 상당한 영향을 미치지 않기 때문에 단순화를 위해 R을 1,400nm로 고정합니다). 필요한 경우 카메라 기반 이미지 획득으로 인한 모션 블러 및 앨리어싱은38,39로 간주되어야 하지만 이 효과는 1kbp 테더를 사용한 5kHz 이상의 고속 측정에서는 무시할 수 있습니다.
- 비드의 y 좌표
- 몇 가지 구문에 대해 2.4-2.7단계를 반복합니다. 3-5개의 서로 다른 비드를 조사하여 마그네틱 비드 간의 힘 변동성을 평균화합니다.
알림: 평균화를 위한 적절한 구성 수를 결정하기 위해 사용 중인 마그네틱 비드 간의 힘 변화를 고려해야 합니다. 이러한 가변성은 작지만, 측정된 힘에서 1 pN 이상의 오차를 야기할 수 있으며, 이는 상용 제품(31)에 대해서도. 관련된 힘의 절대적인 측정이 중요하지 않은 대부분의 응용 분야에서는 일반적으로 3-5개의 비드의 보정 결과를 평균화하는 것으로 충분합니다. 이러한 변동을 설명하는 또 다른 방법은 실험 시작 시 개별 밧줄로 힘을 측정하는 것인데, 이는 시간이 많이 소요될 수 있습니다. 또 다른 옵션은 각각의 구조물(31)에 알려진 힘 레벨에서 지퍼를 풀지 않는 헤어핀 구조물을 매립하는 것이다. - 측정된 힘을 자석 거리의 함수로 플로팅하고 방정식 4를 사용하여 데이터(그림 2F)에 이중 지수 함수를 맞춥니다.
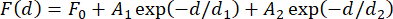 (4개)
(4개)
여기서, F0 (기준선), A1 및 A2 (진폭), d 1 및 d2 (감 쇠 상수)는 피팅 파라미터이다. 두 방법의 힘 값과 그에 따른 이중 지수 피팅이 대체로 일치하는지 확인합니다(그림 2F,G).
알림: 힘 보정이 제대로 수행되었는지 확인하려면 측정된 힘에 대한 확장을 플로팅하여 프로브된 구조의 힘-확장 관계를 확인합니다. - 자기 비드(30, 31)의 힘-의존적 틸팅으로부터 발생하는 비드 높이 오프셋 zoff를 보정하기 위해, 방정식 (5)를 사용하여 비드 반경을 갖는 중심에서 벗어난 테더의 기하학적 구조를 고려하여, 측면 오프셋xoff로부터 zoff를 추정하고, 측정된 연장 값들에 값들을 적용한다. 이 단계는 MATLAB 스크립트 "force calibration.m"(252-254행)에서 구현됩니다.
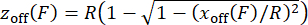 (5개)
(5개)
참고: 이 보정은 특히 회전 반경이 작은 비드(<200nm)의 경우 확장에 약간의 변화를 주지만, 이 오프셋은 그림 2H에서 그림 2I(30,31)로의 변경에서 볼 수 있듯이 종종 탄성 응답에 결정적인 영향을 미칩니다. - 방정식 (6)을 사용하여 확장 가능한 WLC 모델을 데이터에 피팅하여 지속성 길이 Lp를 확인합니다.
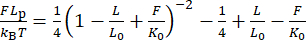 (6개)
(6개)
여기서, L0는 윤곽 길이(5kbp에 대해 1.7μm)이고 K0는 엔탈피 스트레칭에 대한 모듈러스입니다.
참고: dsDNA의 Lp는 인산염 완충 식염수(PBS)와 같은 일반적인 완충액에서 40-50nm로 잘 받아들여지지만, 짧은 분자(<5kbp)에 적용된 WLC 공식은 L0이31,40 감소함에 따라 체계적으로 Lp를 과소평가합니다. 이는 기존 WLC 모델이 체인 길이가 지속성 길이보다 충분히 긴 폴리머를 가정하기 때문입니다. 여기서, 본 발명자들은 5 kbp 구축물에 대해 Lp = 40 ± 3 nm를 얻었고(도 2H), 연장 보정은 추가로 1,100 ± 200 pN의 균질한 K0를 산출하였다(도 2I). 유한 WLC 모델(31, 40)을 적용하고, 확장 분포(41)에서 비-가우시안성에 대한 보정을 적용하면, Lp가 약간 증가할 것이다. - 힘 교정이 확인되면, 이중 지수 모델의 피팅 파라미터를 제공된 LabVIEW 소프트웨어 (보충 파일 2)에 적용하고 소프트웨어가 모터 판독값 (즉, 자석 위치)에서 실시간으로 현재 힘을 계산할 때까지 기다립니다. 역함수 d(F)에 대한 해석 표현식을 사용할 수 없으므로 d 목표 하중 수준에 대한 수치 추정을 통해 0.1pN 단계에서 d 대 F의 룩업 테이블을 준비합니다. 이 테이블을 소프트웨어에 저장하여 강제 제어를 명령하십시오.
3. DNA 헤어핀의 합성
참고: MT 실험을 위한 DNA 헤어핀 구조는 두 개의 맞춤형 프라이머를 사용하여 λ-DNA에서 510bp 영역의 PCR 증폭에 의해 준비되며, 그 중 하나는 5′-말단에 헤어핀 구조를 포함합니다(그림 3A). 이러한 방식으로, 헤어핀 모티프가 PCR 산물의 한쪽 끝에 배치된다.
- 프라이머를 준비하십시오.
- 순방향 프라이머: 유리 표면 부착을 위해 5′-비오틴 표지되고 λ-DNA에 결합하는 프라이머 B_hp. 이 프라이머는 8bp 스템과 λ-결합 영역에 5'인 6nt 루프가 있는 헤어핀 모티프를 포함합니다.
- 역방향 프라이머: 마그네틱 비드 부착을 위해 5′-아지드 표지되고 정방향 프라이머에서 1kbp 떨어진 λ-DNA에 결합하는 프라이머 Z_hp.
- λ-DNA(주형), nTaq 중합효소 및 표준 PCR 조건으로 PCR을 설정하고 실행합니다( 표 1 참조). 상업용 정화 키트로 제품을 청소하십시오.
- 260 nm(A260)에서 UV 흡수로 DNA 농도를 측정하고 아가로스 겔 전기영동(2% gel)( 표 2 참조)을 수행하여 생성물 크기를 검증하였다. 일반적인 수율은 ~600nM 용액의 ~35μL입니다.
4. SNARE 단백질의 제조
참고: 신경 SNARE 복합체는 대장균에서 발현된 세 가지 정제된 쥐 단백질인 VAMP2/synaptobrevin-2, syntaxin-1A 및 SNAP-25를 결합하여 조립됩니다(그림 3B). 이들의 조립을 용이하게 하기 위해 신택신과 SNAP-25는 VAMP2 단편(N-말단 영역이 없음, "ΔN-VAMP2"라고 함)과 함께 "ΔN-복합체"라고 하는 구조로 공동 발현된 다음 DNA 핸들 부착 후 전장 VAMP2와 혼합되어 전체 복합체를 형성합니다.
- SNARE 단백질의 발현을 위해 cDNA를 함유하는 플라스미드를 준비한다 (모든 플라스미드에 대한 DNA 서열은 물질 표에 제시되어 있다).
- 막횡단 도메인이 결여된 6×His-tagged VAMP2를 제조한다(2-97; L32C/I97C)를 pET28a 벡터에 클로닝하였다.
- Habc 및 막횡단 도메인(191-267, I202C/I266C 치환)이 결여된 신택신-1A를 6×His-태그 ΔN-VAMP2(49-96)와 함께 pETDuet-1 벡터로 복제하여 준비합니다.
- pET28a 벡터에 클로닝된 전장 SNAP-25 이소폼 b(2-206, 모든 C 내지 A)를 준비한다. 이것은 ΔN 복합체를 제조하는 데 사용됩니다.
- 스네어 복합체를 재조립하기 위해 MT 분석 완충액에 직접 첨가하기 위해 pET28a 벡터 내로 클로닝된 6×His-태그된 전장 SNAP-25 이소폼 b(1-206, 모든 C 내지 A)를 준비한다.
- Rosetta (DE3) E. coli 세포 두 개를 준비합니다. 한 그룹은 VAMP2 플라스미드(단계 4.1.1)로, 하나는 ΔN-복합체를 발현하기 위해 syntaxin-1A/ΔN-VAMP2 및 태그가 지정되지 않은 SNAP-25 플라스미드(단계 4.1.2 및 4.1.3)로 변환하고, 다른 그룹은 His-태그된 SNAP-25 플라스미드(단계 4.1.4)로 변환합니다.
- 형질전환된 세포를 적절한 항생제(여기서, VAMP2 및 His-태그된 SNAP-25에 대한 카나마이신 및 클로람페니콜; ΔN-복합체에 대한 카나마이신, 클로람페니콜 및 암피실린)와 함께 Luria-Bertani 브로스(LB)로 옮깁니다. 진탕 배양기(220 rpm)에서 배양액의 광학 밀도(OD)가 0.7-0.9에 도달할 때까지 37°C에서 성장시킵니다.
- 단백질 발현을 유도하기 위해 1 mM 이소프로필 β-d-1-티오갈락토피라노사이드(IPTG)를 첨가하고 진탕 배양기(220 rpm)에서 37°C에서 3-4시간 동안 세포를 배양한다.
- 배양액을 4,500 × g 에서 4°C에서 15분 동안 원심분리하여 세포를 펠렛 다운하였다.
- 단백질 정제를 위한 완충액을 준비합니다( 표 2 참조).
- SNARE 발현 세포 펠릿을 40mL의 얼음처럼 차가운 용해 완충액에 현탁하고 얼음에서 초음파 처리하여 세포를 용해합니다(15% 진폭, 5초 켜기 및 5초 끄기, 총 30분).
- 용해물을 15,000 × g 에서 4°C에서 30분 동안 원심분리하여 불용성 물질을 제거한다.
- 1mL의 Ni-NTA 수지로 채워진 중력 컬럼을 통해 상청액을 통과시킵니다. 세척 완충액 A로 수지를 세척한 다음 세척 완충액 B로 세척하고 10mL의 용출 완충액으로 단백질을 용출합니다.
- 탈염 컬럼을 사용하여 용리액에서 트리스(2-카르복시에틸)포스핀(TCEP) 및 이미다졸을 제거합니다(제조업체의 지침을 따름). PBS로 샘플을 용리합니다.
- 원심 필터(10kDa 컷오프)로 단백질을 ~70μM로 농축하면서 단백질을 PBS(일반적으로 2mL 수율)로 유지합니다. 280nm(A280)에서 자외선(UV) 흡수 또는 Bradford 분석으로 단백질 농도를 측정합니다.
- 작은 분취량을 준비하고 액체 질소에서 급속 동결하고 사용할 때까지 -80 °C에서 보관하십시오.
참고: 전체 SNARE 복합체는 DNA 핸들에 ΔN-복합체를 접합한 후 조립됩니다(아래 참조).
5. DNA 손잡이 부착
참고: 한쪽 끝에 1차 아민기를 포함하는 2개의 510bp dsDNA 핸들을 먼저 PCR로 준비한 다음 아민기를 이기능성 가교제인 SM(PEG)2를 사용하여 말레이미드기로 전환합니다. 그런 다음 두 개의 핸들은 부위 특이적 접합을 위해 시스테인 그룹을 통해 SNARE 복합체에 공유 결합됩니다(그림 3B).
- 프라이머를 준비하십시오.
- 순방향 프라이머 준비: 유리 표면 부착을 위해 5′-비오틴 표지되고 λ-DNA에 결합하는 프라이머 B(핸들 B 증폭용); 프라이머 Z(핸들 Z 증폭용)는 마그네틱 비드 부착을 위해 5′-아지드 라벨이 붙어 있고 프라이머 B와 동일한 서열을 가지고 있습니다.
- 역방향 프라이머 준비: 단백질 접합을 위해 5′-아민 표지되고 정방향 프라이머에서 510bp 떨어진 λ-DNA에 결합하는 프라이머 N(핸들 B 및 핸들 Z에 대해 공유됨).
- λ-DNA(주형), nTaq 중합효소 및 표준 PCR 조건( 표 1 참조)을 사용하여 두 세트의 PCR 반응(각 핸들에 대해 200μL 반응이 포함된 18개의 튜브)을 설정하고 실행합니다. PCR 세척 키트로 제품을 세척하고 각 핸들을 45μL의 초순수로 용출합니다. 이후 단계에서 효과적인 반응을 위해 고농도의 핸들을 얻기 위해 최소한의 물을 사용하십시오.
- A260으로 DNA 농도를 측정합니다. 일반적인 수율은 각 핸들에 대해 ~650μL의 ~2μM 용액입니다. 나중에 확인할 수 있도록 작은 샘플을 따로 보관하여 아가로스 겔 전기영동에서 확인하십시오.
- 각 핸들(PBS에서 1μM)을 5mM SM(PEG)2로 반응시킵니다. 부드러운 회전으로 실온에서 배양하십시오. 1시간 후 DNA 정제 키트를 사용하여 미반응 SM(PEG)2를 제거합니다. 각 핸들을 250μL의 PBS로 용리하여 ~2μM 용액을 얻습니다.
- PBS에서 핸들 B와 ΔN-복합체의 용액을 1:16의 몰비(예: 1μM 핸들 B 및 16μM ΔN-복합체)로 혼합하고 교반하면서 실온에서 2시간 동안 배양합니다. 아가로스 겔 전기영동을 위해 작은 샘플을 따로 보관하십시오.
- 이전 단계에서 사용한 ΔN-복합체 위에 2.5배 몰 초과량의 VAMP2 용액을 추가합니다. 교반과 함께 실온에서 1 시간 동안 혼합물을 추가로 배양한다. 이 단계에서 전체 SNARE 복합체가 조립됩니다.
- 신선한 PBS 및 원심 필터(100kDa 컷오프)로 완충액 교환에 의해 유리 단백질을 제거한다: 4°C에서 5분 동안 14,000×g에서 원심분리하고, 적어도 6배 반복하고, 마지막 스핀을 위해 15 분 동안 실행 한다. 유리 단백질의 제거를 모니터링하기 위해 A260/A280 비율의 증가를 측정합니다. 아가로스 겔 전기영동을 위해 작은 샘플을 따로 보관하십시오.
- 핸들 B에 15배 몰 초과량으로 용액에 핸들 Z를 추가합니다. 반응을 촉진하기 위해 핸들 Z의 농도를 최소 1μM 이상으로 유지하십시오. 교반과 함께 혼합물을 4°C에서 밤새 인큐베이션한다.
- 아가로스 겔 전기영동(그림 3B, 삽입)에 의해 중간체(Handle B 및 그 단백질 접합체)와 최종 생성물(두 개의 손잡이가 있는 SNARE 복합체)을 확인합니다( 표 2 참조).
알림: 단백질이 핸들 B에 성공적으로 부착되면 이동성 이동이 감지됩니다. 특히, DNA 핸들에 대한 완전한 SNARE 복합체의 형성은 SDS에서 분해되고 DNA에 결합된 신택신만 남기는 ΔN-복합체와 달리 나트륨 도데실 설페이트(SDS)에 대한 내성으로 확인할 수 있습니다( 그림 3B의 b 및 c 비교). - 작은 분취량을 준비하고 액체 질소에서 급속 동결하고 사용할 때까지 -80 °C에서 보관하십시오.
참고: 최종 용액에는 반응하지 않은 핸들이 포함되어 있지만, 비오틴과 아지드로 이중으로 표지된 원하는 구조만 샘플 중에 선택됩니다.amp플로우 셀에서 조립합니다.
6. 플로우 셀의 제작
참고: MT 측정을 위한 플로우 셀은 양면 테이프로 결합된 두 개의 유리 커버슬립으로 구성됩니다(그림 3C). 하나의 커버슬립은 PEG와 비오틴화 폴리에틸렌 글리콜(PEG)의 혼합물로 코팅되어 비특이적 결합을 방지하고 비오틴-뉴트르아비딘 결합을 통해 표적 분자의 특이적 테더링을 가능하게 합니다(그림 3D). 그런 다음 MT 실험을 위한 재료 용액을 주사기 펌프를 사용하여 플로우 셀에 순차적으로 주입합니다(그림 3C,D).
- 상단(24mm × 50mm, No. 1.5 두께)과 하단(24mm × 60mm, No. 1.5 두께) 표면에 각각 하나씩 두 개의 유리 커버슬립을 준비합니다. 30분 동안 1M KOH에서 초음파 처리하여 커버슬립을 청소합니다. 초음파 처리 후 커버 슬립을 증류수로 헹구고 다음 단계까지 물에 보관하십시오.
- PE게시된 프로토콜42,43에 따라 하단 커버슬립을 작성하십시오. 실란화를 위해 N-[3-(트리메톡시실릴)프로필]에틸렌디아민을 사용하고 100mM 중탄산염 완충액에 비오틴-PEG-SVA와 mPEG-SVA의 1:100(ww) 혼합물을 사용합니다. PEGylated 커버슬립을 -20°C에서 건조하게 유지하고 몇 주 동안 보관하십시오.
- 실험 당일, PEGylated 커버 슬립을 꺼내 질소 총으로 바람 건조시킵니다. 먼지가 있는지 육안으로 검사하여 깨끗한지 확인하십시오.
- 샘플 채널을 만들려면 ~2mm 너비의 양면 테이프 스트립을 준비하고 바닥 커버슬립(PEG화된 표면이 위로 향하게)에 4개의 스트립을 서로 평행하고 ~5mm 간격으로 놓습니다(그림 3C).
참고: 이렇게 하면 단일 플로우 셀에서 3개의 5mm 너비 샘플 채널을 생성할 수 있습니다. - 하단 커버슬립의 중앙에 상단 커버슬립을 놓고 짧은 가장자리에 채널 입구와 출구를 위한 ~5mm의 공간을 남겨둡니다. 상단 커버슬립의 뒷면을 핀셋으로 살짝 눌러 채널을 단단히 밀봉합니다.
- 흡입구 저장소를 만들려면 200μL 피펫 팁의 가장자리를 다듬습니다. ~200μL의 용액을 보유할 수 있도록 더 넓은 개구부에서 ~10mm를 잘라냅니다. 3 개의 흐름 채널에 대해 3 개를 만드십시오. 배출구를 구성하려면 주사기 펌프의 튜브에 맞는 주사기 바늘 3개를 준비합니다.
- 5분 에폭시를 사용하여 저장소와 바늘 허브를 플로우 셀에 붙입니다. 누출을 방지하기 위해 완전한 밀봉이 형성되고 채널이 과도한 접착제로 막히지 않았는지 확인하십시오. 최소 30분 동안 건조시키십시오.
7. 비드-테더 구조물의 조립
참고: 비드-테더 구조용 용액을 포함하여 MT 실험용 재료 용액은 주사기 펌프를 사용하여 플로우 셀에 순차적으로 도입됩니다(그림 3C,D).
- 마그네틱 비드를 준비합니다. 원액에서 M270-에폭시 비드 5mg(디메틸포름아미드 167.5μL에 ~3.3 × 108 비드)을 취하고, 비드를 자기 분리하여 용매를 인산염 완충액( 표 2 참조)으로 교체합니다.
- ~1.1 × 109 비드 mL-1 에서 1M 황산암모늄이 함유된 인산염 완충액에서 비드를 준비하고 2mM 디벤조시클로옥틴(DBCO)-NH2와 반응시킵니다. 혼합물을 실온의 회전 믹서에서 3시간 동안 배양합니다. 반응 후, 비드를 신선한 인산염 완충액으로 3배 세척하여 반응하지 않은 분자를 제거한다.
알림: 세척된 비드는 사용하기 전에 몇 주 동안 4°C에서 추가 회전 없이 보관할 수 있습니다. - 플로우 셀 채널 출구의 바늘을 폴리에틸렌 튜브로 주사기 펌프에 연결합니다. PBS로 채널을 평형화합니다.
- 펌프로 흡입하여 NeutrAvidin, 표적 구조(DNA 헤어핀 또는 DNA 손잡이가 있는 SNARE 복합체), 참조 폴리스티렌 비드 및 DBCO 코팅 마그네틱 비드와 같은 용액을 순차적으로 채널에 주입합니다. 사용하기 전에 잠재적인 비드 응집체를 분산시키기 위해 비드 용액을 완전히 소용돌이칩니다.
- 0.1pN의 힘을 가하면서 결합되지 않은 비드를 씻어냅니다.
알림: 작은 상향 힘의 적용은 결합되지 않은 비드의 제거를 용이하게 하고 특별히 결합된 비드-테더 구조의 파열을 방지하는 데 도움이 됩니다. - SNARE 복합체를 사용한 실험의 경우 최종 완충액에 1.5μM SNAP-25를 포함합니다.
참고: 자유 SNAP-25 분자는 풀림 후 SNARE 복합체를 재결합할 수 있으며 단일 복합체에서 반복 측정이 가능합니다.
8. 표적 구조물의 식별
- 유동 세포 채널의 표면에서 표적 구조물의 단일 분자에 의해 묶인 자기 비드를 검색합니다. 참조 비드가 근처에 있는지 확인하십시오.
- 후보 비드를 회전하고 자유롭게 회전하는지 확인합니다. 비드가 여러 분자에 의해 묶여 있으면 제한된 움직임을 나타냅니다.
- 비드를 몇 바퀴 완전히 돌리고 회전 반경을 찾으십시오 (이 기능은 제공된 소프트웨어에서 구현됩니다). 가급적이면 회전 반경이 작은 비드를 선택하십시오.
주: 이 반경은 비드가 테더 축으로부터 얼마나 중심에서 벗어났는지를 나타내며, 이는 비드-테더 조립체(30, 31) 동안 무작위로 결정된다. 모든 실험에서 비드의 중심에서 벗어난 최소한은 우리가 사용하는 높은 비드 반경 대 테더 확장 비율과 관련된 많은 아티팩트를 완화합니다. - 힘을 0에서 5pN으로 증가시켜 양호한 단일 테더링 비드를 식별합니다. 1kbp 테더(또는 이에 상응하는 두 개의 510bp 핸들)의 스트레칭으로 인한 비드의 회절 패턴에 큰 변화가 있는지 확인합니다. 회절 패턴이 크게 변하지 않으면 힘을 0으로 낮추고 다른 후보 비드를 스캔합니다.
참고: 비드의 ~300nm 리프팅은 실제로 추적 프로세스를 시작하지 않고도 원시 이미지에서 쉽게 알 수 있습니다.
9. 확장 측정을 위한 비드 추적
참고: 비드 트래킹은 본 기사와 함께 제공되는 LabVIEW 소프트웨어에서 비드 이미지를 실시간으로 분석하여 수행됩니다. 트래킹 방법 및 그 변형들은 종래의 MT 시스템의 대부분에서 사용되어 왔으며, 이전의 문헌 2,5,7,26에 설명되어 있다. 고정된 기준 비드에 대한 자기 비드의 위치를 측정함으로써(즉, 차동 추적), 위치 측정은 외부 섭동에 대해 매우 견고해집니다.
- 적절한 마그네틱 비드가 참조 비드와 함께 배치되면 보정 버튼을 클릭하여 비드 추적 준비를 시작합니다.
- 이미지에서 구슬을 클릭하여 구슬의 위치를 정의합니다. 그런 다음 이미지는 비드 주변의 관심 영역(ROI)(예: 3μm 비드의 경우 150 x 150픽셀)으로 자른 다음 추가로 분석하여 정확한 비드 좌표를 추출합니다.
- 자석 회전이 완료될 때까지 기다리십시오. 이 프로세스는 비드(31)의 중심에서 벗어난 부착을 문서화하기 위해 자석을 회전시키면서 비드의 x 및 y 좌표를 기록한다(2D 교차 상관(44)을 계산하거나 비드 이미지의 방사형 대칭(45)을 사용하여 비슷한 성능으로).
- z 방향으로 추적하려면 소프트웨어가 초점면에서 서로 다른 거리에 있는 비드의 회절 이미지 룩업 테이블을 생성할 때까지 기다립니다. 이것은 피에조 스캐너로 대물 렌즈를 등거리 단계로 밟고 각 위치에서 변동 평균 비드 이미지를 기록하여 수행됩니다. 그런 다음 실제 실험에서 비드의 z 좌표는 실시간 비드 이미지를 보간7을 사용하여 룩업 테이블과 비교하여 결정됩니다.
- 조회 테이블 생성이 완료되면 추적 및 자동 초점을 활성화합니다( Track ? 및 AF? 버튼)을 클릭하고 획득 버튼을 클릭하여 비드 위치 기록을 시작합니다.
알림: 자동 초점은 선택 사항이지만 획득 중 z 의 스테이지 드리프트를 수정하는 것이 좋습니다.
10. 강제 적용 계획
- 강제 램프 실험: 구조물의 힘-확장 관계를 확인하려면 일정한 하중 속도(± 1.0pN s-1)로 힘 램프를 위아래로 적용합니다(그림 4A). 예를 들어, 0-20-0 pN 사이클을 세 번 라운드하여 구조물의 전체 길이와 핸들의 힘-확장 곡선을 확인합니다.
- 소프트웨어에서 테더 파라미터를 지정하여 측정된 데이터 위에 WLC 힘 확장 곡선을 오버레이하고 타겟 비드가 적절한 DNA 핸들이 있는 실제 샘플 구조에 의해 테더링되는지 여부를 확인합니다. 구축물의 공지된 윤곽 길이(예를 들어, 1 kbp dsDNA의 경우 ~340 nm) 및 WLC 지속성 길이(짧은 dsDNA31의 경우 30-45 nm)를 시작점으로 사용한다. 필요한 경우 2.11단계에서 설명한 확장 수정 방법을 적용합니다.
- 구조가 확인되면 힘-확장 반응을 자세히 검사하여 표적 분자-헤어핀 또는 SNARE 복합체로 인한 추가 확장을 찾습니다.
- 항력 실험: 표적 분자의 힘 감도를 조사하기 위해 개별 단계에서 적용된 힘을 점진적으로 변경합니다(그림 4B).
참고: MT는 자석이 가만히 있을 때 가해지는 힘이 일정하게 유지되기 때문에 간단하고 효과적인 등력 실험을 가능하게 합니다.- DNA 헤어핀의 경우 0.2-0.5pN 단계로 4-8pN의 힘을 가하고 각 힘 수준에서 ~10초 동안 비드 위치를 측정합니다.
- SNARE 복합체의 경우, 0.1-0.2 pN 단계로 14-16 pN의 힘을 가하고, 각 힘 수준에서 ~10 초 동안 비드 위치를 측정합니다.
- 포스 점프 실험: SNARE 복합체의 전이 이벤트를 관찰합니다.
알림: 항력 실험과 같은 힘 점프 실험에는 힘 수준의 변화가 포함됩니다. 그러나 힘 점프는 적용된 힘의 더 급격한 변화를 사용하여 단백질 복합체의 갑작스러운 파열과 같은 프로브 분자에서 힘 유발 이벤트를 모니터링할 수 있습니다. 예를 들어, SNARE 복합체는 힘 순환(force cycling)에서 구조적 히스테리시스(hysteresis)를 나타내기 때문에(23), 힘-점프(force-jump) 실험을 수행하고 전이에 대한 잠복기를 측정하는 것이 유익하다(도 4C).- 압축 풀기: 온전한 삼원 SNARE 복합체에서 VAMP2 분자를 벗겨내고 syntaxin-1A와 SNAP-25의 이진 복합체를 남깁니다.
- 재압축: 온전한 SNARE 복합체를 재생하기 위해 압축을 푼 VAMP2 분자의 압축.
- 펼쳐진: SNAP-25의 완전한 해리와 함께 SNARE 복합체의 완전한 분해. VAMP2와 신택신 분자만 풀린 후 구조물에 남아 있습니다.
- 다시 접기: 완충액으로부터 유리 SNAP-25 분자의 결합시 SNARE 복합체의 재생.
- 2 pN에서, 자유 SNAP25 분자의 결합을 기다리면서(~30 s) 온전한 SNARE 복합체의 조립을 유도한다. SNARE 복합체의 형성시 확장의 급격한 감소가 관찰됩니다.
- 압축 해제 이벤트를 관찰하려면 10-12pN에서 몇 초 동안 기다렸다가 가능한 최대 모터 속도로 갑자기 14-15pN으로 이동합니다. 목표 힘에 따라 SNARE 복합체는 부분적으로 압축이 풀린 중간체 사이의 가역적 전환(항력 실험에서와 같이) 또는 무작위 대기 시간(또는 대기 시간) 후 더 높은 압축이 풀린 상태로 ~25nm 점프를 나타냅니다.
- 재지퍼 이벤트를 관찰하려면 지퍼 해제가 관찰된 직후 힘을 10-12pN으로 낮추십시오. 다시 말하지만, SNARE 컴플렉스는 임의의 대기 시간 후에 더 낮은 지퍼 상태로의 확률적 전환을 나타냅니다. 압축을 푼 후 풀림이 발생하면 SNAP-25 분자가 누락되어 복합체가 다시 압축되지 않습니다.
- 전개 현상을 관찰하려면 압축을 푼 후 더 오랜 시간 동안 기다렸다가 확장(~2nm)의 추가 증가를 감지합니다.
11. 데이터 분석
참고: MT 데이터로 수행할 수 있는 분석 유형은 대상 시스템에 따라 다릅니다. 그러나 그림 4에 설명된 각 실험에서 유용한 정보를 추출하는 일반적인 방법이 있습니다. 모든 분석은 이 글에서 제공하는 사용자 지정 코드를 사용하여 MATLAB (R2021a)로 수행됩니다. 이러한 코드는 이 문서에 제시된 것과 동일한 데이터를 사용하여 플롯을 생성합니다. 100Hz 추적의 원시 데이터는 분석을 위해 직접 가져왔지만 1.2kHz 추적의 데이터는 일반적으로 노이즈를 줄이기 위해 분석 전에 중앙값 필터링(5포인트 슬라이딩 윈도우 포함)되었습니다(노이즈 분석 제외).
- 강제 램프 실험: 힘-확장 관계(예: 폴리머의 탄성)를 분석하고 힘을 전이하여 나노기계적 특성에 대한 정보를 추출합니다.
- 항력 실험: 상태 모집단과 체류 시간(또는 전이 속도)을 힘의 함수로 분석하여 구조적 변화의 구조적(예: 전이와 관련된 영역), 열역학적(예: 자유 에너지 차이) 및 운동적(예: 에너지 장벽) 매개변수를 추출합니다.
- 포스 점프 실험: 파열 동역학(예: 단백질-단백질 상호작용 및 수용체-리간드 결합) 또는 일시적인 중간체의 수명(예: 생체 분자 풀림)을 분석하여 표적 분자 및 그 상태의 안정성을 추출합니다.
- 대표적인 응용 분야로 DNA 헤어핀 및 SNARE 복합체에 대한 샘플 데이터를 분석합니다.
- DNA 헤어핀의 2가지 상태 전이: 압축 풀기, 개방 거리, 모집단 이동의 힘 의존성, 숨겨진 마르코프 모델(HMM)을 사용한 상태 할당 및 전이율 측정(MATLAB 코드 제공).
- SNARE 복합체의 구조적 변화: 압축 해제력, 중간 상태의 힘 의존성 및 압축 해제 대기 시간, 재압축 시 히스테리시스, 펼치기/다시 접기 동작.
참고: DNA 핸들, DNA 헤어핀 및 SNARE 복합 형태에 대한 힘-확장 모델은 이전 참고 문헌14,31에 나와 있습니다.
결과
힘 교정
두 가지 힘 측정 방법(비드의 측면 변위 분산 및 전력 스펙트럼 분석)의 결과는 0-2pN 차이가 났습니다(그림 2G). 그림 2F의 결과에 따르면 일반 네오디뮴 자석으로 최대 30pN에 안정적으로 도달할 수 있습니다.
8bp DNA 헤어핀의 2상태 전이
우리는 먼저 짧은 DNA 헤어핀의 나노 역학을 조사했습니다 (
토론
이 연구에서 우리는 높은 시공간 정밀도에서 생체 분자의 구조적 변화를 관찰할 수 있는 단일 분자 힘 분광법 설정을 도입했습니다. 사용된 고속 CMOS 카메라는 1,280 x 1,024 해상도에서 1,200 프레임 s-1 을 획득하여 1.2kHz 비드 트래킹을 가능하게 합니다. 그러나 측정 속도는 현재 비드 추적 소프트웨어에 의해 제한되므로 고속 측정에서 ROI는 일반적으로 더 작은 영역으로 감소합니다. SLD의 고?...
공개
저자는 선언할 이해 상충이 없습니다.
감사의 말
이 연구는 한국 정부(MSIT)가 지원하는 한국연구재단(NRF) 보조금(NRF-2022R1C1C1012176, NRF-2021R1A4A1031754 및 NRF-2021R1A6A1A10042944)의 지원을 받았습니다. S.-H.R. NRF 보조금(2021R1C1C2009717)의 지원을 받았습니다.
자료
| Name | Company | Catalog Number | Comments |
| Materials for construct synthesis | |||
| Agarose gel electrophoresis system | Advance | Mupid-2plus | |
| DNA ladder | Bioneer | D-1037 | |
| nTaq polymerase | Enzynomics | P050A | |
| PCR purification kit | LaboPass | CMR0112 | |
| PEGylated SMCC crosslinker / SM(PEG)2 | ThermoFisher Scientific | 22102 | For SNARE–DNA coupling |
| Primer B | Bioneer | 5'-Biotin/TCGCCACCATCATTTCCA-3' | For 5-kbp force calibration construct and DNA handles |
| Primer B_hp | IDT | 5'-Biotin/TTTTTTTTTTGTTCTCTATTT TTTTAGAGAAC /AP site/ /AP site/ TCGCCACCATCATTTCCA-3' | For hairpin construct |
| Primer N | Bioneer | 5'-C6Amine/CATGTGGGTGACGCGAAA-3' | For DNA handles |
| Primer Z | Bioneer | 5'-Azide/TCGCCACCATCATTTCCA-3' | For DNA handles |
| Primer Z_5k | Bioneer | 5'-Azide/TTAGAGAGTATGGGTATATGACA TCG-3' | For 5-kbp force calibration construct |
| Primer Z_hp | Bioneer | 5'-Azide/GTGGCAGCATGACACC-3' | For hairpin construct |
| SYBR Safe DNA Gel Stain | ThermoFisher Scientific | S33102 | |
| λ-DNA | Bioneer | D-2510 | Template strand for PCR |
| DNA sequences for SNARE proteins | |||
| 6×His-tagged SNAP-25b (2-206; capitalized) in pET28a | homemade | tggcgaatgggacgcgccctgtagcggcgca ttaagcgcggcgggtgtggtggttacgcgca gcgtgaccgctacacttgccagcgccctagc gcccgctcctttcgctttcttcccttccttt ctcgccacgttcgccggctttccccgtcaag ctctaaatcgggggctccctttagggttccg atttagtgctttacggcacctcgaccccaaa aaacttgattagggtgatggttcacgtagtg ggccatcgccctgatagacggtttttcgccc tttgacgttggagtccacgttctttaatagt ggactcttgttccaaactggaacaacactca accctatctcggtctattcttttgatttata agggattttgccgatttcggcctattggtta aaaaatgagctgatttaacaaaaatttaacg cgaattttaacaaaatattaacgtttacaat ttcaggtggcacttttcggggaaatgtgcgc ggaacccctatttgtttatttttctaaatac attcaaatatgtatccgctcatgaattaatt cttagaaaaactcatcgagcatcaaatgaaa ctgcaatttattcatatcaggattatcaata ccatatttttgaaaaagccgtttctgtaatg aaggagaaaactcaccgaggcagttccatag gatggcaagatcctggtatcggtctgcgatt ccgactcgtccaacatcaatacaacctatta atttcccctcgtcaaaaataaggttatcaag tgagaaatcaccatgagtgacgactgaatcc ggtgagaatggcaaaagtttatgcatttctt tccagacttgttcaacaggccagccattacg ctcgtcatcaaaatcactcgcatcaaccaaa ccgttattcattcgtgattgcgcctgagcga gacgaaatacgcgatcgctgttaaaaggaca attacaaacaggaatcgaatgcaaccggcgc aggaacactgccagcgcatcaacaatatttt cacctgaatcaggatattcttctaatacctg gaatgctgttttcccggggatcgcagtggtg agtaaccatgcatcatcaggagtacggataa aatgcttgatggtcggaagaggcataaattc cgtcagccagtttagtctgaccatctcatct gtaacatcattggcaacgctacctttgccat gtttcagaaacaactctggcgcatcgggctt cccatacaatcgatagattgtcgcacctgat tgcccgacattatcgcgagcccatttatacc catataaatcagcatccatgttggaatttaa tcgcggcctagagcaagacgtttcccgttga atatggctcataacaccccttgtattactgt ttatgtaagcagacagttttattgttcatga ccaaaatcccttaacgtgagttttcgttcca ctgagcgtcagaccccgtagaaaagatcaaa ggatcttcttgagatcctttttttctgcgcg taatctgctgcttgcaaacaaaaaaaccacc gctaccagcggtggtttgtttgccggatcaa gagctaccaactctttttccgaaggtaactg gcttcagcagagcgcagataccaaatactgt ccttctagtgtagccgtagttaggccaccac ttcaagaactctgtagcaccgcctacatacc tcgctctgctaatcctgttaccagtggctgc tgccagtggcgataagtcgtgtcttaccggg ttggactcaagacgatagttaccggataagg cgcagcggtcgggctgaacggggggttcgtg cacacagcccagcttggagcgaacgacctac accgaactgagatacctacagcgtgagctat gagaaagcgccacgcttcccgaagggagaaa ggcggacaggtatccggtaagcggcagggtc ggaacaggagagcgcacgagggagcttcca gggggaaacgcctggtatctttatagtcctgt cgggtttcgccacctctgacttgagcgtcga tttttgtgatgctcgtcaggggggcggagcc tatggaaaaacgccagcaacgcggccttttt acggttcctggccttttgctggccttttgct cacatgttctttcctgcgttatcccctgatt ctgtggataaccgtattaccgcctttgagtg agctgataccgctcgccgcagccgaacgacc gagcgcagcgagtcagtgagcgaggaagcgg aagagcgcctgatgcggtattttctccttac gcatctgtgcggtatttcacaccgcatatat ggtgcactctcagtacaatctgctctgatgc cgcatagttaagccagtatacactccgctat cgctacgtgactgggtcatggctgcgccccg acacccgccaacacccgctgacgcgccctga cgggcttgtctgctcccggcatccgcttaca gacaagctgtgaccgtctccgggagctgcat gtgtcagaggttttcaccgtcatcaccgaaa cgcgcgaggcagctgcggtaaagctcatcag cgtggtcgtgaagcgattcacagatgtctgc ctgttcatccgcgtccagctcgttgagtttc tccagaagcgttaatgtctggcttctgataa agcgggccatgttaagggcggttttttcctg tttggtcactgatgcctccgtgtaaggggga tttctgttcatgggggtaatgataccgatga aacgagagaggatgctcacgatacgggttac tgatgatgaacatgcccggttactggaacgt tgtgagggtaaacaactggcggtatggatgc ggcgggaccagagaaaaatcactcagggtc aatgccagcgcttcgttaatacagatgtaggt gttccacagggtagccagcagcatcctgcga tgcagatccggaacataatggtgcagggcgc tgacttccgcgtttccagactttacgaaaca cggaaaccgaagaccattcatgttgttgctc aggtcgcagacgttttgcagcagcagtcgct tcacgttcgctcgcgtatcggtgattcattc tgctaaccagtaaggcaaccccgccagccta gccgggtcctcaacgacaggagcacgatcat gcgcacccgtggggccgccatgccggcgata atggcctgcttctcgccgaaacgtttggtgg cgggaccagtgacgaaggcttgagcgagggc gtgcaagattccgaataccgcaagcgacagg ccgatcatcgtcgcgctccagcgaaagcggt cctcgccgaaaatgacccagagcgctgccgg cacctgtcctacgagttgcatgataaagaag acagtcataagtgcggcgacgatagtcatgc cccgcgcccaccggaaggagctgactgggtt gaaggctctcaagggcatcggtcgagatccc ggtgcctaatgagtgagctaacttacattaa ttgcgttgcgctcactgcccgctttccagtc gggaaacctgtcgtgccagctgcattaatga atcggccaacgcgcggggagaggcggtttgc gtattgggcgccagggtggtttttcttttca ccagtgagacgggcaacagctgattgccctt caccgcctggccctgagagagttgcagcaag cggtccacgctggtttgccccagcaggcgaa aatcctgtttgatggtggttaacggcgggat ataacatgagctgtcttcggtatcgtcgtat cccactaccgagatatccgcaccaacgcgca gcccggactcggtaatggcgcgcattgcgcc cagcgccatctgatcgttggcaaccagcatc gcagtgggaacgatgccctcattcagcattt gcatggtttgttgaaaaccggacatggcact ccagtcgccttcccgttccgctatcggctga atttgattgcgagtgagatatttatgccagc cagccagacgcagacgcgccgagacagaa cttaatgggcccgctaacagcgcgatttgctgg tgacccaatgcgaccagatgctccacgccca gtcgcgtaccgtcttcatgggagaaaataat actgttgatgggtgtctggtcagagacatca agaaataacgccggaacattagtgcaggcag cttccacagcaatggcatcctggtcatccag cggatagttaatgatcagcccactgacgcgt tgcgcgagaagattgtgcaccgccgctttac aggcttcgacgccgcttcgttctaccatcga caccaccacgctggcacccagttgatcggcg cgagatttaatcgccgcgacaatttgcgacg gcgcgtgcagggccagactggaggtggcaac gccaatcagcaacgactgtttgcccgccagt tgttgtgccacgcggttgggaatgtaattca gctccgccatcgccgcttccactttttcccg cgttttcgcagaaacgtggctggcctggttc accacgcgggaaacggtctgataagagacac cggcatactctgcgacatcgtataacgttac tggtttcacattcaccaccctgaattgactc tcttccgggcgctatcatgccataccgcgaa aggttttgcgccattcgatggtgtccgggat ctcgacgctctcccttatgcgactcctgcat taggaagcagcccagtagtaggttgaggccg ttgagcaccgccgccgcaaggaatggtgcat gcaaggagatggcgcccaacagtcccccggc cacggggcctgccaccatacccacgccgaaa caagcgctcatgagcccgaagtggcgagccc gatcttccccatcggtgatgtcggcgatata ggcgccagcaaccgcacctgtggcgccggtg atgccggccacgatgcgtccggcgtagagga tcgagatctcgatcccgcgaaattaatacga ctcactataggggaattgtgagcggataaca attcccctctagaaataattttgtttaactt taagaaggagatataccATGGGCAGC AGCCATCATCATCATCATCACA GCAGCGGCCTGGTGCCGCGC GGCAGCCATACTAGCGGAGAT ATCGCCGAGGACGCAGACAT GCGCAATGAGCTGGAGGAGA TGCAGAGGAGGGCTGACCAG CTGGCTGATGAGTCCCTGGA AAGCACCCGTCGCATGCTGC AGCTGGTTGAAGAGAGTAAA GATGCTGGCATCAGGACTTT GGTTATGTTGGATGAGCAAG GCGAACAACTGGAACGCATT GAGGAAGGGATGGACCAAAT CAATAAGGACATGAAAGAAG CAGAAAAGAATTTGACGGAC CTAGGAAAATTCGCCGGCCT TGCCGTGGCCCCCGCCAAC AAGCTTAAATCCAGTGATGC TTACAAAAAAGCCTGGGGC AATAATCAGGATGGAGTAGT GGCCAGCCAGCCTGCCCG TGTGGTGGATGAACGGGAG CAGATGGCCATCAGTGGTG GCTTCATCCGCAGGGTAAC AAATGATGCCCGGGAAAAT GAGATGGATGAGAACCTG GAGCAGGTGAGCGGCATC ATCGGAAACCTCCGCCAC ATGGCTCTAGACATGGGCA ATGAGATTGACACCCAGA ATCGCCAGATCGACAGGA TCATGGAGAAGGCTGATT CCAACAAAACCAGAATTG ATGAAGCCAACCAACGTG CAACAAAGATGCTGGGAA GTGGTTAAggatccgaattcgag ctccgtcgacaagcttgcggccgcactc gagcaccaccaccaccaccactgagat ccggctgctaacaaagcccgaaagga agctgagttggctgctgccaccgctgag caataactagcataaccccttggggcct ctaaacgggtcttgaggggttttttgctga aaggaggaactatatccggat | |
| 6×His-tagged VAMP2 (2-97, L32C/I97C; capitalized) in pET28a | homemade | tggcgaatgggacgcgccctgtagcggcgca ttaagcgcggcgggtgtggtggttacgcgca gcgtgaccgctacacttgccagcgccctagc gcccgctcctttcgctttcttcccttccttt ctcgccacgttcgccggctttccccgtcaag ctctaaatcgggggctccctttagggttccg atttagtgctttacggcacctcgaccccaaa aaacttgattagggtgatggttcacgtagtg ggccatcgccctgatagacggtttttcgccc tttgacgttggagtccacgttctttaatagt ggactcttgttccaaactggaacaacactca accctatctcggtctattcttttgatttata agggattttgccgatttcggcctattggtta aaaaatgagctgatttaacaaaaatttaacg cgaattttaacaaaatattaacgtttacaat ttcaggtggcacttttcggggaaatgtgcgc ggaacccctatttgtttatttttctaaatac attcaaatatgtatccgctcatgaattaatt cttagaaaaactcatcgagcatcaaatgaaa ctgcaatttattcatatcaggattatcaata ccatatttttgaaaaagccgtttctgtaatg aaggagaaaactcaccgaggcagttccatag gatggcaagatcctggtatcggtctgcgatt ccgactcgtccaacatcaatacaacctatta atttcccctcgtcaaaaataaggttatcaag tgagaaatcaccatgagtgacgactgaatcc ggtgagaatggcaaaagtttatgcatttctt tccagacttgttcaacaggccagccattacg ctcgtcatcaaaatcactcgcatcaaccaaa ccgttattcattcgtgattgcgcctgagcga gacgaaatacgcgatcgctgttaaaaggaca attacaaacaggaatcgaatgcaaccggcgc aggaacactgccagcgcatcaacaatatttt cacctgaatcaggatattcttctaatacctg gaatgctgttttcccggggatcgcagtggtg agtaaccatgcatcatcaggagtacggataa aatgcttgatggtcggaagaggcataaattc cgtcagccagtttagtctgaccatctcatct gtaacatcattggcaacgctacctttgccat gtttcagaaacaactctggcgcatcgggctt cccatacaatcgatagattgtcgcacctgat tgcccgacattatcgcgagcccatttatacc catataaatcagcatccatgttggaatttaa tcgcggcctagagcaagacgtttcccgttga atatggctcataacaccccttgtattactgt ttatgtaagcagacagttttattgttcatga ccaaaatcccttaacgtgagttttcgttcca ctgagcgtcagaccccgtagaaaagatcaaa ggatcttcttgagatcctttttttctgcgcg taatctgctgcttgcaaacaaaaaaaccacc gctaccagcggtggtttgtttgccggatcaa gagctaccaactctttttccgaaggtaactg gcttcagcagagcgcagataccaaatactgt ccttctagtgtagccgtagttaggccaccac ttcaagaactctgtagcaccgcctacatacc tcgctctgctaatcctgttaccagtggctgc tgccagtggcgataagtcgtgtcttaccggg ttggactcaagacgatagttaccggataagg cgcagcggtcgggctgaacggggggttcgtg cacacagcccagcttggagcgaacgacctac accgaactgagatacctacagcgtgagctatg agaaagcgccacgcttcccgaagggagaaa ggcggacaggtatccggtaagcggcagggtc ggaacaggagagcgcacgagggagcttcca gggggaaacgcctggtatctttatagtcctgt cgggtttcgccacctctgacttgagcgtcga tttttgtgatgctcgtcaggggggcggagcc tatggaaaaacgccagcaacgcggccttttt acggttcctggccttttgctggccttttgct cacatgttctttcctgcgttatcccctgatt ctgtggataaccgtattaccgcctttgagtg agctgataccgctcgccgcagccgaacgacc gagcgcagcgagtcagtgagcgaggaagc ggaagagcgcctgatgcggtattttctccttac gcatctgtgcggtatttcacaccgcatatat ggtgcactctcagtacaatctgctctgatgc cgcatagttaagccagtatacactccgctat cgctacgtgactgggtcatggctgcgccccg acacccgccaacacccgctgacgcgccctga cgggcttgtctgctcccggcatccgcttaca gacaagctgtgaccgtctccgggagctgcat gtgtcagaggttttcaccgtcatcaccgaaa cgcgcgaggcagctgcggtaaagctcatcag cgtggtcgtgaagcgattcacagatgtctgc ctgttcatccgcgtccagctcgttgagtttc tccagaagcgttaatgtctggcttctgataa agcgggccatgttaagggcggttttttcctg tttggtcactgatgcctccgtgtaaggggga tttctgttcatgggggtaatgataccgatga aacgagagaggatgctcacgatacgggttac tgatgatgaacatgcccggttactggaacgt tgtgagggtaaacaactggcggtatggatgc ggcgggaccagagaaaaatcactcagggtc aatgccagcgcttcgttaatacagatgtaggt gttccacagggtagccagcagcatcctgcga tgcagatccggaacataatggtgcagggcgc tgacttccgcgtttccagactttacgaaaca cggaaaccgaagaccattcatgttgttgctc aggtcgcagacgttttgcagcagcagtcgct tcacgttcgctcgcgtatcggtgattcattc tgctaaccagtaaggcaaccccgccagccta gccgggtcctcaacgacaggagcacgatcat gcgcacccgtggggccgccatgccggcgata atggcctgcttctcgccgaaacgtttggtgg cgggaccagtgacgaaggcttgagcgagggc gtgcaagattccgaataccgcaagcgacagg ccgatcatcgtcgcgctccagcgaaagcggt cctcgccgaaaatgacccagagcgctgccgg cacctgtcctacgagttgcatgataaagaag acagtcataagtgcggcgacgatagtcatgc cccgcgcccaccggaaggagctgactgggtt gaaggctctcaagggcatcggtcgagatccc ggtgcctaatgagtgagctaacttacattaa ttgcgttgcgctcactgcccgctttccagtc gggaaacctgtcgtgccagctgcattaatga atcggccaacgcgcggggagaggcggtttgc gtattgggcgccagggtggtttttcttttca ccagtgagacgggcaacagctgattgccctt caccgcctggccctgagagagttgcagcaag cggtccacgctggtttgccccagcaggcgaa aatcctgtttgatggtggttaacggcgggat ataacatgagctgtcttcggtatcgtcgtat cccactaccgagatatccgcaccaacgcgca gcccggactcggtaatggcgcgcattgcgcc cagcgccatctgatcgttggcaaccagcatc gcagtgggaacgatgccctcattcagcattt gcatggtttgttgaaaaccggacatggcact ccagtcgccttcccgttccgctatcggctga atttgattgcgagtgagatatttatgccagc cagccagacgcagacgcgccgagacagaa cttaatgggcccgctaacagcgcgatttgctgg tgacccaatgcgaccagatgctccacgccca gtcgcgtaccgtcttcatgggagaaaataat actgttgatgggtgtctggtcagagacatca agaaataacgccggaacattagtgcaggcag cttccacagcaatggcatcctggtcatccag cggatagttaatgatcagcccactgacgcgt tgcgcgagaagattgtgcaccgccgctttac aggcttcgacgccgcttcgttctaccatcga caccaccacgctggcacccagttgatcggcg cgagatttaatcgccgcgacaatttgcgacg gcgcgtgcagggccagactggaggtggcaac gccaatcagcaacgactgtttgcccgccagt tgttgtgccacgcggttgggaatgtaattca gctccgccatcgccgcttccactttttcccg cgttttcgcagaaacgtggctggcctggttc accacgcgggaaacggtctgataagagacac cggcatactctgcgacatcgtataacgttac tggtttcacattcaccaccctgaattgactc tcttccgggcgctatcatgccataccgcgaa aggttttgcgccattcgatggtgtccgggat ctcgacgctctcccttatgcgactcctgcat taggaagcagcccagtagtaggttgaggccg ttgagcaccgccgccgcaaggaatggtgcat gcaaggagatggcgcccaacagtcccccggc cacggggcctgccaccatacccacgccgaaa caagcgctcatgagcccgaagtggcgagccc gatcttccccatcggtgatgtcggcgatata ggcgccagcaaccgcacctgtggcgccggtg atgccggccacgatgcgtccggcgtagagga tcgagatctcgatcccgcgaaattaatacga ctcactataggggaattgtgagcggataaca attcccctctagaaataattttgtttaactt taagaaggagatataccATGGGCAGC AGCCATCATCATCATCATCAC AGCAGCGGCCTGGTGCCGC GCGGCAGCCATATGGCAGAT CTCTCGGCTACCGCTGCCAC CGTCCCGCCTGCCGCCCCG GCCGGCGAGGGTGGCCCCC CTGCACCTCCTCCAAATCTTA CCAGTAACAGGAGATGCCAG CAGACCCAGGCCCAGGTGG ATGAGGTGGTGGACATCATG AGGGTGAATGTGGACAAGGT CCTGGAGCGAGACCAGAAG CTATCGGAACTGGATGATCG CGCAGATGCCCTCCAGGCA GGGGCCTCCCAGTTTGAAA CAAGTGCAGCCAAGCTCAA GCGCAAATACTGGTGGAAA AACCTCAAGATGATGTGCTA Aggatccgaattcgagctccgtcg acaagcttgcggccgcactcgagcaccacca ccaccaccactgagatccggctgctaacaaa gcccgaaaggaagctgagttggctgctgcca ccgctgagcaataactagcataaccccttgg ggcctctaaacgggtcttgaggggttttttg ctgaaaggaggaactatatccggat | |
| 6×His-tagged ΔN-VAMP2 (49–96; capitalized) and Syntaxin-1A (191–267, I202C/I266C; capitalized) in pETDuet-1 | homemade | ggggaattgtgagcggataacaattcccctc tagaaataattttgtttaactttaagaagga gatataccATGGGCAGCAGCCATCA TCATCATCATCACAGCAGCGG CCTGGAAGTTCTGTTCCAGGG GCCCGGTAATGTGGACAAGGT CCTGGAGCGAGACCAGAAGCT ATCGGAACTGGATGATCGCGC AGATGCCCTCCAGGCAGGGGC CTCCCAGTTTGAAACAAGTGC AGCCAAGCTCAAGCGCAAATAC TGGTGGAAAAACCTCAAGATGAT GTAAgcggccgcataatgcttaagtcgaaca gaaagtaatcgtattgtacacggccgcataa tcgaaattaatacgactcactataggggaat tgtgagcggataacaattccccatcttagta tattagttaagtataagaaggagatatacat ATGGCCCTCAGTGAGATCGAGA CCAGGCACAGTGAGTGCATC AAGTTGGAGAACAGCATCCG GGAGCTACACGATATGTTCAT GGACATGGCCATGCTGGTGG AGAGCCAGGGGGAGATGATT GACAGGATCGAGTACAATGTG GAACACGCTGTGGACTACGTG GAGAGGGCCGTGTCTGACACC AAGAAGGCCGTCAAGTACCAG AGCAAGGCACGCAGGAAGAA GTGCATGATCTAActcgagtc tggtaaagaaaccgctgctgcgaaatttgaa cgccagcacatggactcgtctactagcgcag cttaattaacctaggctgctgccaccgctga gcaataactagcataaccccttggggcctct aaacgggtcttgaggggttttttgctgaaag gaggaactatatccggattggcgaatgggac gcgccctgtagcggcgcattaagcgcggcgg gtgtggtggttacgcgcagcgtgaccgctac acttgccagcgccctagcgcccgctcctttc gctttcttcccttcctttctcgccacgttcg ccggctttccccgtcaagctctaaatcgggg gctccctttagggttccgatttagtgcttta cggcacctcgaccccaaaaaacttgattagg gtgatggttcacgtagtgggccatcgccctg atagacggtttttcgccctttgacgttggag tccacgttctttaatagtggactcttgttcc aaactggaacaacactcaaccctatctcggt ctattcttttgatttataagggattttgccg atttcggcctattggttaaaaaatgagctga tttaacaaaaatttaacgcgaattttaacaa aatattaacgtttacaatttctggcggcacg atggcatgagattatcaaaaaggatcttcac ctagatccttttaaattaaaaatgaagtttt aaatcaatctaaagtatatatgagtaaactt ggtctgacagttaccaatgcttaatcagtga ggcacctatctcagcgatctgtctatttcgt tcatccatagttgcctgactccccgtcgtgt agataactacgatacgggagggcttaccatc tggccccagtgctgcaatgataccgcgagac ccacgctcaccggctccagatttatcagcaa taaaccagccagccggaagggccgagcgca gaagtggtcctgcaactttatccgcctccatc cagtctattaattgttgccgggaagctagag taagtagttcgccagttaatagtttgcgcaa cgttgttgccattgctacaggcatcgtggtg tcacgctcgtcgtttggtatggcttcattca gctccggttcccaacgatcaaggcgagttac atgatcccccatgttgtgcaaaaaagcggtt agctccttcggtcctccgatcgttgtcagaa gtaagttggccgcagtgttatcactcatggt tatggcagcactgcataattctcttactgtc atgccatccgtaagatgcttttctgtgactg gtgagtactcaaccaagtcattctgagaata gtgtatgcggcgaccgagttgctcttgcccg gcgtcaatacgggataataccgcgccacata gcagaactttaaaagtgctcatcattggaaa acgttcttcggggcgaaaactctcaaggatc ttaccgctgttgagatccagttcgatgtaac ccactcgtgcacccaactgatcttcagcatc ttttactttcaccagcgtttctgggtgagcaaa aacaggaaggcaaaatgccgcaaaaaagg gaataagggcgacacggaaatgttgaatact catactcttcctttttcaatcatgattgaag catttatcagggttattgtctcatgagcgga tacatatttgaatgtatttagaaaaataaac aaataggtcatgaccaaaatcccttaacgtg agttttcgttccactgagcgtcagaccccgt agaaaagatcaaaggatcttcttgagatcct ttttttctgcgcgtaatctgctgcttgcaaa caaaaaaaccaccgctaccagcggtggtttg tttgccggatcaagagctaccaactcttttt ccgaaggtaactggcttcagcagagcgcaga taccaaatactgtccttctagtgtagccgta gttaggccaccacttcaagaactctgtagca ccgcctacatacctcgctctgctaatcctgt taccagtggctgctgccagtggcgataagtc gtgtcttaccgggttggactcaagacgatag ttaccggataaggcgcagcggtcgggctgaa cggggggttcgtgcacacagcccagcttgga gcgaacgacctacaccgaactgagataccta cagcgtgagctatgagaaagcgccacgcttccc gaagggagaaaggcggacaggtatccggta agcggcagggtcggaacaggagagcgcac gagggagcttccagggggaaacgcctggtatc tttatagtcctgtcgggtttcgccacctctg acttgagcgtcgatttttgtgatgctcgtca ggggggcggagcctatggaaaaacgccagc aacgcggcctttttacggttcctggccttttg ctggccttttgctcacatgttctttcctgcg ttatcccctgattctgtggataaccgtatta ccgcctttgagtgagctgataccgctcgccgc agccgaacgaccgagcgcagcgagtcagtg agcgaggaagcggaagagcgcctgatgcgg tattttctccttacgcatctgtgcggtatttc acaccgcatatatggtgcactctcagtacaa tctgctctgatgccgcatagttaagccagta tacactccgctatcgctacgtgactgggtca tggctgcgccccgacacccgccaacacccgc tgacgcgccctgacgggcttgtctgctcccg gcatccgcttacagacaagctgtgaccgtct ccgggagctgcatgtgtcagaggttttcacc gtcatcaccgaaacgcgcgaggcagctgcgg taaagctcatcagcgtggtcgtgaagcgatt cacagatgtctgcctgttcatccgcgtccag ctcgttgagtttctccagaagcgttaatgtc tggcttctgataaagcgggccatgttaaggg cggttttttcctgtttggtcactgatgcctc cgtgtaagggggatttctgttcatgggggta atgataccgatgaaacgagagaggatgctca cgatacgggttactgatgatgaacatgcccg gttactggaacgttgtgagggtaaacaactg gcggtatggatgcggcgggaccagagaaaaa tcactcagggtcaatgccagcgcttcgttaa tacagatgtaggtgttccacagggtagccag cagcatcctgcgatgcagatccggaacataa tggtgcagggcgctgacttccgcgtttccag actttacgaaacacggaaaccgaagaccatt catgttgttgctcaggtcgcagacgttttgc agcagcagtcgcttcacgttcgctcgcgtat cggtgattcattctgctaaccagtaaggcaa ccccgccagcctagccgggtcctcaacgaca ggagcacgatcatgctagtcatgccccgcgc ccaccggaaggagctgactgggttgaaggct ctcaagggcatcggtcgagatcccggtgcct aatgagtgagctaacttacattaattgcgtt gcgctcactgcccgctttccagtcgggaaac ctgtcgtgccagctgcattaatgaatcggcc aacgcgcggggagaggcggtttgcgtattgg gcgccagggtggtttttcttttcaccagtga gacgggcaacagctgattgcccttcaccgcc tggccctgagagagttgcagcaagcggtcca cgctggtttgccccagcaggcgaaaatcctg tttgatggtggttaacggcgggatataacat gagctgtcttcggtatcgtcgtatcccacta ccgagatgtccgcaccaacgcgcagcccgga ctcggtaatggcgcgcattgcgcccagcgcc atctgatcgttggcaaccagcatcgcagtgg gaacgatgccctcattcagcatttgcatggt ttgttgaaaaccggacatggcactccagtcg ccttcccgttccgctatcggctgaatttgat tgcgagtgagatatttatgccagccagccag acgcagacgcgccgagacagaacttaatggg cccgctaacagcgcgatttgctggtgaccca atgcgaccagatgctccacgcccagtcgcgt accgtcttcatgggagaaaataatactgttg atgggtgtctggtcagagacatcaagaaata acgccggaacattagtgcaggcagcttccac agcaatggcatcctggtcatccagcggatag ttaatgatcagcccactgacgcgttgcgcga gaagattgtgcaccgccgctttacaggcttc gacgccgcttcgttctaccatcgacaccacc acgctggcacccagttgatcggcgcgagatt taatcgccgcgacaatttgcgacggcgcgtg cagggccagactggaggtggcaacgccaatc agcaacgactgtttgcccgccagttgttgtg ccacgcggttgggaatgtaattcagctccgc catcgccgcttccactttttcccgcgttttc gcagaaacgtggctggcctggttcaccacgc gggaaacggtctgataagagacaccggcata ctctgcgacatcgtataacgttactggtttc acattcaccaccctgaattgactctcttccg ggcgctatcatgccataccgcgaaaggtttt gcgccattcgatggtgtccgggatctcgacg ctctcccttatgcgactcctgcattaggaag cagcccagtagtaggttgaggccgttgagca ccgccgccgcaaggaatggtgcatgcaagga gatggcgcccaacagtcccccggccacgggg cctgccaccatacccacgccgaaacaagcgc tcatgagcccgaagtggcgagcccgatcttc cccatcggtgatgtcggcgatataggcgcca gcaaccgcacctgtggcgccggtgatgccgg ccacgatgcgtccggcgtagaggatcgagat cgatctcgatcccgcgaaattaatacgactc actata | |
| SNAP-25b (1–206, all C to A; capitalized) in pET28a | homemade | tggcgaatgggacgcgccctgtagcggcgca ttaagcgcggcgggtgtggtggttacgcgca gcgtgaccgctacacttgccagcgccctagc gcccgctcctttcgctttcttcccttccttt ctcgccacgttcgccggctttccccgtcaag ctctaaatcgggggctccctttagggttccg atttagtgctttacggcacctcgaccccaaa aaacttgattagggtgatggttcacgtagtg ggccatcgccctgatagacggtttttcgccc tttgacgttggagtccacgttctttaatagt ggactcttgttccaaactggaacaacactca accctatctcggtctattcttttgatttata agggattttgccgatttcggcctattggtta aaaaatgagctgatttaacaaaaatttaacg cgaattttaacaaaatattaacgtttacaat ttcaggtggcacttttcggggaaatgtgcgc ggaacccctatttgtttatttttctaaatac attcaaatatgtatccgctcatgaattaatt cttagaaaaactcatcgagcatcaaatgaaa ctgcaatttattcatatcaggattatcaata ccatatttttgaaaaagccgtttctgtaatg aaggagaaaactcaccgaggcagttccatag gatggcaagatcctggtatcggtctgcgatt ccgactcgtccaacatcaatacaacctatta atttcccctcgtcaaaaataaggttatcaag tgagaaatcaccatgagtgacgactgaatcc ggtgagaatggcaaaagtttatgcatttctt tccagacttgttcaacaggccagccattacg ctcgtcatcaaaatcactcgcatcaaccaaa ccgttattcattcgtgattgcgcctgagcga gacgaaatacgcgatcgctgttaaaaggaca attacaaacaggaatcgaatgcaaccggcgc aggaacactgccagcgcatcaacaatatttt cacctgaatcaggatattcttctaatacctg gaatgctgttttcccggggatcgcagtggtg agtaaccatgcatcatcaggagtacggataa aatgcttgatggtcggaagaggcataaattc cgtcagccagtttagtctgaccatctcatct gtaacatcattggcaacgctacctttgccat gtttcagaaacaactctggcgcatcgggctt cccatacaatcgatagattgtcgcacctgat tgcccgacattatcgcgagcccatttatacc catataaatcagcatccatgttggaatttaa tcgcggcctagagcaagacgtttcccgttga atatggctcataacaccccttgtattactgt ttatgtaagcagacagttttattgttcatga ccaaaatcccttaacgtgagttttcgttcca ctgagcgtcagaccccgtagaaaagatcaaa ggatcttcttgagatcctttttttctgcgcg taatctgctgcttgcaaacaaaaaaaccacc gctaccagcggtggtttgtttgccggatcaa gagctaccaactctttttccgaaggtaactg gcttcagcagagcgcagataccaaatactgt ccttctagtgtagccgtagttaggccaccac ttcaagaactctgtagcaccgcctacatacc tcgctctgctaatcctgttaccagtggctgc tgccagtggcgataagtcgtgtcttaccggg ttggactcaagacgatagttaccggataagg cgcagcggtcgggctgaacggggggttcgtg cacacagcccagcttggagcgaacgacctac accgaactgagatacctacagcgtgagctatg agaaagcgccacgcttcccgaagggagaaa ggcggacaggtatccggtaagcggcagggtc ggaacaggagagcgcacgagggagcttcc agggggaaacgcctggtatctttatagtcctgt cgggtttcgccacctctgacttgagcgtcga tttttgtgatgctcgtcaggggggcggagcc tatggaaaaacgccagcaacgcggccttttt acggttcctggccttttgctggccttttgct cacatgttctttcctgcgttatcccctgatt ctgtggataaccgtattaccgcctttgagtg agctgataccgctcgccgcagccgaacgacc gagcgcagcgagtcagtgagcgaggaagc ggaagagcgcctgatgcggtattttctccttac gcatctgtgcggtatttcacaccgcatatat ggtgcactctcagtacaatctgctctgatgc cgcatagttaagccagtatacactccgctat cgctacgtgactgggtcatggctgcgccccg acacccgccaacacccgctgacgcgccctga cgggcttgtctgctcccggcatccgcttaca gacaagctgtgaccgtctccgggagctgcat gtgtcagaggttttcaccgtcatcaccgaaa cgcgcgaggcagctgcggtaaagctcatcag cgtggtcgtgaagcgattcacagatgtctgc ctgttcatccgcgtccagctcgttgagtttc tccagaagcgttaatgtctggcttctgataa agcgggccatgttaagggcggttttttcctg tttggtcactgatgcctccgtgtaaggggga tttctgttcatgggggtaatgataccgatga aacgagagaggatgctcacgatacgggttac tgatgatgaacatgcccggttactggaacgt tgtgagggtaaacaactggcggtatggatgc ggcgggaccagagaaaaatcactcagggtc aatgccagcgcttcgttaatacagatgtaggt gttccacagggtagccagcagcatcctgcga tgcagatccggaacataatggtgcagggcgc tgacttccgcgtttccagactttacgaaaca cggaaaccgaagaccattcatgttgttgctc aggtcgcagacgttttgcagcagcagtcgct tcacgttcgctcgcgtatcggtgattcattc tgctaaccagtaaggcaaccccgccagccta gccgggtcctcaacgacaggagcacgatcat gcgcacccgtggggccgccatgccggcgata atggcctgcttctcgccgaaacgtttggtgg cgggaccagtgacgaaggcttgagcgagggc gtgcaagattccgaataccgcaagcgacagg ccgatcatcgtcgcgctccagcgaaagcggt cctcgccgaaaatgacccagagcgctgccgg cacctgtcctacgagttgcatgataaagaag acagtcataagtgcggcgacgatagtcatgc cccgcgcccaccggaaggagctgactgggtt gaaggctctcaagggcatcggtcgagatccc ggtgcctaatgagtgagctaacttacattaa ttgcgttgcgctcactgcccgctttccagtc gggaaacctgtcgtgccagctgcattaatga atcggccaacgcgcggggagaggcggtttgc gtattgggcgccagggtggtttttcttttca ccagtgagacgggcaacagctgattgccctt caccgcctggccctgagagagttgcagcaag cggtccacgctggtttgccccagcaggcgaa aatcctgtttgatggtggttaacggcgggat ataacatgagctgtcttcggtatcgtcgtat cccactaccgagatatccgcaccaacgcgca gcccggactcggtaatggcgcgcattgcgcc cagcgccatctgatcgttggcaaccagcatc gcagtgggaacgatgccctcattcagcattt gcatggtttgttgaaaaccggacatggcact ccagtcgccttcccgttccgctatcggctga atttgattgcgagtgagatatttatgccagc cagccagacgcagacgcgccgagacagaa cttaatgggcccgctaacagcgcgatttgctgg tgacccaatgcgaccagatgctccacgccca gtcgcgtaccgtcttcatgggagaaaataat actgttgatgggtgtctggtcagagacatca agaaataacgccggaacattagtgcaggcag cttccacagcaatggcatcctggtcatccag cggatagttaatgatcagcccactgacgcgt tgcgcgagaagattgtgcaccgccgctttac aggcttcgacgccgcttcgttctaccatcga caccaccacgctggcacccagttgatcggcg cgagatttaatcgccgcgacaatttgcgacg gcgcgtgcagggccagactggaggtggcaac gccaatcagcaacgactgtttgcccgccagt tgttgtgccacgcggttgggaatgtaattca gctccgccatcgccgcttccactttttcccg cgttttcgcagaaacgtggctggcctggttc accacgcgggaaacggtctgataagagacac cggcatactctgcgacatcgtataacgttac tggtttcacattcaccaccctgaattgactc tcttccgggcgctatcatgccataccgcgaa aggttttgcgccattcgatggtgtccgggat ctcgacgctctcccttatgcgactcctgcat taggaagcagcccagtagtaggttgaggccg ttgagcaccgccgccgcaaggaatggtgcat gcaaggagatggcgcccaacagtcccccggc cacggggcctgccaccatacccacgccgaaa caagcgctcatgagcccgaagtggcgagccc gatcttccccatcggtgatgtcggcgatata ggcgccagcaaccgcacctgtggcgccggtg atgccggccacgatgcgtccggcgtagagga tcgagatctcgatcccgcgaaattaatacga ctcactataggggaattgtgagcggataaca attcccctctagaaataattttgtttaactt taagaaggagatataccATGGCCGA GGACGCAGACATGCGCAATG AGCTGGAGGAGATGCAGAGG AGGGCTGACCAGCTGGCTGA TGAGTCCCTGGAAAGCACCC GTCGCATGCTGCAGCTGGTT GAAGAGAGTAAAGATGCTGG CATCAGGACTTTGGTTATGTT GGATGAGCAAGGCGAACAAC TGGAACGCATTGAGGAAGGG ATGGACCAAATCAATAAGGAC ATGAAAGAAGCAGAAAAGAAT TTGACGGACCTAGGAAAATTC GCCGGCCTTGCCGTGGCCCC CGCCAACAAGCTTAAATCCAG TGATGCTTACAAAAAAGCCTG GGGCAATAATCAGGATGGAGT AGTGGCCAGCCAGCCTGCCC GTGTGGTGGATGAACGGGAG CAGATGGCCATCAGTGGTGGC TTCATCCGCAGGGTAACAAAT GATGCCCGGGAAAATGAGATG GATGAGAACCTGGAGCAGGT GAGCGGCATCATCGGAAACCT CCGCCACATGGCTCTAGACAT GGGCAATGAGATTGACACCCA GAATCGCCAGATCGACAGGAT CATGGAGAAGGCTGATTCCAA CAAAACCAGAATTGATGAAGC CAACCAACGTGCAACAAAGAT GCTGGGAAGTGGTTAA ctcgagcaccaccaccaccaccactgag atccggctgctaacaaagcccgaaagga agctgagttggctgctgccaccgctgagc aataactagcataaccccttggggcctc taaacgggtcttgaggggttttttgctgaa aggaggaactatatccggat | |
| Materials for protein purificaiton | |||
| 2-Mercaptoethanol | SIGMA | M3148-25ML | |
| Agar | LPS Solution | AGA500 | |
| Ampicillin, Sodium salt | PLS | AC1043-005-00 | |
| Chloramphenicol | PLS | CR1023-050-00 | |
| Competent cells (E. coli) | Novagen | 70956 | Rosetta(DE3)pLysS |
| Glycerol | SIGMA | G5516-500ML | |
| HEPES | SIGMA | H4034-100G | |
| Hydrochloric acid / HCl | SIGMA | 320331-500ML | |
| Imidazole | SIGMA | I2399-100G | |
| Isopropyl β-D-1-thiogalactopyranoside / IPTG | SIGMA | 10724815001 | |
| Kanamycin Sulfate | PLS | KC1001-005-02 | |
| Luria-Bertani (LB) Broth | LPS Solution | LB-05 | |
| Ni-NTA resin | Qiagen | 30210 | |
| PD MiniTrap G-25 (desalting column) | Cytiva | GE28-9180-07 | For instructions, see: https://www.cytivalifesciences.com/en/us/shop/chromatography/prepacked-columns/desalting-and-buffer-exchange/pd-minitrap-desalting-columns-with-sephadex-g-25-resin-p-06174 |
| Phenylmethylsulfonyl fluoride / PMSF | ThermoFisher Scientific | 36978 | |
| Plasmids for SNARE proteins | cloned in house | N/A | Available upon request |
| Protease inhibitor cocktail | genDEPOT | P3100 | |
| Sodium chloride | SIGMA | S5886-500G | |
| Sodium phosphate dibasic / Na2HPO4 | SIGMA | S7907-100G | |
| Sodium phosphate monobasic / NaH2PO4 | SIGMA | S3139-250G | |
| Tris(2-carboxyethyl)phosphine / TCEP | SIGMA | C4706-2G | |
| Trizma base | SIGMA | T1503-250G | |
| Materials for sample assembly | |||
| Biotin-PEG-SVA | LAYSAN BIO | BIO-PEG-SVA-5K-100MG & MPEG-SVA-5K-1g | For PEGylation |
| Dibenzocyclooctyne-amine / DBCO-NH2 | SIGMA | 761540-10MG | For bead coating |
| Double-sided tape | 3M | 136 | For flow cell assembly |
| Epoxy glue | DEVCON | S-208 | For flow cell assembly |
| Glass coverslip for bottom surface | VWR | 48393-251 | Rectangular, 60×24 mm, #1.5 |
| Glass coverslip for top surface | VWR | 48393-241 | Rectangular, 50×24 mm, #1.5 |
| Magnetic bead | ThermoFisher Scientific | 14301 | Dynabeads M-270 Epoxy, 2.8 μm |
| mPEG-SVA | LAYSAN BIO | mPEG-SVA 1g | For PEGylation |
| N,N-Dimethylformamide / DMF | SIGMA | D4551-250ML | For bead coating |
| N-[3-(trimethoxysilyl)propyl]ethylenediamine | SIGMA | 104884-100ML | For PEGylation |
| Neutravidin | ThermoFisher Scientific | 31000 | For sample tethering |
| Phosphate buffered saline / PBS, pH 7.2 | PLS | PR2007-100-00 | |
| Plastic syringe | Norm-ject | A5 | 5 ml, luer tip |
| Polyethylene Tubing | SCI | BB31695-PE/4 | PE-60 |
| Reference bead | SPHEROTECH | SVP-30-5 | Streptavidin-coated Polystyrene Particles; 3.0-3.4 µm |
| Syringe needle | Kovax | 21G-1 1/4'' | 21 G |
| Syringe pump | KD SCIENTIFIC | 788210 | |
| Equipment for magnetic tweezer instrument | |||
| 1-axis motorized microtranslation stage | PI | M-126.PD1 | For vertical positioning of magnets |
| 2-axis manual translation stage | ST1 | LEE400 | For alignment of magnets to the optical axis |
| Acrylic holder for magnets | DaiKwang Precision | custum order | Drawing available upon request |
| Frame grabber | Active Silicon | AS-FBD-4XCXP6-2PE8 | |
| High-speed CMOS camera | Mikrotron | EoSens 3CXP | |
| Inverted microscope | Olympus | IX73P2F-1-2 | |
| Neodymium magnets | LG magnet | ND 10x10x12t | Dimension: 10 mm × 10 mm × 12 mm; two needed |
| Objective lens | Olympus | UPLXAPO100XO | Oil-immersion, NA 1.45 |
| Objective lens nanopositioner | Mad City Labs | Nano-F100S | |
| Rotation stepper motor | AUTONICS | A3K-S545W | For rotating magnets |
| Superluminescent diode | QPHOTONICS | QSDM-680-2 | 680 nm |
| Software | |||
| LabVIEW | National Instruments | v20.0f1 | |
| MATLAB | MathWorks | v2021a |
참고문헌
- Le, S., Liu, R., Lim, C. T., Yan, J. Uncovering mechanosensing mechanisms at the single protein level using magnetic tweezers. Methods. 94, 13-18 (2016).
- Choi, H. -. K., Kim, H. G., Shon, M. J., Yoon, T. -. Y. High-resolution single-molecule magnetic tweezers. Annual Review of Biochemistry. 91 (1), 33-59 (2022).
- Yang, T., Park, C., Rah, S. -. H., Shon, M. J. Nano-precision tweezers for mechanosensitive proteins and beyond. Molecules and Cells. 45 (1), 16-25 (2022).
- Neuman, K. C., Nagy, A. Single-molecule force spectroscopy: optical tweezers, magnetic tweezers and atomic force microscopy. Nature Methods. 5 (6), 491-505 (2008).
- De Vlaminck, I., Dekker, C. Recent advances in magnetic tweezers. Annual Review of Biophysics. 41 (1), 453-472 (2012).
- Bustamante, C. J., Chemla, Y. R., Liu, S., Wang, M. D. Optical tweezers in single-molecule biophysics. Nature Reviews Methods Primers. 1, 25 (2021).
- Gosse, C., Croquette, V. Magnetic tweezers: micromanipulation and force measurement at the molecular level. Biophysical Journal. 82 (6), 3314-3329 (2002).
- Smith, S. B., Finzi, L., Bustamante, C. Direct mechanical measurements of the elasticity of single DNA molecules by using magnetic beads. Science. 258 (5085), 1122-1126 (1992).
- Lansdorp, B. M., Tabrizi, S. J., Dittmore, A., Saleh, O. A. A high-speed magnetic tweezer beyond 10,000 frames per second. Review of Scientific Instruments. 84 (4), 044301 (2013).
- Cnossen, J. P., Dulin, D., Dekker, N. H. An optimized software framework for real-time, high-throughput tracking of spherical beads. Review of Scientific Instruments. 85 (10), 103712 (2014).
- Dulin, D., et al. High spatiotemporal-resolution magnetic tweezers: calibration and applications for DNA dynamics. Biophysical Journal. 109 (10), 2113-2125 (2015).
- Huhle, A., et al. Camera-based three-dimensional real-time particle tracking at kHz rates and Ångström accuracy. Nature Communications. 6 (1), 5885 (2015).
- Popa, I., et al. A HaloTag anchored ruler for week-long studies of protein dynamics. Journal of the American Chemical Society. 138 (33), 10546-10553 (2016).
- Shon, M. J., Kim, H., Yoon, T. -. Y. Focused clamping of a single neuronal SNARE complex by complexin under high mechanical tension. Nature Communications. 9 (1), 3639 (2018).
- Tapia-Rojo, R., Eckels, E. C., Fernández, J. M. Ephemeral states in protein folding under force captured with a magnetic tweezers design. Proceedings of the National Academy of Sciences. 116 (16), 7873-7878 (2019).
- Löf, A., et al. Multiplexed protein force spectroscopy reveals equilibrium protein folding dynamics and the low-force response of von Willebrand factor. Proceedings of the National Academy of Sciences. 116 (38), 18798-18807 (2019).
- Tapia-Rojo, R., Alonso-Caballero, A., Fernandez, J. M. Direct observation of a coil-to-helix contraction triggered by vinculin binding to talin. Science Advances. 6 (21), (2020).
- Rieu, M., et al. Parallel, linear, and subnanometric 3D tracking of microparticles with Stereo Darkfield Interferometry. Science Advances. 7 (6), (2021).
- Rieu, M., Valle-Orero, J., Ducos, B., Allemand, J. -. F., Croquette, V. Single-molecule kinetic locking allows fluorescence-free quantification of protein/nucleic-acid binding. Communications Biology. 4 (1), 1083 (2021).
- Woodside, M. T., et al. Nanomechanical measurements of the sequence-dependent folding landscapes of single nucleic acid hairpins. Proceedings of the National Academy of Sciences. 103 (16), 6190-6195 (2006).
- Camunas-Soler, J., Ribezzi-Crivellari, M., Ritort, F. Elastic properties of nucleic acids by single-molecule force spectroscopy. Annual Review of Biophysics. 45 (1), 65-84 (2016).
- Südhof, T. C., Rothman, J. E. Membrane fusion: grappling with SNARE and SM proteins. Science. 323 (5913), 474-477 (2009).
- Gao, Y., et al. Single reconstituted neuronal SNARE complexes zipper in three distinct stages. Science. 337 (6100), 1340-1343 (2012).
- Zorman, S., et al. Common intermediates and kinetics, but different energetics, in the assembly of SNARE proteins. eLife. 3, e03348 (2014).
- Zhang, Y., Hughson, F. M. Chaperoning SNARE folding and assembly. Annual Review of Biochemistry. 90 (1), 581-603 (2021).
- Vilfan, I. D., Lipfert, J., Koster, D. A., Lemay, S. G., Dekker, N. H. Magnetic tweezers for single-molecule experiments. Handbook of Single-Molecule Biophysics. , 371-395 (2009).
- You, H., Le, S., Chen, H., Qin, L., Yan, J. Single-molecule manipulation of G-quadruplexes by magnetic tweezers. Journal of Visualized Experiments. (127), e56328 (2017).
- Lipfert, J., Hao, X., Dekker, N. H. Quantitative modeling and optimization of magnetic tweezers. Biophysical Journal. 96 (12), 5040-5049 (2009).
- Dulin, D., Barland, S., Hachair, X., Pedaci, F. Efficient illumination for microsecond tracking microscopy. PLoS One. 9 (9), e107335 (2014).
- Klaue, D., Seidel, R. Torsional stiffness of single superparamagnetic microspheres in an external magnetic field. Physical Review Letters. 102 (2), 028302 (2009).
- Shon, M. J., Rah, S. -. H., Yoon, T. -. Y. Submicrometer elasticity of double-stranded DNA revealed by precision force-extension measurements with magnetic tweezers. Science Advances. 5 (6), 1697 (2019).
- Czerwinski, F., Richardson, A. C., Oddershede, L. B. Quantifying noise in optical tweezers by Allan variance. Optics Express. 17 (15), 13255-13269 (2009).
- Lansdorp, B. M., Saleh, O. A. Power spectrum and Allan variance methods for calibrating single-molecule video-tracking instruments. Review of Scientific Instruments. 83 (2), 025115 (2012).
- Ostrofet, E., Papini, F. S., Dulin, D. High spatiotemporal resolution data from a custom magnetic tweezers instrument. Data in Brief. 30, 105397 (2020).
- Yu, Z., et al. A force calibration standard for magnetic tweezers. Review of Scientific Instruments. 85 (12), 123114 (2014).
- Strick, T. R., Allemand, J. -. F., Bensimon, D., Bensimon, A., Croquette, V. The elasticity of a single supercoiled DNA molecule. Science. 271 (5257), 1835-1837 (1996).
- Daldrop, P., Brutzer, H., Huhle, A., Kauert, D. J., Seidel, R. Extending the range for force calibration in magnetic tweezers. Biophysical Journal. 108 (10), 2550-2561 (2015).
- te Velthuis, A. J. W., Kerssemakers, J. W. J., Lipfert, J., Dekker, N. H. Quantitative guidelines for force calibration through spectral analysis of magnetic tweezers data. Biophysical Journal. 99 (4), 1292-1302 (2010).
- Ostrofet, E., Papini, F. S., Dulin, D. Correction-free force calibration for magnetic tweezers experiments. Scientific Reports. 8 (1), 15920 (2018).
- Seol, Y., Li, J., Nelson, P. C., Perkins, T. T., Betterton, M. D. Elasticity of short DNA molecules: theory and experiment for contour lengths of 0.6-7 µm. Biophysical Journal. 93 (12), 4360-4373 (2007).
- Burnham, D. R., Vlaminck, I. D., Henighan, T., Dekker, C. Skewed Brownian fluctuations in single-molecule magnetic tweezers. PLoS One. 9 (9), 108271 (2014).
- Paul, T., Myong, S. Protocol for generation and regeneration of PEG-passivated slides for single-molecule measurements. STAR Protocols. 3 (1), 101152 (2022).
- Lee, H. -. W., et al. Profiling of protein-protein interactions via single-molecule techniques predicts the dependence of cancers on growth-factor receptors. Nature Biomedical Engineering. 2 (4), 239-253 (2018).
- Cheezum, M. K., Walker, W. F., Guilford, W. H. Quantitative comparison of algorithms for tracking single fluorescent particles. Biophysical Journal. 81 (4), 2378-2388 (2001).
- Parthasarathy, R. Rapid, accurate particle tracking by calculation of radial symmetry centers. Nature Methods. 9 (7), 724-726 (2012).
- Woodside, M. T., Block, S. M. Reconstructing folding energy landscapes by single-molecule force spectroscopy. Annual Review of Biophysics. 43 (1), 19-39 (2014).
- Evans, E., Ritchie, K. Dynamic strength of molecular adhesion bonds. Biophysical Journal. 72 (4), 1541-1555 (1997).
- Zhang, Y. Energetics, kinetics, and pathway of SNARE folding and assembly revealed by optical tweezers. Protein Science. 26 (7), 1252-1265 (2017).
- Chen, H., et al. Improved high-force magnetic tweezers for stretching and refolding of proteins and short DNA. Biophysical Journal. 100 (2), 517-523 (2011).
- Cho, S., et al. Tension exerted on cells by magnetic nanoparticles regulates differentiation of human mesenchymal stem cells. Biomaterials Advances. 139, 213028 (2022).
- Shon, M. J., Cohen, A. E. Nano-mechanical measurements of protein-DNA interactions with a silicon nitride pulley. Nucleic Acids Research. 44 (1), 7 (2016).
- Cheng, Y. Single-particle cryo-EM-How did it get here and where will it go. Science. 361 (6405), 876-880 (2018).
- Jumper, J., et al. Highly accurate protein structure prediction with AlphaFold. Nature. 596 (7873), 583-589 (2021).
- Neupane, K., et al. Direct observation of transition paths during the folding of proteins and nucleic acids. Science. 352 (6282), 239-242 (2016).
- Choi, H. -. K., et al. Watching helical membrane proteins fold reveals a common N-to-C-terminal folding pathway. Science. 366 (6469), 1150-1156 (2019).
- Kim, C., et al. Extreme parsimony in ATP consumption by 20S complexes in the global disassembly of single SNARE complexes. Nature Communications. 12 (1), 3206 (2021).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유