JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
폐 환기의 과분극 129Xe 자기 공명 이미지 획득
요약
과분극 129Xe 자기 공명 영상(MRI)은 폐 기능의 국소적으로 해결된 측면을 연구하는 방법입니다. 이 작업은 펄스 시퀀스 설계, 129Xe 선량 준비, 스캔 워크플로우 및 피험자 안전 모니터링을 위한 모범 사례에 특히 주의를 기울여 폐 환기의 과분극 129Xe MRI에 대한 엔드 투 엔드 표준화된 워크플로우를 제시합니다.
초록
과분극 129Xe MRI는 독특한 구조적, 기능적 폐 영상 기법으로 구성되어 있습니다. 최근 FDA가 129Xe를 MR 조영제로 승인하고 연구 및 임상 기관에서 129Xe MRI에 대한 관심이 증가함에 따라 기관 간 기술 표준화가 점점 더 중요해지고 있습니다. 129Xe MRI 임상시험 컨소시엄(Xe MRI CTC)의 회원들은 129Xe MRI 워크플로우의 각 주요 측면에 대한 모범 사례에 동의했으며, 이러한 권장 사항은 최근 간행물에 요약되어 있습니다. 이 작업은 Xe MRI CTC 권장 사항에 따라 폐 환기에 대한 129개의 Xe MR 이미지를 수집하기 위한 엔드 투 엔드 워크플로우를 개발하기 위한 실용적인 정보를 제공합니다. MR 연구를 위한 129Xe의 준비 및 투여는 전체 연구 및 개별 MR 스캔에 적합한 가스량 선택, 개별 129Xe 용량의 준비 및 전달, 연구 중 피험자 안전 및 129Xe 내약성을 모니터링하기 위한 모범 사례를 포함한 특정 주제와 함께 논의되고 시연됩니다. 펄스 시퀀스 유형 및 최적화된 매개변수, 129Xe 플립 각도 및 중심 주파수 보정, 129Xe MRI 환기 이미지 분석을 포함한 주요 MR 기술 고려 사항도 다룹니다.
서문
과분극 129Xe MRI는 폐 기능 1,2,3의 특정 측면에 대한 비침습적, 공간적으로 분해된 특성화 및 정량화를 위한 흥미로운 도구입니다. 해부학적 양성자 MRI에 사용된 것과 유사한 획득 및 재구성 접근법은 폐에서 흡입된 129Xe의 이미지를 생성하여 환기되지 않는 폐 영역의 시각화 및 환기 분포의 영역 분해 정량화를 가능하게 합니다 4,5,6,7,8 . 보다 발전된 펄스 시퀀스 및 분석 기술은 분광 MRI 9,10,11,12,13을 통한 폐포와 폐 모세혈관 간의 가스 교환 효능 정량화 및 확산 가중 MRI 14,15,16을 통한 폐포 미세구조 무결성 특성 분석을 포함한 추가 보완 정보를 제공합니다.
흡입 129Xe는 폐 질환 환자를 포함한 성인 및 소아 피험자에서 안전하고 내약성이 있는 것으로 입증되었습니다17,18. 129Xe MRI에서 유도된 폐 기능 측정은 만성 폐쇄성 폐질환 6,10,19, 낭포성 섬유증 20,21,22, 특발성 폐섬유증 23,24,25 및 천식 7,10을 포함한 많은 폐 질환 맥락에서 구조적 및 기능적 변화에 대한 민감도를 보여주었습니다 ,26. 129Xe MRI의 높은 안전성과 내약성을 감안할 때, 다른 일반적인 영상 접근법에 비해 MRI의 전리 방사선이 부족하고, 129Xe MRI 결과의 높은 재현성을 감안할 때27,28, 129Xe MRI는 특히 만성 폐 질환에 대한 치료 과정을 받는 개인의 정확한 연속 모니터링에 중요한 가능성을 가지고 있습니다.
129Xe MRI의 안전성과 임상적 약속은 2022년 12월 12세 이상29세의 폐 환기 영상에 대한 FDA 승인으로 이어졌습니다. 이를 감안할 때 129Xe MRI(현재 전 세계적으로 ~20개)를 수행할 수 있는 연구 및 임상 현장의 수가 향후 몇 년 동안 크게 증가할 것으로 예상됩니다. 129Xe MRI가 새로운 기관으로 확산됨에 따라, 시험기관에서 임상적으로 관련된 129Xe MRI 기술을 신속하게 구축하고 스캔을 수행하고 기존 시험기관과 거의 유사한 결과를 생성할 수 있도록 강력한 방법론적 리소스가 존재하는 것이 중요합니다.
이 연구에서는 129Xe MRI 임상시험 컨소시엄(Xe MRI CTC)의 회원 기관이 합의하고 최근 입장 보고서30에 요약된 인간 과분극 129Xe MRI의 폐 환기에 대한 현재 모범 사례를 간략하게 설명합니다. 주제에는 완전한 129Xe MRI 워크플로우에 이상적인 맞춤형 펄스 시퀀스 준비, 과분극 129Xe 가스의 준비 및 관리, 인간 129Xe MRI 세션에 최적화된 워크플로우, MRI 세션 중 피험자의 안전과 편안함을 모니터링하기 위한 모범 사례가 포함됩니다.
프로토콜
인간을 대상으로 하는 모든 연구는 기관 검토 위원회(IRB)의 승인을 받아야 합니다. IRB 참여는 129Xe MRI의 규제 승인 임상 사용에 필요하지 않습니다. 연구에 참여하기 전에 예비 피험자에게 승인된 정보에 입각한 동의 문서를 제공해야 합니다. 동의를 받는 사람은 연구의 목적, 절차, 이점 및 위험을 포함하여 문서의 내용을 설명해야 하고, 모든 질문에 답해야 하며, 정보에 입각한 동의서에 피험자의 서명으로 문서화된 대로 연구를 진행하기 위해 피험자로부터 동의를 얻어야 합니다. 소아 피험자 또는 기타 특별한 상황의 경우, 동의를 얻기 위해 승인된 관행을 따라야 합니다. 이하에 기술된 프로토콜은 버지니아 대학교 IRB의 가이드라인을 따르며, 본 원고의 예시 피험자들은 버지니아 대학교 IRB가 승인한 동의서(IRB 13647, 16215, 16885, 19569)에 서명하였다.
1. 129Xe MRI를 위한 하드웨어 및 펄스 시퀀스 준비
알림: 1단계의 프로토콜 단계는 사람을 스캔하기 전에 수행해야 합니다. 각 과목에 대해 반복할 필요는 없습니다.
- MRI 스캐너가 129Xe를 포함한 다핵 작동이 가능한지 확인합니다.
- 필요한 경우 특수 제작된 코일-스캐너 인터페이스 박스를 사용하여 129Xe 무선 주파수(RF) 코일을 MRI 스캐너에 연결할 수 있는지 확인합니다.
- 스캐너 제조업체에서 요구하는 경우 129Xe RF 코일을 MRI 스캐너에 인터페이스하기 위한 적절한 소프트웨어(코일 파일이라고도 함)가 설치되어 있는지 확인합니다.
- 아래 설명된 대로 129Xe 및 1H 이미징을 위한 펄스 시퀀스를 준비합니다.
- 129Xe 교정의 경우, 표 1에 제공된 펄스 시퀀스 파라미터를 사용하여 일련의 자유 유도 감쇠(FID)로 구성된 국소화되지 않은 분광 시퀀스를 준비합니다.
참고: ~218ppm(용해상 주파수)에서 획득한 FID는 주로 용해상 129Xe MRI의 매개변수를 결정하는 데 사용되며, 이는 본 연구에서 다루지 않습니다. 그러나 이러한 매개변수는 모든 유형의 129Xe MRI 스캔에 충분한 단일 표준화된 129Xe 보정을 개발할 수 있도록 제공됩니다. 또한 현장이 충분한 경험을 쌓으면 129Xe 환기 이미징만 포함하는 연구의 경우 별도의 보정 스캔이 필요하지 않을 수 있습니다. 129Xe 작동 주파수는 스캐너에서 결정한 1H주파수를 129Xe 대 1H 자이로 자기 비율의 비율로 조정하여 정확하게 추정할 수 있으며, 송신기 교정은 축적된 경험과 피험자 무게를 기반으로 추정할 수 있습니다. - 129Xe 환기 MRI의 경우 표 2에 제공된 펄스 시퀀스 매개변수를 사용하여 2차원(2D) RF 손상 그래디언트 에코 시퀀스를 준비합니다. 129Xe가 표적 핵으로 선택되었는지 확인하십시오.
- 기존의 1H해부학적 MRI의 경우 표 2에 제공된 매개변수를 사용하여 싱글샷 터보/고속 스핀 에코 시퀀스 또는 RF 손상 그래디언트 에코 시퀀스를 준비합니다.
알림: 129Xe 환기 및 1H 해부학적 시퀀스의 경우 FOV와 슬라이스 수는 피사체에 따라 다릅니다. 스캔 세션을 시작할 때 이러한 매개변수를 선택하여 3차원 모두에서 폐를 완전히 덮을 수 있도록 합니다.- 위상 오버샘플링을 활성화하여 이미징 FOV에 대한 암의 잠재적인 앨리어싱을 완화합니다.
- MRI 스캐너 공급업체의 제한으로 인해 제안된 거친 평면 내 해상도(4mm x 4mm)에서 싱글샷 터보/고속 스핀 에코 시퀀스가 작동하지 않을 수 있습니다. 이 경우 원하는 해상도의 정수 계수인 해상도(예: 2mm x 2mm)를 사용합니다.
참고: 1시간 해부학적 스캔은 2D RF 손상 그래디언트 에코 시퀀스를 사용하여 획득할 수 있습니다. 이 경우 표 2 에 제공된 환기 스캔 매개변수와 동일한 매개변수를 사용하되 위상 오버샘플링을 활성화하여 암이 이미징 FOV에 앨리어싱되는 것을 방지합니다.
- 129Xe 교정의 경우, 표 1에 제공된 펄스 시퀀스 파라미터를 사용하여 일련의 자유 유도 감쇠(FID)로 구성된 국소화되지 않은 분광 시퀀스를 준비합니다.
- 129Xe 스캔의 경우 열 편파 129Xe 팬텀31, 1 H 스캔의 경우 1H 팬텀을 스캔하여 위에서 설명한 RF 코일 및 펄스 시퀀스의 작동을 확인합니다.
| 매개 변수 | 교정 | ||
| TR (트랜스) | 15밀리초 | ||
| 테 | 0.45 ms (3 T), 0.8 ms (1.5 T) | ||
| RF 펄스 | 창 싱크 | ||
| RF 지속 시간 | 0.65-0.69 ms (3 T), 1.15-1.25 ms (1.5 T) | ||
| 플립 각도 | 20° | ||
| RF 주파수 | 218 ppm (용해상), 0 ppm (기체상) | ||
| 체류 시간 | 39 마이크로초의 | ||
| 대역폭 | 25.6 kHz의 | ||
| 아니요. 샘플 수 | 256(오버샘플링 제외, 사용되는 경우) | ||
| 판독 기간 | 10밀리초 | ||
| FID 수 | 1 노이즈 (RF 없음), 용존 위상 주파수에서 499, 기체상 주파수에서 20. | ||
| 그라디언트 스포일링 | 최소 15mT/m-ms의 모멘트(각 축, 각 FID 후) | ||
| 기간 | ~8초 | ||
표 1: 129Xe 교정을 위한 권장 펄스 시퀀스 파라미터. 파라미터는 국소화되지 않은 분광 129Xe 교정 펄스 시퀀스에 대해 제공됩니다.
| 매개 변수 | 환기 | 해부학 |
| 시퀀스 유형 | RF 스포일드 그래디언트 에코 | 싱글샷 터보/고속 스핀 에코 |
| TR (트랜스) | <10ms | 무한 |
| 테 | <5밀리초 | <50밀리초 |
| 에코 간격 | 해당 없음 | 3-5밀리초 |
| 여기 플립 각도 | 8-12° | 90° |
| 플립 각도 초점 재조정 | 해당 없음 | ≥90°(SAR 한계 내에서 가장 높은 허용 범위) |
| 슬라이스 두께 | 15의 mm | 15의 mm |
| 슬라이스 간격 | 없음 | 없음 |
| 슬라이스 방향 | 코로나 | 코로나 |
| 슬라이스 순서 | 순차(전방에서 후방으로) | 순차(전방에서 후방으로) |
| 단계 인코딩 순서 | 순차(왼쪽에서 오른쪽으로) | 순차(왼쪽에서 오른쪽으로) |
| 넥스 | 1 (최대 7/8 부분 푸리에 허용) | 하프 푸리에 |
| 비대칭 에코 | 허용 | 해당 없음 |
| 복셀 크기 | 4 x 4 x 15 밀리미터3 | 4 x 4 x 15 밀리미터3 |
| 에코당 샘플링 지속 시간 | 5-7밀리초 | 1-1.5밀리초 |
| 검사 기간 | 8-12 초 | ≤16 초 |
표 2: 129Xe 인공호흡 및 1H 해부학적 이미징을 위한 권장 펄스 시퀀스 매개변수. 129Xe 환기 이미징을 위한 2D RF 손상 고속 그래디언트 에코 시퀀스(첫 번째 열)와 1H해부학적 이미징을 위한 2D 싱글샷 터보/고속 스핀 에코 시퀀스(두 번째 열)에 대한 파라미터가 제공됩니다. 해부학적 스캔은 2D RF-spoiled gradient echo sequence를 사용하여 획득할 수도 있습니다. 이 경우 여기에 제공된 환기 스캔 매개변수와 동일한 매개변수를 사용하되 이미징 FOV에 팔의 앨리어싱을 방지하기 위해 필요에 따라 위상 오버샘플링을 추가합니다. 또한 수신기 대역폭을 지정하는 특정 방법은 스캐너 제조업체마다 다르지만 에코당 지정된 샘플링 기간에서 모든 스캐너 제조업체에 대해 올바른 값을 계산할 수 있습니다.
2. 129Xe MRI 후보 스크리닝 및 준비
- MR 안전 양식으로 조사하여 장래 피험자에게 MRI에 대한 금기 사항이 없는지 확인하십시오. 보충 파일 1 은 버지니아 대학교에서 사용되는 예제 양식을 보여줍니다.
- 예상 피험자가 129Xe MRI 검사와 관련된 제외 기준을 충족하지 않는지 확인합니다(여기에는 백분율 예측 FEV1 미만, 이전 6주 이내에 비대상성 호흡기 상태, 129Xe RF 코일의 내부 둘레보다 큰 흉부 둘레, 불안정한 심장 질환 병력이 포함될 수 있지만 이에 국한되지 않음).
알림: 즉각적인 배제를 나타내지는 않지만 신중한 개별 고려가 필요한 추가 기준에는 기준선에서 상당한 보충 산소의 필요성(즉, 비강 캐뉼라에 의해 3L/min 이상) 및 기준선 이상이 있는 신경학적 장애의 병력이 포함됩니다. - 영상 방문 중에 폐 확산 검사(DLCO) 또는 폐활량 측정을 수행하는 경우 연구 방문 당일에 피험자에게 탄산 음료를 섭취하지 않도록 지시합니다. 피험자가 처방된 호흡기 약물을 사용하는 경우 연구 프로토콜에 명시된 경우 복용을 연기하거나 자제하도록 지시합니다.
3. 과분극 129Xe 용량의 준비
참고: 자세한 129Xe 편광자 및 편광 측정 스테이션 지침은 독점적이며 각 공급업체에 따라 다릅니다. 아래 지침은 일반적인 스핀 교환 광학 펌핑 129Xe 편광판 작동에 대한 기본 요약으로 구성됩니다.
- 피험자에 대한 투여량을 결정하십시오. 일반적으로 모든 피험자에 대해 1L의 총 투여량이 선택되며, 이 총 투여량은 129Xe MRI에 대한 FDA 라벨에 명시되어 있습니다. 그러나, 현재의 Xe MRI CTC 권고안(30 )은 총 투여량(크세논과 질소 또는 헬륨)이 피험자의 강제 폐활량(FVC)의 1 /5을 목표로 삼아야 각 피험자가 흡입할 수 있는 편안한 양의 가스를 보장하고 피험자 간의 폐 용적 차이와 관련된 영향을 최소화할 수 있다고 제안한다.
- 피험자에 대한 최근 폐활량 측정 결과를 사용할 수 있는 경우 이를 사용하여 FVC의 1/5을 측정합니다. 폐활량 측정 결과를 사용할 수 없는 경우 키, 성별 및 인종을 기준으로 피험자의 총 폐활량(TLC)을 추정하고 총 선량을 TLC의 1 /6로 추정합니다.
- 분극할 크세논 가스의 부피를 결정하십시오.
참고: 각 용량 백에 대한 목표 크세논 부피는 개념적으로 100% 농축, 100% 편광 129Xe 가스의 등가 부피를 나타내는 용량 등가물(DE) 부피로 제공됩니다. 개념적으로 DE 볼륨은 129Xe 스캔의 예상 신호 대 노이즈 비율(SNR)에 정비례하며, 권장 DE 볼륨은 해당 스캔 유형에 필요한 SNR에 따라 특정 129Xe 스캔 유형에 대해 더 높거나 낮습니다.- 다음과 같이 주어진 크세논 용량에 대한 DE 부피를 계산합니다32:
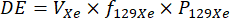
여기서 VXe 는 선량 내 크세논 가스( 129Xe뿐만 아니라 모든 동위원소)의 총 부피이고, f129Xe 는 129Xe동위원소 농축이며, P129Xe 는 129Xe분극입니다. - 수행할 129개의 Xe 스캔 세트에 필요한 총 DE 볼륨을 선택합니다. 개별 보정 및 환기 스캔에 권장되는 DE 부피는 75-150mL입니다.
참고: 환기 이미징의 경우 SNR은 환기된 이미지 복셀과 환기되지 않은 이미지 복셀을 명확하게 구별할 수 있을 만큼 충분히 높아야 합니다. 50mL의 DE 부피는 적어도 20의 예상 SNR을 달성하기 위한 환기 이미징(30 )의 절대 최소값으로 간주됩니다. 교정 스캔의 경우, 기체상 신호만 교정하는 경우 25mL의 낮은 DE 부피가 허용될 수 있습니다. 기체상 및 용해상 신호를 모두 교정하는 경우 최소 75mL를 사용해야 합니다.
- 다음과 같이 주어진 크세논 용량에 대한 DE 부피를 계산합니다32:
- 필요한 총 DE 부피, 크세논 가스의 알려진 129Xe 등방성 농축 및 이전 분극 실행을 기반으로 추정된 129Xe 분극을 사용하여 분극에 필요한 총 크세논 가스 부피를 계산합니다. 129Xe 동위원소 농축이 85%이고 편광이 20%라고 가정할 때 1회의 환기 스캔(DE 부피 = 75mL)에 대한 계산 예가 아래에 나와 있습니다.32:
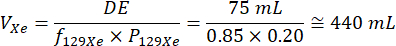
각 제논 투여량에 대해 이 계산을 수행하여 각 투여량 백에 분배할 극성 크세논 가스의 정확한 부피를 결정합니다.- BMI(<21)가 낮은 피험자는 다른 피험자보다 129Xe 흡입 후 더 심오한 중추신경계(CNS) 영향의 위험이 더 높습니다. BMI가 낮은 피험자를 촬영하기 전에 의사와 상담하고 이러한 잠재적인 문제를 피하기 위해 129Xe 선량을 최소화하는 것을 고려하십시오.
- 편광판 공급업체에서 제공한 모든 지침에 따라 129Xe 편광판을 준비합니다.
- 편광판 공급업체에 따라 단계가 포함될 수 있습니다: Helmholtz 코일 전원 공급 장치가 켜져 있는지 확인하십시오. 불순물을 제거하기 위해 배출구 매니폴드를 비우십시오. 차가운 손가락 주위/아래에 액체 질소 듀어를 설치하십시오. 레이저의 전원을 켜고 예열하십시오. 오븐의 공기 흐름을 켜고 오븐 컨트롤러를 사용하여 오븐을 적절한 온도로 설정한 다음 오븐을 예열합니다.
주의 : 액체 질소는 피부, 눈 또는 의복에 닿으면 심각한 동상을 유발할 수 있으며 고강도 레이저 광선은 보호 장치 없이 눈에 닿으면 눈 부상을 유발할 수 있습니다. 적절한 주의를 기울이고 필요에 따라 보호 장비를 착용하십시오.
- 편광판 공급업체에 따라 단계가 포함될 수 있습니다: Helmholtz 코일 전원 공급 장치가 켜져 있는지 확인하십시오. 불순물을 제거하기 위해 배출구 매니폴드를 비우십시오. 차가운 손가락 주위/아래에 액체 질소 듀어를 설치하십시오. 레이저의 전원을 켜고 예열하십시오. 오븐의 공기 흐름을 켜고 오븐 컨트롤러를 사용하여 오븐을 적절한 온도로 설정한 다음 오븐을 예열합니다.
- 129Xe 편광 측정 스테이션의 전원이 켜져 있고 소프트웨어가 선량 편광을 측정할 준비가 되었는지 확인합니다.
- 다음 단계를 수행하여 과분극 129Xe 수집을 시작합니다.
- 차가운 손가락 워밍 재킷으로 질소 흐름을 시작합니다.
- 크세논 혼합물이 차가운 손가락으로 흐르기 시작합니다. polarizer 설명서의 polarizer performance curves를 참조하여 최적의 유속을 선택하십시오.
- 차가운 손가락을 둘러싼 듀어에 액체 질소를 추가합니다.
- 정확한 편광 볼륨을 보장하기 위해 데이터 시트에 편광 시작 시간을 기록합니다.
- 수집이 시작되면 유량 및 오븐 컨트롤러를 조정하여 일관된 유량과 온도를 유지하고 필요에 따라 액체 질소를 추가하여 듀어를 가득 채운 상태로 유지합니다.
- 크세논이 축적되는 동안 백의 불순물 및/또는 탈분극 가스를 최소화하기 위해 편광판 출구 매니폴드를 사용하여 백을 최소 3회 반복적으로 퍼지 및 배출하여 투여량 수집을 위한 Tedlar 투여 백을 준비합니다.
- 원하는 hyperpolarized 129Xe volume의 분취를 위한 적절한 시간이 경과하면 편광판 설명서의 지시에 따라 hyperpolarized 129Xe 분광을 종료합니다.
- 차가운 손가락에 침전된 얼어붙은 129Xe를 아래 설명과 같이 해동합니다.
- 129Xe 투여 백을 배출구 매니폴드의 크세논 배출구에 부착합니다.
- 액체 질소 듀어를 조심스럽게 제거하고 실온의 물이 담긴 해동 용기로 교체하십시오.
- 해동하는 동안 압력을 지속적으로 모니터링하여 압력이 편광판 설명서에 제공된 임계값에 도달하면 콜드 핑거에서 크세논 배출구로 유량 밸브를 열고 압력이 떨어지면 밸브를 빠르게 닫습니다.
- 투여 백에서 원하는 양의 크세논에 도달할 때까지 이러한 방식으로 승화된 크세논 가스를 투여 백에 계속 분배합니다.
- 버퍼 가스(질소 또는 헬륨)가 이전에 백에 추가되지 않은 경우 이때 추가하십시오.
- 원하는 모든 크세논 및 완충 가스가 백에 추가되면 백 튜브의 핀치 클램프를 빠르게 닫고 크세논 배출 밸브를 닫은 다음 편광판에서 전체 용량 백을 분리합니다.
- 백을 129Xe 편광 측정 스테이션의 Helmholtz 코일 쌍에 의해 생성된 자기장으로 즉시 이동합니다.
주의 : 크세논 가스가 따뜻해지고 승화됨에 따라 차가운 손가락에 압력이 빠르게 형성되어 압력이 안전 한계를 넘어 형성되면 잠재적인 폭발 위험이 발생합니다. 편광판 설명서에 제공된 이 단계의 지침을 정확히 따르고 이 단계를 수행하는 동안 보안경을 착용하십시오.
- 편광 측정 스테이션 공급업체에서 제공한 지침에 따라 129Xe 편광 측정 스테이션의 각 선량 백에서 편광을 측정하고 기록합니다.
- 편광이 측정되면 피험자에게 투여할 준비가 될 때까지 편광 측정 스테이션의 Helmholtz 코일 쌍에 의해 생성된 자기장에 129Xe 투여 백을 보관합니다.
4. 피험자의 사전 스캔 준비 및 코칭
참고: 피험자가 6분 보행 테스트가 포함된 전체 검사를 받는 경우 129Xe MRI 결과에 잠재적으로 영향을 미칠 수 있는 방식으로 피험자를 지치게 하는 것을 방지하기 위해 129Xe MRI가 완료될 때까지 걷기를 하지 않는 것이 좋습니다. 이는 특히 심폐 질환 환자와 관련이 있습니다.
- 피험자가 2단계에서 설명한 대로 모든 방문 전 지침을 올바르게 수행했는지, 피험자가 선별된 이후 연구 제외 기준을 충족하거나 MRI 금기 사항을 구성하는 건강 변화가 발생하지 않았는지 확인합니다.
- 심전도(ECG)를 포함하여 피험자에 대해 필요한 모든 신체 검사를 수행합니다. 체온, 심박수, 호흡수, 혈중 산소 포화도(SpO2) 및 혈압을 포함한 바이탈 모음; 폐활량 측정; 및 DLCO 테스트.
- 낮은 SpO2 (<92%), 혈압 상승 또는 피험자에 대한 기존 기준선과 테스트 결과의 상당한 편차를 포함하여 잠재적인 경고 징후에 대해 이러한 테스트를 모니터링합니다.
알림: 이러한 판독값, 특히 기준선 SpO2는 129Xe흡입 중에 경미한 일시적인 산소 불포화도가 발생할 것으로 예상되기 때문에 확인됩니다. 기준선 SpO2<92% 또는 기타 경고 징후가 있는 피험자의 경우 의사와 상담하여 129Xe MRI 검사에 대한 피험자의 적합성과 129Xe 흡입 사이에 보충 O2를 사용할지 여부를 확인하십시오. - 아래에 설명된 대로 올바른 129Xe 흡입 절차로 피험자를 지도하십시오.
- 피험자가 스캐너 밖에서 연습할 수 있도록 공기가 들어 있는 하나 이상의 테들라 백을 준비합니다. 실제 연구 중에 백에서 흡입될 크세논 및 완충 가스의 총 부피와 일치하는 공기량을 사용하십시오.
- 숨 참기 스캔 중에 피사체가 착용할 수 있도록 코 클립을 준비합니다. 숨을 참기 시작하기 전에 코 클립을 피사체의 코에 맞춥니다(연습 및 실제 스캔 모두).
- 아래 지침에 따라 각 시도에 대해 하나의 공기 충전 백을 사용하여 피험자를 코치하십시오. 피험자는 기능적 잔류 용량의 목표 부피에서 주머니를 흡입하기 시작해야 한다. 아래 절차를 밟는 동안, 피험자의 흉부를 관찰하여 지시한 대로 지시를 이행하고 있는지 확인한다.
- 가방을 준비하되 아직 피험자에게 투여하지 마십시오. 피험자에게 다음과 같이 질문하십시오. 규칙적으로 숨을 들이마십니다. 숨을 내쉬세요. 규칙적으로 숨을 들이마신다. 숨을 내쉬세요.
- 테들라 백에 부착된 튜브를 피험자의 입에 넣는다. 피험자가 숨을 들이쉴 수 있는 가방을 잡고 밸브를 엽니다. 피험자에게 다음과 같이 질문하십시오: 숨을 들이쉬십시오. 숨을 들이마신다. 숨을 들이마신다.
- 피험자가 가방 내용물을 모두 흡입하면, 피험자에게 다음과 같이 요청한다: 숨을 참는다. 즉시 스캐너 작업자에게 다음을 지시하십시오.
알림: 피사체를 스캔할 때 스캐너 작업자는 Go! 이 지시는 피험자를 위한 것이 아니지만(즉, 피험자는 가만히 있어야 하며, 직전에 지시된 대로 계속 숨을 참아야 한다), 피험자에게 스캔이 임박했음을 경고한다. - 스캔이 완료될 때까지 기다리거나 연습할 때 일반적인 10 Xe 스캔이 경과하는 데 필요한 대략적인 시간인 15-129초 동안 카운트합니다.
- 피험자에게 숨을 쉬라고 한다. 이 시점에서 피험자는 숨을 내쉰다. 피험자에게 이 시점에서 심호흡을 여러 번 하고 내쉬도록 지도하여 폐에서 129Xe를 더 빨리 제거하고 정상 산소 포화도 수준으로 더 빨리 돌아갈 수 있도록 합니다.
- 피험자가 이 지침을 안정적으로 수행할 수 있는지 확인하십시오. 전체 가스량을 흡입할 수 없거나, 숨을 참을 수 없거나, 테스트 중 숨 참기 시도 중에 지속적으로 기침을 하는 피험자를 제외하는 것을 고려하십시오.
참고: 이 테스트의 결과는 가능한 이미징 품질을 결정하는 데 중요합니다. 신뢰할 수 있는 피험자 순응도에 대한 이러한 검사는 소아 영상 및 중증 폐 질환의 영상 맥락에서 특히 중요한데, 이러한 범주 중 하나 또는 둘 다에 속하는 피험자는 필요한 숨 참기를 안정적으로 완료하는 데 어려움을 겪을 가능성이 더 높기 때문입니다.
5. MRI 스캐너실 준비 및 스캐너 환자 테이블에 피험자 위치 지정
- MRI 스캐너실에 들어가거나 들어갈 것으로 예상되는 사람(피험자 및 직원)은 스캐너실에 들어가기 전에 주머니와 사람에게서 모든 금속 및/또는 전자 물체를 꺼내야 합니다.
- 129Xe 조끼 코일을 스캐너에 꽂고 MRI 스캐너 환자 테이블에 올려 놓아 준비합니다.
- 피험자에게 환자 탁자 위에 발을 먼저 눕히고 누운 자세(또는 스캐너실의 배치에 더 적합한 경우 머리를 먼저 누운 자세)로 눕도록 지시합니다. 피험자의 머리, 무릎 등에 베개를 놓고, 피험자와 상의하여 피험자가 검사 내내 편안하게 가만히 누워 있을 수 있도록 한다.
- 129Xe 조끼 코일을 피험자의 가슴에 고정합니다. 머리-발 방향의 코일 정중선이 폐 주변부의 신호 감소를 피하기 위해 편안한 폐 팽창 수준에서 피험자 폐의 예상 정중선에 최대한 가깝게 놓이도록 합니다.
알림: 코일을 피사체의 발 방향으로 너무 멀리 배치하는 것은 일반적인 오류입니다. 위의 지시에 따라 코일을 배치하면 코일이 순진하게 예상할 수 있는 것보다 피험자의 머리 쪽으로 더 멀리 놓일 수 있습니다. 추가로, 피험자의 가슴 지름이 필요하다면 피험자의 팔을 머리 위와 코일 바깥쪽에 위치시켜야 할 수도 있다. 이 포지셔닝이 필요한 특정 가슴 직경은 특정 스캐너 및 코일 하드웨어에 따라 다릅니다. 작은 피사체의 경우 팔을 머리 위와 코일 외부 또는 측면과 코일 내부에 배치할 수 있습니다. - MRI 스캐너실의 환자 테이블 옆에 MRI 안전 맥박 산소 측정기를 설치하고 맥박 산소 측정기 프로브를 피험자에게 연결합니다. 맥박 산소 측정기가 올바르게 판독되고 있는지 확인하십시오.
- 피험자의 코에 비강 캐뉼라를 놓고(또는 건강한 피험자의 경우 스캐너실에 대기시켜 두십시오) 투여 흡입 후 피험자의 SpO2 가 10분 이상 2% 이상 떨어지면 사용할 산소 공급원에 연결합니다. 산소 탱크와 조절기를 도달 가능한 거리 내의 지역 안전 정책에 따라 MR 안전 방식으로 배치하십시오.
- 환자 테이블을 MRI 스캐너로 전진시켜 코일/피험자의 폐 정중선을 스캐너의 등중심에 맞춥니다.
6. 스캔 절차
- MRI 스캐너의 사용자 인터페이스에서 피험자 데이터를 입력하고 이전에 준비된(1단계에서 설명한대로) 129Xe MRI 프로토콜을 엽니다.
- 3단계에서 설명한 대로 129Xe 도즈가 준비되었고 129Xe 도즈 백이 편광 측정 스테이션의 Helmholtz 코일 쌍(또는 동등한 장치)에 의해 생성된 자기장에 있어 129Xe 탈분극 속도를 최소화하는지 확인합니다.
- 아래 설명된 대로 공급업체에서 제공하는 표준 프로토콜(예: 3면 로컬라이저)을 사용하여 1시간 로컬라이저 스캔을 수행합니다.
- 피험자에게 편안하고 자연스러운 숨을 들이마시고 숨을 참으라고 지시한다. 피험자가 숨을 참는 동안 로컬라이저 스캔을 실행합니다.
- MRI 스캐너 인터페이스에서 로컬라이저 스캔 결과를 봅니다. 이미지에 아티팩트가 표시되는 경우(예: 금속이 포함된 의류가 제거되지 않은 경우) 문제를 해결하고 로컬라이저를 반복합니다. 로컬라이저 FOV가 피사체의 중심에 제대로 맞지 않으면 피사체의 위치를 변경하고 반복합니다. 적절한 지역화 이미지를 얻었으면 다음 단계로 진행합니다.
- 아래 설명된 대로 129Xe 스캔에 대한 초기 사전 스캔 조정을 수행합니다.
- 로컬라이저에서 1H중심 주파수를 3.61529(1H와 129Xe의 각 자이로자기 비율의 근사치)로 나누어 초기 129Xe중심 주파수를 설정합니다.
- 유사한 신체 습관을 가진 이전 피험자의 보정 결과를 기반으로 초기 129Xe 송신기 설정을 설정하고, 1H기준 전압을 기반으로 스케일링합니다.tage 또는 피험자의 측정된 체중. 129Xe 송신기 설정에 대한 세부 정보는 스캐너 및 129Xe 코일 제조업체에 따라 다릅니다.
- 모든 129Xe 획득에 스캐너의 기본 shim 설정을 사용합니다.
- 위에서 설명한 사전 스캔 조정을 수행한 후 129Xe 보정 스캔을 획득하여 아래 설명된 대로 129Xe 중심 주파수 및 송신기 설정을 찾습니다.
- 준비된 프로토콜에서 129Xe 교정 시퀀스를 로드합니다. 모든 펄스 시퀀스 매개변수가 원하는 대로인지 확인하고 클릭 한 번으로 스캔을 실행할 수 있도록 스캔 실행 설정을 지정합니다.
- 편광 측정 스테이션에서 129Xe 보정 스캔을 위한 129Xe 도즈 백을 스캐너실로 가져옵니다. 복용 백을 피험자 근처에 준비하거나 놓습니다. 자기장 강도가 급격히 변하는 보어 개구부 근처의 영역을 피하십시오.
- 피험자가 4단계에서 설명한 코치된 흡입 절차에 따라 가방에서 129Xe 용량을 흡입하도록 돕습니다.
- Go!가 들리는 즉시 스캔을 실행하십시오. 피험자를 돕는 개인이 신호를 보냅니다.
- 스캔이 진행되는 동안 피사체를 모니터링합니다. 피험자가 눈에 띄게 숨을 내쉬거나, 기침을 하거나, 움직이거나, 움직이면 가능하면 스캔을 반복하십시오.
- 스캔이 끝나자마자 피험자에게 숨을 내쉬고 자유롭게 숨을 쉬도록 지시합니다.
- 스캔 후 맥박 산소 측정기를 사용하여 피험자의 심박수와 SpO2 를 모니터링하고 피험자와의 구두 의사 소통을 통해 일시적인 중추 신경계 영향(예: 현기증, 현기증, 행복감 및 감각 이상)을 모니터링합니다.
참고: 3.2단계에서 언급한 바와 같이 체지방 함량이 낮은 피험자를 제외하고 거의 모든 피험자는 개입이 필요하지 않은 매우 경미한 CNS 효과를 경험하게 됩니다. - 기준선에서 벗어난 부분이 사라질 때까지 기다렸다가 다른 129Xe 용량을 투여하십시오. 기준선에서 유의미한 편차가 발생하지 않으면 2분 이상 기다렸다가 129Xe용량을 추가로 투여하십시오.
알림: 산소 불포화 및 회복의 일반적인 시간 과정은 다음과 같습니다: 포화 제거는 129Xe 흡입을 완료한 후 10-20 심장 박동을 시작하고, 천저(nadir)는 흡입 완료 후 20-30 심장 박동을 발생시키며, 회복은 흡입 완료 후 45-50 심장 박동 이내에 발생합니다. 대부분의 불포화는 129Xe 흡입 후 30초 이내에 해결되며 일반적으로 2분 이내에 완전히 해결될 것으로 예상됩니다. 지속적인 불포화 상태(피험자 기준선의 10% 이상)가 2분 이상 계속되는 경우 추가 129Xe 용량을 투여하지 않거나 연구를 종료하는 것이 좋습니다.
- 아래 설명된 대로 129Xe 보정 분석을 수행합니다(예: 독립형 분석 도구 사용).
- 첫 번째 기체상 FID의 스펙트럼을 사용하여 129Xe중심 주파수를 결정합니다.
- 아래 설명된 대로 129Xe 송신기 조정을 결정합니다.
- 20개의 기체상 FID의 피크 강도를 다음 함수30에 피팅하고 α 플립 각도를 구합니다.
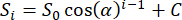
여기서 Si는 i번째 여기로 인한 신호 강도의 크기이고, S0는 첫 번째 여기로부터의 신호 강도의 크기이며, C는 노이즈 오프셋 파라미터입니다. - α 얻으면 표 129에서 권장하는 대로 의도한 교정 플립 각도로 20°가 사용되었다고 가정하고 후속 스캔을 위한 초기 1 Xe 송신기 설정을 1°/α 조정합니다.
- 20개의 기체상 FID의 피크 강도를 다음 함수30에 피팅하고 α 플립 각도를 구합니다.
- 최종 129Xe 사전 스캔 조정이 이루어지고 피험자가 다음 129Xe 투여를 받을 준비가 되면 아래 설명된 대로 129Xe 환기 스캔을 수행합니다.
- 준비된 프로토콜에서 129Xe 환기 시퀀스를 로드합니다. 모든 펄스 시퀀스 매개변수가 원하는 대로인지 확인하고 한 번의 클릭 후 즉시 스캔이 시작되도록 스캔 실행 설정을 지정합니다.
- 로컬라이저 결과에 따라 FOV 크기 및 중심 위치를 선택합니다. FOV의 중심이 3차원 모두에서 폐의 중심과 일치하도록 하고 FOV가 양쪽 폐 전체를 포함하여 전체 흉강을 편안하게 포함할 수 있을 만큼 충분히 커지도록 목표로 합니다.
- 편광 측정 스테이션에서 129Xe 환기 스캔을 위한 129Xe 선량 백을 스캐너실로 가져옵니다. 복용 백을 피험자 근처에 준비하거나 놓습니다. 자기장 강도가 급격히 변하는 보어 개구부 근처의 영역을 피하십시오.
- 피험자가 4단계에서 설명한 코치된 흡입 절차에 따라 가방에서 129Xe 용량을 흡입하도록 돕습니다.
- Go!가 들리는 즉시 스캔을 실행하십시오. 피험자를 돕는 개인이 신호를 보냅니다.
- 스캔이 진행되는 동안 피사체를 모니터링합니다. 피험자가 눈에 띄게 숨을 내쉬거나, 기침을 하거나, 움직이거나, 움직이면 가능하면 스캔을 반복하십시오.
- 스캔이 끝나자마자 피험자에게 숨을 내쉬고 자유롭게 숨을 쉬도록 지시합니다.
- 스캔 후 맥박 산소 측정기를 사용하여 피험자의 심박수와 SpO2 를 모니터링하고 피험자와의 구두 의사 소통을 통해 일시적인 중추 신경계 영향(예: 현기증, 현기증, 행복감 및 감각 이상)을 모니터링합니다.
- 기준선에서 벗어난 부분이 사라질 때까지 기다렸다가 다른 129Xe 용량을 투여하십시오. 기준선에서 유의미한 편차가 발생하지 않으면 2분 이상 기다렸다가 129Xe용량을 추가로 투여하십시오.
- 아래 설명에 따라 1시간 해부학적 스캔을 수행합니다.
- 준비된 프로토콜에서 1H해부학적 서열을 로드합니다. 모든 펄스 시퀀스 매개변수가 원하는 대로인지 확인하고 클릭 한 번으로 스캔을 실행할 수 있도록 스캔 실행 설정을 지정합니다.
- 공기로 채워지고 129Xe 환기 스캔에 사용된 투여 백의 부피와 일치하는 투여 백을 스캐너실로 가져옵니다.
- 피험자가 4단계에서 설명한 코치된 흡입 절차에 따라 가방에서 공기 용량을 흡입하는 것을 돕습니다.
- Go!가 들리는 즉시 스캔을 실행하십시오. 피험자를 돕는 개인이 신호를 보냅니다.
- 스캔이 진행되는 동안 피사체를 모니터링합니다. 피험자가 눈에 띄게 숨을 내쉬거나, 기침을 하거나, 움직이거나, 움직이면 가능하면 스캔을 반복하십시오.
- 스캔이 끝나자마자 피험자에게 숨을 내쉬고 자유롭게 숨을 쉬도록 지시합니다.
7. 스캔 후 절차
- 스캔 절차 전과 동일한 방식으로 피험자의 바이탈을 측정합니다. 바이탈이 비정상적일 경우, 피험자에게 30-60분 및/또는 바이탈이 거의 기준선으로 돌아올 때까지 기다렸다가 출발하도록 지시한다.
8. 129Xe MRI 인공호흡 데이터 분석
참고: 획득한 129Xe 환기 및 1H 해부학적 이미지는 공급업체의 기본 이미지 재구성 파이프라인을 사용하여 MRI 스캐너 컴퓨터에서 자동으로 재구성되어야 합니다.
- 129Xe 환기 및 1H 해부학 스캔을 허용되는 최소 보간 수준을 사용하여 DICOM 이미지 파일로 내보냅니다(이상적으로는 없음).
- 다음 방정식8을 사용하여 프로그래밍 또는 이미지 분석 소프트웨어로 환기 결함 비율(VDP)을 계산합니다.
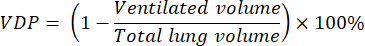
- 129Xe 환기 스캔을 수동으로 또는 기존의 여러 자동화 접근법 중 하나를 사용하여 환기량을 측정합니다33.
참고: 129Xe 이미지의 이진화 분할을 위한 간단한 방법은 다음과 같이 정의된 임계값을 사용합니다8: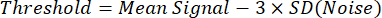
여기서 "평균 신호"는 폐 내에서 강한 129Xe 신호의 사용자 정의 관심 영역 내에서 129Xe 신호 강도의 평균이고, "SD(노이즈)"는 폐 또는 기관에서 멀리 떨어진 시야의 가장자리 근처 영역 내에서 129Xe 신호 강도의 표준 편차입니다. - 수동으로 또는 기존의 자동화된 접근 방식을 사용하여 1H해부학적 스캔을 분할하여 총 폐 용적을 결정합니다34.
- 이러한 분할이 수행되면 분할된 복셀 수에 이미지 복셀 부피를 곱한 값으로 해당 볼륨을 계산합니다(이미지를 DICOM 파일로 변환할 때 수행되는 모든 보간 고려).
- 129Xe 환기 스캔을 수동으로 또는 기존의 여러 자동화 접근법 중 하나를 사용하여 환기량을 측정합니다33.
결과
그림 1 은 건강한 사람의 대표적인 환기 및 3면 로컬라이저 이미지를 보여줍니다. 높은 129Xe 신호는 환기 영상에서 폐 전체에서 관찰될 수 있으며, 이 사람에게서 환기 장애는 분명하지 않습니다.
그림 2, 그림 3 및 그림 4 는 질병에 걸린 개인의 대표적인 환기 및 해부학적 이미지?...
토론
위에서 설명한 환기 및 해부학적 MRI 접근법은 구현의 단순성을 유지하면서 이미지 품질과 SNR을 극대화하도록 설계되었으며, 이러한 시퀀스 프로토콜은 일반적으로 다핵 작동이 활성화된 경우 공급업체 제품 펄스 시퀀스에서 조정할 수 있으며 이미지는 스캐너 컴퓨터에서 자동으로 재구성됩니다. 여기에 설명된 2D 접근법의 한 가지 단점은 슬라이스 선택적 여기 RF 펄스를 사용한다는 것인데, 이?...
공개
저자 J.F.M., J.P.M. 및 Y.M.S.는 Polarean, Inc.가 지원하는 임상시험에 참여하며, 저자 J.F.M. 및 Y.M.S.는 Polarean, Inc.에 컨설팅 서비스를 제공합니다($5000 미만). 저자 JPM은 Polarean, Inc.로부터 연구 지원을 받습니다.
감사의 말
이 연구는 미국 국립보건원(National Institutes of Health, 보조금 번호 R01-CA172595-01, R01-HL132177, R01-HL167202, S10-OD018079, UL1-TR003015)과 지멘스 메디컬 솔루션즈(Siemens Medical Solutions)의 지원을 받았습니다.
자료
| Name | Company | Catalog Number | Comments |
| 1.5T or 3T human MRI scanner | Siemens | MAGNETOM Symphony (1.5T) or Vida (3T); older models fine, as long as multinuclear option is/can be installed; scanners also available from GE and Philips | |
| 129Xe hyperpolarizer | Polarean | 9820 | |
| 129Xe MRI phantom | |||
| 129Xe MRI vest coil | Clinical MR Solutions | Also available from other vendors | |
| 129Xe polarization measurement station | Polarean | 2881 | |
| 1H MRI phantom | |||
| Coil file for 129Xe MRI vest coil | Also available from other vendors for their respective coils | ||
| ECG machine | |||
| Helium buffer gas | |||
| Interface box from coil to scanner | May be built into coil, but needs to be included separately if not | ||
| Liquid nitrogen | |||
| MRI-safe pulse oximeter | Philips | Expression MR200 | |
| Nitrogen buffer gas | |||
| PFT machine | |||
| Programming/image analysis software | MATLAB | R2023a | Various other options available |
| Pulse sequence design software | Siemens | IDEA software package; also available from GE and Philips for their respective scanners | |
| Scanner multinuclear option | Siemens | Scanner integrated hardware/software package; also available from GE and Philips for their respective scanners | |
| Tedlar gas sampling bags (500, 750, 1000, 1250, 1500 mL) | |||
| Xenon gas (129Xe isotopically enriched) |
참고문헌
- Roos, J. E., McAdams, H. P., Kaushik, S. S., Driehuys, B. Hyperpolarized gas MRI: Technique and applications. Magn Reson Imaging Clin N Am. 23 (2), 217-229 (2015).
- Mugler, J. P., Altes, T. A. Hyperpolarized 129Xe MRI of the human lung. J Magn Reson Imaging. 37 (2), 313-331 (2013).
- Ebner, L., et al. The role of hyperpolarized 129xenon in MR imaging of pulmonary function. Eur J Radiol. 86, 343-352 (2017).
- He, M., Driehuys, B., Que, L. G., Huang, Y. C. T. Using hyperpolarized 129Xe MRI to quantify the pulmonary ventilation distribution. Acad Radiol. 23 (12), 1521-1531 (2016).
- Walkup, L. L., et al. Xenon-129 MRI detects ventilation deficits in paediatric stem cell transplant patients unable to perform spirometry. Eur Respir J. 53 (5), 1801779 (2019).
- Virgincar, R. S., et al. Quantitative analysis of hyperpolarized 129Xe ventilation imaging in healthy volunteers and subjects with chronic obstructive pulmonary disease. NMR Biomed. 26 (4), 424-435 (2013).
- Ebner, L., et al. Hyperpolarized 129Xenon magnetic resonance imaging to quantify regional ventilation differences in mild to moderate Asthma: A prospective comparison between semiautomated ventilation defect percentage calculation and pulmonary function tests. Invest Radiol. 52 (2), 120-127 (2017).
- Woodhouse, N., et al. Combined helium-3/proton magnetic resonance imaging measurement of ventilated lung volumes in smokers compared to never-smokers. J Magn Reson Imaging. 21 (4), 365-369 (2005).
- Mugler, J. P., et al. Simultaneous magnetic resonance imaging of ventilation distribution and gas uptake in the human lung using hyperpolarized xenon-129. Proc Natl Acad Sci U S A. 107 (50), 21707-21712 (2010).
- Qing, K., et al. Assessment of lung function in asthma and COPD using hyperpolarized 129Xe chemical shift saturation recovery spectroscopy and dissolved-phase MRI. NMR Biomed. 27 (12), 1490-1501 (2014).
- Cleveland, Z. I., et al. Hyperpolarized 129Xe MR imaging of alveolar gas uptake in humans. PLoS One. 5 (8), 12192 (2010).
- Wang, Z., et al. Using hyperpolarized 129Xe gas-exchange MRI to model the regional airspace, membrane, and capillary contributions to diffusing capacity. J Appl Physiol. 130 (5), 1398-1409 (2021).
- Guan, S., et al. 3D single-breath chemical shift imaging hyperpolarized Xe-129 MRI of healthy, CF, IPF, and COPD subjects. Tomography. 8 (5), 2574-2587 (2022).
- Ouriadov, A., et al. Lung morphometry using hyperpolarized (129) Xe apparent diffusion coefficient anisotropy in chronic obstructive pulmonary disease. Magn Reson Med. 70 (129), 1699-1706 (2013).
- Yablonskiy, D. A., Sukstanskii, A. L., Quirk, J. D., Woods, J. C., Conradi, M. S. Probing lung microstructure with hyperpolarized noble gas diffusion MRI: theoretical models and experimental results. Magn Reson Med. 71 (2), 486-505 (2014).
- Chan, H. F., Stewart, N. J., Norquay, G., Collier, G. J., Wild, J. M. 3D diffusion-weighted 129 Xe MRI for whole lung morphometry. Magn Reson Med. 79 (6), 2986-2995 (2018).
- Walkup, L. L., et al. tolerability and safety of pediatric hyperpolarized 129Xe magnetic resonance imaging in healthy volunteers and children with cystic fibrosis. Pediatr Radiol. 46 (12), 1651-1662 (2016).
- Driehuys, B., et al. Chronic obstructive pulmonary disease: safety and tolerability of hyperpolarized 129Xe MR imaging in healthy volunteers and patients. Radiology. 262 (1), 279-289 (2012).
- Myc, L., et al. Characterisation of gas exchange in COPD with dissolved-phase hyperpolarised xenon-129 MRI. Thorax. 76 (2), 178-181 (2021).
- Kaushik, S. S., et al. Measuring diffusion limitation with a perfusion-limited gas-Hyperpolarized 129Xe gas-transfer spectroscopy in patients with idiopathic pulmonary fibrosis. J Appl Physiol. 117 (6), 577-585 (2014).
- Dournes, G., et al. The clinical use of lung MRI in cystic fibrosis: What, now, how. Chest. 159 (6), 2205-2217 (2021).
- Thomen, R. P., et al. Hyperpolarized 129Xe for investigation of mild cystic fibrosis lung disease in pediatric patients. J Cyst Fibros. 16 (2), 275-282 (2017).
- Mammarappallil, J. G., Rankine, L., Wild, J. M., Driehuys, B. New developments in imaging idiopathic pulmonary fibrosis with hyperpolarized xenon magnetic resonance imaging. J Thorac Imaging. 34 (2), 136-150 (2019).
- Rankine, L. J., et al. 129Xenon gas exchange magnetic resonance imaging as a potential prognostic marker for progression of idiopathic pulmonary fibrosis. Ann Am Thorac. 17 (1), 121-125 (2020).
- Mata, J., et al. Evaluation of regional lung function in pulmonary fibrosis with xenon-129 MRI. Tomography. 7 (3), 452-465 (2021).
- Svenningsen, S., et al. Hyperpolarized (3) He and (129) Xe MRI: Differences in asthma before bronchodilation. J Magn Reson Imaging. 38 (3), 1521-1530 (2013).
- Stewart, N. J., et al. Comparison of 3He and 129Xe MRI for evaluation of lung microstructure and ventilation at 1.5T. J Magn Reson Imaging. 48 (3), 632-642 (2018).
- Hughes, P. J. C., et al. Assessment of the influence of lung inflation state on the quantitative parameters derived from hyperpolarized gas lung ventilation MRI in healthy volunteers. J Appl Physiol. 126 (1), 183-192 (2019).
- Polarean. . FDA Approves Polarean's XENOVIEWTM (xenon Xe 129 hyperpolarized) for use with MRI for the evaluation of lung ventilation. , (2022).
- Niedbalski, P. J., et al. Protocols for multi-site trials using hyperpolarized 129Xe MRI for imaging of ventilation, alveolar-airspace size, and gas exchange: A position paper from the 129Xe MRI clinical trials consortium. Magn Reson Med. 86 (6), 2966-2986 (2021).
- Bier, E. A., et al. A thermally polarized 129 Xe phantom for quality assurance in multi-center hyperpolarized gas MRI studies. Magn Reson Med. 82 (5), 1961-1968 (2019).
- He, M., et al. Dose and pulse sequence considerations for hyperpolarized 129Xe ventilation MRI. Magn Reson Imaging. 33 (7), 877-885 (2015).
- Tustison, N. J., et al. Image- versus histogram-based considerations in semantic segmentation of pulmonary hyperpolarized gas images. Magn Reson Med. 86 (5), 2822-2836 (2021).
- Tustison, N. J., et al. Convolutional neural networks with template-based data augmentation for functional lung image quantification. Acad Radiol. 26 (3), 412-423 (2019).
- Wild, J. M., et al. Comparison between 2D and 3D gradient-echo sequences for MRI of human lung ventilation with hyperpolarized 3He. Magn Reson Med. 52 (3), 673-678 (2004).
- Willmering, M. M., et al. Improved pulmonary 129 Xe ventilation imaging via 3D-spiral UTE MRI. Magn Reson Med. 84 (1), 312-320 (2020).
- Collier, G. J., et al. Single breath-held acquisition of coregistered 3D 129 Xe lung ventilation and anatomical proton images of the human lung with compressed sensing. Magn Reson Med. 82 (1), 342-347 (2019).
- Zha, W., et al. Semiautomated ventilation defect quantification in exercise-induced bronchoconstriction using hyperpolarized helium-3 magnetic resonance imaging: a repeatability study. Acad Radiol. 23 (9), 1104-1114 (2016).
- Ray, N., Acton, S. T., Altes, T. A., de Lange, E. E., Brookeman, J. R. Merging parametric active contours within homogeneous image regions for MRI-based lung segmentation. IEEE Trans Med Imaging. 22 (2), 189-199 (2003).
- Hughes, P. J. C., et al. Spatial fuzzy c-means thresholding for semiautomated calculation of percentage lung ventilated volume from hyperpolarized gas and 1 H MRI. J Magn Reson Imaging. 47 (3), 640-646 (2018).
- Tustison, N. J., et al. Ventilation-based segmentation of the lungs using hyperpolarized (3)He MRI. J Magn Reson Imaging. 34 (3), 831-841 (2011).
- Kanhere, N., et al. Correlation of lung clearance index with hyperpolarized 129Xe magnetic resonance imaging in pediatric subjects with cystic fibrosis. Am J Respir Crit Care Med. 196 (8), 1073-1075 (2017).
- Rayment, J. H., et al. Hyperpolarised 129Xe magnetic resonance imaging to monitor treatment response in children with cystic fibrosis. Eur Respir J. 53 (5), 1802188 (2019).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유