É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Identificação da quinase Cyclin-dependente 1 sítios de fosforilação específica por uma quinase In Vitro do ensaio
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Quinase cyclin-dependente 1 (Cdk1) é ativada na fase G2 do ciclo celular e regula muitos caminhos celulares. Aqui, apresentamos um protocolo para um ensaio da quinase em vitro Cdk1, que permite a identificação dos sítios de fosforilação Cdk1-específicos para o estabelecimento de alvos celulares deste importante quinase.
Resumo
Quinase cyclin-dependente 1 (Cdk1) é um controlador mestre para o ciclo celular em todos os eucariontes e fosforila um estimado 8-13% da proteoma; no entanto, o número de destinos identificados para Cdk1, particularmente em células humanas ainda é baixo. A identificação dos sítios de fosforilação Cdk1 específico é importante, como eles fornecem mecanicistas insights sobre como Cdk1 controla o ciclo celular. Regulação do ciclo celular é essencial para a segregação do cromossomo fiel, e defeitos neste processo complicado levam a aberrações cromossômicas e câncer.
Aqui, descrevemos um em vitro quinase que é usado para identificar locais de fosforilação Cdk1 específicos. Neste ensaio, uma proteína purificada é fosforilada em vitro por comercialmente disponível humana Cdk1/cyclin B. bem sucedido fosforilação é confirmada por SDS-PAGE, e locais de fosforilação são posteriormente identificados por espectrometria de massa. Descrevemos também protocolos de purificação que o rendimento de preparações de proteína altamente puro e homogêneo apropriadas para o ensaio da quinase e um ensaio para a verificação funcional dos sítios identificados fosforilação, que explora a interação entre um sinal de localização nuclear clássica (cNLS) e seu transporte nuclear receptor carioferinas α. Para ajudar com delineamento experimental, revemos abordagens para predição de sítios de fosforilação Cdk1 específicas de sequências de proteínas. Juntos esses protocolos apresentam uma abordagem muito poderosa que produz sites de fosforilação Cdk1 específicos e permite estudos mecanicistas em como Cdk1 controla o ciclo celular. Desde que esse método se baseia em proteínas purified, pode ser aplicado a qualquer modelo organismo e produz resultados confiáveis, especialmente quando combinado com estudos funcionais de célula.
Introdução
As cinases são enzimas que tranferem grupos fosfato do ATP para substratos e regulam muitos processos celulares. Esta fosforilação é reversível, rápido, adiciona duas cargas negativas e armazena energia livre e é uma das modificações posttranslational mais comuns usadas pelas células. Cdk1, que é também conhecido como o homólogo de proteína 2 de ciclo de divisão celular (cdc2) é um controlador mestre do ciclo celular em todos os eucariontes1,2,3,4,5e fosforila um Estima-se 8-13% do proteome6,7.
Enquanto estudos recentes de proteomic identificaram muitos sítios de fosforilação de proteínas, na maioria dos casos, a quinase responsável por essas modificações é desconhecida. O número de conhecidos destinos Cdk1, particularmente em células humanas é baixo7. A identificação dos sítios de fosforilação Cdk1 específico é importante, como permite estudos mecanicistas que estabelecem como Cdk1 controla o ciclo celular. Regulação do ciclo celular é importante para a segregação do cromossomo fiel e divisão celular, e uma miríade de processos celulares precisam ocorrer para apoiar esta importante função fisiológica. Isso inclui travar a transcrição e tradução antes do início da mitose, bem como uma reorganização dramática na estrutura celular e organização, tais como a desmontagem do envoltório nuclear, condensação do cromossomo e montagem do fuso mitótico. Desregulamentação e erros nestes processos causam câncer, defeitos de nascimento ou morte celular mitótica. Inibidores específicos de Cdk1 como RO-3306 foram desenvolvidos8, que fornece ferramentas poderosas para estudos funcionais, e alguns destes inibidores são atualmente em ensaios clínicos para tratamento de câncer (veja9 para revisão).
Aqui, descrevemos um em vitro quinase que permite a identificação dos sítios de fosforilação Cdk1 específicos. Neste ensaio, comercialmente disponível humana Cdk1/cyclin B é usado para fosforilar um alvo purificado da proteína em vitro. Fosforilação do substrato aumenta a sua massa e adiciona duas cargas negativas; Portanto, fosforilação sucesso é confirmada por um deslocamento para cima da banda gel de proteína em SDS-PAGE. Sites específicos de Cdk1 fosforilação são posteriormente identificados por análise de espectrometria de massa da proteína em vitro fosforilada. Para ajudar com delineamento experimental, revisamos também ferramentas computacionais e referências para a previsão dos sítios de fosforilação Cdk1 específica da sequência de proteínas. Além disso, podemos também descrever protocolos de purificação que o rendimento de preparações de proteína altamente puro e homogêneo apropriadas para o ensaio da quinase. Finalmente, os sítios de fosforilação identificado devem ser verificados por estudos funcionais, e um ensaio simples é descrito aqui para essa finalidade. Combinada, esta é uma abordagem muito poderosa que produz sites de fosforilação Cdk1 específicos e permite estudos mecanicistas em como Cdk1 controla o ciclo celular7,10,11. Desde que esse método se baseia em proteínas purified, pode ser aplicado a quaisquer resultados fiáveis modelo organismo e rendimentos. No entanto, é recomendada verificação funcional da fosforilação obtidos sites em vitro , como as células têm mecanismos reguladores adicionais no lugar, como modificações posttranslational, parceiros de interação ou localização celular que pode processar sites fosforilação acessível ou inacessível para reconhecimento por Cdk1.
Cdk1 reconhece um site de fosforilação de consenso que consiste em arquivos em (Ser/Thr-Pro-X-Lys/Arg), onde X é qualquer resíduo e uma serina ou treonina é o sítio de fosforilação. Especialmente importante para o reconhecimento é a presença da prolina na posição + 1. Além disso, os resíduos básicos são preferidos nas posições + 2 ou + 3, com a maioria dos sites de fosforilação Cdk1 específicas contendo um Lys ou Arg + a 3 posição6,12.
Ativação de Cdk1 é fortemente regulamentada e leva ao aparecimento de mitose1,2,3,4,5. A atividade de quinases cyclin-dependente em geral depende de sua associação com ciclinas distintas (ciclina A, B, C, D e E em seres humanos), que são expressos em níveis durante todo o ciclo celular13de oscilação. Expressão de Cdk1 é constante em todo o ciclo celular e a regulação da sua actividade baseia-se na sua associação com as subunidades reguladoras cyclin A e cyclin B5,13,14,15, como bem como modificações borne-translational. Formação do complexo Cdk1/cyclin B é necessária para a quinase ativação5,14,15,16,17,18. Na fase G2, ciclina B é traduzido no citoplasma e importada para o núcleo onde se liga ao Cdk15,14,15,16,17,18; no entanto, B Cdk1/cyclin realiza inativada por fosforilação em resíduos Thr14 e Tyr15 pelos humano Cdk1-inibitório quinases Myt1 (quinase cdc2-inibitório de membrana-associado tirosina e treonina-específico) e Wee1, respectivamente,19, 20,21. Na fase tardia do G2, desfosforilação de Thr14 e Tyr15 por divisão celular ciclo 25 fosfatase (cdc25) ativa a atividade da quinase do complexo Cdk1/cyclin B e desencadeia o início da mitose12,14, 18 , 20 , 22 , 23. a fosforilação de Thr161 também é necessária para ativação de Cdk1/cyclin B e é mediada por Cdk7, o Cdk-activação da quinase (CAK)18. Degradação da ciclina B em anáfase inactivates Cdk1, permitindo a saída de mitose24,25. Ativação de Cdk1/cyclin B, portanto, é um processo complicado. O protocolo aqui apresentado é realizado com b de Cdk1/cyclin comercialmente disponível. Durante a expressão recombinante deste complexo em células de inseto, é ativado na vivo por quinases endógena14,20 e permanece ativa no estado purificado. Resultante ativo, recombinante humana Cdk1/cyclin B é apropriado para ensaios de quinase em vitro .
Aqui, descrevemos um protocolo para a identificação dos sítios de fosforilação Cdk1 específicas do centrômero humano proteína F (CENP-F)10. CENP-F é uma proteína de cinetócoro que reside no núcleo durante a interfase (G1 e S-fase) e é exportada para o citosol no G2 fase26,,27,28 em uma maneira dependente Cdk110, 11. localização nuclear é conferida por um bipartido cNLS26. cNLSs são reconhecidos pelo transporte nuclear factor carioferinas α, que facilita, em conjunto com carioferinas β e RanGDP, a importação de cNLS-carga para o núcleo de29. A exportação nuclear na fase G2 é facilitada através de uma exportação desconhecido caminho10. Uma vez que o CENP-F reside no citosol, ele é recrutado para o envelope nuclear e recrutas por sua vez o motor proteína Dineína complexo30,31. Esta via é importante posicionar o núcleo respectivo para a centrossoma durante os estágios iniciais da montagem do fuso mitótico de forma dependente de Dineína, que é importante para o timing correto de entrada mitótica e para um processo fundamental no cérebro desenvolvimento de31,30,32. Começando na fase G2, CENP-F é também montado no cinetócoro onde tem papéis importantes para cromossomo fiel segregação27,28,33,34,35 . Um passo chave reguladora destas vias é a exportação nuclear do CENP-F na fase G2, que é dependente de Cdk110,11. Descrevemos aqui um protocolo para a identificação dos sítios de fosforilação Cdk1 específicos no cNLS do CENP-F. Phosphomimetic mutações desses sites devagar importação nuclear do CENP-F, sugerindo que B Cdk1/cyclin diretamente regula a localização celular do CENP-F por fosforilação de sua cNLS10.
Em geral, este ensaio da quinase em vitro permite a identificação de substratos específicos para proteínas quinase Cdk1. Purified alvo são fosforilada em vitro pelo complexo B Cdk1/cyclin comercialmente disponível e os locais de fosforilação posteriormente são identificados por espectrometria de massa. A identificação dos sítios de fosforilação específica Cdk1 suporta mecanicistas estudos que revelam como a Cdk1 controla o ciclo celular.
Protocolo
1. Previsão de Sites específicos Cdk1 fosforilação da sequência de proteína
- Antes de começar o ensaio da quinase, analisar a sequência da proteína para sites de fosforilação previstas Cdk1 específicos e pesquisar a literatura para sítios de fosforilação experimentalmente estabelecido com especificidade quinase desconhecido. Use as seguintes ferramentas, bancos de dados e referências que são resumidas.
- Use o iGPS 3.0 software36,37 (http://gps.biocuckoo.org/online_full.php) para prever locais de fosforilação Cdk1 específicas na sequência da proteína alvo. Use o link aqui para uma previsão abrangente que inclui anotações de estrutura secundária e acessibilidade de superfície.
- No software, digite a sequência de proteínas em formato FASTA. Para a especificidade da quinase, verificar quinase serina/treonina, CMGC, CDK, CDC2, CDK1e desmarque todas as outras especificidades. Selecione médio como o limiar e clique no botão Enviar .
- Compare os sites previstos resultantes com o site de fosforilação do consenso de Cdk1 (Ser/Thr-Pro-X-Lys/Arg).
- Importante, verifique o local previsto para a prolina ao lado o resíduo fosforilada (alguns substratos Cdk1 são phosphorylated em um mínimo local (Ser/Thr-Pro)6,12). Além disso, verifique se há resíduos básicos, que são os preferidos nas posições + 2 ou + 3, com a maioria dos sites de fosforilação Cdk1 específicas contendo um Lys ou Arg no6,+ 3 posição12.
- Verifique também que o site é acessível para o reconhecimento, como a presença de um site cheio de consenso não é suficiente para a Cdk1 fosforilação.
- Inspecione a superfície acessibilidade e anotação de predição de estrutura secundária na saída iGPS, que afirma que se o site é previsto para ser acessível; N - e C-termini de proteínas são em muitos casos, flexíveis e acessíveis para fosforilação.
- Se uma estrutura de raio-x da proteína alvo estiver disponível, verifique a acessibilidade dos sítios de fosforilação putativo inspecionando seu local na estrutura de.
- Busca na literatura para sítios de fosforilação experimentalmente estabelecido com especificidade quinase desconhecido, usando o banco de dados UniProtKB/Swiss-Prot38 (http://www.uniprot.org).
- Digite o nome da proteína na caixa Pesquisar e clique no botão Pesquisar . Selecione a entrada de sequência correta. Sítios de fosforilação são anotados e referenciados na seção de modificações de aminoácido .
- Busca por estudos de proteômica de extratos mitóticos da célula humana linhas7,39,40, que são particularmente úteis porque Cdk1 torna-se ativo na fase G2 do ciclo celular.
- Identifica cNLS bipartido por NLSmapper (opcional).
Nota: Para as proteínas que vaivém entre o citoplasma e o núcleo, um mecanismo comum para regulação da localização celular é a fosforilação de uma cNLS bipartido na posição do principal motivo pelo Cdk1-1. A fosforilação abole a localização nuclear em G2 fase10,41,42,43.- Para tais proteínas shuttling, identifica o cNLS na sequência da proteína por NLSmapper43 (http://nls-mapper.iab.keio.ac.jp/cgi-bin/NLS_Mapper_form.cgi). Colar a sequência de proteínas como texto na caixa sequência, selecione um escore de corte de 5.0 e eleger para procurar o NLS em toda a região. Clique no botão Prever NLS .
- Compare o resultante cNLS previsto contra a sequência do consenso de um cNLS bipartido, que consiste no menor motivo (Lys-Arg), um vinculador pelo menos 10 resíduos e motivo de grandes arquivos em (Lys-Lys/Arg-X-Lys/Arg), onde X é qualquer resíduo que não está carregado negativamente .
- Verifique se o local previsto de fosforilação Cdk1 (*) está localizado ao lado do motivo principal na posição do vinculador-1: Ser/Thr*-Pro/X-X-Lys-Lys/Arg-X-Lys/Arg.
Nota: A fosforilação de uma cNLS bipartido na posição-1 por Cdk1 estabeleceu-se como um mecanismo regulatório para celular localização para vários shuttling proteínas10,41,42, 43.
2. a expressão de proteínas recombinantes em Escherichia Coli
- Use o plasmídeo de expressão de passos 2.1.1-2.1.2 para a expressão de proteínas recombinantes em e. coli.
- Para criar a expressão humana do CENP-F (resíduos 2.987-3.065) construir, gerar inserções amplificar fragmentos de DNA por reação em cadeia da polimerase (PCR) de uma construção completo do CENP-F (adesão GenBank: U19769.1). Use os seguintes primers: AGTCGGGGATCCCAGCAATCTAAACAAGATTCCCG e AGTCGGCTCGAGTCATTATTCTGCAGGGTGAATACCACTCATG.
Nota: O plasmídeo humano completo do CENP-F foi generosamente fornecido pelo Dr. X. Zhu, institutos de ciências biológicas, da Academia Chinesa de Ciências, Shanghai, China.- Clone a inserção para o vetor de pGEX6p1 com os locais de restrição BamHI e XhoI. Use este plasmídeo para expressar proteínas da fusão N-terminal Glutationa S-transferase (GST) da CENP-F (resíduos 2.987-3.065).
Nota: O GST-tag pode ser clivado fora pela protease PreScission (doravante referida como protease PS).
- Clone a inserção para o vetor de pGEX6p1 com os locais de restrição BamHI e XhoI. Use este plasmídeo para expressar proteínas da fusão N-terminal Glutationa S-transferase (GST) da CENP-F (resíduos 2.987-3.065).
- Para os humanos carioferinas expressão de α construir, gerar inserções amplificar fragmentos de DNA por PCR de um modelo de cDNA α2 carioferinas completos (adesão sequência NM_002264.3; as primeiras demão: GCACTACATATGTCCACCAACGAGAATGCTAATA e TCACGCCTCGAGTTATCAAAAGTTAAAGGTCCCAGGAGCC).
Nota: Devido a semelhança entre as isoformas, essa construção de α2 carioferinas é referida no texto subsequente como carioferinas α.- Clone a inserção em vetor com os locais de restrição NdeI e XhoI pET28a-pres.
Nota: Este é um vetor de pET28a modificado, no qual a sequência de codificação para o local de clivagem de trombina foi substituída por uma sequência que codifica para um local de clivagem de protease de PS. Use este plasmídeo de expressar uma proteína de fusão das carioferinas α com um N-terminal dele6-marca, onde o seu6-etiqueta pode ser clivada fora por protease do PS.
- Clone a inserção em vetor com os locais de restrição NdeI e XhoI pET28a-pres.
- Para criar a expressão humana do CENP-F (resíduos 2.987-3.065) construir, gerar inserções amplificar fragmentos de DNA por reação em cadeia da polimerase (PCR) de uma construção completo do CENP-F (adesão GenBank: U19769.1). Use os seguintes primers: AGTCGGGGATCCCAGCAATCTAAACAAGATTCCCG e AGTCGGCTCGAGTCATTATTCTGCAGGGTGAATACCACTCATG.
- Para criar mutações pontuais de uma proteína de destino, execute o mutagenesis local-dirigido com um kit.
- Expresse as proteínas recombinantes em e. coli para purificação subsequente.
- As seguintes existências: canamicina 50 mg/mL (1:1, 000 solução estoque), cloranfenicol 35 mg/mL em 70% etanol (1:1, 000), ampicilina 100 mg/mL (1:1, 000) e 1 M isopropílico β-D-1-thiogalactopyranoside (IPTG; 1:5, 000).
- Estéril, as ações de filtro e armazenar a-20 ° C. Evite ciclos repetidos de congelamento-descongelamento por IPTG.
- Transforme 1 µ l de plasmídeo de expressão em 50 µ l de células competentes da Escherichia coli 2 Rosetta (DE3) pLysS estirpe, de acordo com as instruções do fabricante.
- Placa de cultura em ágar Luria-Bertani (LB) com cloranfenicol (35 µ g/mL LB) e ampicilina (100 µ g/mL LB) para a construção do CENP-F, ou cloranfenicol e canamicina (cultura de 50 µ g/mL) para a construção α carioferinas. Incubar as placas para 12-20 h a 37 ° C.
- Escolher uma única colônia e inocular 50 mL de LB suplementado com antibióticos (consulte a etapa 2.3.4). Incubar o preculture agitando a 160-180 rpm para 12-20 h a 37 ° C.
- Preparar 1 L de LB médio em um 2.800 mL perplexo Fernbach balão. Fazer dois balões para cada preculture e autoclave-los. Para permitir a aeração, não encha os frascos ao volume de mais de dois terços de balão. Erlenmeyers podem ser usados também.
- Adicionar antibióticos (etapa 2.3.4) e 10 mL de uma solução de glicose de 40% (p/v) estéril filtrada por 1 L de refrigeração lb. Adicionar 20 mL de preculture por 1 L de meio LB.
Nota: A absorvância a 600 nm de uma 01:10 diluição do preculture deve estar entre 0,15-0,2. - Incubar os frascos agitando a 160-180 rpm a 37 ° C. Medir a absorvância em 600 nm de cultura de bactérias regularmente. Se a absorvência atinge 0,5-0,6, induzir a expressão da proteína pela adição de 0,2 mM IPTG (200 µ l de estoque de 1 M por 1 L de meio LB).
Nota: É importante que as células são induzidas a absorvância correta. Geralmente leva 3-4 h para chegar a esta fase. - Incubar os frascos agitando por 3 h a 37 ° C. Recolher as células por centrifugação (15 min, 4.100 x g, 4 ° C, de rotor basculante). Desprezar o sobrenadante. Resuspenda as pelotas de célula em 20 mL de tampão de ligação GST (CENP-F) ou seu6-tampão de ligação (carioferinas α) por 1 L de cultura. Armazenar as células a-80 ° C.
- Preparar o buffer de GST-vinculação (10 mM Tris pH 8.0 a 25 ° C, 150 mM de NaCl, 1 mM ditiotreitol (DTT), 0,5 mM EDTA) e seus6-vinculação tampão (10 mM Tris pH 8.0 a 25 ° C, 250 mM NaCl, pH 8.0, do Imidazole de 5mm 5mm β-mercaptoetanol (BME)) com antecedência.
3. purificação da proteína recombinante por cromatografia de afinidade de glutationa e Gel filtração
- Fazer as seguintes ações: 1 M DTT (1:1, 000 ações, estéril filtrados com tamanho de poro 0,2 µM e desgaseificado); fluoreto de phenylmethylsulfonyl 250 mM (PMSF; 1:1,000 estoque em Dimetilsulfóxido). Loja a-20 ° C. Evite ciclos repetidos de congelamento-descongelamento.
- Faça os seguintes buffers e resfriá-las a 4 ° C.
- Prepare o tampão de ligação de GST usando pH de 10 mM Tris 8.0 a 25 ° C, 150 mM de NaCl, 1 milímetro DTT, 0.5 mM EDTA.
- Prepare o tampão de eluição de GST usando glutationa reduzida de 10mm (0,15 g/50 mL) dissolvida em um tampão de pH 8.0 do Tris 50mm a 25 ° C, 150 mM de NaCl, 1 milímetro DTT. Confirmar que o pH do buffer final é 8.0 e usar no mesmo dia que foi feito.
- Prepare o Gel filtração reserva usando pH 7.5 do Tris de 20 mM a 25 ° C, 60 mM de NaCl, 2 mM DTT. Estéril do filtro o buffer com um filtro de garrafa-top (tamanho de poro de 0,2 µM). Desgaseifica o buffer, agitando sob vácuo (-6 psi) por 15 min.
- Adicione TDT para todos acima buffers no dia do uso.
- Descongele as células da secção 2 que contêm a construção do CENP-F. Ajuste o volume de 40 mL com o buffer de GST-ligação. Adicionar 1 mM DTT, 0,25 mM PMSF, 0.5 mM EDTA (solução 0,5 M, pH 8,0), cloridrato de benzamidina 7 mg (1 mM) e 40 mg D/L metionina.
Nota: Para reduzir a degradação proteolítica, execute todas as etapas, a 4 ° C, de preferência em uma sala fria, exceto onde anotado. Manter as células, lysates e frações de proteína purificada no gelo em todos os momentos e adicionar os inibidores de protease. Para evitar a oxidação de resíduos de cisteína e a metionina, adicione redutores tais como TDT e metionina no dia do experimento. Para reduzir a degradação proteolítica, trabalhe através dos passos rapidamente. - Lyse as células em um sonicador como segue. Encha um copo de vidro com o lisado e mergulhe-a em um banho de água gelada. Proceda à sonicação a cultura (1 min 40 s, em 100 W (50%) saída/amplitude, com 10 pulsos de s e 10 s resto ciclos). Adicione 250 µM PMSF após sonication. Inspecionar o lisado celular, que deve olhar mais transparente e não ser mais viscoso.
- Claro o lisado por centrifugação a 12.000-40.000 x g, 25 min, 4 ° C. Use tubos de centrífuga fundo redondo e um rotor de ângulo fixo.
- Execute o equilibrio , adicionando 2 mL de glutationa agarose 1:1 da pasta para uma coluna de cromatografia descartáveis. A coluna resultante terá um volume de 1 mL. Lave a coluna com 25 mL de água ultrapura e 25 mL de tampão de ligação GST.
- Execute a ligação da seguinte maneira. Trabalhando em um quarto frio ou fria caixa, decante o lisado de Pelotas. Filtrar o lisado (tamanho do pore 0,2 µm) e despeje-o na coluna conectada. A coluna do tampão e incube-lo enquanto oscilador suavemente durante 30 min a 4 ° C.
- Para lavar a coluna, colocá-lo sobre uma grelha e deixe a resina resolver e coletar o fluxo através de. Lave a coluna duas vezes com 25 mL de tampão de ligação GST.
-
Eluir por clivagem proteolítica.
- Ligue a coluna. Adicione 400 µ l de tampão de ligação GST e 250 µ l de protease PS (2 mg/mL caldo com uma atividade de 1.000 U/mg, ou purificada em laboratório ou comprado; ver Tabela de materiais).
- A coluna do tampão e agitar levemente para Ressuspender a resina no buffer. Incubar as colunas para 16-20 h a 4 ° C. Em seguida, adicione 4 mL de tampão de ligação GST para Eluir o fragmento CENP-F clivado proteoliticamente da coluna.
-
Eluição de glutationa
- Ligue a coluna, adicionar 4 mL de tampão de eluição de GST (4 volumes de coluna) e incube por 10 min Eluir o limite GST-tag. Recolha o eluato. Regenere as colunas antes de re-uso conforme descrito pelo fabricante.
- Analise a fração de eluição de protease de PS e a fração de eluição de glutationa por SDS-PAGE 16% géis de acrilamida. Execute eletroforese a 25 V/cm por 45 min. mancha os géis por Coomassie Blue. A fração de protease PS irá conter o fragmento purificado do CENP-F, Considerando que a fração de glutationa conterá o clivada GST-tag. Inspecione o gel para avaliar a eficiência de clivagem proteolítica.
- Concentre-se no PS eluato de protease de 0,5 mL, usando unidades de filtro centrífugo com um peso molecular de 3 kDa corte (ver Tabela de materiais). Adicionar o eluato no compartimento superior do filtro e centrifugue em incrementos de 10-15 min a 4.100 x g, 4 ° C (rotor basculante) para concentrar a amostra. Misture pipetando após cada incremento.
- Conectar um adequado coluna de filtração do gel (ver Tabela de materiais para a compra de informações) para um sistema de cromatografia líquida (FPLC) proteína rápida e equilibrar isso com volume 1 coluna do amortecedor de gel filtração.
- Centrifugue o fragmento CENP-F concentrado numa microcentrifuga (20 min, 21.700 x g, 4 ° C). Injete a amostra na coluna e Elui-lo com volume 1 coluna do amortecedor de gel filtração. Colete frações de 0,6 mL.
Nota: O amortecedor de filtração de gel é otimizado para compatibilidade com a quinase subsequentes. Teste se a proteína alvo é estável nesta reserva. Se não é estável, tente adicionar mais cloreto de sódio. - Analise as frações de pico por SDS-PAGE (etapa 3.11). As frações de pico que contêm fragmentos de CENP-F puros da piscina. Concentre-se os fragmentos CENP-F purificados a 3,3 mg/mL (passo 3.12). Analise os fragmentos de CENP-F purificados por SDS-PAGE (etapa 3.11).
-
Determinação da concentração da proteína
- Diluir a amostra 1: 100 em água ultrapura e colocá-lo em um microcubeta de quartzo. Espectros de gravar em um intervalo de comprimento de onda de 220-300 nm num espectrofotómetro.
Nota: A concentração de proteína c (mg/mL) é derivado da seguinte equação: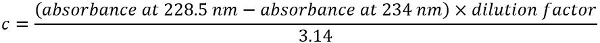
- Diluir a amostra 1: 100 em água ultrapura e colocá-lo em um microcubeta de quartzo. Espectros de gravar em um intervalo de comprimento de onda de 220-300 nm num espectrofotómetro.
- Faça 50 alíquotas µ l da proteína purificada em microtubos 0,5 mL e congelam -los em nitrogênio líquido. Armazenar as alíquotas a-80 ° C.
4. purificação da proteína recombinante por cromatografia de afinidade Ni-NTA
- Faça os seguintes buffers e refrigerar a 4 ° C.
- Preparar o seu6-tampão de ligação usando pH 8.0 do Tris de 10 mM a 25 ° C, 250 mM NaCl, pH do Imidazole 5mm 8.0, 5mm BME. Adicione BME para todos os buffers no dia do uso.
- Preparar o seu6-tampão de lavagem da mesma forma como o seu6-tampão de vinculação, mas usando 20mm imidazol.
- Preparar o seu6-tampão de eluição da mesma maneira como o buffer de vinculação, mas usando 150mm imidazol.
-
Descongelar as células da secção 2 que contêm o carioferinas α construir e ajustar o volume de 40 mL com os seus6 -tampão de ligação. Adicione 5 mM BME, 0,250 mM PMSF, cloridrato de benzamidina 7 mg (1 mM) e metionina 40 mg D/L.
- Proceda como descrito nos passos 3.4-3.8 com as seguintes variações: Use seu6-tampão de ligação em vez de buffer de GST-ligação para todas as etapas. Em vez de agarose de glutationa, use 4 mL da afinidade niquelar do gel (ver Tabela de materiais) para tornar a coluna, que terá um volume de coluna de 2 mL.
Nota: Colunas de afinidade de níquel são incompatíveis com TDT e EDTA. Em vez do gel de afinidade de níquel, Ni2 +- nitrilotriacético agarose de ácido (NTA) pode ser usado, se a concentração de imidazol no tampão de eluição aumenta para 250 mM (ver Tabela de materiais).
- Proceda como descrito nos passos 3.4-3.8 com as seguintes variações: Use seu6-tampão de ligação em vez de buffer de GST-ligação para todas as etapas. Em vez de agarose de glutationa, use 4 mL da afinidade niquelar do gel (ver Tabela de materiais) para tornar a coluna, que terá um volume de coluna de 2 mL.
- Lavar o colunas com 8 mL de seu6-tampão de lavagem.
- Elute o α carioferinas com 12 mL de seu6-eluição do buffer e analisar o eluato por SDS-PAGE (etapa 3.11).
- Adicionar 250 µ l de protease PS (passo 3.9) para o eluato e incubar durante 16-20 h a 4 ° C. Entretanto, Dialize o eluato duas vezes contra 1 L de seu6-tampão de ligação para 2-20 h, usando uma membrana de diálise com 6-8 kDa peso molecular corte.
- Regenere a coluna de gel de afinidade niquelar conforme descrito pelo fabricante. Equilibrar a coluna com 25 mL de seu6-tampão de ligação. Adicionar a proteína dializada à coluna e executar a etapa de ligação , conforme descrito na etapa 3.7.
- Coletar o fluxo através de, que contém o α carioferinas purificado (com os seus6-marca clivada fora) e eluir a proteína restante com um adicional 4 mL de seu6-tampão de ligação. Estas frações da piscina. Eluir em seguida as colunas com 12 mL de seu6-tampão de eluição. Esta fração contém impurezas.
- Analisar o α uncleaved e clivada carioferinas da escadaria 4.4-4.5 e as duas frações de eluição desta etapa por SDS-PAGE (etapa 3.11) para avaliar a eficiência de seu6-tag clivagem e pureza.
- Concentrar o α carioferinas para 8 mg/mL e congelam em nitrogênio líquido (etapas 3.15-3.17).
5. ensaio in Vitro da quinase com Cdk1/Cyclin B
-
Em vitro quinase
Nota: Após a chegada da quinase, fazer pequenas alíquotas, eles congelam em nitrogênio líquido e armazená-los a-80 ° C. Use no prazo de 6 meses. Enquanto o peso molecular é 34 kDa para Cdk1 e 48 kDa para ciclina B, a massa molecular aparente de ciclina B em SDS-PAGE é cerca de 60 kDa.- Preparar o 10x PK buffer (fornecido com a quinase) usando 0.5 M Tris-HCl 0,1 M MgCl2, 1 mM EDTA, 20 mM DTT, 0,1% Brij 35, pH 7,5 a 25 ° C.
- Preparar o estoque de ATP de 10x: faça uma solução de 4 mM ATP em PK tampão 1x e verificar o pH final do estoque. Armazene em pequenas alíquotas a-20 ° C e evitar ciclos de congelamento e descongelamento.
- Fragmento de Mix 40 µ l do CENP-F (em uma concentração de 3,3 mg/mL, ou 400 µM), 6 µ l 10 x tampão PK, água ultrapura de 3 µ l, 6 ações de x 10 µ l ATP e 5 µ l humana B Cdk1/cyclin (1 µ g, 100 U) em um microtubo de 0,5 mL.
Nota: O fragmento do CENP-F tem uma massa molar de 8,6 kDa e quatro sítios de fosforilação de Cdk1 específico. Para um novo substrato, ajuste a concentração de quinase no ensaio de acordo com a concentração molar da proteína e de acordo com o número de sítios de fosforilação. A atividade da unidade populacional de Cdk1/cyclin B recombinante humano é de 20.000 U/mL e a atividade específica é 1.000.000 U / mg. 1 U é definido como a quantidade de Cdk1/cyclin B necessária para catalisar a transferência de 1 pmol de fosfato para substrato de peptídeo de Cdk1 PKTPKKAKKL-NH2 (50 µM) em 1 min a 30 ° C (ver Tabela de materiais). - Preparar uma reação de controle sem Cdk1/cyclin B. Incubar as reações em um banho de água para 1 / 16 h a 30 ° C.
- Analisar 2,5 µ l da reação da quinase do ensaio e 2,5 µ l do controle por SDS-PAGE (etapa 3.11), usando um gel com 16% de acrilamida. Para aumentar a resolução, estenda o tempo de execução.
- Adicione um volume igual de solução de cloridrato de guanidina de 6 M para a reação de ensaio da quinase restantes (e controle). A concentração de cloridrato de guanidina final será de 3 M. analisar estas amostras por espectrometria de massa (seção 6) para identificar os locais de fosforilação ou enviar as amostras para uma instalação de espectrometria de massa para análise e em seguida executar a função de verificação ( Seção 7).
Nota: Para a análise de espectrometria de massa subsequente, é muito importante que a eficiência da fosforilação dos sites individuais é tão alta quanto possível, de preferência 100%, caso contrário não podem ser mapeados os sítios de fosforilação. Para aumentar consideravelmente a eficiência da fosforilação, adicionar quantidades maiores de Cdk1/cyclin B e aumentar o tempo de incubação para 16 h. A concentração de ATP também pode ser duplicada. - Para solução de problemas, realizar um ensaio em vitro da quinase do CENP-F (resíduos 2.987-3.065) como controle positivo. Use o frescos lotes de Cdk1/cyclin B com atividades de alto.
6. identificação dos sítios de fosforilação Cdk1 específicos por espectrometria de massa
- Para desnaturar e do desalt as amostras da proteína, execute do furo micrométrico cromatografia líquida fase reversa com uma coluna de PLRP300.
- Para obter o número de sítios de fosforilação no fragmento CENP-F, analise o intacto em vitro fosforilada CENP-F 84-mer por espectrometria de massa ion trap de ionização electrospray (ESI-ITMS)44,45.
- Para avaliar o local ácido phosphoamino do CENP-F, preparar a tripsina digere do em vitro fosforilada amostras de proteína CENP-F. Do desalt a tripsina digere com pontas de pipeta de dessalinização.
- Analise o digere tryptic do CENP-F por ionização electrospray Fourier transform íon cíclotron ressonância espectrometria de massa (MS ESI-FTICR). Realizar análise em um espectrômetro de massa de ESI-FTICR com um tempo de acumulação de 169 µs.
Nota: A precisão das massas determinado pelo ESI-FTICR MS é dentro de 0,005 amu. Para quantificar a proporção de cada espécie fosforilada respectivo para a quantidade de proteína total, determine as alturas dos picos dos espectros de massa.
7. verificação de funcional: Testando os efeitos de mutações de Phosphomimetic em interações da proteína-proteína por analíticas cromatografia de exclusão
Nota: para verificação funcional dos sítios identificados fosforilação Cdk1-específicas, phosphomimetic mutantes do CENP-F fragmentos foram criados , substituindo os sítios de fosforilação identificado por aspartates. A carga negativa de aspartato imita os efeitos da fosforilação. Um mutante S3048D do fragmento do CENP-F (resíduos 2.987-3.065) foi criado.
- Para verificação funcional, comparar a vinculação do selvagem-tipo e fragmentos phosphomimetic CENP-F para α carioferinas. usam uma filtração de gel analítico como o ensaio de ligação. Para a filtração de gel de analítica, purificar fragmentos CENP-F por cromatografia de afinidade de glutationa (passos 3.1-3.12) e ignorar a etapa de filtração de gel.
- Concentre a proteína para 5-6 mg/mL. Congelam alíquotas de proteína em nitrogênio líquido (etapas 3.15-3.17).
- Fragmentos de mistura o CENP-F purificado (0,1 mg, selvagem-tipo ou a variante de S3048D) e purificado carioferinas α (0,7 mg), em uma relação molar de 1:1. Ajuste o volume da amostra a 200 µ l com amortecedor de gel filtração. Incubar a amostra por 30 min no gelo, filtrar a amostra (tamanho de poro de 0,2 µm) e limpar a amostra por centrifugação (25 min, 21.700 x g, 4 ° C)
- Separe a amostra por cromatografia de exclusão (etapas 3.13-3.14). Use um amortecedor de gel filtração consistindo de 20 mM HEPES, pH 7,5, NaCl, de 150 mM e 2 mM DTT. Realize os experimentos de filtração de gel analítico sob condições idênticas para todas as amostras.
- Calibre a coluna de filtração de gel analítico com padrões de peso molecular de massa molar conhecida como descrito pelo fabricante.
- Analisar as frações de eluição por 16% SDS-PAGE (etapa 3.11).
Resultados
Recentemente nós usamos um em vitro quinase (Figura 1) para identificar locais de fosforilação Cdk1 específicos em um fragmento do CENP-F que continha um cNLS10. Este sinal confira localização nuclear do CENP-F durante a maior parte da interfase. Na fase G2, CENP-F é exportado do núcleo para o citosol na forma Cdk1-dependente. Para obter insights mecanicistas sobre como Cdk1 regula a localização celular do CENP-F, an...
Discussão
Nosso ensaio da quinase em vitro é um método muito poderoso para identificar alvos moleculares para a quinase Cdk1, que é um controlador mestre do ciclo celular e regula muitos processos celulares importantes. O método determina se uma proteína purificada é um substrato para a Cdk1 e permite a identificação dos sítios de fosforilação específica. Isto facilita estudos mecanicistas para regulação de processos celulares por fosforilação através de Cdk1.
O fator mais crí...
Divulgações
Os autores não têm nada para divulgar.
Agradecimentos
Agradecemos o Dr. David King, Howard Hughes Medical Institute, Universidade da Califórnia em Berkeley por análise de espectrometria de massa e comentários úteis. Agradecemos o Dr. Xuelian Zhu, Shanghai, institutos de ciências biológicas, da Academia Chinesa de Ciências, Shanghai, China para fornecer uma construção completo do CENP-F. Finalmente, agradecemos a Dr. Susan Bane, Dr. Brian Callahan e Dr. Christof Grewer na Binghamton University para acesso ao equipamento. Esta pesquisa foi financiada pela Fundação de pesquisa para a Universidade Estadual de Nova York e o departamento de química, Universidade Estadual de Nova York em Binghamton.
Materiais
| Name | Company | Catalog Number | Comments |
| 2800 ml baffled Fernbach flask | Corning | 44232XL | |
| ampicillin | Gold Biotechnology | A-301-25 | |
| ATP | Fisher Scientfiic | BP413-25 | |
| benzamidine hydrochloride | Millipore Sigma | B6506-25 | |
| bottletop filter | Corning | 431161 | |
| Cdk1/cyclin B recombinant, human 20,000 U/mL | New England Biolabs | P6020 | |
| Cdk1/cyclin B (alternate source) | EMD Millipore | 14-450 | |
| Cdk1/cyclin B (alternate source) | Invitrogen | PV3292 | |
| Cdk1/cyclin B + 10x PK buffer | New England Biolabs | P6020 | |
| CENP-F (residues 2987 – 3065) pGEX6P1 plasmid | Available upon request. | ||
| centrifuge: Heraeus Multifuge X3R, cooled, with TX-1000 swing-out rotor | Thermo Scientific | 10033-778 | |
| centrifugal filter units: Amicon Ultra-15 centrifugal filter units, 3 kDa cutoff, Ultracel-PL membranes | EMD Millipore | UFC900324 | |
| chlorampenicol | Gold Biotechnology | C-105-100 | |
| D/L methionine | Agros Organics / Fisher | 125650010 | |
| desalting pipet tips: Zip tips | Millipore Sigma | ZTC18S008 | |
| disposable chromatography columns, Econo-Pac 1.5 x 12 cm | Biorad | 7321010 | |
| dithiothreitol | Gold Biotechnology | DTT50 | |
| E. coli Rosetta 2(DE3)pLysS strain | EMD Millipore | 71403 | |
| electrospray ionization Fourier transform ion | Bruker Amazon | Apex III | |
| cyclotron resonance mass spectrometer | |||
| electrospray ionization ion trap mass spectrometer | Bruker Amazon | custom | |
| fixed angle rotor: Fiberlite F15-8x-50cy | Thermo Scientific | 97040-276 | |
| FPLC system: Äkta Pure FPLC | GE Healthcare | 29032697 | |
| Gel filtration column: Superdex 200 Increase 10/300 GL | GE Healthcare | 28990944 | |
| glutathione agarose | Pierce | 16101 | |
| glutathione, reduced | Millipore Sigma | G4251-50g | |
| incubation shaker: multitron shaker | Infors | I10102 | |
| isopropyl β-D-1-thiogalactopyranoside | Gold Biotechnology | I2481C50 | |
| kanamycin | Gold Biotechnology | K-120-25 | |
| karyopherin α pet-28a pres plasmid | Available upon request. | ||
| Luria Bertani medium | Fisher Scientfiic | BP1426-2 | |
| microcentrifuge 5418R, refrigerated | Eppendorf | 5401000013 | |
| microtubes (0.5 ml) | Eppendorf | 30121023 | |
| microtubes (1.5 ml) | Eppendorf | 30120086 | |
| Nickel affinity gel: His-Select Nickel affinity gel | Millipore Sigma | P6611-100ml | |
| pGEX-6P-1 plasmid | Millipore Sigma | GE28-9546-48 | |
| phenylmethylsulfonyl fluoride | Gold Biotechnology | P470-10 | |
| PS protease: PreScission protease | GE Healthcare | 27084301 | |
| Phos-tag acrylamide | Wako Pure Chem. Ind. | 304-93521 | |
| reduced gluthathione | Millipore Sigma | G4251-50g | |
| roundbottom centrifuge tubes (Oakridge tubes) | Fisher Scientfiic | 055291D | |
| site-directed mutagenesis kit: QuikChange Lightning | Agilent | 210518 | |
| Site-Directed Mutagenesis Kit | |||
| sonifier: Branson S-250D sonifier | Branson | 15 338 125 | |
| Spectra/Por 1RC dialysis membrane (6-8 kDa cutoff) | Spectrum Labs | 08 670B | |
| swing out rotor TX-1000 | Thermo Scientific | 10033-778 |
Referências
- Nurse, P. Cyclin dependent kinases and cell cycle control (Nobel Lecture). ChemBioChem. 3 (7), 596-603 (2002).
- Lee, M. G., Nurse, P. Complementation used to clone a human homologue of the fission yeast cell cycle control gene cdc2. Nature. 327, 31 (1987).
- Lohka, M. J., Hayes, M. K., Maller, J. L. Purification of maturation-promoting factor, an intracellular regulator of early mitotic events. Proc Natl Acad of Sci U S A. 85 (9), 3009-3013 (1988).
- Gautier, J., Norbury, C., Lohka, M., Nurse, P., Maller, J. Purified maturation-promoting factor contains the product of a Xenopus homolog of the fission yeast cell cycle control gene. Cell. 54 (3), 433-439 (1988).
- Gautier, J., Minshull, J., Lohka, M., Glotzer, M., Hunt, T., Maller, J. L. Cyclin is a component of maturation-promoting factor from Xenopus. Cell. 60 (3), 487-494 (1990).
- Ubersax, J. A., Woodbury, E. L., Quang, P. N., Paraz, M., Blethrow, J. D., Shah, K., Shokat, K. M., Morgan, D. O. Targets of the cyclin-dependent kinase Cdk1. Nature. 425 (6960), 859-864 (2003).
- Petrone, A., Adamo, M. E., Cheng, C., Kettenbach, A. N. Identification of Candidate Cyclin-dependent kinase 1 (Cdk1) Substrates in Mitosis by Quantitative Phosphoproteomics. Mol Cell Proteomics. 15 (7), 2448-2461 (2016).
- Vassilev, L. T., Tovar, C., Chen, S., Knezevic, D., Zhao, X., Sun, H., Heimbrook, D. C., Chen, L. Selective small-molecule inhibitor reveals critical mitotic functions of human CDK1. Proc Natl Acad of Sci U S A. 103 (28), 10660-10665 (2006).
- Balakrishnan, A., Vyas, A., Deshpande, K., Vyas, D. Pharmacological cyclin dependent kinase inhibitors: Implications for colorectal cancer. World J Gastroenterol. 22 (7), 2159-2164 (2016).
- Loftus, K. M., Coutavas, E., Cui, H., King, D., Ceravolo, A., Pereiras, D., Solmaz, S. Mechanism for G2 phase-specific nuclear export of the kinetochore protein CENP-F. Cell Cycle. 16 (15), 1414-1429 (2017).
- Baffet, A. D., Hu, D. J., Vallee, R. B. Cdk1 activates pre-mitotic nuclear envelope dynein recruitment and apical nuclear migration in neural stem cells. Dev Cell. 33 (6), 703-716 (2015).
- Songyang, Z., Blechner, S., Hoagland, N., Hoekstra, M. F., Piwnica-Worms, H., Cantley, L. C. Use of an oriented peptide library to determine the optimal substrates of protein kinases. Curr Biol. 4 (11), 973-982 (1994).
- Malumbres, M. Cyclin-dependent kinases. Genome Biol. 15 (6), 122 (2014).
- Peeper, D. S., Parker, L. L., Ewen, M. E., Toebes, M., Hall, F. L., Xu, M., Zantema, A., van der Eb, A. J., Piwnica-Worms, H. A- and B-type cyclins differentially modulate substrate specificity of cyclin-cdk complexes. EMBO J. 12 (5), 1947-1954 (1993).
- Trembley, J., Ebbert, J., Kren, B., Steer, C. Differential regulation of cyclin B1 RNA and protein expression during hepatocyte growth in vivo. Cell Growth Differ. 7 (7), 903-916 (1996).
- Pines, J., Hunter, T. The differential localization of human cyclins A and B is due to a cytoplasmic retention signal in cyclin B. EMBO J. 13 (16), 3772-3781 (1994).
- Morgan, D. O. Principles of CDK regulation. Nature. 374, 131 (1995).
- Larochelle, S., Merrick, K. A., Terret, M. -. E., Wohlbold, L., Barboza, N. M., Zhang, C., Shokat, K. M., Jallepalli, P. V., Fisher, R. P. Requirements for Cdk7 in the assembly of Cdk1/cyclin B and activation of Cdk2 revealed by chemical genetics in human cells. Mol cell. 25 (6), 839-850 (2007).
- Parker, L. L., Sylvestre, P. J., Byrnes, M. J., Liu, F., Piwnica-Worms, H. Identification of a 95-kDa WEE1-like tyrosine kinase in HeLa cells. Proc Natl Acad of Sci U S A. 92 (21), 9638-9642 (1995).
- Atherton-Fessler, S., Parker, L. L., Geahlen, R. L., Piwnica-Worms, H. Mechanisms of p34cdc2 regulation. Mol Cell Biol. 13 (3), 1675-1685 (1993).
- Liu, F., Stanton, J. J., Wu, Z., Piwnica-Worms, H. The human Myt1 kinase preferentially phosphorylates Cdc2 on threonine 14 and localizes to the endoplasmic reticulum and Golgi complex. Mol Cell Biol. 17 (2), 571-583 (1997).
- McGowan, C. H., Russell, P. Human Wee1 kinase inhibits cell division by phosphorylating p34cdc2 exclusively on Tyr15. EMBO J. 12 (1), 75-85 (1993).
- Strausfeld, U., Labbé, J. C., Fesquet, D., Cavadore, J. C., Picard, A., Sadhu, K., Russell, P., Dorée, M. Dephosphorylation and activation of a p34cdc2/cyclin B complex in vitro by human CDC25 protein. Nature. 351, 242 (1991).
- Leuken, R., Clijsters, L., Wolthuis, R. To cell cycle, swing the APC/C. Biochim Biophys Acta. 1786 (1), 49-59 (2008).
- Acquaviva, C., Pines, J. The anaphase-promoting complex/cyclosome: APC/C. J Cell Sci. 119 (12), 2401-2404 (2006).
- Zhu, X., Chang, K. -. H., He, D., Mancini, M. A., Brinkley, W. R., Lee, W. -. H. The C-terminus of mitosin is essential for its nuclear localization, centromere/kinetochore targeting, and dimerization. J Biol Chem. 270 (33), 19545-19550 (1995).
- Liao, H., Winkfein, R. J., Mack, G., Rattner, J. B., Yen, T. J. CENP-F is a protein of the nuclear matrix that assembles onto kinetochores at late G2 and is rapidly degraded after mitosis. J Cell Biol. 130 (3), 507-518 (1995).
- Rattner, J. B., Rao, A., Fritzler, M. J., Valencia, D. W., Yen, T. J. CENP-F is a ca 400 kDa kinetochore protein that exhibits a cell-cycle dependent localization. Cell Motil Cytoskeleton. 26 (3), 214-226 (1993).
- Christie, M., Chang, C. -. W., Rona, G., Smith, K. M., Stewart, A. G., Takeda, A. A. S., Fontes, M. R. M., Stewart, M., Vertessy, B. G., Forwood, J. K., Kobe, B. Structural biology and regulation of protein import into the nucleus. J Mol Biol. 428 (10A), 2060-2090 (2016).
- Zuccolo, M., Alves, A., Galy, V., Bolhy, S., Formstecher, E., Racine, V., Sibarita, J. B., Fukagawa, T., Shiekhattar, R., Yen, T., Doye, V. The human Nup107/160 nuclear pore subcomplex contributes to proper kinetochore functions. EMBO J. 26, 1853-1864 (2007).
- Bolhy, S., Bouhlel, I., Dultz, E., Nayak, T., Zuccolo, M., Gatti, X., Vallee, R., Ellenberg, J., Doye, V. A Nup133-dependent NPC-anchored network tethers centrosomes to the nuclear envelope in prophase. J Cell Biol. 192 (5), 855-871 (2011).
- Hu, D. J., Baffet, A. D., Nayak, T., Akhmanova, A., Doye, V., Vallee, R. B. Dynein recruitment to nuclear pores activates apical nuclear migration and mitotic entry in brain progenitor cells. Cell. 154 (6), 1300-1313 (2013).
- Vergnolle, M. S., Taylor, S. S. Cenp-F links kinetochores to Ndel1/Nde1/Lis1/Dynein microtubule motor complexes. Curr Biol. 17 (13), 1173-1179 (2007).
- Yang, Z. Y., Guo, J., Li, N., Qian, M., Wang, S. N., Zhu, X. L. Mitosin/CENP-F is a conserved kinetochore protein subjected to cytoplasmic dynein-mediated poleward transport. Cell Res. 13 (4), 275-283 (2003).
- Yang, Z., Guo, J., Chen, Q., Ding, C., Du, J., Zhu, X. Silencing mitosin induces misaligned chromosomes, premature chromosome decondensation before anaphase onset, and mitotic cell death. Mol Cell Biol. 25 (10), 4062-4074 (2005).
- Xue, Y., Ren, J., Gao, X., Jin, C., Wen, L., Yao, X. GPS 2.0, a tool to predict kinase-specific phosphorylation sites in hierarchy. Mol Cell Proteomics. 7 (9), 1598-1608 (2008).
- Song, C., Ye, M., Liu, Z., Cheng, H., Jiang, X., Han, G., Songyang, Z., Tan, Y., Wang, H., Ren, J., Xue, Y., Zou, H. Systematic analysis of protein phosphorylation networks from phosphoproteomic data. Mol Cell Proteomics. 11 (10), 1070-1083 (2012).
- UniProt-Consortium. UniProt: the universal protein knowledgebase. Nucleic Acids Res. 45 (D1), D158-D169 (2017).
- Olsen, J. V., Vermeulen, M., Santamaria, A., Kumar, C., Miller, M. L., Jensen, L. J., Gnad, F., Cox, J., Jensen, T. S., Nigg, E. A., Brunak, S., Mann, M. Quantitative phosphoproteomics reveals widespread full phosphorylation site occupancy during mitosis. Science Signal. 3 (104), ra3 (2010).
- Dephoure, N., Zhou, C., Villén, J., Beausoleil, S. A., Bakalarski, C. E., Elledge, S. J., Gygi, S. P. A quantitative atlas of mitotic phosphorylation. Proc Natl Acad of Sci U S A. 105 (31), 10762-10767 (2008).
- Rona, G., Marfori, M., Borsos, M., Scheer, I., Takacs, E., Toth, J., Babos, F., Magyar, A., Erdei, A., Bozoky, Z., Buday, L., Kobe, B., Vertessy, B. G. Phosphorylation adjacent to the nuclear localization signal of human dUTPase abolishes nuclear import: structural and mechanistic insights. Acta Cryst D. 69 (12), 2495-2505 (2013).
- Harreman, M. T., Kline, T. M., Milford, H. G., Harben, M. B., Hodel, A. E., Corbett, A. H. Regulation of nuclear import by phosphorylation adjacent to nuclear localization signals. J Biol Chem. 279 (20), 20613-20621 (2004).
- Kosugi, S., Hasebe, M., Tomita, M., Yanagawa, H. Systematic identification of cell cycle-dependent yeast nucleocytoplasmic shuttling proteins by prediction of composite motifs. Proc Natl Acad Sci U S A. 106 (25), 10171-10176 (2009).
- McLachlin, D. T., Chait, B. T. Analysis of phosphorylated proteins and peptides by mass spectrometry. Curr Opin Chem Biol. 5 (5), 591-602 (2001).
- Van Berkel, G. J., Glish, G. L., McLuckey, S. A. Electrospray ionization combined with ion trap mass spectrometry. Anal Chem. 62 (13), 1284-1295 (1990).
- Hodel, A. E., Harreman, M. T., Pulliam, K. F., Harben, M. E., Holmes, J. S., Hodel, M. R., Berland, K. M., Corbett, A. H. Nuclear localization signal receptor affinity correlates with in vivo localization in Saccharomyces cerevisiae. J Biol Chem. 281 (33), 23545-23556 (2006).
- Hong, K. U., Kim, H. -. J., Kim, H. -. S., Seong, Y. -. S., Hong, K. -. M., Bae, C. -. D., Park, J. Cdk1-Cyclin B1-mediated Phosphorylation of Tumor-associated Microtubule-associated Protein/Cytoskeleton-associated Protein 2 in Mitosis. J Biol Chem. 284 (24), 16501-16512 (2009).
- Meraldi, P., Lukas, J., Fry, A. M., Bartek, J., Nigg, E. A. Centrosome duplication in mammalian somatic cells requires E2F and Cdk2–Cyclin A. Nature Cell Biol. 1, 88 (1999).
- Heuvel, S., Harlow, E. Distinct roles for cyclin-dependent kinases in cell cycle control. Science. 262 (5142), 2050-2054 (1993).
- Kinoshita, E., Kinoshita-Kikuta, E., Takiyama, K., Koike, T. Phosphate-binding Tag, a New Tool to Visualize Phosphorylated Proteins. Mol Cell Proteomics. 5 (4), 749-757 (2006).
- Takeda, H., Kawasaki, A., Takahashi, M., Yamada, A., Koike, T. Matrix-assisted laser desorption/ionization time-of-flight mass spectrometry of phosphorylated compounds using a novel phosphate capture molecule. Rapid Commun Mass Spectrom. 17 (18), 2075-2081 (2003).
- Linder, M. I., Köhler, M., Boersema, P., Weberruss, M., Wandke, C., Marino, J., Ashiono, C., Picotti, P., Antonin, W., Kutay, U. Mitotic Disassembly of Nuclear Pore Complexes Involves CDK1- and PLK1-Mediated Phosphorylation of Key Interconnecting Nucleoporins. Dev Cell. 43 (2), (2017).
- Arai, T., Haze, K., Iimura-Morita, Y., Machida, T., Iida, M., Tanaka, K., Komatani, H. Identification of β-catenin as a novel substrate of polo-like kinase 1. Cell Cycle. 7 (22), 3556-3563 (2008).
- Hansen, D. V., Tung, J. J., Jackson, P. K. CaMKII and Polo-like kinase 1 sequentially phosphorylate the cytostatic factor Emi2/XErp1 to trigger its destruction and meiotic exit. Proc Natl Acad of Sci U S A. 103 (3), 608-613 (2006).
- Zhang, Y., Dong, Z., Nomura, M., Zhong, S., Chen, N., Bode, A. M., Dong, Z. Signal Transduction Pathways Involved in Phosphorylation and Activation of p70S6K Following Exposure to UVA Irradiation. J Biol Chem. 276 (24), 20913-20923 (2001).
- Richard, D. E., Berra, E., Gothié, E., Roux, D., Pouysségur, J. p42/p44 Mitogen-activated Protein Kinases Phosphorylate Hypoxia-inducible Factor 1α (HIF-1α) and Enhance the Transcriptional Activity of HIF-1. J Biol Chem. 274 (46), 32631-32637 (1999).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados