É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Avaliando as medidas de resultados da conectividade da unidade motora do diafragma do rato como biomarcadores quantitativos da degeneração e compensação do neurônio motor frênico
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Neste estudo, apresentamos um método in vivo para estimar o número e o tamanho da unidade motora para quantificar a conectividade da unidade motora do diafragma de ratos. Uma abordagem passo a passo para essas técnicas é descrita.
Resumo
A perda da função muscular ventilatória é uma consequência da lesão do neurônio motor e da neurodegeneração (por exemplo, lesão da medula espinhal cervical e esclerose lateral amiotrófica, respectivamente). Os neurônios motores frênicos são o elo final entre o sistema nervoso central e o músculo, e suas respectivas unidades motoras (grupos de fibras musculares inervadas por um único neurônio motor) representam a menor unidade funcional do sistema ventilatório neuromuscular. O potencial de ação muscular composto (CMAP), o potencial de unidade motora única (SMUP) e a estimativa do número de unidades motoras (MUNE) são abordagens eletrofisiológicas estabelecidas que permitem a avaliação longitudinal da integridade da unidade motora em modelos animais ao longo do tempo, mas têm sido aplicadas principalmente aos músculos dos membros. Portanto, os objetivos deste estudo são descrever uma abordagem em estudos pré-clínicos com roedores que pode ser usada longitudinalmente para quantificar o MUNE frênico, o tamanho da unidade motora (representado como SMUP) e o CMAP e, em seguida, demonstrar a utilidade dessas abordagens em um modelo de perda de neurônios motores. Biomarcadores sensíveis, objetivos e translacionalmente relevantes para lesão neuronal, degeneração e regeneração em lesões e doenças do neurônio motor podem ajudar significativamente e acelerar as descobertas de pesquisas experimentais para testes clínicos.
Introdução
Os neurônios motores frênicos (MNs), estendendo-se dos níveis de miótomo C3 a C6, formam o elo final do sistema nervoso central (SNC) ao músculo diafragma1. As unidades motoras frênicas (MUs) são compostas por um único MN espinhal e suas fibras musculares diafragmáticas inervadas formando a menor unidade funcional do sistema neuromuscular respiratório. A função ventilatória requer contração adequada do músculo diafragma obtida por meio da ativação coordenada do pool frênico deMU2,3. Muitas doenças neurológicas, incluindo a esclerose lateral amiotrófica (ELA), resultam em grave comprometimento ventilatório, contribuindo para a causa da morte4.
Várias abordagens eletrofisiológicas podem ser empregadas para avaliar e monitorar a integridade do pool de unidades motoras (MU) in vivo. O potencial de ação muscular composto (CMAP) reflete a despolarização somada de todas as fibras musculares em um músculo ou grupo muscular específico após a estimulação do nervo periférico e é sensível a uma variedade de condições neuromusculares, incluindo ELA 5,6 e atrofia muscular espinhal (AME)7,8,9. Uma limitação da avaliação do CMAP é que o brotamento colateral pode levar à manutenção da amplitude e área do CMAP, mesmo na presença de perda de MU10. Para superar essa limitação, modificações foram feitas na técnica de CMAP para avaliar o número de unidades motoras e o tamanho11. Além disso, um estudo in vivo que investigou a avaliação funcional da CMAP do diafragma por um sistema eletrofisiológico sugeriu que também pode ser viável utilizar a técnica de registro da CMAP do diafragma descrita para estimativa do número de unidades motoras12.
A técnica de estimativa do número de unidades motoras incrementais (MUNE) foi inicialmente introduzida no início da década de 1970 por McComas et al. para o músculo extensor curto dos dedos em humanos13. A abordagem incremental MUNE foi uma modificação da técnica tradicional de registro CMAP, durante a qual uma estimulação gradualmente crescente foi fornecida para registrar incrementos submáximos quantais, tudo ou nada, como índices de respostas de unidade motora única. Os incrementos somados e médios foram usados para calcular uma estimativa para o tamanho de um único potencial de unidade motora (SMUP). Esse tamanho calculado foi então dividido na amplitude do CMAP para estimar o número de MUs que inervam o músculo examinado11. O MUNE demonstra alta sensibilidade na detecção e monitoramento da perda de unidades motoras, permitindo a identificação de disfunção da unidade motora antes de alterações observáveis em medidas como amplitude ou área de CMAP14,15. Em pacientes com ELA, o MUNE provou ser excepcionalmente sensível, servindo como um biomarcador proeminente para o início, progressão e prognóstico da doença16,17.
Numerosas adaptações do MUNE foram desenvolvidas e amplamente utilizadas para avaliar a função do MU em condições como neurodegeneração, lesão neural e o processo natural de envelhecimento 18,19,20,21. Desde a descrição inicial, várias adaptações utilizando respostas eletrofisiológicas e medições de força incremental (mecânica) foram empregadas em estudos em humanos e modelos animais22. O MUNE fornece uma avaliação funcional não invasiva da conectividade do neurônio motor com o músculo. A aplicação longitudinal do MUNE permite a compreensão da progressão da doença ou do fenótipo induzido e a avaliação dos efeitos protetores ou regenerativos das intervenções terapêuticas, tanto em ambientes clínicos quanto pré-clínicos. Independentemente da eficácia da reprodutibilidade das medidas do MUNE e da relevância clínica da técnica para pools de MU na maior parte do corpo humano, os esforços têm se concentrado principalmente nos músculos dos membros nos músculos de roedores 10,23,24,25.
Portanto, os objetivos deste estudo foram descrever uma abordagem para obter potencial de ação muscular composto (CMAP), SMUP e número de unidades motoras frênicas (MUNE) como avaliações in vivo que podem ser usadas longitudinalmente em estudos pré-clínicos com roedores para quantificar o MUNE, tamanho da unidade motora (representada como SMUP) e CMAP. Além disso, apresentamos dados representativos que destacam a perda do número de MU do diafragma após a administração intrapleural de um agente degenerativo frênico do NM, fragmento B da toxina da cólera conjugado à saporina (CTB-SAP).
Protocolo
Todos os procedimentos foram aprovados e conduzidos em conformidade com as diretrizes estabelecidas pelo Comitê Institucional de Cuidados e Uso de Animais da Universidade de Missouri. Os experimentos foram realizados em ratos Sprague-Dawley machos adultos, com idade entre 11 e 15 semanas. Esses ratos foram alojados em pares e mantidos sob um ciclo claro-escuro de 12:12, com acesso a alimentos peletizados comerciais padrão e água tratada com HCl disponível o tempo todo.
1. Preparação do animal e administração da anestesia
- Use equipamento de proteção individual adequado ao manusear ratos.
- Administrar anestésico inalatório com isoflurano a 3-5%, garantindo a indução adequada. Uma vez que o rato esteja adequadamente anestesiado, coloque-o em decúbito dorsal e mantenha a anestesia com isoflurano inalado a 1-3%. Verifique a suficiência da profundidade da anestesia aplicando pressão suavemente na almofada do pé do membro posterior usando uma pinça para garantir que não haja resposta de retirada.
NOTA: Com base no tamanho e peso do rato, monitore a profundidade da anestesia e ajuste a concentração de isoflurano de acordo. - Mantenha a temperatura de 37 °C usando uma placa de aquecimento termostática para evitar variações de temperatura que possam afetar a amplitude e a latência do CMAP.
- Aplique uma pomada veterinária à base de petróleo nos olhos para evitar o ressecamento. Monitore a profundidade da anestesia observando a frequência respiratória e verificando as respostas de retirada ao aplicar pressão na almofada do pé com uma pinça.
- Remova os pelos do terço inferior do tórax e pescoço para serem estudados com aparadores. Monitore a respiração do rato durante todo o experimento.
NOTA: Após os registros CMAP e MUNE e a descontinuação da anestesia, não deixe o rato sem vigilância até que ele tenha recuperado a consciência suficiente. Não devolva o animal à gaiola de casa até que esteja totalmente recuperado.
2. Colocação e configuração do eletrodo
- Coloque um par de eletrodos de agulha monopolares de 28 G para registrar o CMAP, SMUP e MUNE conforme ilustrado na Figura 1.
- Coloque o eletrodo de agulha ativo (E1) por via subcutânea sobre a linha clavicular média inferior à última borda da costela e o eletrodo de agulha de referência (E2) por via subcutânea no ângulo entre o processo xifóide e a última cartilagem esternocostal.
NOTA: Os eletrodos da agulha não devem ser inseridos no músculo diafragma; em vez disso, eles devem ser posicionados na área subcutânea.
- Coloque o eletrodo de agulha ativo (E1) por via subcutânea sobre a linha clavicular média inferior à última borda da costela e o eletrodo de agulha de referência (E2) por via subcutânea no ângulo entre o processo xifóide e a última cartilagem esternocostal.
- Para a estimulação do nervo frênico na lâmina carotídea, use um par de eletrodos de agulha monopolar 28 G como cátodo e ânodo para estimulação nervosa e colocados subcutaneamente sobre o pescoço lateral entre os músculos escaleno anterior e médio, separados por aproximadamente 1 cm. Certifique-se de que a colocação das agulhas estimulantes esteja no nível abaixo da quarta vértebra cervical (C4).
NOTA: Evite inserir os eletrodos estimulantes muito fundo para evitar lesões no nervo frênico ou em outra estrutura. A Figura 1 ilustra a colocação do eletrodo. - Para o eletrodo de aterramento, coloque um eletrodo de superfície descartável na cauda.
3. Aquisição de dados
- CMAP frênico
- Registre as respostas frênicas do CMAP aplicando pulsos catódicos monofásicos de onda quadrada com duração de 0,1 ms e intensidade variando de 60 a 100 mA para estimular o nervo frênico.
- Obtenha respostas CMAP enquanto aumenta progressivamente a intensidade do estímulo até que a amplitude da resposta deixe de mostrar qualquer aumento adicional. Para garantir a estimulação supramáxima, aumente a intensidade do estímulo para aproximadamente 120% do nível usado para obter uma resposta máxima e registre uma resposta adicional. Se o tamanho do CMAP não aumentar mais, considere essa resposta como o CMAP máximo.
NOTA: Fornecer estimulação durante a expiração é preferível para minimizar o ruído da atividade muscular simultânea durante a gravação do CMAP. - Meça e documente as amplitudes pico a pico do CMAP em milivolts (mV) (Figura 2).
NOTA: A amplitude do CMAP pode ser avaliada de base a pico e pico a pico. Os sistemas de eletrodiagnóstico clínico são frequentemente padronizados para avaliar a base ao pico, que é calculada a partir da linha de base isoelétrica até o pico negativo inicial.
- Tamanho médio do potencial de unidade motora única (SMUP) e cálculo do MUNE
- Calcule o tamanho médio do SMUP usando uma técnica de estimulação incremental.
- Para obter respostas incrementais, administre estimulação submáxima com duração de 0,1 ms na frequência de 1 Hz, aumentando gradualmente a intensidade em incrementos de 0,03 mA até que uma resposta mínima de tudo ou nada seja alcançada. Adquira a resposta inicial com uma intensidade de estímulo variando entre 2 mA e 10 mA.
- Se a resposta inicial não ocorrer com uma intensidade de estímulo entre 2 mA e 10 mA, modifique a posição do cátodo estimulante, aproximando-o ou afastando-o do nervo frênico no pescoço, para diminuir ou aumentar a intensidade do estímulo necessário, respectivamente.
- Se a primeira resposta incremental for alcançada com uma intensidade de estímulo variando de 2 mA a 10 mA, salve a primeira resposta e adquira incrementos adicionais com intensidades de estímulo progressivamente mais altas, ajustando em incrementos de 0,03 mA, para obter um total de 9 incrementos adicionais que atendam aos seguintes critérios na etapa 3.2.2.
NOTA: Cada SMUP é quantificado subtraindo cada incremento do incremento anterior.
- Ao medir as respostas incrementais, certifique-se de que cada incremento atenda aos seguintes critérios:
- Certifique-se de que o pico negativo inicial das respostas incrementais esteja alinhado temporalmente com o pico negativo da resposta CMAP máxima.
NOTA: Os pequenos movimentos observados devido ao ruído de fundo dos ciclos respiratórios são inerentes à natureza do experimento. No entanto, a presença consistente de SMUPs durante a observação ao vivo confirma sua identidade para esse CMAP específico. - Como o diafragma é um músculo dinâmico envolvido na respiração, cada ciclo respiratório pode induzir o movimento basal. Assim, verifique a estabilidade e a ausência de fracionamento em cada resposta incremental, confirmando a consistência em três respostas duplicadas.
NOTA: Para distinguir os potenciais evocados de baixa amplitude, especialmente o primeiro SMUP, do ruído de fundo devido à atividade respiratória, é importante permanecer vigilante e observar por 3-4 ciclos respiratórios. Garanta também o alinhamento dos picos com os do CMAP para precisão. - Certifique-se de que cada incremento seja distinto e maior que o anterior. Portanto, distinga visualmente as respostas incrementais em tempo real, observando-as à medida que se sobrepõem aos incrementos registrados anteriormente.
NOTA: Várias réplicas do estímulo em cada amplitude podem ser conduzidas para garantir a consistência nos incrementos e a conformidade com os critérios predefinidos. - Depois de verificar visualmente cada incremento com os critérios acima mencionados, confirme se a amplitude do incremento é de pelo menos 25 μV. Se o incremento for inferior a 25 μV, rejeitar a medição e reavaliar a resposta.
- Após o registro de 10 respostas incrementais, verifique se a amplitude de cada resposta de incremento não é maior que um terço da amplitude combinada de todos os 10 incrementos, representando a amplitude total da resposta final. Se este critério não for satisfeito, repetir a medição das 10 respostas incrementais.
NOTA: O limite de um terço é baseado na suposição de que cada resposta incremental representa a ativação de uma única unidade motora. Se a amplitude de qualquer resposta incremental exceder um terço da amplitude combinada de todos os dez incrementos, isso sugere que a resposta pode não ser exclusivamente atribuível à ativação de uma única unidade motora. Em vez disso, pode ser influenciado pelo recrutamento de unidades motoras adicionais ou pela presença de atividade inespecífica, como ruído elétrico ou artefatos22,26. - Para estimar a amplitude média dos SMUPs, calcule a média dos valores dos 10 incrementos. Outro método para medir a amplitude média do SMUP é dividir toda a amplitude da resposta incremental final pelo número total de incrementos11.
- Certifique-se de que o pico negativo inicial das respostas incrementais esteja alinhado temporalmente com o pico negativo da resposta CMAP máxima.
- Determine o MUNE dividindo a amplitude máxima do CMAP (pico a pico) pela amplitude média do SMUP (pico a pico). Em certos sistemas eletrofisiológicos, os SMUPs são registrados em microvolts (μV), enquanto o CMAP é geralmente expresso em milivolts (mV). Se necessário, converta as medições CMAP e SMUP para as mesmas unidades antes de calcular o MUNE.
NOTA: CMAP pico a pico, SMUP médio e MUNE são normalmente calculados automaticamente por sistemas de eletromiografia clínica):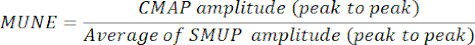
CMAP = Potencial de Ação Muscular Composto
SMUP = Potencial de Unidade de Motor Único
MUNE = Estimativa do Número de Unidades Motoras
- Calcule o tamanho médio do SMUP usando uma técnica de estimulação incremental.
Resultados
As técnicas CMAP, SMUP e MUNE descritas neste relatório permitem o registro da função neuromuscular no músculo diafragma empregando a colocação de eletrodos minimamente invasivos (Figura 1). Os parâmetros de amplitude e área podem ser empregados para caracterizar o tamanho supramáximo do CMAP, fornecendo uma medida global da produção do grupo muscular (Figura 2). No entanto, em nossos métodos atuais, contamos com a ...
Discussão
Nas doenças degenerativas do NM, como a ELA, é crucial avaliar as MUs envolvidas na ventilação28. Apesar da ocorrência de degeneração respiratória do NM em pacientes com ELA, o início específico e a progressão da morte por NM permanecem incompletamente compreendidos 29,30,31. Reconhecendo a importância desse aspecto, vários modelos, tanto de base genética (p...
Divulgações
A WDA recebeu financiamento de pesquisa da NMD Pharma, Avidity Biosciences e honorários de consultoria da NMD Pharma, Avidity Biosciences, Dyne Therapeutics, Novartis, Design Therapeutics, Catalyst Pharmaceuticals e Novartis.
Agradecimentos
Este trabalho foi financiado por uma bolsa do Programa de Pesquisa de Lesões/Doenças da Medula Espinhal do Programa de Pesquisa de Lesões/Doenças da Medula Espinhal do Missouri (NLN e WDA).
Materiais
| Name | Company | Catalog Number | Comments |
| 2 mL Glass Syringe | Kent Scientific Corporation | SOMNO-2ML | |
| 50 mL, Model 705 RN syringe | Hamilton Company | 7637-01 | Utilized to conduct intrapleural injection |
| 5008 - Formulab Diet | LabDiet | 0001325 | |
| Autoclavable 26 G needles (26S RN 9.52 mm 40°) | Hamilton Company | 7804-04 | Utilized to conduct intrapleural injection |
| Cholera toxin B-subunit (CTB) | MilliporeSigma | C9903 | Utilized for intrapleural injection to label surviving motor neurons |
| Cholera toxin B-subunit conjugated to saporin (CTB-SAP) | Advanced Targeting Systems | IT-14 | Utilized for intrapleural injection to cause motor neuron death |
| Detachable Cable | Technomed | 202845-0000 | to connect the recorder electrode to the electrodiagnostic machine |
| Disposable 2" x 2" disc electrode with leads | Cadwell | 302290-000 | ground electrode |
| disposable monopolar needles 28 G | Technomed | 202270-000 | cathode and anode stimulating electrodes- recording electrodes |
| EMG needle cable (Amp/stim switch box) | Cadwell | 190266-200 | to connect monopolar electrodes to electrodiagnostic stimulator |
| Helping Hands alligator clip with iron base | Radio Shack | 64-079 | Maintaining recording electrode placement |
| Isoflurane (250 mL bottle) | Piramal Healthcare | ||
| monoject curved tip irrigating syringe | Covidien | 81412012 | utilized for application of electrode gel |
| PhysioSuite Physiological Monitoring System with RightTemp Homeothermic Warming | Kent Scientific Corporation | PS-RT | Includes infrared warming pad, rectal probe, and pad temperature probe |
| Pro trimmer Pet Grooming Kit | Oster | 078577-010-003 | clippers for hair removal |
| Saporin (SAP) | Advanced Targeting Systems | PR-01 | Utilized for intrapleural injection (control agent when injected by itself) |
| Sierra Summit EMG system | Cadwell Industries, Inc., Kennewick, WA | portable electrodiagnostic system | |
| SomnoSuite Low-Flow Digital Anesthesia System | Kent Scientific Corporation | SOMNO | Includes anti-spill, anti-vapor bottle top adapter; Y adapter tubing; charcoal scavenging filter |
| Sprague-Dawley rat | Envigo colony 208a, Indianapolis, IN | ||
| Veterinarian petroleum-based ophthalmic ointment | Puralube | 26870 | applied during anesthesia to avoid corneal injury |
Referências
- Mantilla, C. B., Zhan, W. -. Z., Sieck, G. C. Retrograde labeling of phrenic motoneurons by intrapleural injection. J Neurosci Methods. 182 (2), 244-249 (2009).
- Nichols, N. L., Satriotomo, I., Harrigan, D. J., Mitchell, G. S. Acute intermittent hypoxia induced phrenic long-term facilitation despite increased sod1 expression in a rat model of als. Exp Neurol. 273, 138-150 (2015).
- Nichols, N. L., Craig, T. A., Tanner, M. A. Phrenic long-term facilitation following intrapleural ctb-sap-induced respiratory motor neuron death. Respir Physiol Neurobiol. 256, 43-49 (2018).
- Kiernan, M. C., et al. Amyotrophic lateral sclerosis. Lancet. 377 (9769), 942-955 (2011).
- Boërio, D., Kalmar, B., Greensmith, L., Bostock, H. Excitability properties of mouse motor axons in the mutant sod1g93a model of amyotrophic lateral sclerosis. Muscle Nerve. 41 (6), 774-784 (2010).
- Shibuya, K., et al. Motor cortical function determines prognosis in sporadic als. Neurology. 87 (5), 513-520 (2016).
- Lewelt, A., et al. Compound muscle action potential and motor function in children with spinal muscular atrophy. Muscle Nerve. 42 (5), 703-708 (2010).
- Mcgovern, V. L., et al. Smn expression is required in motor neurons to rescue electrophysiological deficits in the smnδ7 mouse model of sma. Hum Mol Genet. 24 (19), 5524-5541 (2015).
- Arnold, W. D., et al. Electrophysiological biomarkers in spinal muscular atrophy: Preclinical proof of concept. Ann Clin Transl Neurol. 1 (1), 34-44 (2014).
- Harrigan, M. E., et al. Assessing rat forelimb and hindlimb motor unit connectivity as objective and robust biomarkers of spinal motor neuron function. Sci Rep. 9 (1), 16699 (2019).
- Arnold, W. D., et al. Electrophysiological motor unit number estimation (mune) measuring compound muscle action potential (cmap) in mouse hindlimb muscles. J. Vis. Exp: JoVE. (103), e52899 (2015).
- Martin, M., Li, K., Wright, M. C., Lepore, A. C. Functional and morphological assessment of diaphragm innervation by phrenic motor neurons. J. Vis. Exp: JoVE. (99), e52605 (2015).
- Mccomas, A., Fawcett, P. R. W., Campbell, M., Sica, R. Electrophysiological estimation of the number of motor units within a human muscle. J Neurol Neurosurg Psychiatry. 34 (2), 121-131 (1971).
- Felice, K. J. A longitudinal study comparing thenar motor unit number estimates to other quantitative tests in patients with amyotrophic lateral sclerosis. Muscle Nerve. 20 (2), 179-185 (1997).
- Vucic, S., Rutkove, S. B. Neurophysiological biomarkers in amyotrophic lateral sclerosis. Curr Opin Neurol. 31 (5), 640-647 (2018).
- Carleton, S., Brown, W. Changes in motor unit populations in motor neurone disease. J Neurol Neurosurg Psychiatry. 42 (1), 42-51 (1979).
- Yuen, E. C., Olney, R. K. Longitudinal study of fiber density and motor unit number estimate in patients with amyotrophic lateral sclerosis. Neurology. 49 (2), 573-578 (1997).
- Gooch, C. L., et al. Motor unit number estimation: A technology and literature review. Muscle Nerve. 50 (6), 884-893 (2014).
- Henderson, R. D., Ridall, P. G., Hutchinson, N. M., Pettitt, A. N., Mccombe, P. A. Bayesian statistical mune method. Muscle Nerve. 36 (2), 206-213 (2007).
- Shefner, J., et al. Multipoint incremental motor unit number estimation as an outcome measure in als. Neurology. 77 (3), 235-241 (2011).
- Stein, R. B., Yang, J. F. Methods for estimating the number of motor units in human muscles. Ann Neurol. 28 (4), 487-495 (1990).
- Shefner, J. M. Motor unit number estimation in human neurological diseases and animal models. Clin Neurophysiol. 112 (6), 955-964 (2001).
- Ahad, M., Rutkove, S. Correlation between muscle electrical impedance data and standard neurophysiologic parameters after experimental neurogenic injury. Physiol Meas. 31 (11), 1437 (2010).
- Kasselman, L. J., Shefner, J. M., Rutkove, S. B. Motor unit number estimation in the rat tail using a modified multipoint stimulation technique. Muscle Nerve. 40 (1), 115-121 (2009).
- Ngo, S., et al. The relationship between bayesian motor unit number estimation and histological measurements of motor neurons in wild-type and sod1g93a mice. Clin Neurophysiol. 123 (10), 2080-2091 (2012).
- Feasby, T., Brown, W. Variation of motor unit size in the human extensor digitorum brevis and thenar muscles. J Neurol Neurosurg Psychiatry. 37 (8), 916-926 (1974).
- Nichols, N. L., Vinit, S., Bauernschmidt, L., Mitchell, G. S. Respiratory function after selective respiratory motor neuron death from intrapleural ctb-saporin injections. Exp Neurol. 267, 18-29 (2015).
- Nichols, N. L., et al. Ventilatory control in als. Respir Physiol Neurobiol. 189 (2), 429-437 (2013).
- Cifra, A., Nani, F., Nistri, A. Respiratory motoneurons and pathological conditions: Lessons from hypoglossal motoneurons challenged by excitotoxic or oxidative stress. Respir Physiol Neurobiol. 179 (1), 89-96 (2011).
- Kobayashi, Z., et al. Fals with gly72ser mutation in sod1 gene: Report of a family including the first autopsy case. J Neurol Sci. 300 (1), 9-13 (2011).
- Su, M., Wakabayashi, K., Tanno, Y., Inuzuka, T., Takahashi, H. An autopsy case of amyotrophic lateral sclerosis with concomitant alzheimer's and incidental lewy body diseases. No to shinkei= Brain and nerve. 48 (10), 931-936 (1996).
- Lladó, J., et al. Degeneration of respiratory motor neurons in the sod1 g93a transgenic rat model of als. Neurobiol Dis. 21 (1), 110-118 (2006).
- Borkowski, L. F., Smith, C. L., Keilholz, A. N., Nichols, N. L. Divergent receptor utilization is necessary for phrenic long-term facilitation over the course of motor neuron loss following ctb-sap intrapleural injections. J Neurophysiol. 126 (3), 709-722 (2021).
- Nicolopoulos-Stournaras, S., Iles, J. F. Motor neuron columns in the lumbar spinal cord of the rat. J Comp Neurol. 217 (1), 75-85 (1983).
- Tosolini, A. P., Morris, R. Targeting motor end plates for delivery of adenoviruses: An approach to maximize uptake and transduction of spinal cord motor neurons. Sci Rep. 6 (1), 33058 (2016).
- Mchanwell, S., Biscoe, T. The localization of motoneurons supplying the hindlimb muscles of the mouse. Phil. Trans. R. , 477-508 (1981).
- Nair, J., et al. Histological identification of phrenic afferent projections to the spinal cord. Respir Physiol Neurobiol. 236, 57-68 (2017).
- Courtine, G., et al. Can experiments in nonhuman primates expedite the translation of treatments for spinal cord injury in humans. Nat Med. 13 (5), 561-566 (2007).
- Friedli, L., et al. Pronounced species divergence in corticospinal tract reorganization and functional recovery after lateralized spinal cord injury favors primates. Sci Transl Med. 7 (302), 134 (2015).
- Arnold, R., et al. Nerve excitability in the rat forelimb: A technique to improve translational utility. J Neurosci Methods. 275, 19-24 (2017).
- Boriek, A., Rodarte, J., Reid, M. Shape and tension distribution of the passive rat diaphragm. Am J Physiol Regul Integr Comp Physiol. 280, R33-R41 (2001).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados