Organoides do Epitélio da Superfície do Ovário Humano como Plataforma para Estudar a Regeneração Tecidual
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Este protocolo descreve o estabelecimento de organoides de tecido tridimensionais (3D) a partir de células primárias do epitélio da superfície ovariana humana (hOSE). O protocolo inclui isolamento de hOSE de ovários recém-coletados, expansão celular do hOSE, procedimentos de criopreservação-descongelamento e derivação de organoides. Imunofluorescência, análise quantitativa e demonstração da utilidade como plataforma de triagem estão incluídas.
Resumo
O epitélio da superfície ovariana (OSE), a camada mais externa do ovário, sofre ruptura durante cada ovulação e desempenha um papel crucial na cicatrização de feridas ovarianas enquanto restaura a integridade ovariana. Além disso, o OSE pode servir como fonte de câncer de ovário epitelial. Embora as propriedades regenerativas da OSE tenham sido bem estudadas em camundongos, a compreensão do mecanismo preciso de reparo tecidual no ovário humano permanece dificultada pelo acesso limitado aos ovários humanos e protocolos de cultura in vitro adequados. Organoides específicos de tecidos, modelos in vitro miniaturizados que replicam aspectos estruturais e funcionais do órgão original, oferecem novas oportunidades para estudar a fisiologia do órgão, modelagem de doenças e testes de drogas.
Aqui, descrevemos um método para isolar OSE humano primário (hOSE) de ovários inteiros e estabelecer organoides hOSE. Incluímos uma caracterização morfológica e celular mostrando heterogeneidade entre os doadores. Além disso, demonstramos a capacidade deste método de cultura de avaliar os efeitos hormonais no crescimento do organoide OSE durante um período de 2 semanas. Este método pode permitir a descoberta de fatores que contribuem para a regeneração da OSE e facilitar a triagem de medicamentos específicos do paciente para OSE maligno.
Introdução
O ovário é considerado um dos órgãos mais dinâmicos do corpo, passando por ciclos constantes de cicatrização e remodelação de feridas ao longo da vida reprodutiva do indivíduo. Um dos principais atores envolvidos na regeneração do tecido ovariano após cada ciclo ovulatório é o epitélio da superfície ovariana (OSE)1. O OSE é uma camada única derivada do mesotélio contendo células epiteliais planas, cuboidais e colunares que cobrem toda a superfície ovariana2. Antes da ovulação, o tecido estromal ovariano na superfície do folículo ovulatório sofre ruptura proteolítica para permitir a liberação do complexo cumulus-oócito. A área ferida, conhecida como estigma ovulatório, é então reparada, com fechamento completo da superfície ovariana alcançado em menos de 72 horas em camundongos3. A capacidade altamente eficiente do OSE de proliferar e fechar a ferida ovulatória destaca a suposta existência de uma população de células-tronco residentes4. Devido à disponibilidade limitada de ovários humanos de doadores em idade reprodutiva, a maior parte do conhecimento sobre os mecanismos de reparo da OSE vem de modelos animais. No entanto, características específicas da espécie dificultam a tradução da pesquisa ovariana baseada em animaispara humanos 5.
Estudos in vitro utilizaram predominantemente cultura de células bidimensionais (2D) de OSE humano, em que as células cresceram em uma monocamada presa à superfície de uma placa de cultura, devido à sua relação custo-benefício e fácil cultura 6,7,8. No entanto, essa abordagem tem limitações, replicando a complexidade da dinâmica do tecido ovariano9. Nesse sentido, as plataformas de cultura de células 3D com foco especial em organoides ovarianos revolucionaram a pesquisa ovariana10. Os organoides teciduais são representações in vitro miniaturizadas do órgão do qual são derivados, exibindo capacidade de auto-organização 3D e imitando funções-chave e estruturas de suas contrapartes in vivo 11. Essa tecnologia oferece a possibilidade de lançar luz sobre questões fundamentais relacionadas ao desenvolvimento, regeneração e reparo tecidual no ovário humano10. Nos últimos anos, os pesquisadores também aplicaram o conhecimento sobre organoides ovarianos para a geração de organoides de câncer de ovário (CO) específicos do paciente para modelagem de doenças e medicina personalizada 12,13,14.
Com base em diferentes métodos usados para a geração de organoides OSE de camundongos e organoides de trompas de Falópio (FT)15,16, bem como organoides OSE humanos12 e organoides FT17, descrevemos aqui um protocolo para a derivação de organoides OSE humanos de ovários humanos com potenciais aplicações em estudos de regeneração de OSE. Este protocolo isola eficientemente as células OSE primárias de ovários humanos inteiros e inclui uma descrição passo a passo da expansão celular 2D e da geração de organoides 3D hOSE. Os organoides hOSE apresentaram variabilidade (específica do doador) na morfologia e crescimento, destacando sua utilidade para estudos personalizados. Além disso, este protocolo inclui manutenção, passagem e imunofluorescência do organoide hOSE dentro da mesma placa de cultura. Além disso, fornece uma descrição das diferentes morfologias que os organoides hOSE podem adotar e caracteriza alterações no imunofenótipo durante o cultivo. Por fim, mostra utilidade ao investigar a influência de pistas ambientais, como hormônios ovarianos, na formação e crescimento de organoides hOSE com base no número e tamanho de organoides hOSE.
A aplicação da tecnologia organoide hOSE aumentará nossa compreensão do ovário, com ênfase específica nos mecanismos responsáveis por sua notável capacidade regenerativa. À medida que os modelos ovarianos humanos 3D continuam a evoluir, a dependência de modelos animais na pesquisa ovariana diminuirá, levando a terapias inovadoras no campo da medicina regenerativa18.
Protocolo
O estudo foi conduzido de acordo com as diretrizes da Declaração de Helsinque. O desenho do estudo foi submetido ao Comitê de Ética Médica do Centro Médico da Universidade de Leiden (LUMC), e uma carta de não objeção foi obtida (B18.029) antes do estudo. O tecido ovariano humano primário usado foi coletado de pessoas transmasculinas submetidas a cirurgia de afirmação de gênero no hospital VUmc (Amsterdã, Holanda). O consentimento informado assinado foi obtido de todos os doadores. Todos os materiais utilizados neste protocolo estão listados na Tabela de Materiais.
1. Isolamento primário humano de células OSE
- Após a ooforectomia, coloque os ovários em NaCl a 0,9% ou solução salina estéril semelhante e transporte-os para o laboratório em gelo.
- Transfira os ovários individuais para um tubo cônico de 50 mL contendo 2-3 mL de meio de digestão (Tabela 1) ou o suficiente para cobrir o ovário.
CUIDADO: Se o ovário não estiver intacto (parte do órgão foi cortada para análise histológica), é crucial não cobrir essa parte com o meio de digestão. - Coloque o tubo em banho de esferas pré-aquecido (ou banho-maria) a 37 °C por 30 min.
- Transfira cuidadosamente o ovário para uma placa de Petri de 60 mm contendo 10 mL de meio de coleta (Tabela 1).
- Raspe suavemente a superfície ovariana que contém as células hOSE usando um raspador de células. Lave o raspador em meio e repita esta etapa pelo menos três vezes (Figura 1).
CUIDADO: Se o ovário não estiver intacto, evite raspar e submergir a área danificada para minimizar a contaminação com tipos de células indesejadas. - Transferir as células hOSE do meio de recolha para um tubo de 15 ml.
- Gire as células hOSE a 240 x g por 5 min.
- Se o pellet mostrar uma cor vermelha, indicativa de contaminação com glóbulos vermelhos (RBC), ressuspenda o pellet com 1 mL de tampão de lise de hemácias. Incubar por 3 min em temperatura ambiente (RT) com pipetagem ocasional, adicionar 4 mL de PBS com cálcio e magnésio (PBS+/+) e centrifugar a 240 x g por 5 min. Se os eritrócitos persistirem, repita esta etapa.
- Criopreserve o pellet de células hOSE (Seção 2), use-o para cultura 2D (Seção 3) ou organoides 3D (Seção 4) (Figura 1).
2. Criopreservação-descongelamento de células hOSE
- Criopreservação
- Ressuspenda o hOSE cell pellet em 1 mL de meio de congelamento celular.
- Transfira a suspensão celular para criogeniais (2x criogeniais por ovário).
- Coloque os criogenianos em um recipiente de congelamento e coloque-o a -80 ° C durante a noite.
- Transfira os criogenianos congelados para um tanque de nitrogênio líquido para armazenamento de longo prazo.
- Descongelar:
- Remova o criovial do nitrogênio líquido.
- Coloque o criogênico em um banho de esferas pré-aquecido (ou banho-maria) a 37 ° C por 5 min ou até que apenas um pequeno núcleo congelado seja visível dentro do criogenial.
- Pipetar a suspensão de células hOSE em um tubo de 15 mL com 10 mL de meio de coleta (Tabela 1).
- Centrifugue a 240 x g por 5 min.
- Use o pellet de célula hOSE para cultura 2D (Seção 3) ou organoides 3D (Seção 4).
3. Cultura 2D hOSE em monocamada
- Ressuspenda o pellet hOSE em 1 mL de meio OSE_2D (Tabela 1) e transfira-o para um poço de uma placa de 12 poços.
- Adicione 1 mL de OSE_2D meio extra no poço e cultive a 37 ° C em uma incubadora umidificada (5% CO2) por 72 h para garantir que as células hOSE se liguem antes da primeira troca de meio.
- Atualize o meio a cada 2-3 dias até que as células hOSE atinjam 70%-90% de confluência (P0) (Figura 2A).
NOTA: Se as hemácias ainda estiverem presentes na cultura, elas serão removidas durante a primeira troca de meio e apenas as células hOSE permanecerão presas ao poço. - Para células hOSE passantes, siga as etapas descritas abaixo.
- Remova os meios de cultura do poço.
- Lave com 1 mL de PBS estéril.
- Remova o PBS e adicione 0,05% de tripsina / EDTA suficiente para cobrir as células.
- Coloque a placa a 37 °C em uma incubadora umidificada (5% CO2) por 4-7 min até perceber que as células se arredondam e se desprendem do poço.
- Pare a reação enzimática adicionando 1 mL de meio de coleta.
- Colete as células hOSE e centrifugue a 240 x g por 5 min.
- Semeie as células em um novo poço na densidade desejada, atualize o meio a cada 2-3 dias até que as células hOSE atinjam 70% -90% de confluência e repita a etapa 3.4.
NOTA: As células primárias de hOSE podem ser cultivadas em até três passagens. Depois, a maioria das células se tornará senescente (Figura 2A).
- Use as células hOSE expandidas para caracterização adicional usando imunofluorescência (Figura 2B) para testar os efeitos de meios de cultura (Figura 2C) ou para organoides 3D (Seção 4).
4. 3D cultura de organoides hOSE
- Lâmina com câmara multipoço pré-aquecida a 37 °C.
- Conte as células hOSE (recém-isoladas ou descongeladas criopreservadas) com um contador de células automatizado ou manualmente com um hemocitômetro.
- Ressuspenda o número desejado de células hOSE para 1 mL de meio básico OSE gelado (Tabela 1) em um tubo de 1,5 mL.
- Centrifugue a 240 x g por 5 min.
- Ressuspenda o pellet hOSE na quantidade desejada de solução de extrato de membrana basal não diluída (BME) gelada para obter uma concentração celular de 1 x 104 células / 10 μL de BME.
- Pipete a solução hOSE-BME para cima e para baixo para garantir uma distribuição homogênea.
- Faça 10 μL de gotículas de solução de hOSE-BME por poço na lâmina pré-aquecida com câmara de vários poços.
NOTA: Certifique-se de que cada gota esteja no centro do poço para obter uma forma de gota. - Coloque a placa com as gotículas de cabeça para baixo a 37 °C em uma incubadora umidificada (5% CO2) por 15 min para permitir a solidificação do gel.
- Adicionar 100 μL de meio OSE_3D (Tabela 1) e cultivar a 37 °C em incubadora umidificada (5% CO2).
- Atualize o meio a cada 3-4 dias.
NOTA: os organoides hOSE continuam a crescer pelo menos até 28 dias em cultura (Figura 3A, B), mas a passagem a cada 14-28 dias (a taxa de crescimento depende do doador, fresca versus crio hOSE) é recomendada para estimular a proliferação celular e a sobrevivência dos organoides. Três linhas organoides hOSE independentes foram passadas pelo menos 4 vezes sem sinais de senescência. Os organoides hOSE apresentam morfologias diferentes (Figura 3C). - Para a passagem de organoides hOSE:
- Remova o meio e adicione 100 μL de DMEM/F12 avançado gelado a cada poço.
- Raspe o fundo dos poços com uma ponta de pipeta P1000 para soltar as gotículas de gel.
- Transfira cada gota de gel flutuante para um tubo de 1,5 mL.
- Centrifugue os tubos com as gotículas de gel a 240 x g por 5 min.
- Remova o sobrenadante, ressuspenda o pellet em 300 μL de tampão de dissociação celular e coloque os tubos em um banho de esferas pré-aquecido (ou banho-maria) a 37 ° C por 5-10 min.
NOTA: Se alguns organoides permanecerem intactos, pipete para cima e para baixo algumas vezes com a ponta da pipeta gelada revestida com soro bovino fetal para interrompê-los mecanicamente. O revestimento das pontas da pipeta com soro fetal bovino evita que os organoides grudem na ponta. - Adicione 300 μL de meio organoide básico hOSE e centrifugue a 240 x g por 5 min.
- Ressuspenda o pellet na quantidade desejada de solução BME não diluída, semeie-os novamente em uma proporção adequada (distribua o conteúdo de 1 gota em 1-4 gotículas) e cultive conforme mencionado acima.
NOTA: Os organoides não são dissociados em células únicas e, portanto, as células não podem ser contadas com precisão para passagem posterior.
5. Imunofluorescência de montagem total de organoides 3D hOSE
NOTA: A imunofluorescência de montagem total pode ser realizada no mesmo poço de cultura (em gotículas) se forem utilizadas lâminas com câmaras de vários poços adequadas para técnicas de microscopia.
- Fixe os organoides hOSE nas gotículas em paraformaldeído (PFA) a 4% por 20 min em RT.
- Lave duas vezes com PBS por 5 min em RT em uma plataforma giratória / agitada.
- Permeabilize os organoides hOSE nas gotículas usando 100 μL de tampão de permeabilização (Tabela 1) por 15 min em RT.
- Lavar três vezes com 100 μL de tampão de bloqueio (Quadro 1) durante 15 min em RT e bloquear durante a noite (o/n) a 4 °C numa plataforma rotativa/agitada.
- Incubar com 100 μL de mistura de anticorpos primários diluídos em tampão de bloqueio a 4 °C o/n em uma plataforma rotativa/agitada.
NOTA: Consulte a Tabela de Materiais para obter uma lista de anticorpos primários usados, o tipo de célula marcado e o modelo animal usado para validar a expressão 12,19,20,21,22,23,24,25. - Leve a placa à RT e lave-a três vezes com 100 μL de tampão de bloqueio por 15 min em RT em uma plataforma giratória / agitada.
- Incubar com 100 μL de mistura de anticorpos secundários diluídos em tampão de bloqueio por 2 h em RT em uma plataforma rotativa / agitada, mas protegida da luz.
NOTA: Consulte a Tabela de Materiais para obter uma lista de anticorpos secundários usados. Para proteger da luz, coloque o prato dentro de uma caixa escura ou cubra-o com papel alumínio. - Lavar três vezes em 100 μL de PBS durante 15 min em RT sobre uma plataforma rotativa/agitada.
- Conservar a placa a 4 °C coberta com folha de alumínio até à obtenção de imagens (figura 4).
6. Quantificação do tamanho do organoide hOSE
- Tire fotos de campo claro 10x (imagem TIFF) em um microscópio.
- Baixe e instale Fiji (https://imagej.net/software/fiji/)26.
- Meça a área da imagem dos organoides hOSE com o software ImageJ Fiji:
- Carregue arquivos TIFF de imagem em Fiji.
- Crie um limite para o software reconhecer os organoides hOSE (área mais escura) na imagem de campo claro carregada clicando em Imagem > Ajustar > limite. Ajuste os valores abaixo e acima até que a maior parte do fundo seja removida e os organoides individuais sejam mantidos.
- Abra a ferramenta ROI clicando em Analisar > ferramenta > ROI.
- Selecione a ferramenta Varinha e clique na região com um organoide hOSE até ver uma linha amarela ao redor de todo o perímetro do organoide. No painel ROI, clique em Adicionar e medir para obter o valor da área desse organoide OSE.
- Repita a etapa 6.3.4. para cada organoide hOSE a ser medido.
Resultados Representativos
Cultura hOSE 2D
As células hOSE recém-isoladas foram plaqueadas em uma placa de 12 poços e cultivadas por 3 semanas. Durante esse período, as células foram passadas três vezes (Figura 2A). As células primárias de hOSE em cultura exibiram uma morfologia semelhante a paralelepípedos até a passagem 3 (P3), mas depois disso começaram a mostrar sinais de senescência, de acordo com resultados anteriores relatando que o período limitado de hOSE pode ser passado27. Além disso, foi demonstrado que a OSE murina sofre transição epitelial-mesenquimal (EMT) in vitro, exibindo características semelhantes a fibroblastos, como rearranjo do citoesqueleto de actina e deposição de colágeno I19. Em concordância, ACTA2 + CD44 + hOSE mostrou regulação positiva pronunciada de COL1A1 entre P2 e P3 ( Figura 2B ), sugerindo que as células hOSE sofrem EMT durante a cultura.
A sinalização TGF-β é um importante regulador da EMT28 capaz de induzir EMT em vários tipos de células epiteliais29. Embora o TGF-β não tenha sido adicionado ao meio OSE_2D, o FBS adicionado pode conter níveis detectáveis dessa citocina30,31. Por esse motivo, testamos se a adição do receptor tipo I inibidor de TGF-β SB-431542 poderia prevenir a EMT, permitindo uma cultura 2D prolongada. Surpreendentemente, a suplementação do meio OSE_2D com 10 μM de SB-43154232dificultou a proliferação celular (Figura 2C). Concluímos que a sinalização de TGF-β é essencial para a proliferação de OSE, e outros experimentos de cultura 2D foram realizados sem o inibidor.
Cultura organoide 3D hOSE
Com base nas condições de cultura publicadas para cultivar organoides OSE humanos12, derivamos organoides hOSE embebidos em gotículas de BME e cultivados em meio OSE_3D (contendo uma concentração padrão de 100 nM de estradiol) por até 28 dias. Em 7 dias, muitos organoides hOSE derivados de células OSE recém-isoladas estavam císticos com um diâmetro médio de 130 mm ( Figura 3A, B ). Esses resultados foram semelhantes aos relatados por Kopper e colegas sobre a derivação de organoides hOSE de tecido ovariano humano picado e digerido enzimaticamente12. Curiosamente, os organoides hOSE derivados de células OSE recém-isoladas cresceram maiores (diâmetro médio de 160 mm) do que os organoides hOSE de células OSE expandidas 2D (diâmetro médio de 100 mm) após 14 dias em cultura (Figura 3B), provavelmente devido à propensão das células OSE expandidas 2D para diminuir a proliferação. Além disso, enquanto muitos organoides hOSE 3D consistiam em uma monocamada de células epiteliais planas (painel superior esquerdo da Figura 3C ), alguns exibiam uma monocamada cuboidal de células (painel superior direito da Figura 3C ), outros eram multicamadas (painel inferior direito da Figura 3C ) ou formavam um aglomerado de células não lumenizadas (painel inferior esquerdo da Figura 3C ).
Para testar se os organoides hOSE também poderiam ser derivados usando OSE_2D meio, células hOSE recém-isoladas foram incorporadas em gotículas de BME e cultivadas em meio OSE_2D por 12 dias. Após 6 dias, células fusiformes eram visíveis, sugerindo que as células hOSE estavam sofrendo EMT nas gotículas. É importante ressaltar que nenhum organoide hOSE foi formado usando OSE_2D meio (Figura 3D).
Características celulares dos organoides hOSE
No ovário humano adulto, a queratina 8 (KRT8) marca especificamente a população OSE (Figura 4A) e, consequentemente, os organoides hOSE retiveram a expressão de KRT8, validando sua identidade celular (Figura 4B). Em células OSE de camundongo, a localização nuclear da proteína associada a Yes1 (YAP1) foi especificamente associada a células-tronco / progenitoras OSE capazes de expandir e curar a área ferida após a ovulação24,33. YAP mostrou localização nuclear na maioria das células em organoides hOSE independente de seu tamanho (Figura 4B). Outros marcadores relatados como expressos em células OSE de camundongos, como CD4420 e LGR522, também foram investigados. Curiosamente, tanto CD44 quanto LGR5 foram expressos em pequenos organoides hOSE (<100 μm de diâmetro), enquanto em organoides maiores, CD44 e LGR5 pareciam regulados negativamente (Figura 4B).
Em seguida, investigamos se os organoides hOSE exibiam a polaridade apical-basal tipicamente observada em organoides embutidos em BME (apical-in) 34 . A proteína basolateral integrina beta 1 (ITGB1) e a proteína apical podocalixina (PODXL) foram usadas para mostrar a polaridade celular nos organoides hOSE, confirmando uma polaridade apical-in clara independente do tamanho do organoide hOSE (Figura 4B).
Sabe-se que a OSE humana expressa o marcador mesenquimal N-caderina (CDH2), enquanto a expressão do marcador epitelial E-caderina (CDH1) é limitada às células OSE colunares (Figura 4A)2. Curiosamente, os organoides hOSE derivados neste trabalho expressaram marcadores mesenquimais CDH2 e vimentina (VIM), e grandes organoides císticos hOSE com epitélio cuboidal/colunar foram CDH1+ e CDH2+VIM+ (Figura 4C). Ainda não está claro se os organoides CDH1+ hOSE foram derivados de células primárias CDH1+ OSE ou de células CDH1-OSE que sofreram diferenciação epitelial ou transformação (neoplásica) in vitro25,35.
Apresentando o uso de organoides hOSE: efeito de pistas ovulatórias em organoides hOSE
Os hormônios folículo-estimulante e gonadotrofina coriônica humana podem ser usados para induzir o crescimento folicular e a ovulação, ao passo que, após a ovulação, há um aumento acentuado na concentração de hormônios produzidos no ovário, como progesterona e estradiol36. Para mostrar a usabilidade dos organoides hOSE como uma plataforma de triagem, examinamos o efeito desses hormônios nos organoides hOSE, usando o número e o tamanho dos organoides como saída de quantificação (usando Fiji). Para isso, derivamos organoides hOSE em meios OSE_3D sem estradiol (sem hormônio) e em meios OSE_3D contendo FSH, hCG, estradiol ou progesterona em diferentes concentrações (Figura 5A).
O número de organoides hOSE derivados de células hOSE criopreservadas-descongeladas (não expandidas) de 3 doadores diferentes (n = 3) foi quantificado por gotícula após 7 dias de cultura ( Figura 5A , B ). O meio de cultura foi trocado a cada 3 dias. Não foram observadas diferenças significativas no número total de organoides hOSE por gotícula que se formou em hormônios contendo meio em comparação com meio sem hormônios (Figura 5A, B). Para quantificar o efeito dos hormônios no tamanho do organoide, após 14 dias em cultura, cada gota (de cada condição) foi fotografada e a área dos 4 maiores organoides hOSE foi medida usando Fiji. Curiosamente, a geração de organoides hOSE de dois doadores diferentes (n = 2) na presença de progesterona (1000 nM) ou estradiol (200 nM) resultou em pelo menos um organoide muito grande (cerca de 700 μm de diâmetro) por gotícula (Figura 5C, D).
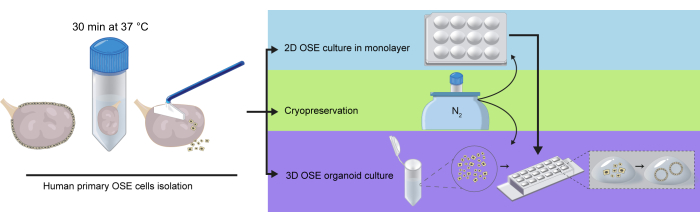
Figura 1: Representação esquemática do isolamento de células hOSE de ovários inteiros. Os ovários foram incubados em solução de digestão por 30 min a 37 ° C. As células hOSE foram destacadas da superfície ovariana por raspagem suave e posteriormente criopreservadas, diretamente semeadas em cultura 2D OSE em monocamada ou incorporadas em extrato de membrana basal (BME) para cultura organoide 3D hOSE. As células hOSE descongeladas criopreservadas podem ser usadas para cultura 2D ou formação de organoides 3D, e as células hOSE expandidas 2D podem ser usadas para gerar organoides hOSE 3D. Clique aqui para ver uma versão maior desta figura.

Figura 2: Cultura primária 2D de células hOSE. (A) Imagens de campo claro de células hOSE nas passagens 0 (P0), 2 (P2) e 3 (P3) representando a morfologia típica de paralelepípedos epiteliais. As barras de escala são de 750 μm nos painéis superiores e 125 μm nos painéis inferiores. (B) Imunofluorescência para ACTA2, CD44, COL1A1 em células hOSE 2D em P2 e P3. As barras de escala são de 50 μm. (C) Imagens de campo claro de células hOSE cultivadas com 10 μM de SB-431542 em P0, P2 e P3. As células apresentaram sinais de senescência de P2 e não atingiram alta confluência durante o cultivo. As barras de escala são de 750 μm nos painéis superiores e 125 μm nos painéis inferiores. Clique aqui para ver uma versão maior desta figura.
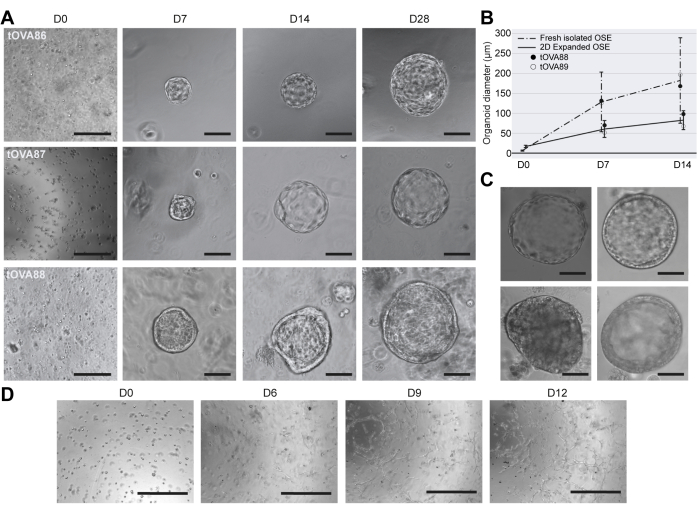
Figura 3: Caracterização morfológica de organoides hOSE. (A) Imagens de campo claro de três derivações independentes de organoides hOSE de três doadores diferentes (tOVA86, tOVA87, tOVA88). As imagens foram obtidas após o embeding celular (D0), dia 7 (D7), dia 14 (D14) e dia 28 (D28) de cultura. As barras de escala são 750 μm em D0 e 50 μm para o resto. (B) Diâmetro dos organoides hOSE derivados de células hOSE recém-isoladas (linha tracejada) e células hOSE expandidas 2D (linha sólida). Representado é o tamanho médio ± desvio padrão medido em D0, D7 e D14. Os resultados de dois doadores diferentes (tOVA88 e tOVA89) são mostrados. (C) Imagens de campo claro de organoides hOSE mostrando diferentes morfologias: camada plana única (canto superior esquerdo), camada colunar única (canto superior direito), multicamadas (canto inferior direito) e agregado de células não lumenizadas (canto inferior esquerdo). As barras de escala são de 100 μm. (D) Imagens de campo claro de células hOSE embutidas em BME e cultivadas por 12 dias com OSE_2D meio. As imagens foram tiradas após a incorporação de células (D0), dia 6 (D6), dia 9 (D9) e dia 12 (D12). Células semelhantes a fibroblastos ultrapassaram a cultura e nenhuma estrutura semelhante a organoide foi formada. As barras de escala são de 750 μm. Clique aqui para ver uma versão maior desta figura.
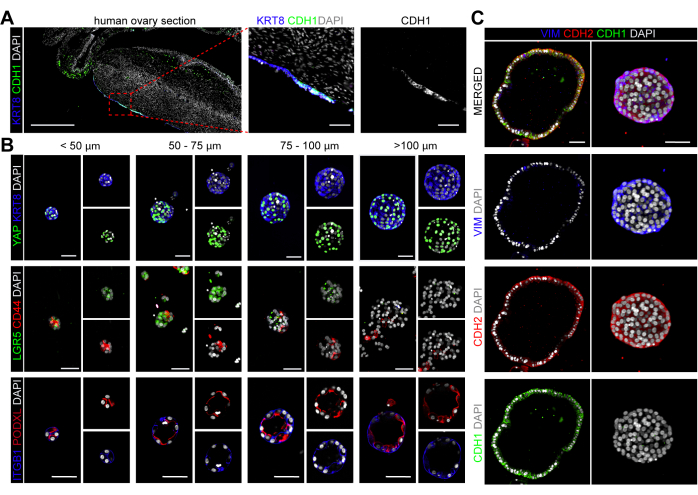
Figura 4: Caracterização celular de organoides hOSE. (A) Imunofluorescência para KRT8 e CDH1 em secção ovariana humana. A barra de escala no painel esquerdo é de 500 μm e os painéis do meio e direito são de 50 μm. (B) Imunofluorescência para KRT8 e YAP, LGR5 e CD44 e ITGB1 e PODXL em organoides hOSE de diferentes tamanhos (<50 μm, 50-75 μm, 75-100 μm >100 μm). As barras de escala são de 50 μm. (C) Imunofluorescência para VIM, CDH1, CDH2 em organoides hOSE. As barras de escala são de 50 μm. Clique aqui para ver uma versão maior desta figura.
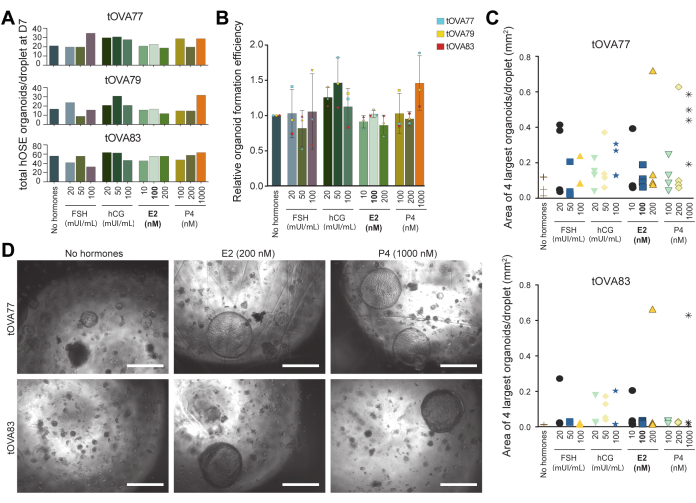
Figura 5: Efeito das pistas ovulatórias na formação de organoides hOSE. (A) Número total de organoides hOSE por gotícula formada no dia 7 em diferentes meios de cultura. Os organoides hOSE foram derivados de três doadores diferentes (tOVA77, tOVA79, tOVA83). Em negrito está o meio OSE_3D usado para derivação de organoides. (B) Formação relativa de organoides em comparação com o meio sem hormônios. Os valores agrupados dos organoides hOSE foram derivados de três doadores diferentes (tOVA77, tOVA79, tOVA83). (C) Gráfico que descreve a área da imagem dos 4 maiores organoides hOSE no dia 14 em cada uma das condições experimentais testadas em dois doadores diferentes (tOVA77, tOVA83). (D) Imagens de campo claro mostrando organoides hOSE na cultura do dia 14 com meio sem hormônios, 200 nM E2 e 1000 nM P4 de dois doadores diferentes (tOVA77, tOVA83). As barras de escala são de 750 μm. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Composição das soluções de trabalho utilizadas no estudo. Clique aqui para baixar esta tabela.
Discussão
A tecnologia organoide 3D está emergindo como uma ferramenta indispensável para a pesquisa médica. Por um lado, esta plataforma in vitro oferece a possibilidade de estudar questões mecanicistas fundamentais sobre regeneração de tecidos, cicatrização e desenvolvimento de feridas18. Por outro lado, os organoides 3D derivados de amostras de pacientes permitem estudos de medicina personalizados, incluindo diagnósticos, testes de drogas e terapia celular 12,13,14,37,38. No campo da pesquisa ovariana, o hOSE ganhou interesse substancial desde sua implicação como origem dos carcinomas epiteliais de ovário39. Embora se pense que a maioria dos carcinomas de ovário seroso de alto grau (HGSOC), um dos cânceres epiteliais de ovário mais comuns, surge das trompas de falópio40, pesquisas atuais em organoides ovarianos 3D de camundongos propuseram uma potencial origem dupla de HGSOC a partir de OSE e trompa de Falópio 15,16.
Aqui, descrevemos um protocolo para a derivação de organoides hOSE 3D e delineamos sua aplicação para trazer novos conhecimentos mecanicistas na regeneração do tecido ovariano. Este protocolo inclui um método passo a passo para isolar células hOSE primárias de ovários humanos e gerar organoides 3D hOSE. Para garantir a derivação eficiente do organoide hOSE, é crucial minimizar a manipulação ovariana. Devido à sua localização na superfície ovariana e organização em monocamada, a hOSE é propensa a danos e perdas durante a ooforectomia e manipulação de órgãos. Por esse motivo, favorecemos um método enzimático e de raspagem aplicado a todo o ovário para isolar hOSE 2,8. No presente protocolo, um tratamento enzimático leve foi aplicado para interromper as conexões intercelulares hOSE, seguido de raspagem suave da superfície ovariana.
Comparando a cultura 2D com a cultura 3D hOSE, é importante notar que, apesar da alta taxa inicial de proliferação de células hOSE em cultura 2D, suas características celulares foram alteradas devido à EMT, sugerindo que as condições de cultura 2D aplicadas não são adequadas para manter uma morfologia epitelial. Por outro lado, os organoides 3D hOSE podem ser passados pelo menos 4 vezes sem sinais de senescência. O meio de cultura organoide OSE_3D usado foi baseado no usado por Kopper e colegas para a derivação de organoides OC e hOSE saudáveis12 e por Kessler e colegas para a derivação de organoides FT humanos17. A principal diferença foi a substituição dos meios condicionados Wnt3a e R-Espondina 1 humanos por proteínas recombinantes disponíveis comercialmente para facilitar a reprodutibilidade.
As técnicas de imunofluorescência geralmente envolvem a remoção da amostra de tecido da placa de cultura e o processamento para parafina ou crioseccionamento. Ao trabalhar com estruturas muito pequenas, o risco de perdê-las durante o processamento da amostra é alto. Neste protocolo, a derivação dos organoides hOSE ocorre em placas de cultura de células que permitem a imagem de microscopia direta sem a necessidade de remover os organoides hOSE da matriz BME. Além disso, o método de imunofluorescência de montagem total usado aqui, descrito por Rezanejad e colegas para organoides ductais pancreáticos41, permitiu a observação in situ da localização de proteínas dentro de organoides morfologicamente intactos. Demonstramos que, ao realizar este protocolo de imunofluorescência em organoides hOSE derivados em lâminas com câmara múltipla, há penetração de anticorpos altamente eficiente com um sinal de fundo muito baixo.
Embora a maioria dos organoides hOSE derivados usando este método não tenha expressão de CDH1, alguns organoides CDH1+ hOSE se formaram, atingindo tamanhos maiores em comparação com os organoides CDH1-hOSE. A expressão de CDH1 tem sido associada a fenótipos neoplásicos de hOSE 2,35. Os ovários utilizados para o isolamento da hOSE foram doados por doadores transmasculinos saudáveis em idade reprodutiva (27,1 ± 5 anos). Essas doadoras estavam em tratamento com testosterona por um período de 38 ± 15 meses antes da ooforectomia. Não podemos descartar a possibilidade de que as células CDH1+ hOSE na superfície ovariana possam ser atribuídas ao tratamento com testosterona. Embora o tratamento com andrógenos tenha sido associado a alterações ovarianas, como anovulação42, hiperplasia da área cortical43 e aumento da rigidez cortical44, a patologia ovariana geral permanece benigna durante o uso de testosterona45.
Em resumo, este protocolo destaca o potencial de geração de organoides hOSE 3D para decodificar questões mecanicistas sobre a regeneração do tecido ovariano. É importante ressaltar que esse método também pode ser aplicado para a detecção de células malignas presentes em biópsias ovarianas de pacientes com risco de desenvolvimento de câncer. Coletivamente, este método suporta aplicações potenciais desta plataforma inovadora in vitro para estudos fundamentais da função ovariana e aplicações clínicas para tratamentos médicos individualizados.
Divulgações
Nenhum.
Agradecimentos
Gostaríamos de agradecer a todos os pacientes que doaram tecidos para este estudo, aos membros do grupo Chuva de Sousa Lopes pelas discussões úteis e a I. De Poorter pela elaboração dos desenhos usados na Figura 1. Esta pesquisa foi financiada pelo Conselho Europeu de Pesquisa, número de concessão ERC-CoG-2016- 725722 (OVOGROWTH) para J.S.D.V. e S.M.C.d.S.L.; e a Fundação Novo Nordisk (reNEW), número de subvenção NNF21CC0073729 para J.S.D.V. e S.M.C.d.S.L.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.05% Trypsin/EDTA | Invitrogen | 25200-056 | |
| 12-well Culture Plate | Corning | 3336 | Sterile |
| 15 mL tubes | Greiner | 188271 | Sterile |
| 28cm Cell Scraper | Greiner Bio-One | 541070 | |
| 50 mL tubes | Greiner | 227261 | Sterile |
| 60 mm Petri dish | Greiner Bio-One | 628160 | |
| A83-01 | Stem Cell Technologies | 72024 | |
| Advanced DMEM/F12 | Gibco | 12634-010 | |
| B27 supplement (50x) | ThermoFisher Scientific | 17504-044 | |
| Bead bath | M714 | ||
| Bovine serum albumin (BSA) | Sigma Aldrich | 10735086001 | |
| Cell Dissociation Buffer | ThermoFisher Scientific | 13151014 | |
| Cryo-container "Mr. Frosty" | BD Falcom | 479-3200 | |
| DMEM Medium | ThermoFisher Scientific | 41966-029 | |
| Donkey anti-Goat IgG Alexa Fluor 647 | Invitrogen | A-21447 | |
| Donkey anti-Mouse IgG Alexa Fluor 488 | Invitrogen | A-21202 | |
| Donkey anti-Mouse IgG Alexa Fluor 647 | Invitrogen | A-31571 | |
| Donkey anti-Rabbit IgG Alexa Fluor 488 | Invitrogen | A-21206 | |
| Donkey anti-Rabbit IgG Alexa Fluor 594 | Invitrogen | A-21207 | |
| Donkey anti-Sheep IgG Alexa Flour 647 | Invitrogen | A-21448 | |
| Fetal Bovine Serum (FBS) | ThermoFisher Scientific | A4736401 | |
| Follicle Stimulating Hormone (FSH) | Sigma Aldrich | F4021 | |
| Forskolin | Peprotech | 6652995 | |
| Glutamax (100x) | Gibco | 35050-038 | |
| Goat anti-CDH2 (N/R-cadherin) | Santa Cruz | SC-1502 | Mesenchymal Cells; Wong et al 1999 (human)25 |
| Goat anti-PODXL (podocalyxin of GP135) | R&D Systems | AF1658 | Apical Polarity; Bryant et al 2014 (canine)21 |
| Goat anti-Rat IgG Alexa Fluor 555 | Invitrogen | A-21434 | |
| hEGF | R&D Systems | 263-EG | |
| HEPES | Gibco | 15630-056 | |
| Hydrocortisone | Sigma Aldrich | H0888 | |
| Insulin-Transferrin-Selenium-Ethanolamine (ITS-X; 100x) | ThermoFisher Scientific | 51500-056 | |
| Liberase DH Research Grade | Sigma Aldrich | A4736401 | |
| Luna-II cell counter | Logos Biosystems | L40001 | |
| Matrigel | Sigma Aldrich | 354277 | |
| McCoy’s 5A Medium | ThermoFisher Scientific | 26600-023 | |
| Mouse anti-ITGB1 (integrin beta 1) | Santa Cruz | SC-53711 | Basolateral Polarity; Bryant et al 2014 (canine)21 |
| Mouse anti-KRT8 (cytokeratin 8) | Santa Cruz | SC-101459 | OSE Cells; Kopper et al 2019 (human)12 |
| Mouse anti-VIM (vimentin) | Abcam | AB0809 | Mesenchymal Cells; Abedini et al 2020 (mouse)19 |
| Mycozap Plus-CL | Lonza | V2A-2011 | |
| N-Acetyl-L-cysteine | Sigma Aldrich | A9165 | |
| Nicotinamide | Sigma Aldrich | N0636-100G | |
| OVITRELLE-Choriogonadotropin alfa (hCG) | Merk | G03GA08 | |
| Progesterone (P4) | Sigma Aldrich | P8783 | |
| Rabbit anti-ACTA2 (alpha smooth muscle actin) | Abcam | AB5694 | Mesenchymal Cells; Abedini et al 2020 (mouse)19 |
| Rabbit anti-CDH1 (E-cadherin) | Cell Signaling | CST 3195S | Epithelial Cells; Wong et al 1999 (human)25 |
| Rabbit anti-LGR5 | Abcam | AB75850 | OSE Progenitor Cells; Flesken-Nikitin et al 2013 (mouse)22 |
| Rabbit anti-YAP | Cell Signaling | 14074S | Proliferative OSE; Wang et al 2022 (mouse)24 |
| Rat anti-CD44 PE-conjugated | eBioscience | 12-0441-81 | OSE Progenitor Cells; Bowen et al 2009 (human)20 |
| Recombinant Human Heregulinβ-1 | Peprotech | 100-03 | |
| Recombinant Human Noggin | Peprotech | 120-10C | |
| Recombinant Human Wnt3a | R&D Systems | 5036-WN-010 | |
| Recombinant Rspondin-1 | Peprotech | 120-38 | |
| Red blood cells lysis buffer | eBiosciences | 00-4333-57 | |
| Revitacell Supplement (100x) | ThermoFisher Scientific | A26445-01 | |
| RNAse free DNAse | Qiagen | 79254 | |
| SB-431542 | Tocris Bioscience | 1624/10 | |
| Sheep anti-COL1A1 (pro-collagen 1 alpha 1) | R&D Systems | AF6220 | Mesenchymal Cells; Hosper et al 2013 (human)23 |
| Y-27632 | StemCell Technologies | 72304 | |
| β-Estradiol (E2) | Sigma-Aldrich | E8875 | |
| μ-Slide 18-well culture plate | Ibidi | 8181 | Sterile |
Referências
- Ng, A., Barker, N. Ovary and fimbrial stem cells: biology, niche and cancer origins. Nat Rev Mol Cell Biol. 16 (10), 625-638 (2015).
- Auersperg, N., Wong, A. S., Choi, K. C., Kang, S. K., Leung, P. C. Ovarian surface epithelium: biology, endocrinology, and pathology. Endocr Rev. 22 (2), 255-288 (2001).
- Tan, O. L., Fleming, J. S. Proliferating cell nuclear antigen immunoreactivity in the ovarian surface epithelium of mice of varying ages and total lifetime ovulation number following ovulation. Biol Reprod. 71 (5), 1501-1507 (2004).
- Carter, L. E., et al. Transcriptional heterogeneity of stemness phenotypes in the ovarian epithelium. Commun Biol. 4 (1), 527 (2021).
- Chumduri, C., Turco, M. Y. Organoids of the female reproductive tract. J Mol Med (Berl). 99 (4), 531-553 (2021).
- Edmondson, R. J., Monaghan, J. M., Davies, B. R. The human ovarian surface epithelium is an androgen responsive tissue. Br J Cancer. 86 (6), 879-885 (2002).
- Karlan, B. Y., Jones, J., Greenwald, M., Lagasse, L. D. Steroid hormone effects on the proliferation of human ovarian surface epithelium in vitro. Am J Obstet Gynecol. 173 (1), 97-104 (1995).
- Nakamura, M., Katabuchi, H., Ohba, T., Fukumatsu, Y., Okamura, H. Isolation, growth and characteristics of human ovarian surface epithelium. Virchows Arch. 424 (1), 59-67 (1994).
- Horvath, P., et al. Screening out irrelevant cell-based models of disease. Nat Rev Drug Discov. 15 (11), 751-769 (2016).
- Del Valle, J. S., Chuva de Sousa Lopes, S. M. Bioengineered 3D ovarian models as paramount technology for female health management and reproduction. Bioengineering (Basel). 10 (7), 832 (2023).
- Clevers, H. Modeling development and disease with organoids. Cell. 165 (7), 1586-1597 (2016).
- Kopper, O., et al. An organoid platform for ovarian cancer captures intra- and interpatient heterogeneity. Nat Med. 25 (5), 838-849 (2019).
- Maenhoudt, N., et al. Developing organoids from ovarian cancer as experimental and preclinical models. Stem Cell Reports. 14 (4), 717-729 (2020).
- Senkowski, W., et al. A platform for efficient establishment and drug-response profiling of high-grade serous ovarian cancer organoids. Dev Cell. 58 (12), 1106-1121.e7 (2023).
- Lohmussaar, K., et al. Assessing the origin of high-grade serous ovarian cancer using CRISPR-modification of mouse organoids. Nat Commun. 11 (1), 2660 (2020).
- Zhang, S., et al. Both fallopian tube and ovarian surface epithelium are cells-of-origin for high-grade serous ovarian carcinoma. Nat Commun. 10 (1), 5367 (2019).
- Kessler, M., et al. The Notch and Wnt pathways regulate stemness and differentiation in human fallopian tube organoids. Nat Commun. 6, 8989 (2015).
- Kim, J., Koo, B. K., Knoblich, J. A. Human organoids: model systems for human biology and medicine. Nat Rev Mol Cell Biol. 21 (10), 571-584 (2020).
- Abedini, A., Sayed, C., Carter, L. E., Boerboom, D., Vanderhyden, B. C. Non-canonical WNT5a regulates Epithelial-to-Mesenchymal Transition in the mouse ovarian surface epithelium. Sci Rep. 10 (1), 9695 (2020).
- Bowen, N. J., et al. Gene expression profiling supports the hypothesis that human ovarian surface epithelia are multipotent and capable of serving as ovarian cancer-initiating cells. BMC Med Genomics. 2, 71 (2009).
- Bryant, D. M., et al. A molecular switch for the orientation of epithelial cell polarization. Dev Cell. 31 (2), 171-187 (2014).
- Flesken-Nikitin, A., et al. Ovarian surface epithelium at the junction area contains a cancer-prone stem cell niche. Nature. 495 (7440), 241-245 (2013).
- Hosper, N. A., et al. Epithelial-to-mesenchymal transition in fibrosis: collagen type I expression is highly upregulated after EMT, but does not contribute to collagen deposition. Exp Cell Res. 319 (19), 3000-3009 (2013).
- Wang, J., et al. Selective YAP activation in Procr cells is essential for ovarian stem/progenitor expansion and epithelium repair. Elife. 11, e75449 (2022).
- Wong, A. S., et al. Constitutive and conditional cadherin expression in cultured human ovarian surface epithelium: influence of family history of ovarian cancer. Int J Cancer. 81 (2), 180-188 (1999).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nat Methods. 9 (7), 676-682 (2012).
- Shepherd, T. G., Theriault, B. L., Campbell, E. J., Nachtigal, M. W. Primary culture of ovarian surface epithelial cells and ascites-derived ovarian cancer cells from patients. Nat Protoc. 1 (6), 2643-2649 (2006).
- Xu, J., Lamouille, S., Derynck, R. TGF-beta-induced epithelial to mesenchymal transition. Cell Res. 19 (2), 156-172 (2009).
- Miettinen, P. J., Ebner, R., Lopez, A. R., Derynck, R. TGF-beta induced transdifferentiation of mammary epithelial cells to mesenchymal cells: involvement of type I receptors. J Cell Biol. 127 (6 Pt 2), 2021-2036 (1994).
- Danielpour, D., et al. Sandwich enzyme-linked immunosorbent assays (SELISAs) quantitate and distinguish two forms of transforming growth factor-beta (TGF-beta 1 and TGF-beta 2) in complex biological fluids. Growth Factors. 2 (1), 61-71 (1989).
- Oida, T., Weiner, H. L. Depletion of TGF-beta from fetal bovine serum. J Immunol Methods. 362 (1-2), 195-198 (2010).
- Halder, S. K., Beauchamp, R. D., Datta, P. K. A specific inhibitor of TGF-beta receptor kinase, SB-431542, as a potent antitumor agent for human cancers. Neoplasia. 7 (5), 509-521 (2005).
- Wang, J., Wang, D., Chu, K., Li, W., Zeng, Y. A. Procr-expressing progenitor cells are responsible for murine ovulatory rupture repair of ovarian surface epithelium. Nat Commun. 10 (1), 4966 (2019).
- Kawata, M., et al. Polarity switching of ovarian cancer cell clusters via SRC family kinase is involved in the peritoneal dissemination. Cancer Sci. 113 (10), 3437-3448 (2022).
- Davies, B. R., Worsley, S. D., Ponder, B. A. Expression of E-cadherin, alpha-catenin and beta-catenin in normal ovarian surface epithelium and epithelial ovarian cancers. Histopathology. 32 (1), 69-80 (1998).
- Skory, R. M., Xu, Y., Shea, L. D., Woodruff, T. K. Engineering the ovarian cycle using in vitro follicle culture. Hum Reprod. 30 (6), 1386-1395 (2015).
- Boretto, M., et al. Patient-derived organoids from endometrial disease capture clinical heterogeneity and are amenable to drug screening. Nat Cell Biol. 21 (8), 1041-1051 (2019).
- Phan, N., et al. A simple high-throughput approach identifies actionable drug sensitivities in patient-derived tumor organoids. Commun Biol. 2, 78 (2019).
- Ducie, J., et al. Molecular analysis of high-grade serous ovarian carcinoma with and without associated serous tubal intra-epithelial carcinoma. Nat Commun. 8 (1), 990 (2017).
- Lee, Y., et al. A candidate precursor to serous carcinoma that originates in the distal fallopian tube. J Pathol. 211 (1), 26-35 (2007).
- Rezanejad, H., Lock, J. H., Sullivan, B. A., Bonner-Weir, S. Generation of pancreatic ductal organoids and whole-mount immunostaining of intact organoids. Curr Protoc Cell Biol. 83 (1), e82 (2019).
- Asseler, J. D., et al. One-third of amenorrheic transmasculine people on testosterone ovulate. Cell Rep Med. 5 (3), 101440 (2024).
- Ikeda, K., et al. Excessive androgen exposure in female-to-male transsexual persons of reproductive age induces hyperplasia of the ovarian cortex and stroma but not polycystic ovary morphology. Hum Reprod. 28 (2), 453-461 (2013).
- De Roo, C., et al. Texture profile analysis reveals a stiffer ovarian cortex after testosterone therapy: a pilot study. J Assist Reprod Genet. 36 (9), 1837-1843 (2019).
- Grimstad, F. W., et al. Ovarian histopathology in transmasculine persons on testosterone: A multicenter case series. J Sex Med. 17 (9), 1807-1818 (2020).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados