Twee Technieken om Hypoparathyroid Mice Maken: parathyroïdectomie Met behulp van GFP Klieren en difterie-toxine-Mediated bijschildklier Ablation
In This Article
Summary
Mice with acquired hypoparathyroidism would be useful for studying novel drug therapies for hypoparathyroidism. Two procedures to create such mice are demonstrated. The GFP-PTX mouse is generated by surgical parathyroidectomy guided by green fluorescing parathyroid glands. A second, non-surgical approach is based on parathyroid-specific expression of the diphtheria toxin receptor.
Abstract
Hypoparathyroidism (HP) is a disorder characterized by low levels of PTH which lead to hypocalcemia, hyperphosphatemia, and low bone turnover. The most common cause of the disease is accidental removal of the parathyroid glands during thyroid surgery. Novel therapies for HP are needed, but testing them requires reliable animal models of acquired HP.
Here, we demonstrate the generation of two mouse models of acquired HP. In the GFP-PTX model, mice with green fluorescent protein (GFP) expressed specifically in the parathyroids (PTHcre-mTmG) were created by crossing PTHcre+ mice with Rosa-mTmGfl/fl mice. Green fluorescing parathyroid glands are easily identified under a fluorescence dissecting microscope and parathyroidectomy is performed in less than 20 min. After fluorescence-guided surgery, mice are profoundly hypocalcemic. Contrary to the traditional thyro-parathyroidectomy, this precise surgical approach leaves thyroid glands and thyroid function intact. The second model, which does not require surgery, is based on a diphtheria-toxin approach. PTHcre-iDTR mice, which express the diphtheria toxin (DT) receptor specifically in the parathyroids, were generated by crossing the inducible DTR mouse with the PTHcre mouse. Parathyroid cells are thus rendered sensitive to diphtheria toxin (DT) and can be selectively destroyed by systemically injecting mice with DT. The resulting hypocalcemic phenotype is stable.
Introduction
Sinds de eerste systematische beschrijving van de bijschildklieren in menselijke en in verschillende andere soorten van Sandström in 1880 1, kan begrijpen wat deze kleine endocrien orgaan voor menselijke fysiologie met voortdurend verbeterd. Bijschildklieren scheiden bijschildklierhormoon (PTH), de belangrijkste regulator van calcium metabolisme. PTH is een belangrijke hormoon op fosfaat homeostase en botturnover 1, 2. Per ongeluk verwijderen of beschadiging van de bijschildklieren tijdens de hals chirurgie is de meest voorkomende oorzaak van hypoparathyreoïdie, een ziekte die wordt gekenmerkt door een lage bloed calcium, lage PTH, en verhoogde fosfor 1.
Om beter studie hypoparathyroïdie en testen van nieuwe therapieën, betrouwbare en gemakkelijk toegankelijke muismodellen nodig verworven. Muizen worden veel gebruikt in onderzoek, omdat een groot aantal genetische hulpmiddelen zijnvailable in deze soort toelaat verfijnde mechanistische studies in vivo. Hoewel chirurgische parathyroïdectomie (PTX) kan worden gebruikt bij ratten 2, 3, 4, 5, en grotere zoogdieren 6, 7, 8, het technische uitdaging bij muizen vanwege de kleine omvang van de klieren en hun variabele anatomische verdeling 9. Daarom is thyro-parathyroïdectomie (TPTX) typisch uitgevoerd bij muizen, waarbij de schildklier en bijschildklieren elkaar 10 verwijderd. Echter, lage schildklierhormoon niveaus zijn een potentiële confounder in experimenten, complicerende dit model. Bovendien worden C-cellen in de schildklier, die calcitonine, een hormoon belangrijke calcium homeostase in knaagdieren, produceren ook verloren na verwijdering van de driyroids 11.
Verschillende genetische muismodellen van hypoparathyroïdie bestaan die de PTH-null muis 12, de GCM2-null muis 13, en de Nuf muis met een activerende mutatie in het calcium receptor (CASR) 14, 15 omvatten. Echter, deze genetische defecten reeds tijdens de embryonale ontwikkeling aanwezig, en de functie van de bijschildklieren is derhalve reeds tijdens embryogenese aangetast. Dit kan invloed hebben op de ontwikkeling van organen zoals het skelet. Dit in tegenstelling tot patiënten met postoperatieve hypoparathyroidism die de ziekte op latere leeftijd verwerven. Bovendien zijn sommige muismodellen vertonen vroegtijdige sterfte en verminderde vruchtbaarheid, die het gebruik 12, 13, 14 verder compliceert.
We ontwikkelden twee nieuwe muis modellen voor verworven hypoparathyreoïdie. Met behulp van genetisch gemanipuleerde muizen die GFP tot expressie specifiek in de bijschildklieren kan de bijschildklieren gemakkelijke identificatie voor chirurgische verwijdering zonder de schildklier. Deze muis werd geproduceerd door het kruisen van de PTH-Cre muizen, waarin Cre recombinase tot expressie brengt onder de controle van de 5,5 kb promotor PTH 16 met ROSA mTmG muis. De resulterende PTHcre; mTmG muizen uitdrukken groen fluorescerend eiwit specifiek in parathyroïde cellen. De tweede muismodel gebruikt dezelfde PTH-Cre, dit keer naar een STOP cassette uit de induceerbare DTR muis specifiek verwijderen, wat resulteert in expressie van het difterietoxine receptor in de bijschildklieren. Systemische toediening van DT vernietigt parathyroïde cellen, waardoor de dieren hypoparathyroid zonder operatie.
De twee muismodellen die in deze studie tonen een stabiele hypocalcemische fenotype over de drie maanden durende observatie period. De procedures zijn eenvoudig uit te voeren, het fenotype is reproduceerbaar, en de hypoparathyroid muizen vertonen een hoge overlevingskans 17.
Protocol
Deze studie is goedgekeurd door de Institutional Animal Care en gebruik Comite (IACUC) van het Massachusetts General Hospital. Verkrijgen van passende institutionele goedkeuring voor dit dier studie voordat u begint. Sommige technieken zouden moeten worden aangepast aan lokale IACUC eisen.
1. GFP-PTX Muizen
- Verkrijgen PTHcre + muizen en Rosa-mTmG muizen op 8-10 weken oud voor verdere paring.
- Terugkruising de PTHcre + muizen (gemengde 129; FVB achtergrond) met C57BL / 6-muizen gedurende 6 generaties muizen met C57BL / 6 achtergrond te verkrijgen.
- Inteelt PTHcre + muizen PTHcre + / + muizen 17 te verkrijgen.
OPMERKING: Om genotypering uit te voeren, halen het DNA uit het puntje van de staart en het gebruiken voor PCR. De PCR-primers als volgt controleren heterozygotie en homozygotie van de PTHcre transgene zijn: forward primer A, CCTGTCAAGGATGTGGAAGA, reverse primer A ', TCAGATCACACCACACAGCA, forward primer B, CAGTTGTCTTTAGTTTACTCAGCATCAG, reverse primer B ', GATAATCGCGAACATCTTCAGGTT 17. - Cross PTHcre + / + muizen 16 met Rosa-mTmG muizen 18. Spenen PTHcre; mTmG pups toen 4 weken oud.
- Verdoven 8-10 weken oud PTHcre; mTmG muizen door ip injectie van tribroomethanol (Avertin) bij 0,6 mg / g lichaamsgewicht, of andere middelen zoals ketamine / xylazine. Gebruik buprenorfine 0,1 mg / kg sc elke 12 uur als een pijnstillend middel 48 uur na de operatie volgens een goedgekeurd protocol. Zorgen voor passende diepte van de anesthesie door de teen knijpen terugtrekking reflex of andere middelen. Plaats het dier in rugligging.
- Uit te breiden en de voorbereiding van de ventrale halsgebied door het scheren van de huid met behulp van enkele rand messen. Ontsmet de geschoren huid met een povidonjodium antiseptische pad.
- Bedek het dier met steriele chirurgische afdekdoeken om verontreiniging van de operatieplaats deze en gebruik geautoclaveerd microsurgical instrumenten voor de chirurgische ingreep.
- Snijd een 2 cm longitudinale incisie in de huid met een chirurgische scalpel. Ontleden fascia en duw de speekselklieren aan de kant door stompe dissectie met gebogen gekartelde tang.
- Onder de dissectie microscoop met halogeenlicht en een 4 - 5x vergroting, knippen en scheiden de paratracheale spieren met behulp van scherpe tang tips en bloot de luchtpijp.
- Identificeer de schildklier met de rechter en linker kwab naast de luchtpijp.
- Schakel de lichtbron om tl-licht en visualiseren van de twee groene-fluorescerende bijschildklieren.
OPMERKING: Gewoonlijk worden de twee bijschildklieren bij of nabij het oppervlak van de schildklier, maar soms zijn ze zich verder weg. - Haal de groene bijschildklieren met behulp van chirurgische pincet en schaar. Gebruik steriel gaasje voor hemostase en zorgvuldig te controleren langs de luchtpijp om ervoor te zorgen dat alle groene weefsel is verwijderd.
- Sluit de paratracheale spieren door onderbroken hechtdraad met behulp van 6-0 polyglactin 910 hechtingen. Sluit de incisie in de huid door Halsted hechtdraad met behulp van 6-0 polyglactin 910 hechtingen.
- Optioneel: Injecteer 10 ul / g lichaamsgewicht normale steriele 0,9% natriumchlorideoplossing de muizenmaagjes vloeistofvervanging.
- Plaats postchirurgische dieren een aparte kooi op een warme incubator (37 ° C) gedurende lichaamstemperatuur herstel. Zodra de muizen zijn wakker en in de liggende positie, zet pellet chow en water met wat gelatine eten op de kooi vloer.
- Na een postsurgical observatie periode van 2 uur, terug muis om het dier faciliteit en volg de lokale voorschriften voor postoperatieve zorg.
- 3 dagen na parathyroïdectomie, het verkrijgen van 10 pi staart bloed en geïoniseerd Ca ++ met behulp van een analysator te meten, zoals het bloed gas systeem Ca ++ / pH-analyzer. Succesvolle parathyroïdectomie resultaten in het bloed geïoniseerd Ca ++ gelijk of lager dan -2SD van schijn-geopereerde control muizen (1,20 mmol / l in onze experimenten n = 30).
2. PTH-Cre-muizen iDTR
- Verkrijgen PTHcre + en DTR fl / fl muizen op 8-10 weken oud om te paren.
- Terugkruising de PTHcre muizen (gemengde 129; FVB achtergrond) met C57BL / 6-muizen gedurende 6 generaties muizen met C57BL / 6 achtergrond te verkrijgen.
- Inteelt de PTHcre + (C57BL / 6 achtergrond) muizen PTHcre + / + muizen 17 te verkrijgen.
LET OP: Voor het uitvoeren van genotypering, DNA van muizen staart tips werd geëxtraheerd en gebruikt voor PCR. Genotypering primers: voorwaartse primer A, CCTGTCAAGGATGTGGAAGA, reverse primer A ', TCAGATCACACCACACAGCA, forward primer B, CAGTTGTCTTTAGTTTACTCAGCATCAG, reverse primer B', GATAATCGCGAACATCTTCAGGTT 17. - Mate PTHcre + / + muizen 16 met DTR fl / fl muizen 19 tot PTHcre-iDTR muizen te verkrijgen.
- Bereid DT-oplossing door verdunning diphtherieen toxine poeder met steriele zoutoplossing tot een concentratie van 0,5 ug / ml. Steriel filter en bewaar monsters bij -80 ° C.
- Kies 8-10 weken oud PTHcre-iDTR muizen voor injectie experiment. Dooi DT monster tot kamertemperatuur toedienen DT intraperitoneaal in 5 ug / kg (10 ul / g) lichaamsgewicht van het dier. Voor maximale efficiëntie en toxiciteit minste wordt DT toediening herhaald voor een totaal van 2 injecties in een 3-daags interval 17.
- 3 dagen na de tweede injectie, neemt 10 pi staart bloed van elke PTHcre-iDTR / PTHcre-iDTR-mTmG muis en meet bloed Ca ++ met behulp van een Blood Gas Systeem Ca ++ / pH-analyzer.
OPMERKING: We definiëren muizen bloed geïoniseerd Ca ++ lager dan 1,18 mmol / L als hypoparathyroid muizen, 2SD gelijk onder het gemiddelde van het voertuig geïnjecteerde controlemuizen (n = 22).
Representative Results
Ligging van de bijschildklieren
Eerst namen we de verdeling van de bijschildklieren van 54 PTHcre-mTmG muizen waargenomen onder de fluorescerende dissectie microscoop. 74% (40/54) muizen hadden twee groene bijschildklieren (Figuur 1 A, C, E), 26% (14/54) muizen hadden een extra derde bijschildklier (Figuur 1B, D, F). Geen muis met een klier of meer dan drie klieren waargenomen. Meestal bijschildklieren zijn gelegen nabij de bovenrand van de schildklier (58%, 71/122 Figuur 1A (1,2) B (1,2), C (2), D (1,2), E (2), F (3)). 27% (33/122) klieren zijn gelegen nabij de onderrand van de schildklier (figuur 1C (1), D (3), F (1)) en 13% (16/122) werden van de t gelegenhyroid gland (Figuur 1B (3), E (1), F (2)). Onze bevindingen komen overeen met en uit te breiden eerdere bevindingen van verschillende locaties van de bijschildklieren 20.
GFP-PTX Muizen
De hele operatie uit narcose tot het sluiten van de huid incisie duurde ongeveer 20 minuten per muis. De overlevingskans van postoperatieve muizen gedurende een 3-maanden observatieperiode was 96,3% (53/55). 92,4% (49/53) GFP-PTX muizen vertoonden geïoniseerd calcium niveaus die 2 SD onder het gemiddelde van schijn-geopereerde controle muizen of lager waren. De hypoparathyroid fenotype in de GFP-PTX muizen (hypocalcemie, lage PTH en verhoogde serum fosfaat) was stabiel gedurende de gehele observatieperiode van 3 maanden. Belangrijker schildklierfunctie niet verschilde van schijn-geopereerde dieren 3 maanden na de operatie (TSH = 42 ± 24 tegenover 30 ± 15 mU / l, p = 0,171; T4 = 30,0 ± 0,6 vs. 3,1 ± 0,9 ug / dl, p = 0,707 (figuur 2).
PTH-cre-iDTR Muizen
DT geïnjecteerd PTH-Cre-iDTR muizen ontwikkelden hypoparathyroïdie (lage bloed geïoniseerd calcium, verhoogde bloed fosfor en ten onrechte een lage normale PTH niveaus). We hebben eerder gemeld dat enkele PTH positieve cellen ontsnappen aan de ablatie van difterietoxine, waarin de meetbare circulerend PTH en daarom enigszins mildere fenotype van deze muizen 17.
Hypoparathyroïdie in GFP-PTX Muizen en PTH-cre-iDTR Muizen
Aanzienlijke vermindering van het bloed Ca ++ en serum PTH-niveaus werden waargenomen in GFP-PTX muizen 3 dagen na de operatie, in vergelijking met niveaus gevonden in schijn-geopereerde muizen (Ca ++ = 1,05 ± 0,40 vs. 1,30 ± 0,03 mmol / l, p <0,05; PTH = 32 ± 22 vs. 580 ± 137 pg / ml, p <0,05). De hypoparathyroïdie fenotype was stabiel over de 3-maanden observatieperiode (figuur 3A, met toestemming van (referentie # 17)). Na 2 injecties met 5 ug / kg DT 3 dagen interval dosis en regime geoptimaliseerd om zo weinig mogelijk DT om de maximale hypoparathyroid fenotype geven de DT geïnjecteerd-PTH cre-iDTR muizen vertoonden significante hypocalcemie en verlaagde PTH ten opzichte voertuig controle muizen, die in de 90 dagen observatieperiode bleef (Ca ++ = 1,10 ± 0,07 mmol / l versus 1,26 ± 0,05 mmol / l, p <0,05; PTH = 218 ± 156 pg / ml versus 572 ± 164 pg / ml, p <0,05) (Figuur 3B, met toestemming van (referentie # 17)).
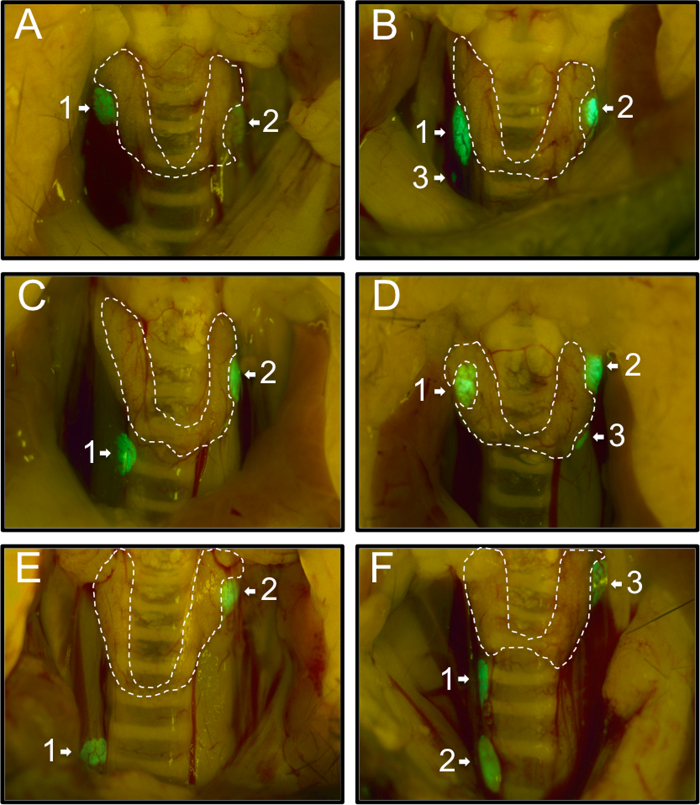
Figuur 1: Vertegenwoordiger Beelden van de verschillende locaties van de bijschildklieren in 54 PTHcre-mTmG Muizen bij TL Dissection Microscope. Muizen hadden hetzij twee (A, C, E) of drie (B, D, F) groene bijschildklieren. Meest bijschildklieren zijn gelegen nabij de bovenrand (A (1,2) B (1,2), C (2), D (1,2), E (2), F (3) of nabij de onderrand van de schildklier (C (1), D (3), F (1)). In zeldzame gevallen, sommige waren ectopisch gelegen (B (3), E (1), F (2)). klik hier om bekijk een grotere versie van dit cijfer.
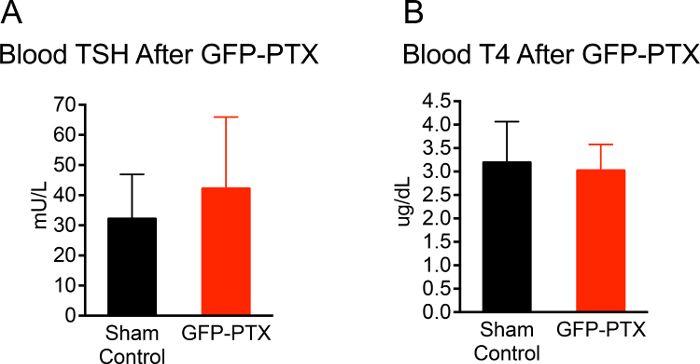
Figuur 2: TSH en T4 niveau van GFP-PTX Muizen. 3 maanden na GFP-PTX werd serum verkregen voor TSH en T4 measurem enten. GFP-PTX muizen TSH (42 ± 24 mU / L) (A) en T4 concentraties (3,0 ± 0,6 ug / dl) (B) die niet verschilt van controlemuizen (TSH = 30 ± 15 mU / L, p waren = 0,171, n = 11, T4 = 3,1 ± 0,9, p = 0,707, n = 11). Klik hier om een grotere versie van deze figuur te bekijken.
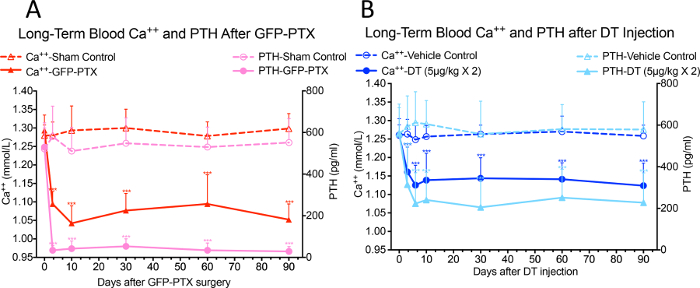
Figuur 3: Blood Ca ++ en PTH Levels in GFP-PTX Muizen en DT geïnjecteerd-PTH Cre-iDTR Muizen. Zowel GFP-PTX muizen (A) en DT-PTH geïnjecteerd cre-iDTR muizen (B) vertoonden stabiele hypocalcemie en verlaagde PTH niveaus gedurende 3 maanden observatieperiode (N = 6-8, *** p <0,001) (herdrukt met toestemming van referentie # 17).es / ftp_upload / 55010 / 55010fig3large.jpg "target =" _ blank "> Klik hier om een grotere versie van deze figuur te bekijken.
Discussion
We tonen de techniek van GFP geleide parathyreoïdectomie transgene muizen met GFP expressie selectief in de bijschildklieren. In de PTHcre, mTmG muizen, dubbele fluorescentie (groen GFP-expressie van Cre cellen en rode tomaten in niet-Cre tot expressie cellen) konden wij duidelijk aan, en nauwkeurig alle bijschildklieren verwijderen zonder de schildklieren. Terwijl we de voorkeur aan het gebruik van de dubbele-fluorescentie mTmG muizen voor de mogelijkheid om fluorescerend rood non-bijschildklierweefsel identificeren, moeten onze procedure ook goed werken met behulp van enkele fluorescerende dieren zoals de tomaat rood (B6.Cg-Ct (ROSA) 26Sortm14 ( CAG-tdTomato) Hze / J) muis. De procedure is relatief gemakkelijk uit te voeren, vereist ongeveer 20 minuten per muis, en resulteert in een ernstige en aanhoudende hypoparathyroid fenotype.
Bovendien is een ander voordeel van de GFP-positieve bijschildklieren is het gemak van detecteren van afwijkende bijschildklieren. Onze studies tonen aanmislocalisatie van de bijschildklieren op ongeveer een kwart van B6 muizen (figuur 1), die gemakkelijk in onze muismodel worden gedetecteerd door de groene fluorescentie. Anders dan thyro-parathyreoïdectomie, onze techniek vermijdt de verwijdering van de schildklier met daaropvolgende noodzaak schildklierhormonen en het onbekende effect van verwijdering van de schildklier calcitonine producerende C-cellen. Fluorescent gelabelde bijschildklieren kan ook worden gebruikt voor andere onderzoeken die de isolatie van de bijschildklieren nodig. De beperking van dit model omvat de vereiste operatie. Basic microchirurgie vaardigheden en een dissectie microscoop met een fluorescerende lichtbron nodig.
Een tweede techniek voor het genereren hypoparathyroid muizen die de noodzaak van chirurgie elimineert aangetoond. Difterietoxine-behandelde PTHcre-iDTR muizen vertonen een milder hypoparathyroïdie fenotype, maar gewoon voor dat het injecteren van DT intraperitoneaal in de muis. De kritische deel for genereren dit model werd de optimalisatie van de dosis en het doseringsschema. Hoge doses DT tot toxiciteit maar lage doses verlaagde de werkzaamheid van de benadering. We hebben vastgesteld dat de dosis regiment 2 injecties met 5 ug / kg, toegediend 3 dagen na elkaar, resulteerde in betrouwbaar en stabiel hypocalcemie geen / minimale mortaliteit.
Uiteindelijk hopen we dat deze twee benaderingen leveren nuttige muismodellen voor verworven hypoparathyreoïdie. Volgens een nieuw langwerkend PTH rapporteerden wij het eerste gebruik van beide modellen het bepalen van de effectiviteit van nieuwe geneesmiddelen voor hypoparathyreoïdie 17.
Disclosures
The authors declare that they have no competing financial interests.
Acknowledgements
Dit werk werd ondersteund door de NIH subsidies R01-DK100584 en China State Key Laboratory Mondziekten Open Funding SKLOD2015OF01 (RB). Wij danken Wenping Zhao, Tadatoshi Sato, en Kelly Lauter om hulp.
Materials
| Name | Company | Catalog Number | Comments |
| ROSAmT/mG mice | The Jackson Laboratory | 7676 | |
| PTH-Cre mice | The Jackson Laboratory | 5989 | |
| iDTRmice | The Jackson Laboratory | 7900 | |
| 6-0 polyglactin 910 suture with needle | Ethicon, Inc | J510G | |
| Safety Single Edge Razor Blades | American Safety Razor Company | 66-0089 | |
| Disposable Scalpel | Feather Safety Razor Co., LTD | 72042-11 | |
| Povidone-Iodine Prep Pads | Dynarex Corporation | 1108 | |
| Ply gauze | Busse. Inc | BHD707 | |
| 0.9% Sodium Chloride Solution | HOSPIRA Worldwide, Inc | 07983-09 | |
| 1mL 29G Insulin Syringe | BECTON DICKINSON | 329622 | |
| Surgical Incise Drapes | 3M | 6640EZ | |
| Dumstar Biology forceps | Roboz Surgical Instrument Co., Inc | RS-4984 | |
| Micro Dissecting Spring Scissors | Roboz Surgical Instrument Co., Inc | RS-5605 | |
| Needle Holder | MILTEX.,Inc | V98-42 | |
| 2,2,2-Tribromethanol | Sigma-Aldrich | T48402 | |
| 2-Methyl-2-Butanol | Sigma-Aldrich | 152463 | For dissolve the 2,2,2-Tribromethanol |
| Diphtheria Toxin Powder | Sigma-Aldrich | D0564 | Dissolve in 0.9% sodium chloride solution at 1mg/mL as the stock solution in -80C |
| Multicap Blood Collection Capillary tubes | Siemens Healthcare Diagnostics Ltd | 855578 | For collecting blood in iCa2+ analysis using RapidLab 348 Ca2+/pH analyzer |
| RapidLab 348 Ca2+/pH analyzer | Siemens Healthcare | For iCa2+ analysis |
References
- Brandi, M. L., Brown, E. M. . Hypoparathyroidism. , (2015).
- van Abel, M. Coordinated control of renal Ca(2+) transport proteins by parathyroid hormone. Kidney Int. 68, 1708-1721 (2005).
- Sebastian, E. M., Suva, L. J., Friedman, P. A. Differential effects of intermittent PTH(1-34) and PTH(7-34) on bone microarchitecture and aortic calcification in experimental renal failure. Bone. 43, 1022-1030 (2008).
- Rodriguez-Ortiz, M. E. Calcium deficiency reduces circulating levels of FGF23. J Am Soc Nephrol. 23, 1190-1197 (2012).
- Liao, H. W. Relationship between Fibroblast Growth Factor 23 and Biochemical and Bone Histomorphometric Alterations in a Chronic Kidney Disease Rat Model Undergoing Parathyroidectomy. PloS one. 10, e0133278 (2015).
- Fox, J., Care, A. D. Effect of low calcium and low phosphorus diets on the intestinal absorption of water in intact and parathyroidectomized pigs. Calcif Tissue Int. 31, 253-255 (1980).
- Finco, D. R., Brown, S. A., Ferguson, D. C., Crowell, W. A. Selective parathyroidectomy of the dog. Can J Vet Res. 57, 288-292 (1993).
- Can, I. Parathyroid allotransplantation in rabbits without cultivation. Int J Clin Exp Med. 7, 280-284 (2014).
- Dunn, T. B. Melanoblasts in the stroma of the parathyroid glands of strain C58 mice. j Natl Cancer Inst. 10, 725-733 (1949).
- Sakai, A. Osteoclast development in immobilized bone is suppressed by parathyroidectomy in mice. J Bone Miner Metab. 23, 8-14 (2005).
- Miao, D. Skeletal abnormalities in Pth-null mice are influenced by dietary calcium. Endocrinology. 145, 2046-2053 (2004).
- Gunther, T. Genetic ablation of parathyroid glands reveals another source of parathyroid hormone. Nature. 406, 199-203 (2000).
- Hough, T. A. Activating calcium-sensing receptor mutation in the mouse is associated with cataracts and ectopic calcification. Proc Natl Acad Sci U S A. 101, 13566-13571 (2004).
- Hannan, F. M. The Calcilytic Agent NPS 2143 Rectifies Hypocalcemia in a Mouse Model With an Activating Calcium-Sensing Receptor (CaSR) Mutation: Relevance to Autosomal Dominant Hypocalcemia Type 1 (ADH1). Endocrinology. 156, 3114-3121 (2015).
- Libutti, S. K. Parathyroid gland-specific deletion of the mouse Men1 gene results in parathyroid neoplasia and hypercalcemic hyperparathyroidism. Cancer Res. 63, 8022-8028 (2003).
- Bi, R. Diphtheria Toxin- and GFP-Based Mouse Models of Acquired Hypoparathyroidism and Treatment with a Long-Acting Parathyroid Hormone Analog. J Bone Miner Res. , (2015).
- Muzumdar, M. D., Tasic, B., Miyamichi, K., Li, L., Luo, L. A global double-fluorescent Cre reporter mouse. Genesis. 45, 593-605 (2007).
- Buch, T. A Cre-inducible diphtheria toxin receptor mediates cell lineage ablation after toxin administration. Nat Methods. 2, 419-426 (2005).
- Dunn, T. B. Melanoblasts in the stroma of the parathyroid glands of strain C58 mice. J Natl Cancer Inst. 10, 725-733 (1949).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved