JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
사이토 반응성 및 확산에서 체 외에 허 혈 성 같은 조건 모니터링
* 이 저자들은 동등하게 기여했습니다
요약
허 혈 성 뇌졸중 공부 하기 어려운 어떤 영향을 받는 뇌 영역에 이다의 구체적인 기여 산소 포도 당 부족 (지도부)에 노출 하는 복잡 한 이벤트입니다. 이 문서는 고립 된 이다 그들의 반응성 및 확산 지도부 조건 하에서 연구 하는 방법론을 소개 합니다.
초록
허 혈 성 뇌졸중은 혈전 또는 두뇌의 부분에 혈액 흐름을 방해 하는 embolus로 인 한 복잡 한 뇌 손상. 이것은 산소와 포도 당, 에너지 실패 원인과 신경 죽음의 부족. 허 혈 성 뇌졸중 모욕 후 이다 반응 되 고 그것은 개발로 부상 사이트 격 증. 이 시나리오에서는 허 혈에 노출 된 뇌 영역에 이다의 구체적인 기여를 공부 하기 어렵습니다. 따라서,이 문서의 기본 사이토 반응성 산소 포도 당 부족 (지도부) 라는 허 혈 같은 환경의 체 외에 모델 확산을 공부 하는 방법을 소개 합니다. 이다 1-4 일에서 고립 되었다-오래 된 신생아 쥐와 일반적인 astrocytic 셀 수 사이토 선택 마커 폐해 Fibrillary 산 성 단백질 (GFAP) 및 핵 얼룩을 사용 하 여 평가 했다. 기간 이다 지도부 조건에 복종 된다 수 사용자 지정할 수, 그들은에 노출 되는 산소의 백분율 뿐만 아니라. 이 유연성 과학자를 셀 체 외의 다른 그룹에서 허 혈 성 같은 상태 기간 특성을 수 있습니다. 이 문서에서는 사이토 반응성, hypertrophic 형태학 및 확산 증식 세포 핵 항 원 (PCNA)를 사용 하 여 면역 형광 검사로 측정 된 유도 지도부의 시간대를 설명 합니다. 확산, 게다가 이다 에너지와 산화 스트레스를 받게 하 고 응답 지도부 셀 중간에 녹는 요소를 해제 하 여. 이 매체는 수집 고 분자 이다 세포 세포 상호 작용 없이 기본 신경 문화에 의해 발표의 효과 분석 하는 데 사용 될 수 있습니다. 요약 하자면,이 1 차 셀 문화 모델 부상 시 절연된 이다의 역할을 이해 하 효율적으로 사용할 수 있습니다.
서문
선 "는 급성 신경 부전 혈관 근원의 증상 및 징후, 뇌의 초점 분야의 참여 하에 해당의 급격 하거나 급속 한 개발"1,2로 정의 됩니다. 뇌졸중의 두 가지 유형이 있다: 출혈 및 허 혈 성. 혈관 장애는 동맥 류 또는 arteriovenous 오작동, 약화의 동맥, 후부 파열과 동반 하 여 발생 하는 경우이, 죽음에 이르게 하는 대부분의 경우에는 출혈 성 뇌졸중3 이라고 불린다. 혈전 또는 embolus 혈액 흐름을 방해, 산소와 포도 당 두뇌 지역에의 임시 박탈을 일으키는 그것 이라고 뇌경색4합니다. 영향을 받는 지역 또는 항상성 및 대사 불균형, 에너지 장애, 신경 죽음, 및 염증5, 환자6평생 장애를 일으킬 수 있는 허 혈 성 핵심 리드 주위 세포를 키 우다 실패.
허 혈 성 뇌졸중은 반응 하 고 다른 시간 지점에서 그들의 효과 발휘 하는 셀의 여러 종류를 포함 multifactorial 부상이 다. 많은 상호 작용 개별 셀의 동작을 연구 하는 어려운 환경을 만들. 그래서, 우리가 어떻게 이러한 복잡 한 환경에서 특정 세포 유형에의 기여를 연구? 허 혈의 허용 시험관에 모델 이루어져 있다 산소와 포도 당 부족 (지도부), 세포를 노출 특정 기간에 대 한 다음 normoxic 환경에 세포의 복원. 이 시스템은 혈 reperfusion 뒤 허 혈 성 뇌졸중을 시뮬레이션 합니다. 이 방법에서는, 세포 또는 조직 전문된 hypoxic 챔버를 사용 하 여 산소의 제거는 환경에서 포도 당 자유로운 매체에 노출 됩니다. 지도부 부 화 시간 몇 분에서 최대 24 h, 가설을 테스트 하 고 싶어에 따라 달라질 수 있습니다. 연구 하는 지도부의 시대에 따라 그리고 normoxic 환경, 스트로크 (즉, 급성 또는 아민)의 특정 고기를 얻을 수 있다. 기본 절연된 이다, normoxic 조건에 후부 복원와 지도부에 노출 선 체 외7모방을 잘 공부 셀룰러 모델 이다. 지도부를 사용 하 여 뇌졸중 같은 환경에서 격리 된 셀의 독립적인 분자 메커니즘을 밝힐 수 있다.
사이토 생물학의 우리의 지식을 증가, 그것은 분명 그들은 시 냅 스를 유지 하 고 신경 수리, 개발, 및 소성8유지에 대 한 중요 한 되고있다. 정상적인 조건 하에서 이다 놓고 cytokines, 발산, 성장 인자 및 gliotransmitters, 신진 대사 균형 및 시 냅 스5,9내 항상성 유지에 응답. 허 혈 성 뇌졸중 등 급성 neuroinflammation에이 셀 수 있다 반응 될, 장기 overexpression의 폐해 Fibrillary 산 성 단백질 (GFAP), 표시 및 그들의 형태학5,10, 에 비 표시 11 , 12. 허 혈 성 경색 개발로, 항상성 이다에 의해 제공 된다 영향을, 일반 조미료 통풍 관, 에너지 대사, 활성 분자, 그리고 항 산화 활동13의 교환에 관한.
다시 활성화 이다 백혈구14lesioned 지역 이동 하는 동안 경색 조직 주위 확산. Astrocytic 확산 증식 세포 핵 항 원 (PCNA), Ki67, 등 bromodeoxyuridine (BrdU)15마커를 사용 하 여 측정 될 수 있다. 이 증식 응답 시간-종속 방식으로 생성 되 고 glial 흉터, 부상9후 손상 된 사이트의 실질에 따라 돌이킬 반응성 이다의 배열을 형성 하는 데 도움이. 이 흉터의 초기 기능 중 하나는이 지역에서 면역 세포 넘쳐 흐름을 제한 것입니다. 그러나, 연구 흉터 확장 하, 그들은 릴리스 axonal 성장 억제 분자 고 부상된 지역16주위 확장에서 축 삭을 방지 물리적 장벽을 만드는 축 삭에 대 한 물리적 장애물이 되는 것으로 나타났습니다. 그럼에도 불구 하 고, 그 척수 상해 후 완전히 glial 흉터 대형을 방지 수 있습니다 손상17축 삭 재생을 보여주는 과학적인 증거가 있다. 따라서, 컨텍스트는 특정 astrocytic 응답 측정, 공부 하는 상해의 프레임 워크에 고려 되어야 한다.
제시 하는 방법론 산소가 포도 당 결핍 후 이다의 개별된 기능 연구에 적용할 수 있습니다 그리고 탐정 대답을 원하는 질문에 따라 수정할 수 있습니다. 예를 들어 형태학 상 변화와 다른 지도부 시간에 표현 하는 마커, 게다가 이다 지도부에 노출에서 supernatants 분석 될 수 있다 더 식별 성 요인,이 세포에 의해 발표 또는 바른된 미디어로 평가 하는 데 사용 하는 다른 뇌 세포에 효과입니다. 이 이렇게 규제 하 고 허 혈 성 뇌졸중 시나리오에서 그들의 응답을 조절 하는 요인의 설명으로 이어질 수 있는 사이토 반응성에 대 한 연구를 수 있습니다.
프로토콜
1-4 일 산 후 쥐 (Sprague Dawley) 오래 된 외피가 분리 하는 데 사용 됩니다. 안락사는 잘린, NIH 지침에 의해 승인.
1. 악기의 준비와 수술에 대 한 자료
- 압력솥에 Sterilize 계기 (온도: 121 ° C, 압력: 15 psi, 시간: 30 분) 강철 상자 또는 살 균 주머니 씰링 인스턴트를 사용 하 여. 자료 테이블에에서 자료를 참조 하십시오.
2. DMEM 준비 완료
- 압력가 물 700 mL를 포함 하는 1 리터 비 커에 추가 Dulbecco ' s 수정이 글 ' s 실 온에서 중간 파우더.
- 3.7 g/L 나트륨 중 탄산염, 솔루션은 자력으로 자극 하는 동안 추가.
- 조정 7.4, 압력가 마로 소독 물에 pH 1 L, 볼륨을가지고 필터링 합니다. 10 %FBS 1% 미디어의 원하는 볼륨 보충 목적을 위해 문화, 페니실린/스, 및 37 ˚C에서 따뜻한. 자료 테이블에에서 자료를 참조 하십시오.
참고: PH 7.4 미디어 pH 미터 전극 삽입을 통해 조정 했다. 천천히 1 M NaOH를 스 포 이트를 사용 하 여 추가 미디어 감동 해야 합니다,.
3. 기본 사이토 문화
참고: 시드, 후 셀 미디어 3 일 마다 변경 되어야 하 고 셀 confluency (11-13 일)까지 성장 될 수 있다. 제 3의 날에 여러 번 리프트 microglial 세포와 문화에서 oligodendrocyte 조상 세포를 플라스 크를 모두 제거는 ' 오래 된 ' 미디어, PBS의 10 mL를 사용 하 여 두 번 세척, PBS, 발음 다음 신선한 새로운 미디어를 추가. 자료 테이블에에서 자료를 참조 하십시오.
- 수행 조직 문화 후드에서 절 개
- . 얻기 1-4 일 (2 쥐 두뇌 75 cm 2 플라스 크 당 사용 하는) 오래 된 신생아 쥐 새끼.
- 3 60 mm 페 트리 접시를 준비 하 고 각각에 완전 한 DMEM의 5 mL를 플라스틱.
참고: 그들은 다음과 같이 분할 될 수 있다: #1 각 쥐 뇌, 두뇌의 모든 외피가 (meninges) 없이 모든 벗 겨 외피가 #3 #2. - 파악 강아지와 70% 에탄올 스프레이. 그것은 목을 벨 하 고 작은 생물 학적 폐기물 컨테이너에 시체를 버리고.
- 마이크로 해 부 핀셋을 사용 하 여, 머리를 누른 노출은 두개골 머리 위에 피부를 잘라.
- 또 한 쌍의가 위, 게는 " T " 절 개는 코 쪽으로 두개골의 뒤쪽에서 시작. 집게의 쌍을 사용 하 여 부드럽게 제거 두개골.
- 핀셋의 쌍으로 노출 된 뇌를 제거 하 고 뇌 이전 매체 가득 배양 접시 중 하나에 놓습니다.
- 후속 단계에 대 한 살 균 계기의 다른 세트를 사용 하 여.
- 는 마이크로 해 부 집게를 사용 하 여 부드럽게 60 mm 페 트리 접시의 뚜껑을 거꾸로 한 두뇌를 위. 페 트리 접시는 멸 균 거 즈에 배치 됩니다, 그것은 두뇌를 명확 하 게 볼 수 고 해 부 쉽습니다.
- 마이크로 해 부 집게와 뇌를 꾸준히 하 고 분리 되는 대뇌 반구 마이크로 해 부 집게의 날카로운 끝을 가진 중간 균열을 따라 부드럽게 놀리는.
- Deflect 백색 질 뒤에 남겨두고 외피가 껍질 하 고 이전 표시 #2 페 트리 접시에 그들을 전송. 모든 두뇌, # 2를 표시 하는 페 트리 접시에 모든 해 부 외피가 결합에 대 한 절차를 반복.
- 각 피 질 밑에서 해 마에 밖으로가 고 그것을 삭제
- 마이크로 해 부 족집게와 60 mm 페 트리를 사용 하 여 개별 대뇌 피 질의 엽에서 meninges 껍질을 부드럽게 하 고 # 3를 표시 하는 페 트리 접시에 그들을 배치.
- 3 60 mm 페 트리 접시를 준비 하 고 각각에 완전 한 DMEM의 5 mL를 플라스틱.
- 조직 분리: 균질 화기 믹서 메서드
- 살 균 믹서 기 가방으로 조직/중간 정지 (뇌의 껍질을 벗 겨 외피가)을 부 어 하 고 가방에 5 mL 전체 볼륨을가지고 충분 한 매체 추가.
- 닫힌된 문 위에 보이는 가방 약 2 cm를 떠나 균질 화기 믹서 기에 가방을 놓습니다. 셀 분리 고속에서 2.5 분 동안 이루어집니다.
참고: 또는,이 가방을 닫고 부드럽게 후드에서 비 커와 요동에 의해 수행할 수 있습니다. 피복 부 대와 비이 커를 사용 하 여 마찰을 피하기 위해 있는지 확인 하십시오. - 번호 60 메쉬 체에 세포 현 탁 액을 부 어 하 고 다음에 번호 100 체, 중력에 의해 필터링을 통해 필터링 된 흐름을 붓는 다.
- 사용 하 여 15 mL 튜브, 원심에서 5 분에 대 한 임상 원심 분리기 (선호: 스윙 양동이 터)에 200 x g 세포 현 탁 액
- 부는 비 커에 상쾌한 어 그리고 혈 청 학적인 피 펫을 사용 하 여, 다시 일시 중단 최대 미디어의 5 mL에에서 셀의 펠 릿을 해리.
- 셀 계산
- micropipette와 함께 microcentrifuge 1.5 mL 튜브에 세포 현 탁 액의 100 µ L를 수집 하 고 trypan 파랑의 100 µ L를 추가.
- 는 hemocytometer에 수집 된 서 스 펜 션의 10 µ L 하 고 광장의 네 모퉁이 있는 모든 셀을 카운트.
- 셀의 밀도 계산 하는 플라스 크를 준비 하기 전에 공식입니다:
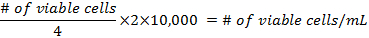
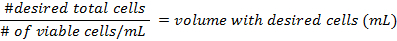
- 25 c m 2 플라스 크 당 적어도 500000 셀 추가. 각 플라스 크에 DMEM의 5 mL를 플라스틱 혼합물은 플라스 크의 목에 도달 하지 해야 합니다. 3 일 동안, 5% CO 2, 37 ° C 배양 기에 넣어 다음 미디어 변경.
- 사이토 정화 기법: 미디어 변경, 기계, 및 화학 전략
참고: 이다의 신진 대사 속도 다른 세포 유형에 비해 높은에 따라서, 영양 박탈 조건,이 셀이 몇 일 후 낮은 생존 율을 보여. 이다, 달리 microglia 영양 부족에 의해 영향을 받지 않습니다 및 이러한 환경 18에서 증식. Microglial 세포의 감소 된 수를 유지 하려면 저자는 astroglial 세포 배양 3 일 마다 변경 합니다. 셀 미디어에서 지속적인 변화가 또한 플라스 크 19에서 astrocytic 셀 단층 위에 성장할 수 있는 microglial 인구를 줄일 것 이다. 비 점착 microglial 세포는 플라스 크의 각 미디어 발음을- 사용은 파스퇴르 피 펫. 워시 모든 파편 dropwise 방식 (5 mL/플라스 크) 각은 플라스 크를 살 균 필터링 PBS를 사용 하 여 뒤에 왼쪽.
- 추가 (항생제와 태아 둔감 한 혈 청)와 살 균 필터링 DMEM dropwise 각 플라스 크 (5 mL/플라스 크). 부드럽게 전체 표면을 커버 하는 원형 운동에 선동.
- 는 37 곳 셀 &# 176; 플라스 크 confluency에 도달할 때까지 8-10 일 동안 5% CO 2 C 인큐베이터 (> 95% 플레이트 범위).
참고: 여러 프로토콜 이다 confluency에 도달, 24 h 2에서 문화를 떨고와 같은 기계적인 방법을 셀이이 이다, 주로 microglia 및 전조 위에 있는 셀의 초연에 이르게 나타났습니다 19 , 20. - 비 astrocytic 세포 문화에 30 분 동안 180 rpm에서 궤도 동요를 수행 하 여 줄일 수 있습니다. 상쾌한에 세포를 제거한 후 신선한 미디어 플라스 크 (~ 15 mL)에 pipetted은.
- Oligodendrocyte 조상 세포를 제거 하는 6 h 21 , , 22 23, aspirate 상쾌한을 피펫으로 신선한 미디어 200 rpm을 떨고 속도 증가.
참고: Microglia 문화에의 존재를 줄이려면 두 가지 화학 방법을 순차적으로 사용할 수 있습니다 (동시에) 1 차 셀 문화 방법론에서: Arabinose 시 토 신 (아 라-C) 및 L-신 메 틸 에스테 르 (LME) 24. - 셀 confluency (100%)를 도달 했을 때, 즉시 microglia의 기계적 제거 후 3-4 일이이 세포로 치료가 될 수는 antimitotic 복합 Arabinose 시 토 신 (아 라-C)의 8 µ M DMEM에 5 일 (신선한 아 라-C DMEM 매일 변경)에 대 한.
참고: 시간 아 라-c 요점은 중요 한이 화합물 이기 때문에 antimitotic 마약, microglia 19 , 25 및 섬유 아 세포와 같은 급속 하 게 분할 세포의 수를 감소 시키는 26 . Microglia, 달리 confluent, 이다 중지 접촉 저해 27를 통해 확산. - Ara C 치료에서 회복 하기 위해 셀에 대 한 일. 더 후 셀 도달 confluency, microglial 오염 줄이기 위해
- DMEM pH 7.4, 37 ˚C에서 1 h에 고정에서 50mm L 신 메 틸 에스테 르 (LME)의 사용.
참고: LME 십자가 세포와, 세포의 막 그리고 분해 되 고, 후 생산 L 신이이 세포의 리소좀 축적. 이 아미노산의 축적 한 삼투성 붓기와 리소좀 28 , 29의 파열에 지도 한다. LME microglia, 다른 셀 20 , 30에 비해 제거에 매우 효과적 이다.
4. 6 잘 플레이트에 이다 육성
- 폴 리 D lysine과 코팅 coverslips
- 넣어 한 coverslip 각 35 mm 페 트리 접시에, 그때 각 coverslip 희석된 폴 리-D-리 솔루션의 100 µ L을 추가 하 고 대기 1 헤
- 폴 리-D-리 신을 제거 하 고 2 살 균 물으로 두 번 세척.
- 물을 제거 하 고 coverslips 후드 내부 건조 기다립니다. 2 주 동안-20 ° C에서 coverslips 저장.
참고: 고정 희석된 폴 리-D-리 솔루션; 그것은 최대 2 주 동안 저장 될 수 있다.
- Trypsinization
- 는 플라스 크에서 중간 발음 파스퇴르 피 펫을 사용 하 여. 부드럽게 셀 린스를 살 균 필터링 PBS의 5 mL/플라스 크 추가.
- Aspirate PBS를 끄고 살 균 필터링 0.25 %Trypsin 및 0.5 m EDTA 솔루션의 5 mL/플라스 크를 추가. 37 ˚C, 10 분에 대 한 5% CO 2 배양 기에에서 플라스 크를 배치
참고: 셀은 잠복기 동안 따뜻한 플라스 크 mL 5/37에서 신선한 완전 한 DMEM의 ° c. - 후 10 분, 외피의 모든 세포는 플라스 크를 낸 되도록 교 반 하십시오. 신속 하 게 무력화는 트립 신 각 플라스 크에 따뜻한 완벽 한 DMEM의 5 mL을 추가.
- 부드럽게 위아래로 여러 번 어떤 헤어 셀 플라스틱 " 덩어리 ". 15 mL 원뿔 원심 분리기 튜브에 두 개의 플라스 크에서 일시 중단 된 셀 전송.
- 200 x 5 분 동안 원심 분리기 g 세포 pellet를 수집. 다시 중간의 500 µ L에 펠 릿을 일시 중단 하 고는 플라스 크에 세포를 진행.
참고: 셀으로 만들 수 분석의 예: 1) 반전 녹음 방송 연쇄 반응 (RT-PCR) 유전자 발현; 분석 하 단백질 표정; 평가 하 2) 서쪽 오 점 3) 흐름 cytometry 분석 계량 신경 조상 세포의 수와 관심;의 단백질을 4) 면역 형광 단백질 식 및 지역화 분석.
- 시드 이다
- trypsin으로 기본 이다 치료 후 (4.2 참조), microcentrifuge 1.5 mL 튜브에 세포 현 탁 액의 100 μ를 수집 하 고 추가 0.5 %trypan 파랑의 100 μ.
- Trypan에서 수집 된 서 스 펜 션의 추가 10 μ는 hemocytometer 파랑 및 가능한 모든 셀을 카운트.
- 는 플라스 크를 준비 하기 전에 셀의 밀도 계산 하는 공식 단계 3.3에서에서 사용.
- 준비 다 잘 요리 한 살 균을 추가 하 여, 폴 리-D-리 신 각 우물에 coverslip 코팅. 플라스틱 50000 셀 하 고 신선한 매체 (약 2 mL)와 각 다 잘 접시에 볼륨의 나머지를 작성.
- 멀티 잘 요리 5% CO 2 37 ˚C 인큐베이터에 놓고, 5-7 일 후에 이다 수 성장 하 고는 coverslips의 전체 표면을 커버.
5. 기본 이다에 대 한 지도부 프로토콜
- 지도부 중간 준비
- 보충 Dulbecco ' s 수정이 글 ' s 매체 무료 포도 당 3.7 g/L 나트륨 중 탄산염, 그리고 1% 페니실린/스. 표 4에 자료를 참조 하십시오.
- 2 95% N / 5%를 버블링 하 여 포도 당 자유로운 매체의 20 mL를 제거 15 L/min (흐름 미터 표시) 매체에 가스 시스템에 혈 청 학적인 피 펫을 삽입 하 여 흐름에 10 분 CO 2.
참고: 산소의 제거, 후 7.4 (단계 2.1에 참고 참조)에 pH를 조정. - 필터링 50 mL 튜브 필터 시스템을 사용 하 여 제거 된 포도 당 자유로운 매체.
참고: 버블링 2 95% N / 5%, 모든 실험에 대 한 신선한 지도부 매체 확인 셀 산소의 제거는 환경에 노출 되어 있는지 확인 하려면 사용 하기 전에 CO 2.
- 실험 절차
- 이전 준비 coverslips (4.3.5 단계로 참조)에서 사이토 미디어 조직 문화 후드 안에 제거 그리고 세포에 있는 포도 당을 제거 하려면 두 번 셀룰러 PBS로 세척.
- 는 지도부 미디어의 2 개 mL를 추가 각 잘 하 고 다 잘 요리 그들의 뚜껑에서 hypoxia 챔버 내부 배치
- 입구 밸브에 가스 혼합물을 연결 하 고 출구 밸브를 열어 둡니다. 플러시 챔버 가스 혼합 2 95% N / 5% CO 2, 5 분에 대 한 15 L/분
- 가스 흐름을 막을 먼저 출구 밸브에 클램프를 닫고 다음 가스 입구 밸브 배관에 클램프를 닫습니다.
참고: 비눗물으로 챔버의 인감을 취재 하 여 가스 누설입니다 확인 하십시오. 아니 거품 형성 한다 물개 안전 경우. - 37 ° C 1 시간 또는 지도부에 6 h에서 셀 문화 인큐베이터 전체 챔버를 넣습니다.
- 보육 시간, 끝난 후 지도부 미디어 발음 및 신중 하 게 각 4.67 cm 2는 normoxic를 위해 잘 완전 한 DMEM의 2 개 mL를 피펫으로 24 h. 처리
6. 기본 사이토 면역 형광 검사 준비를 위한 프로토콜
참고: 사이토 순도 평가, 다른 뇌 세포 종류와 같은 신경, microglia, 및 oligodendrocytes에 의해 검출 될 수 있다 다른 사용 하 여 면역 형광 세포 마커. 확산 마커, PCNA, 및 propidium 요오드 화물 (PI) 기본 이다 normoxic 조건 다음 지도부에 노출에 사용할 수 있습니다. 자료 테이블에에서 자료를 참조 하십시오.
- 면역 형광 검사 준비
참고:이 일반적인 면역 형광 검사 프로토콜, 사소한 수정 (예를 들어, 더 이상 부 화 기간, 최적의 신호를 달성 하기 위해 수행할 수 있습니다 부 화 온도)입니다. 표 1에서 각 마커는 제조업체에 따라 사용할 수 있습니다 ' s 프로토콜.- 세포 생존 능력을 평가 하는
- 세포와 37 ° C에서 5 분 동안 incubated 수 파이 (완전 한 DMEM 5 µ M)와 PI 얼룩을 보여 주는 5 분 셀은 보다 적게 가능한 한 2 mL의 PBS로 두번 세척.
참고: 세포 치료 단계 5.2.6 사용. - PI 염색 후 세포를 해결 하기 위해 4 ˚C에서 20 분, 4.67 c m 2 당 4% 포 르 말린의 2 개 mL를 추가 합니다. PCNA와 함께 표시 하는 샘플에 대 한 기본 고정 솔루션은 메탄올 4 ˚C에서 10 분.
주의: 포 르 말린과 메탄올은 독성.
참고: 항상 각 회사에서 특정 항 체 프로토콜을 확인 하십시오. - 5 분에 대 한 PBS의 2 mL로 세포 세척 하 고이 단계를 반복 하 여 3 번.
- 솔루션을 차단에 셀을 품 어 (0.5% 비 이온 계면 활성 제, 10% FBS PBS에) 부드러운 진동으로 실 온에서 30 분.
- 5 분에 대 한 PBS의 2 mL로 세포 세척, 세척을 3 번 반복.
- 1 차적인 항 체 (PCNA, GFAP) 1%의 솔루션에서으로 4 ° C에서 하룻밤 (16h), 품 어 PBS에서 FBS.
- 1 차적인 항 체 솔루션을 제거, 5 분, PBS의 2 mL로 세포 세척 하 고 3 번이이 단계를 반복.
- 1%의 솔루션에 fluorophore와 활용 된 이차 항 체와 품 PBS, 실 온에서 1 h에서 FBS.
- 셀 2 mL PBS의 5 분을 씻어, 3 번이이 단계를 반복 합니다. DAPI의 1 µ g/mL를 추가 (4 ' 6, '-diamidino-2-phenylindole) 얼룩 세포 핵 5 분.
- PBS 5 분의 2 mL로 세포 세척,이 단계를 두 번 반복 시키고 PBS에.
- 설치 매체를 사용 하 여 현미경 슬라이드에 coverslips 준비.
- 세포와 37 ° C에서 5 분 동안 incubated 수 파이 (완전 한 DMEM 5 µ M)와 PI 얼룩을 보여 주는 5 분 셀은 보다 적게 가능한 한 2 mL의 PBS로 두번 세척.
- Confocal 현미경
- 현미경을 설정한 후 위 coverslip 측면 아래로 현미경 단계.
- 소프트웨어를 사용 하 여 선택 GFAP Cy3 활용 된 항 체에 대 한 543nm에서 레이저 빔.
7. 세포 생존 능력 분석 결과
- Trypsinize와 다음 단계로 4.3 및 4.4 이다 계량.
- 96 잘 접시 1 x 10 4 셀/잘 추가 하 고 confluency에 그들을 성장.
- 교양된 96 잘 접시 중 normoxic 1 h 지도부에 노출 5 단계에서 방법론을 사용 하 여, 또는 6 h 지도부.
- 지도부 후 치료, normoxic 미디어 24 h에 대 한 모든 셀에 추가 되 고 생존 MTT 시 분석 결과 사용 하 여 측정 된다 (제조자로 사용 ' s 명령을 나타냅니다).
- 5 mg/mL MTT 솔루션에서 각 잘을 총 볼륨의 10%를 추가 하 고 MTT 시와 37 ˚C에서 3 h에 품 어.
- 는 미디어를 제거 하 고 결정 200 µ L 디 메 틸 sulfoxide를 사용 하 여 resuspend. 570에서 분 광 광도 계에 접시를 읽고 nm.
참고: 제어 셀을 기준으로 감소 흡 광도 적은 생존 연관 됩니다.
결과
기본 astrocytic 문화의 주요 관심사 중 하나는 뉴런, oligodendrocytes, 섬유 아 세포, microglia 등 다른 세포의 존재 이다. 그림 1에서 쥐 외피가에서 고립 된 셀 미디어 변경 3 일 마다 졌고 중 치료 또는 치료와 함께 추가 LME 1 h. 24 시간 후에, 세포에 GFAP immunostained 되었고 DAPI와 counterstained. LME 치료 셀 8% 보여주었다 동안 치료 셀 긍정적인 세포 GFAP-39% 비의 평균...
토론
이 프로토콜 이다 쥐 외피가에서 격리를 설명합니다. 이 방법에서는, 그것은 microglia, oligodendrocytes, 섬유 아 세포 등 다른 세포 종류와 오염 감소에 중요 한입니다. Microglia의 수를 줄이기 위해, 몇 가지 단계를 취할 수 있습니다: 미디어, 떨고, 궤도 및 화학 치료를 변경. 가장 눈에 띄는 셀 오염 물질에 대 한 선택적 세포 마커를 사용 하 여 면역 형광 또는 문화 순수성을 확인 실험을 수행할 수 있습?...
공개
저자는 공개 없다.
감사의 말
저자는 기술 지원에 대 한 파 올라 로페스 Pieraldi를 감사 드립니다. A.H.M.는 보조금 8G12MD007600 및 U54-NS083924이이 간행물을 지원에 대 한 감사. 우리 시설 지원에 대 한 NIH-NIMHD-G12-MD007583 그랜트를 감사합니다. D.E.R.A.는 NIHNIGMS-R25GM110513에서 제공 하는 원정대에 대 한 감사입니다. 우리는 일반적인 계측 영역의 사용에 대 한 감사와 광학 이미징 시설 RCMI 프로그램의 사용에 대 한 박사 Priscila Sanabria의 원조 G12MD007583 부여. 또한, 우리는 그의 뛰어난 역할을 촬영 하 고 편집 하는 시각적 프로토콜에 대 한 호세 빠 디 야 감사 드립니다.
자료
| Name | Company | Catalog Number | Comments |
| Instruments for Surgery - Step 1 | |||
| Operating scissor 5.5” | Roboz Company | RS-6812 | Tools used to decapitate the rats. |
| Curved forceps 7” | Roboz Company | RS-5271 | Holds the skin of the rat while the skull is removed. |
| Micro-dissecting scissors 4” | Roboz Company | RS-5882 | Cuts both the skin and skull of the rat. |
| Micro-dissecting forceps 4” angled, fine sharp | Roboz Company | RS-5095 | Holds the skin of the rat while the skull is removed. |
| Micro-dissecting forceps 4” slightly curved 0.8 | Roboz Company | RS-5135 | Tool used to separate cortices. |
| Micro-dissecting tweezers | Roboz Company | RS-4972 | Peels brain meninges. |
| Dissection microscope | Olympus | SZX16 | Important for removing the meninge from the cortices. |
| DMEM Preparation - step 2 | |||
| Dulbecco’s Modified Eagle’s Medium (DMEM) | GibCo. Company | 11995-065 | Supports the growth of cells. |
| Sodium bicarbonate | Sigma-Aldrich Company | S7277 | Supplement for the cell culture media. |
| Fetal bovine serum (FBS) | GibCo. Company | 10437-010 | Serum-supplement for the cell culture. |
| Penicillin-Streptomycin | GibCo. Company | 15140-148 | Inhibits the growth of bacterias in the cell culture. |
| Filter System 1L with 0.22um pore | Corning | 431098 | |
| Astrocyte culture - step 3 | |||
| Serological pipets 5mL | VWR | 89130-896 | To pipette DMEM to containers with cells. |
| Serological pipets 10mL | VWR | 89130-898 | To pipette DMEM to containers with cells. |
| Serological pipets 25mL | VWR | 89130-900 | To pipette DMEM to containers with cells. |
| Centrifuge conical tube 15mL | Santa Cruz Biotechnology | sc-200250 | |
| Safe-lock tube 1.5mL | Eppendorf | 022363204 | |
| Barrier Tips 200 uL | Santa Cruz Biotechnology | sc-201725 | |
| Barrier Tips 1 mL | Santa Cruz Biotechnology | sc-201727 | |
| Biohazard Orange Bag 14 x 19" | VWR | 14220-048 | |
| 60mm petri dishes | Falcon | 351007 | |
| Sterile gauze pads | Honeywell Safety | 89133-086 | |
| Stomacher 80 Biomaster | Sewar Lab System | 030010019 | Triturate the brain tissue. |
| Stomacher 80 Blender Sterile Bags | Sewar Lab System | BA6040 | Sterile bag for the stomacher cell homogenizer. |
| Beaker 400mL | Pyrex | 1000 | |
| Sterile cell dissociation sieve, mesh #60 | Sigma-Aldrich Company | S1020 | To obtain a uniform single cell suspension. |
| Sterile cell dissociation sieve, mesh #100 | Sigma-Aldrich Company | S3895 | To obtain a uniform single cell suspension. |
| Invert phase microscope | Nikon | Eclypse Ti-S | Verify cells for contamination or abnormal cell growth. |
| 75cm2 sterile flasks | Falcon | 353136 | |
| Multi-well plate | Falcon | 353046 | |
| Micro cover glasses (coverslips), 18mm, round | VWR | 48380-046 | |
| Bright-Line hemacytometer | Sigma-Aldrich Company | Z359629 | |
| Pasteur pipettes | Fisher Scientific | 13-678-20D | |
| Ethyl alcohol | Sigma-Aldrich Company | E7023 | |
| L-leucine methyl ester hydrochloride 98% (LME) | Sigma-Aldrich Company | L1002 | Promotes the elimination of microglia cells in the primary cortical astrocyte cultutre. |
| Cytosine β-D-arabinofuranoside (Ara-C) | Sigma-Aldrich Company | C1768 | |
| Poly-D-Lysine Hydrobromide, mol wt 70,000-150,000 | Sigma-Aldrich Company | P0899 | |
| Trypsin/EDTA | GibCo. Company | 15400-054 | |
| Trypan Blue | Sigma-Aldrich Company | T8154 | |
| Phosphate buffer saline (PBS) tablets | Calbiochem | 524650 | |
| Sterile Water | Sigma-Aldrich Company | W3500 | |
| OGD Medium Preparation - step 5 | |||
| Centrifuge conical tube 50 mL | VWR | 89039-658 | |
| Dulbecco’s modified Eagle’s medium-free glucose | Sigma-Aldrich Company | D5030 | Supports the growth of cells. |
| Sodium bicarbonate | Sigma-Aldrich Company | S7277 | Supplement for the cell culture media. |
| Penicillin-Streptomycin | GibCo. Company | 15140-148 | Inhibits the growth of bacterias in the cell culture. |
| 200mM L-glutamine | GibCo. Company | 25030-081 | Amino acid that supplements the growth of cells. |
| Phospahet buffer saline (PBS) tablets | Calbiochem | 524650 | |
| Filter System 50mL with 0.22um pore | Corning | 430320 | |
| Centrifuge conical tube 50 mL | VWR | 89039-658 | |
| Single Flow Meter | Billups-Rothenberg | SMF3001 | Measure gas flow in oxygen purge. |
| Hypoxia Incubator Chamber | StemCell | 27310 | Generates a hypoxic environment for the cell culture. |
| Traceable Dissolved Oxygen Meter | VWR | 21800-022 | |
| 95% N2/ 5% CO2 Gas Mixture | Linde | Purges the environment of oxygen. | |
| primary astrocyte immunofluorescence - step 6 | |||
| Phosphate buffer saline (PBS) tablets | Calbiochem | 524650 | |
| Formaline Solution Neutral Buffer 10% | Sigma-Aldrich | HT501128 | Solution used to fix cells. |
| Methanol | Fisher | A4544 | Solution used to fix cells. |
| Non-ionic surfactant (Triton X-100) | Sigma-Aldrich | T8787 | |
| Fetal bovine serum (FBS) | GibCo. Company | 10437-010 | Serum-supplement for the cell culture. |
| Anti-NeuN | Cell Signaling | 24307 | Detects mature neurons, serves to validate the astrocytic culture. |
| Anti-PCNA | Cell Signaling | 2586 | Detects proliferating cells. |
| Propidium Iodide (PI) | Sigma-Aldrich Company | P4170 | Apoptosis staining. |
| Anti-Olig1 | Abcam | AB68105 | Detects mature oligodendrocytes. |
| Anti-Iba1+ | Wako | 016-20001 | Detects microglial cells. |
| Anti-GFAP Conjugated with Cy3 | Sigma-Aldrich Company | C9205 | Detects reactive astrocytes in the treated cells. |
| Alexa Fluor 488 | Molecular Probe Life Technology | A1101 | Anti-Mouse Secondary Antibody |
| Alexa Fluor 555 | Molecular Probe Life Technology | A21428 | Anti-Rabbit Secondary Antibody |
| 4’,6’-diamidino-2-phenylindole (DAPI) | Sigma-Aldrich Company | D9542 | Nuclear staining |
| Confocal microscope | Olympus |
참고문헌
- Goldstein, L. B., Bertels, C., Davis, J. N. Interrater reliability of the NIH stroke scale. Arch Neurol. 46 (6), 660-662 (1989).
- Hinkle, J. L., Guanci, M. M. Acute ischemic stroke review. J Neurosci Nurs. 39 (5), 285-293 (2007).
- Kassner, A., Merali, Z. Assessment of Blood-Brain Barrier Disruption in Stroke. Stroke. 46 (11), 3310-3315 (2015).
- Moskowitz, M. A., Lo, E. H., Iadecola, C. The science of stroke: mechanisms in search of treatments. Neuron. 67 (2), 181-198 (2010).
- Ben Haim, L., Carrillo-de Sauvage, M. A., Ceyzeriat, K., Escartin, C. Elusive roles for reactive astrocytes in neurodegenerative diseases. Front Cell Neurosci. 9, 278 (2015).
- Broderick, J., et al. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage in Adults 2007 Update: A Guideline From the American Heart Association/American Stroke Association Stroke Council, High Blood Pressure Research Council, and the Quality of Care and Outcomes in Research Interdisciplinary Working Group: The American Academy of Neurology affirms the value of this guideline as an educational tool for neurologists. Stroke. 38 (6), 2001-2023 (2007).
- Wang, R., et al. Oxygen-glucose deprivation induced glial scar-like change in astrocytes. PLoS One. 7 (5), e37574 (2012).
- Sofroniew, M. V. Reactive astrocytes in neural repair and protection. The Neuroscientist. 11 (5), 400-407 (2005).
- Sofroniew, M. V., Vinters, H. V. Astrocytes: biology and pathology. Acta neuropathologica. 119 (1), 7-35 (2010).
- Souza, D. G., Bellaver, B., Souza, D. O., Quincozes-Santos, A. Characterization of adult rat astrocyte cultures. PLoS One. 8 (3), e60282 (2013).
- Puschmann, T. B., et al. HB-EGF affects astrocyte morphology, proliferation, differentiation, and the expression of intermediate filament proteins. J Neurochem. 128 (6), 878-889 (2014).
- Robinson, C., Apgar, C., Shapiro, L. A. Astrocyte Hypertrophy Contributes to Aberrant Neurogenesis after Traumatic Brain Injury. Neural Plast. , 1347987 (2016).
- Brekke, E., Berger, H. R., Wideroe, M., Sonnewald, U., Morken, T. S. Glucose and Intermediary Metabolism and Astrocyte-Neuron Interactions Following Neonatal Hypoxia-Ischemia in Rat. Neurochem Res. , (2016).
- Cekanaviciute, E., et al. Astrocytic transforming growth factor-beta signaling reduces subacute neuroinflammation after stroke in mice. Glia. 62 (8), 1227-1240 (2014).
- Zhu, Z., et al. Inhibiting cell cycle progression reduces reactive astrogliosis initiated by scratch injury in vitro and by cerebral ischemia in vivo. Glia. 55 (5), 546-558 (2007).
- Bovolenta, P., Wandosell, F., Nieto-Sampedro, M. Neurite outgrowth over resting and reactive astrocytes. Restor Neurol Neurosci. 2 (4), 221-228 (1991).
- Anderson, M. A., et al. Astrocyte scar formation aids central nervous system axon regeneration. Nature. 532 (7598), 195-200 (2016).
- Hao, C., Richardson, A., Fedoroff, S. Macrophage-like cells originate from neuroepithelium in culture: characterization and properties of the macrophage-like cells. Int J Dev Neurosci. 9 (1), 1-14 (1991).
- Saura, J. Microglial cells in astroglial cultures: a cautionary note. J Neuroinflammation. 4, 26 (2007).
- Giulian, D., Baker, T. J. Characterization of ameboid microglia isolated from developing mammalian brain. J Neurosci. 6 (8), 2163-2178 (1986).
- Schildge, S., Bohrer, C., Beck, K., Schachtrup, C. Isolation and culture of mouse cortical astrocytes. J Vis Exp. (71), (2013).
- Armstrong, R. C. Isolation and characterization of immature oligodendrocyte lineage cells. Methods. 16 (3), 282-292 (1998).
- McCarthy, K. D., de Vellis, J. Preparation of separate astroglial and oligodendroglial cell cultures from rat cerebral tissue. J Cell Biol. 85 (3), 890-902 (1980).
- Pont-Lezica, L., Colasse, S., Bessis, A. Depletion of microglia from primary cellular cultures. Methods Mol Biol. 1041, 55-61 (2013).
- Svensson, M., Aldskogius, H. Synaptic density of axotomized hypoglossal motorneurons following pharmacological blockade of the microglial cell proliferation. Exp Neurol. 120 (1), 123-131 (1993).
- Wong, V. K., Shapourifar-Tehrani, S., Kitada, S., Choo, P. H., Lee, D. A. Inhibition of rabbit ocular fibroblast proliferation by 5-fluorouracil and cytosine arabinoside. J Ocul Pharmacol. 7 (1), 27-39 (1991).
- Nakatsuji, Y., Miller, R. H. Density dependent modulation of cell cycle protein expression in astrocytes. J Neurosci Res. 66 (3), 487-496 (2001).
- Reeves, J. P. Accumulation of amino acids by lysosomes incubated with amino acid methyl esters. J Biol Chem. 254 (18), 8914-8921 (1979).
- Thiele, D. L., Kurosaka, M., Lipsky, P. E. Phenotype of the accessory cell necessary for mitogen-stimulated T and B cell responses in human peripheral blood: delineation by its sensitivity to the lysosomotropic agent, L-leucine methyl ester. J Immunol. 131 (5), 2282-2290 (1983).
- Hamby, M. E., Uliasz, T. F., Hewett, S. J., Hewett, J. A. Characterization of an improved procedure for the removal of microglia from confluent monolayers of primary astrocytes. J Neurosci Methods. 150 (1), 128-137 (2006).
- Corvalan, V., Cole, R., de Vellis, J., Hagiwara, S. Neuronal modulation of calcium channel activity in cultured rat astrocytes. Proc Natl Acad Sci U S A. 87 (11), 4345-4348 (1990).
- Butler, I. B., Schoonen, M. A., Rickard, D. T. Removal of dissolved oxygen from water: A comparison of four common techniques. Talanta. 41 (2), 211-215 (1994).
- Tasca, C. I., Dal-Cim, T., Cimarosti, H. In vitro oxygen-glucose deprivation to study ischemic cell death. Methods Mol Biol. 1254, 197-210 (2015).
- Wu, D., Yotnda, P. Induction and testing of hypoxia in cell culture. J Vis Exp. (54), (2011).
- Rivera-Aponte, D., et al. Hyperglycemia reduces functional expression of astrocytic Kir4. 1 channels and glial glutamate uptake. Neuroscience. 310, 216-223 (2015).
- Berger, R., Garnier, Y., Pfeiffer, D., Jensen, A. Lipopolysaccharides do not alter metabolic disturbances in hippocampal slices of fetal guinea pigs after oxygen-glucose deprivation. Pediatric research. 48 (4), 531-535 (2000).
- Anderson, T. R., Jarvis, C. R., Biedermann, A. J., Molnar, C., Andrew, R. D. Blocking the anoxic depolarization protects without functional compromise following simulated stroke in cortical brain slices. Journal of neurophysiology. 93 (2), 963-979 (2005).
- Jarvis, C. R., Anderson, T. R., Andrew, R. D. Anoxic depolarization mediates acute damage independent of glutamate in neocortical brain slices. Cerebral Cortex. 11 (3), 249-259 (2001).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유