Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Multi-Fiber Photometrie zur Aufzeichnung neuronaler Aktivität bei frei beweglichen Tieren
In diesem Artikel
Zusammenfassung
In diesem Protokoll wird erläutert, wie Multifaserphotometrieaufzeichnungen implementiert und durchgeführt werden, wie Kalzium-unabhängige Artefakte korrigiert werden und wie wichtige Überlegungen für die duale Photometrie-Bildgebung berücksichtigt werden.
Zusammenfassung
Die Aufzeichnung der Aktivität einer Gruppe von Neuronen in einem frei beweglichen Tier ist ein schwieriges Unterfangen. Darüber hinaus wird es, da das Gehirn in kleinere und kleinere funktionelle Untergruppen zerlegt wird, von größter Bedeutung, aus Projektionen und/oder genetisch definierten Subpopulationen von Neuronen aufzuzeichnen. Fiber-Photometrie ist ein zugänglicher und leistungsstarker Ansatz, der diese Herausforderungen bewältigen kann. Durch die Kombination optischer und genetischer Methoden kann die neuronale Aktivität in tiefen Gehirnstrukturen gemessen werden, indem genetisch kodierte Kalziumindikatoren exexzessiert werden, die die neuronale Aktivität in ein optisches Signal übersetzen, das leicht messbar ist. Das aktuelle Protokoll beschreibt die Komponenten eines Multifaser-Photometriesystems, wie man auf tiefe Gehirnstrukturen zugreift, um Licht zu liefern und zu sammeln, eine Methode, um Bewegungsartefakte zu berücksichtigen, und wie fluoreszierende Signale verarbeitet und analysiert werden. Das Protokoll beschreibt experimentelle Überlegungen bei der Durchführung von Einzel- und Dual-Farb-Bildgebung, entweder aus einzelnen oder mehreren implantierten Optischen Fasern.
Einleitung
Die Fähigkeit, neuronale Reaktionen mit bestimmten Aspekten des Verhaltens eines Tieres zu korrelieren, ist entscheidend, um die Rolle zu verstehen, die eine bestimmte Gruppe von Neuronen bei der Leitung oder Reaktion auf eine Handlung oder einen Reiz spielt. Angesichts der Komplexität des Verhaltens von Tieren, mit den unzähligen inneren Zuständen und äußeren Reizen, die selbst die einfachsten Aktionen beeinflussen können, rüstet die Aufzeichnung eines Signals mit Einer-Versuchs-Auflösung die Forscher mit den notwendigen Werkzeugen aus, um diese zu überwinden. Einschränkungen.
Die Faserphotometrie ist für viele Forscher auf dem Gebiet der Systemneurowissenschaften aufgrund ihrer relativen Einfachheit im Vergleich zu anderen In-vivo-Aufnahmetechniken, ihrem hohen Signal-Rausch-Verhältnis und der Fähigkeit, in einer Vielzahl von Verhaltensparadigmen1,2,3,4,5,6,7,8. Im Gegensatz zu herkömmlichen elektrophysiologischen Methoden ist die Photometrie der optische Ansatz, der am häufigsten in Verbindung mit genetisch kodierten Calciumindikatoren (GECIs, gCaMP-Serie)9verwendet wird. GECIs ändern ihre Fluoreszenzfähigkeit, je nach, ob sie an Kalzium gebunden sind oder nicht. Da die innere Konzentration von Kalzium in Neuronen sehr streng reguliert ist und spannungsgebundene Kalziumkanäle sich öffnen, wenn ein Neuron ein Aktionspotential abfeuert, erhöht sich die innere Kalziumkonzentration vorübergehend, was zu vorübergehenden Fähigkeit eines GECI zur Fluoreszenz, kann ein guter Proxy für neuronaleFeuerung 9sein.
Mit der Faserphotometrie wird das Anregungslicht eine dünne Multimode-Optikfaser ins Gehirn geleitet, und ein Emissionssignal wird durch dieselbe Faser wieder nach oben gesammelt. Da diese Glasfasern leicht und biegsam sind, kann sich ein Tier weitgehend ungehindert bewegen, was diese Technik mit einer Vielzahl von Verhaltenstests und -bedingungen kompatibel macht. Einige Bedingungen, wie schnelle Bewegungen oder das Biegen des Glasfaser-Patchkabels über den Radius hinaus, in dem es die gesamte interne Reflexion aufrechterhalten kann, können Signalartefakte einführen. Um Signalvon Rauschen zu verkennen, können wir eine Eigenschaft von GCaMP ausnutzen, die als "isosbestic point" bekannt ist. Kurz gesagt, mit GCaMP, da die Wellenlänge des Anregungslichts nach links verschoben wird, nimmt seine Emission im kalziumgebundenen Zustand ab und die Emission im Kalzium-ungebundenen Zustand nimmt geringfügig zu. Der Punkt, an dem die relative Intensität dieser beiden Emissionen gleich ist, wird als isosbestischer Punkt bezeichnet. Wenn GCaMP an dieser Stelle angeregt wird, wird seine Emission nicht durch Veränderungen der inneren Kalziumkonzentrationen beeinflusst, und die Varianz des Signals ist am häufigsten auf die Dämpfung des Signals durch Überbiegung des Glasfaser-Patchkabels oder die Bewegung des Neuronalgewebes zurückzuführen. relativ zur implantierten Faser.
Die Ein-Einheiten-Elektrophysiologie ist aufgrund ihrer einzelligen und Single-Spike-Level-Auflösung nach wie vor der Goldstandard für frei bewegliche In-vivo-Aufnahmen. Es kann jedoch schwierig sein, die molekulare Identität der zellen zu bestimmen, die aufgezeichnet werden, und die Post-hoc-Analyse kann ziemlich mühsam sein. Faserphotometrie hat zwar keine einzellige Auflösung, ermöglicht es Forschern jedoch, Fragen zu stellen, die mit herkömmlichen Techniken nicht angegangen werden können. Durch die Kombination viraler Strategien mit transgenen Tieren kann die Expression von GECIs auf genetisch definierte neuronale Typen gerichtet werden, um populations- oder projektionsdefinierte neuronale Aktivität aufzuzeichnen, die durch die Überwachung des Calciumsignals direkt am Axon durchgeführt werden kann. Klemmen10,11. Darüber hinaus ist es durch die Implantation mehrerer faseroptischer Kanülen möglich, die neuronale Aktivität aus mehreren Hirnregionen und -wegen im selben Tier gleichzeitig zu überwachen12,13.
In diesem Manuskript beschreiben wir eine Technik für Einzel- und Multifaserphotometrie, wie man kalziumunabhängige Artefakte korrigiert und detailliert beschreibt, wie man mono- und dualfarbene Aufnahmen durchführt. Wir bieten auch Beispiele für die Arten von Fragen, die man stellen kann, und deren zunehmende Komplexität (siehe Abbildung 1). Das Faserphotometrie-Setup für Multifaseraufzeichnungen, die in diesem Protokoll detailliert sind, kann mithilfe einer Liste von Materialien erstellt werden, die unter https://sites.google.com/view/multifp/hardware (Abbildung 2) zu finden sind.
Es ist wichtig, dass das System sowohl für 410 nm als auch für 470 nm Anregungswellenlängen für kalziumunabhängige und kalziumabhängige Fluoreszenzemissionen aus GCaMP6 oder seinen Varianten ausgestattet ist. Für kundenspezifische Setups oder wenn keine Software zum Ausführen des Systems verfügbar ist, kann das kostenlose Open-Source-Programm Bonsai (http://www.open-ephys.org/bonsai/) verwendet werden. Alternativ kann die Faserphotometrie über MATLAB (z.B. https://github.com/deisseroth-lab/multifiber)12 oder eine andere Programmiersprache14ausgeführt werden. Die Software und Hardware des Systems sollte die Manipulation der 410 nm und 470 nm LEDs und der Kamera, die Extraktion von Bildern (Abbildung 2), und die Berechnung der mittleren Fluoreszenzintensität in den Bereichen von Interesse (ROIs) um die Fasern auf die Bilder. Der Ausgang sollte eine Tabelle mit mittleren Intensitätswerten sein, die mit den LEDs 470 nm und 410 nm von jeder Faser im Patchkabel aufgezeichnet werden. Bei Multifaserexperimenten können gebündelte Fasern mit 400 m die Bewegung von Mäusen einschränken. In solchen Fällen empfehlen wir die Verwendung von 200 m Patchkabeln, die mehr Flexibilität bieten. Es kann auch möglich sein, kleinere Dummy-Kabel während des Trainings von Mäusen zu verwenden.
Es ist entscheidend, in der Lage zu sein, Zeitpunkte für Ereignisse von Interesse während der Faserphotometrie-Erfassung zu extrahieren. Wenn das System nicht ohne weiteres ein integriertes System zur Integration von TTLs für bestimmte Ereignisse bereitstellt, besteht eine alternative Strategie darin, einzelnen aufgezeichneten Zeitpunkten einen Zeitstempel zuzuweisen, um sich an bestimmten Zeiten und Ereignissen während des Experiments auszurichten. Die Zeitstempelung kann mit der Computeruhr erfolgen.
Protokoll
Alle Experimente wurden in Übereinstimmung mit den Institutional Animal Care and Use Committees der University of California, San Diego, und dem Canadian Guide for the Care and Use of Laboratory Animals durchgeführt und von der Université Laval Animal Protection genehmigt. ausschuß.
1. Ausrichtung des optischen Pfades zwischen der CMOS-Kamera (komplementärer Metalloxid-Halbleiter) und dem einzelnen oder verzweigten Patchkabel
- Lösen Sie alle Schrauben am 5-Achsen-Übersetzer (11, Abbildung 2B).
- Schrauben Sie das Patchkabel (12, Abbildung 2B) an den Adapter [SMA (Subminiatur A) oder FC (Faseroptikstecker)] ein, der am 5-Achsen-Übersetzer befestigt ist.
- Schalten Sie das 470 nm Anregungslicht (1, Abbildung 2B) bei geringer Leistung (100 W) ein und platzieren Sie die Spitze des Patchcords, das auf einen autofluoreszierenden Kunststoffschlitten zeigt. Dies hat keinen Einfluss auf zukünftige Aufnahmen, sondern dient ausschließlich der Visualisierung des Ausrichtungsprozesses.
- Aufnahme von der CMOS-Kamera (13, Abbildung 2B) im Live-Modus. Erhöhen Sie die Verstärkung oder passen Sie die Suchtabelle (LUT) an, bis das Bild nicht vollständig schwarz ist. Es geht darum, ein Bild im Mittelpunkt des Ziels zu sehen (10, Abbildung 2B).
- Bringen Sie den 5-Achsen-Übersetzer auf das Ziel zu, um sicherzustellen, dass das 470 nm Licht auf der Faser am SMA- oder FC-Ende des Patchkabels zentriert ist, bis ein Bild auf der Kamera aufgelöst werden kann.
- Passen Sie die X- und Y-Achsen an, bis das Bild zentriert und gut aufgelöst ist.
- Visualisieren Sie das Licht, das vom Ferrule-Ende des Patchkabels ausgesendet wird. Es sollte als isotrope Kreis erscheinen. Wenn ein verzweigendes Patchkabel verwendet wird, sollte die Menge an Licht, das an den Ferrule-Enden jedes Patchkabels emittiert wird, ähnlich sein. Wenn der Kreis nicht isottrop ist oder das emittierte Licht ungleich ist, stellen Sie den 5-Achsen-Übersetzer in der X-Y-Achse ein.
2. Einrichtung von ROIs um Fasern zur Messung der mittleren Fluoreszenzintensität
- Schalten Sie alle Anregungsleuchten ein, um die Fasern besser zu visualisieren. Passen Sie die Kameraverstärkung so an, dass keine Pixel gesättigt sind und ein klares Bild der Fasern vorhanden ist.
- Live-Aufnahme oder nehmen Sie ein vorläufiges Bild.
- Zeichnen Sie ROIs um die Fasern und halten Sie sie für die Messung der mittleren Intensitätswerte während der Aufnahmen(Abbildung 2A).
- Testen Sie bei mehreren Faseraufzeichnungen die Unabhängigkeit in Signalen.
- Live-Rekord aus allen Fasern.
- Zeigen Sie eine Faser auf eine Lichtquelle und tippen Sie mit einem Finger. Sehr große Schwankungen sollten nur in diesem Kanal auftreten (akzeptable Leckage 1:1000).
- Wenn die Signale nicht unabhängig sind, zeichnen Sie konservativere ROIs neu und wiederholen Sie den Unabhängigkeitstest.
- Um zu beschriften und zu verfolgen, welcher ROI entspricht, welche Faser, farbiges Klebeband oder Nagellack am Ende der Fasern aufgetragen werden kann. Nehmen Sie ein Bild vor dem Start eines Experiments als sekundäre Erinnerung auf.
3. Einrichtung der Aufnahmearena
- Hängen Sie das Patchkabel über der Arena mit Ständern, Klammern oder Halterungen.
- Stellen Sie sicher, dass sich das Tier ungehindert durch die gesamte Arena bewegen kann, ungehindert durch die Länge der Faser.
- Unabhängig davon, ob eine Operantbox oder ein offenes Feld verwendet wird, stellen Sie sicher, dass das Patchkabel in der Lage ist, das Tier mit minimaler Biegung zu erreichen. Wenn dies einen Nasensack erfordert, stellen Sie sicher, dass genügend Platz über dem Kopf vorhanden ist, um eine Beugung der Faser zu verhindern. Vermeiden Sie übermäßiges Biegen oder Verdrehen des Patchkabels.
4. In-vivo-Aufnahmen
HINWEIS: Das Verfahren der optischen Kanülenimplantation für Faserphotometrieexperimente ist identisch mit dem Verfahren für die Optogenetik, wie in Sparta et al15beschrieben. Wir empfehlen die Verwendung von Zahnzement (siehe Tabelle der Materialien), der eine robuste Verankerung der Kopfkappe am Schädelknochen ermöglicht. Dentalzement ist besonders nützlich, wenn Verankerungsschrauben nicht verwendet werden können.
- Überprüfen Sie visuell das distale Ende der Fasern der Patchschnur per Auge und mit einem Minifasermikroskop. Wenn die Oberfläche der Fasern zerkratzt ist, polieren Sie die Fasern mit Faserpol-/Lappenfolie mit feinem Körnung (1 m und 0,3 m).
- Reinigen Sie die distalen Enden des Patchkabels mit 70% Ethanol und einem Baumwollspitzenapplikator.
- Reinigen Sie die faseroptischen Kanülen mit 70% Ethanol und einem Baumwollspitzenapplikator.
- Verbinden Sie das Ferrule-Ende des Patchkabels mit der implantierten Faser mit einer Keramik-Split-Sleeve mit einem schwarzen Schrumpfrohr bedeckt. Achten Sie während des Anschlusses darauf, dass die Hülse fest ist, ansonsten eine neue Hülse verwenden.
HINWEIS: Es wird eine große Menge an Signalverlust, wenn es einen Platz zwischen dem Patch-Kabel Ferrule und dem Implantat, und die Aufnahmen werden nicht funktionieren. - Lassen Sie das Tier einige Minuten vor Beginn der Verhaltenstests erholen.
- Starten Sie die Aufzeichnung des optischen Signals und führen Sie das Experiment aus.
- Behalten Sie während der Aufnahme die Live-Trace sorgfältig im Auge, um qualitativ hochwertige Aufnahmen zu gewährleisten. Es wird erwartet, dass das Signal in den ersten 2 min der Aufnahme als Funktion der Zeit schnell abnimmt. Dieser Effekt wird durch wärmevermittelten LED-Zerfall verursacht, wodurch die Wärmezunahme den Widerstand des optischen Elements erhöht.
- Wenn ein Sprung in das Signal auftritt, das die Ein-/Aus-Kinetik von GCaMP überschreitet, ist dies oft ein Hinweis darauf, dass die Hülse nicht eng genug ist und sich der Abstand zwischen patch cord und dem Implantat ändert. In diesem Fall stoppen Sie das Experiment und verbinden Sie das Tier mit einer neuen Hülse wieder.
5. Fiberphotometrie Datenanalyse
HINWEIS: Dies ist eine Methode zur Datenanalyse, die für die meisten Aufzeichnungen gut funktioniert. Es können jedoch alternative Ansätze umgesetzt werden. Beispielcode für die Datenanalyse finden Sie hier: https://github.com/katemartian/Photometry_data_processing.
- Extrahieren Sie mittlere Fluoreszenzintensitätswerte, die von 470 nm (Int470) und 410 nm (Int410) LEDs aufgezeichnet wurden, entsprechend jeder einzelnen Faser.
- Glätten Sie jedes Signal mit einem beweglichen Mittelwertalgorithmus (Abbildung 3A).
- Führen Sie die Basiskorrektur jedes Signals(Abbildung 3A und 3B) mit dem adaptiven iterativ neu gewichteten Penalized Least Squares (airPLS) Algorithmus (https://github.com/zmzhang/airPLS airPLS) durch, um die Steigung und die niedrige Frequenz zu entfernen. Schwankungen der Signale.
- Standardisieren Sie jedes Signal mit dem Mittelwert und der Standardabweichung(Abbildung 3C):
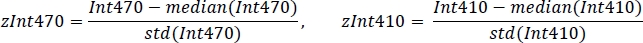
- Mit nicht-negativen robusten linearen Regression, passen standardisierte zInt410 bis zInt470 Signale (Abbildung 3D) an die Regressionsfunktion:
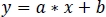
- Verwenden Sie die Parameter der linearen Regression (a, b), um neue Werte von zInt410 zu finden, die an zInt470 (fitInt410, Abbildung 3D,E) angepasst sind:
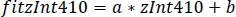
- Verwenden Sie die Parameter der linearen Regression (a, b), um neue Werte von zInt410 zu finden, die an zInt470 (fitInt410, Abbildung 3D,E) angepasst sind:
- Berechnen Sie die normalisierte dF/F (z dF/F) (Abbildung 3F):
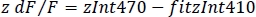
6. Gleichzeitige duale Aufnahmen
- Fügen Sie dem Photometriesystem eine 560 nm LED hinzu, um den roten fluoreszierenden Kalziumsensor und die entsprechenden dichroitischen Spiegel und Filter zu erregen (siehe Kim et al., 2016 für eine detaillierte Beschreibung)12.
- Fügen Sie einen Bildspalter zwischen dem Objektiv und der CMOS-Kamera hinzu, um die grünen und roten Emissionswellenlängen zu trennen (siehe Abbildung 5). Der Bildteiler bildet zwei gespiegelte Bilder auf dem Kamerasensor, entsprechend den roten und grünen Signalen (z. B. erzeugt ein Patchkabel mit 3 Zweigen ein Bild mit 6 Fasern).
- Zeichnen Sie ROIs um alle Fasern in beiden Farben, wie oben beschrieben. Achten Sie darauf, jeden ROI mit der entsprechenden Faser und dem entsprechenden Kanal (grün und rot) eindeutig zu identifizieren (Abbildung 4A).
- Lösen Sie die gleichzeitige Anregung mit 470 nm und 560 nm LEDs aus und wechseln Sie sie mit 410 nm LED ab (Abbildung 5A).
7. Duale Farbdatenanalyse
- Folgen Sie den Schritten in Abschnitt 5, um fitInt410 für das Int470 Signal zu finden und z dF/Fzu berechnen.
- Da der isosbestische Punkt für rot versetzte GECIs in der Regel unbekannt ist, kann das mit 410 nm LED im grünen Kanal aufgezeichnete Signal zur Bewegungskorrektur über beide Kanäle hinweg verwendet werden. Folgen Sie den Schritten in Abschnitt 5, um fitInt410 für das Int560 Signal zu finden und z dF/Fzu berechnen.
Ergebnisse
Neuronale Korrelationen von Verhaltensreaktionen können je nach einer Vielzahl von Faktoren variieren. In diesem Beispiel haben wir die In-vivo-Faserphotometrie verwendet, um die Aktivität von Axonklemmen aus dem lateralen hypothalamischen Bereich (LHA) zu messen, die in der lateralen Hatula (LHb) enden. Wildtyp-Mäuse wurden mit einem Adeno-assoziierten Virus (AAV) injiziert, das GCaMP6s (AAV-hSyn-GCaMP6s) in die LHA kodiert, und eine Optische Faser wurde mit der Spitze unmittelbar über dem LHb implantiert (
Diskussion
Die Faserphotometrie ist ein zugänglicher Ansatz, der es Forschern ermöglicht, Massenkalzium-Dynamiken von definierten neuronalen Populationen bei frei beweglichen Tieren aufzuzeichnen. Diese Methode kann mit einer Vielzahl von Verhaltenstests kombiniert werden, einschließlich "bewegungslastige" Aufgaben wie erzwungene Schwimmtests2, Angstkonditionierung18, soziale Interaktionen1,4und andere7 ,<...
Offenlegungen
Sage Aronson ist CEO und Gründer von Neurophotometrics Ltd., die Multifaser-Photometriesysteme vertreibt.
Danksagungen
Diese Arbeit wurde durch ein Stipendium des Natural Sciences and Engineering Research Council of Canada (NSERC: RGPIN-2017-06131) an C.P. C. P. unterstützt. Wir danken auch dem Plateforme d'Outils Moléculaires (https://www.neurophotonics.ca/fr/pom) für die Herstellung der in dieser Studie verwendeten viralen Vektoren.
Materialien
| Name | Company | Catalog Number | Comments |
| 1/4"-20 Stainless Steel Cap Screw, 1" Long | Thorlabs | SH25S100 | |
| 1/4"-20 Stainless Steel Cap Screw, 1/2" Long | Thorlabs | SH25S050 | |
| 1/4"-20 Stainless Steel Cap Screw, 3/8" Long | Thorlabs | SH25S038 | |
| 1000 µm, 0.50 NA, SMA-SMA Fiber Patch Cable | Thorlabs | M59L01 | |
| 12.7 mm Optical Post | Thorlabs | TR30/M | |
| 12.7 mm Pedestal Post Holder | Thorlabs | PH20EM | |
| 15 V, 2.4 A Power Supply Unit with 3.5 mm Jack Connector for T-Cube | Thorlabs | KPS101 | |
| 20x objective | Thorlabs | RMS20X | #10 in Figure 2, #11 in Figure 5 |
| 30 mm Cage Cube with Dichroic Filter Mount | Thorlabs | CM1-DCH/M | #8-9 in Figure 2, #8-10 in Figure 5 |
| 405 nm LED | Doric Lenses | CLED_405 | #2 in Figure 2 |
| 410 nm bandpass filter | Thorlabs | FB410-10 | #5 in Figure 2; #7 in Figure 5 |
| 465 nm. LED | Doric Lenses | CLED_465 | #1 in Figure 2 |
| 470 nm bandpass filter | Thorlabs | FB470-10 | #4 in Figure 2; #6 in Figure 5 |
| 560 nm bandpass filter | Semrock | FF01-560/14-25 | #5 in Figure 5 |
| 560 nm LED | Doric Lenses | CLED_560 | #1 in Figure 3 |
| 5-axis kinematic Mount | Thorlabs | K5X1 | #11 in Figure 2, #12 in Figure 5 |
| Achromatic Doublet | Thorlabs | AC254-035-A-ML | #7 in Figure 2 |
| Adaptor for 405 collimator | Thorlabs | AD11F | #3 in Figure 2; #4 in Figure 5 |
| Adaptor for ajustable collimator | Thorlabs | AD127-F | #3 in Figure 2; #4 in Figure 5 |
| Aluminum Breadboard | Thorlabs | MB1824 | |
| Clamping Fork | Thorlabs | CF125 | |
| Cube connector | Thorlabs | CM1-CC | |
| Dual 493/574 dichroic | Semrock | FF493/574-Di01-25x36 | #10 in Figure 5 |
| Emission filter for GCaMP6 | Semrock | FF01-535/22-25 | #6 in Figure 2 |
| Enclosure with Black Hardboard Panels | Thorlabs | XE25C9 | |
| Externally SM1-Threaded End Cap for Machining | Thorlabs | SM1CP2M | |
| Fast-change SM1 Lens Tube Filter Holder | Thorlabs | SM1QP | #4-6 in Figure 2, #5-7 in Figure 5 |
| Fixed Collimator for 405 nm light | Thorlabs | F671SMA-405 | #3 in Figure 2; #4 in Figure 5 |
| Fixed collimator for 470 and 560 nm light | Thorlabs | F240SMA-532 | #3 in Figure 2; #4 in Figure 5 |
| Green emission filter | Semrock | FF01-520/35-25 | In light beam splitter |
| High-Resolution USB 3.0 CMOS Camera | Thorlabs | DCC3260M | #13 in Figure 2, #15 in Figure 5 |
| Light beam splitter | Neurophotometrics | SPLIT | #14 in Figure 5 |
| Longpass Dichroic Mirror, 425 nm Cutoff | Thorlabs | DMLP425R | #8 in Figure 2, #9 in Figure 5 |
| Longpass Dichroic Mirror, 495 nm Cutoff | Semrock | FF495-Di03 | #9 in Figure 2, #8 in Figure 5 |
| Metabond dental cement | C&B | ||
| M8 - M8 cable | Doric Lenses | Cable_M8-M8 | |
| Optic fiber cannulas | Doric Lenses | Need to specify that these will be used to photometry experiments requiring low autofluorescence | |
| Optic fiber Patchcords | Doric Lenses | Need to specify that these will be used to photometry experiments requiring low autofluorescence | |
| Red emission filter | Semrock | FF01-600/37-25 | In light beam splitter |
| T7 LabJack | LabJack | ||
| T-cube LED Driver | Thorlabs | LEDD1B | |
| USB 3.0 I/O Cable, Hirose 25, for DCC3240 | Thorlabs | CAB-DCU-T3 |
Referenzen
- Gunaydin, L. A., et al. Natural Neural Projection Dynamics Underlying Social Behavior. Cell. 157 (7), 1535-1551 (2014).
- Proulx, C. D., et al. A neural pathway controlling motivation to exert effort. Proceedings of the National Academy of Sciences of the United States of America. 115 (22), 5792-5797 (2018).
- Muir, J., et al. In Vivo Fiber Photometry Reveals Signature of Future Stress Susceptibility in Nucleus Accumbens. Neuropsychopharmacology. 43 (2), 255-263 (2017).
- Wang, D., et al. Learning shapes the aversion and reward responses of lateral habenula neurons. eLife. 6, (2017).
- de Jong, J. W., et al. A Neural Circuit Mechanism for Encoding Aversive Stimuli in the Mesolimbic Dopamine System. Neuron. 101 (1), 133-151 (2018).
- Lerner, T. N., et al. Intact-Brain Analyses Reveal Distinct Information Carried by SNc Dopamine Subcircuits. Cell. 162 (3), 635-647 (2015).
- Calipari, E. S., et al. In vivo imaging identifies temporal signature of D1 and D2 medium spiny neurons in cocaine reward. Proceedings of the National Academy of Sciences of the United States of America. 113 (10), 2726-2731 (2016).
- González, A. J., et al. Inhibitory Interplay between Orexin Neurons and Eating. Current Biology. 26 (18), 2486-2491 (2016).
- Chen, T. -. W., et al. Ultrasensitive fluorescent proteins for imaging neuronal activity. Nature. 499 (7458), 295-300 (2013).
- Barker, D. J., et al. Lateral Preoptic Control of the Lateral Habenula through Convergent Glutamate and GABA Transmission. Cell Reports. 21 (7), 1757-1769 (2017).
- Siciliano, C. A., Tye, K. M. Leveraging calcium imaging to illuminate circuit dysfunction in addiction. Alcohol. 74, 47-63 (2018).
- Kim, C. K., et al. Simultaneous fast measurement of circuit dynamics at multiple sites across the mammalian brain. Nature Methods. 13 (4), 325-328 (2016).
- Sych, Y., Chernysheva, M., Sumanovski, L. T., Helmchen, F. High-density multi-fiber photometry for studying large-scale brain circuit dynamics. Nature Methods. 16 (6), 553-560 (2019).
- Akam, T., Walton, M. E. pyPhotometry: Open source Python based hardware and software for fiber photometry data acquisition. Scientific Reports. 9 (1), 3521 (2019).
- Sparta, D. R., et al. Construction of implantable optical fibers for long-term optogenetic manipulation of neural circuits. Nature Protocol. 7 (1), 12-23 (2011).
- Stamatakis, A. M., et al. Lateral Hypothalamic Area Glutamatergic Neurons and Their Projections to the Lateral Habenula Regulate Feeding and Reward. The Journal of Neuroscience. 36 (2), 302-311 (2016).
- Tervo, G. D., et al. A Designer AAV Variant Permits Efficient Retrograde Access to Projection Neurons. Neuron. 92 (2), 372-382 (2016).
- Yu, K., da Silva, P., Albeanu, D. F., Li, B. Central Amygdala Somatostatin Neurons Gate Passive and Active Defensive Behaviors. The Journal of Neuroscience. 36 (24), 6488-6496 (2016).
- Falkner, A. L., Grosenick, L., Davidson, T. J., Deisseroth, K., Lin, D. Hypothalamic control of male aggression-seeking behavior. Nature Neuroscience. 19 (4), 596-604 (2016).
- Ren, J., et al. Anatomically Defined and Functionally Distinct Dorsal Raphe Serotonin Sub-systems. Cell. 175 (2), 472-487 (2018).
- Barnett, L. M., Hughes, T. E., Drobizhev, M. Deciphering the molecular mechanism responsible for GCaMP6m’s Ca2+-dependent change in fluorescence. PLOS ONE. 12 (2), 0170934 (2017).
- Sun, F., et al. A Genetically Encoded Fluorescent Sensor Enables Rapid and Specific Detection of Dopamine in Flies, Fish, and Mice. Cell. 174 (2), 481-496 (2018).
- Patriarchi, T., et al. Ultrafast neuronal imaging of dopamine dynamics with designed genetically encoded sensors. Science. 360 (6396), (2018).
- Feng, J., et al. A Genetically Encoded Fluorescent Sensor for Rapid and Specific In Detection of Norepinephrine. Neuron. 102 (4), 745-761 (2019).
- Akerboom, J., et al. Genetically encoded calcium indicators for multi-color neural activity imaging and combination with optogenetics. Frontiers in Molecular Neuroscience. 6, 1-29 (2013).
- Dana, H., et al. Sensitive red protein calcium indicators for imaging neural activity. eLife. 5, (2016).
- Wang, H., Jing, M., Li, Y. Lighting up the brain: genetically encoded fluorescent sensors for imaging neurotransmitters and neuromodulators. Current Opinion in Neurobiology. 50, 171-178 (2018).
- Lu, L., et al. Wireless optoelectronic photometers for monitoring neuronal dynamics in the deep brain. Proceedings of the National Academy of Sciences. 115 (7), 1374-1383 (2018).
- Jennings, J. H., et al. Visualizing Hypothalamic Network Dynamics for Appetitive and Consummatory Behaviors. Cell. 160 (3), 516-527 (2014).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten