É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Dinâmica de oligomerização dos receptores de superfície celular em células vivas pela microscopia de fluorescência de reflexão interna total combinada com análise de número e brilho
Neste Artigo
Resumo
Descrevemos uma abordagem de imagem para a determinação do estado oligomérico médio de oligomeros de receptores marcados por mEGFP induzidos pela ligação de ligand na membrana plasmática das células vivas. O protocolo é baseado na microscopia de Fluorescência Total de Reflexão Interna (TIRF) combinada com análise de Número e Brilho (N&B).
Resumo
Apesar da importância e ubiquidade da oligomerização do receptor, poucos métodos são aplicáveis para detectar eventos de agrupamento e medir o grau de agrupamento. Aqui, descrevemos uma abordagem de imagem para determinar o estado oligomérico médio de homocomplexos do receptor marcado pelo mEGFP na membrana das células vivas. O protocolo é baseado na microscopia de Fluorescência Total de Reflexão Interna (TIRF) combinada com análise de Número e Brilho (N&B). A N&B é um método semelhante à espectroscopia fluorescência-correlação (FCS) e fótons contando histograma (PCH), que são baseados na análise estatística das flutuações da intensidade da fluorescência da fluorofia difundindo dentro e fora de uma iluminação volume durante um tempo de observação. Em particular, a N&B é uma simplificação da PCH para obter informações sobre o número médio de proteínas em misturas oligoméricas. As amplitudes da flutuação da intensidade são descritas pelo brilho molecular do fluorophore e pelo número médio de fluorophores dentro do volume da iluminação. Assim, a N&B considera apenas o primeiro e segundo momentos da distribuição de amplitude, ou seja, a intensidade média e a variação. Esta é, ao mesmo tempo, a força e a fraqueza do método. Como apenas dois momentos são considerados, a N&B não pode determinar a fração molar de oligomeros desconhecidos em uma mistura, mas estima apenas o estado médio de oligomerização da mistura. No entanto, ele pode ser aplicado a séries de tempo relativamente pequenas (em comparação com outros métodos de momento) de imagens de células vivas em uma base pixel-a-pixel, simplesmente monitorando as flutuações de tempo da intensidade da fluorescência. Ele reduz o tempo eficaz por pixel para alguns microssegundos, permitindo a aquisição no intervalo de tempo de segundos a milissegundos, o que é necessário para cinética de oligomerização rápida. Finalmente, grandes áreas celulares, bem como compartimentos subcelulares podem ser explorados.
Introdução
Descrevemos uma abordagem de imagem total de reflexão interna fluorescência-número e brilho (TIRF-N&B) para determinar o estado oligomérico médio das moléculas receptoras na membrana plasmática das células vivas, com o objetivo de vincular a montagem do receptor dinâmica para a função biológica das proteínas (Figura 1).
Após a ligação extracelular do ligand, os receptores iniciam a transdução de sinal intracelular dependendo de sua conformação, oligomerização, potenciais co-receptores e composição da membrana. Apesar da importância e ubiquidade da oligomerização do receptor, reconhecida como um evento-chave na sinalização celular1,2,3,4,5,6, 7,poucos métodos podem detectar eventos de agrupamento e medir o grau de agrupamento experimentalmente8,9. O volume confocal (x, y - 300 nm, z 900 nm) é insuficientemente resolvido para provar a interação molecular e stoichiometria, mesmo após a otimização por algoritmos de restauração de imagem10. A composição sub-unitária de oligomeros proteicos não pode ser resolvida de forma puramente espacial, mesmo por métodos de super-resolução em x,y resolução de 20-70 nm, como PALM11, STORM12,e STED13. Além disso, sua resolução temporal (na ordem dos minutos por imagem) não pode seguir a cinética na faixa de segundos. Único molécula passo-branqueamento resolve a stoichiometria de oligomeros de proteína apenas se eles são imóvel14.
Um dos métodos mais versáteis para medir a densidade e o oligomerização de proteínas fluorescentes marcadas dentro de imagens individuais é a análise de distribuição de intensidade espacial (SpIDA), que depende da amostragem espacial. É aplicável a células quimicamente fixas e vivas, e permite a análise de várias regiões de interesse da célula simultaneamente usando microscopia fluorescência padrão15. Alternativamente, métodos momentâneos, como espectroscopia fluorescência-correlação (FCS)16,fótons contando histograma (PCH)17, e Número e Brilho (N&B)18,19, são adequados para oligomer quantitativo Medidas. Esses métodos analisam as flutuações de intensidade da fluorescência que podem ser observadas no tempo em que os fluorofforas se difundem dentro e fora de um volume de iluminação. As amplitudes das flutuações de intensidade podem ser descritas exclusivamente pelo brilho molecular do fluorofforre (ε) e pelo número médio de fluorofônicos (n) dentro do volume de iluminação17 (Figura 2). Normalmente, o coeficiente de difusão dos fluorofforos e o número médio de moléculas (inversamente relacionadas ao valor G(0) dentro do volume de iluminação podem ser obtidos pela FCS20. No entanto, uma vez que o tempo de difusão apenas escalas com a raiz cúbica da massa, FCS não é suficientemente sensível para detectar alterações na massa molecular21. Na prática, a FCS de cor única não consegue detectar a dimerização dos receptores de membrana. PCH resolve misturas de diferentes oligomeros com precisão. Usando mais de dois momentos da distribuição da amplitude, detecta moléculas do brilho diferente que ocupam o mesmo volume da iluminação. Digitalização FCS22 e desenvolvimentos, como a interessante par-correlação de brilho molecular (pCOMB) abordagem23, introduzido para estender a gama de aplicabilidade dos métodos de correlação fluorescência em sistemas biológicos24 , permanecem métodos de ponto único sem a capacidade de medições rápidas em uma grande área de uma célula, exigindo muitas observações consecutivas em cada pixel e aquisição de dados na ordem de segundos.
A N&B é uma versão simplificada do PCH que considera apenas o primeiro e segundo momentos da amplitude da distribuição de fluorescência, ou seja, a intensidade média, e a variação, σ2 (Figura 2)18,19 e, por causa disso, não pode determinar a fração molar de oligomeros desconhecidos em uma mistura, mas estima somente o estado médio do oligomerization da mistura. No entanto, a N&B tem a vantagem de trabalhar com uma série de imagens de imagens de células vivas relativamente menores do que a PCH em uma base pixel-a-pixel, simplesmente monitorando as flutuações no tempo da intensidade da fluorescência. Como a N&B reduz o tempo por pixel para alguns microssegundos, ela pode seguir cinética de oligomerização rápida sobre grandes áreas celulares, permitindo a aquisição de imagem em uma escala de tempo de segundos em microscopia de varredura de raster (por exemplo, confocal, 2 fótons) e milissegundos em microscopia baseada em câmera (por exemplo, TIRFM).
Vários relatos demonstraram a capacidade da N&B de quantificar o número de subunidades em aglomerados de proteínas por meio de imagens de regiões celulares estendidas. Os clusters Paxillin-EGFP foram detectados nos locais de adesão nas células CHO-K125,e a agregação intracelular do peptídeo httex1p patogênico foi descrita nas células COS-726. A N&B foi aplicada para seguir a oligomerização ativa da ligand do receptorErbB 27,e o efeito do ligand FGF21 em Klothob (KLB) e fgfr1c em célulasHeLa 28. A combinação de imagens tirf e análise de N&B foi usada para mostrar que a dinamina-2 é principalmente tetramérica em toda a membrana celular29. Aplicamos a N&B a imagens de varredura de raster e TIRF para provar a dimerização conduzida por ligand dos receptores de membrana celular uPAR e FGFR130,31.
Métodos de correlação de fluorescência, como N&B, FCS e PCH, são baseados na noção de que, em um volume aberto, o número de bolhas de partículas segue uma distribuição de Poisson. Como somente os fótons que os fluorofônicos emitem podem ser detectados, o valor médio para uma intensidade 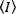 de fluorescência medida versus o tempo em um pixel da imagem, é o produto do número médio de fluorofosforas no volume de iluminação, n, e sua brilho molecular, ε17:
de fluorescência medida versus o tempo em um pixel da imagem, é o produto do número médio de fluorofosforas no volume de iluminação, n, e sua brilho molecular, ε17:
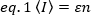
onde o ε é expresso como o número de fótons emitidos por unidade de tempo (convencionalmente por segundo) por molécula quando a molécula está no centro do volume de iluminação.
O brilho é propriedade de cada fluorofofóbico em uma determinada aquisição criada, enquanto a intensidade é a soma de todas as contribuições de todos os fluorofos. Em competições biológicas, o brilho aumentará com o aumento do número de fluorofos que flutuam junto, dando a informação no estado do oligomerization da proteína fluorescente-etiquetada. As amplitudes de flutuação em um determinado pixel é medido a partir da variação do sinal de fluorescência, σ2:
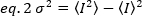
Onde a média do quadrado 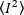 de intensidade, e o quadrado
de intensidade, e o quadrado 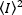 da média de intensidade, são computados a partir dos valores de intensidade individual em cada pixel de cada quadro:
da média de intensidade, são computados a partir dos valores de intensidade individual em cada pixel de cada quadro:
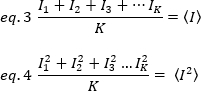
onde K é o número de quadros totais na série de tempo. Experimentalmente, é necessário calcular para toda a série de imagens a variação que descreve a dispersão dos valores de intensidade individual em cada pixel de uma única imagem em torno do valor de intensidade média. A variação inclui todas as flutuações de diferentes origens. Em uma primeira aproximação, a variação devido às partículas de difusão no volume de iluminação, σ20,pode ser separada da variância devido ao ruído do tiro do detector, σ2d. As duas variações são independentes; assim, a variação total é dada por sua soma:
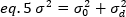
A variação, devido a flutuações moleculares dentro e fora do volume de detecção, é linearmente dependente do brilho e intensidade moleculares:
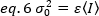
Reorganizando eq. 6 de acordo com o eq. 1:
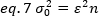
De acordo com o conceito típico de espectroscopia de correlação de fluorescência, a equação 7 afirma que a variação devido ao número de flutuações depende do quadrado do brilho das partículas.
Em seguida, a variação devido às flutuações do detector é uma função linear da intensidade detectada, a suposição de que o detector é operado abaixo de seu limite de saturação19:
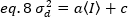
No caso dos detectores de contagem de fótons =1e c=0, assim a variação do detector é igual à intensidade média:
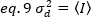
Para aplicar esses conceitos a medições reais em células vivas, Gratton e colegas18 definem o brilho aparente, B, para cada pixel como a proporção da variação sobre a intensidade média:
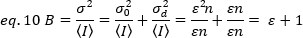
B é o parâmetro que é medido experimentalmente. Neste trabalho, imagens de séries de tempo de receptores FGFR1 na membrana plasmática das células HeLa são capturadas pela microscopia TIRF e o brilho aparente médio, B, é determinado pela análise de N&B. Então, após a adição de FGF2, séries de tempo consecutivos são capturadas para acompanhar as mudanças na auto-montagem das moléculas receptoras na superfície da membrana após a estimulação do receptor com o ligand canônico.
No entanto, uma vez que o detector do microscópio TIRF é uma câmera EMCCD, a expressão para o brilho aparente precisa ser modificada como19:
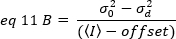
onde o deslocamento é o deslocamento da intensidade da eletrônica da deteção que é uma característica das ajustes do detetor. A variação e a intensidade média de um detector analógico são, respectivamente, dadas por:
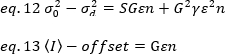
onde G é o ganho analógico em níveis digitais (DL/fótons), S, os níveis digitais por fóton19, é dado pela inclinação de uma intensidade versus variação parcela para uma fonte de luz com intensidade constante (sem flutuações temporais). O fator γ está relacionado à forma do volume de detecção de pixels. De acordo com Hassler et al.32,o fator γ é igual a 0,3 para imagens TIRF trabalhando no ganho máximo da câmera de detecção19. Os parâmetros de deslocamento, S e G são características da câmera e do microscópio. O brilho aparente, B, é obtido reorganizando eq. 11 de acordo com eq. 12 e 13:
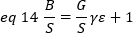
Experimentalmente, o ε é uma função complexa da intensidade do laser e da eficiência de detecção do sistema. No entanto, uma vez que B / S é linearmente dependente de ε, só é importante determinar o valor relativo do ε para um determinado modo de detecção:
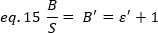
onde o ε' é proporcional ao ε. Ainda assim, uma calibração é realizada usando uma referência interna.
Protocolo
1. Preparação da amostra
- Dia 1. Células HeLa semente em meio completo em uma concentração de 100.000-200.000 células / mL em pratos de fundo de vidro. Sementes 6-8 replicar pratos.
Nota: Neste exemplo, o meio é complementado com 10% de calor inativado Fetal Bovine Serum (FBS), 1 mM piruvado de sódio, 100 U/100 μg penicilina/estreptomicina. Vários pratos de replicar são preparados. - Dia 2-3. Quando as células estão em sub-confluência, transfect metade dos pratos com o plasmídeo de proteína e a segunda metade com plasmídeos de referência (monomer e dimer), em meio livre de soro.
Nota: A transfecção é feita em meio livre de soro complementado com antibióticos, 0,1% De Soro Bovi Albumin e 25 mM HEPES buffer, sem Fenol Red. - Dia 3-4. Verifique se as células transfeccionadas são aderentes ao fundo dos pratos e a membrana celular é fluorescente. Descarte pratos com células cobertas de vegetação ou com fluorescência muito baixa.
Nota: Não deixe que as células cresçam demais. As células devem ser bem distribuídas e ser aderidas à área de vidro do prato (Figura 1A). Os pratos inferiores de vidro pré-revestidos podem ser usados favorecendo a adesão celular. A cultura celular é testada para contaminação por micoplasma antes de qualquer experimento. Neste exemplo, as células são transfeccionadas com plasmplasmida (A207K)mEGFP-FGFR1 e as células de referência são transfectadas com plasmsiem GPI-(A207K) e plasmplas mEGFP de GPI usando protocolos padrão. Para a microscopia de células vivas, recomenda-se um meio livre de indicadores; 25 mM tampão HEPES é adicionado para evitar alterações de pH durante a imagem.
2. TIRF Imaging - Alinhamento da Linha Laser e Otimização da Iluminação TIRF
- Quatro horas antes do experimento, ativar a incubadora de temperatura do microscópio em 37 °C.
- Ligue o microscópio, computadores e câmeras e esperar que as câmeras atinjam a temperatura de trabalho adequada.
Nota: A temperatura de trabalho da câmera utilizada neste estudo é de -75 °C. - Coloque uma pequena gota de óleo no objetivo. Coloque um prato de amostra no lugar. Feche as portas da incubadora e deixe a temperatura do prato equilibrar (~ 10 min).
- Ligue a lâmpada de epifluorescência e o laser de 488 nm.
- Selecione o modo de contraste de epifluorescência para explorar a amostra, pesquisando uma célula para se concentrar no ocular.
Nota: O uso de uma lâmpada fluorescente para procurar pilhas através do ocular não é imperativo. Uma linha laser apropriada pode ser usada preferivelmente. - Selecione o filtro adequado para coletar a emissão verde através da câmera do microscópio (Band Pass Ex 490/20 (500) Band Pass Em 525/50, ou similar.
- Mude da porta ocular para a câmera (câmera #1 na Figura 1)no modo epifluorescência, refine o foco e a mudança para o modo TIRF. Os modos epifluorescência e TIRF podem ser nomeados com uma nomenclatura diferente, dependendo da marca do microscópio.
Nota: Pode haver problemas focando ou alinhando o laser se não houver marcadores fluorescentes na interface coverslip. Para alinhar o laser corretamente (essencial para a boa TIRF), concentre-se no deslizamento de capa. Muitas vezes é muito difícil determinar se o coverslip está em foco. Como sugestão, concentre-se nas bordas das células. - Ativar o alinhamento automático seguindo as instruções do microscópio TIRF.
Nota: Resumidamente, para passos de 2,4 a 2,8, primeiro encontrar as células através do ocular e se concentrar neles, em seguida, enviar a emissão para a porta da câmera do microscópio TIRF, re-foco das células na tela do computador microscópio e ativar o procedimento para o alinhamento a laser. O alinhamento consiste em encontrar o ângulo crítico em que a iluminação se torna evanescente(Figura 3). Microscópios comerciais podem ter protocolos de alinhamento ligeiramente diferentes e também ser totalmente automatizados; outros podem ter uma pequena câmera para facilitar a visualização das condições de ângulo crítico. - Escolha uma profundidade de iluminação adequada e otimize a direção do campo evanescente(Figura 3).
Nota: A profundidade de penetração é mantida constante para todos os controles e amostras.
3. TIRF Imaging: Captura da Série Time
- Defina uma região de interesse (ROI) de pelo menos 256 x 256 pixels.
Nota: Nesta configuração, a captura é feita com câmera #2 software que controla diretamente apenas a câmera (Veja a lenda da Figura 1). - Defina a exposição a 1 ms e o ganho em EM para 1.000 (este é o fator G no eq. 12 e 13). A tal velocidade, pode ser necessário ajustar ou aumentar a potência laser. Aqui a potência a laser é de 0,5 mW.
Nota: Dependendo do tipo da câmera e dos limites impostos pelo coeficiente de difusão da proteína, intensidade e fundo de fluorescência, os critérios gerais para definir a potência laser não são para saturar o detector, minimizar o clareamento de fotos e capturar como rápido possível em um S/N razoável. O ganho EM é sempre definido no máximo da câmera (ver Introdução). - Executar uma primeira seqüência de teste em condições iniciais e estima aproximadamente o valor S / N. As condições são aceitáveis em S/N = 2-3 ou superior, medida no primeiro quadro da série de primeira vez.
- Use o controle deslizante do sistema de divisão de emissões que conecta a câmera #2 ao microscópio para mascarar um lado da imagem (Figura 1B, Figura 4A-B)
Nota: Neste conjunto, um conector de imagem multicanal é instalado na câmera #2 para permitir a aquisição de duas imagens espacialmente idênticas simultaneamente. O sistema é equipado com slides para a montagem de diferentes filtros de emissão. Um dos controles deslizantes monta uma máscara preta para cobrir um lado da imagem. A área mascarada é usada para a calibração interna de cada série de tempo, para determinar os parâmetros da câmera (eq. 12 e eq. 13). Desta forma, não há necessidade de uma etapa de calibração independente e, importante, calibração é realizada em paralelo com a captura de cada série de tempo. Na ausência deste sistema, a câmera pode ser calibrada aplicando protocolos publicados33. - Selecione a opção de autosave do arquivo da câmera.
- Comece a aquisição da série de imagens. Adquirir um mínimo de 700 quadros em uma relação Mínima S / N de 2.
Nota: O número de quadros necessários para análise depende da estabilidade da amostra para o fotobranqueamento e da dispersão dos dados. Portanto, a qualidade de cada série de tempos é avaliada durante a análise de N&B. - Sem tirar o prato do microscópio, adicione o ligand.
- Selecione uma célula com uma membrana de fluorescência brilhante e comece rapidamente a primeira série da corrida cinética.
Nota: Se a adição do ligand é feito rapidamente, esta primeira captura define o ponto = 0 tempo da cinética ligand. O software registra a hora exata da captura. - Pesquise uma segunda célula e adquira o segundo ponto de encontro da cinética.
Nota: As rotinas de visita ao ponto estão disponíveis em alguns microscópios equipados com estágios motorizados x,y,z. Estes permitem a memorização de múltiplas posições no prato celular, e pode ajudar a manter um intervalo mais constante de tempo entre a imagem-série em diferentes células. - Capture uma nova célula para cada ponto de tempo da corrida cinética.
Nota: Após a captura, uma célula é parcialmente fotobranda e não pode ser re-imagem. Por causa disso, a cinética é obtida acombinando séries de tempo de muitas células, cada uma capturada em um momento diferente. - Para cada novo prato, repita o protocolo do passo 2.3 para 3.9.
Nota: Para pratos de referência, adicione um volume do veículo (PBS complementado com 0,01% de albumina de soro bovina) equivalente ao usado para o ligand.
4. Número e Brilho (N&B): Verificação de qualidade da Série Time
- Converter e salvar como . TIFF os arquivos adquiridos com o software da câmera (.sif arquivos neste exemplo).
- Importação. Tiff arquivos na rotina de software de análise, ativando a interface gráfica do usuário N & B (GUI) MATLAB.
Nota: Uma rotina de N&B executável matlab personalizada é usada aqui (análise de N&B na https://www.cnic.es/en/investigacion/2/1187/tecnologia). Abrindo um importado. O arquivo TIFF, a rotina gera a imagem de intensidade média, o perfil de intensidade média e permite inspecionar a série quadro a quadro(Figura Suplementar 1). Outros softwares estão disponíveis para análise de N&B (por exemplo, software SimFCS). - Descartar séries para as quais o perfil de intensidade média mostra mais de 10% de fotobranqueamento, e séries em que houve uma distorção ou tradução evidente da membrana celular durante a aquisição.
- Os frames de colheita que são evidente fora-de-foco.
Nota: Uma ferramenta de corte é implementada na rotina para descartar quadros individuais ou múltiplos dentro da série de imagens. Esta operação é permitida porque o tempo quadro-a-quadro não é crítico, enquanto o pixel habitar o tempo (tempo de exposição) é (ver Discussão). - Mantenha para a série de análise apenas com pelo menos 500 prazos.
5. Número e Brilho (N&B): Determinação dos Parâmetros da Câmera (Offset, σ e S)
- Ativar a rotina calibrar câmera.
- Selecione uma área de pelo menos 20 x 50 pixels na região de ruído do detector(Figura 4).
Nota: A rotina origina um histograma dos valores (também definido Nível Digital, DL) e retorna um enredo logarithm da Frequência versus Níveis Digitais. - No lote de frequência de registro versus nível digital, mova o cursor vermelho linear para delimitar o gaussiano e a parte linear da curva.
Nota: O cursor vermelho divide as duas seções da curva, e ativa a rotina retornando o deslocamento, que é o centro da função gaussiana da resposta da câmera, o σ do ajuste gaussian, e o fator S, que é a inclinação da parte linear da câmera respons e (Figura 4C-D).
6. Número e Brilho (N&B): Computação dos valores B na Região Selecionada de interesse (ROI)
- Ativar a chave B.
Nota: Essa ação gera a imagem de intensidade média(Figura 5,primeira coluna) e a imagem B em que cada valor B individual está associado ao pixel relacionado na imagem(Figura Suplementar 1). - Aplique um binning mínimo (2 2) para reduzir a dispersão dos dados e para gerar o histograma B-I (Figura 5,segunda coluna).
Nota: O histograma B-I representa a distribuição dos valores B de todos os pixels da imagem versus a intensidade do pixel. Y = B/S; X =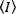 ( - offset)/S (Figura Suplementar 1 e eq. 11 e 15).
( - offset)/S (Figura Suplementar 1 e eq. 11 e 15). - Inspecione o histograma B-I usando o cursor quadrado interativo.
- Selecione um ROI quadrado para a análise(Figura 5,terceira coluna).
Nota: O cursor sincroniza uma máscara móvel na imagem de intensidade média, destacando os pixels que são selecionados dentro da área do cursor quadrado(Figura Suplementar 1). Por esta inspeção, é possível excluir da análise o fundo e as áreas com intensidade muito baixa. - Gerar o mapa B do ROI selecionado (Figura 5,quarta coluna).
- Salve o arquivo ASCII dos valores B associados à seleção.
- Importe o arquivo ASCII em um software gráfico para calcular a distribuição de frequência dos dados e obter o valor B médio ± S.E (Figura 5,quinta coluna).
Nota: Se os dados forem homogêneos, a distribuição de frequência dos valores B aproxima-se de uma distribuição gaussiana. - Aplique eq. 15 para derivar
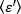 o
o 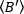 brilho médio = - 1 [((contagens/molécula) por tempo de permanência] para cada célula em cada ponto de tempo da corrida cinética. Normalizar os dados de acordo com:
brilho médio = - 1 [((contagens/molécula) por tempo de permanência] para cada célula em cada ponto de tempo da corrida cinética. Normalizar os dados de acordo com: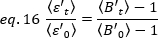
onde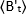 está o valor B médio medido no tempo "t" após adição de ligand, e
está o valor B médio medido no tempo "t" após adição de ligand, e 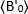 é o valor B médio medido no momento t=0 (10-20 s após adição de ligand).
é o valor B médio medido no momento t=0 (10-20 s após adição de ligand).
Nota: A normalização dos resultados permite a comparação direta de experimentos realizados em dias diferentes. Compensa diferenças no brilho medido devido ao poder do laser e às flutuações técnicas. - Trace o Brilho Médio Normalizado versus tempo de aquisição para construir a corrida cinética (Figura 6).
Resultados
Os resultados de duas células representativas HeLa-mEGFP-FGFR1 semeadas no mesmo prato cultural são mostrados na Figura 5 e na Tabela Suplementar 1. As duas células foram capturadas no tempo 0 min(Figura 5A, superior) e 7 min(Figura 5A, inferior) após a adição do ligand FGF2.
Discussão
A N&B requer várias precauções na escolha do modelo celular e da estratégia de rotulagem. Ele pode ser aplicado apenas para células vivas que permanecem aderidas de forma enova durante o tempo de captura de imagem. Flutuações extras devido ao deslocamento rígido de toda a célula podem ser tratadas com abordagens adequadas de restauração de imagem38. No entanto, geralmente quando uma célula se move, a membrana celular também se deforma, e a deformação da estrutura, produzindo grande ...
Divulgações
Os autores não têm nada a divulgar.
Agradecimentos
O CNIC é apoiado pelo Ministério de Ciencia, Innovación y Universidades e pela Fundação Pro CNIC, e é um Centro de Excelência Severo Ochoa (SEV-2015-0505). Também somos apoiados pelo Fundo Europeu de Desenvolvimento Regional (FEDER) "Una manera de hacer Europa". A UC reconhece o apoio da Associazione Italiana Ricerca sul Cancro, da Association for International Cancer Research (agora conhecida como Worldwide Cancer Research) e do Ministério da Saúde italiano. A.T. reconhece o "Fondazione Banca del Monte di Lombardia" por apoiar parcialmente seu trabalho com a Bolsa PV "Progetto Professionalità Ivano Becchi" 2011-2012.
Materiais
| Name | Company | Catalog Number | Comments |
| 3-Colour Fast TIRF Leica AM TIRF MC inverted microscope, with smi-automatic TIRF alignment. The microscope is equipped with a diode 488 nm laser, a 100x1.46 oil TIRF objective, Ex/Em Bandpass filters at 490/20 and 525/50, temperature/CO2 incubator and Andor DU 8285 VP EMCCD camera. The microscope is operated by Leica LIF software. | Leica Microsystems, Wetzlar, Germany | ||
| Albumin from Bovine Serum 98% minimun | Sigma-Aldrich, St. Louis, MI, USA | A7906-100G | |
| DMEM without Phenol Red with 25 mM HEPES | GIBCO Thermo Fisher Scientific,Waltham, MA, USA | 21063029 | Used serum free for microscopy |
| DMEM high-glucose GlutaMAX I | GIBCO Thermo Fisher Scientific,Waltham, MA, USA | 10566-016 | Used for complete medium |
| Dulbecco's Phosphate Buffered Saline 10x (PBS) | Biowest, Nuaillé, France | X0515-500 | |
| Emission splitting system Photometrics DV2 | TeledynePhotometrics, Tucson, AZ, USA | ||
| Fetal Bovine Serum, qualified, Brazil | GIBCO Thermo Fisher Scientific,Waltham, MA, USA | 10270106 | 10% inactivated supplement for complete medium |
| Glass bottom 35-mm sterile 1.5 dishes | MatTek, Ashland, MA, USA | P35G-0.170-14-C | uncoated, glass thickness 0.17 microns |
| GraphPad Prism | GraphPad Software Inc., San Diego, CA, USA | ||
| Human cervical carcinoma (HeLa), serum-free animal component (AC) cells | Millipore-Sigma ECACC, Darmstadt, Germany | CB_08011102 | |
| iXonEM+ 897 EMCCD (back-illuminated) ANDOR camera controlled by ANDOR Solis software | Oxford Instruments, Andor TM Technology, Abingdon-on-Thames, UK | This camera, installed in an additional port of the microscope, is used for acquiring the N&B time series | |
| Matlab Executable N&B routine | Unit of Microscopy and Dynamic Imaging, CNIC, Madrid, Spain | download at https://www.cnic.es/en/investigacion/2/1187/tecnologia | |
| MatLab v.2018b | The MathWorks, Inc. Natick, MA, USA | download at https://www.mathworks.com/products/matlab.html | |
| Penicillin:Streptomycin for tissue culture 100x | Biowhittaker Inc. Walkersville, MD, USA | LONZA 17-602E | supplement for medium at Penicillin/Streptomycin 100U/100µg. |
| pN1-mEGFP-FGFR1 expression vector | Unit of Gynecological Oncology Research, European Institute of Oncology IRCCS, Milan, Italy | Zamai et al., 2019 | |
| pN1-N-Gly-mEGFP-GPI expression vector | Unit of Microscopy and Dynamic Imaging, CNIC, Madrid, Spain | Hellriegel et al., 2011 | |
| pN1-N-Gly-mEGFP-mEGFP-GPI expression vector | Unit of Microscopy and Dynamic Imaging, CNIC, Madrid, Spain | Hellriegel et al., 2011 | |
| Recombinant FGF2 | PeproTech EC, Ltd., London, UK | Ligand solution: 20ng/mL of FGF2 in PBS supplemented with 0.01%BSA. | |
| Sodium pyruvate GIBCO | ThermoFisher Scientific | 11360070 | 1mM supplement for medium |
| TransIt-LT1 Transfection Reagent | MirusBio LLC, Madison, WI, USA | MIR 2300 | |
| Trypsin-EDTA (0.25%), phenol red | GIBCO Thermo Fisher Scientific,Waltham, MA, USA | 25200056 | |
| Type F Immersion liquid 10 mL | Leica Microsystems, Wetzlar, Germany | 11513 859 | |
| UltraPure BSA (50 mg/mL) | ThermoFisher Scientific | AM2618 | 0.1% supplement for medium without phenol red used for transfections |
Referências
- Agwuegbo, U. C., Jonas, K. C. Molecular and functional insights into gonadotropin hormone receptor dimerization and oligomerization. Minerva Ginecologica. 70 (5), 539-548 (2018).
- Ferre, S., et al. G protein-coupled receptor oligomerization revisited: functional and pharmacological perspectives. Pharmacological Reviews. 66 (2), 413-434 (2014).
- Marsango, S., Ward, R. J., Alvarez-Curto, E., Milligan, G. Muscarinic receptor oligomerization. Neuropharmacology. 136 (Pt C), 401-410 (2018).
- Oishi, A., Cecon, E., Jockers, R. Melatonin Receptor Signaling: Impact of Receptor Oligomerization on Receptor Function. International Review of Cell and Molecular Biology. 338, 59-77 (2018).
- Thelen, M., Munoz, L. M., Rodriguez-Frade, J. M., Mellado, M. Chemokine receptor oligomerization: functional considerations. Current Opinion in Pharmacology. 10 (1), 38-43 (2010).
- Van Craenenbroeck, K. GPCR oligomerization: contribution to receptor biogenesis. Subcellular Biochemistry. 63, 43-65 (2012).
- Wnorowski, A., Jozwiak, K. Homo- and hetero-oligomerization of beta2-adrenergic receptor in receptor trafficking, signaling pathways and receptor pharmacology. Cell Signaling Technology. 26 (10), 2259-2265 (2014).
- Fricke, F., Dietz, M. S., Heilemann, M. Single-molecule methods to study membrane receptor oligomerization. Chemphyschem. 16 (4), 713-721 (2015).
- Vidi, P. A., Ejendal, K. F., Przybyla, J. A., Watts, V. J. Fluorescent protein complementation assays: new tools to study G protein-coupled receptor oligomerization and GPCR-mediated signaling. Molecular and Cellular Endocrinology. 331 (2), 185-193 (2011).
- Trussell, H. J., et al., Trussell, J., et al. . Academic Press Library in Signal Processing. 4, 3-9 (2014).
- Betzig, E., et al. Imaging intracellular fluorescent proteins at nanometer resolution. Science. 313 (5793), 1642-1645 (2006).
- Rust, M. J., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nature Methods. 3 (10), 793-795 (2006).
- Nagerl, U. V., Willig, K. I., Hein, B., Hell, S. W., Bonhoeffer, T. Live-cell imaging of dendritic spines by STED microscopy. Proceedings of the National Academy of Sciences of the United States of America. 105 (48), 18982-18987 (2008).
- Tsekouras, K., Custer, T. C., Jashnsaz, H., Walter, N. G., Presse, S. A novel method to accurately locate and count large numbers of steps by photobleaching. Molecular Biology of the Cell. 27 (22), 3601-3615 (2016).
- Godin, A. G., et al. Revealing protein oligomerization and densities in situ using spatial intensity distribution analysis. Proceedings of the National Academy of Sciences of the United States of America. 108 (17), 7010-7015 (2011).
- Qian, H., Elson, E. L. Distribution of molecular aggregation by analysis of fluctuation moments. Proceedings of the National Academy of Sciences of the United States of America. 87 (14), 5479-5483 (1990).
- Chen, Y., Muller, J. D., So, P. T., Gratton, E. The photon counting histogram in fluorescence fluctuation spectroscopy. Biophysical Journal. 77 (1), 553-567 (1999).
- Dalal, R. B., Digman, M. A., Horwitz, A. F., Vetri, V., Gratton, E. Determination of particle number and brightness using a laser scanning confocal microscope operating in the analog mode. Microscopy Research and Technique. 71 (1), 69-81 (2008).
- Unruh, J. R., Gratton, E. Analysis of molecular concentration and brightness from fluorescence fluctuation data with an electron multiplied CCD camera. Biophysical Journal. 95 (11), 5385-5398 (2008).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and chemical applications of fluorescence correlation spectroscopy: a review. Biochemistry. 41 (3), 697-705 (2002).
- Muller, J. D., Chen, Y., Gratton, E. Fluorescence correlation spectroscopy. Methods in Enzymology. 361, 69-92 (2003).
- Levi, V., Ruan, Q., Kis-Petikova, K., Gratton, E. Scanning FCS, a novel method for three-dimensional particle tracking. Biochemical Society Transactions. 31 (Pt 5), 997-1000 (2003).
- Hinde, E., et al. Quantifying the dynamics of the oligomeric transcription factor STAT3 by pair correlation of molecular brightness. Nature Communications. 7, 11047 (2016).
- Waithe, D., et al. Optimized processing and analysis of conventional confocal microscopy generated scanning FCS data. Methods. 140-141, 62-73 (2018).
- Digman, M. A., Dalal, R., Horwitz, A. F., Gratton, E. Mapping the number of molecules and brightness in the laser scanning microscope. Biophysical Journal. 94 (6), 2320-2332 (2008).
- Ossato, G., et al. A two-step path to inclusion formation of huntingtin peptides revealed by number and brightness analysis. Biophysical Journal. 98 (12), 3078-3085 (2010).
- Nagy, P., Claus, J., Jovin, T. M., Arndt-Jovin, D. J. Distribution of resting and ligand-bound ErbB1 and ErbB2 receptor tyrosine kinases in living cells using number and brightness analysis. Proceedings of the National Academy of Sciences of the United States of America. 107 (38), 16524-16529 (2010).
- Ming, A. Y., et al. Dynamics and Distribution of Klothobeta (KLB) and fibroblast growth factor receptor-1 (FGFR1) in living cells reveal the fibroblast growth factor-21 (FGF21)-induced receptor complex. Journal of Biological Chemistry. 287 (24), 19997-20006 (2012).
- Ross, J. A., et al. Oligomerization state of dynamin 2 in cell membranes using TIRF and number and brightness analysis. Biophysical Journal. 100 (3), L15-L17 (2011).
- Hellriegel, C., Caiolfa, V. R., Corti, V., Sidenius, N., Zamai, M. Number and brightness image analysis reveals ATF-induced dimerization kinetics of uPAR in the cell membrane. FASEB J. 25 (9), 2883-2897 (2011).
- Zamai, M., et al. Number and brightness analysis reveals that NCAM and FGF2 elicit different assembly and dynamics of FGFR1 in live cells. Journal of Cell Science. 132 (1), (2019).
- Hassler, K., et al. Total internal reflection fluorescence correlation spectroscopy (TIR-FCS) with low background and high count-rate per molecule. Optics Express. 13 (19), 7415-7423 (2005).
- Di Rienzo, C., Gratton, E., Beltram, F., Cardarelli, F. From fast fluorescence imaging to molecular diffusion law on live cell membranes in a commercial microscope. Journal of Visualized Experiments. (92), e51994 (2014).
- Beenken, A., Mohammadi, M. The FGF family: biology, pathophysiology and therapy. Nature Reviews Drug Discovery. 8 (3), 235-253 (2009).
- Joubert, J., Sharma, D. Light microscopy digital imaging. Current Protocols in Cytometry. , (2011).
- Gell, C., Berndt, M., Enderlein, J., Diez, S. TIRF microscopy evanescent field calibration using tilted fluorescent microtubules. Journal of Microscopy. 234 (1), 38-46 (2009).
- Burghardt, T. P. Measuring incidence angle for through-the-objective total internal reflection fluorescence microscopy. Journal of Biomedical Optics. 17 (12), 126007 (2012).
- Trullo, A., Corti, V., Arza, E., Caiolfa, V. R., Zamai, M. Application limits and data correction in number of molecules and brightness analysis. Microscopy Research and Technique. 76 (11), 1135-1146 (2013).
- Caiolfa, V. R., et al. Monomer-dimer dynamics and distribution of GPI-anchored uPAR are determined by cell surface protein assemblies. Journal of Cell Biology. 179 (5), 1067-1082 (2007).
- Campbell, R. E., et al. A monomeric red fluorescent protein. Proceedings of the National Academy of Sciences of the United States of America. 99 (12), 7877-7882 (2002).
- Cutrale, F., et al. Using enhanced number and brightness to measure protein oligomerization dynamics in live cells. Nature Protocols. 14 (2), 616-638 (2019).
- Dunsing, V., Chiantia, S. A Fluorescence Fluctuation Spectroscopy Assay of Protein-Protein Interactions at Cell-Cell Contacts. Journal of Visualized Experiments. (142), (2018).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados