Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Quantification du flux sanguin fœtal humain avec imagerie par résonance magnétique et compensation de mouvement
Dans cet article
Résumé
Nous présentons ici un protocole pour mesurer rapidement le flux sanguin fœtal avec l’IRM et effectuer rétrospectivement la correction du mouvement et le contrôle cardiaque.
Résumé
L’imagerie par résonance magnétique (IRM) est un outil important pour l’évaluation clinique de la morphologie cardiovasculaire et de la fonction cardiaque. C’est également la norme de soins reconnue pour la quantification du flux sanguin basée sur l’IRM à contraste de phase. Bien qu’une telle mesure du débit sanguin soit possible chez les adultes depuis des décennies, des méthodes visant à étendre cette capacité au flux sanguin fœtal n’ont été développées que récemment.
La quantification du flux sanguin fœtal dans les principaux vaisseaux est importante pour surveiller les pathologies fœtales telles que les cardiopathies congénitales (CHD) et le retard de croissance fœtale (FGR). La coronaropathie provoque des altérations de la structure cardiaque et du système vasculaire qui modifient le cours du sang chez le fœtus. Dans la RGF, la voie du flux sanguin est modifiée par la dilatation des shunts de sorte que l’apport sanguin oxygéné au cerveau est augmenté. La quantification du flux sanguin permet d’évaluer la gravité de la pathologie fœtale, ce qui permet une prise en charge in utero appropriée des patients et une planification des soins postnatals.
Les principaux défis de l’application de l’IRM de contraste de phase au fœtus humain comprennent la petite taille des vaisseaux sanguins, la fréquence cardiaque fœtale élevée, la corruption potentielle des données IRM due à la respiration maternelle, les mouvements fœtaux imprévisibles et le manque de méthodes conventionnelles de contrôle cardiaque pour synchroniser l’acquisition des données. Ici, nous décrivons les développements techniques récents de notre laboratoire qui ont permis la quantification du flux sanguin fœtal à l’aide de l’IRM à contraste de phase, y compris les progrès de l’imagerie accélérée, de la compensation de mouvement et du contrôle cardiaque.
Introduction
Une évaluation complète de la circulation fœtale est nécessaire pour surveiller les pathologies fœtales telles que le retard de croissance fœtale (RGF) et les cardiopathies congénitales (CHD)1,2,3. In utero, la prise en charge des patientes et la planification des soins postnatals dépendent de la gravité de la pathologie fœtale 4,5,6,7. La faisabilité de la quantification du flux sanguin fœtal avec l’IRM et ses applications dans l’évaluation des pathologies fœtales ont récemment été démontrées 3,8,9. La méthode d’imagerie, cependant, fait face à des défis, tels que l’augmentation des temps d’imagerie pour atteindre une résolution spatio-temporelle élevée, le manque de méthodes de synchronisation cardiaque et les mouvements fœtaux imprévisibles10.
Le système vasculaire fœtal comprend de petites structures (~ 5 mm de diamètre pour les principaux vaisseaux sanguins qui comprennent l’aorte descendante, le canal artériel, l’aorte ascendante, l’artère pulmonaire principale et la veine cave supérieure11,12,13). Pour résoudre ces structures et quantifier l’écoulement, l’imagerie à haute résolution spatiale est nécessaire. De plus, la fréquence cardiaque fœtale est environ le double de celle d’un adulte. Une résolution temporelle élevée est donc également nécessaire pour résoudre le mouvement cardiaque dynamique et le flux sanguin tout au long du cycle cardiaque fœtal. L’imagerie conventionnelle à cette haute résolution spatio-temporelle nécessite des temps d’acquisition relativement longs. Pour résoudre ce problème, l’IRM fœtale accélérée14,15,16 a été introduite. En bref, ces techniques d’accélération impliquent un sous-échantillonnage dans le domaine fréquentiel lors de l’acquisition des données et une reconstruction rétrospective haute fidélité à l’aide de techniques itératives. L’une de ces approches est la reconstruction par détection comprimée (CS), qui permet de reconstruire des images à partir de données fortement sous-échantillonnées lorsque l’image reconstruite est clairsemée dans un domaine connu et que les artefacts de sous-échantillonnage sont incohérents17.
Le mouvement en imagerie fœtale présente un défi majeur. La corruption du mouvement peut résulter d’un mouvement respiratoire maternel, d’un mouvement de masse maternel ou d’un mouvement fœtal macroscopique. La respiration maternelle conduit à des traductions périodiques du fœtus, alors que les mouvements fœtaux sont plus complexes. Les mouvements fœtaux peuvent être classés comme localisés ou bruts10,18. Les mouvements localisés impliquent le mouvement de segments du corps seulement. Ils durent généralement environ 10 à 14 s et leur fréquence augmente avec la gestation (~90 par heure à terme)10. Ces mouvements provoquent généralement de petites corruptions et n’affectent pas la zone d’imagerie d’intérêt. Cependant, les mouvements fœtaux grossiers peuvent entraîner une corruption grave de l’image avec des composants de mouvement à travers le plan. Ces mouvements sont des mouvements du corps entier médiés par la colonne vertébrale et durent 60-90 s.
Pour éviter les artefacts du mouvement fœtal, des mesures sont d’abord prises pour minimiser les mouvements maternels. Les femmes enceintes sont rendues plus détendues à l’aide d’oreillers de soutien sur le lit du scanner et vêtues de blouses confortables et peuvent avoir leurs partenaires présents à côté du scannerpour réduire la claustrophobie 19,20. Pour atténuer les effets du mouvement respiratoire maternel, des études ont effectué des examens IRM fœtaux sous la respiration maternelle21,22,23. Cependant, ces acquisitions doivent être courtes (~15 s) compte tenu de la tolérance réduite à la rétention du souffle des sujettes enceintes. Récemment, des méthodes rétrospectives de correction du mouvement ont été introduites pour l’IRM fœtale14,15,16. Ces méthodes suivent les mouvements du fœtus à l’aide de boîtes à outils d’enregistrement et corrigent les mouvements ou rejettent les parties non corrigibles des données acquises.
Enfin, les images d’IRM cardiaque postnatale sont classiquement acquises à l’aide d’un électrocardiogramme (ECG) pour synchroniser l’acquisition des données avec le cycle cardiaque. Sans déclenchement, le mouvement cardiaque et le flux pulsatile tout au long du cycle cardiaque sont combinés, produisant des artefacts. Malheureusement, le signal ECG fœtal souffre d’interférences du signal ECG maternel24 et de distorsions du champ magnétique25. Par conséquent, d’autres approches non invasives de l’échographie cardiaque fœtale ont été proposées, y compris l’auto-évaluation, l’optimisation métrique (MOG) et l’échographie Doppler21,26,27,28.
Comme décrit dans les sections suivantes, notre approche IRM pour quantifier le flux sanguin fœtal tire parti d’une nouvelle méthode de contrôle, MOG, développée dans notre laboratoire et combinée à la correction du mouvement et à la reconstruction itérative des acquisitions IRM accélérées. L’approche est basée sur un pipeline dans une étude publiée précédemment14 et est composée des cinq étapes suivantes: (1) acquisition du flux sanguin fœtal, (2) reconstructions en temps réel, (3) correction du mouvement, (4) gating cardiaque et (5) reconstructions fermées.
Protocole
Toutes les IRM ont été effectuées avec le consentement éclairé de volontaires dans le cadre d’une étude approuvée par notre comité d’éthique de la recherche institutionnel.
REMARQUE: Les méthodes décrites ci-dessous ont été utilisées sur un système d’IRM 3T. L’acquisition est réalisée à l’aide d’une séquence IRM à contraste de phase radiale. Cette séquence a été préparée en modifiant la trajectoire de lecture (pour obtenir un motif stellaire) de l’IRM cartésienne à contraste de phase du fabricant. Les protocoles de séquence et d’échantillon sont disponibles sur demande via notre plateforme d’échange C2P. Toutes les reconstructions de ce travail ont été effectuées sur un ordinateur de bureau standard avec les spécifications suivantes : 32 Go de mémoire, processeur 3,40 GHz avec 8 cœurs et carte graphique de 2 Go avec 1024 cœurs CUDA (Compute Unified Device Architecture). La reconstruction d’image a été réalisée sur MATLAB. La transformée de Fourier rapide non uniforme (NUFFT)29 a été réalisée sur l’unité de traitement graphique (GPU). Les paramètres de correction de mouvement ont été calculés à l’aide d’elastix30. La figure 1 représente le protocole dans un ordre chronologique, en suivant la façon dont les codes de vitesse acquis (codés par couleur à la figure 1) sont traités avec des images représentatives à chaque étape de la reconstruction. Le code de reconstruction est disponible à https://github.com/datta-g/Fetal_PC_MRI. Bien que nous fournissions les étapes du protocole ici, la plupart de ces étapes d’algorithme sont automatisées dans notre pipeline.
1. Positionnement du sujet et examens de localisation
- Aidez la mère à se positionner sur la table d’IRM dans la position confortable qu’elle préfère, habituellement couchée sur le dos ou sur le décubitus latéral, pour l’examen d’IRM.
- Placez la bobine cardiaque sur la région abdominale de la mère.
- Chargez la table d’IRM dans l’alésage magnétique et informez la mère que l’analyse est sur le point de commencer.
- Exécutez un examen localisateur pour localiser le corps du fœtus (résolution: 0,9 x 0,9 x 10 mm3, TE / TR: 5,0 / 15,0 ms, FOV: 450 x 450 mm2, tranches: 6).
- Effectuez un examen de localisation affiné pour localiser le système vasculaire fœtal avec le groupe de tranches centré sur le cœur fœtal (résolution 1,1 x 1,1 x 6,0 mm3, TE/TR: 2,69/1335,4 ms, FOV: 350 x 350 mm2, tranches: 10, orientation: axiale au fœtus).
- Répétez les localisateurs raffinés avec des orientations sagittales et coronales pour une vue plus claire des vaisseaux fœtaux.
- Répétez les localisateurs raffinés en cas de mouvement fœtal grossier.
2. Acquisition de données sur le débit sanguin fœtal
- Localisez les vaisseaux fœtaux à l’aide des examens de localisation. Par exemple, l’aorte descendante est un long vaisseau droit près de la colonne vertébrale dans les plans sagittaux. L’aorte ascendante et les artères pulmonaires principales peuvent être identifiées comme des vaisseaux quittant respectivement les ventricules gauche et droit. Le canal artériel peut être suivi comme un segment en aval de l’artère pulmonaire principale proximale à l’aorte descendante. La veine cave supérieure peut être identifiée à partir de plans axiaux près de la base du cœur fœtal comme le vaisseau adjacent à l’aorte ascendante.
- Prescrire une tranche perpendiculaire à l’axe du vaisseau fœtal d’intérêt. Faites pivoter et déplacez le guide de tranche sur la console de l’IRM de manière à ce qu’il croise perpendiculairement le vaisseau cible.
- Réglez les paramètres de balayage (type d’acquisition : IRM à contraste de phase radial, résolution : 1,3 x 1,3 x 5,0 mm 3, temps d’écho (TE)/temps de répétition (TR) :3,25/5,75 ms, champ de vision (FOV) : 240 x 240 mm2, tranche : 1, encodage de vitesse : 100-150 cm/s selon le vaisseau d’intérêt, direction de codage de la vitesse : à travers le plan, vues radiales : 1500 par encodage, respiration libre).
- Exécutez l’analyse et vérifiez l’ordonnance en fonction de la reconstruction initiale moyenne dans le temps effectuée et affichée sur l’ordinateur console IRM. Répétez les analyses de localisation et de contraste de phase si le vaisseau cible est absent ou non identifiable de la reconstruction initiale. Les données brutes acquises sont représentées dans le schéma de la figure 1A avec la vitesse compensée et par les acquisitions planes codées en rouge et bleu, respectivement.
- Répétez l’acquisition des données de flux sanguin fœtal pour chaque vaisseau sanguin cible.
REMARQUE : Les données brutes acquises (format : fichiers DAT) doivent être transférées pour une reconstruction hors ligne. Par exemple, sur les scanners Siemens, cela peut être effectué en exécutant 'twix'. Les données brutes acquises sont faites un clic droit à partir de la liste des acquisitions et « copier le fichier total raid » est choisi.
3. Correction de mouvement des mesures fœtales
- Reconstruire des séries en temps réel (résolution temporelle : 370 ms, vues radiales : 64) à partir des données acquises à l’aide de CS avec 15 itérations d’une optimisation de descente de gradient conjugué exploitant la régularisation de la variation totale spatiale (STV, poids : 0,008) et de la variation totale temporelle (TTV, poids : 0,08) représentée par le schéma de la figure 1B.
- Sélectionnez une région d’intérêt (ROI) englobant le navire d’intérêt à partir de cette première reconstruction en temps réel à l’aide d’une interface utilisateur graphique développée dans MATLAB. Dans cette étape, l’utilisateur doit dessiner un contour qui entoure l’anatomie fœtale, comme les grands vaisseaux cibles ou le cœur fœtal.
- Effectuez un suivi des mouvements du corps rigide avec elastix 30 (basé sur des informations mutuelles normalisées avec des paramètres optimisés empiriquement: 4 niveaux pyramidaux,300 itérations et transformations translationnelles).
- Rejeter les trames en temps réel suivies qui partagent une faible information mutuelle (MI) avec toutes les autres trames (où MI est inférieur à 1,5 fois la plage interquartile du MI moyen). Ces images sont réputées être représentées par un mouvement plan ou un mouvement fœtal grossier.
- Utilisez les données IRM correspondant à la plus longue série de cadres continus en temps réel (sans lacunes) des images restantes comme période de repos utilisée pour une reconstruction ultérieure.
- Interpoler les paramètres de correction de mouvement translationnels de la résolution temporelle de la série en temps réel (370 ms) au TR de l’acquisition au repos (5,75 ms).
- Appliquer des paramètres interpolés à la période de repos définie des données IRM en modulant la phase comme dans:
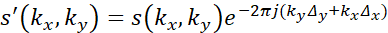
où s’est la donnée corrigée du mouvement, k x et k y sont les coordonnées dans k-espace, s est les données acquises non corrigées, Δ x et Δ y sont les déplacements suivis dans l’espace, et j représente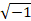 .
.
NOTE: Toutes les valeurs numériques des coefficients de régularisation dans ce travail ont été optimisées dans des expériences antérieures. Cela a été accompli à l’aide d’une recherche par grille de force brute pour trouver les coefficients de régularisation qui minimisaient l’erreur entre les reconstructions d’un ensemble de données de référence fœtale fortement échantillonné et les cas sous-échantillonnés rétrospectivement du même ensemble de données.
4. Résolution de la fréquence cardiaque fœtale
- Reconstruire une deuxième série d’images en temps réel à une résolution temporelle plus élevée (résolution temporelle: 46 ms, vues radiales: 8) en utilisant les données acquises à l’aide de CS, encore une fois avec 15 itérations d’une optimisation de descente de gradient conjugué avec STV (poids: 0,008) et TTV (poids: 0,08) régularisation représentée par le schéma de la figure 1C.
- Resélectionnez un retour sur investissement englobant le vaisseau fœtal d’intérêt.
- Exécutez un MOG multiparamètre sur la série en temps réel pour calculer la fréquence cardiaque fœtale dépendante du temps.
- Bin motion a corrigé les données IRM en 15 phases cardiaques en utilisant la forme d’onde de fréquence cardiaque dérivée. Dans cette étape, les limites temporelles des phases cardiaques sont calculées à l’aide de la fréquence cardiaque de l’étape précédente. Par exemple, les limites de la ième phase du kème battement de cœur sont données par:
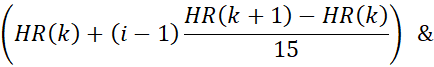
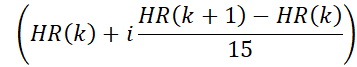
où HR(K) est le moment où le kième battement cardiaque se produit. L’horodatage de la n ième acquisition radiale est donné par (n x TR). Les données dont les horodatages se situent dans les limites d’une phase cardiaque sont affectées à cette phase.
REMARQUE: MOG est une technique de contrôle26 qui comprend le regroupement itératif des données acquises basé sur un modèle de fréquence cardiaque fœtale multi-paramètres pour créer des images CINE qui optimisent une métrique d’image sur une région d’intérêt.
5. Reconstruction des CINE fœtaux
- Reconstruire les CINE du flux fœtal en utilisant les données IRM corrigées du mouvement et le CS avec 10 itérations d’une optimisation de descente de gradient conjugué avec régularisation STV (poids: 0,025) et TTV (poids: 0,01). Deux CINE sont produits à cette étape : l’un pour l’acquisition compensée par le flux, CFC, et l’autre avec les données codées en flux, CFE, comme représenté dans le schéma de la figure 1D.
- Calculer l’image de vitesse donnée par la phase du produit élémentaire de CFE et le conjugué complexe de CFC.
- Appliquer la correction de phase de fond31 pour corriger les effets des courants de Foucault. Brièvement, dans cette étape automatique, un plan est ajusté à la phase des tissus statiques fœtaux et maternels. La correction est effectuée en soustrayant le plan de la phase sensible à la vitesse calculée en 4.2.
- Écrivez les données reconstruites dans des fichiers DICOM.
- Chargez les DICOM dans un logiciel d’analyse de flux, tel que Segment v2.232.
- Dessinez un retour sur investissement englobant la lumière du vaisseau sanguin d’intérêt à l’aide des images anatomiques et sensibles à la vitesse.
- Propager le retour sur investissement à toutes les phases cardiaques et corriger les changements de diamètre du vaisseau.
- Enregistrer les mesures de débit.
Résultats
En général, les examens IRM de phase du flux ciblent six vaisseaux fœtaux principaux: l’aorte descendante, l’aorte ascendante, l’artère pulmonaire principale, le canal artériel, la veine cave supérieure et la veine ombilicale. Ces vaisseaux intéressent le clinicien car ils sont souvent impliqués dans la coronaropathie et la FGR, influençant la distribution du sang dans tout le fœtus9. Une durée de balayage typique avec l’IRM à contraste de phase radial est de 17 s par vaisseau,...
Discussion
Cette méthode permet la mesure non invasive du flux sanguin dans les grands vaisseaux fœtaux humains et permet une correction rétrospective du mouvement et un blocage cardiaque en utilisant des techniques de reconstruction itérative. La quantification du flux sanguin fœtal a été réalisée par IRM au cours des 1,3,8,9 dernièresannées. Ces études avaien...
Déclarations de divulgation
Aucun.
Remerciements
Aucun.
matériels
| Name | Company | Catalog Number | Comments |
| elastix | Image Sciences Institute, University Medical Center Utrecht | Image registration software | |
| Geforce GTX 960 | Nvidia | 04G-P4-3967-KR | |
| gpuNUFFT | CAI²R | Non-uniform fast Fourier transform | |
| MAGNETOM Prisma | Siemens | 10849583 | |
| MATLAB | MathWorks | ||
| Radial Phase Contrast MRI sequence | Trajectory modification of manufacturer's Cartesian Phase Contrast sequence | ||
| Segment | Medvisio | Data analysis | |
| VENGEANCE | Corsair | LPX DDR4-2666 |
Références
- Zhu, M. Y., et al. The hemodynamics of late-onset intrauterine growth restriction by MRI. American Journal of Obstetrics and Gynecology. 214 (3), 1-17 (2016).
- Zhu, M. Y., Jaeggi, E., Roy, C. W., Macgowan, C. K., Seed, M. Reduced combined ventricular output and increased oxygen extraction fraction in a fetus with complete heart block demonstrated by MRI. HeartRhythm Case Reports. 2 (2), 164-168 (2016).
- Sun, L., et al. Reduced Fetal Cerebral Oxygen Consumption is Associated With Smaller Brain Size in Fetuses With Congenital Heart Disease. Circulation. 131 (15), 1313-1323 (2015).
- Freud, L. R., et al. Fetal aortic valvuloplasty for evolving hypoplastic left heart syndrome: postnatal outcomes of the first 100 patients. Circulation. 130 (8), 638-645 (2014).
- Peleg, D., Kennedy, C. M., Hunter, S. K. Intrauterine growth restriction: identification and management. American Family Physician. 58 (2), 453-467 (1998).
- Krishna, U., Bhalerao, S. Placental Insufficiency and Fetal Growth Restriction. Journal of Obstetrics and Gynaecology of India. 61 (5), 505-511 (2011).
- Seravalli, V., Miller, J. L., Block-Abraham, D., Baschat, A. A. Ductus venosus Doppler in the assessment of fetal cardiovascular health: an updated practical approach. Acta Obstetricia et Gynecologica Scandinavica. 95 (6), 635-644 (2016).
- Seed, M., et al. Feasibility of quantification of the distribution of blood flow in the normal human fetal circulation using CMR: a cross-sectional study. Journal of Cardiovascular Magnetic Resonance. 14 (1), 79 (2012).
- Prsa, M., et al. Reference ranges of blood flow in the major vessels of the normal human fetal circulation at term by phase-contrast magnetic resonance imaging. Circulation. Cardiovascular Imaging. 7 (4), 663-670 (2014).
- Piontelli, A. . Development of Normal Fetal Movements: The Last 15 Weeks of Gestation. , (2015).
- Cartier, M., et al. The normal diameter of the fetal aorta and pulmonary artery: echocardiographic evaluation in utero. American Journal of Roentgenology. 149 (5), 1003-1007 (1987).
- Ruano, R., de Fátima Yukie Maeda, M., Niigaki, J. I., Zugaib, M. Pulmonary artery diameters in healthy fetuses from 19 to 40 weeks' gestation. Journal of Ultrasound in Medicine. 26 (3), 309-316 (2007).
- Nowak, D., Kozłowska, H., Żurada, A., Gielecki, J. Diameter of the ductus arteriosus as a predictor of patent ductus arteriosus (PDA). Central European Journal of Medicine. 6 (4), 418-424 (2011).
- Goolaub, D. S., et al. Multidimensional fetal flow imaging with cardiovascular magnetic resonance: a feasibility study. Journal of Cardiovascular Magnetic Resonance. 20 (1), 77 (2018).
- Roy, C. W., Seed, M., Kingdom, J. C., Macgowan, C. K. Motion compensated cine CMR of the fetal heart using radial undersampling and compressed sensing. Journal of Cardiovascular Magnetic Resonance. 19 (1), 29 (2017).
- van Amerom, J. F. P., et al. Fetal cardiac cine imaging using highly accelerated dynamic MRI with retrospective motion correction and outlier rejection. Magnetic Resonance in Medicine. 79 (1), 327-338 (2018).
- Lustig, M., Donoho, D., Pauly, J. M. Sparse MRI: The application of compressed sensing for rapid MR imaging. Magnetic Resonance in Medicine. 58 (6), 1182-1195 (2007).
- Edwards, D. D., Edwards, J. S. Fetal movement: development and time course. Science. 169 (3940), 95-97 (1970).
- Malamateniou, C., et al. Motion-Compensation Techniques in Neonatal and Fetal MR Imaging. American Journal of Neuroradiology. 34 (6), 1124-1136 (2013).
- Rutherford, M., et al. MR imaging methods for assessing fetal brain development. Developmental Neurobiology. 68 (6), 700-711 (2008).
- Haris, K., et al. Self-gated fetal cardiac MRI with tiny golden angle iGRASP: A feasibility study: Self-Gated Fetal Cardiac MRI with iGRASP. Journal of Magnetic Resonance Imaging. 46 (1), 207-217 (2017).
- Glenn, O. A. MR imaging of the fetal brain. Pediatric Radiology. 40 (1), 68-81 (2010).
- Rodríguez-Soto, A. E., et al. MRI Quantification of Human Fetal O2 Delivery Rate in the Second and Third Trimesters of Pregnancy. Magnetic Resonance in Medicine. 80 (3), 1148-1157 (2018).
- Sameni, R., Clifford, G. D. A Review of Fetal ECG Signal Processing; Issues and Promising Directions. The Open Pacing, Electrophysiology & Therapy Journal. 3, 4-20 (2010).
- Millis, R. Advances in Electrocardiograms: Methods and Analysis. BoD - Books on Demand. , (2012).
- Jansz, M. S., et al. Metric optimized gating for fetal cardiac MRI. Magnetic Resonance in Medicine. 64 (5), 1304-1314 (2010).
- Yamamura, J., et al. Cardiac MRI of the fetal heart using a novel triggering method: initial results in an animal model. Journal of Magnetic Resonance Imaging: JMRI. 35 (5), 1071-1076 (2012).
- Larson, A. C., et al. Self-gated cardiac cine MRI. Magnetic Resonance in Medicine. 51 (1), 93-102 (2004).
- Knoll, F., Schwarzl, A., Diwoky, C., Sodickson, D. K. gpuNUFFT-An open source GPU library for 3D regridding with direct Matlab interface. Proceedings of the 22nd Annual Meeting of ISMRM. , (2014).
- Klein, S., Staring, M., Murphy, K., Viergever, M. A., Pluim, J. P. W. elastix: a toolbox for intensity-based medical image registration. IEEE Transactions on Medical Imaging. 29 (1), 196-205 (2010).
- Walker, P. G., et al. Semiautomated method for noise reduction and background phase error correction in MR phase velocity data. Journal of Magnetic Resonance Imaging. 3 (3), 521-530 (1993).
- Heiberg, E., et al. Design and validation of Segment - freely available software for cardiovascular image analysis. BMC Medical Imaging. 10 (1), 1 (2010).
- Inder, T. E., Volpe, J. J. Chapter 17 - Intrauterine, Intrapartum Assessments in the Term Infant. Volpe's Neurology of the Newborn (Sixth Edition). , 458-483 (2018).
- Pelc, N. J., Herfkens, R. J., Shimakawa, A., Enzmann, D. R. Phase contrast cine magnetic resonance imaging. Magnetic Resonance Quarterly. 7 (4), 229-254 (1991).
- Steeden, J. A., Atkinson, D., Hansen, M. S., Taylor, A. M., Muthurangu, V. Rapid flow assessment of congenital heart disease with high-spatiotemporal-resolution gated spiral phase-contrast MR imaging. Radiology. 260 (1), 79-87 (2011).
- Kowalik, G. T., Knight, D., Steeden, J. A., Muthurangu, V. Perturbed spiral real-time phase-contrast MR with compressive sensing reconstruction for assessment of flow in children. Magnetic Resonance in Medicine. 83 (6), 2077-2091 (2020).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon