ייצור ביופילם ביומסה חיידקית גדולה יותר באמצעות מכשירי מיקרופלאט עמוק באר עמוקה צלחת PCR
In This Article
Summary
פרוטוקול זה מציג מתודולוגיה לביצוע צמיחת ביופילם ומדידות ביומסה באמצעות התקני לוח PCR עמוקים בהרכבה עצמית עבור הקרנת ביופילם סטטית של מכסה 96-היטב.
Abstract
ביופילמים חיידקיים קשים להשמדה ממשטחים באמצעות התערבויות אנטי מיקרוביאליות קונבנציונליות. שיטות מיקרו-פלטה בעלות תפוקה גבוהה של 96 well משמשות לעתים קרובות לטפח ביופילמים חיידקיים לבדיקות רגישות מיקרוביאלית מהירות לחישוב ערכי ריכוז השמדת ביופילם מינימלי (MBEC). התקני ביופילם סטנדרטיים מורכבים ממכסים צמודים פוליסטירן המותקנים במיקרו-פלטות של 96 well והם אידיאליים למדידת ביומסה ביופילם וערכי MBEC, אך התקנים אלה מוגבלים על ידי שטח פנים זמין של peg להצטברות ביומסה ועלות. כאן, אנו מתארים פרוטוקול לשימוש פוליפרופילן בהרכבה עצמית 96-גם עמוק היטב PCR צלחת PCR מצורף התקן כדי לגדל Escherichia coli BW25113 ו Pseudomonas aeruginosa PAO1 biofilms. השוואה של ביופילמים 24 שעות ביממה שנוצרו במכשירי באר סטנדרטיים ועמוקים על ידי כל מין באמצעות כתמי ביומסה סגול קריסטל ובדיקות נחישות MBEC מתוארים. שטח הפנים הגדול יותר של מכשירי באר עמוקה צפוי להגדיל את היווצרות הביופילם הכוללת על ידי שני המינים פי 2-4. P. aeruginosa נוצר ביומסה גדולה יותר באופן משמעותי / mm2 על יתדות באר עמוקה בהשוואה למכשיר הסטנדרטי. E. coli היה ביומסה גדולה יותר / mm2 על התקני פוליסטירן סטנדרטיים בהשוואה למכשיר באר עמוקה. בדיקות השמדת ביופילם עם חומרי חיטוי כגון נתרן היפוכלוריט (אקונומיקה) או בנזלקוניום כלוריד (BZK) הראו כי שתי התרכובות יכולות לחסל E. coli ו - P. aeruginosa biofilms משני המכשירים אך בערכי MBEC שונים. השמדת ביופילם BZK הביאה לערכי E. coli MBEC משתנים בין התקנים, עם זאת, אקונומיקה הדגימה ערכי MBEC הניתנים לשחזור הן עבור מינים והן עבור התקנים. מחקר זה מספק שיטת באר עמוקה תפוקה גבוהה לגידול כמויות גדולות יותר של ביופילמים במכשירי פוליפרופילן למחקרים במורד הזרם הדורשים כמויות גבוהות יותר של ביופילם סטטי.
Introduction
פסאודומונס ארוגינוזה ואשריצ'יה קולי הם פרוטאובקטריה גראם-שלילית הנחקרים בדרך כלל על יכולתם ליצור קהילות תאים ססיליות המחוברות לפני השטח המכונות ביופילמס1. שני המינים, כאשר גדלים כמו biofilms, יכול להפריש מטריצה של חומרים פולימריים חוץ תאיים (EPS) המורכב בעיקר של פוליסכרידים שונים וחלבונים, שיכולים לכלול גם DNA חוץ תאית ו/או שומנים, מתן הגנה תאית נוספת הישרדות משופרת בסביבות קשות, מוגבלות בחומרים מזינים2,3. פיזיולוגיה ביופילם והיווצרות על ידי שני המינים היא בעלת רלוונטיות קלינית, שכן הם מייצגים את חמשת הפתוגנים האנטי-מיקרוביאליים המבודדים ביותר מדם המטופלים בבית החולים, בדרכי השתן וזיהומי ריאות בקנדה4,5. חשוב גם לציין כי ביופילמים מוערכים מהווים כמעט 80% מכלל הזיהומים הכרוניים החוזרים ונשנים הנגרמים על ידי מינים חיידקיים אלה6. בשל חומרי EPS המופרשים ופעילות מטבולית איטית יותר7,8, ביופילמים מבוססים הופכים קשים יותר להשמדה כאשר הם נוצרים על משטחים כגון מכשירים רפואיים מושתלים, רקמות צלקת, ובריאות של חולי סיסטיק פיברוזיס9,10, מה שמוסיף להתנגדות האנטי מיקרוביאלית שלהם.
תכונות הצמיחה הסרבנות של ביופילמים חיידקיים לעתים קרובות להפוך אותם עמידים יותר לעיכוב מיקרוביאלי ו/או השמדה2,9. לכן, הקמת שיטות הפריה חוץ גופית לחקר השמדה מיקרוביאלית ביופילם חיידקי היא בעלת חשיבות עליונה לבחירת תרכובות יעילות למיגור זיהומים כאשר הם נוצרים על פלסטיק רפואי (למשל, קטטרים במגורים) ושתלים רפואיים. שיטות ההשמדה המהירות ביותר של ביופילם ביופילם אנטי-מיקרוביאלית בוחנות את צמיחת הביופילם כתרבות ביופילם "סטטית" ולא כתרבויות "רציפה", שבהן צמיחת חיידקים סטטיים מנוטרת בשלבים מוקדמים עד מאוחרים של היווצרות ביופילם על פני מסגרת זמן קצרה (24-96 שעות) באותו מדיום צמיחה. שיטות ביופילם מתמשכות מסורבלות לניתוח מהיר מכיוון שהן דורשות צמיחה ביופילמית המוערכת על פני מסגרות זמן ארוכות יותר הגדלות בתאים המאפשרות זרימה רציפה והחלפה של מדיה צמיחה עם פחות replicates11. בשל הזמן והמאמץ הנדרשים כדי לתחזק ולהקים ביופילמים רציפים, ביופילמים במבחנה סטטיים הם הפופולריים ביותר, שכן הם מותאמים בקלות לבדיקות רגישות מיקרוביאלית בתפוקה גבוהה בלוחות מיקרוטיטר מפלסטיק 96-well במקום מערכות תא זרימה משוכללות המגבילות את מספר התרבויות שנבדקו בו זמנית 12,13 . בדיקות המיקרופלאט הסטטיות הפשוטות ביותר של biofilm "in-well" משתמשות בלוחות מיקרוטירן או ויניל סטנדרטיים (קיבולת של 300 μL) כדי למדוד היווצרות ביופילם בצדדים ובתחתית של כל באר ולעתים קרובות כטבעות באוויר לממשק משטח נוזלי. היווצרות ביופילם חיידקי בבאר נמדדת על ידי הכתמת הביומסה שהופקדה דבוקה לבארות לאחר הסרת הנוזל הבינוני לצמיחה והביופילמים נשטפים 12,13. בדיקות אלה הן פופולריות מבחינה כלכלית, אך לעתים קרובות יש בעיות רבייה בשל העיצוב הטבוע שלהם, כמו biofilms שהופקדו נוטים נזק או אובדן במהלך שטיפה עבור התאוששות תאים ו biomass מכתים הליכים 11,14.
כדי להפחית את הפסדי הביופילם, התקני ביופילם מסחריים סטנדרטיים השתפרו על עיצובי מיקרופלסטיק ביופילם בבאר על ידי הוספת מכסה פוליסטירן מוצמד 96 היטב לתכנון הלוחות הסטנדרטי 96 in-well, המכונה "התקן הביופילם הסטנדרטי" כאן. התוספת של מכסה צמוד מרחיבה את שטח הפנים הזמין בכל מיקרופלטה היטב, ומאפשרת דבקות משופרת במשטח ותצורת ביומסה ביופילם15,16. התקני מכסה מתויגים ביופילם סטנדרטיים מאפשרים שחזור, הסרה ושטיפה גדולים יותר של ביופילם עבור בדיקות רגישות וביופילם אנטי מיקרוביאלית עוקבות ובדיקות השמדה כאשר מכסים צמודים מוחדרים ללוחות מיקרוטיטר חדשים המכילים אתגרים של תרופות או מצבי גדילה. בדומה לטכניקות מיקרופלסטיק ביופילם בבאר, החומרים התאוששו ממכשירי המכסה שהוסרו ושטופו מאפשרים בדיקות הישרדות תאים וכתמים ביופלזמה ביופילם, בדרך כלל מעורבים קריסטל סגול (CV) ניסוחים צבע 17,18,19. התקני ביופילם סטנדרטיים הם גם אופטימליים להקרנת רגישות אנטי-מיקרוביאלית ביופילם. בדיקות אלה לפקח על עיכוב גדילה biofilm בשתי דרכים: 1) כאשר antimicrobials מתווספים לתאים בתחילת הצמיחה, זה יכול לקבוע את הריכוז המינימלי לעיכוב ביופילם (MBIC) ערך. 2) כאשר ביופילמים מבוססים נוצרים על היתדות לאחר 24 שעות ולאחר מכן נחשף antimicrobials, זה יכול לקבוע את ריכוז השמדת biofilm המינימלי (MBEC) ערך 17,20. בדומה למכשירי מיקרופלסטיק ביופילם בבאר, להתקני ביופילם סטנדרטיים יש כמה מגבלות בולטות, כגון העלות הגבוהה שלהם למכשיר, הם אינם ניתנים להעברה אוטומטית, ועמידים פחות לממסים כימיים בשל חומר צלחת פוליסטירן המשמש. התקנים ביופילם סטנדרטיים יש גם שטח פנים נמוך ליחס peg, אשר מגביל את נפחי העבודה המרביים בכל באר ל 200 μL. גורמים אלה יכולים להפוך התקני ביופילם סטנדרטיים למאתגרים יותר לשימוש במחקרים הדורשים כמויות גדולות יותר של ביופילם בתבנית בעלת תפוקה גבוהה.
כאן, אנו מתארים שיטת ביופילם סטטית עם מכסה 96-well שפותחה במעבדה שלנו באמצעות פוליפרופילן זמין מסחרית חצי חצאית 0.5 מ"ל 96-well לוחות PCR מצויד לוחות microtiter 96-well מצויד 96-well microtiter לוחות בעל בארות עמוק יותר מאשר הצלחת הסטנדרטית (שולחן החומרים). התקנים מורכבים אלה יש נפח עבודה מרבי של 750 μL כאשר נעשה שימוש לגידול biofilm (כאן המכונה "התקן ביופילם באר עמוקה"). היתרונות של שימוש במכשירי ביופילם עמוקים אלה הם העלות הנמוכה יותר שלהם בהשוואה למכשירי ביופילם סטנדרטיים, הם יכולים להיות מעוקרים על ידי autoclaving, והם מגדילים את שטח הפנים להיווצרות ביופילם על צלחת PCR חיצונית גדולה יותר "צינור / יתדות". בשיטה זו אנו מציגים את היישומים של מכשירים אלה לגידול ואפיון ביופילם ביומסה שנוצרה על ידי Escherichia coli BW25113 ו P. aeruginosa PAO1. שיטות לקביעת ערכי MBEC באמצעות בדיקות השמדת ביופילם מתוארות באמצעות תרכובת אמוניום רבעוני בנזלקוניום כלוריד (BZK) ונתרן היפוכלוריט (אקונומיקה) אנטימיקרוביאלים. BZK חיטוי/חיטוי נבחר כמו תרכובת זו משמשת לעתים קרובות כדי לעכב biofilms מפני משטחים מזוהמים, אבל זה על פי דיווחים פחות יעיל במיגור biofilms מבוסס היטב21. אקונומיקה היא חומר כימי יעיל ביותר למיגור ביופילמים מבוססים והיא עמוד התווך בחיטוי כימי 22. שני חומרי החיטוי מספקים השוואה שימושית של ערכי MBEC עבור כל התקן ביופילם21. פרוטוקול להערכת התקן ביופילם זה באמצעות כתמי קורות חיים ובדיקות השמדת ביופילם לקביעת MBEC מסוכם במאמר זה. תרשים זרימה של פרוטוקול נכלל לסקירה פשוטה יותר של זרימת העבודה עבור שיטות אלה (איור 1).
Protocol
1. הכנת תרבות אספטית לצמיחה ביופילם (ימים 0-1)
- ביום 0, פסים את זני החיידקים הרצויים לבדיקה מתוך מלאי שמור בהקפאה (בגליצרול או דימתילסולפוקסיד (DMSO)) ישירות על צלחת אגר מזין עם בחירה מיקרוביאלית כפי שהזן דורש. לוחות אגר דגירה בטמפרטורה האופטימלית (37 °C (37 °C )) וזמן (18-22 שעות) לצמיחת המתח.
- למחרת (יום 1), לחסן מושבה מצלחת אגר ב 5 מ"ל של מדיה צמיחה בתנאי צמיחה אופטימליים. תרבויות אלה ישמשו כיום 2 מתחיל חיסונים עבור התקנים biofilm (ראה שלב 2.2; איור 1).
הערה: עבור מחקר זה, E. coli K-12 BW21153 ו P. aeruginosa PAO1 גדלו לוריא-ברטאני (LB) בינוני ב 37 °C (67 °F עבור 18 שעות עם רועד ב 160 סיבובים לדקה (סל"ד).- הכן לפחות 3 זנים בתרבית עצמאית כדי ליצור שכפולים ביולוגיים למדידת ביופילם בשל השונות הסטטיסטית של היווצרות ביופלזמה ביופילם במכשירי המכסה המצורפים.
2. הכנה וחיסון של צלחות (יום 2)
- מלאו את הבארות החיצוניות של צלחת פוליפרופילן בעלת 96 מ"ל/1 מ"ל/באר אוטומטית עם 750 μL/well מים סטריליים (איור 2A). מלא את בארות השליטה השליליות (בארות מדיה uninoculated; עמודה B) עם מדיה צמיחה 750 μL ואת הבארות הנותרות עם 675 μL צמיחה מדיה.
הערה: שלב 2.1 לעיל והשלבים שלהלן מפרטים את אמצעי האחסון המתאימים להתקן הביופילם בבאר העמוקה. אם משתמשים בהתקן הביופילם הסטנדרטי, יש לשנות את אמצעי האחסון כדלקמן: 75 μL של תרבות inoculum ל 20 μL; 675 μL של מדיה צמיחה ל 180 μL; 750 μL של מים סטריליים / מדיה צמיחה ל 200 μL; 800 μL של CV כתמים / חומצה אצטית / פתרונות לשטוף ל 210 μL. בנוסף, עבור שלב 3.6 להלן, הספיגה ב 500nm (A550 ננומטר) ניתן לקרוא ישירות במיקרופלט פוליסטירן לאחר ערבוב בעת ערבוב בעת שימוש מיקרופלט התקן ביופילם סטנדרטי. - באמצעות תרביות לילה יום 1, לתקנן את התרביות לצפיפות אופטית ב 600 ננומטר (OD600nm) = 1.0 או תקן מקפרלנד של 0.5-1 יחידות.
- צור דילול סדרתי של פי 10 של כל תרבית מתוקננת במבחנות או צלחת מיקרוטיטר עמוקה של 96 היטב עד להגעה לדילול של 10-3 .
- חסן את המדיה המכילה בארות כפי שמוצג באיור 2B עם 75 μL של התרבות המדוללת 1 x 10-3 , לדילול חיידקי סופי של 10-4.
- הכנס בזהירות לוחית PCR משועבדת אוטומטית (מכסה צמוד) לתוך צלחת באר עמוקה מחוסנת. לוחות דגירה בתנאי מאמץ אופטימליים (37 °C (37 °C )) עם רעד (מקסימום 160 סל"ד) באינקובטור עם 50-60% לחות במשך 24 שעות.
3. קביעת ביומסה ביופילם ממכשירים באמצעות כתמי קורות חיים (יום 3)
- הסר באופן אספטי את המכסה התקוע ביופילם מכל מכשיר ושטוף על ידי החדרה לתוך צלחת באר עמוקה autoclaved מוכן עם 800 μL של תמיסת מלח פוספט סטרילית חוצץ (PBS)/ גם עבור 30 s כדי להסיר תאים פלנקטוניים.
- להכתמת ביומסה CV, העבירו את מכסה צלחת ה-PCR המוצמדת לצלחת חדשה שהוכנה עם 800 μL/well 0.1% (w/v) CV ב-dH2O וכתם למשך 5 דקות.
- הסר כתם עודף על ידי שטיפה של המכסה התקוע בצלחת באר עמוקה שהוכנה עם 800 μL / גם PBS סטרילי. אפשר לצלחות להתייבש במשך 10 דקות בארון בטיחות ביולוגית עם יתדות הפונות כלפי מעלה.
- מעבירים את מכסה צלחת ה-PCR היבשה לצלחת המכילה 800 μL/well 30% (v/v) חומצה אצטית ומאפשרים למכסה להסיר כתם למשך 5 דקות.
- הסר את מכסה יתד PCR המושחת וערבב את הפתרון ביסודיות על ידי צנרת. העבר 200 μL מלוחות הבאר העמוקים למיקרו-לוחית 96 באר סטנדרטית ומדוד את ספיגת פתרון הסרת ההכתמה באורך גל של 550 ננומטר (A550nm) בקורא מיקרו-לוחית אולטרה סגול (UV)/ גלוי (Vis).
- באמצעות ערכי A550nm הנמדדים, הפחת את הערך הריק הממוצע (בקרה שלילית) A550nm מכל ערך מדגם ביופילם. ממוצע כל ערך דגימת ביופילם A550nm מוסתר ריק המייצג שכפולים ביולוגיים מדגם.
4. ביופילים מאתגרים עם מיקרוביאלים לחישוב ערך MBEC אנטי-מיקרוביאלי של 24 שעות (יום 3)
- הכן פתרון מלאי מיקרוביאלית במים כי הוא פעמיים (2x) הריכוז של הריכוז האנטי מיקרוביאלי הגבוה ביותר הרצוי להיבדק.
- צור סדרת דילול כפולה של תמיסת המניות האנטי-מיקרוביאלית במדיה מרוכזת פי 2, כך שיהיו 8 ריכוזים מיקרוביאליים.
- כפי שניתן לראות באיור 2B, מלאו את הבארות החיצוניות של צלחת באר עמוקה משועבדת אוטומטית במים סטריליים של 750 μL/Well. מילוי עמודות B (שליטה שלילית; ללא חיידקים) ו- C (שליטה חיובית; ללא חשיפה מיקרוביאלית) של הצלחת עם 750 μL / גם צמיחה מדיה. מלאו את הבארות הנותרות ב-750 μL/Well של סדרת הדילול האנטי-מיקרוביאלית כפי שמוצג באיור 2B.
- הסר ושטוף את המכסה התקוע כמתואר בשלב 3.1 והעבר אותם לצלחת האתגר האנטי-מיקרוביאלית.
- לוחות דגירה עם רעד (מקסימום 160 סל"ד) בתנאי מאמץ מתאימים ולמסגרת זמן החשיפה הרצויה.
5. התאוששות של ביופלזמה ביופילם ממכסים צמודים (יום 4)
- הסר את המכסים החשופים מיקרוביאלית ושטוף כמתואר בשלב 3.1. העבר את המכסה התקוע לצלחת באר עמוקה עם 750 μL / היטב התאוששות מדיה בבארות הפנימיות ו 750 μL / גם סטרילי dH2O בבארות החיצוניות.
- להכנת מדיית שחזור של 70 מ"ל, שלבו 35 מ"ל של LB מרוכז 2x, 0.7 מ"ל של 100% טווין-20, 3.5 מ"ל של פתרון נטרול אוניברסלי פי 20 ו-30.8 מ"ל של dH2O סטרילי בבקבוק סטרילי.
- כדי להכין פתרון נטרול אוניברסלי מרוכז 20x, להוסיף 1.0 גרם של L-היסטידין, 1.0 גרם של L-ציסטאין, ו 2.0 גרם של גלוטתיון מופחת לנפח סופי של 20 מ"ל של dH2O. לסנן לחטא את הפתרון באמצעות מסנן 0.2 מיקרומטר ולאחסן ב 4 °C (4 °F).
- שים את המכשיר משלב 5.1 לתוך פח משני מצויד בתוך אמבט מים sonicating. Sonicate המכשירים במשך 30 דקות כדי לחלץ את biofilm מיתדות לתוך התקשורת ההתאוששות.
- לאחר sonication, להסיר את המכסה התקוע ולהניח מכסה צלחת שטוחה סטרילית על צלחת עמוקה היטב התאוששות צלחת מדיה. ניתן להשליך את המכסה המצורף.
- לוחות דגירה עם מדיה התאוששות משלב 5.3 בתנאי צמיחת המתח האופטימליים בן לילה (16-18 שעות).
6. קביעת ערכי MBEC של התקן (יום 5)
- למחרת, להעביר 200 μL מכל באר של צלחת באר עמוקה דגירה משלב 5.4 לצלחת מיקרוטיטר חדשה 96-well. קרא את OD600nm של כל באר באמצעות קורא מיקרו-לוחית טווח UV /Vis.
- הפחת שליטה שלילית (ריק uninoculated) ערכי OD600nm מכל ביופילם המכיל מדגם היטב.
- חשב את ערך ה- MBEC עבור כל דגימה באמצעות ערכי OD600nm , כאשר ערך MBEC הוא הריכוז האנטי מיקרוביאלי הנמוך ביותר שהביא לערך OD600nm הנמוך ביותר (שלא ניתן להבחין בו מהבקרה הלא מובחנת) עבור מדגם ספציפי של מינים/ זן שטופלו במיקרוביאלית.
תוצאות
מטרת המחקר הייתה לספק שיטה לביצוע נפח גדול יותר, תפוקה גבוהה (96-well), מדידות התקן ביופילם סטטי באמצעות מכשירי ביופילם עמוקים היטב. כאן, השווינו לוחית PCR חצי חצאיות בהרכבה עצמית המוחדרת למיקרו-לוחית באר עמוקה, הידועה בשם התקן הבאר העמוקה, למכשיר מכסה סטנדרטי נפוץ של ביופילם כדי לבחון את היכולות שלהם ליצור ביופילמים סטטיים. ביומסה מוכתמת CV ובדיקות השמדת ביופילם (MBEC) שימשו להערכת היווצרות ביופילם על ידי שני המכשירים.
כדי להשוות היווצרות ביופילם על ידי מינים שונים בכל מכשיר, הערכנו ביומסה ביופילם שנוצרה על ידי E. coli BW25113 ו P. aeruginosa PAO1 באמצעות ביופילם CV מכתים פרוטוקול17. למרות כתמי קורות חיים מדווחים בדרך כלל כערכי A550nm, בשל ההבדלים בנפחי הצמיחה של כל מכשיר ואזורי הפנים הזמינים שלהם המרנו ערכי כתם CV A550nm לריכוזי קורות חיים טוחנים בתמיסה. ריכוזי קורות חיים טוחנים היוו הבדלי נפח של כל מכשיר ואפשרו השוואה של ריכוזי קורות חיים המייצגים ביומסה התאוששה מכל מכשיר. התוצאות הראו כי שני המינים הפיקו באופן משמעותי יותר ביומסה במכשירי ביופילם עמוקים (פי 2.1 כפול E. coli; פי 4.1 P. aeruginosa) בהשוואה למכשיר הביופילם הסטנדרטי (איור 3A-B). תוצאה זו הייתה צפויה בהתחשב בשטח הפנים הגדול יותר של יתד PCR העמוקה (320.4 מ"מ2) בהשוואה לשטח הפנים הסטנדרטי של יתד ההתקן (108.9 מ"מ2). ממצא זה עולה בקנה אחד גם עם הגידול בנפחים המוגברים (750 μL) המשמשים בהתקן הביופילם עמוק היטב בהשוואה לבארות המכשיר הסטנדרטיות (200 μL). לפיכך, מכשירי באר עמוקה הגדילו הצטברות ביופלזמה ביופילם על יתדות צינור PCR לעומת יתדות קטנות יותר עם התקני ביופילם סטנדרטיים.
שני מכשירי הביופילם יצרו ביופילמים הניתנים לשחזור כאשר השווינו ביופילמים משוכפלים ביולוגית שנוצרו על ידי E. coli ו- P. aeruginosa (איור 3A-B). למרות התבוננות בהבדלים גדולים יותר בערכי M A550nm מוכתמים CV טכניים עבור כל זן שגדל על התקן הבאר העמוקה, לא היו הבדלים משמעותיים סטטיסטית כאשר השווינו את ערכי ה- CV M החציוניים עבור השכפול הביולוגי של כל מין במכשירים העמוקים או הסטנדרטיים באמצעות ניתוח דו-כיווני של שונות (ANOVA) או T-tests של סטודנט (שניהם p p > 0.05). ממצא זה מראה כי היווצרות ביופילם על ידי באר עמוקה והתקנים סטנדרטיים טופס biofilms לשחזור. עם זאת, התוצאות מכתימות קורות חיים הראו גם כי כאשר לקחנו בחשבון הבדלים בשטח הפנים יתד על כל מכשיר, היווצרות ביופלזמה biofilm על ידי E. coli ו P. aeruginosa הראה הבדלים משמעותיים סטטיסטית הצטברות ביומסה (טבלה 1). חישוב של ביומסה מוכתמת CV ממוצעת (M) לכל שטח פנים יתד ב- mm2 (CV M / mm2) עבור E. coli הראה כי היווצרות ביופילם הייתה נמוכה פי 1.5 במכשירי באר עמוקה פוליפרופילן בהשוואה למכשיר הביופילם הסטנדרטי (טבלה 1). עם זאת, התוצאה ההפוכה הושגה עבור P. aeruginosa, אשר הדגים פי 1.4 גבוה יותר CV M / mm2 על התקני פוליפרופילן עמוק באר בהשוואה למכשירי ביופילם סטנדרטיים (טבלה 1). למרות ההבדלים הספציפיים למינים שנצפו בהצטברות ביומסה ביופילם עם כל מכשיר, מכשיר הבאר העמוקה עדיין הדגים היווצרות ביומסה כוללת גדולה יותר (עלייה של פי 2-4) ביופילם על ידי כל מין (איור 3).
כדי לקבוע את יישומי בדיקת הרגישות האנטי-מיקרוביאלית של מכשיר הביופילם העמוק, השווינו שני חומרי חיטוי נפוצים, BZK ואקונומיקה, לפוטנציאל השמדת הביופילם שלהם. שני הכימיקלים משמשים בדרך כלל כדי למנוע (BZK) ו /או לחסל (אקונומיקה) ביופילמים חיידקיים ביישומים קליניים ותעשייתיים21,22,23. כל תרכובת נוספה בהגדלת ריכוזים של פי 2 לביופילמים שנוצרו על ידי E. coli ו- P. aeruginosa במכשירי הביופילם הסטנדרטיים והעמוקים22,23 (איורים 1, 2B). הריכוז הנמוך ביותר של BZK או אקונומיקה שהביאו לערכי OD600nm שלא ניתן להבחין בהם מבארות בקרה שליליות הוגדרו כערך MBEC. טיפול בביופילמים שנוצרו במכשירי ביופילם סטנדרטיים עם אקונומיקה הביא לאותם ערכי MBEC אקונומיקה של 0.625% עבור E. coli ו- P. aeruginosa (טבלה 1, איור 4A-B). ערכי MBEC אקונומיקה שנקבעו עבור E. coli ו- P. aeruginosa biofilm שנוצרו על מכשירי באר עמוקה הראו ערכי MBEC נמוכים פי 2-4 על ידי שני המינים (E. coli; 0.156%; P. aeruginosa 0.313%) בהשוואה למכשירים סטנדרטיים (טבלה 1). הבדל של פי 2 בערכי אקונומיקה MBEC בין מינים צוין עבור מכשיר הבאר העמוקה, שבו P. aeruginosa נדרש ריכוז גבוה פי 2 של אקונומיקה כדי למגר ביופילמים לעומת E. coli (איור 4A-B, טבלה 1). ההבדל MBEC אקונומיקה פי שניים בין P. aeruginosa ו- E. coli בהתקן באר עמוקה נראה בקורלציה הפוכה עם היווצרות ביומסה מוכתמת CV פי 1.5 על ידי P. aeruginosa לעומת E. coli (איור 3A-B). הכמות הגדולה יותר של ביומסה שנוצרה על ידי P. aeruginosa על יתדות התקן באר עמוקה עשויה גם להסביר מדוע ריכוז אקונומיקה גבוה יותר נדרש כדי לחסל את הביופילמים של P. aeruginosa בהשוואה ל- E. coli על בארות עמוקות (איור 3A-B, טבלה 1). לפיכך, בדיקות מיגור ביופילם התקן עמוקות מראות כי שני המינים היו רגישים להלבנה אך בריכוזי אקונומיקה נמוכים יותר (פי 2-4) בהשוואה למכשירים סטנדרטיים. זה מתואם באופן הפוך עם שטח הפנים הגדול פי 3 של peg ונפחים של יתדות צלחת PCR התקן עמוק היטב. זה מצביע על כך עבור חשיפה אקונומיקה, שטח פנים ביומסה גדול יותר עשוי להוריד את ריכוזי אקונומיקה הדרושים למיגור biofilm.
בדיקות מיגור ביופילם של BZK הראו שונות רבה יותר בצמיחה התאוששה (ערכי OD600nm) וערכי MBEC על ידי כל מין בהשוואה לתוצאות אקונומיקה (איור 4C-D). שונות זו אינה בלתי צפויה בהתבסס על מחקרים קודמים המראים כי BZK היה יעיל יותר במניעת היווצרות ביופילם מאשר השמדת ביופילמים מבוססים24,25,26. באמצעות התקן הביופילם הסטנדרטי, רק ביופילמים P. aeruginosa שטופלו ב- BZK הראו ערך MBEC עקבי (2560 מיקרוגרם/ מ"ל) שהיה נמוך פי 8 מערך ה- MBEC (20480 מיקרוגרם/ מ"ל) שהושג עבור זן זה בהתקן הבאר העמוקה (טבלה 1, איור 4C). תוצאות אלה עשויות לשקף הבדלים בכמויות של ביומסה P. aeruginosa שנוצר על משטחים עמוקים היטב מוקף היטב קומפוזיציות פלסטיק בהשוואה יתדות המכשיר הסטנדרטי. השמדת BZK של ביופילמים שנוצרו על ידי E. coli הן על הבאר העמוקה והן במכשירים הסטנדרטיים היו גרועים באותה מידה, וכתוצאה מכך מגוון רחב של ערכי BZK MBEC מ 2560-40960 מיקרוגרם / מ"ל עבור התקן הבאר העמוקה ו 320-10240 מיקרוגרם / מ"ל במכשיר הסטנדרטי (איור 4D). עבור E. coli, שונות זו הוסברה על ידי מקרה מזדמן שבו 1-2 לשכפל בארות הראו צמיחה נמוכה אך משמעותית סטטיסטית במדיית ההתאוששות, כי שגיאה מוגברת ודיוק קביעת BZK MBEC מופחת עם כל אחד מהמכשירים (איור 4D, טבלה 1). שונות זו מדגישה את חוסר היעילות של שימוש ב- BZK במיגור ביופילמים של E. coli כפי שצוין בעבר במחקרים24,25,26. לעומת זאת, ניתן להשמיד באופן אמין את הביופילמים של P. aeruginosa על ידי BZK בריכוז מוגדר עם שני המכשירים, אך עם הפרש ריכוז BZK של פי 8 (איור 4C). לסיכום, ערכי BZK השמדת MBEC של ביופילמים שנוצרו על ידי P. aeruginosa להראות ערכי MBEC נפרדים עם כל מכשיר, עם זאת, שני ההתקנים הם עניים באותה מידה בהבחנה E. coli מדויק BZK הפנוטיפים השמדה.
לפיכך, שיטת התקן biofilm באר עמוק המתוארת כאן יעילה באופן דומה ליצירת ביופילמים לשחזור בהשוואה למכשיר ביופילם סטנדרטי..

איור 1. סקירה סכמטית של הניסוי. יום 0 בידוד של מושבות בודדות מהמלאי ההקפאה; יום 1 חיסון של תקשורת צמיחה עם מושבות בודדות; יום 2 חיסון של צלחת ביופילם; יום 3 CV כתמים או אתגר מיקרוביאלי; יום 4 biofilm sonication לתוך מדיה התאוששות; ויום 5 קריאת OD600nm של צלחת שחזור כדי לקבוע את ערכי MBEC. כמה תמונות באיור שסופקו על ידי Servier רפואי אמנות (smart.servier.com). לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 2. פריסות לוח לדוגמה המוצגות עבור שלבים שונים של הפרוטוקול. A) הגדרת הלוח הסופית לצמיחה הראשונית של ביופילם של 24 שעות באמצעות תרביות חיידקים של יום 1 משני זני חיידקים (E. coli ו - P. aeruginosa), כל אחד עם שלושה העתקים ביולוגיים. בארות בקרה שליליות (אפורות) משמשות לבקרות סטריליות (לא נוספו חיידקים). B) הגדרת צלחת לאתגר מיקרוביאלי של ביופילמים. צבעים כהים מצביעים על הגדלת הריכוז האנטי-מיקרוביאלי. שליטה שלילית היא בארות ללא תוספת חיידקים (אפור) ובקרות חיוביות הן ביופילמים ללא חשיפה מיקרוביאלית (כתומה). מכסי יתד ביופילם שנלקחו מלוח A מועברים לצלחת באר עמוקה זו לחשיפה מיקרוביאלית. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
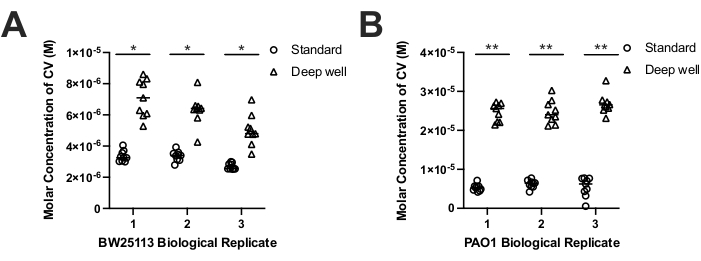
איור 3. ריכוז הטוחנת (M) של E. coli BW25113 מוכתם CV. (A) ו- P. aeruginosa PAO1 (B) ביופילם ביומסה התאוששה ממכשירים סטנדרטיים (עיגולים) ובאר עמוקה (משולשים). כתמי CV נמדדו על ידי קריאת הספיגה של CV ב 550 ננומטר (A550nm), וקריאות A550nm עמוקות הותאמו על ידי גורם של 3.809 (800 μL / 210 μL) כדי להסביר את ההבדלים בנפח בין המכשירים. ריכוז טוחנת CV (ז) נקבע על ידי חוק באר-למברט (ריכוז קורות חיים = A550nm / εl); כאשר אורך הנתיב (l) של 210 μL בצלחת מיקרוטר תחתונה שטוחה היטב 96 נקבע להיות 0.56 ס"מ ואת מקדם ההכחדה (ε) של קורות חיים במים ב A550nm של 251500 ס"מ-1M-139. התוצאות מייצגות 9 העתקים טכניים משלושה העתקים ביולוגיים של כל זן הגדלים כקובץ ביופילם והערך החציוני של כל העתק ביולוגי מוצג כפס אופקי בכל חלקה. הבדלים מובהקים סטטיסטית בביומסה בין המכשירים נקבעו בין ערכים חציוניים משוכפלים ביולוגיים באמצעות בדיקת t משויכת דו-זנבית (E. coli p = 0.008-0.018 (*); P. aeruginosa p= 0.002-0.009 (**)) מוצג כסורגים עם כוכביות. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
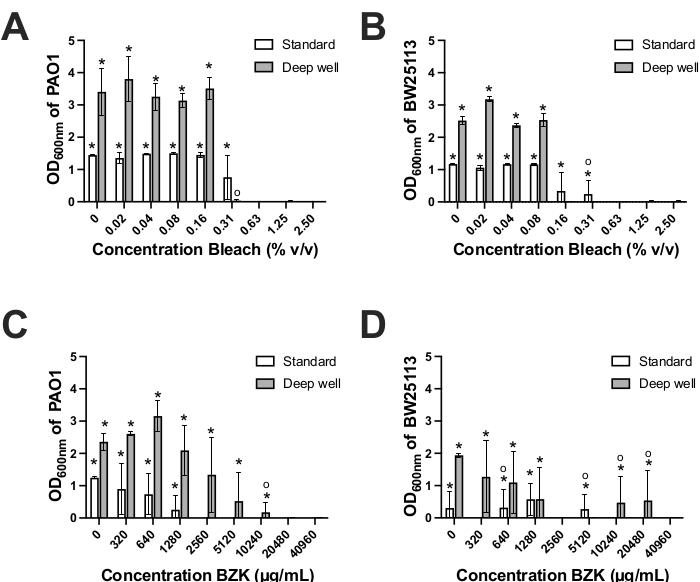
איור 4. קביעת ריכוז MBEC מיקרוביאלית. קביעת ריכוז MBEC מיקרוביאלית עבור אקונומיקה (A,B) ו- BZK (C,D) עבור P. aeruginosa PAO1 (A, C) ו - E. coli BW25113 (B,D) כאשר גדל על סטנדרטי (סורגים לבנים) ובאר עמוקה (פסים אפורים) התקנים מתויגים biofilm. התוצאות נקבעו על ידי קריאה של OD600nm של biofilm התאושש לאחר sonication לתוך מדיה התאוששות דגירה לילה. באר עמוקה OD600nm הותאם על ידי גורם של 3.75 (750 μL / 210 μL) כדי להסביר הבדלי נפח בין ההתקנים. התוצאות מייצגות שלושה שכפולים ביולוגיים וקווי שגיאה מראים את סטיית התקן בין שכפולים בכל ריכוז מיקרוביאלי39. כוכביות (*) מעל כל תרשים מייצג פעילות מציינות הבדלים מובהקים סטטיסטית בערכי OD600nm מפקדים ריקים עם ערכי p < 0.05 באמצעות חישובי T של סטודנט דו-זנבי. סימני עיגול (o) מעל כל התוויית מייצגי פעילויות מציינים מדידות שבהן רק ל- 1 או 2 משוכפלים היו ערכי OD600nm משמעותיים סטטיסטית מפקדים ריקים. לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
| BZK MBEC (מיקרוגרם/מ"ל) | אקונומיקה MBEC (% v/v) | |||
| נבדק זן | התקן באר עמוקה | התקן רגיל | התקן באר עמוקה | התקן רגיל |
| אי קולי BW25113 | 2560-40960 | 320-10240 | 0.156 | 0.625 |
| פ. ארוגינוזה PAO1 | 20480 | 2560 | 0.313 | 0.625 |
| התקן באר עמוקה | התקן רגיל | p-value** | שינוי קיפול (באר עמוקה / סטנדרטי) | |
| נבדק זן | ממוצע CV M*/ מ"מ2 ± SD | ממוצע CV M*/ מ"מ2 ± SD | ||
| אי קולי BW25113 | 1.99 x 10-8 ± 3.25 x10-9 | 3.03 x 10-8 ± 3.31 x 10-9 | 0.0176 | -1.52 |
| פ. ארוגינוזה PAO1 | 8.01 x 10-8 ± 9.42 x 10-9 | 5.72 x 10-8 ± 9.42 x 10-9 | 0.034 | 1.4 |
טבלה 1. סיכום של E. coli BW25113 ו P. aeruginosa PAO1 פירושו ערכי ביומסה M / mm2 מוכתמים CV וערכי MBEC השמדת ביופילם עבור BZK ואקונומיקה במכשירים שונים.
*ערכי CV M/mm2 ממוצעים מחושבים באמצעות ערכי CV M של שכפול ביולוגי חציוני (איור 3).
**p-ערכים שנקבעו באמצעות מבחן T דו-זנבי של סטודנט.
Discussion
מחקר זה מתאר שיטות לשימוש בנפח גדול יותר 96-well תפוקה גבוהה תפוקה גבוהה התקן צמיחה biofilm סטטי מעורבים פוליפרופילן עמוק היטב microplate מצויד במכסה לוחית PCR חצי חצאיות להיווצרות ביופילם (התקן biofilm באר עמוקה; טבלת חומרים). השווינו ביופילמים שנוצרו עם מכשיר זה למכשיר ביופילם סטנדרטי פוליסטירן זמין מסחרית (טבלת חומרים). שיטת התקן הבאר העמוקה משתמשת באותם שלבים ופתרונות מתודולוגיים כמו התקן 17 הסטנדרטי באמצעי אחסון מותאמים ששונו עבור התקני הבאר העמוקה, מה שהופך את המכשיר הזה לאידיאלי להיווצרות ביופילם בקנה מידה גדול וניתוח ניסיוני. הצמיחה של E. coli BW25113 ו P. aeruginosa PAO1, שני מינים גרם שליליים הידועים ליצור biofilms, נבדקו עבור היווצרות ביומסה שלהם וחיטוי (BZK / אקונומיקה) ערכי MBEC באמצעות בשני המכשירים. השוואה של ביומסה מוכתמת CV שנוצרה על יתדות מכל מכשיר הראתה שגם E. coli וגם P. aeruginosa יצרו ביופילמים עם ביומסה גבוהה יותר במכשיר הביופילם העמוק בהשוואה למכשיר הסטנדרטי (איור 3A-B). ביומסה ביופילם מוגברת שיקפה את שטח הפנים הגדול יותר של יתדות באר עמוקה בהשוואה לשטח הפנים יתד המכשיר הסטנדרטי. כאשר לקחנו בחשבון את ההבדלים באזורי פני השטח של היתד (mm2) עם שני המכשירים, נרשמו הבדלים בהיווצרות ביומסה של ביומסה CV גדולה יותר באופן משמעותי למ"מ2 על יתדות התקן פוליסטירן סטנדרטי מאשר עם יתדות צינור PCR של המכשיר עמוק (טבלה 1). P. aeruginosa יצר ביומסה מוכתמת CV גדול יותר / peg mm2 בהשוואה למכשירים סטנדרטיים (טבלה 1). ממצאים אלה עשויים להדגיש הבדלים ספציפיים למינים בהיווצרות ביופלזמה ביופילם במכשירים השונים.
יש לציין כי השמדת אקונומיקה של ביופילמים של E. coli ו- P. aeruginosa במכשירי באר עמוקה התרחשה בריכוזים נמוכים פי 2-4 מהמכשיר הסטנדרטי (איור 4A-B, טבלה 1). ההבדלים בערכי MBEC אקונומיקה המזוהים מכל התקן מושפעים ככל הנראה מהבדלים בצורות יתדות ההתקן (באר עמוקה "יתדות" הן צינורות מחודדים ויתדות סטנדרטיות הן גליליות), הבדלי הרכב פלסטיק (פוליפרופילן לעומת פוליסטירן) והבדלים בנפח (750 μL לעומת 200 μL). לדוגמה, ל-P. aeruginosa היה ביומסה CV M גדולה יותר/ מ"מ2 על יתדות התקן באר עמוקה בהשוואה למכשירים סטנדרטיים, אבל ל-E. coli היה פחות ביומסה על יתדות באר עמוקה (איור 3). זה מצביע על כך שריכוזי חיטוי הנדרשים להשמדת ביופילם עשויים להיות מושפעים מהביומסה שנוצרת על ידי כל מין, כמו גם משטח הפנים הזמין. בנוסף, הבדלים בצורת יתד המכשיר עשויים להשפיע על תנאי גדילה שונים עבור מינים מסוימים. במחקר שלנו, P. aeruginosa עשוי ליצור ביומסה גדולה יותר על יתדות באר עמוקה בשל שטח הפנים הגדול יותר שלהם aeration, כמו מין זה הוא aerobe חובה בניגוד E. coli, שהוא אנרובה הפקולטית. עד כה, לא זיהינו כל מחקרים שפורסמו כי השוו ישירות E. coli ו P. aeruginosa biofilm היווצרות יחד על פוליפרופילן27,28,29 ופוליסטירן30,31 חומרים. עם זאת, דיווחים של חזק E. coli ו P. aeruginosa היווצרות biofilm כבר ציינו במחקרים עצמאיים בוחן או פוליפרופילן או חומרים פוליסטירן. לגבי פסאודומונדים, פסאודומונס רבים spp. יכול להשתמש בפלסטיק כגון פוליפרופילן כמקורות פחמן פוטנציאליים32. לפיכך, הזמינות של זה פוליפרופילן עמוק היטב biofilm המכשיר הוא התקדמות שימושית במחקרים ביופילם סטטי. פוליפרופילן הוא כימית עמיד יותר מאשר פוליסטירן והוא חומר רלוונטי מבחינה קלינית, כפי שהוא משמש לעתים קרובות שתלים רפואיים, תפרים, רשתות עבור ניתוחי בקע או אגן33,34.
למרות ביומסה biofilm נוצר על ידי שני המכשירים, המכשיר באר עמוקה היה שונות מעט גבוהה יותר ביומסה המבוססת על שיטת הכתמת CV ו OD600nm biofilm השמדת ערכי MBEC עבור אקונומיקה ו- BZK. זה יכול להיות מוסבר על ידי 3 גורמים עיקריים: 1) התקנים באר עמוקה יש שטח פנים peg גדול יותר מאשר התקנים סטנדרטיים שהיו בזווית לעומת יתדות התקן סטנדרטי. 2) שני המינים שנבדקו עשויים להיות בעלי יכולות שונות לדבוק בחומרי פוליפרופילן ופוליסטירן של כל מכשיר. 3) הנפחים של מדיה צמיחה בשימוש בכל מכשיר (750 μL עמוק היטב, 200 μL סטנדרטי) ומרווח בין היתד מוכנס לקירות הצד היטב שונה. בעיות אלה אינן מהווה בעיה אם רק סוג אחד של מכשיר משמש עבור כל ניסויי הביופילם, עם זאת, אם שני המכשירים נבחרים אז ההשוואות שערכנו כאן צריך להתבצע כדי לזהות הבדלים36,37. בשל ההבדלים בחומר הפלסטי המשמשים בכל מכשיר, אין להשוות ישירות את ביופילם ביופלזמה מוכתמת CV וערכי MBEC בין מכשירים שונים. עם זאת, אם שיטות וניסויים נערכים על אותו מכשיר (עמוק טוב או סטנדרטי), התוצאות המתקבלות עבור מינים ומיקרוביאלים שנבדקו דומים.
פרוטוקול זה מראה כי התקני לוח PCR עמוקים בהרכבה עצמית הם התקן ביופילם נפח גדול יותר למדידת היווצרות ביופילם והשמדה כי הוא גם חסכוני. מנקודת מבט של עלות, מכשירי ביופילם סטנדרטיים עם 96 מכסים מתויגים היטב נעים בקמעונאות במחיר של 29-36 דולר ארה"ב (USD) למכשיר (טבלת חומרים). התקני ביופילם סטנדרטיים פוליסטירן אינם ניתנים לlavlavable והם פחות סובלניים לממסים / חומצות בשל תכונות כימיות פלסטיק שלה. לוחות פוליפרופילן עמוקים בהרכבה עצמית המתוארים בזאת, מצוידים בלוח PCR נפרד 96 היטב חצאית היטב (טבלת חומרים) עלות בסך הכל $14 USD למכשיר מורכב, המהווה מחצית העלות הרגילה של התקן biofilm. יש לציין כי המחירים עשויים להשתנות בהתאם לאזור, המפיץ והזמינות, והעלויות שלנו לאחר הנחות מוסדיות הסתדרו עד $9 USD למכשיר באר עמוקה. אלה בהרכבה עצמית עמוק פוליפרופילן PCR צלחת התקנים יש את היתרון הנוסף של להיות autoclavable לעיקור ומציעים 2-4 פעמים יותר ביופילם ביומסה מאשר התקנים סטנדרטיים.
לסיכום, פרוטוקול זה והממצאים הייצוגיים מהשוואות הצמיחה של ביופילם של הבאר העמוקה והתקני הביופילם הסטנדרטיים מראים כי שני המכשירים מסוגלים לטפח ביופילמים חיידקיים, אך מכשירי באר עמוקה יוצרים פי 2-4 יותר ביופילם. התקן הביופילם העמוק מציע חלופה בת קיימא ובמחיר סביר לניסויי היווצרות ביופילם בנפח גבוה יותר, כגון מחקרי סינון רגישות לתרופות. טכניקה זו עשויה ליצור ביופילמים שימושיים עבור עקירות '-omics' במורד הזרם (פרוטאומי, מטבולומי, transcriptomic, transcriptomic) או בדיקות ניסיוניות (אנזימטי, פלואורסצנטי) שעשויות לדרוש כמויות גדולות יותר של חומרים ביופילם לניתוחים. התקן הביופילם העמוק מומלץ למעבדות המעוניינות לחקור ביופילמים בבדיקה בעלת תפוקה גבוהה של 96-well באמצעות עלות נמוכה יותר, נפח גדול יותר, חומרים פלסטיים עמידים כימית שרלוונטיים מבחינה קלינית.
Disclosures
למחברים אין שום גילויים לעשות.
Acknowledgements
המימון לעבודה זו ניתן על ידי מענקים תפעוליים ל- DCB מהמועצה למדע הטבע ומחקר ההנדסה של קנדה דיסקברי גרנט (RGPIN- 2016-05891) ול- MRM ו- GRG מממשלת גנומיקה קנדית מחקר ופיתוח יוזמת מענק (GRDI) תוכנית (GRDI7 2254557).
Materials
| Name | Company | Catalog Number | Comments |
| 10 mL serological pipets, individ wrap paper/plastic (200/CS) | Fisher Scientific | 13-678-11F | disposable serological pipettes for aseptic media/ culture transfer |
| 2 mL serological pipets, individ wrap paper/plastic, 500/CS | Fisher Scientific | 13-678-11C | disposable serological pipettes for aseptic media/ culture transfer |
| Axygen Aerosol Filter Tips, Sterile, 5 racks/ PK, 1000 tips/rack | Fisher Scientific | 14-222-766 | sterile pipettor tips for media aliquoting |
| Axygen deep well storage microplates, round wells, 1.1 mL cap, 5/PK, P-DW-11-C | Fisher Scientific | P-DW-11-C | microplate for 96 well deepwell device biofilm cultivation |
| Axygen Filter tips, 350 µL tips racked, 96/rack, 10 racks, low retention barrier tips | Fisher Scientific | TF-350-L-R-S | sterile pipettor tips for media aliquoting |
| Basin/reservoir natural PS 50 mL, Sterile, 5/bag, 40 bags, CS200 | Avantor/ VWR | 89094-676 | sterile basins/ reservoirs for microplate preparation |
| BD Difco Dehydrated Culture Media: Granulated Agar, 500 g | Fisher Scientific | DF0145-17-0 | materials for LB agar preparation |
| Biotek Synergy Neo2 multimode plate reader | Biotek | NEO2MB | microplate UV/Vis region plate reader |
| Branson M3800 Ultrasonic Bath, 117 V | Avantor/ VWR | CPX-952-316R | sonicating water bath |
| crystal violet (CV), ACS grade, 100 g | Fisher Scientific | C581-100 | biofilm biomass stain |
| Dimethyl sulfoxide (DMSO), 1 L, ACS grade 99.9%, poly bottle, BDH | Avantor/ VWR | CABDH1115-1LP | media components for cryopreservation |
| Easypet 3, pipet controller | Avantor/ VWR | CA11027-980 | serological pipettor for aseptic media/ culture transfer |
| Eppendorf Research Plus 8 multi-channel pipettor , 10-100 µL | Avantor/ VWR | CA89125-338 | multichannel pipettes for aseptic media/ culture transfer |
| Eppendorf Research Plus 8 multi-channel pipettor , 30-300 µL | Avantor/ VWR | CA89125-340 | multichannel pipettes for aseptic media/ culture transfer |
| Glacial acetic acid, CAS 64-19-7, 2.5L, ACS grade | Fisher Scientific | A38-212 | CV destain |
| Glass test tubes, 150 mm x 18 mm, 72/Pack, PYREX | Fisher Scientific | 14957H/ 9820-18 | materials for cell culturing |
| Glycerol, 4 L glass bottle ACS | Fisher Scientific | BP229-4 | media components for cryopreservation |
| L-Cysteine, 98%, 250 g | Avantor/ VWR | 97061-204 | universal neutralizing solution |
| L-glutathione reduced, 98%, 25 g | Fisher Scientific | AAJ6216614 | universal neutralizing solution |
| L-Hisitidine, 98%, 100 g | Avantor/ VWR | CA97062-598 | universal neutralizing solution |
| MBEC Assay Inoculator with 96 well tray, 100/CS | Innovotech | 19112 | material for 96 well MBEC device biofilm cultivation |
| McFarland Standard, 0.5 EA | Fisher Scientific | R20410 | cell culture standardization |
| McFarland Standard, 1.0 EA | Fisher Scientific | R20411 | cell culture standardization |
| NUNC 96-well microtiter plates, w/lid, 50/CS | Fisher Scientific | 167008 | microplate for 96 well MBEC device biofilm cultivation and OD measurements |
| PCR plate, semi-skirted 96 well, fast PCR, polypropylene, 25ea/PK | Sarstedt | 72.1981.202 | pegged lid for 96 well deepwell device biofilm cultivation |
| Petri dish, 100 mm x 15 mm, semi-TK CS/500 | Fisher Scientific | FB0875712 | materials for LB agar preparation |
| Potassium phosphate dibasic, ACS 500 g | Fisher Scientific | P288-500 | PBS component/ buffer |
| Sodium chloride, ACS grade, 3 kg | Fisher Scientific | S2713 | media components for LB broth and PBS |
| sodium phosphate monobasic, 1 kg | Fisher Scientific | S369-1 | PBS component/ buffer |
| Syringe filters, Sterile, PES 0.45 um, 25 mm, PK50 | Avantor/ VWR | 28145-505 | non-autoclavable solution sterilization |
| Tin foil, heavy duty, 50 feet | Grocery store | --- | materials for deepwell device sterilization |
| Tryptone (peptone from casein), 2.2 kg/EA | Fisher Scientific | B11922 | media components for LB broth |
| Tween-20, 100 mL | Fisher Scientific | BP337-100 | recovery media solution |
| Ultra-deepwell, 2.5 mL deep well plates (square well), with lid, polypropylene, 10/CS | Avantor/ VWR | 37001-520 | materials for biofilm dilution preparation |
| Yeast Extract, Fisher Bioreagents, 500 g | Fisher Scientific | BP1422-500 | media components for LB broth |
References
- Verderosa, A. D., Totsika, M., Fairfull-Smith, K. E. Bacterial Biofilm Eradication Agents: A Current Review. Frontiers in Chemistry. 7, 1-17 (2019).
- Sharma, D., Misba, L., Khan, A. U. Antibiotics versus biofilm: An emerging battleground in microbial communities. Antimicrobial Resistance and Infection Control. 8 (1), 1-10 (2019).
- Fux, C. A., Costerton, J. W., Stewart, P. S., Stoodley, P. Survival strategies of infectious biofilms. Trends in Microbiology. 13 (1), 34-40 (2005).
- Lagacé-Wiens, P. R. S., et al. Trends in antimicrobial resistance over 10 years among key bacterial pathogens from Canadian hospitals: results of the CANWARD study 2007-16. The Journal of Antimicrobial Chemotherapy. 74, 22-31 (2019).
- Karlowsky, J. A., et al. In vitro susceptibility of urinary Escherichia coli isolates to first- and second-line empirically prescribed oral antimicrobials: CANWARD surveillance study results for Canadian outpatients, 2007-2016. International Journal of Antimicrobial Agents. 54 (1), 62-68 (2019).
- Mah, T. F. Biofilm-specific antibiotic resistance. Future Microbiology. 7 (9), 1061-1072 (2012).
- Amato, S. M., et al. The role of metabolism in bacterial persistence. Frontiers in Microbiology. 5, 1-9 (2014).
- Flemming, H. -. C., Neu, T. R., Wozniak, D. J. The EPS matrix: The "house of biofilm cells.". Journal of Bacteriology. 189 (22), 7945-7947 (2007).
- Dela Fuente-Núñez, C., Reffuveille, F., Fernández, L., Hancock, R. E. W. Bacterial biofilm development as a multicellular adaptation: Antibiotic resistance and new therapeutic strategies. Current Opinion in Microbiology. 16 (5), 580-589 (2013).
- Høiby, N., et al. The clinical impact of bacterial biofilms. International Journal of Oral Science. 3 (2), 55-65 (2011).
- Merritt, J. H., Kadouri, D. E., O'Toole, G. A. Growing and analyzing static biofilms. Current Protocols in Microbiology. 01, (2005).
- Coffey, B. M., Anderson, G. G. Biofilm formation in the 96-well microtiter plate. Methods in Molecular Biology. 1149, 631-641 (2014).
- O'Toole, G. A. Microtiter dish Biofilm formation assay. Journal of Visualized Experiments. (47), e2437 (2010).
- Azeredo, J., et al. Critical review on biofilm methods. Critical Reviews in Microbiology. 43 (3), 313-351 (2017).
- Harrison, J. J., Turner, R. J., Ceri, H. High-throughput metal susceptibility testing of microbial biofilms. BMC Microbiology. 5 (53), (2005).
- Ceri, H., et al. The MBEC Assay System: Multiple Equivalent Bioffims for Antibiotic and Biocide Susceptibility Testing. Methods in Enzymology. 337, 377-385 (2001).
- Harrison, J. J., et al. Microtiter susceptibility testing of microbes growing on peg lids: a miniaturized biofilm model for high-throughput screening. Nature Protocols. 5 (7), 1236-1254 (2010).
- vanden Driessche, F., Rigole, P., Brackman, G., Coenye, T. Optimization of resazurin-based viability staining for quantification of microbial biofilms. Journal of Microbiological Methods. 98, (2014).
- Sabaeifard, P., Abdi-Ali, A., Gamazo, C., Irache, J. M., Soudi, M. R. Improved effect of amikacin-loaded poly(D,L-lactide-co-glycolide) nanoparticles against planktonic and biofilm cells of Pseudomonas aeruginosa. Journal of Medical Microbiology. 66 (2), 137-148 (2017).
- Thieme, L., et al. MBEC Versus MBIC: the Lack of Differentiation between Biofilm Reducing and Inhibitory Effects as a Current Problem in Biofilm Methodology. Biological Procedures Online. 21 (1), 18 (2019).
- Jennings, M. C., Ator, L. E., Paniak, T. J., Minbiole, K. P. C., Wuest, W. M. Biofilm-eradicating properties of quaternary ammonium amphiphiles: Simple mimics of antimicrobial peptides. Chembiochem. 15 (15), 2211-2215 (2014).
- Lineback, C. B., et al. Hydrogen peroxide and sodium hypochlorite disinfectants are more effective against Staphylococcus aureus and Pseudomonas aeruginosa biofilms than quaternary ammonium compounds. Antimicrobial Resistance & Infection Control. 7 (1), 154 (2018).
- Minbiole, K. P. C., et al. From antimicrobial activity to mechanism of resistance: The multifaceted role of simple quaternary ammonium compounds in bacterial eradication. Tetrahedron. 72 (25), 3559-3566 (2016).
- Mangalappalli-Illathu, A. K., Korber, D. R. Adaptive resistance and differential protein expression of Salmonella enterica serovar enteritidis biofilms exposed to benzalkonium chloride. Antimicrobial Agents and Chemotherapy. 50 (11), 3588-3596 (2006).
- El-Banna, T., Abd El-Aziz, A., Sonbol, F., El-Ekhnawy, E. Adaptation of Pseudomonas aeruginosa clinical isolates to benzalkonium chloride retards its growth and enhances biofilm production. Molecular Biology Reports. 46, 3437-3443 (2019).
- Ebrahimi, A., et al. Effects of benzalkonium Chloride on planktonic growth and biofilm formation by animal bacterial pathogens. Jundishapur Journal of Microbiology. 8 (2), 59764 (2015).
- Reśliński, A., et al. Evaluation of Staphylococcus aureus and Escherichia coli biofilm formation on the surface of polypropylene mesh. Medycyna doświadczalna i mikrobiologia. 63 (1), 21-27 (2011).
- Verhorstert, K. W. J., et al. In vitro bacterial adhesion and biofilm formation on fully absorbable poly-4-hydroxybutyrate and nonabsorbable polypropylene pelvic floor implants. Cite This: ACS Applied Materials & Interfaces. 12, 53646-53653 (2020).
- Arkatkar, A., Juwarkar, A. A., Bhaduri, S., Uppara, P. V., Doble, M. Growth of Pseudomonas and Bacillus biofilms on pretreated polypropylene surface. International Biodeterioration & Biodegradation. 64 (6), (2010).
- Jones, J. F., et al. Oriented adhesion of Escherichia coli to polystyrene particles. Applied and Environmental Microbiology. 69 (11), 6515-6519 (2003).
- Zameer, F., et al. Evaluation of adhesive and anti-adhesive properties of Pseudomonas aeruginosa biofilms and their inhibition by herbal plants. Iranian Journal of Microbiology. 8 (2), 108-119 (2016).
- Arkatkar, A., Juwarkar, A. A., Bhaduri, S., Uppara, P. V., Doble, M. Growth of Pseudomonas and Bacillus biofilms on pretreated polypropylene surface. International Biodeterioration and Biodegradation. 64 (6), 530-536 (2010).
- Dieterich, M., et al. Implant-Based Breast Reconstruction Using a Titanium-Coated Polypropylene Mesh (TiLOOP Bra). Plastic and Reconstructive Surgery. 132 (1), 8-19 (2013).
- Clavé, A., et al. Polypropylene as a reinforcement in pelvic surgery is not inert: comparative analysis of 100 explants. International Urogynecology Journal. 21 (3), 261-270 (2010).
- Zameer, F., et al. Evaluation of adhesive and anti-adhesive properties of Pseudomonas aeruginosa biofilms and their inhibition by herbal plants. Iranian Journal of Microbiology. 8 (2), 108-119 (2016).
- Chen, R., Liu, X., Han, L., Zhang, Z., Li, Y. Morphology, thermal behavior, rheological, and mechanical properties of polypropylene/polystyrene blends based on elongation flow. Polymers for Advanced Technologies. 31 (11), 2722-2732 (2020).
- Vial Loading Trays Polystyrene vs. polypropylene: Which tubes are best for your research. ChemTech International Available from: https://chemtech-us.com/polystyrene-vs-polypropylene-which-tubes-are-best-for-your-research/ (2020)
- Bock, L. J., Hind, C. K., Sutton, J. M., Wand, M. E. Growth media and assay plate material can impact on the effectiveness of cationic biocides and antibiotics against different bacterial species. Letters in Applied Microbiology. 66 (5), 368-377 (2018).
- . Crystal violet Available from: https://omic.org/spectra/PhotochemCAD/html/048.html (2017)
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved