Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Détermination de l’affinité de liaison (KD) des anticorps radiomarqués aux antigènes immobilisés
Dans cet article
Résumé
Ici, une méthode est décrite pour déterminer l’affinité de liaison (KD) des anticorps radiomarqués aux antigènes immobilisés. KD est la constante de dissociation d’équilibre qui peut être déterminée à partir d’une expérience de liaison à saturation en mesurant la liaison totale, spécifique et non spécifique d’un anticorps radiomarqué à différentes concentrations à son antigène.
Résumé
La détermination de l’affinité de liaison (KD) est un aspect important de la caractérisation des anticorps radiomarqués (rAb). Typiquement, l’affinité de liaison est représentée par la constante de dissociation d’équilibre, KD, et peut être calculée comme la concentration d’anticorps à laquelle la moitié des sites de liaison d’anticorps sont occupés à l’équilibre. Cette méthode peut être généralisée à n’importe quel anticorps radiomarqué ou à d’autres échafaudages protéiques et peptidiques. Contrairement aux méthodes cellulaires, le choix d’antigènes immobilisés est particulièrement utile pour valider les affinités de liaison après stockage à long terme des anticorps, distinguer les affinités de liaison des bras de la région de liaison à l’antigène fragmentaire (Fab) dans les constructions d’anticorps bispécifiques et déterminer s’il existe une variabilité dans l’expression de l’antigène entre les différentes lignées cellulaires. Cette méthode consiste à immobiliser une quantité fixe d’antigène dans des puits spécifiés sur une plaque cassable de 96 puits. Ensuite, la liaison non spécifique a été bloquée dans tous les puits avec de l’albumine sérique bovine (BSA). Par la suite, le rAb a été ajouté dans un gradient de concentration à tous les puits. Une gamme de concentrations a été choisie pour permettre au rAb d’atteindre la saturation, c’est-à-dire une concentration d’anticorps à laquelle tous les antigènes sont continuellement liés par le rAb. Dans les puits désignés sans antigène immobilisé, une liaison non spécifique du rAb peut être déterminée. En soustrayant la liaison non spécifique de la liaison totale dans les puits avec l’antigène immobilisé, la liaison spécifique du rAb à l’antigène peut être déterminée. Le KD du rAb a été calculé à partir de la courbe de liaison de saturation résultante. À titre d’exemple, l’affinité de liaison a été déterminée à l’aide de l’amivantamab radiomarqué, un anticorps bispécifique pour les protéines du récepteur du facteur de croissance épidermique (EGFR) et de transition mésenchymateuse-épithéliale cytoplasmique (cMET).
Introduction
Les anticorps radiomarqués (rAb) ont une variété d’utilisations en médecine. Alors que la majorité sont utilisés en oncologie comme agents d’imagerie et thérapeutiques, il existe des applications d’imagerie pour l’inflammation liée à la rhumatologie, la cardiologie et la neurologie1. L’imagerie rAbs a une sensibilité élevée pour détecter les lésions et a le potentiel d’aider à la sélection des patients pour le traitement 2,3,4,5. Ils sont également utilisés pour la thérapie en raison de leur spécificité pour leurs antigènes respectifs. Dans une stratégie connue sous le nom de théranostique, le même rAb est utilisé à la fois pour l’imagerie et le traitement6.
Idéalement, l’anticorps choisi pour le radiomarquage est déjà prouvé pour avoir une affinité et une spécificité de liaison élevées en utilisant des méthodes non radiomarquées. Le radiomarquage des anticorps peut être réalisé par modification chimique directe des anticorps avec un radionucléide qui forme des liaisons covalentes stables (par exemple, l’iode radioactif), ou indirectement par conjugaison avec des chélateurs qui se coordonnent ensuite avec les radiométaux 7,8. Le radiomarquage direct, comme celui de l’iode radioactif, modifie spécifiquement les résidus de tyrosine et d’histidine sur l’anticorps. Si ces résidus sont importants pour la liaison à l’antigène, alors cette radioconjugalisation modifierait l’affinité de liaison. Inversement, il existe de multiples protocoles établis pour la conjugaison et le radiomarquage indirect des anticorps. Par exemple, un chélateur commun utilisé pour lier le zirconium-89 (89Zr) pour l’imagerie TEP des anticorps est la p-isothiocyanatobenzyl-desferrioxamine (DFO), qui est conjuguée au hasard aux résidus de lysine de l’anticorps 9,10. S’il y a des résidus de lysine dans la région de liaison à l’antigène, la conjugaison à ces sites pourrait entraver stériquement la liaison à l’antigène et donc compromettre la liaison anticorps-antigène. Ainsi, les différentes méthodes de radioconjugation utilisées pour le radiomarquage indirect ou direct des anticorps peuvent potentiellement affecter l’immunoréactivité, définie comme la capacité de l’anticorps radioconjugué à se lier à son antigène 7,11. Les méthodes de conjugaison spécifiques au site peuvent contourner cette limitation, mais ces techniques nécessitent une ingénierie des anticorps pour incorporer des résidus de cystéine supplémentaires ou une expertise dans les réactions enzymatiques sur les résidus de glucides 12,13,14,15,16. Une fois qu’un anticorps est radiomarqué, il est important de vérifier si l’immunoréactivité est retenue dans le cadre de la caractérisation du rAb. Une façon de mesurer l’immunoréactivité consiste à déterminer l’affinité de liaison du rAb.
Le but de ce protocole est de décrire un processus de détermination de l’affinité de liaison pour les rAbs à l’aide d’un test de saturation radioligand établi pour quantifier la liaison rAb-antigène. La tendance contraignante est décrite à la figure 1. La quantité d’antigène liée augmentera à mesure que plus de rAb est ajouté à une quantité fixe d’antigène immobilisé. Une fois que tous les sites de liaison à l’antigène sont saturés, un plateau sera atteint et l’ajout de rAbs supplémentaires n’aura aucun effet sur la quantité d’antigène lié. Dans ce modèle, la constante de dissociation d’équilibre (KD) est la concentration d’anticorps qui occupe la moitié des récepteurs de l’antigène17. Le KD représente la façon dont un anticorps se lie à sa cible avec un KD inférieur correspondant à une affinité de liaison plus élevée. Il a déjà été rapporté qu’un rAb idéal devrait avoir un KD de 1 nanomolaire ou moins18. Cependant, des rAbs plus récents ont été développés avec KD dans la gamme des nanomolaires bas et sont considérés comme appropriés pour les applications d’imagerie noninvasives 19,20,21,22. Un autre paramètre qui peut être déterminé dans le test de saturation radioligand de rAbs est Bmax, qui correspond à la quantité maximale de liaison à l’antigène. Bmax peut être utilisé pour calculer le nombre de molécules d’antigène si nécessaire.

Figure 1 : Courbe de liaison de saturation représentative. Le pourcentage d’antigène lié est tracé en fonction de concentrations croissantes d’anticorps ajoutés à une quantité fixe d’antigène. Les pop-outs montrent la liaison à différents points. La concentration et la liaison correspondant respectivement à KD et Bmax sont indiquées. Cette figure a été créée avec BioRender.com. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Ce test est particulièrement important pour les constructions d’anticorps bispécifiques radiomarqués afin de déterminer le KD pour chaque segment de la région de liaison à l’antigène (Fab) du bras de liaison des anticorps bispécifiques radiomarqués avec leurs antigènes respectifs. Ce protocole peut être utilisé pour déterminer le KD de chaque bras Fab séparément sur les antigènes immobilisés afin de caractériser indépendamment si l’affinité de liaison de chaque bras Fab pour son antigène respectif a été affectée après radioconjugation. Ce protocole est démontré par l’utilisation de l’amivantamab radiomarqué, un anticorps bispécifique pour le récepteur du facteur de croissance épidermique (EGFR) et les protéines de transition mésenchymateuse-épithéliale cytoplasmique (cMET)19. Des anticorps radiomarqués à un seul bras, où un bras Fab se lie à l’EGFR (α-EGFR) ou au cMET (α-cMET) et l’autre bras Fab est un contrôle d’isotype, ont également été utilisés comme exemples19. Ce protocole est également approprié pour tout anticorps radiomarqué avec un antigène connu qui peut être immobilisé. Dans ce protocole, une série de dilution du rAb est ajoutée à une quantité fixe d’antigène immobilisé dans des puits désignés spécifiques à chaque bras Fab du rAb. Le rAb est également ajouté aux puits qui n’ont été bloqués qu’avec de l’albumine sérique bovine (BSA), sans antigène, pour déterminer la liaison non spécifique. Pour déterminer la liaison spécifique, la liaison non spécifique à l’antigène immobilisé est soustraite de la liaison rAb totale. La courbe de liaison de saturation résultante est ensuite utilisée pour déterminer KD, comme décrit ci-dessus.
L’un des avantages de cette méthode est une reproductibilité plus élevée lors de l’utilisation d’antigènes purifiés par rapport à l’utilisation de lignées cellulaires comme source d’antigènes, étant donné que les niveaux d’expression de l’antigène pourraient être affectés pendant la culture cellulaire et que différentes lignées cellulaires ont des niveaux variables d’expression de l’antigène. Dans le cas des anticorps bispécifiques radiomarqués, les lignées cellulaires qui n’expriment que l’un des antigènes sans l’autre peuvent ne pas être disponibles, ce qui rendrait la caractérisation de l’affinité de liaison des bras Fab individuels très difficile. Notamment, le principal avantage de la méthode de dosage de saturation radioligand par rapport aux méthodes non radiomarquées est la caractérisation spécifique de l’affinité de liaison du rAb sans la contribution de la fraction non conjuguée du rAb. À la connaissance des auteurs, il n’existe actuellement aucune technique de purification pour séparer le rAb de son anticorps parent non conjugué. Compte tenu de la taille relativement petite du chélateur et du radionucléide, leur contribution au poids moléculaire global du rAb est insignifiante en chromatographie d’exclusion de taille. Ainsi, le produit généré à partir de toute technique de radiomarquage est presque toujours un mélange du rAb et de son anticorps parent non conjugué. La caractérisation de l’affinité de liaison à l’aide du test de saturation radiomarqué garantit que le produit testé est uniquement le rAb.
Protocole
REMARQUE : Reportez-vous à la figure 2 pour obtenir une représentation graphique du protocole.
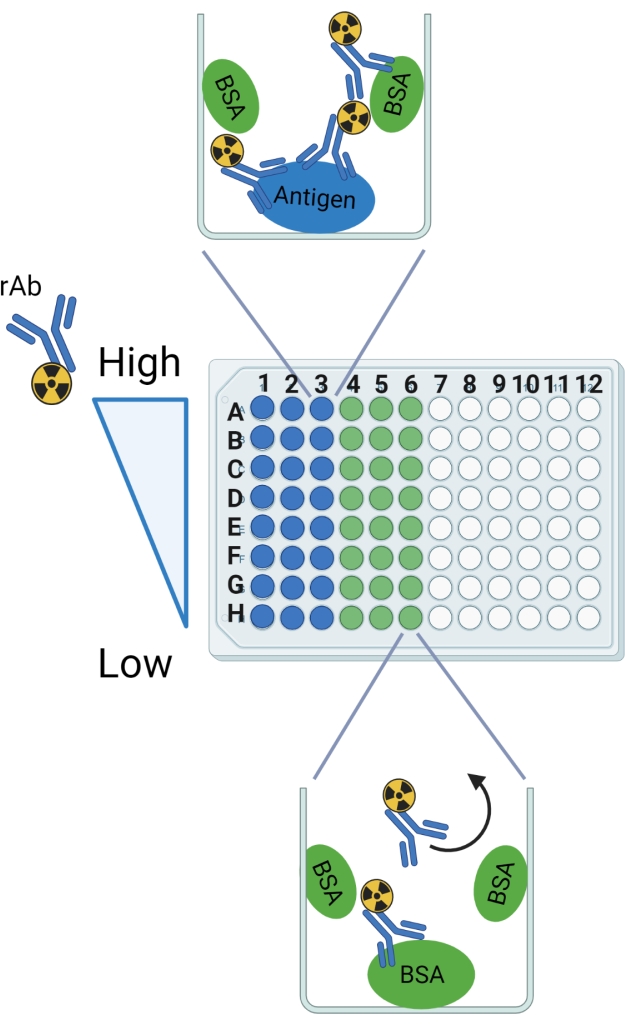
Figure 2 : Schéma du protocole. Les étiquettes de ligne et de colonne sont indiquées comme guide pour la mise en place de la plaque cassable à 96 puits. La liaison anticipée est montrée dans un puits d’exemple pour l’antigène et le BSA. La flèche incurvée désigne le rAb qui devrait être lavé des puits avec BSA seulement. Cette figure a été créée avec BioRender.com. Veuillez cliquer ici pour voir une version agrandie de cette figure.
1. Préparation du tampon
- Préparer 50 mL de tampon d’immobilisation (solution aqueuse de 50 mMNa2CO3; pH = 9,0).
- Peser 191 mg de NaHCO3 et 23,9 mg de Na2CO3 sur du papier de pesage et transférer dans un tube conique de 50 mL. Ajouter 40 mL d’eau de 18 MΩ et vortex pour dissoudre. Ajuster le pH à 9,0 si nécessaire avant de porter le volume total à 50 mL avec 18 MΩ d’eau.
- Préparer environ 200 mL de tampon de lavage (solution saline tamponnée au phosphate (PBS) contenant 0,05 % de Tween-20) en ajoutant 200 mL de PBS, puis 100 μL de Tween-20 à une bouteille de 250 mL.
- Préparer 50 mL de tampon de liaison (PBS contenant 0,05 % de Tween-20 et 0,1 % d’albumine sérique bovine (BSA)).
- Peser 50 mg de BSA sur du papier de pesage et transférer dans un tube conique de 50 mL. Ajouter 50 mL de PBS puis 25 μL de Tween-20 au tube. Vortex doucement pour mélanger.
- Préparer 50 mL de tampon bloquant (3 % de BSA dans PBS).
- Peser 1,5 g de BSA sur du papier de pesage et transférer dans un tube conique de 50 mL. Ajouter 50 mL de PBS et vortex doucement pour mélanger.
REMARQUE: Il est recommandé de conserver tous les tampons jusqu’à 1 semaine à 4 ° C pour de meilleurs résultats.
- Peser 1,5 g de BSA sur du papier de pesage et transférer dans un tube conique de 50 mL. Ajouter 50 mL de PBS et vortex doucement pour mélanger.
2. Immobilisation des antigènes
- Diluer l’antigène dans un tampon d’immobilisation pour atteindre une concentration de 5 μg/mL.
- Ajouter 100 μL par puits d’antigène au fond de 24 puits d’une plaque à fond plat cassable de 96 puits dans un réseau de 8 x 3 (colonnes 1 à 3 pour les rangées A à H). Couvrez la plaque avec du ruban adhésif.
REMARQUE: S’assurer que la surface de la plaque de puits a été traitée pour maximiser l’adsorption des domaines hydrophobes et hydrophiles mixtes. Ces plaques prétraitées sont disponibles dans le commerce. - Incuber à 4 °C pendant la nuit.
- Le lendemain, lavez la plaque 3x avec un tampon de lavage.
- Inversez la plaque rapidement dans l’évier pour éliminer le liquide et tapotez la plaque sur un tas d’essuie-tout pour éliminer l’excès de liquide.
- À l’aide d’une pipette multicanal, ajouter 300 μL par puits de tampon de lavage aux puits contenant l’antigène. Retirer le liquide comme décrit au point 2.4.1. Répétez l’étape de lavage trois fois au total.
3. Blocage des sites non spécifiques avec BSA
- À l’aide d’une pipette multicanal, ajouter 300 μL par puits de tampon bloquant aux 24 puits revêtus d’antigène et aux 24 puits vides de la plaque de 96 puits (colonnes 1 à 6 pour les rangées A à H).
- Incuber la plaque pendant 1 h à température ambiante.
- Lavez la plaque avec 300 μL par puits de tampon de lavage au total trois fois. Reportez-vous à l’étape 2.4 pour une description détaillée du lavage de la plaque.
4. Dilutions en série et ajout de la solution de rAb
ATTENTION : Les étapes suivantes concernent la radioactivité. Les étapes ne devraient être effectuées que par les personnes ayant reçu une formation en radioprotection. Les chercheurs devraient doubler le gant et effectuer des étapes avec un blindage adéquat.
- Synthétiser le rAb à l’étude en utilisant la méthode de choix. Les rAbs utilisés comme exemple ont été synthétisés comme décrit précédemment19.
REMARQUE: Ce protocole se concentre sur la caractérisation d’un rAb une fois radiomarqué. - Effectuer 8 dilutions série 3 fois (désignées pour les rangées A-H sur la plaque) du rAb dans le tampon de liaison.
REMARQUE: Les concentrations des dilutions en série varient pour chaque rAb. Les détails sont abordés dans la section Discussion. Si le facteur de dilution change, le volume nécessaire pour chaque dilution doit être recalculé pour assurer un volume suffisant pour 1) la liaison du rAb dans chaque puits, 2) l’ensemencement de la dilution suivante et 3) l’aliquote d’une solution étalon rAb pour le comptage gamma afin de mesurer la radioactivité du rAb total ajouté à chaque puits.- Calculer le volume de rAb de stock nécessaire pour obtenir une solution de 1,2 mL de la première concentration (étiquette A).
- Ajouter 800 μL de tampon de liaison aux tubes de microcentrifugation étiquetés B, C, D, ... à H. Ajouter 1,2 mL moins le volume calculé à l’étape 4.2.1 du tampon de liaison à un tube de microcentrifugation étiqueté A.
- Ajouter le volume de stock rAb calculé en 4.2.1 au tube A. Vortex doucement pour mélanger puis tourner vers le bas à l’aide d’une mini microcentrifugeuse pour recueillir tout le liquide au fond du tube.
- Ajouter 400 μL du tube A au tube B. Vortex à mélanger puis filer vers le bas à l’aide d’une mini microcentrifugeuse. Répétez l’ajout de B à C, C à D, ..., G à H.
- Ajouter 100 μL par puits de chaque dilution à trois puits immobilisés par antigène et à trois puits bloqués par BSA seulement. Par exemple, ajouter la dilution A aux puits A1-A3 (antigène) et A4-A6 (BSA).
- Ajouter 100 μL de chaque dilution aux tubes de microcentrifugation marqués A std - H std. Enregistrez ces tubes en tant qu’étalons rAb à doser dans le compteur gamma.
- Incuber la plaque pendant 1 h à 37 °C avec un léger balancement.
5. Plaques de lavage et dosage de la radioactivité
- Étiqueter les tubes de microcentrifugation pour chaque puits (A1 à A6, B1 à B6 ... par H1-H6). Utilisez deux marqueurs de couleur différente pour coder les échantillons si vous le souhaitez, l’un pour les puits recouverts d’antigène et l’autre pour les puits contenant uniquement du BSA.
- Aspirer le rAb de chaque puits à l’aide d’un aspirateur à vide.
- À l’aide d’une pipette multicanal, ajoutez 300 μL de tampon de lavage à chaque puits. Aspirer le tampon de lavage. Répétez le lavage cinq fois au total.
- Séparez les puits en tubes de microcentrifugation appropriés.
- Compter la radioactivité dans les tubes à l’aide d’un compteur gamma. Comptez d’abord les tubes avec l’antigène (H1, H2, H3 à A1, A2, A3), puis ceux avec BSA uniquement (H4, H5, H6 à A4, A5, A6). Pour minimiser les interférences, comptez séparément les étalons pour chaque dilution (H std à A std) à un moment différent.
6. Analyse des données
REMARQUE: Les fichiers supplémentaires contiennent des feuilles de calcul et des modèles d’analyse statistique correspondants pour l’analyse et le traçage des données.
- Dans une feuille de calcul, calculez la liaison totale, spécifique et non spécifique pour chaque exemple (voir le modèle de feuille de calcul joint en tant que fichier supplémentaire).
- Calculez l’activité liée comme les comptes par minute (CPM) de l’échantillon (obtenu à partir du compteur gamma) divisés par le CPM de la norme appropriée. Calculez « % Bound » comme Activité liée fois 100.
- Calculer « Total Bound, mol/L » en multipliant « % Bound » par la concentration (mol/L) du rAb ajouté. Calculer « Total Bound, mol » en multipliant « Total Bound, mol/L » par le volume de rAb ajouté en litres (0,0001 L).
- Calculer « Liaison spécifique, mol » en soustrayant « Total Bound, mol » des dilutions BSA des dilutions d’antigène de telle sorte que A1 s’apparie avec A4, A2 avec A5, A3 avec A6, B1 avec B4, etc.
- Calculez « Liaison non spécifique, mol » en soustrayant « Liaison spécifique, mol » de « Liaison totale, mol » pour chaque puits.
- Dans le logiciel de traçage d’analyse statistique, tracez la concentration de rAb ajouté (nmol/L) sur l’axe des x par rapport à la liaison (mol) sur l’axe des y. Créez des groupes distincts à tracer en trilicate la liaison totale, la liaison spécifique et la liaison non spécifique. Effectuez une analyse d’ajustement non linéaire en sélectionnant les paramètres suivants dans le logiciel utilisé (Tableau des matériaux; voir le modèle d’analyse statistique joint sous forme de fichier supplémentaire).
- Sélectionnez Nouvelle analyse. Sous Analyses XY, sélectionnez Régression non linéaire (ajustement de la courbe). Assurez-vous que toutes les données sont sélectionnées sous Analyser quels ensembles de données ? puis sélectionnez OK.
- Sous l’onglet Modèle , sous Liaison - Saturation, sélectionnez Un site - Liaison spécifique. Sous l’onglet Confiance , sélectionnez Identifier les ajustements « ambigus ». Laissez tous les autres paramètres par défaut et sélectionnez OK.
REMARQUE: Cela calculera le KD et le Bmax pour la liaison totale, spécifique et non spécifique. Le KD de la liaison spécifique est le KD en nmol/L du rAb lié à l’antigène.
Résultats
Cette méthode calcule l’affinité de liaison (KD) pour un rAb sur la base du test de liaison de saturation où différentes concentrations de rAb ont été ajoutées à une quantité fixe d’antigène immobilisé. La courbe de liaison doit suivre une croissance logarithmique où elle est initialement raide, puis plafonne à mesure que l’antigène est saturé. Pour s’assurer que le KD déterminé est exact, les concentrations de rAb doivent être suffisamment élevées pour atteindre la satur...
Discussion
Dans le cadre du développement des rAbs, il est important de s’assurer qu’un rAb se lie spécifiquement à sa cible avec une affinité de liaison élevée. La détermination de l’affinité de liaison peut indiquer si l’immunoréactivité du rAb est affectée par la radioconjugation par le biais du test de saturation radioligand utilisant un antigène immobilisé. La détermination de la liaison du rAb à la BSA peut être utilisée pour quantifier la liaison non spécifique afin de mesurer plus précisément la ...
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts.
Remerciements
Les auteurs remercient 3D Imaging pour la production de [89Zr]Zr-oxalate et le Dr Sheri Moores de Janssen Pharmaceuticals pour avoir fourni des anticorps.
matériels
| Name | Company | Catalog Number | Comments |
| Bovine Serum Albumin (BSA) | Sigma-Aldrich | A9647 | |
| Gamma Counter | Hidex | Hidex Automatic Gamma Counter | |
| GraphPad Prism Software | GraphPad | version 9.2; used for statistical analyses in this study | |
| Immuno Breakable MaxiSorp 96-well plates | Thermo Scientific | 473768 | |
| Microplate Sealing Tape | Corning | 4612 | |
| Microsoft Excel | Microsoft | ||
| Phosphate Buffered Saline (PBS) | Gibco | 14190144 | |
| Sodium Bicarbonate | JT Baker | 3506-01 | |
| Sodium Carbonate | Sigma-Aldrich | S7795 | |
| Tween-20 | Sigma-Aldrich | P7949 |
Références
- Krecisz, P., Czarnecka, K., Krolicki, L., Mikiciuk-Olasik, E., Szymanski, P. Radiolabeled Peptides and Antibodies in Medicine. Bioconjugate Chemistry. 32 (1), 25-42 (2021).
- Dun, Y., Huang, G., Liu, J., Wei, W. ImmunoPET imaging of hematological malignancies: From preclinical promise to clinical reality. Drug Discovery Today. 27 (4), 1196-1203 (2022).
- Lohrmann, C., et al. Retooling a Blood-Based Biomarker: Phase I assessment of the high-affinity CA19-9 antibody HuMab-5B1 for immuno-pet imaging of pancreatic cancer. Clinical Cancer Research. 25 (23), 7014-7023 (2019).
- Pandit-Taskar, N., et al. A phase I/II study for analytic validation of 89Zr-J591 immunoPET as a molecular imaging agent for metastatic prostate cancer. Clinical Cancer Research. 21 (23), 5277-5285 (2015).
- Rousseau, C., et al. Initial clinical results of a novel immuno-PET theranostic probe in human epidermal growth factor receptor 2-negative breast cancer. Journal of Nuclear Medicine. 61 (8), 1205-1211 (2020).
- Moek, K. L., et al. Theranostics using antibodies and antibody-related therapeutics. Journal of Nuclear Medicine. 58 (2), 83-90 (2017).
- Chomet, M., van Dongen, G., Vugts, D. J. State of the art in radiolabeling of antibodies with common and uncommon radiometals for preclinical and clinical immuno-PET. Bioconjugate Chemistry. 32 (7), 1315-1330 (2021).
- Kumar, K., Ghosh, A. Radiochemistry, production processes, labeling methods, and immunoPET imaging pharmaceuticals of Iodine-124. Molecules. 26 (2), 414 (2021).
- Vosjan, M. J., et al. Conjugation and radiolabeling of monoclonal antibodies with zirconium-89 for PET imaging using the bifunctional chelate p-isothiocyanatobenzyl-desferrioxamine. Nature Protocols. 5 (4), 739-743 (2010).
- Zeglis, B. M., Lewis, J. S. The bioconjugation and radiosynthesis of 89Zr-DFO-labeled antibodies. Journal of Visualized Experiments: JoVE. (96), e52521 (2015).
- Wei, W., et al. ImmunoPET: concept, design, and applications. Chemical Reviews. 120 (8), 3787-3851 (2020).
- Tavaré, R., et al. An effective immuno-PET imaging method to monitor CD8-dependent responses to immunotherapy. Cancer Research. 76 (1), 73-82 (2016).
- Tavaré, R., et al. Engineered antibody fragments for immuno-PET imaging of endogenous CD8+ T cells in vivo. Proceedings of the National Academy of Sciences. 111 (3), 1108-1113 (2014).
- Zeglis, B. M., et al. Chemoenzymatic strategy for the synthesis of site-specifically labeled immunoconjugates for multimodal PET and optical imaging. Bioconjugate Chemistry. 25 (12), 2123-2128 (2014).
- Zeglis, B. M., et al. Enzyme-mediated methodology for the site-specific radiolabeling of antibodies based on catalyst-free click chemistry. Bioconjugate Chemistry. 24 (6), 1057-1067 (2013).
- Kristensen, L. K., et al. Site-specifically labeled 89Zr-DFO-trastuzumab improves immuno-reactivity and tumor uptake for immuno-PET in a subcutaneous HER2-positive xenograft mouse model. Theranostics. 9 (15), 4409-4420 (2019).
- Maguire, J. J., Kuc, R. E., Davenport, A. P., Davenport, A. P. . Radioligand binding assays and their analysis. in Receptor Binding Techniques. , 31-77 (2012).
- Davenport, A. P., Russell, F. D., Mather, S. J. Radioligand bindsing assays: theory and practice. Current Directions in Radiopharmaceutical Research and Development. , 169-179 (1996).
- Cavaliere, A., et al. Development of [89Zr]ZrDFO-amivantamab bispecific to EGFR and c-MET for PET imaging of triple negative breast cancer. European Journal of Nuclear Medicine and Molecular Imaging. 48 (2), 383-394 (2021).
- Marquez, B. V., et al. Evaluation of (89)Zr-pertuzumab in breast cancer xenografts. Molecular Pharmaceutics. 11 (11), 3988-3995 (2014).
- Marquez-Nostra, B. V., et al. Preclinical PET imaging of glycoprotein non-metastatic melanoma B in triple negative breast cancer: feasibility of an antibody-based companion diagnostic agent. Oncotarget. 8 (61), 104303-104314 (2017).
- Ghai, A., et al. Development of [(89)Zr]DFO-elotuzumab for immunoPET imaging of CS1 in multiple myeloma. European Journal of Nuclear Medicine and Molecular Imaging. 48 (5), 1302-1311 (2021).
- McKnight, B. N., et al. Imaging EGFR and HER3 through (89)Zr-labeled MEHD7945A (Duligotuzumab). Scientific Reports. 8 (1), 1-13 (2018).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon