需要订阅 JoVE 才能查看此. 登录或开始免费试用。
小动物高分辨率心脏正电子发射断层扫描/计算机断层扫描
摘要
在这里,我们提出了一种实验成像协议,用于使用高分辨率正电子发射断层扫描/计算机断层扫描来量化小动物的心脏功能和形态。考虑小鼠和大鼠,讨论计算机断层扫描造影剂对两个物种的不同要求。
摘要
正电子发射断层扫描(PET)和计算机断层扫描(CT)是最常用的诊断成像技术之一,两者都有助于了解心脏功能和代谢。在临床前研究中,采用具有高灵敏度和高时空分辨率的专用扫描仪,旨在应对小鼠和大鼠的小心脏尺寸和非常高的心率所带来的苛刻技术要求。本文描述了一种用于实验小鼠和/或大鼠心脏病模型的双模心脏PET / CT成像方案,从动物制备和图像采集和重建到图像处理和可视化。
特别是, 18F标记的氟脱氧葡萄糖([18F]FDG)-PET扫描允许测量和可视化左心室(LV)不同部分的葡萄糖代谢。极地地图是显示此信息的便捷工具。CT 部分包括使用无心电图 (ECG) 导联的回顾性门控对整个心脏 (4D-CT) 进行时间分辨 3D 重建,从而可以对左心室进行形态功能评估,并随后量化最重要的心脏功能参数,例如射血分数 (EF) 和每搏输出量 (SV)。使用集成的PET / CT扫描仪,该协议可以在同一麻醉诱导内执行,而无需在不同的扫描仪之间重新定位动物。因此,PET / CT可以被视为几种心脏病小动物模型中心脏形态功能和代谢评估的综合工具。
引言
小动物模型对于促进对心血管疾病的认识极为重要1,2。在过去的几十年里,非侵入性诊断成像工具彻底改变了我们在临床和临床前环境中看待心脏功能的方式。就心脏病的小动物模型而言,已经开发出具有非常高时空分辨率的特定成像工具。因此,此类仪器可以满足在特定疾病模型中(例如心力衰竭(HF)3或心肌梗塞(MI)4)中对小鼠和大鼠非常小且非常快速移动的心脏进行相关代谢和动力学心肌参数的准确定量的需求。为此目的有几种方式,每种方式都有自己的优点和缺点。超声(英文)成像是使用最广泛的方式,因为它具有极大的灵活性、非常高的时间分辨率和相对较低的成本。自从使用超高频5,6探头的系统出现以来,美国心脏成像在小动物中的采用已经大大增加,其空间分辨率低于50μm。
US 用于全 3D 心脏成像的主要缺点之一是需要沿心脏轴进行线性扫描,方法是将探头安装在电动平移台上,以创建整个心脏的完整动态 B 模式图像7。最终,该过程产生(在每个探头位置获取的图像进行准确的空间和时间配准后)在面内和面外方向之间具有不同空间分辨率的4D图像。心脏MR(CMR)8也存在空间分辨率不均匀的问题,这 仍然是心脏功能成像的黄金标准。可以使用计算机断层扫描(CT)和正电子发射断层扫描(PET)9来获得真正的各向同性3D成像。PET在每注射探针量(在纳摩尔范围内)的图像信号方面提供了一种非常灵敏的工具,尽管与CT,MR或US相比,它的空间分辨率降低。PET的主要优点是它能够显示器官病理生理学背后的细胞和分子机制。例如,注射[18F]FDG后的PET扫描可以重建体内葡萄糖代谢的3D图。通过将其与动态(即时间分辨)数据采集相结合,示踪动力学建模可用于计算葡萄糖摄取代谢率(MRGlu)的参数图,这将提供有关心肌活力的重要信息10。
CT需要大量高浓度的外部造影剂(CA)(每毫升高达400毫克碘),以提供相关组织成分(例如,血液与肌肉)的可测量增强,但它在空间和时间分辨率方面表现出色,特别是在使用专为小动物成像设计的最先进的微型CT扫描仪时。11 可以应用心脏PET / CT的典型疾病模型是心肌梗塞和心力衰竭的实验评估以及对治疗的相关反应。在小动物中诱导心肌梗死的常见方法是手术结扎左前降(LAD)冠状动脉12,13 ,然后在随后的几天纵向评估疾病的进展和心脏重塑4。然而,小动物心脏的定量形态功能评估在很大程度上也适用于其他疾病模型,例如评估衰老对心脏功能的影响14 或肥胖模型中受体表达的改变15。所提出的成像方案不限于任何给定的疾病模型,因此,在小型啮齿动物临床前研究的几种背景下可能是最广泛的兴趣。
在本文中,我们提出了一种使用小动物集成PET / CT进行心脏成像的从头到尾实验方案。尽管所提出的协议是为特定的双峰集成扫描仪设计的,但所述程序的PET和CT部分可以在来自不同制造商的单独扫描仪上独立执行。在使用中的PET/CT扫描仪中,操作顺序在预编程的工作流程中组织。每个工作流程的主要分支是一个或多个采集协议;每个采集协议可以有一个或多个用于特定预处理协议的分支,反过来,每个预处理协议可以有一个或多个用于特定重建协议的分支。描述了在成像床上制备动物和在成像过程中要注射的外部试剂的制备。图像采集程序完成后,提供了基于常用软件工具的定量图像分析示例程序。主协议专为鼠标模型设计;尽管小鼠仍然是该领域最常用的物种,但我们在主协议结束时也展示了对大鼠成像协议的改编。显示了小鼠和大鼠的代表性结果,展示了所描述程序可能预期的输出类型。本文最后进行了彻底的讨论,以强调该技术的优缺点、关键点以及如何使用不同的PET放射性示踪剂,而几乎不修改准备和采集/重建步骤。
研究方案
动物实验是根据欧洲指令(1986年第86/609/EEC号指令和2010/63/UE指令)和意大利法律(D.Lgs.26/2014)要求的《国际实验动物处理指南》中的建议进行的。
1. PET/CT 成像方案和工作流程的设置
注意:此处介绍的方案是专门为小鼠模型的心脏成像而设计的。与大鼠一起工作可能意味着对实际方案进行一些修改,主要是因为动物的体型更大(大约重10倍)。步骤中特别提到了大鼠成像的修改;如果没有提到修改,那么小鼠成像的相同步骤可用于大鼠。
- 打开 PET/CT 扫描仪的图形用户界面 (GUI)(参见 目录)并创建一组新协议(包括用于数据采集、预处理和图像重建的参数):(i) 动态 PET 扫描, (二) a 低剂量 CT 扫描 用于衰减校正(中国电信委员会)不含造影剂,以及(iii)a 对比增强电影 CT 扫描.
注意:为采集、预处理和重建阶段创建新协议(即断层扫描的特定软件指令)是一个简单的过程;如果遇到问题,用户可以在GUI用户手册中找到更详细的信息。- 对于 PET 扫描,打开扫描仪 (GUI) 的“协议”选项卡,使用以下参数创建三个新 协议 (用于 采集、预处理 和 重建):
- 对于采集协议:设置3,600秒的总扫描时间和单人床位置。使用正确的名称保存此协议,以便后续导入工作流。对以下几点中的所有后续协议也执行相同的操作。
- 对于鼠标的预处理协议:选择 250-750 keV 能量窗口 (EW) 并启用以下校正:放射性衰变、随机巧合和死区时间。将成帧协议(即原始数据的动态拆分)设置如下:8 x 5 秒、8 x 10 秒、3 x 40 秒、2 x 60 秒、2 x 120 秒、10 x 300 秒 (= 3,600 秒)。对于大鼠,选择350-750 keV能量窗口(EW),使用与鼠标协议相同的框架。
- 对于 重建 方案:选择高质量的、基于蒙特卡洛的 3D 有序子集期望最大化 (3D-OSEM-MC) 算法,具有 8 个 子集 和 8 次迭代,启用 归一化、定量 校正和 CT 衰减校正 。
- 对于用于衰减校正 (CTAC) 的低剂量 CT 扫描,请使用以下参数:
- 对于采集协议:单帧,单床位置,全扫描; 电子管设置:80 kV,低电流(低剂量); 360°576个视图,每个视图的曝光时间为34毫秒(扫描时间为20秒);旋转类型:连续,灵敏度模式:高灵敏度。
- 对于预处理方案:240μm体素大小,横向FOV:大鼠,轴向FOV:100%。
- 对于 重建 协议: 滤光片窗口:平滑,体素大小:标准 ,启用 光束硬化 和环预校正,禁用环伪影 校正后。
- 对于造影剂增强门控 CT 扫描,使用以下设置创建三个新方案(用于 采集、预处理 和 重建):
- 对于鼠标的采集协议:设置单帧,单人床位置,全扫描;管设置:65 kV,全电流(低噪声);360°8,000视图,每个视图曝光时间为15毫秒(120秒扫描时间);旋转类型:连续,灵敏度模式:高灵敏度。对于大鼠,将采集协议参数设置如下:80 kV 管电压,360° 16,000 个视图,每个视图 12 ms 曝光时间(192 s 扫描时间)。
- 对于鼠标的预处理协议:选择120μm体素大小;横向视野(FOV):鼠标;轴向FOV:50%。对于大鼠,选择240μm体素大小;横向视野(FOV):大鼠;轴向FOV:50%。
- 对于 重建 协议: 过滤器窗口:平滑,体素大小:标准;启用 光束硬化 和环预校正,禁用环伪影后 校正。
- 在 GUI 中打开“工作流”选项卡,然后创建一个新的 工作流 ,添加刚刚创建的协议:PET 的步骤 1.1.1.1-1.1.1.3,步骤 1.1.2.1。-1.1.2.3.对于 CTAC 和步骤 1.1.3.1。-1.1.3.3.对于门控 CT,按给定顺序排列。在这两种情况下,请确保协议按以下顺序嵌套: 采集 |预处理 |重建。
注意:可以在PET扫描开始时使用持续时间为<5 s的动态PET帧,以更好地捕获动脉输入功能的峰值,但不建议这样做,因为这会导致图像嘈杂,定量精度降低。在步骤1.1.2.2中,我们对横向FOV使用了“Rat”大小。这通常用于CTAC中的大鼠和小鼠。
- 对于 PET 扫描,打开扫描仪 (GUI) 的“协议”选项卡,使用以下参数创建三个新 协议 (用于 采集、预处理 和 重建):
2. PET/CT成像的动物制备
注意:对于本方案,所有动物禁食过夜。
- 最初在诱导室中用3%-4%(v / v)异氟醚麻醉小鼠,然后用1%-2%(v / v)异氟醚维持。
- 称量小鼠并测量基础血糖以监测动物的状况。要采集所需的血液样本,请使用锋利的剪刀在尾尖做一个小切口,然后轻轻按摩尾巴以直接在试纸上收集一滴血滴(~1μL)。
- 继续使用 29G 蝴蝶( 小鼠 )和 24G 大鼠(大 鼠)在尾静脉水平插入静脉通路。
- 要执行插管技术,请使用同时加热(通常在加热灯下)并对针头插入点进行消毒以血管舒张静脉。插管后,用丝带将蝴蝶固定在尾巴上,以便在手术过程中将其固定到位。
注意:[18F]FDG研究需要禁食。不同的示踪剂可能涉及不同的动物制备,但关于该主题的彻底讨论超出了本协议的范围。就[18F]FDG而言,避免禁食会导致非常不同的示踪剂生物分布16。
- 要执行插管技术,请使用同时加热(通常在加热灯下)并对针头插入点进行消毒以血管舒张静脉。插管后,用丝带将蝴蝶固定在尾巴上,以便在手术过程中将其固定到位。
- 打开连接到PET-CT扫描仪的麻醉系统(异氟醚1%-2%,小鼠0.8L / min O2 和大鼠1-1.2L / min)并将小鼠转移到床上。
- 将鼠标仰卧位,头部先放在PET-CT断层扫描机的扫描仪床上,将其鼻子放在鼻罩中进行麻醉,并用胶带轻轻地将鼠标头固定在面罩上。
- 将鼠标的上肢和下肢固定在扫描仪台上,以防止在成像过程中出现任何可能导致运动伪影的不自主运动。
- 分别使用直肠探头和呼吸枕头监测体温和呼吸频率。
3.PET示踪剂剂量制备
- 对于小鼠,用胰岛素注射器(1mL)以100-150μL的体积抽取10MBq的[18F]FDG。对于大鼠,在0.20-0.25mL中吸取较高剂量的15MBq。
注意:避免更高的活动,因为此协议中讨论的PET扫描仪具有非常高的灵敏度,只需要适度的活动即可获得高质量的图像。 - 如果小瓶中示踪剂的原始浓度过高,请使用生理溶液(0.9% w/v NaCl)将示踪剂剂量稀释至50-100 MBq/mL的浓度。
- 使用PET剂量校准器测量注射器中的实际活性。注释预注射活动和测量时间,因为这些值将在以后使用 PET 扫描仪 GUI 的特定输入模块使用。
4. CT造影剂制备
- 将每20g小鼠重量的碘化脂质乳剂造影剂抽取0.2mL到1mL注射器中。对于较重的小鼠,将注射体积限制在0.5mL的CA。如果使用碘美洛,将小鼠的注射速率设置为10mL / h(~0.17mL / min),并将注射体积限制为0.5 mL。
- 对于大鼠,将2.3-3mL碘美普尔稀释至200mg / mL浓度吸入5mL注射器中。
注意:如果没有小动物脂质乳剂CA,则可以使用通过注射泵连续注射的碘美洛,如下所述。 - 将注射器连接到注射泵,并将泵设置为实际注射器的尺寸和直径。
- 将注射器连接到CA管和针头,并用CA预填充管。
- 将进样速率设置为 24 mL/h (= 0.4 mL/min),将进样量限制为 2 mL。
注意:在大鼠中使用基于碘化脂质乳剂的血池CA也是可能的,尽管由于单次注射体积较大,该程序的成本相对较高。如果首选此选项(例如,通过避免注射泵来简化方案),则可以采用以下程序:
- 对于大鼠,将2.3-3mL碘美普尔稀释至200mg / mL浓度吸入5mL注射器中。
- 将每公斤体重7.5毫升的碘脂质乳剂造影剂吸入5毫升注射器中。对于较重的大鼠,也将注射体积限制在 2 mL 的 CA。
5. 成像前的动物比对和初步操作
- 将动物固定在成像床上后,在断层扫描 GUI 上创建一个新的研究。在研究名称模块中添加 研究名称 标识符,然后从下拉菜单中选择之前保存的成像工作流程。
- 使用 动物/标本信息选择合适的解剖部位 |解剖部分 | 通过动物 /标本信息进行心脏和动物定位 |定位 |仰卧/头先。注释相应模块的动物重量(以克为单位): 动物/标本信息 |动物体重。
注意:本节中的所有其他信息都是可选的,但尽可能多地提供请求的信息以在重建映像的 DICOM 标头中找到它很有用,从而便于后续数据查询。 - 在 PET 扫描信息中选择放射性核素 |F18 用于 [18F]FDG 研究和其他 18种 F 标记化合物;如果使用其他示踪剂(例如,[13N]NH3),则修改。在 PET 扫描信息中同时写下示踪剂的名称 |跟踪器 名称模块,因为此名称将在图像重建完成后在 DICOM 标头中报告。
注意:有关示踪剂注射时间、活性和体积的信息是强制性的,但可以在PET采集期间提供。 - 在 CT扫描信息中,写下有关造影剂的所有可用信息。
注意:所有这些信息都是可选的,但如果提供,可以方便后续的数据查询。 - 按 执行 扫描并等待 GUI 的另一个选项卡打开,允许动物定位和其他扫描选项的规范。
- 在 CT 校准中选择 CT 校准类型 |使用默认 CT 校准。
- 在 研究准备 部分,从下拉菜单中选择每个扫描方案,然后选中 等待用户确认后 再进行扫描复选框。
注意:此步骤非常重要,因为它将使扫描仪处于待机状态,等待用户输入,然后再开始相应的采集阶段。对于PET扫描,这将允许示踪剂注射和实际PET扫描开始的同步;对于CTAC扫描,它将允许用户在CT扫描期间发射X射线之前关闭盖子(屏蔽)(如果在CT扫描开始之前打开盖子,研究将自动中止);对于Cine-CT扫描,此暂停将允许用户以所需的延迟启动CA输液协议和CT数据扫描。 - 对于动物定位,请使用 GUI 左侧窗格中的开关打开 电机控制 模块。
注意:这将打开动物床上的定心激光器,并启用放置在扫描仪侧面的手动床对齐按钮。 - 使用手动床对齐按钮将动物的胸部移动到激光标记上。仔细检查动物的纵向和垂直对齐方式。
- 根据定心激光将动物放置在正确的位置后,按下关闭激光以保存当前的 激光 标记位置,该位置将在相应的采集阶段移动到PET和CT扫描仪的中心。然后,关闭电机控制模块。
6. 宠物扫描
- 按 开始采集 将动物移动到 PET 扫描仪 FOV 上。尾巴和套管将留在FOV之外,以允许示踪剂注射。扫描程序将保持空闲状态,直到用户按下“ 继续 ”按钮。
- 用校准的PET示踪剂剂量准备注射器。
- 按下 “继续 ”按钮开始采集,并在扫描开始后5秒内开始将示踪剂注入套管(图1)。
注意:注射持续时间将为~20-25秒。 - 将注射器放入PET剂量校准器中以测量注射器中的残留活性。注释实际活动和测量时间。
- 在扫描仪 GUI 的 硬件监视器 选项卡中,使用 更新 PET 示踪剂信息 按钮插入实际注射时间、活动和体积。
- 在扫描过程中,定期检查动物的生理参数。
- 在扫描过程中,按照步骤2.2中的说明在以下时间点测量血糖:PET扫描开始后5分钟,20分钟,40分钟和60分钟。
- 测量血糖后,将试纸放入伽马计数器中并进行活性测量60秒。记录进行活性测量的实际时间,并校正放射性衰变,将示踪剂注入时间作为参考时间。通过考虑葡萄糖试纸中 1 μL 的平均血容量(即使用公式 [1]),将记录的活性值转换为活性浓度 (Bq/mL):
C 血 = A血/0.001 毫升 [Bq/mL] (1)
其中A 血(t) 是试纸中血液样品的衰减校正测量活性,以 Bq 表示。
注意:PET扫描开始和示踪剂注射可以由同一操作员执行,方法是在注射过程中使用断层扫描机的移动控制装置,该设备放置在扫描仪靠近操作员部位的侧面工作台上。允许扫描开始和注入开始之间有更长的延迟,但动态序列开头的一些重建帧将保持空白。建议避免延迟超过 10 秒(即,使用当前协议导致两个空白帧)。

图 1:PET 示踪剂的注入。 此操作在 PET 扫描开始后立即执行。动物在PET视野内(头部先行,尾巴在操作员一侧可见)。缩写:PET = 正电子发射断层扫描。 请点击此处查看此图的大图。
7. 电脑断层扫描
- 在注射CT造影剂之前,请在合上扫描仪盖并按下GUI上的 “继续” 按钮后立即开始CTAC扫描。在这次非常短的采集结束时,采用以下程序,通过在采集前使用与注射PET示踪剂相同的血管通路注射CA来确保适当增强血池。
- 碘脂乳液CA:
- 完成CTAC扫描后,使用已经连接到小鼠尾静脉的套管注射碘脂质乳剂CA。典型的注射持续时间约为30-60秒。
- 注射完成后立即开始成像。按扫描仪 GUI 上的 继续 以开始 Cine-CT 采集。
- 碘美普尔/注射泵:
- 如果使用正常的X射线CA,例如碘美普尔,请使用注射泵,允许以恒定速率缓慢注射。
- 对于小鼠,通过将注射体积限制为0.5mL,将CA的注射速率设置为10mL / h(~0.17mL / min)。使用此设置,在~3分钟后停止注射。对于大鼠,将泵设置为24mL / h(= 0.4mL / min)的速率,并将注射量限制为2 mL。使用此设置,5分钟后停止注射。
- 将连接到CA管的针头连接到尾静脉的套管,确保管子和针头都预先填充了CA。
- 开始注射。合上扫描仪盖,准备进行Cine-CT扫描。
- 在小鼠注射开始60秒后和大鼠注射开始90秒后按下断层扫描GUI上的继续按钮,以便开始Cine-CT采集。CA的注射将大约与小鼠的Cine-CT扫描完成和大鼠完成同时停止。
- 碘脂乳液CA:
- 完成Cine-CT扫描后,断开动物与生理监测系统的连接并移除尾静脉套管。 根据实际方案,动物在所述成像程序后被恢复或安乐死。在第一种情况下,动物在红外灯下温暖的环境中在笼子里被唤醒。监测它们直到完全觉醒,在气体麻醉后需要 15/30 分钟。在需要例如在成像程序结束时收获组织的方案中,根据D.Lgs.26/2014的附件VI,在诱导室(5%异氟醚)中使用麻醉剂过量对动物实施安乐死。
注意:对于本协议中讨论的 18种F基放射性核素,示踪剂注射后24小时足以达到动物身体上的残留放射性水平,这对于所有实际目的都是安全的。
8. 使用固有心肺门控重建心脏 4DCT 图像
注意:完成成像研究后,将自动执行标准的PET和CT重建。然而,4D(电影)心脏CT序列的重建必须手动进行,并且需要一些用户交互。本节将讨论这种特殊类型的重建,这是随后形态功能心脏CT分析所必需的。
- 打开断层扫描 GUI 的心脏门控模块,选择要分析的影像学研究。
- 在显示的动物的X光片(图2)上选择一个感兴趣区域(ROI),以构建时间依赖性的心脏运动曲线,代表门控信号 - kyx线图。垂直移动预绘制的矩形ROI,以选择心尖和横膈膜的方式。然后,选择 门控信号分析。用户界面现在将在时域和频域上显示门控信号。
- 在第一个频域图中,通过突出显示频谱的第一组峰值来选择呼吸频段(有关示例频谱,请参阅 图3 )。
- 在第二个频域图中,选择心脏运动频带,突出显示第二个最尖锐的峰值。
- 在下一阶段,观察叠加颜色标记(点)的时域门控信号,显示已识别的呼吸峰值和心肌收缩峰值。如果标记位置与原始门控信号的呼吸和心脏峰值非常吻合,则进入下一阶段。否则:
- 如果门控信号的形状与 图3中显示的形状差异太大,请返回步骤8.2并选择另一个ROI。
- 如果门控信号的形状与图3所示的形状相当相似,请返回步骤 8.3和步骤8.4,并在门控信号频谱上选择不同的频段。
- 在下一阶段,至少选择四个心脏门。
注意:典型的Cine-CT重建由8-12个心脏门组成。 - 使用下拉菜单选择正确的呼吸窗口:呼吸窗口 | 20%-80%。
注意:这将保留重建中60%的采集数据,不包括峰值吸气阶段,从而提高每个心脏阶段重建心肌壁的清晰度。 - 执行重建以将回顾性门控的Cine-CT图像转换为DICOM格式,准备导入软件以进行后续功能分析。
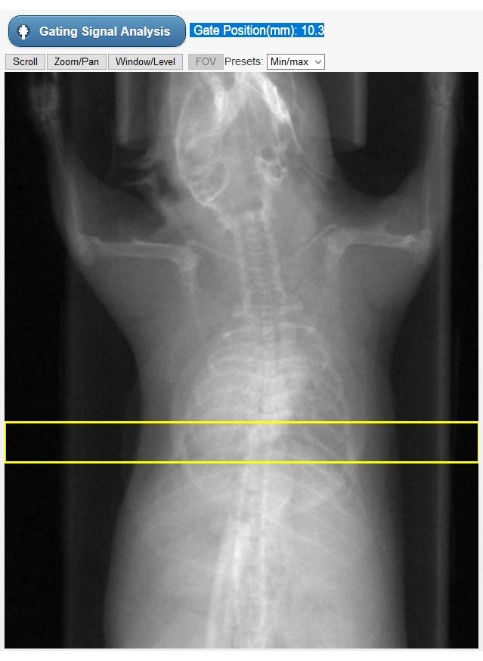
图 2:用于固有门控的 ROI 选择工具。 在Cine-CT重建阶段,该图像显示在断层扫描的GUI中。用户必须选择从原始CT投影中获得固有门控信号(kyx图)的ROI(黄色矩形)的位置。叠加在动物胸部的圆形物体是研究期间仅用于生理监测的呼吸枕。缩写:ROI = 感兴趣区域;CT = 计算机断层扫描;GUI = 图形用户界面。 请点击此处查看此图的大图。
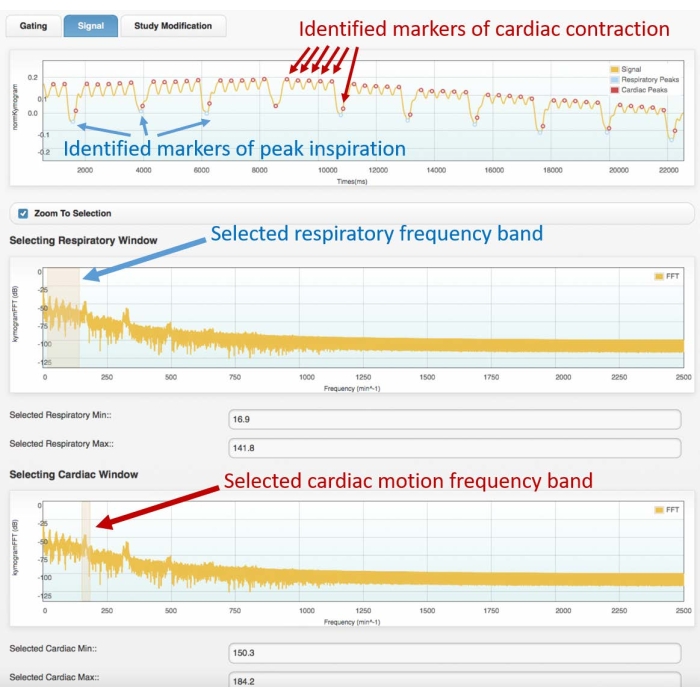
图 3:示例门控信号(顶部框架)和相应的频谱(中心和底部)。 使用中庭软件的心脏门控模块获得的图像。用户必须为呼吸(中心框架)和心脏运动(底部框架)选择合适的频段。这将允许识别门控信号上的呼吸和心脏标志物,在进行4D重建之前,用户必须对其进行检查。峰识别错误或错误分配(例如,呼吸到心脏,反之亦然)将导致不正确的重建。显示的数据是通过对健康的成年雄性Wistar大鼠(507g)的4D Cine-CT扫描的分析中获得的,该大鼠以0.4mL / min的速率注射了2mL碘美普尔,200mg / mL,持续5分钟(顶部的图表在采集的前22秒放大,以便更好地可视化识别的心脏和呼吸运动)。缩写:CT = 计算机断层扫描。 请点击此处查看此图的大图。
9. PET心脏分析
注意:本节介绍如何对小动物左心室的动态[18F]FDG数据进行动力学分析。该分析基于Carimas软件。以下说明不能替代软件用户手册17。下面介绍的过程基于动态PET数据的Patlak图形分析18。有关此分析的详细信息,请参阅“讨论”部分。
- 打开动态 PET 扫描的 DICOM 映像。
- 选择 心形插件 模块。
- 放大小鼠/大鼠心脏上的图像,然后选择大多数血池活动已经被洗掉的最后一个时间范围(或等效地,过去三到五个时间范围的总和)。
- 按照屏幕上的说明沿动物心脏的主轴(短轴、垂直和水平长轴)重新定向图像。通过移动心脏底部和顶点的显示标记来交互地执行此操作(图4)。
- 选择 细分 工具。
注意:默认情况下,自动分段处于启用状态,这在大多数情况下会产生可靠的结果。 - 如果自动分割的结果不可接受,请通过启用 手动模式 (禁用ROI搜索)来优化分段心肌和/或左心室腔的形状。
- 在 建模 工具中,选择要用于动态PET分析的适当动力学模型。在这种情况下,请选择 “图形 | Patlak 启用 Patlak 图分析,用于计算每个心脏部门的葡萄糖摄取代谢率 (MRGlu)。
- 在 极坐标图 工具中,选择正确数量的显示的心形段。在这种情况下,请选择 17 个段。
- 现在,按拟合按钮以执行 Patlak 分析的 拟合 过程。
- 在拟合过程结束时,观察显示的Ki 值的极坐标图(即,以mL/[mL ×分钟]表示的线性回归斜率)。
- 使用表中所示每个扇区的 Ki 值,使用公式 (2) 计算 MRGlu:
MR Glu = (Ki × PGlu)/LC (2)
其中PGlu 是血浆葡萄糖浓度(mmol/L)的血液样本衍生值,集总常数(LC)是用于补偿正常葡萄糖和FDG之间摄取差异的经验系数。例如,参见Ng等人22 ,了解各种实验条件下集总常数的典型值。
注意:在开始PET分析之前,最好在PET分析软件工具中目视检查PET体积的动态序列。这对于排除研究期间时间范围内宏观动物运动是必要的。如果存在运动,则应在分析之前进行适当的图像配准(超出本协议的范围),如果可能的话。
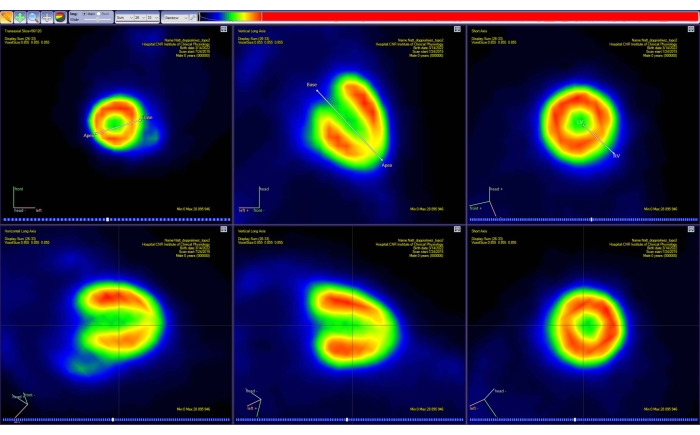
图 4:PET 分析软件的重新定向工具。 3D 空间中两条简单线段的投影显示在三个标准平面(经轴、冠状和矢状)中的每一个上。第一段允许用户选择心脏底部和顶点,而第二段允许用户选择心脏的左侧和右侧。此步骤会产生一个新的(插值的)PET图像(底行),心脏沿标准AHA表示重新定向。用Carimas从一只重51g的健康成年雄性CD-1小鼠中获得图像,并注射10 MBq的[18F]FDG。缩写:PET = 正电子发射断层扫描;AHA = 美国心脏协会;FDG = 氟脱氧葡萄糖。 请点击此处查看此图的大图。
10. 电影CT心脏分析
注意:本节介绍如何对Cine-CT心脏图像进行定量分析,以收集心脏功能的全局定量数据。该分析基于Osirix MD软件。以下说明不能替代 Osirix 用户手册24。
- 在软件中加载Cine-CT扫描的DICOM图像。
- 使用内置 4D 查看器打开动态数据集。
- 使用 3D 多平面重塑 (MPR) 工具,沿短轴重新定向图像数据(图 5)。
- 将重定向的数据导出到 DICOM,确保导出整个 4D 数据,并保留切片厚度(与原始数据相同)和图像位深度(每个体素 16 位)
- 使用 4D 查看器打开导出的 4D MPR 图像。
- 选择与舒张末期相对应的时间范围。使用主工具栏上的时间滑块浏览所有时间范围,以确保选择了正确的心脏阶段。
- 在此时间范围内,选择封闭的 多边形注释 工具并手动描绘左心室的心内膜壁。
- 对从底部到顶点的 10-20 个切片执行相同的操作,确保所有 ROI 具有相同的名称(例如,LVENDO)。
- 在“ROI”菜单上,选择“ROI 卷 |生成缺失的 ROI,通过插值手动绘制的 ROI,在所有短轴切片上生成 ROI。
- 在“ROI”菜单上,选择“ROI 卷 |计算卷:计算具有相同 ROI 名称的 ROI 组的卷。
- 浏览时间范围并选择对应于收缩末期(较小的左心室容量)的阶段,然后重复上述步骤10.7-10.10。
- 使用公式 (3) 和 (4) 计算冲程体积 (SV) 和射血分数:
SV = EDV - ESV[mL] (3)
EF = 100 × SV/EDV [%] (4)
其中EDV是舒张末期容积,ESV是收缩末期容积。
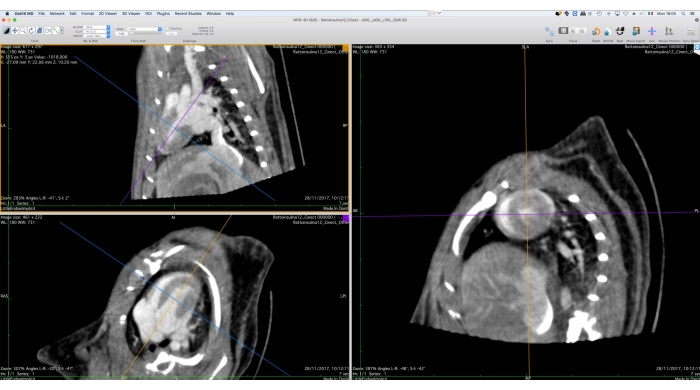
图 5:多平面重整工具的图形界面。 此工具用于重新定向 Cine-CT 数据以进行后续功能分析。用户应旋转和平移屏幕左侧的参考轴,以使心脏的短轴视图显示在右侧。在此过程结束时,用户可以将重定向的图像导出为 DICOM 文件集。图像是用Osirix MD获得的,指的是一只健康的成年雄性Wistar大鼠(507g),以0.4mL / min的速率注射2mL碘美普尔,200mg / mL,持续5分钟,用过滤反向投影重建,体素大小为0.24mm3。 请点击此处查看此图的大图。
结果
在本节中,显示了按照目前描述的程序进行PET和CT分析的典型结果。 图6 显示了对照(健康)CD-1小鼠的[18F]FDG PET扫描的自动心肌和左心室腔分割的结果。尽管右心室在重建的图像中并不总是可见,但基于DICOM接头的方向轴可用于正确区分室间隔与其他左心室壁,这是按照美国心脏协会(AHA)建议25可靠识别标准扇区所必需的。.在心肌缺血的情况下,...
讨论
本文提出的协议侧重于通过使用高分辨率PET / CT成像对心脏损伤小动物模型进行转化心血管研究的典型实验程序。所呈现的结果表明PET和Cine-CT图像具有很高的定量和定性价值,提供了整个心脏关于其葡萄糖代谢,形状和收缩动力学的功能和结构信息。此外,获得的所有图像都是3D的,时间分辨的,并且呈现各向同性的像素间距;从图像处理的角度来看,这是有益的,因为它不需要预扫描操作员依赖?...
披露声明
Daniele Panetta获得了Inviscan Sas的micro-CT仪器研发资助。
致谢
这项研究得到了JPI-HDHL-INTIMIC “GUTMOM”项目的部分支持:后代的母亲肥胖和认知功能障碍:肠道微生物的因果作用和早期饮食预防(项目编号INTIMIC-085,意大利教育部,大学和研究部第946/2019号法令)。
材料
| Name | Company | Catalog Number | Comments |
| 0.9% sterile saline | Fresenius Kabi | 0.9% sodium chloride for injection | |
| 1025L Physiological Monitoring | Small Animal Instruments | Physiological monitoring system for small animal imaging | |
| 5 mL syringes | Artsana | Syringes with needle for injection of PET tracer | |
| Atomlab 500 | Else Nuclear | PET Dose calibrator | |
| Atrium software | Inviscan | Version 1.5.5 | PET/CT operating software |
| Butterfly catheters | Delta Med | 27.5 G needle | |
| Carimas software | Turku PET Center | Version 2.10 | Image analysis software |
| Fenestra VC | Medilumine | Lipid emulsion iodinated contrast agent for small animals | |
| Heat lamp | Heat lamp with clamp and switch | ||
| Insulin syringes | Artsana | Syringes with needle for injection of CT CA | |
| Iomeron 400 mgI/mL | Bracco | Iomeprol, vascular contrast agent | |
| IRIS PET/CT | Inviscan | PET/CT scanner for small animals | |
| Isoflurane | Zoetis | Inhalation anesthetic, 250 mL | |
| OneTouch Glucometer | Johnson&Johnson Medical | Glucose meter kit | |
| Osirix MD software | Pixmeo | Version 11 | Image analysis software |
| Oxygen | Air liquide | Compressed gas | |
| Rectal probe for 1025L | Small Animal Instruments | Rectal probe with cable for SAII 1025L systems | |
| Respiratory sensor for 1025L | Small Animal Instruments | Respiratory pillow with tubings for SAII 1025L systems | |
| TJ-3A syringe pump | Longer | Motorized syringe pump for CT CA injection |
参考文献
- Zaragoza, C. Animal models of cardiovascular diseases. Journal of Biomedicine and Biotechnology. 2011, 497841 (2011).
- Russell, J. C., Proctor, S. D. Small animal models of cardiovascular disease: Tools for the study of the roles of metabolic syndrome, dyslipidemia, and atherosclerosis. Cardiovascular Pathology. 15 (6), 318-330 (2006).
- Riehle, C., Bauersachs, J. Small animal models of heart failure. Cardiovascular Research. 115 (13), 1838-1849 (2019).
- Menichetti, L., et al. MicroPET/CT imaging of αvß3 integrin via a novel 68Ga-NOTA-RGD peptidomimetic conjugate in rat myocardial infarction. European Journal of Nuclear Medicine and Molecular Imaging. 40 (8), 1265-1274 (2013).
- Zhou, H., et al. Development of a micro-computed tomography-based image-guided conformal radiotherapy system for small animals. International Journal of Radiation Oncology, Biology, Physics. 78 (1), 297-305 (2010).
- Di Lascio, N., Kusmic, C., Stea, F., Faita, F. Ultrasound-based pulse wave velocity evaluation in mice. Journal of Visualized Experiments. (120), e54362 (2017).
- Dann, M. M., et al. Quantification of murine myocardial infarct size using 2-D and 4-D high-frequency ultrasound. American Journal of Physiology-Heart and Circulatory Physiology. 322 (3), 359-372 (2022).
- Espe, E. K. Novel insight into the detailed myocardial motion and deformation of the rodent heart using high-resolution phase contrast cardiovascular magnetic resonance. Journal of Cardiovascular Magnetic Resonance. 15 (1), 82 (2013).
- Vanhove, C., et al. Accurate molecular imaging of small animals taking into account animal models, handling, anaesthesia, quality control and imaging system performance. EJNMMI Physics. 2 (1), 31 (2015).
- Garcia, M. J., et al. State of the art: Imaging for myocardial viability: A scientific statement from the American Heart Association. Circulation: Cardiovascular Imaging. 13 (7), 000053 (2020).
- Panetta, D., et al. Cardiac computed tomography perfusion: Contrast agents, challenges and emerging methodologies from preclinical research to the clinics. Academic Radiology. 28 (1), 1-18 (2020).
- Kusmic, C. Up-regulation of heme oxygenase-1 after infarct initiation reduces mortality, infarct size and left ventricular remodeling: experimental evidence and proof of concept. Journal of Translational Medicine. 12 (1), 89 (2014).
- Muthuramu, I., Lox, M., Jacobs, F., De Geest, B. Permanent ligation of the left anterior descending coronary artery in mice: A model of post-myocardial infarction remodelling and heart failure. Journal of Visualized Experiments. (94), e52206 (2014).
- Fischer, M., et al. Comparison of metabolic and functional parameters using cardiac 18F-FDG-PET in early to mid-adulthood male and female mice. EJNMMI Research. 11 (1), 7 (2021).
- Valenta, I., et al. Feasibility evaluation of myocardial cannabinoid type 1 receptor imaging in obesity: A translational approach. JACC: Cardiovascular Imaging. 11 (2), 320-332 (2018).
- Fueger, B. J., et al. Impact of animal handling on the results of 18F-FDG PET studies in mice. Journal of Nuclear Medicine. 47 (6), 999-1006 (2006).
- . Carimas User Manual Available from: https://turkupetcentre.fl/carimas/files/archive/Html/a1.html (2022)
- Peters, A. M. Graphical analysis of dynamic data: The Patlak-Rutland plot. Nuclear Medicine Communications. 15 (9), 669-672 (1994).
- Choi, Y., et al. Parametric images of myocardial metabolic rate of glucose generated from dynamic cardiac PET and 2-[18F]fluoro-2-deoxy-d-glucose studies. Journal of Nuclear Medicine. 32 (4), 733-738 (1991).
- Laffon, E., Marthan, R. Is Patlak y-intercept a relevant metrics. European Journal of Nuclear Medicine and Molecular Imaging. 48 (5), 1287-1290 (2021).
- Flores, J. E., McFarland, L. M., Vanderbilt, A., Ogasawara, A. K., Williams, S. -. P. The effects of anesthetic agent and carrier gas on blood glucose and tissue uptake in mice undergoing dynamic FDG-PET imaging: Sevoflurane and isoflurane compared in air and in oxygen. Molecular Imaging and Biology. 10 (4), 192-200 (2008).
- Ng, C. K. Sensitivity of myocardial fluorodeoxyglucose lumped constant to glucose and insulin. American Journal of Physiology-Heart and Circulatory Physiology. 260 (2), 593-603 (1991).
- Shoghi, K. I., Welch, M. J. Hybrid image and blood sampling input function for quantification of small animal dynamic PET data. Nuclear Medicine and Biology. 34 (8), 989-994 (2007).
- Heuberger, J., Pixmeo, S., Rosset, A. OsiriX User Manual. Blurb. , (2017).
- Cerqueira, M. D., et al. Standardized myocardial segmentation and nomenclature for tomographic imaging of the heart. A statement for healthcare professionals from the Cardiac Imaging Committee of the Council on Clinical Cardiology of the American Heart Association. Circulation. 105 (4), 539-542 (2002).
- Kolanowski, T. J., et al. Multiparametric evaluation of post-MI small animal models using metabolic ([18F]FDG) and perfusion-based (SYN1) heart viability tracers. International Journal of Molecular Sciences. 22 (22), 12591 (2021).
- Guiducci, L., et al. Contribution of organ blood flow, intrinsic tissue clearance and glycaemia to the regulation of glucose use in obese and type 2 diabetic rats: A PET study. Nutrition Metabolism and Cardiovascular Diseases. 21 (9), 726-732 (2011).
- Tadinada, S. M., et al. Functional resilience of C57BL/6J mouse heart to dietary fat overload. American Journal of Physiology-Heart and Circulatory Physiology. 321 (5), 850-864 (2021).
- Dreyfuss, A. D., et al. A novel mouse model of radiation-induced cardiac injury reveals biological and radiological biomarkers of cardiac dysfunction with potential clinical relevance. Clinical Cancer Research. 27 (8), 2266-2276 (2021).
- Hsu, B. PET tracers and techniques for measuring myocardial blood flow in patients with coronary artery disease. Journal of Biomedical Research. 27 (6), 452-459 (2013).
- Dinkel, J., et al. Intrinsic gating for small-animal computed tomography. Circulation: Cardiovascular Imaging. 1 (3), 235-243 (2008).
- Kuntz, J., et al. Fully automated intrinsic respiratory and cardiac gating for small animal CT. Physics in Medicine and Biology. 55 (7), 2069-2085 (2010).
- Li, Y., Zhang, W., Wu, H., Liu, G. Advanced tracers in PET imaging of cardiovascular disease. BioMed Research International. 2014, 504532 (2014).
- Kim, D. -. Y., Cho, S. -. G., Bom, H. -. S. Emerging tracers for nuclear cardiac PET imaging. Nuclear Medicine and Molecular Imaging. 52 (4), 266-278 (2018).
- Maddahi, J., Packard, R. R. S. Cardiac PET perfusion tracers: Current status and future directions. Seminars in Nuclear Medicine. 44 (5), 333-343 (2014).
- Bentourkia, M. Kinetic modeling of PET data without blood sampling. IEEE Transactions on Nuclear Science. 52 (3), 697-702 (2005).
- Lammertsma, A. A. Forward to the past: The case for quantitative PET imaging. Journal of Nuclear Medicine. 58 (7), 1019-1024 (2017).
- Nahrendorf, M., et al. High-resolution imaging of murine myocardial infarction with delayed-enhancement cine micro-CT. American Journal of Physiology-Heart and Circulatory Physiology. 292 (6), 3172-3178 (2007).
- Badea, C. T., Fubara, B., Hedlund, L. W., Johnson, G. A. 4-D micro-CT of the mouse heart. Molecular Imaging. 4 (2), 110-116 (2005).
- Technical Resources. MediLumine Available from: https://www.medilumine.com/technical-resources (2019)
- Nebuloni, L., Kuhn, G. A., Müller, R. A Comparative analysis of water-soluble and blood-pool contrast agents for in vivo vascular imaging with micro-CT. Academic Radiology. 20 (10), 1247-1255 (2013).
- Panetta, D., et al. Performance evaluation of the CT component of the IRIS PET/CT preclinical tomograph. Nuclear Instruments & Methods in Physics Research Section A: Accelerators Spectrometers Detectors and Associated Equipment. 805, 135-144 (2016).
- Gu, J., et al. At what dose can total body and whole abdominal irradiation cause lethal intestinal injury among C57BL/6J mice. Dose-Response. 18 (3), 1559325820956783 (2020).
- Amirrashedi, M., Zaidi, H., Ay, M. R. Advances in preclinical PET instrumentation. PET Clinics. 15 (4), 403-426 (2020).
- Clark, D. P., Badea, C. T. Advances in micro-CT imaging of small animals. Physica Medica. 88, 175-192 (2021).
- Belcari, N., Del Guerra, A., Panetta, D., Grupen, C., Buvat, I. High-Resolution and Animal Imaging Instrumentation and Techniques. Handbook of Particle Detection and Imaging. , 1497-1535 (2021).
- Wang, G., Rahmim, A., Gunn, R. N. PET Parametric imaging: Past, present, and future. IEEE Transactions on Radiation and Plasma Medical Sciences. 4 (6), 663-675 (2020).
- Befera, N. T., Badea, C. T., Johnson, G. A. Comparison of 4D-microSPECT and microCT for murine cardiac function. Molecular Imaging and Biology. 16 (2), 235-245 (2014).
- van Deel, E., Ridwan, Y., van Vliet, J. N., Belenkov, S., Essers, J. In vivo quantitative assessment of myocardial structure, function, perfusion and viability using cardiac micro-computed tomography. Journal of Visualized Experiments. (108), e53603 (2016).
- Lee, C. -. L., et al. Assessing cardiac injury in mice with dual energy-microCT, 4D-microCT and microSPECT imaging following partial-heart irradiation. International Journal of Radiation Oncology, Biology, Physics. 88 (3), 686-693 (2014).
- Harms, H., et al. Comparison of clinical non-commercial tools for automated quantification of myocardial blood flow using oxygen-15-labelled water PET/CT. European Heart Journal - Cardiovascular Imaging. 15 (4), 431-441 (2013).
- Nesterov, S. V., et al. Myocardial perfusion quantitation with 15O-labelled water PET: High reproducibility of the new cardiac analysis software (CarimasTM). European Journal of Nuclear Medicine and Molecular Imaging. 36 (10), 1594-1602 (2009).
- Nesterov, S. V., et al. Myocardial perfusion quantification with Rb-82 PET: Good interobserver agreement of Carimas software on global, regional, and segmental levels. Annals of Nuclear Medicine. 36, 507-514 (2022).
- Nesterov, S. V., et al. One-tissue compartment model for myocardial perfusion quantification with N-13 ammonia PET provides matching results: A cross-comparison between Carimas, FlowQuant, and PMOD. Journal of Nuclear Cardiology. , (2021).
- Thackeray, J. T., Kuntner-Hannes, C., Haemisch, Y. Preclinical Multimodality Imaging and Image Fusion in Cardiovascular Disease. Image Fusion in Preclinical Applications. , 161-181 (2019).
- Vohra, R., Batra, A., Forbes, S. C., Vandenborne, K., Walter, G. A. Magnetic resonance monitoring of disease progression in mdx mice on different genetic backgrounds. The American Journal of Pathology. 187 (9), 2060-2070 (2017).
- Baehr, A., et al. Agrin promotes coordinated therapeutic processes leading to improved cardiac repair in pigs. Circulation. 142 (9), 868-881 (2020).
- Lalwani, K., et al. Contrast agents for quantitative microCT of lung tumors in mice. Comparative Medicine. 63 (6), 482-490 (2013).
- Bertoldo, A., et al. Evaluation of compartmental and spectral analysis models of [18F]FDG kinetics for heart and brain studies with PET. IEEE Transactions on Bio-medical Engineering. 45 (12), 1429-1448 (1998).
- Li, Y., Kundu, B. K. An improved optimization algorithm of the three-compartment model with spillover and partial volume corrections for dynamic FDG PET images of small animal hearts in vivo. Physics in Medicine and Biology. 63 (5), 055003 (2018).
- Mabrouk, R., Dubeau, F., Bentourkia, M., Bentabet, L. Extraction of time activity curves from gated FDG-PET images for small animals' heart studies. Computerized Medical Imaging and Graphics. 36 (6), 484-491 (2012).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。